Effects of Acid and Alkali Cooking on Edible Quality of Lotus Rhizome
-
摘要: 醋酸和碳酸氢钠常被用作添加剂以调节果蔬的质地,然而在质地改善过程中其对莲藕营养品质的影响尚不清楚。本研究以蒸馏水为对照,使用0.1%醋酸(v/v)及0.1%碳酸氢钠(w/v)煮制莲藕,对其硬度、色泽、维生素C、总酚、消化等指标进行测定,并对碳酸氢钠处理后的莲藕风味成分进行分析。结果表明,醋酸处理可以显著提高莲藕的煮制硬度并使莲藕片始终保持较白的色泽,而碳酸氢钠处理后其煮制硬度显著降低,并呈红褐色。莲藕鲜样的总酚含量(约1300 μg/g)和VC含量(约0.3 mg/g)最高,加热处理会导致莲藕总酚和VC含量大幅下降,除醋酸处理组莲藕总酚含量(约900 μg/g)较高外,蒸馏水和碳酸氢钠处理组之间无显著性差异。碳酸氢钠处理会改变莲藕的消化吸收模式,导致胃消化液中的总碳水化合物水平较低(约300 g/L),而蒸馏水和醋酸处理组之间差异较小,但是在模拟肠消化中肠消化液中的总碳水化合水平依旧会升高。电子鼻和固相微萃取-气相色谱质谱联用(SPME-GC-MS)结果显示构成莲藕风味的挥发性成分主要由二甲基硫、正辛醛、壬醛、葵醛组成,碳酸氢钠处理之后,莲藕的二甲基硫以及酯类化合物均有所增加。酸碱煮制对莲藕的硬度和色泽的影响相反,但未显著改变总酚和VC含量,醋酸代替蒸馏水烹煮不会显著改变体外胃肠消化模式,但碱煮会使碳水化合物的消化利用集中在肠消化阶段。碳酸氢钠煮制后产生的有机酸和酯类以及二甲基硫含量的升高形成碱煮莲藕的特殊风味。
-
关键词:
- 莲藕 /
- 烹煮 /
- 食用品质 /
- 风味 /
- 固相微萃取-气相色谱质谱(SPME-GC-MS)
Abstract: Acetic acid (AA) and sodium bicarbonate (SB) are commonly used as additives for regulating the texture of fruits and vegetables. However, the effects on the nutritional quality of lotus rhizome during texture modification are not well-understood. In this study, with distilled water as control group, the effects of cooking with 0.1% acetic acid (v/v) and 0.1% sodium bicarbonate (w/v) on the hardness, color, vitamin C, total phenol and digestion of lotus rhizome were investigated. The flavor components of lotus rhizome treated with sodium bicarbonate were also analyzed. The results showed that AA treatment could significantly improved the cooking hardness of lotus rhizome while keeping its white color, but SB-cooking significantly reduced the hardness of lotus rhizome and possessed a reddish color. The highest total phenol (about 1300 μg/g) and VC content (about 0.3 mg/g) were found in fresh sample. Cooking resulted in a significant decrease in the total phenol and VC content, with no significant difference observed between distilled water and sodium bicarbonate treatment groups except for the higher total phenol content of AA-treated group (about 900 μg/g). SB treatment altered the digestion and absorption pattern of lotus rhizome, resulting in a lower level of total carbohydrate in the gastric digestive juices (about 300 g/L). Less differences were found between the distilled water and AA treatment, while in the simulated intestinal digestion, the total carbohydrate levels of both remained high. The results of electron nose and solid-phase microextraction-gas chromatography-mass spectrometry (SPME-GC-MS) showed that the volatile components of lotus rhizome flavor mainly included dimethyl sulfide, n-octanal, nonanal, and sunflower aldehyde, etc. The dimethyl sulfide as well as esters of lotus rhizome were increased after SB treatment. Acid and alkaline cooking had opposite effects on the hardness and color of lotus rhizome, but did not significantly alter the total phenol and VC contents. Instead of distilled water, cooking with acetic acid did not significantly alter the in vitro gastrointestinal digestion pattern, but alkaline cooking concentrated the carbohydrate digestion utilization in the intestinal digestion phase. The organic acids and esters produced by sodium bicarbonate cooking and the elevated dimethyl sulfide content formed the special flavor of alkali-cooked lotus rhizome. -
莲藕(Nelumbo nucifera Gaertn)是多年生水生蔬菜睡莲科的肥大根茎,具有许多单子叶植物特征的最古老双子叶植物之一,在中国、印度、日本和澳大利亚等国广泛种植[1]。在我国主要分布于长江、黄河、珠江流域的山东、湖北、湖南、浙江、广东等地,其中湖北省的莲藕产量和种植面积多年来居全国首位[2]。根据莲藕质地的不同,可以分为粉藕和脆藕,粉藕主要用来煲汤、糯米藕等,热加工后质地粉糯,色泽红润。粉藕典型的代表品种有:沔城藕、洪湖藕等;脆藕适宜炒食、凉拌,热加工后仍保持脆爽口感。脆藕典型的品种代表有芦林湖藕、河南飘花藕、鹰潭晚藕等。
莲藕中含有丰富的碳水化合物、蛋白质、维生素、矿物质、鞣质等营养元素。据测定,每100 g鲜藕含约含有水分77.9~89 g,淀粉10~20 g,蛋白质1~2 g,维生素C 25~55 mg,以及胡萝卜素、多酚化合物、钙、磷、铁等[3]。莲藕中的酚类化合物含量较高,孙杰等[4]认为莲藕的中的酚类主要包括没食子酸、绿原酸、儿茶素、咖啡酸、香豆素和白藜芦醇,且以游离态为主。藕皮、藕节中的总酚和总黄酮含量高于可食用部分,但可食用部分对整藕的抗氧化性贡献最大。莲藕多糖可减缓糖尿病小鼠消瘦的症状,降低血糖,提高糖尿病小鼠葡萄糖耐受能力和糖尿病小鼠肝、肾和胰腺等重要组织的超氧化物歧化酶活性,降低血清丙二醛含量[5]。金文筠[6]利用超微粉碎和酸酶解法从藕节中提取出可溶性膳食纤维,研究表明其能显著提高高密度脂蛋白胆固醇(HDL-C)的含量,降低低密度脂蛋白胆固醇含量(LDL-C),同时能降低动脉粥样硬化几率并具有最佳的调节血脂作用。此外,藕节中的化学成分有三萜类、天冬酰胺、鞣质、生物碱和黄酮类等化合物,其中3-表白桦脂酸(3-Epibetulinic acid)是其主要的化学成分,具有良好的止血活性[7]。
质构是影响植物性食品品质的重要因素之一。植物性食品,如莲藕、木薯、土豆、菜豆和荸荠等,在热加工过程中往往表现出质地劣变的趋势,食用质地下降或不易于煮烂。质地劣变直接影响热加工食品的商品性和营养价值[8]。因此如巴氏灭菌、优化超声、辐照条件,超高压处理等延缓植物性食品热加工质地劣变研究正成为热点[9]。醋酸和碳酸氢钠是两种常用的食品添加剂,最大残留量为按生产需要适量使用,赵雯霖[10]利用0.1%醋酸浸泡土豆片并发现热处理后其煮制硬度显著上升,土豆组织细胞壁能够维持一个较为稳定的状态。Chigwedere等[11]通过加入0.1 mol/L的碳酸氢钠溶液煮制过度成熟的菜豆,结果表明碱处理可以显著降低菜豆的硬度,改善其口感,并且发现质地的维持主要与菜豆的种皮有关。研究表明,醋酸和碳酸氢钠处理可以改善果蔬的质地,但是质地改善是否会对果蔬的营养品质造成影响仍然未知。莲藕质地的差异是影响其加工方式以及价格的主要原因,因此掌握莲藕热加工后质地差异的机理并通过调控达到期望的口感至关重要。因此,本实验用0.1%醋酸(v/v)以及0.1%碳酸氢钠(w/v)溶液处理莲藕,测定不同处理对硬度、色泽、维生素C、总酚、消化的影响以及碱处理对莲藕风味成分的变化(虽然实验使用的醋酸浓度仅为0.1%,但处理后的样品醋味浓郁刺鼻,不适用于煮制食用,因此仅研究碳酸氢钠对莲藕煮后风味的影响),评价酸碱处理对于莲藕硬度、营养、消化的影响和碱处理后风味的影响,为莲藕热加工提供理论参考。
1. 材料与方法
1.1 材料与仪器
莲藕品种 鄂莲5号,购于华中农业大学菜市场(湖北省武汉市洪山区狮子山街1号);乙酸、碳酸氢钠、无水乙醇、甲醇、没食子酸、草酸、2,6-二氯靛酚、抗坏血酸、盐酸、氢氧化钠、胃蛋白酶(3000 U/g)、胰酶(4000 U/g)、葡萄糖、苯酚、浓硫酸、氯化钠 (以上试剂均为分析纯) 均来自于国药集团化学试剂有限公司。
TA.XT.PLUS质构仪 配有直径2 mm P/6平底圆柱型探头,英国SMS公司;TSQ8000Evo气质联用仪 配有HP-5(30 m×320 µm,0.25 µm)毛细管柱,美国Thermo公司;DVB/CAR/PDMS SPME萃取纤维头、50/30 μm手动SPME进样器 美国Supelco公司;FOX 4000电子鼻 法国Alpha M.O.S公司;HH-2数显磁力搅拌水浴锅 江苏金坛市荣华仪器制造有限公司;BSA124S分析天平 德国赛多利斯集团;DZ-500K倾斜式真空包装机 上海申越包装机械有限公司;KQ-600DB数控超声波清洗机 昆山市超声仪器有限公司;Sorvall ST16R高速冷冻离心机 美国Thermo公司;FSH-2数显高速分散器 常州市金坛友联仪器研究所;PB-10 pH计 赛多利斯科学仪器有限公司;UV Ultra色差仪 美国Hunterlab公司;PCE-30000电热恒温干燥箱 上海普索仪器制造有限公司。
1.2 实验方法
1.2.1 实验样品的准备
新鲜莲藕在流水下清洗,切掉首尾两端,仅保留中间可食用部分。削皮后切成厚度为3 mm的均匀薄片,随机分成三组装入尼龙袋(24 cm×17 cm),每袋装入莲藕70 g,溶液100 mL。第一组为对照组,溶液为蒸馏水(DW);第二组为醋酸(0.1%(v/v))处理组(AA);第三组为碳酸氢钠(0.1%(w/v))处理组(SB)。每组真空包装封口,置于100 ℃沸水中煮制30 min后迅速置于流水中冷却。样品水分沥干后立即用于下一步试验。
1.2.2 莲藕硬度的测定
不同处理的莲藕片硬度分别用TA.XT.Plus型质构仪,直径2 mm P/6平底圆柱型探头进行测定。操作参数参考Zhao等[12]的方法,具体如下:测试速率:1.00 mm/s;测后速率:1.00 mm/s;绘图速率:1.00 mm/s;压缩比:30%;停留间隔:2 s。采用第一次被压缩时最大峰值来表示莲藕片的硬度,每组样品平行十次测试。
1.2.3 莲藕色度的测定
L*和a*值由手持式色差仪检测。莲藕片冷却沥干后,用滤纸吸干表面残余的水分,置于白色底板上,将色差仪对准莲藕无孔洞处测定,平行三次取平均值作为结果。分别将不同处理的莲藕片放置于白色瓷盘中,LED常亮灯下用照相机拍摄。
1.2.4 莲藕总酚含量的测定
采用福林-酚法分析样品中总酚含量[13],标准曲线制作:精确称取50 mg没食子酸,配制浓度为100 µg/mL的没食子酸标准溶液。分别移取100、200、300、400、500、600 µL没食子酸标准溶液于试管中,空白试管加入1 mL蒸馏水。各试管分别加入3 mL福林试剂,摇匀,反应7~8 min后,加入3 mL 10% Na2CO3溶液,再次摇匀,室温下置于暗室显色30 min,加水定容至10 mL,在765 nm处测定吸光值。样品处理:称取莲藕样品5 g(W),加入少许40%甲醇研浆。用20 mL 40%甲醇转移至50 mL三角瓶中,55 ℃超声处理30 min(480 W)。10000 r/min,4 ℃离心10 min,重复提取两次,收集上清液,用蒸馏水定容至50 mL,以此为样液。取上述样液0.5 mL置于刻度试管中,实验方法同标准曲线,以未加样液的管做参比,在760 nm处测定吸光值,每组平行3次,由标准曲线查得对应的浓度(N),并按下列公式计算出总酚的含量(标准曲线Y=0.1317X+0.0583,R2=0.9995)。
式中:W表示样品质量,g;N表示测得总酚浓度,μg/mL;G表示样液体积,mL。
1.2.5 莲藕VC含量的测定
依据GB 5009.86-2016《食品中抗坏血酸的测定》中的2,6-二氯靛酚滴定法来测定不同莲藕样品中的VC的含量,实验过程略有修改。每克莲藕样品加入0.5 mL 2%的草酸溶液,利用高速分散器研磨匀浆后,样品在4 ℃下离心(8000 r/min,10 min),所得上清液用2%草酸溶液适量稀释,定容后取10 mL滤液用于测定。同时做空白试验。
1.2.6 体外模拟胃肠消化
体外模拟胃消化过程:称取60 g莲藕样品捣碎,用1.0 mol/L的盐酸溶液调节pH至2.0,加入胃蛋白酶至浓度为4 g/L,溶液总体积为250 mL。置于37 ℃恒温摇床消化0、30、60、120 min。消化完成后,于沸水浴10 min灭酶,10000 r/min离心收集上清液,于−20 ℃保存,残渣置于烘箱85 ℃烘干至恒重。体外模拟肠消化过程:取上一步干燥残渣,用1.0 mol/L的氢氧化钠溶液调节pH至6.8,加入胰酶至浓度为10 g/L,消化及灭酶步骤如上。上清液于−20 ℃保存,残渣置于烘箱85 ℃烘干至恒重。
1.2.7 胃肠消化液多糖含量分析
取上一步上清液过0.45 µm水相滤膜,滤液通过苯酚-硫酸法测定多糖含量。标准曲线制作:准确称取葡萄糖标准品55 mg,定容至500 mL,分别吸取0、0.2、0.3、0.4、0.5、0.6 mL标准溶液于试管中,用蒸馏水补至1.0 mL,然后加入6%苯酚0.5 mL及浓硫酸2.5 mL,摇匀冷却,室温放置20 min,于490 nm处测吸光值。以1 mL水为空白,横坐标为移取葡萄糖标准溶液体积,纵坐标为吸光度,绘制标准曲线。样品含量测定:吸取1 mL样品并定容至250 mL,吸取1 mL样品于试管中,其余步骤同标准曲线。每次测定平行三次,以标准曲线计算多糖含量(标准曲线方程为Y=13.02727X−0.1123,R2=0.99816)。
1.2.8 电子鼻分析碱处理对莲藕风味的影响
不同处理的莲藕样品分别切丁后取2 g置于10 mL的顶空进样瓶中并加盖密封处理。将进样瓶置于FOX 4000型号的电子鼻装置上进行测定。电子鼻系统共有三组18个传感器(表1),分别为第一组:LY2/LG、LY2/G、LY2/AA、LY2/GH、LY2/gCTL、LY2/gCT;第二组T30/1、P10/1、P10/2、P40/1、T70/2、PA/2;第三组P30/1、P40/2、P30/2、T40/2、T40/1、TA/2。各传感器的响应特性如附表所示。测定参数具体如下:载气参数:载气为合成的干燥空气并且流速为150 mL/min;顶空注射参数:注射体积为2500 μL,注射速度为2500 μL/s;获取参数:延滞时间为300 s,获取时间120 s,获取周期1 s。样品不加热处理并且每个样品平行三次测定。
表 1 各传感器的响应特性Table 1. Response characteristics of each sensor传感器名称 性能描述 参考物质 LY2/LG 对氧化能力较强的气体灵敏 氯、氟、氮氧化合物 LY2/G 对有毒气体灵敏 氨、胺类、碳氧化合物 LY2/AA 对有机化合物灵敏 乙醇、丙酮、氨 LY2/GH 对有毒气体灵敏 氨、胺类化合物 LY2/gCTL 对易燃气体灵敏 硫化氢 LY2/gCT 对有毒气体灵敏 丙烷、丁烷 T30/1 对有机化合物灵敏 极性化合物、氯化物 P10/1 对可燃气体灵敏 碳氢化合物、氨、氯 P10/2 对易燃气体灵敏 非极性化合物;甲烷、乙烷 P40/1 对氧化能力较强的气体灵敏 氟 T70/2 对芳香族化合物灵敏 甲苯、二甲苯 PA/2 对有机化合物、有毒气体灵敏 乙醇、氨水 P30/1 对可燃气体、有机化合物灵敏 碳氢化合物、燃烧产物 P40/2 对氧化能力较强的气体灵敏 氯、硫化氢、氟化物 P30/2 对有机化合物灵敏 硫化氢、酮 T40/2 对氧化能力较强的气体灵敏 氯 T40/1 对氧化能力较强的气体灵敏 氟 TA/2 对有机化合物灵敏 乙醇 1.2.9 GC-MS分析碱处理对莲藕风味的影响
准确称取40 g藕丁于顶空瓶中并分成两组,分别用蒸馏水和0.1%碳酸氢钠溶液定容至100 mL。将顶空瓶置于沸水煮制30 min后迅速置于流水下冷却。利用高速均质机均质10 s后加入氯化钠5 g以及50 μL的0.1%(v/v)环己酮溶液(乙醇溶解)。置于50 ℃磁力搅拌水浴锅上平衡20 min。平衡结束后插入已活化好的50/30 μm DVB/CAR/PDMS的SPME萃取头萃取40 min。然后再插入气质联用仪进样口解析5 min。气相色谱条件设置:载气为氦气,柱流速1 mL/min,进样口温度设为250 ℃,不分流进样,电子电离源,离子源温度280 ℃,四级杆温度150 ℃,电子能量70 ev,扫描质量范围m/z 45~550。升温程序:起始温度40 ℃,以5 ℃/min速率升至230 ℃,保持3 min。通过计算机谱库(NIST 11/Wiley 7.0)对样品中挥发性成分进行检索匹配,采用面积归一化法对挥发性成分定量分析。
1.3 数据处理
各组实验重复三次,所得数据取平均值,采用Excel进行汇总计算分析,用Origin 2018以及GraphPad Prism 6作图,用DPS7.05软件根据LSD(Least significant difference)法进行显著性分析,P<0.05表示差异显著。
2. 结果与分析
2.1 酸碱处理对莲藕硬度和色泽的影响
图1和表2共同反映了酸碱处理对莲藕片色泽和硬度的影响。其中L*表示亮度,其值越大表示样品越白。a*反映的是样品红绿差异,其值越大样品越红。莲藕片经DW煮制30 min后,色泽呈现红褐色,藕片边缘有部分发蓝变黑的现象。导致莲藕色泽变化的原因包含酶促褐变和非酶褐变两种,其中以酶促褐变因素占主导,主要是由于多酚氧化酶与各种酚酶底物发生反应的结果,另外,也可能是莲藕组织中溶出的酚类物质在空气中氧气作用下发生氧化聚合的结果,其具体原因需要进一步探究。加入0.1%的AA煮制30 min后,相较于对照组,莲藕片色泽发白并且边缘并没有出现发蓝变黑的现象。是由于酚类物质在酸性环境下更稳定,不易发生氧化反应,并且高温环境对多酚氧化酶具有一定的灭活作用,从而使莲藕片原有的色泽得以保持,而加入0.1% SB煮制后莲藕片a*显著升高(P<0.05),色泽红润。
表 2 酸碱处理对莲藕L*值、a*值以及硬度的影响Table 2. Effects of acid and alkali treatment on L* value, a* value and the hardness of lotus rhizome样品处理组 L*值 a*值 硬度(g) DW煮制 55.17±0.23b 1.87±0.21b 1745.62±94.12b 0.1% AA煮制 58.27±0.43a 1.24±0.31c 2475.71±74.47a 0.1% SB煮制 51.49±0.19c 2.79±0.15a 1347.49±83.49c 注:同列不同小写字母表示存在显著差异(P<0.05)。 醋酸煮制后硬度值也有显著升高(P<0.05),说明经过0.1% AA处理不仅可以维持莲藕片本身白润的色泽,并且能够提高莲藕的煮制硬度。Zhao等[14]也发现0.8%乙酸浸泡后的马铃薯片硬度大于对照组,他们认为乙酸可以有效保持马铃薯完整细胞壁,防止热加工后马铃薯内部细胞间隙的变大,从而防止硬度的降低。Liu等[15]通过对比电镜图发现酸处理能够使马铃薯细胞中的果胶发生胶凝化,因而在加热后使细胞结构保持完整。邹妍等[16]在乙酸泡后的马铃薯片显微图像中发现细胞间连接更紧密,硬度才得以保持。碱煮使莲藕片硬度显著下降(P<0.05),整体质地易碎。醋酸和碳酸氢钠煮制会导致莲藕出现截然相反的质地,这可能与细胞结构中与质地相关的果胶组分结构、含量变化和降解有关:果胶在碱性条件下易发生β-消除,并且高温环境加速果胶的降解。因此醋酸烹煮的藕片硬度高于碳酸氢钠处理组。
莲藕在不同的烹饪方式中对其硬度和色泽有不同的要求。例如,在炒食中,一般希望口感脆爽硬度稍大并且颜色白润,而在煲汤中,则希望莲藕质地粉糯,颜色红褐色从而更好的增加食欲。实验证明通过酸碱处理后,可以达到莲藕在不同的烹饪方式中对其硬度和色泽的要求。
2.2 酸碱处理对莲藕总酚含量的影响
酚类化合物是广泛存在于水果、蔬菜和谷类食物中的植物次生代谢产物,有多种生物活性,尤其在预防心脑血管、癌症以及衰老方面发挥着十分重要的作用[17]。由图2可以看出,莲藕鲜样的总酚含量最高,约为1300 μg/g。烹调加热可以软化植物细胞的细胞壁,与水直接接触后促进酚类物质溶出,从而进入蒸煮水,造成多酚的流失。热处理对酚类化合物有氧化分解作用,煮制对其破坏较大[18]。因此经过30 min煮制后,莲藕总酚含量显著下降(P<0.05),说明莲藕中的酚类物质同样具有热不稳定性。对于煮制后的莲藕样品,AA处理可以使得莲藕的总酚含量维持在较高的水平,约为900 μg/g,这可能是因为低浓度乙酸存在的酸性环境对多酚有保护作用,避免了多酚的氧化降解,多酚或脂质之间的氢键和疏水作用力被破坏,从而使得莲藕多酚能有效扩散出来,从而使其检测含量相对较高[19]。0.1% SB处理与蒸馏水处理组莲藕的总酚含量并无显著差别(P>0.05)。一般来说,在碱性条件下,莲藕多酚易被氧化形成醌类化合物,从而造成总酚含量的部分损失[20]。然而在碱性条件下,莲藕的细胞壁受到较大破坏,在提取过程中细胞中的酚类物质易被释放出来,从而造成其总酚含量与对照组蒸馏水煮制的总酚含量没有显著差异(P>0.05)。
![]() 图 2 不同处理对莲藕总酚含量的影响注:使用Duncan多重比较测试,不同字母表示不同处理间差异显著(P<0.05);图3同。Figure 2. Effects of different treatments on the content of total phenols in lotus rhizome
图 2 不同处理对莲藕总酚含量的影响注:使用Duncan多重比较测试,不同字母表示不同处理间差异显著(P<0.05);图3同。Figure 2. Effects of different treatments on the content of total phenols in lotus rhizome2.3 酸碱处理对莲藕VC含量的影响
维生素C作为体内一种重要的抗氧化剂,对机体正常代谢和生长发挥着不可替代的作用,同时它也是一种最容易在烹调过程中损失的营养素,因此在烹饪中食物维生素C的保存率可作为衡量烹调加工对营养价值影响程度的具体指标之一[21]。由图3可知,鲜样的VC含量最高,约为0.3 mg/g,烹煮造成莲藕VC含量降低约65%~75%。Hunter等[22]也发现了水煮后豌豆和菠菜中维生素C损失显著,可能是维生素C主要流失到了蒸煮水中。各项研究结果表明,烹饪过程中蔬菜不与水接触可防止酚类物质的流失,因而是保留酚类化合物较好的方法[23]。从图3中可以看出,不论何种处理,其莲藕的VC含量均维持在0.1 mg/g左右。一般来说,VC在酸性环境下更加稳定,在中性和碱性条件中,VC会受到金属离子(铜、铁等)或光照的作用加速其被降解损失的速度[24]。然而本研究中蒸煮介质中未添加额外的金属离子等促降解因子,因此莲藕的VC含量在不同处理组之间并没有显著性差异(P>0.05)。
2.4 酸碱处理莲藕的体外模拟胃肠消化
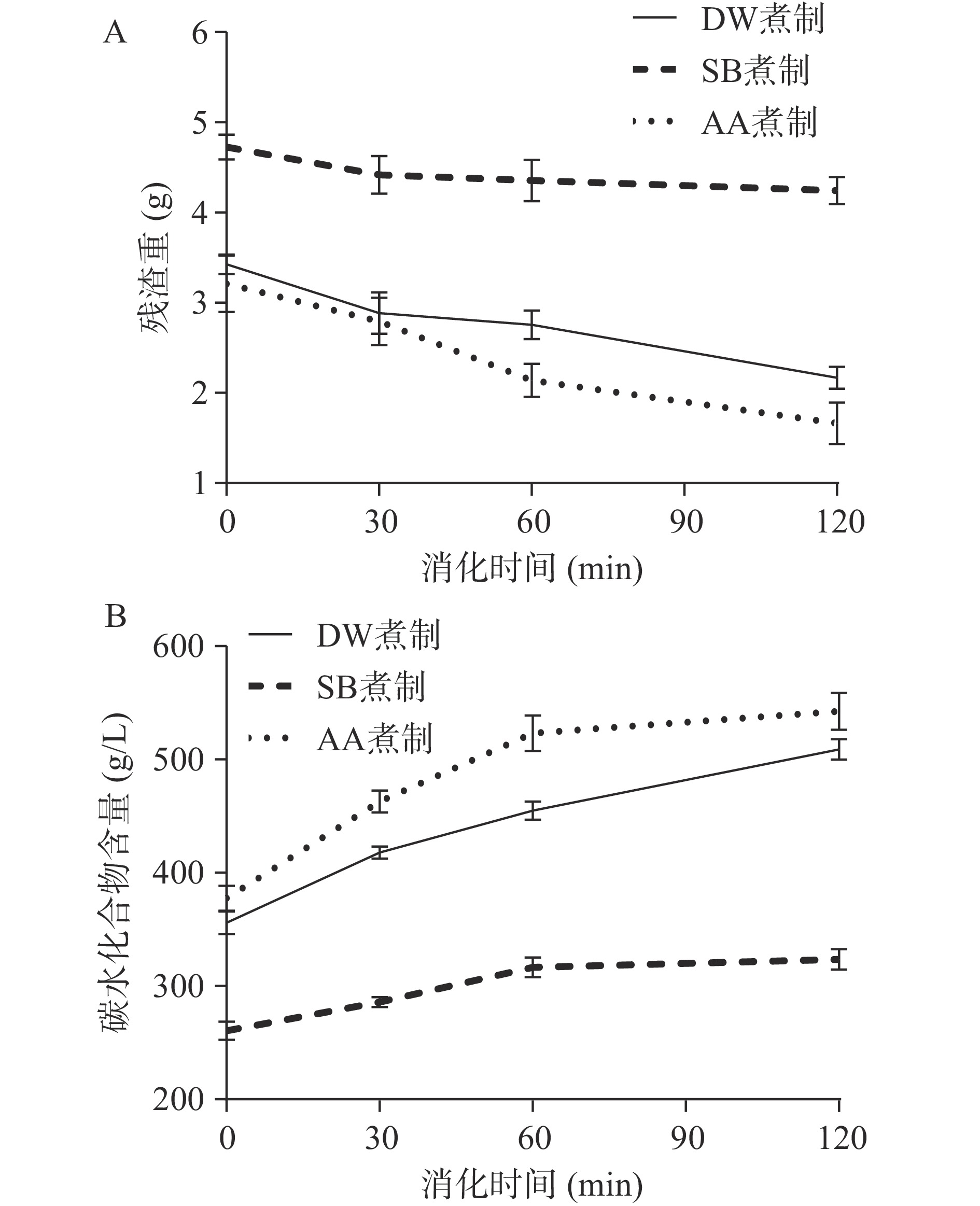
图4展示了不同处理的莲藕片在同一模拟胃消化条件下,其食物残渣重量与消化液中碳水化合物总量的变化。由图4可知,碳酸氢钠处理组在胃消化一开始阶段中消化液中碳水化合含量约为260 g/L,并在消化过程中迅速达到平衡至300 g/L,增长幅度缓慢。而DW处理组和AA处理组的增长趋势一致:在蒸馏水煮制和醋酸处理后,其初始消化液中碳水化合物总量就达到370 g/L左右,并在模拟胃消化的过程中迅速增加到500 g/L。而SB处理组则与另外两组有较大差异:经过短暂打浆模拟咀嚼过程后,SB处理组的食物残渣含量依然维持在较高的水平,这可能是因为经过烹煮软化处理后,莲藕细胞壁之间的粘结力减弱,在打浆的过程中,细胞大多完整分离而非破裂,胞内物质释放较少,因而导致食物残渣的重量较高,整个120 min模拟胃消化过程中食物残渣重量整体呈缓慢降低趋势。相比于碱性烹煮,DW处理组以及AA处理组莲藕细胞壁之间起黏附连接作用的果胶破坏程度较小[25],细胞壁之间粘结力较大,从而导致打浆后细胞壁之间因机械力撕扯破碎,胞内物质释放较充分,使胃消化液初始残渣重量处于较低水平。经过120 min模拟胃消化后,胞内物质逐步释放完全,消化液残渣重量也逐渐降低。胃消化液中的碳水化合物含量的变化也可以反映胞内物质释放水平。
图5展示了莲藕经过胃肠模拟消化后,其食物残渣重量和消化液中碳水化合物含量的变化。由图5可知,经过上一步胃消化后,DW处理组和AA处理的食物残渣量随着消化时间的增加仅略微下降,而消化液中碳水化合物的含量也仅略微升高,说明经过打浆后,莲藕细胞壁胞内物质释放完全。而SB处理组食物残渣的含量在肠消化的30 min内迅速降低后逐渐达到平衡,其消化液中可溶性碳水化合物的含量也在前30 min迅速升高后,缓慢上升。这说明,莲藕细胞壁在加碱煮制后虽然胞内物质释放率低,但是由于烹煮后细胞壁表面破碎的空洞较多,胰酶依旧可以进入细胞内水解淀粉,从而可以提高消化液中可溶性碳水化合物的含量,并且SB烹煮后莲藕残渣的碱性有利于增强胰酶的水解活性(胰酶最适pH为7.8~8.5)。而酸处理和蒸馏水处理组中混合物环境pH低,酶活性要低于碱煮处理组,消化速率较慢,另外,淀粉在高温下降解,α-1,4糖苷键和α-1,6糖苷键被水解,生成糊精、低聚糖、麦芽糖、葡萄糖等水溶性小分子物质,因此上清液中总糖含量略高,碱性条件下淀粉易糊化,抗酶解能力较强。Njoroge等[26]也在大豆中观察到相似的结果:光学显微镜下发现加碱软化后的大豆细胞壁较为完整,而蒸馏水煮制组或者陈年的豆子研磨后,细胞破裂严重。Brummer等[27]和Noah等[28]同样也报道过淀粉颗粒可能由于被细胞壁包围,从而使得消化吸收的速率减慢,进而导致低血糖指数。
2.5 电子鼻分析碱处理对莲藕风味的影响
电子鼻作为一种仿生设备,利用气体传感器阵列的响应曲线来识别样品中的挥发性气味,具有操作简单、灵敏度高、重现性好等优点[29]。图6是不同处理处理莲藕样品的电子鼻主成分分析图,从图中可以看出,数据的累计贡献率为86.16%,其中主成分一的贡献率为65.71%,主成分二的贡献率为20.45%,这两个主成分几乎反应了样品的所有信息。同一样品之间可能因为传感器的不稳定性导致平行数据间的差异,但总体来说仍表现出良好的聚类特性。样品在分布图上距离越近代表香气组成相似度越高,蒸馏水烹煮和0.1%的碳酸氢钠烹煮对莲藕特征风味的影响不大,能够在不同口感要求的基础上保持一定的莲藕风味。碳酸氢钠处理的莲藕数据都落在PC1的正半轴上,而蒸馏水煮制的莲藕都落在了PC1的负半轴上,而在PC2上并无显著差异(P>0.05),说明加碱处理对于煮后莲藕风味的影响主要在PC1上,加碱处理确实对莲藕的风味具有一定的影响,但是PC2上的相似分布说明加碱烹煮仍然保持了莲藕的部分特征性挥发性风味成分,主体风味成分接近。与对照组相比,碱处理后感应值差别较大的是P30/2(对有机化合物灵敏)、P10/2(对易燃气体灵敏)、P40/2(对氧化能力较强的气体灵敏)、T70/2(对芳香族化合物灵敏),说明电子鼻主要依靠这四种传感器对两种处理的藕进行区分。电子鼻分析的是风味物质整体对香气的贡献,为了进一步分析加碱烹煮对莲藕挥发性成分的影响,采用GC-MS进一步分析鉴定。
2.6 GC-MS分析碱处理对莲藕风味的影响
本实验采用固相微萃取技术对不同处理莲藕的挥发性风味物质进行萃取,利用GC-MS联用技术对挥发性风味物质进行解析,其总离子流图见图7,挥发性物质种类及其相对含量见表3。
表 3 固相微萃取-气质联用法测定不同处理莲藕的挥发性物质种类及相对含量(%)Table 3. SPME-GCMS method for the determination of the types and relative contents of volatile substances in different treatments of lotus rhizome (%)英文名 中文名 RT(min) DW煮制 SB煮制 Dimethyl sulfide 二甲基硫 1.99 15.17 29.73 1-Pentanol 正戊醇 4.28 nd 2.15 Hexanal 正己醛 5.76 4.40 2.11 Furan, 2-pentyl- 2-正戊基呋喃 11.72 6.27 nd Octanal 正辛醛 12.11 9.10 2.29 1-Hexanol, 2-ethyl- 2-乙基己醇 12.92 6.72 8.58 Undecane 十一烷 13.78 1.87 1.23 Nonanal 壬醛 15.30 33.22 9.98 Carveol 香芹醇 15.61 0.56 nd Undecanal 十一醛 15.94 2.98 nd Eicosanoic acid, 2-ethyl-2-methyl-, methyl 2-乙基-2-甲基花生酸 16.65 nd 2.46 Hexanoic acid, 2-methyl-2-propyl-, methyl 2-甲基-2-丙基己酸 16.79 nd 0.97 Eicosanoic acid, 2-ethyl-2-methyl-, methyl ester 2-乙基-2-甲基花生酸甲酯 16.86 nd 1.01 Eicosanoic acid, 2-ethyl-2-methyl-, methyl 2-乙基-2-甲基花生酸 17.00 nd 1.41 Hexanoic acid, 2-methyl-2-propyl-, methyl ester 2-甲基-2-丙基己酸甲酯 17.35 nd 4.31 5-Methyl-3-propylhexanoic acid, methyl ester 5-甲基-3-丙基己酸 17.40 nd 3.69 Butanoic acid, 2-ethyl-, methyl ester 2-乙基丁酸甲酯 17.55 nd 1.98 Butanoic acid, 2-acetyl-3-methyl-, methyl 2-乙酰基-3-甲基丁酸 17.72 nd 4.22 Butanoic acid, 2-acetyl-3-methyl-, ethyl ester 2-乙酰基-3-甲基丁酸乙酯 17.86 nd 0.88 Dodecane 正十二烷 18.19 2.78 2.02 Decanal 葵醛 18.32 8.04 2.81 3-Phenylpropanol 3-苯丙醇 18.97 0.96 nd Pentadecane 正十五烷 20.29 nd 1.14 Hexadecane 十六烷 20.31 nd 0.75 Dodecane 正十二烷 21.01 3.49 1.14 Butylated Hydroxytoluene 2,6-二叔丁基对甲酚 26.24 4.55 13.85 注:RT为保留时间;nd代表未检出。 由检测结果得知,蒸馏水煮制的莲藕风味组成有14种,加碱煮制之后的风味组成共22种。在已鉴定出的风味物质成分中,有10种成分是水煮和碱煮莲藕共有的,它们主要属于酯类、链烷和萜烯类化合物,主要风味成分是:二甲基硫、正辛醛、壬醛、葵醛,2,6-二叔丁基对甲酚,这些风味物质基本上代表了莲藕的典型风味特征,说明莲藕的呈香风味并不是由单一一种物质决定,而是由多种物质共同起作用。正辛醛在香料工业上常用于配制玫瑰、香石竹、橙花、桔香古龙等香精,在食品工业上用以产生甜橙香气;壬醛具有玫瑰、柑橘等香气,有较强的油脂气味。二甲基硫是多种食品的重要香气及风味成分,可用于食品香料添加剂[30],通常被描述为芦笋、玉米的味道,郭斐等[31]也在8款建宁莲子中均鉴定出二甲基硫。
加碱处理后,莲藕的二甲基硫含量从对照组的15.17%上升到29.73%,说明碱处理可以显著提高莲藕风味物质二甲基硫的含量(P<0.05)。除此以外,加碱处理后各种有机酸和酯类(一般具有令人愉快的水果香气、呈清香果香)等风味物质开始出现,共同作用增加碱煮莲藕风味;加碱处理之后也有部分风味物质出现了下降的趋势,如正己醛、正辛醛、壬醛、葵醛等。醛类化合物一般是莲藕在煮制的过程中脂肪氧合酶催化下不饱和脂肪酸氧化形成过氧化物的过程中产生的[32],脂质氧化是生成莲藕风味的重要途径,形成莲藕的蒸煮风味,0.1%碳酸氢钠处理后对脂质氧化反应有一定抑制作用,因此导致醛类物质含量下降。2-正戊基呋喃(呈蔬菜香、豆香,亚油酸氧化产生)、香芹醇、十一醛、3-苯丙醇在碱处理后未检出,说明碳酸氢钠处理后此类风味物质消失,或含量低于检测限。韩丽娟等[33]发现不同品种水煮莲藕挥发性物质的种类和含量不同都有可能造成风味差异,并且不同类型的挥发性成分会呈现不同的味觉体验。
在莲藕的挥发性物质中还检测到较为大量的2,6-二叔丁基对甲酚,2,6-二叔丁基对甲酚是一种已知的抗氧化剂,对于真菌包括尖孢镰刀菌的生长具有一定的抑制作用[34]。2,6-二叔丁基对甲酚可以保持食品的新鲜、营养成分、口味、颜色,作为抗氧化剂广泛用于药品和食品中[35],它的大量出现可能与莲藕是多年生水生蔬菜,在生长发育的过程中受到了水体污染的影响有关。
韩小苗等[36]采用正戊烷/二氯甲烷(体积比2:1)萃取结合气相色谱-质谱联用仪(GC-MS)分析,对三种不同品种的鲜藕风味进行了测定,结果表明三种鲜藕的风味物质主要是酯类、烷烃类和芳香烃类化合物,其中的酯类物质对鲜藕的风味贡献最大并且占总检出物质的65%左右。罗庆[37]利用有机试剂萃取结合气象色谱质谱联用技术研究了不同的鄂莲5号杂交品种烹煮不同时间后的风味变化,结果表明鲜藕当中的主要风味物质是苯甲酸乙酯、十四酸甲酯、十八烷,风味物质含量也会由于煮制和蒸制处理的不同而发生显著变化。
3. 结论
0.1% AA处理可以显著提高水煮莲藕片的硬度,处理之后莲藕颜色发白。0.1% SB处理可以显著降低莲藕的煮制硬度,处理之后藕片颜色红润。热处理方式在一定程度上影响着植物性食品细胞结构,从而影响其质构性质,需要进一步对细胞壁进行详细的生化分析或微观结构研究,来解释莲藕硬度和颜色性状变化的客观原因;莲藕鲜样的总酚含量最高,经过煮制之后,莲藕总酚含量显著下降,AA处理组可以显著提高莲藕的总酚含量,SB处理组与蒸馏水处理组之间并无显著差异;莲藕鲜样的VC含量最高,煮制之后不同处理组的VC含量均显著下降,且不同处理组之间无显著性差异;AA处理组和对照组之间在体外模拟消化实验中无显著差异,然而碳酸氢钠软化处理会使得莲藕在短暂匀浆处理之后释放到消化液中的碳水化合物总量降低,这与不同的pH环境中细胞壁组织破碎松散程度及莲藕淀粉水解程度差异有关,研究酸碱烹煮后莲藕的体外模拟胃肠消化实验可以为植物性食物代谢动力学、营养物质生物利用率评估等方面提供更多参考;电子鼻的结果表明,碳酸氢钠处理组和蒸馏水对照组之间的风味具有差异,固相微萃取-气相色谱质谱联用技术进一步表明莲藕的风味主要是由二甲基硫、正辛醛、壬醛、葵醛等物质组成,碳酸氢钠处理后二甲基硫显著增加,各种有机酸、以及酯类化合物开始出现,代表了碳酸氢钠烹煮后莲藕出现的特征风味。本研究为烹煮过程中不同食品添加剂的加入对莲藕的营养品质及风味的影响研究提供参考。但是关于较低浓度下醋酸烹煮对莲藕风味的影响及酸碱烹煮对莲藕呈味物质的影响机制仍然有待进一步探究。
-
图 2 不同处理对莲藕总酚含量的影响
注:使用Duncan多重比较测试,不同字母表示不同处理间差异显著(P<0.05);图3同。
Figure 2. Effects of different treatments on the content of total phenols in lotus rhizome
表 1 各传感器的响应特性
Table 1 Response characteristics of each sensor
传感器名称 性能描述 参考物质 LY2/LG 对氧化能力较强的气体灵敏 氯、氟、氮氧化合物 LY2/G 对有毒气体灵敏 氨、胺类、碳氧化合物 LY2/AA 对有机化合物灵敏 乙醇、丙酮、氨 LY2/GH 对有毒气体灵敏 氨、胺类化合物 LY2/gCTL 对易燃气体灵敏 硫化氢 LY2/gCT 对有毒气体灵敏 丙烷、丁烷 T30/1 对有机化合物灵敏 极性化合物、氯化物 P10/1 对可燃气体灵敏 碳氢化合物、氨、氯 P10/2 对易燃气体灵敏 非极性化合物;甲烷、乙烷 P40/1 对氧化能力较强的气体灵敏 氟 T70/2 对芳香族化合物灵敏 甲苯、二甲苯 PA/2 对有机化合物、有毒气体灵敏 乙醇、氨水 P30/1 对可燃气体、有机化合物灵敏 碳氢化合物、燃烧产物 P40/2 对氧化能力较强的气体灵敏 氯、硫化氢、氟化物 P30/2 对有机化合物灵敏 硫化氢、酮 T40/2 对氧化能力较强的气体灵敏 氯 T40/1 对氧化能力较强的气体灵敏 氟 TA/2 对有机化合物灵敏 乙醇 表 2 酸碱处理对莲藕L*值、a*值以及硬度的影响
Table 2 Effects of acid and alkali treatment on L* value, a* value and the hardness of lotus rhizome
样品处理组 L*值 a*值 硬度(g) DW煮制 55.17±0.23b 1.87±0.21b 1745.62±94.12b 0.1% AA煮制 58.27±0.43a 1.24±0.31c 2475.71±74.47a 0.1% SB煮制 51.49±0.19c 2.79±0.15a 1347.49±83.49c 注:同列不同小写字母表示存在显著差异(P<0.05)。 表 3 固相微萃取-气质联用法测定不同处理莲藕的挥发性物质种类及相对含量(%)
Table 3 SPME-GCMS method for the determination of the types and relative contents of volatile substances in different treatments of lotus rhizome (%)
英文名 中文名 RT(min) DW煮制 SB煮制 Dimethyl sulfide 二甲基硫 1.99 15.17 29.73 1-Pentanol 正戊醇 4.28 nd 2.15 Hexanal 正己醛 5.76 4.40 2.11 Furan, 2-pentyl- 2-正戊基呋喃 11.72 6.27 nd Octanal 正辛醛 12.11 9.10 2.29 1-Hexanol, 2-ethyl- 2-乙基己醇 12.92 6.72 8.58 Undecane 十一烷 13.78 1.87 1.23 Nonanal 壬醛 15.30 33.22 9.98 Carveol 香芹醇 15.61 0.56 nd Undecanal 十一醛 15.94 2.98 nd Eicosanoic acid, 2-ethyl-2-methyl-, methyl 2-乙基-2-甲基花生酸 16.65 nd 2.46 Hexanoic acid, 2-methyl-2-propyl-, methyl 2-甲基-2-丙基己酸 16.79 nd 0.97 Eicosanoic acid, 2-ethyl-2-methyl-, methyl ester 2-乙基-2-甲基花生酸甲酯 16.86 nd 1.01 Eicosanoic acid, 2-ethyl-2-methyl-, methyl 2-乙基-2-甲基花生酸 17.00 nd 1.41 Hexanoic acid, 2-methyl-2-propyl-, methyl ester 2-甲基-2-丙基己酸甲酯 17.35 nd 4.31 5-Methyl-3-propylhexanoic acid, methyl ester 5-甲基-3-丙基己酸 17.40 nd 3.69 Butanoic acid, 2-ethyl-, methyl ester 2-乙基丁酸甲酯 17.55 nd 1.98 Butanoic acid, 2-acetyl-3-methyl-, methyl 2-乙酰基-3-甲基丁酸 17.72 nd 4.22 Butanoic acid, 2-acetyl-3-methyl-, ethyl ester 2-乙酰基-3-甲基丁酸乙酯 17.86 nd 0.88 Dodecane 正十二烷 18.19 2.78 2.02 Decanal 葵醛 18.32 8.04 2.81 3-Phenylpropanol 3-苯丙醇 18.97 0.96 nd Pentadecane 正十五烷 20.29 nd 1.14 Hexadecane 十六烷 20.31 nd 0.75 Dodecane 正十二烷 21.01 3.49 1.14 Butylated Hydroxytoluene 2,6-二叔丁基对甲酚 26.24 4.55 13.85 注:RT为保留时间;nd代表未检出。 -
[1] 李良俊, 张晓冬, 潘恩超, 等. 莲藕膨大过程中淀粉合成相关酶的活性变化及其与淀粉积累的关系[J]. 中国农业科学,2006,39(11):2307−2312. [LI L J, ZHANG X D, PAN E C, et al. Relationship of starch synthesis with its related enzymes' activities during rhizome development of lotus (Nelumbo Nucifera Gaertn)[J]. Scientia Agricultura Sinica,2006,39(11):2307−2312. doi: 10.3321/j.issn:0578-1752.2006.11.021 [LI L J, ZHANG X D, PAN E C, et al. Relationship of starch synthesis with its related enzymes' activities during rhizome development of lotus (Nelumbo Nucifera Gaertn)[J]. Scientia Agricultura Sinica, 2006, 39(11): 2307-2312. doi: 10.3321/j.issn:0578-1752.2006.11.021
[2] 彭立军, 彭西甜, 龚艳, 等. 湖北省莲藕质量安全状况及产业发展的思考[J]. 农产品质量与安全,2017(5):56−59. [PENG L J, PENG X T, GONG Y, et al. Quality and safety of lotus root in Hubei Province and its industrial development[J]. Quality and Safety of Agro-Products,2017(5):56−59. doi: 10.3969/j.issn.1674-8255.2017.05.011 [PENG L J, PENG X T, GONG Y, et al. Quality and safety of lotus root in Hubei Province and its industrial development[J]. Quality and Safety of Agro-Products, 2017(5): 56-59. doi: 10.3969/j.issn.1674-8255.2017.05.011
[3] 张福平, 陈蔚辉, 黄泽虹, 等. 莲藕的营养保健功能[J]. 中国果菜,2002(6):43. [ZHANG F P, CHEN W H, HUANG Z H, et al. The nutrition and health function of lotus root[J]. China Fruit and Vegetable,2002(6):43. doi: 10.3969/j.issn.1008-1038.2002.06.054 [ZHANG F P, CHEN W H, HUANG Z H, et al. The nutrition and health function of lotus root[J]. China Fruit and Vegetable, 2002(6): 43. doi: 10.3969/j.issn.1008-1038.2002.06.054
[4] 孙杰, 陆双双, 徐燕燕, 等. 莲藕不同部位酚类物质含量、组成及抗氧化活性比较[J]. 武汉轻工大学学报,2015,34(2):20−25. [SUN J, LU S S, XU Y Y, et al. Comparison on the content, composition and antioxidant activity of phenolics among different parts of lotus root[J]. Journal of Wuhan Polytechnic University,2015,34(2):20−25. doi: 10.3969/j.issn.2095-7386.2015.02.005 [SUN Jie, LU S S, XU Y Y, et al. Comparison on the content, composition and antioxidant activity of phenolics among different parts of lotus root[J]. Journal of Wuhan Polytechnic University, 2015, 34(2): 20-25. doi: 10.3969/j.issn.2095-7386.2015.02.005
[5] 罗登宏, 周桃英, 袁仲, 等. 莲藕多糖的降血糖活性及对体内抗氧化能力的影响[J]. 安徽农业科学,2011,39(6):3334−3335. [LUO D H, ZHOU T Y, YUAN Z, et al. Hypoglycemic activity of Rhizoma Nelumbinis Nuciferae polysaccharide and its effect on in vivo antioxidant activity[J]. Journal of Anhui Agricultural Sciences,2011,39(6):3334−3335. doi: 10.3969/j.issn.0517-6611.2011.06.072 [LUO D H, ZHOU T Y, YUAN Z, et al. Hypoglycemic activity of RHIZOMA NELUMBINIS NUCIFERAE polysaccharide and its effect on in vivo antioxidant activity[J]. Journal of Anhui Agricultural Sciences, 2011, 39(6): 3334-3335. doi: 10.3969/j.issn.0517-6611.2011.06.072
[6] 金文筠. 藕节膳食纤维制备及其抑菌作用研究[D]. 武汉: 华中农业大学, 2016. [JIN W J. Extraction of dietary fibers from nodes of lotus root and its effect on body weight[D]. Wuhan: Huazhong Agricultural University, 2016. [7] 孙付军, 靳光乾, 张敏, 等. 藕节炒炭止血有效活性部位及其成分筛选研究[J]. 辽宁中医杂志,2011,38(1):177−178. [SUN F J, JIN G Q, ZHANG M, et al. Lotus rhizome node carbonizing by stir-frying active site of bleeding and its components of effective screening study[J]. Liaoning Journal of Traditional Chinese Medicine,2011,38(1):177−178. [SUN F J, JIN G Q, ZHANG M, et al. Lotus Rhizome Node carbonizing by stir-frying active site of bleeding and its components of effective screening study[J]. Liaoning Journal of Traditional Chinese Medicine, 2011, 38(1): 177-178.
[8] SHINGO U, MASAHIRO H, KUMIKO K, et al. Physical properties of root crops treated with novel softening technology capable of retaining the shape, color, and nutritional value of foods[J]. Dysphagia,2015,30(2):105−113. doi: 10.1007/s00455-014-9581-2
[9] KUMAR R, VIJAYALAKSHMI S, NADANASABAPATHI S. Effect of thermal and nonthermal processing on textural quality of plant tissues[J]. Critical Reviews in Food Science and Nutrition,2016,56(16):2665−2694. doi: 10.1080/10408398.2014.908348
[10] 赵雯霖. 马铃薯及莲藕组织中多糖特性对其硬度影响机理研究[D]. 武汉: 华中农业大学, 2017: 11−13 ZHAO Wenlin. Mechanisms of the tissue hardness change caused by p0lysaccharide characteristics in potatoes and lotus rhizomes[D]. Wuhan: Huazhong Agricultural University, 2017: 11−13.
[11] CHIGWEDERE C M, OLAOYE T F, KYOMUGASHO C, et al. Mechanistic insight into softening of Canadian wonder common beans (Phaseolus vulgaris) during cooking[J]. Food Research International,2018,106:522−531. doi: 10.1016/j.foodres.2018.01.016
[12] ZHAO W, XIE W, DU S, et al. Changes in physicochemical properties related to the texture of lotus rhizomes subjected to heat blanching and calcium immersion[J]. Food Chemistry,2016,211:409−414. doi: 10.1016/j.foodchem.2016.05.075
[13] KAZEMI M, KHODAIYAN F, HOSSEINI S S. Eggplant peel as a high potential source of high methylated pectin: Ultrasonic extraction optimization and characterization[J]. LWT-Food Science and Technology,2019,105:182−189. doi: 10.1016/j.lwt.2019.01.060
[14] ZHAO W, SHEHZAD H, YAN S, et al. Acetic acid pretreatment improves the hardness of cooked potato slices[J]. Food Chemistry,2017,228:204−210. doi: 10.1016/j.foodchem.2017.01.156
[15] LIU J, WEN C W, WANG M, et al. Enhancing the hardness of potato slices after boiling by combined treatment with lactic acid and calcium chloride: Mechanism and optimization[J]. Food Chemistry,2020,308:124832. doi: 10.1016/j.foodchem.2019.05.106
[16] 邹妍, 李佳容, 李飞, 等. 利用乙酸协同氯化钙提升马铃薯片热加工质构特性[J]. 现代食品科技,2022,38(4):140−146, 200. [ZOU Y, LI J R, LI F, et al. Improving texture properties of sliced potatoes during thermal processing by acetic acid in synergy with calcium chloride[J]. Modern Food Science and Technology,2022,38(4):140−146, 200. ZOU Y, LI J R, LI F, et al. Improving texture properties of sliced potatoes during thermal processing by acetic acid in synergy with calcium chloride[J]. Modern Food Science and Technology, 2022, 38(4): 140-146, 200.
[17] 高畅, 程大海, 高欣, 等. 蓝莓果渣提取物总酚含量及抗氧化活性研究[J]. 植物研究,2010,30(2):253−256. [GAO C, CHENG D H, GAO X, et al. Total phenolic content and antioxidant activities of blueberry pomace extracts[J]. Bulletin of Botanical Research,2010,30(2):253−256. doi: 10.7525/j.issn.1673-5102.2010.02.022 [GAO C, CHENG D H, GAO X, et al. Total phenolic content and antioxidant activities of blueberry pomace extracts[J]. Bulletin of Botanical Research, 2010, 30(2): 253-256. doi: 10.7525/j.issn.1673-5102.2010.02.022
[18] 李新原, 李斌, 颜廷才, 等. 超高压与超声波对蓝靛果多酚提取及抗氧化活性的影响[J]. 食品科学,2017,38(2):271−277. [LI X Y, LI B, YAN T C, et al. Comparative effects of ultra-high pressure and ultrasonic treatment on the extraction and antioxidant activity of polyphenols from lonicera caerulea fruits[J]. Food Science,2017,38(2):271−277. doi: 10.7506/spkx1002-6630-201702042 [LI X Y, LI B, YAN T C, et al. Comparative effects of ultra-high pressure and ultrasonic treatment on the extraction and antioxidant activity of polyphenols from lonicera caerulea fruits[J]. Food Science, 2017, 38(2): 271-277. doi: 10.7506/spkx1002-6630-201702042
[19] 刘婧琳, 郭玉蓉, 张敏龙, 等. 酸性条件下提取苹果渣多酚[J]. 农产品加工(学刊),2012(5):22−26. [LIU J L, GUO Y R, ZHANG M L, et al. Using acetic acid as solvent to extract polyphenol from apple pomace[J]. Academic Periodical of Farm Products Processing,2012(5):22−26. [LIU J L, GUO Y R, ZHANG M L, et al. Using acetic acid as solvent to extract polyphenol from apple pomace[J]. Academic Periodical of Farm Products Processing, 2012(5): 22-26.
[20] 于新, 蓝碧锋, 张金云, 等. 莲藕采后生理及保鲜技术研究进展[J]. 广州食品工业科技,2002(3):50−53. [YU X, LAN B F, ZAHNG J Y, et al. Progress in the research on post-harvest physiology and storage techniques of Nelumbo Nucifera Gaertn[J]. Guangzhou Food Science & Technology,2002(3):50−53. [YU X, LAN B F, ZAHNG J Y, et al. Progress in the research on post-harvest physiology and storage techniques of Nelumbo Nucifera Gaertn[J]. Guangzhou Food Science & Technology, 2002(3): 50-53.
[21] 葛声, 冯晓慧, 唐彦, 等. 三种烹饪方式对蔬菜中维生素C含量的影响研究[J]. 中国食物与营养,2012,18(10):85−88. [GE S, FENG X H, TANG Y, et al. Effects of different cooking methods on vitamin C in vegetables[J]. Food and Nutrition in China,2012,18(10):85−88. [GE S, FENG X H, TANG Y, et al. Effects of different cooking methods on vitamin C in vegetables[J]. Food and Nutrition in China, 2012, 18(10): 85-88.
[22] HUNTER K J, FLETCHER J M. The antioxidant activity and composition of fresh, frozen, jarred and canned vegetables[J]. Innovative Food Science and Emerging Technologies,2018,3(4):399−406.
[23] WANG F L, FANG R, QIN L M, et al. A review of the effects of cooking methods on the nutrition, antioxidant capacity and color of vegetables[J]. Science and Technology of Food Industry,2022,43(2):411−419.
[24] 曾翔云. 维生素C的生理功能与膳食保障[J]. 中国食物与营养,2005(4):52−54. [ZENG X Y. The physiological function and guarantee measures of vitamin C[J]. Food and Nutrition in China,2005(4):52−54. doi: 10.3969/j.issn.1006-9577.2005.04.017 [ZENG X Y. The physiological function and guarantee measures of vitamin C[J]. Food and Nutrition in China, 2005(4): 52-54. doi: 10.3969/j.issn.1006-9577.2005.04.017
[25] LIU Y, LIU J, LIU G, et al. Sodium bicarbonate reduces the cooked hardness of lotus rhizome via side chain rearrangement and pectin degradation[J]. Food Chemistry,2021(2):130962.
[26] NJOROGE D M, KINYANJUI P K, CHIGWEDERE C M, et al. Mechanistic insight into common bean pectic polysaccharide changes during storage, soaking and thermal treatment in relation to the hard-to-cook defect[J]. Food Research International,2016,81:39−49. doi: 10.1016/j.foodres.2015.12.024
[27] BRUMMER Y, KAVIANI M, TOSH S M. Structural and functional characteristics of dietary fibre in beans, lentils, peas and chickpeas[J]. Food Research International,2015,67:117−125(Jan). doi: 10.1016/j.foodres.2014.11.009
[28] NOAH L, GUILLON F, BOUCHET B, et al. Digestion of carbohydrate from white beans (Phaseolus vulgaris L.) in healthy humans[J]. Journal of Nutrition,1998,128(6):977−985. doi: 10.1093/jn/128.6.977
[29] 赵梦醒, 丁晓敏, 曹荣, 等. 基于电子鼻技术的鲈鱼新鲜度评价[J]. 食品科学,2013,34(6):143−147. [ZHAO M X, DING X M, CAO R, et al. Identification of lateolabrax japonicus freshness by electronic nose[J]. Food Science,2013,34(6):143−147. doi: 10.7506/spkx1002-6630-201306031 [ZHAO M X, DING X M, CAO R, et al. Identification of lateolabrax japonicus freshness by electronic nose[J]. Food Science, 2013, 34(6): 143-147. doi: 10.7506/spkx1002-6630-201306031
[30] 孙军勇, 顾国贤. 啤酒中二甲基硫化物的形成机理及其控制[J]. 酿酒,2001(2):53−57. [SUN J Y, GU G X. The control and formation of dimethyl sulfide in beer[J]. Liquor Making,2001(2):53−57. [SUN J Y, GU G X. The control and formation of dimethyl sulfide in beer[J]. Liquor Making, 2001(2): 53-57.
[31] 郭斐, 李如玉, 苏晓霞, 等. 建宁莲子挥发性风味化合物分析[J]. 食品安全质量检测学报,2022,13(21):6862−6869. [GUO F, LI R Y, SU X X. Analysis of volatile flavor compounds of Jianning lotus seeds[J]. Journal of Food Safety and Quality,2022,13(21):6862−6869. [GUO F, LI R Y, SU X X. Analysis of volatile flavor compounds of Jianning lotus seeds[J]. Journal of Food Safety and Quality, 2022, 13(21): 6862-6869.
[32] 吴燕, 周君, 明庭红, 等. 基于电子鼻结合气相色谱-质谱联用技术解析不同产地马铃薯挥发性物质的差异[J]. 食品科学,2016,37(24):130−136. [[WU Y, ZHOU J, MING T H, et al. Analysis of volatile components of potato from different habitats by electronic nose and GC-MS[J]. Food Science,2016,37(24):130−136. doi: 10.7506/spkx1002-6630-201624020 [WU Y, ZHOU J, MING T H, et al. Analysis of volatile components of potato from different habitats by electronic nose and GC-MS[J]. Food Science, 2016, 37(24): 130-136. doi: 10.7506/spkx1002-6630-201624020
[33] 韩丽娟, 黄楚雄, 李洁, 等. 不同品种莲藕水煮风味物质比较[J]. 食品科学,2020,41(22):245−251. [HAN L J, HUANG C X, LI J, et al. Comparison of flavor substances of water-boiled lotus roots from different varieties[J]. Food Science,2020,41(22):245−251. doi: 10.7506/spkx1002-6630-20191104-037 [HAN L J, HUANG C X, LI J, et al. Comparison of flavor substances of water-boiled lotus roots from different varieties[J]. Food Science, 2020, 41(22): 245-251. doi: 10.7506/spkx1002-6630-20191104-037
[34] LI S, LI X, LAMIKANRA O, et al. Effect of cooking on physicochemical properties and volatile compounds in lotus root (Nelumbo nucifera Gaertn)[J]. Food Chemistry,2017,216:316−323. doi: 10.1016/j.foodchem.2016.08.044
[35] 左玉, 吴俏卓, 王接昌, 等. 抗氧化剂在食品中的应用[J]. 粮食与油脂,2022,35(4):32−34, 38. [ZUO Y, WU Q Z, WANG J C, et al. The application of antioxidants in food[J]. Cereals & Oils,2022,35(4):32−34, 38. doi: 10.3969/j.issn.1008-9578.2022.04.009 ZUO Y, WU Q Z, WANG J C, SONG Z. The application of antioxidants in food[J]. Cereals & Oils, 2022, 35(4): 32-34, 38. doi: 10.3969/j.issn.1008-9578.2022.04.009
[36] 韩小苗, 罗庆, 吴苏喜. 3种鲜藕的质构特性及风味物质测定与评价[J]. 食品与机械,2017,33(9):64−68. [HAN X M, LUO Q, WU S X. Evaluation of textural properties and flavor substances of three varieties of fresh lotus root[J]. Food & Machinery,2017,33(9):64−68. HAN X M, LUO Q, WU S X. Evaluation of textural properties and flavor substances of three varieties of fresh lotus root[J]. Food & Machinery, 2017, 33(9): 64-68.
[37] 罗庆. 不同品种莲藕的风味特性及加工稳定性研究[D]. 武汉: 武汉轻工大学, 2015 LUO Q. Study on the flavor characteristics and processing stability of different varieties of lotus root[D]. Wuhan: Wuhan Polytechnic University, 2015.
-
期刊类型引用(8)
1. 张乾坤,康桦华,刘梦竹,涂杜,徐志宏. 肉品保鲜包装材料与新技术研究进展. 包装工程. 2024(03): 126-138 .  百度学术
百度学术
2. 王金霞,杨波,罗瑞明,李荣,陈雪妍,张倩,胡丽筠. 宰后贮藏期间滩羊肉线粒体氧化磷酸化与色泽稳定性的关系. 食品科学. 2024(08): 202-209 .  百度学术
百度学术
3. 王华安,刘启超,黄得草,张利军,刘美玉. 中高氧气调包装对冷鲜鸭肉品质的影响. 农产品加工. 2024(21): 36-40+46 .  百度学术
百度学术
4. 赵红波,叶磊海,杨黎耀,郎欢,陆燕萍,柴振林,欧菊芳. 冷鲜猪肉在贮藏过程中生物胺含量变化及不同包装方式对生物胺含量变化的影响研究. 食品安全质量检测学报. 2023(12): 126-135 .  百度学术
百度学术
5. 刘文轩,罗欣,杨啸吟,张一敏,朱立贤,毛衍伟,梁荣蓉,马伟民,杨振刚. 脂肪含量对雪花牛排在高氧气调包装贮藏期间肉色稳定性的影响. 现代食品科技. 2022(02): 110-118 .  百度学术
百度学术
6. 霍霞飞,张德权,苏媛媛,古明辉,陈丽,李少博,王卫,郑晓春. 三甲胺和二甲胺表征冷鲜羊肉新鲜度. 肉类研究. 2022(07): 13-19 .  百度学术
百度学术
7. 周立,张锐,王卫,张佳敏,王素,侯成立,白婷. 不同气调包装对冷鲜羊肉保鲜效果研究. 包装工程. 2022(21): 1-9 .  百度学术
百度学术
8. 马红艳,张德权,陈丽,郑晓春. 荧光特征分子表征冷鲜羊肉新鲜度. 农业工程学报. 2022(22): 270-279 .  百度学术
百度学术
其他类型引用(8)





 下载:
下载:






 下载:
下载:



