Effects of Cryo-grinding on the Extraction and Physicochemical Properties of Silk Fibroin
-
摘要: 本文将冷冻研磨技术引入到丝素蛋白的提取工艺中,以期实现丝素蛋白高效制备且性能可控的目的。具体地,将蚕茧在液氮中预冻12 h后进行低温研磨,并将得到的样品(GSF322)与未研磨样品SF(对照)进行理化性能对比。结果表明,SF,GSF322的得率相当,但脱胶时间从90 min减少到40 min;圆二色谱分析显示,预处理过程不会破坏丝素蛋白的立体结构;浊度实验研究表明,通过调控研磨时间可以有效调节丝素蛋白的体外组装能力,研磨3 min的丝素样品具有最好的体外组装能力;Zeta电位实验结果显示,预处理后,GSF322分子链上带正电荷的基团增多,更多-NH2的暴露导致材料亲水性增强。溶解性实验则证明,经过研磨处理后的GSF322在水中溶解率更高。热稳定性测试中,GSF322的脱水峰较SF的峰值高,表明其热稳定性更好。综合来说,在丝素蛋白的提取中,用冷冻研磨法来进行蚕茧的预处理,不仅可以提高丝素的提取效率,而且也可以调控其理化性能。Abstract: Herein, cryo-grinding technique was introduced into the extraction process of silk fibroin, aiming to achieve efficient preparation and controllable performance of silk fibroin. More specifically, the cocoon was pre-frozen in liquid nitrogen for 12 h before being ground, and the physical and chemical properties of the obtained sample (GSF322) were compared with the control one (SF). Results revealed that, compared with SF, the degumming duration for GSF322 dwindled from 90 min to 40 min with a close yield. Circular dichroism analysis demonstrated that the pretreatment process would not destroy the steric structure of the macromolecule. Turbidity assay implied that the assembly activity of the polymer in vitro could also be manipulated via assorted grinding periods, among which the sample ground for 3 min had the best assembly capacity. Dissection of the Zeta potential displayed that, after grinding, the positively-charged groups on the molecular chain of GSF322 might multiply, resulting in the exposure of more -NH2 groups in the surroundings and enhanced hydrophilicity of the material, which was in accordance with the trend from the water solubility experiment. Moreover, in the thermostability test, the dehydration peak for GSF322 was higher than that of SF, showing better thermal stability. To conclude, concerning the extraction process for silk fibroin, the cryogrinding approach sheds light on both the strengthening of the extraction efficiency as well as the tuning of the physiochemical aptitudes of the polymer.
-
Keywords:
- silk fibroin /
- degumming /
- cryo-grinding /
- self-assembly /
- thermal stability
-
丝素蛋白(Silk fibroin,SF)是从家蚕蚕茧中提取的一种蛋白质,是熟蚕结茧时所分泌的丝液凝固而成的连续长纤维,它被认为是唯一一种以丝状形式存在的天然纤维,同时,丝素蛋白也是美国食品和药品监督管理局(FDA)批准的天然蛋白质[1],近年来,丝素蛋白以及含有丝素蛋白的复合材料也越来越多地应用于医疗卫生[2-6]、食品[7-9]、化妆品[10]等领域。丝素蛋白不易溶于水,主要由重链、轻链和P25蛋白组成,比例为6:6:1[11-12];丝素蛋白含有人体必需氨基酸,且无毒、无免疫原性,研究证明丝素蛋白在体外和体内的生物相容性更好,可支持细胞和组织的生长[13-14]。而蚕茧外层的丝胶已被证明会引起炎症,当丝素蛋白和丝胶蛋白混合使用时,会引起免疫原性[15-16],因此,蚕茧需经脱胶步骤制备丝素蛋白。
蚕茧的脱胶是丝素蛋白在食品及医学材料领域应用的关键步骤之一[17]。常见的脱胶方法有碱性试剂脱胶、酸性试剂脱胶、高温高压脱胶、表面活性剂脱胶和蛋白酶脱胶等[18]。碱性脱胶是常用的脱胶方法,其优点是强力、简单、有效,但脱胶过程通常需要重复多次才能完全去除外层丝胶蛋白,因此碱性溶液对内层丝素蛋白也造成损害,会导致丝素蛋白机械性能和丝素蛋白分子量的下降,并且脱胶废水含有大量丝胶,直接排入河道造成环境污染和能源的大量浪费[19-22]。因此,寻找一种减少碱性脱胶时间,同时提高丝素蛋白水溶性的新的提取方法已成为拓展丝素蛋白应用的当务之急。
在蛋白质的提取方法中,研磨的应用越来越多,研磨属机械力化学,是利用机械能来诱发化学反应或引发材料组织、结构和性能变化,并以此来制备新材料的一门学科[23-24]。冷冻研磨是指借助冷却剂(如液氮)冷却一定时间后进行研磨[25],冷冻研磨技术常应用于生物分析、生物材料和食品粉碎,比如谷物、香料、生物材料和组织等[26-28]。由于热塑性、弹性或纤维材料的研磨效率不如脆性材料,而在液氮中的低温低于大多数材料的脆性点,材料变得易碎,因此可以更有效地研磨[29-30]。冷冻研磨是低温下进行材料粉碎的一种有效手段,通过微粒化物料不仅可以改变材料物性、提高溶解分散速度,研磨过程中强大的机械力还可能引发材料的理化性能变化,起到调控原料性能的作用[31]。目前,还未发现有文献将冷冻研磨预处理方法应用于丝素蛋白的提取中,因此,本文尝试采用冷冻研磨技术对蚕茧进行预处理,并与未预处理得到的丝素蛋白在氨基酸组成、自组装能力、溶解性能及热稳定性等进行对比研究,以此获得调控丝素蛋白理化性能的最优条件。
1. 材料与方法
1.1 材料与仪器
家蚕蚕茧 购于苏州浒关蚕种场;溴化锂 上海展云化工有限公司;无水碳酸钠、氯化钠、碳酸氢钠、氯化钙 国药集团化学试剂有限公司;以上均为分析纯。
MM400冷冻混合球磨仪 弗尔德(上海)仪器设备有限公司;J-1500圆二色谱仪 日本JASCO;GZX-9070MBE 数显鼓风恒温干燥箱 英峪予华仪器厂;L-8900蛋白水解液氨基酸分析系统 日本日立公司;Zetasizer Nano ZS纳米粒度、Zeta电位及分子量分析仪 英国马尔文;Cary-50紫外可见分光光度计 美国Varian 公司;V-1100可见光分光光度计 上海美谱达仪器有限公司;LGJ-10D冷冻干燥机 北京四环科学仪器厂;NEXUS 傅里叶红外光谱分析仪 美国Thermo Nicolet公司;DSC0Q10差示扫描量热仪 美国TA公司。
1.2 实验方法
1.2.1 再生丝素蛋白和冷冻研磨再生丝素蛋白的制备
a.再生丝素蛋白(SF)的制备:取5 g蚕茧,放入500 mL 0.5%(W/V)的Na2CO3中,溶液沸腾后煮30 min,然后取出晾干,再重复此煮沸步骤2次,结束后将蚕丝捞出用去离子水冲洗3~4遍,拧干水分放入烘箱中90 ℃烘3 h。烘干后的脱胶蚕丝用40 mL 9.3 mol/L的溴化锂溶液溶解,溶解后的再生丝素蛋白溶液在4 ℃的冰箱中透析3 d。将透析完的丝素蛋白放入冷冻干燥机中冻干3 d,得到再生丝素蛋白[32](命名为SF,对照样品)。
b.冷冻研磨预处理提取丝素蛋白:将2.0 g蚕茧剪成0.5×0.5 cm的小块,放入液氮中冷冻12 h后,使用MM400冷冻混合球磨仪研磨(研磨频率25 Hz),研磨后在500 mL 0.5%的Na2CO3中煮沸,结束后将蚕丝捞出,后续处理同前述a。
预处理条件:设置不同研磨时间,分别研磨3、4和5 min。煮沸时间为30 min,煮沸次数为3次时,研磨时间为3 min的样品命名为GSF3,研磨时间为4 min的样品命名为GSF4,研磨时间为5 min的样品命名为GSF5。
研究固定研磨时间为3 min,将煮沸时间设置为30 min和20 min,煮沸次数设置为3次和2次进行对比。煮沸30 min,重复3次的样品命名为GSF3,煮沸30 min,重复2次的样品命名为GSF332,煮沸20 min重复2次的样品命名为GSF322。
1.2.2 得率的测定
将样品SF、GSF3、GSF332、GSF322、GSF4、GSF5冻干后称重。得率计算公式如下:
W(%)=W1/W0×100 式中:W0为脱胶前蚕丝重量,g;W1为冻干后丝素蛋白样品重量,g。
1.2.3 红外光谱测定
采用傅里叶红外光谱分析仪测定丝素蛋白的特征吸收峰[33]。取适量KBr粉末,再加入干燥后的样品(GSF322、SF)研磨均匀后压片(KBr与样品的质量比为100:1)。测试范围为2000~600 cm−1,分辨率为8 cm−1,扫描次数为16次。
1.2.4 圆二色谱测定
用超纯水配制0.1 mg/mL的丝素蛋白溶液,超纯水为背景。波长扫描范围设置250~190 nm,50 nm/min扫描速率,扫描精度0.5 nm,扫描3次[27]。
1.2.5 浊度的测定
将2 mg/mL丝素蛋白在紫外分光光度计测试波长为290 nm、时间为120 min、温度为70 ℃的条件下测定吸光值,并绘制浊度曲线[27]。
1.2.6 Zeta电位测定
丝素蛋白水溶液样品质量浓度为1 mg/mL,使用纳米粒度仪测定不同pH(1~7和7.4)下的Zeta电位,每个样品测试3次,结果取平均值。
1.2.7 溶解性测定
称取20 mg冻干丝素蛋白,分别在0.1 mol/L HCl、0.1 mol/L NaOH、0.5% CaCl2和去离子水各1 mL中溶解,溶解后离心过滤,将滤出的残渣在烘箱中烘干2 h,滤纸和残余丝素蛋白一起称重得M1,剩余丝素蛋白质量M=M1-滤纸质量。按以下公式计算溶解率。
溶解率(%)=(20−M)/20×100 式中:20为称取丝素蛋白的质量,g;M为剩余丝素蛋白的质量,g。
1.2.8 热稳定性测定
采用差式热量扫描仪(DSC)测定丝素蛋白样品的热变性温度,将样品装入铝盒,并以空铝盒为空白对照,固体模式测量,3 ℃/min升温速率进行温度扫描,扫描范围在20~250 ℃之间。精确称取10~15 mg左右的样品进行样品的热变性温度的测量。
1.3 数据处理
采用Origin8.5(OriginLab Crop,Northampton,MA,USA)自带统计学软件进行数据处理及分析。
2. 结果与分析
2.1 优化蚕茧的预处理条件
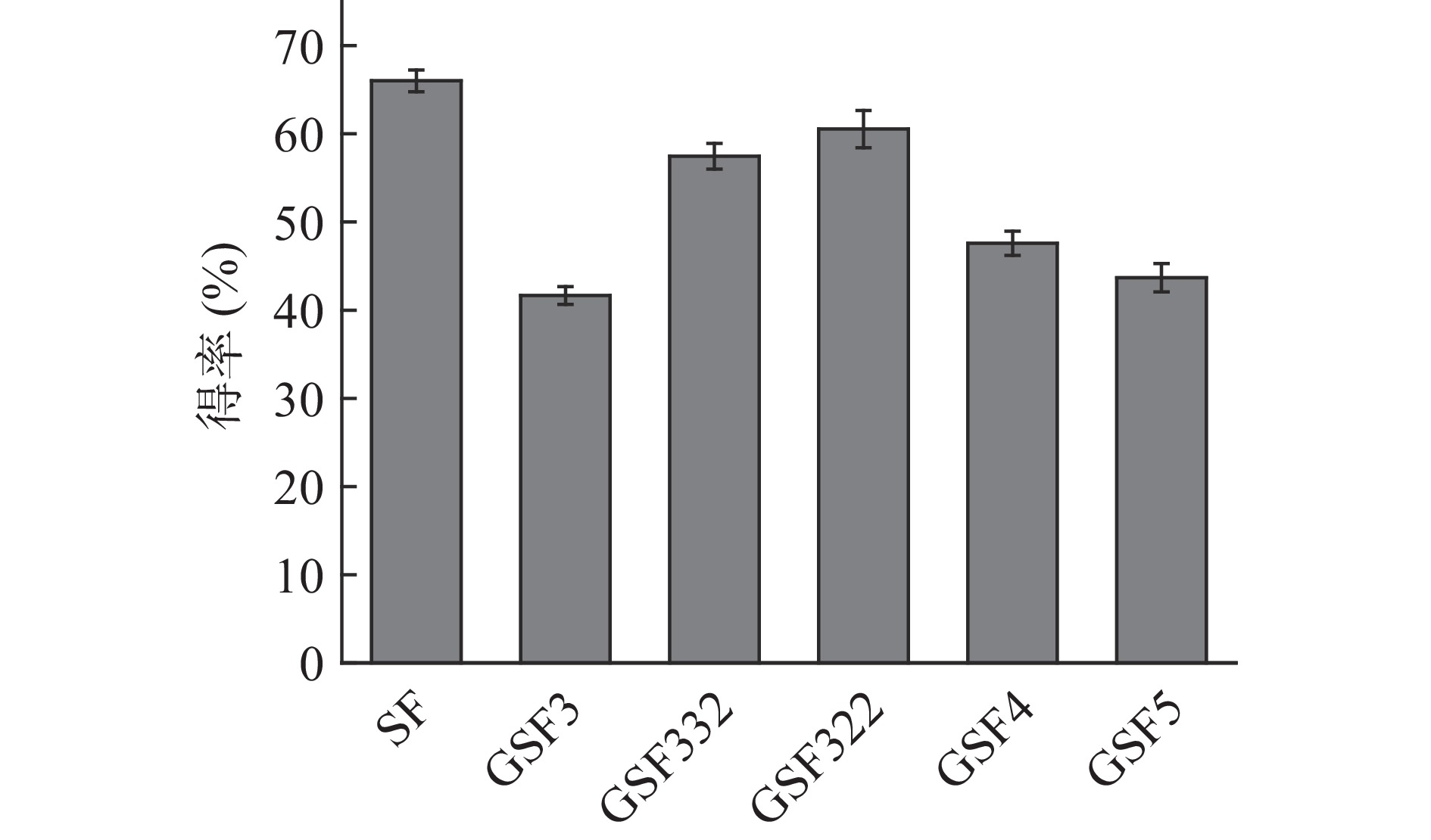
采用冷冻研磨预处理技术提取丝素蛋白,得率如图1所示,由图1可知,样品GSF3、GSF4、GSF5的得率相差不大,但均低于未冷冻研磨得到的再生丝素蛋白SF的得率(66%),得率降低可能的原因是蚕丝在冷冻研磨后需要用碱水煮沸三遍后过滤,由于研磨使得蚕丝粒径变小[31],因此,过滤时会有一定的损失,导致得率下降;另外因为研磨时间过长,部分丝素分子降解为小分子[34-35],在透析过程中也会损失,因此,预处理条件固定为研磨3 min。
当固定研磨时间为3 min时,碱煮时间和次数对样品的得率均有影响,与未冷冻研磨预处理的样品SF相比,样品GSF3的得率仅为41.7%,这可能是因为冷冻研磨后碱煮次数多对丝素蛋白分子中的结构破坏比较大,因此得率降低;当减少碱煮次数时,样品GSF332(碱煮30 min,重复2次)的得率提高至57.5%;进一步减少碱煮时间后,样品GSF322的得率提高至61%,与SF的得率相差不大。因此,本实验考虑效率和环保的影响,选择研磨3 min,脱胶条件为碱煮20 min,重复2次为最佳提取条件。该条件比SF提取步骤少了一次碱煮步骤,同时节约55%(约50 min)的碱煮时间。后续实验中以样品GSF322与SF、GSF4、GSF5的理化测试结果进行比较。
2.2 红外光谱分析
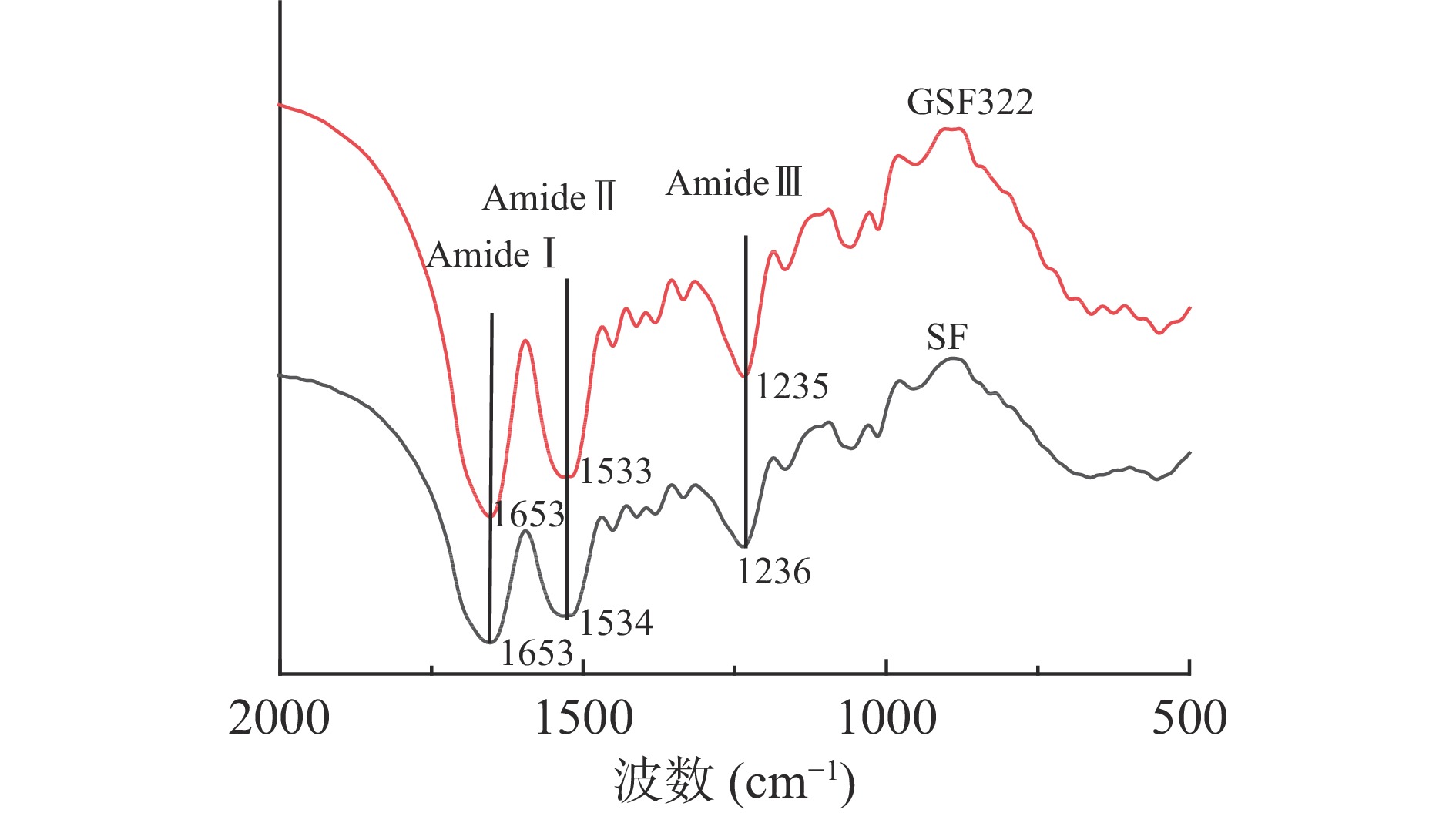
采用傅里叶红外光谱对丝素蛋白分子进行结构鉴定和分析[33]。典型的丝素蛋白红外光谱无规卷曲特征谱带:酰胺I带(1650~1660 cm−1)、酰胺II带(1532~1542 cm−1)、酰胺III带(1235 cm−1)。以SF为对照,选择GSF322进行对比,因为GSF3、GSF322、GSF332、GSF4、GSF5这几个样品在红外光谱中吸收峰的位置基本一致,看不出明显区别,因此,选择GSF322和SF进行对比。结果如图2所示,可以发现,两种样品的红外吸收光谱具有类似的吸收峰,样品GSF322所表现出的红外特征峰为:酰胺I(C=O伸缩振动)、酰胺II(N-H变形振动)、酰胺III(N-H变角和C-H伸缩振动)的特征谱带波数分别为1653、1533、1235 cm−1,SF所表现出的红外特征峰为:酰胺I、酰胺II和酰胺III的特征谱带波数分别为1653、1534、1236 cm−1。由此可见,SF和GSF322的关键吸收峰位置基本一致,且构象也均以无规卷曲结构为主。
2.3 圆二色谱
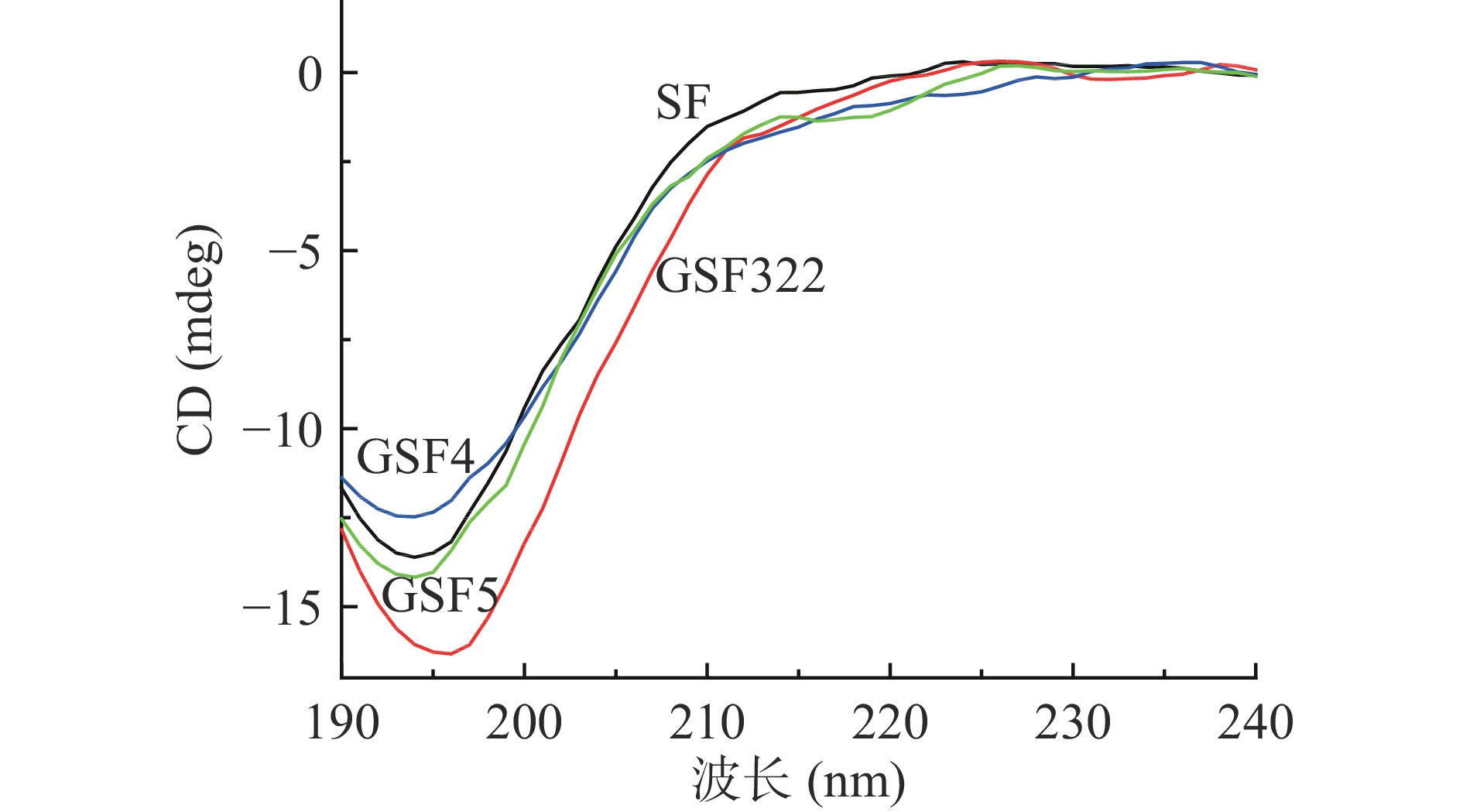
由图3可知,各个冷冻研磨条件的丝素蛋白和未冷冻研磨再生丝素蛋白均在195 nm处有明显的负峰,即无规卷曲的特征负峰。对比未冷冻研磨处理的CD图,可以发现,不同研磨时间处理后的丝素样品负吸收峰并没有呈现规律性变化,正峰值也同样如此。可知各个冷冻研磨条件的再生丝素蛋白和未冷冻研磨再生丝素蛋白构象均以无规卷曲为主,冷冻研磨并没有使丝素蛋白分子的三螺旋结构发生本质变化,丝素蛋白仍能保持其体外组装活性。
2.4 浊度
图4为不同冷冻研磨条件丝素蛋白自组装趋势图,由图可以看出样品GSF322的浊度曲线上升最快,斜率最大吸光度最高,自组装速率和自组装能力均最好,这可能是因为,适当的研磨时间使得丝素蛋白分子间的作用力发生改变,促使部分分子向β-折叠转变,因而提高了样品的自组装能力[36-37]。样品GSF4的斜率和吸光值均优于未冷冻研磨的SF,而GSF5,其组装能力要差于对照样品SF,这可能是因为研磨时间过长,使得丝素蛋白大分子部分断裂为小分子[38],因此影响其体外组装能力,这和前面的提取率实验结果基本一致。因此,冷冻研磨预处理选择研磨3 min最合适,为了进一步研究研磨预处理对丝素蛋白性质的影响,后续实验均以GSF322和SF进行性能测试对比。
2.5 Zeta电位
从图5中可以看出SF等电点是2.39,GSF322的等电点是2.48,GSF322的等电点与SF相比略有增加,这可能是由于冷冻研磨使丝素蛋白分子链中的碱性基团更多暴露出来,因而导致等电点略有增加。图6显示出 SF、GSF322在 pH 为 7.4 条件下的 Zeta电位值,SF的电位值为−8.02,经过冷冻研磨预处理的样品GSF322的电位值则增加到−5.01。表明,GSF322分子链上正电荷基团增多,推测原因是由于碱性氨基酸含量的增多导致的-NH2基含量增多,从而使得等电点略有增大[39]。
2.6 溶解性分析
由图7可以看出,丝素蛋白样品GSF322在酸、碱、盐中的溶解度均较再生丝素蛋白样品SF的溶解率低,推测是因为GSF322的分子链上正电荷多,因此与酸碱盐均有排斥作用,因此表现出溶解度降低的现象,丝素蛋白在CaCl2溶液中表现出更低的溶解性,可能是因为溶液中Ca2+容易与丝素蛋白上裸露的羧基络合,使得丝素蛋白分子量变大,因而溶解率降低明显。而在水中,两个样品的溶解度相差不大,GSF322溶解性表现略高一些,这可能由于研磨后样品中一些极性、酸性和碱性氨基酸总量增加,导致丝素分子亲水性增加,从而溶解率增加[40]。
2.7 热稳定性
由图8,GSF322的热分解峰峰值为111.8 ℃,SF的热分解峰峰值则降至107.7 ℃。在脱胶时,Na2CO3的强碱性会破坏丝素蛋白的分子链,导致其分子量降低,从而影响丝素蛋白的热学性能。GSF322的热分解峰略有升高可能是由于对蚕丝进行的冷冻研磨预处理缩短了Na2CO3脱胶时间,减少Na2CO3对丝素蛋白肽的破坏,使GSF322保留较为完整的结构,从而增强了其热稳定性[20]。
3. 结论
以家蚕蚕茧为研究材料,采用冷冻研磨方式进行脱胶前预处理,预处理最优条件为冷冻12 h后研磨3 min,丝素蛋白提取条件优化为碱中煮沸20 min,重复2次,整个过程脱胶时间仅为40 min,比未预处理时减少56%,同时减少了碱液的排放,得率与对照样SF几乎相当,但在水中的溶解性增加。圆二色谱实验说明预处理对丝素蛋白的三螺旋结构无影响;浊度实验发现样品GSF322的体外组装能力增强,部分丝素蛋白分子由无规卷曲向β-折叠构象转变;Zeta电位实验表明GSF322分子链上更多氨基基团暴露出来,在溶解率实验中进一步证明这可能是其溶解性增加的原因。综合以上,丝素蛋白提取条件为:蚕茧经液氮冷冻12 h,研磨仪研磨3 min后在碱液中煮2次。预处理后,相比未预处理的提取方式,水溶性及其它理化性能均优于未预处理样品SF。下一步工作将继续研究冷冻研磨对丝素蛋白的生物性能的调控作用,以期为丝素蛋白在食品及医学材料领域提供理论支持。
-
-
[1] HUANG X W, LIANG H, LI Z, et a1. Monodisperse phase transfer and surface bioengineering of metal nanoparticles via a silk fibroin protein corona[J]. Nanoscale,2017,9(8):2695−2700. doi: 10.1039/C6NR09581J
[2] LIM H R, KIM H S, QAZI R, et al. Advanced soft materials, sensor integrations, and applications of wearable flexible hybrid electronics in healthcare, energy, and environment[J]. Advanced Materials,2020,32:1901924.1−1901924.43.
[3] ZHANG X H, SHENG N N, WANG L A, et al. Supramolecular nanofibrillar hydrogels as highly stretchable, elastic and sensitive ionic sensors[J]. Materials Horizons Journal,2019,6:326−333. doi: 10.1039/C8MH01188E
[4] CHEN F, LU S P, ZHU L, et al. Conductive regenerated silk-fibroin-based hydrogels with integrated high mechanical performances[J]. J Mater Chem B,2019,7:1708−1715. doi: 10.1039/C8TB02445F
[5] LI Y L, XIAO Y, LIU C S. The horizon of materiobiology: A perspective on material-guided cell behaviors and tissue engineering[J]. Chem Rev,2017,117:4376−4421.
[6] DHASMANA A, SINGH L, ROY P, et al. Silk fibroin protein modified acellular dermal matrix for tissue repairing and regeneration[J]. Mat Sci Eng C-Mater Biol Appl,2019,97:313−324. doi: 10.1016/j.msec.2018.12.038
[7] 李平, 宛晓春, 陶文沂, 等. 丝素蛋白膜固定β葡萄糖苷酶及其改良食品风味的研究[J]. 菌物学报,2014,23(1):73−78. [LI P, WAN X C, TAO W Y, et al. Study on the immobilization of β-glucosidase by silk fibroin membrane and its improvement of food flavor[J]. Acta Bacteriologica Sinica,2014,23(1):73−78. LI P, WAN X C, TAO W Y, et al. Study on the immobilization of β-glucosidase by silk fibroin membrane and its improvement of food flavor[J]. Acta Bacteriologica Sinica, 2014, 23(1): 73-78.
[8] MARELLI B, BRENCKLE M A, KAPLAN D L, et al. Silk fibroin as edible coating for perishable food preservation[J]. Scientific Reports,2016,6:25236. doi: 10.1038/srep25263
[9] 屠洁, 刘冠卉, 燕薇. 4种常用稳定剂和丝素蛋白对搅拌型酸奶黏度和保水性的影响[J]. 食品科学,2012,33(21):136−140. [TU J, LIU G H, YAN W. Effects of four common stabilizers combined with silk fibroin on viscosity and water-holding capacity of stirred yogurt[J]. Food Science,2012,33(21):136−140. TU J, LIU G H, YAN W. Effects of four common stabilizers combined with silk fibroin on viscosity and water-holding capacity of stirred yogurt[J]. Food Science, 2012, 33(21): 136-140.
[10] 李莹莹, 王昉, 刘其春. 丝素蛋白及其复合材料的研究进展[J]. 材料工程,2018,46(8):14−26. [LI Y Y, WANG F, LIU Q C. Research progress of silk fibroin and its composite materials[J]. Materials Engineering,2018,46(8):14−26. doi: 10.11868/j.issn.1001-4381.2017.001242 LI Y Y, WANG F, LIU Q C. Research progress of silk fibroin and its composite materials[J]. Materials Engineering, 2018, 46(8): 14-26. doi: 10.11868/j.issn.1001-4381.2017.001242
[11] ARANGO M C, MONTOYA Y, PERESIN M S, et al. Silk sericin as a biomaterial for tissue engineering: A review[J]. International Journal of Polymeric Materials,2021,70(15/18):1115−1129.
[12] CHELAZZI D, BADILLO-SANCHEZ D, GIORGI R, et al. Self-regenerated silk fibroin with controlled crystallinity for the reinforcement of silk[J]. Journal of Colloid and Interface Science,2020,576:230−240. doi: 10.1016/j.jcis.2020.04.114
[13] GUO X, LIN N, LU S, et al. Preparation and biocompatibility characterization of silk fibroin 3D scaffolds[J]. ACS Applied Bio Materials,2021,4(2):1369−1380. doi: 10.1021/acsabm.0c01239
[14] JMA B, SM C, SG C, et al. Silk fibroin as biomaterial for bone tissue engineering[J]. Acta Biomaterialia,2016,31:1−16. doi: 10.1016/j.actbio.2015.09.005
[15] GUAN Y, YANG X Y, WANG L, et al. A novel silk/polyester woven small diameter arterial prosthesis: Degumming and the influence on cytocompatibility[J]. Fibers and Polymers,2015,16:1533−1539. doi: 10.1007/s12221-015-4934-5
[16] SUN W, GREGIRY D A, TOMEH M A, et al. Silk fibroin as a functional biomaterial for tissue engineering[J]. International Journal of Molecular Sciences,2021,22(3):1499. doi: 10.3390/ijms22031499
[17] WANG L P, LUO Z W, et al. Effect of degumming methods on the degradation behavior of silk fibroin biomaterials[J]. Fibers and Polymers,2019,20:45−50. doi: 10.1007/s12221-019-8658-9
[18] ZHENG Z, GUO S, LIU Y, et al. Lithium-free processing of silk fibroin[J]. Journal of Biomaterials Applications,2016,31(3):450−463. doi: 10.1177/0885328216653259
[19] RUI W, ZHU Y, ZHUO S, et al. Degumming of raw silk via steam treatment[J]. Journal of Cleaner Production,2018,203(PT.1−1216):492−497.
[20] WANG Z, YANG H, LI W, et al. Effect of silk degumming on the structure and properties of silk fibroin[J]. The Journal of the Textile Institute,2019,110(1):134−140. doi: 10.1080/00405000.2018.1473074
[21] VYAS S K, SHUKLA S R. Comparative study of degumming of silk varieties by different techniques[J]. Journal of the Textile Institute Proceedings & Abstracts,2015,107(2):191−199.
[22] RASTOGI S, KANDASU B. Processing trends of silk fibers: Silk degumming, regeneration and physical functionalization[J]. Journal of the Textile Institute,2020,111(12):1−17.
[23] TOWNSEND B, PEYRONEL F, CAHHAGHAN-PATEACHAR N, et al. Shear-induced aggregation or disaggregation in edible oils: Models, computer simulation, and USAXS measurements[J]. J Appl Phys,2017,122(22):224304−224314. doi: 10.1063/1.5004023
[24] WILSON J F, BOLESLAV Z, ONDŘEJ Š, et al. Study of the shear-thinning effect between polymer nanoparticle surfaces during shear-induced aggregation[J]. Ind Eng Chem Res,2021,60(29):10654−10665. doi: 10.1021/acs.iecr.1c00232
[25] MEGHWAL M, GOSWAMI T K. Comparative study on ambient and cryogenic grinding of fenugreek and black pepper seeds using rotor, ball, hammer and pin mill[J]. Powder Technology,2014,267:245−255. doi: 10.1016/j.powtec.2014.07.025
[26] HE L, YANG J, XU C Z, et al. Effect of pre-shearing treatment on the molecular structure, fibrillogenesis behavior and gel properties of collagen[J]. New J Chem,2020,44(17):6760−6770. doi: 10.1039/D0NJ00054J
[27] SUN M, WEI X, WANG H B, et al. Structure restoration of thermally denatured collagen by ultrahigh pressure treatment[J]. Food Bioprocess Tech,2020,13(2):367−378. doi: 10.1007/s11947-019-02389-6
[28] YANG J, WANG H B, HE L, et al. Reconstituted fibril from heterogenic collagens-a new method to regulate properties of collagen gels[J]. Macromol Res,2019,27(11):1124−1135. doi: 10.1007/s13233-019-7160-y
[29] CHEN X, LIU L, YUAN D, et al. Preparation of nano-sized Bi2Te3 thermoelectric material powders by cryogenic grinding[J]. Progress in Natural Science Materials International,2012,3:201−206.
[30] 赵绪龙, 马广鹏, 武继锋, 等. 冷冻研磨结合LC-MS/MS法检测指甲中甲基苯丙胺、苯丙胺成分[J]. 刑事技术,2020,6:601−605. [ZHAO X L, MA G P, WU J F, et al. Determination of methamphetamine and amphetamine in nail through frozen grinding coupled into high performance liquid chromatography-tandem mass spectrometry[J]. Forensic Science and Technology,2020,6:601−605. doi: 10.16467/j.1008-3650.2020.06.011 ZHAO X L, MA G P, WU J F, et al. Determination of methamphetamine and amphetamine in nail through frozen grinding coupled into high performance liquid chromatography-tandem mass spectrometry[J]. Forensic Science and Technology, 2020, 6: 601-605. doi: 10.16467/j.1008-3650.2020.06.011
[31] BARANOWSKA-KOREZYE A, BARANOWSKA-KOREZYE A, HUDECKI A, et al. Silk powder from cocoons and woven fabric as a potential bio-modifier[J]. Materials,2021,14(22):6919. doi: 10.3390/ma14226919
[32] HESS S, BEEK J V, PANNELLL K. Acid hydrolysis of silk fibroins and determination of the enrichment of isotopically labeled amino acids using precolumn derivatization and high-performance liquid chromatography-electrospray ionization-mass spectrometry[J]. Analytical Biochemistry,2002,311(1):19−26. doi: 10.1016/S0003-2697(02)00402-5
[33] BATH J D, ELLIS J W. Some features and implications of the near infrared absorption spectra of various proteins: Gelatin, silk fibroin, and zinc insulinate[J]. J Phys Chem,2002,45(2):204−209.
[34] FRENDEL A, SCHMIDT-NAAKE G. Controlled molecular weight degradation by vibration grinding[J]. 2001, 24(8): 798-803.
[35] WANG Y Q, ZHAO P, LIU H, et al. Structure and temperature induced crystallization of natural rubber with different milling times[J]. Polym Sci Ser A,2021,63(3):228−237. doi: 10.1134/S0965545X21030135
[36] AMOURA H, MOKRANE H, NADIEMI B. Effect of wet and dry milling on the functional properties of whole sorghum grain flour and kalian[J]. J Food Sci Technol,2020,57:1100−1109. doi: 10.1007/s13197-019-04145-2
[37] ZHONG J, MA M J, LI W Y, et al. Self-assembly of regenerated silk fibroin from random coil nanostructures to antiparallel β-sheet nanostructures[J]. Biopolymers: Original Research on Biomolecules and Biomolecular Assemblies,2014,101(12):1181−1192.
[38] SHAMSHINA J L, STEIN R S, ABIDI N. Choosing the right strategy: Cryogrinding vs. ball milling-comparing apples to apples[J]. Green Chemistry,2021,23(23):9646−9657. doi: 10.1039/D1GC03128G
[39] 丁梦瑶, 戴梦男, 李蒙, 等. 不同分子质量丝素蛋白的分离与表征[J]. 纺织学报,2021,42(7):46−53. [DING M Y, DAI M G, LI M, et al. Separation and characterization of silk fibroin with different molecular weight[J]. Journal of Textile Research,2021,42(7):46−53. doi: 10.13475/j.fzxb.20201006308 DING M Y, DAI M G, LI M, et al. Separation and characterization of silk fibroin with different molecular weight[J]. Journal of Textile Research, 2021, 42(7): 46-53. doi: 10.13475/j.fzxb.20201006308
[40] ZHOU J, ZHENG D, ZHANG F, et al. A novel method to bind soybean protein onto the surface of poly (Ethylene terephthalate) fabric[J]. Textile Research Journal,2016,87(4):460−473.
-
期刊类型引用(2)
1. 吴广武,白蓉,方虎,赵成,陈佩圆. 维生素C调控合成纯球霰石及其形成机理. 硅酸盐通报. 2025(01): 195-201+242 .  百度学术
百度学术
2. 范旭,朱迎澳,朱嘉敏,陈倩,王辉. 明胶改善海藻酸钠水凝胶膜的物理性能研究. 食品工业科技. 2023(15): 108-115 .  本站查看
本站查看
其他类型引用(3)







 下载:
下载:





 下载:
下载:



