Preparation Process Optimization and Evaluation of Antioxidant Activity of Burdock Polysaccharide Zinc Complex
-
摘要: 本研究以牛蒡多糖和硫酸锌为原料,通过硫酸锌法合成牛蒡多糖锌。采用单因素实验和响应面试验优化牛蒡多糖锌的制备工艺,并对其抗氧化活性进行研究。结果表明:牛蒡多糖锌的最佳制备工艺为:牛蒡多糖与硫酸锌的质量比为37:1、温度50 ℃、时间121 min、pH8.6,此时螯合率为93.21%±0.58%。抗氧化试验表明:当浓度为1.0 mg/mL时,牛蒡多糖锌对DPPH自由基、超氧阴离子自由基和ABTS+自由基的清除率分别为84.59%±0.60%、67.27%±1.00%、38.88%±1.68%,自由基清除能力均优于牛蒡多糖;而牛蒡多糖锌对羟基自由基的清除率略低于牛蒡多糖。锌修饰牛蒡多糖可增强牛蒡多糖的抗氧化能力,为牛蒡多糖的高值化利用提供了参考。Abstract: In this study, burdock polysaccharide zinc complex was synthesized by the zinc sulfate method with burdock polysaccharide and zinc sulfate as raw materials. Single factor and response surface methodology were used to optimize the preparation process of burdock polysaccharide zinc complex, and the antioxidant activity of burdock polysaccharide zinc complex was studied. The results showed that the optimum preparation process of burdock polysaccharide zinc complex was as follows: The weight ratio of burdock polysaccharide to zinc sulfate was 37:1, the temperature was 50 ℃, the time was 121 min and the pH was 8.6, the chelation rate was 93.21%±0.58%. The antioxidant test showed that when the concentration was 1.0 mg/mL, the scavenging rates of burdock polysaccharide zinc complex on DPPH radical, superoxide anion radical and ABTS+ radical were 84.59%±0.60%, 67.27%±1.00% and 38.88%±1.68%, respectively, which were better than burdock polysaccharide. However, the scavenging rate of hydroxyl radicals of burdock polysaccharide zinc complex was slightly lower than that of the burdock polysaccharide. The antioxidant capacity of burdock polysaccharide after zinc modification could be enhanced, and this work could provide a reference for the high value utilization of burdock polysaccharide.
-
Keywords:
- burdock polysaccharide /
- zinc /
- preparation process /
- antioxidant activity
-
牛蒡,俗称“东洋参”,为菊科牛蒡属草本植物,种植广泛,资源量大[1-2]。目前常见的牛蒡品种有:柳川理想、东京理想、东京白肌及白肌大长等[3]。牛蒡中富含多糖,具有抗氧化、抗肿瘤、抗炎、降血糖、肠道益生等多种生理功效[4-6]。多糖的生物活性与其结构密切相关,对多糖进行改性修饰可以丰富并提高多糖的生物活性,扩大应用范围[7-8],改性修饰是指通过化学方法将其他活性基团引入多糖链,主要包括羧甲基化、硫酸化、乙酰化、与金属鳌合等。目前对牛蒡多糖的研究主要集中在多糖的提取[9-10]、结构解析[11-12]及生物活性研究[4, 13]等方面,有关牛蒡多糖的改性研究较少。
锌是人体必需的微量元素之一[14],在体内代谢调节、细胞内信号传导与调节、生长发育、免疫调节和生殖遗传等方面发挥重要作用[15-16]。缺锌会引起锌酸活力减退,诱发冠心病、高血压等疾病[17]。将多糖与锌离子螯合制备多糖锌,不仅可以克服市面常见补锌剂对胃肠道刺激作用大、生物利用率低的缺点,还具有抑菌、抗炎等[18]多种生理功效。因此,多糖锌的研究与开发具有重要意义。
多糖与锌离子的螯合主要是多糖中的羟基和羧基与锌离子发生配位反应,生成二者的螯合物[19]。作为一种新的取代基,螯合后的锌离子具有使氢键解离能减弱、供氢能力变强、抗氧化活性增强的能力[20-21]。目前对多糖锌的研究主要有南瓜皮多糖锌[22]、生姜皮多糖锌[23]、孔石莼多糖锌[24]、平贝母多糖锌[25]等,但牛蒡多糖锌的制备及其抗氧化活性研究未见报道。
本研究以牛蒡多糖为原料,采用硫酸锌法制备牛蒡多糖锌,通过单因素实验和响应面试验优化制备工艺,并研究牛蒡多糖锌的抗氧化活性,旨在开发出一种新型补锌产品,为牛蒡资源的综合利用提供理论支持。
1. 材料与方法
1.1 材料与仪器
牛蒡 品种为柳川理想,江苏沛县轶伟有限公司;硫酸锌、无水乙醇、磷酸氢二钠、磷酸二氢钠 分析纯,天津市凯通化学试剂有限公司;锌标准储备液(1000 μg/mL) 国家检验认证有限公司;盐酸 优级纯,天津市科密欧化学试剂有限公司;氢氧化钠 分析纯,天津市科密欧化学试剂有限公司;硝酸 优级纯,苏州晶瑞化学股份有限公司;DPPH 化学纯,梯希爱(上海)化成工业发展有限公司;硫酸亚铁 化学纯,博山化学试剂厂;水杨酸 分析纯,上海源叶生物科技有限公司;ABTS 超纯,上海麦克林生化科技有限公司;过硫酸钾 分析纯,国药集团化学试剂有限公司;Tris-HCl缓冲液、邻苯三酚 北京索莱宝科技有限公司;抗坏血酸 分析纯,上海蓝季科技发展有限公司;透析袋(500 Da) 怡康科贸生物试剂耗材实验有限公司。
SECURA224-ICN电子天平 北京赛多利斯仪器有限公司;S210 pH计 梅特勒-托利多仪器有限公司;DKZ-2B水浴恒温振荡器 上海一恒科技仪器有限公司;7800电感耦合等离子体质谱仪(ICP-MS) 美国安捷伦科技公司;FD-304冷冻干燥机 济南骏德仪器有限公司;SPECTRAMAX M5多功能酶标仪 美谷分子仪器(上海)有限公司。
1.2 实验方法
1.2.1 牛蒡多糖的提取
水提醇沉法提取牛蒡多糖[11]。称取2 kg牛蒡粉末,以1:10的料液比于100 ℃下浸提三次,过滤,滤液用4倍体积的无水乙醇醇沉,静置,离心(4000 r/min)10 min。Sevage法脱蛋白(氯仿:正丁醇=4:1),饱和氯化钙溶液脱果胶,透析,冻干得牛蒡多糖粉末。牛蒡多糖的得率为9.36%。苯酚-硫酸法[26]测定总糖含量为78.64%±0.81%。
1.2.2 牛蒡多糖锌的制备
采用硫酸锌法制备牛蒡多糖锌[27]。固定硫酸锌溶液的浓度(0.1 g/L),加入等体积的牛蒡多糖溶液,设置不同的质量比、温度、时间、pH于恒温振荡器中振荡,反应结束用4倍体积无水乙醇醇沉过夜,离心(4000 r/min)10 min,沉淀复溶后,透析48 h,冷冻干燥机冻干72 h得到牛蒡多糖锌。苯酚硫酸法测定总糖含量为69.48%±1.59%。
1.2.3 单因素实验
1.2.3.1 牛蒡多糖与硫酸锌的质量比对螯合率的影响
固定硫酸锌的浓度为0.1 g/L,反应温度60 ℃,反应时间90 min,自然pH(5~6),牛蒡多糖与硫酸锌的质量比分别为25:1、30:1、35:1、40:1、45:1、50:1,于恒温振荡器中振荡。反应结束后醇沉,离心后取上清液,电感耦合等离子体质谱仪(ICP-MS)测定锌含量[28]。
1.2.3.2 反应温度对螯合率的影响
固定硫酸锌的浓度为0.1 g/L,牛蒡多糖与硫酸锌的质量比30:1,反应时间90 min,自然pH(5~6),反应温度分别为30、40、50、60、70、80 ℃,参考“1.2.3.1”进行实验。
1.2.3.3 反应时间对螯合率的影响
固定硫酸锌的浓度为0.1 g/L,牛蒡多糖与硫酸锌的质量比30:1,反应温度60 ℃,自然pH(5~6),反应时间分别为30、60、90、120、150 min,参考“1.2.3.1”进行实验。
1.2.3.4 反应pH对螯合率的影响
固定硫酸锌的浓度为0.1 g/L,牛蒡多糖与硫酸锌的质量比30:1,反应温度60 ℃,反应时间90 min,反应pH分别为4、5、6、7、8、9,参考“1.2.3.1”进行实验。
1.2.4 响应面试验
在单因素实验的基础上,以锌离子螯合率为响应值,牛蒡多糖与硫酸锌的质量比、反应温度、反应时间、反应pH为自变量,采用Design-Expert 8.0.6统计分析软件建立Box-Behnken模型,进行四因素三水平的响应面试验。响应面试验设计因素与水平见表1。
表 1 响应面试验因素与水平Table 1. Response surface experimental factors and levels水平 因素 A牛蒡多糖与硫酸锌
的质量比B反应温度
(℃)C反应时间
(min)D反应
pH−1 30:1 50 90 7 0 35:1 60 120 8 1 40:1 70 150 9 1.2.5 锌元素含量的测定
1.2.5.1 锌标准曲线的绘制
利用锌标准溶液配制浓度为0、0.1、0.2、0.4、0.6、0.8、1.0 µg/mL的锌溶液,以锌元素的浓度(X,μg/mL)为横坐标,响应信号值(Y)为纵坐标,电感耦合等离子体质谱仪测定,绘制标准曲线。测得标准曲线方程为Y=9.2073X+0.1047,R2=0.9997。
电感耦合等离子体质谱仪(ICP-MS)相关参数如下[29]:射频功率1550 W,等离子体气体流速15 L/min,辅助气体流速0.9 L/min,蠕动泵转速0.1 rps,雾化室温度2 ℃,采样深度8 mm。
1.2.5.2 螯合率的计算
螯合率(%)=初始锌含量−上清锌含量初始锌含量×100 1.2.5.3 锌含量的测定
称取牛蒡多糖锌0.02 g,消解样品(微波消解程序见表2)后冷却至室温定容至50 mL,ICP-MS 测定锌含量[30]。
表 2 微波消解升温程序Table 2. Temperature rise procedure of microwave digestion步骤 控制温度(℃) 升温时间(min) 恒温时间(min) 1 120 5 3 2 165 5 0 3 190 10 15 1.2.6 牛蒡多糖锌抗氧化活性评价
1.2.6.1 DPPH自由基清除试验
参考符玉霞等[31]的方法并稍作修改,配制不同浓度的牛蒡多糖和牛蒡多糖锌溶液(0、0.2、0.4、0.6、0.8、1.0 mg/mL),各取3 mL于试管中,加入等体积的0.15 mmol/L的DPPH-乙醇溶液,混匀,室温避光反应30 min,用酶标仪于517 nm下测定吸光值A1。以不同质量浓度的抗坏血酸作为阳性对照,测定其DPPH自由基的清除能力。按以下公式计算DPPH自由基的清除率:
清除率(%)=(1−A1−A2A0)×100 式中:A1:反应完样品溶液的吸光值;A2:样品溶液自身的吸光值;A0:空白对照的吸光值。
1.2.6.2 超氧阴离子自由基清除试验
参考Li等[32]的方法并稍作修改,配制不同浓度的牛蒡多糖和牛蒡多糖锌溶液(0、0.2、0.4、0.6、0.8、1.0 mg/mL),各取1 mL于试管中,加入4.5 mL的Tris-HCl缓冲液(50 mmol/L,pH8.2),混匀, 25 ℃水浴反应20 min,随后加入0.1 mL的3 mmol/L的邻苯三酚溶液,25 ℃反应5 min,立即加入1 mL 8 mmol/L的盐酸终止反应,用酶标仪于320 nm下测定吸光值A1。以不同质量浓度的抗坏血酸作为阳性对照,测定其超氧阴离子自由基的清除能力。参考“1.2.6.1”公式计算超氧阴离子自由基的清除率。
1.2.6.3 羟基自由基清除试验
参考阮进基等[33]的方法并稍作修改,配制不同浓度的牛蒡多糖和牛蒡多糖锌溶液(0、0.2、0.4、0.6、0.8、1.0 mg/mL),各取1 mL于试管中,分别加入1 mL 9 mmol/L的硫酸亚铁、9 mmol/L的水杨酸和8.8 mmol/L的过氧化氢溶液,混匀,37 ℃水浴反应30 min,用酶标仪于510 nm下测定吸光值A1。以不同质量浓度的抗坏血酸作为阳性对照,测定其羟基自由基的清除能力。参考“1.2.6.1”公式计算羟基自由基的清除率。
1.2.6.4 ABTS+自由基清除试验
参考何坤明等[34]的方法并稍作修改,称取0.3841 g ABTS和0.0662 g过硫酸钾,分别用20 mL蒸馏水溶解,混合并定容至100 mL,在室温下放置12~16 h得到ABTS+溶液。将ABTS+溶液利用pH为7.4的磷酸盐缓冲液稀释至吸光值为0.7±0.02(734 nm)备用。配制不同浓度的牛蒡多糖和牛蒡多糖锌溶液(0、0.2、0.4、0.6、0.8、1.0 mg/mL),各取0.1 mL于试管中,加入2 mL ABTS+溶液,混匀,室温避光反应6 min,用酶标仪于734 nm下测定吸光值A1。以不同质量浓度的抗坏血酸作为阳性对照,测定其ABTS+自由基的清除能力。参考“1.2.6.1”公式计算ABTS+自由基的清除率。
1.3 数据处理
试验重复三次,利用Design Expert 8.0.6进行数据统计分析,采用Origin 2017软件绘图,SPSS 26.0软件进行显著性分析,P<0.05表示有显著性差异。
2. 结果与分析
2.1 单因素实验结果
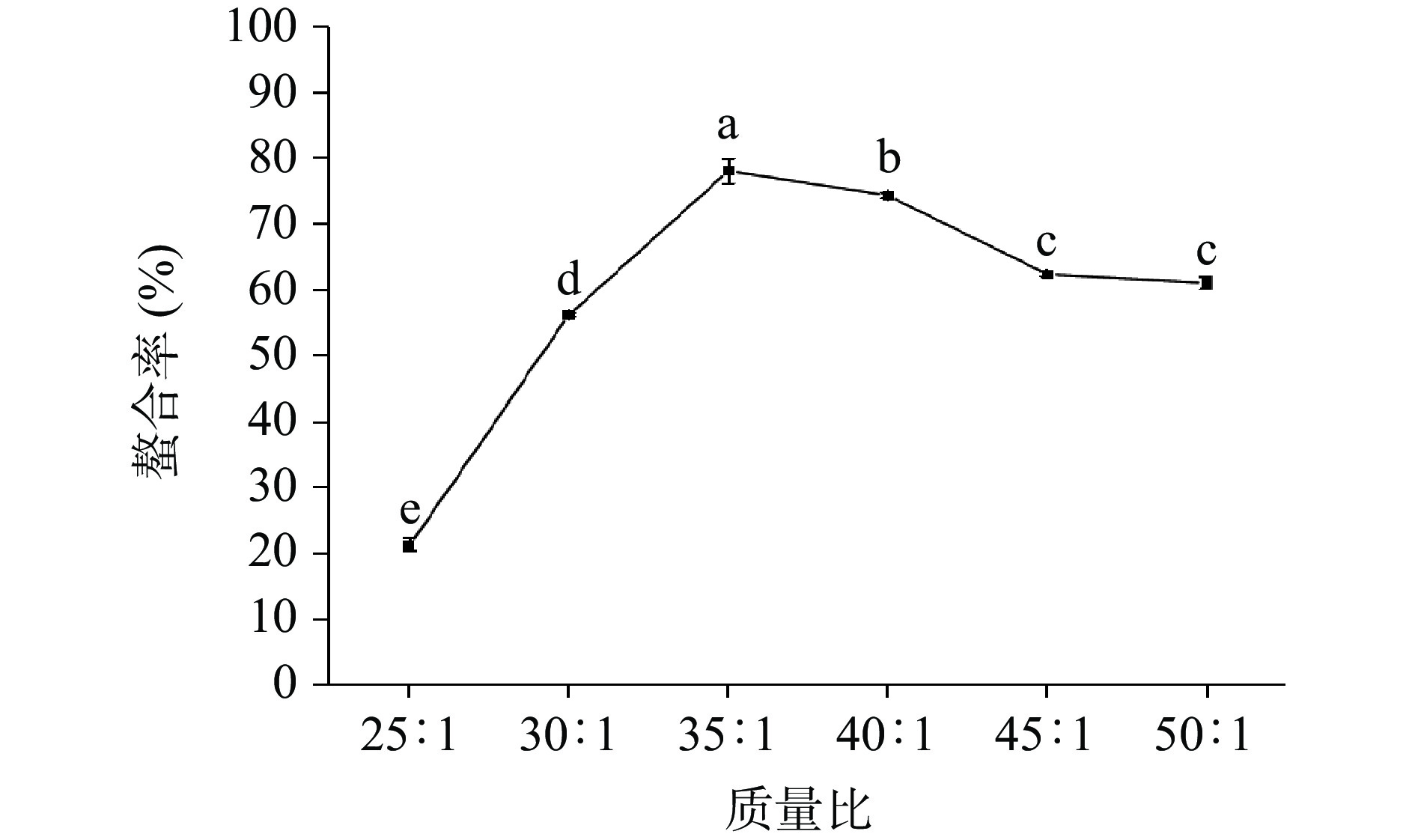
2.1.1 牛蒡多糖与硫酸锌的质量比对螯合率的影响
如图1所示,螯合率随着多糖浓度的增加呈现出先上升后下降最后趋于稳定的趋势。多糖与硫酸锌的质量比为35:1时,螯合率达到最大值78.16%。多糖浓度较低时,锌离子没有充足的结合位点,螯合率较低;随着多糖浓度增加,分子间相互作用力的增强导致体系粘度增大,阻碍结合位点的暴露,螯合率下降[35]。因此,选择牛蒡多糖与硫酸锌的质量比30:1~40:1进行后续响应面试验。
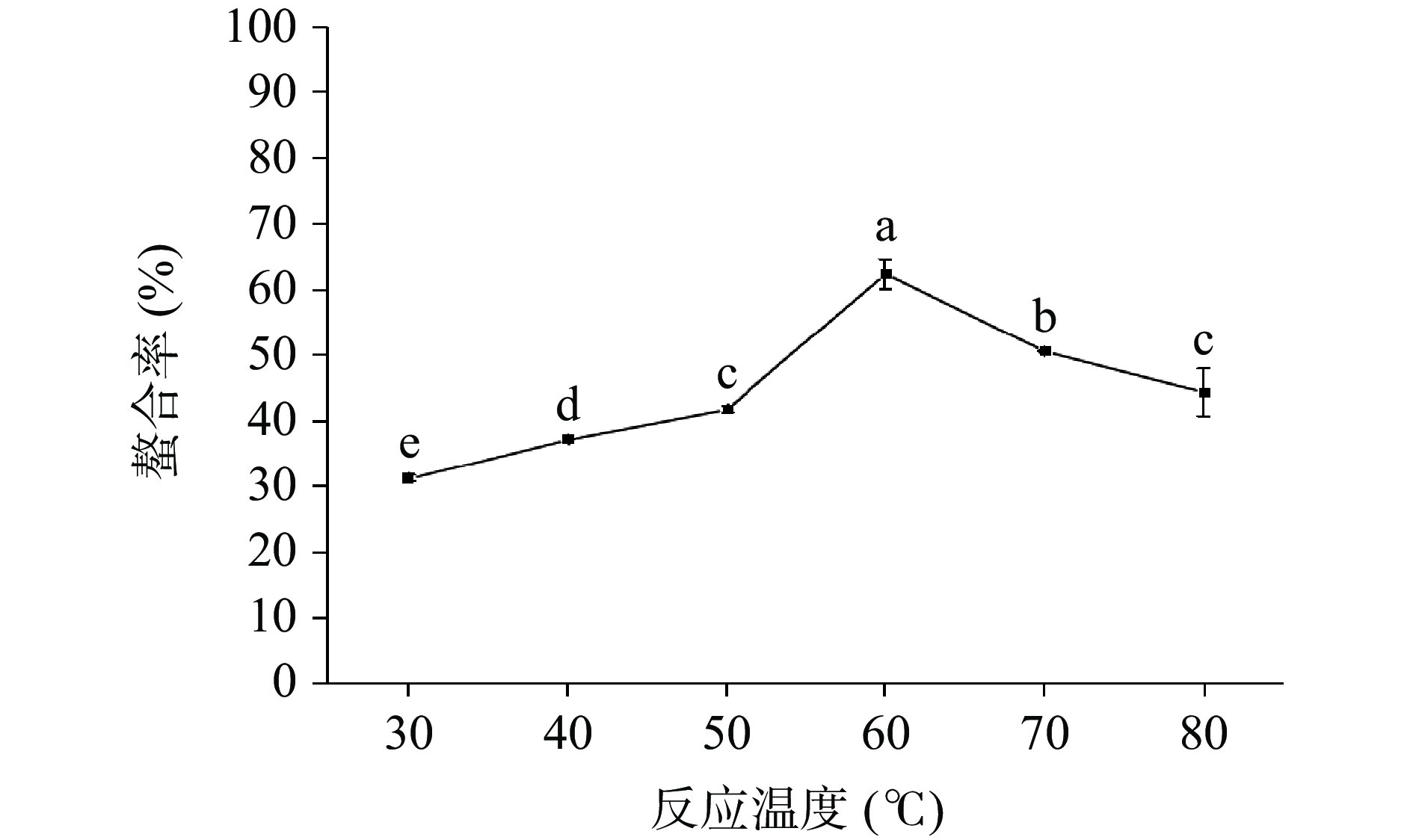
2.1.2 反应温度对螯合率的影响
如图2所示,螯合率随着反应温度的升高呈现出先上升后下降的趋势,当温度为60 ℃时,螯合率达到最大值62.52%。推测在30~60 ℃之间,随着温度的上升,分子的运动速度加快、分子平均能量增大,分子间有效碰撞次数增多,提高了多糖与锌离子的结合;温度过高,碰撞过于剧烈,不利于反应的发生,导致螯合率降低[36]。因此,选择反应温度50~70 ℃进行后续响应面试验。
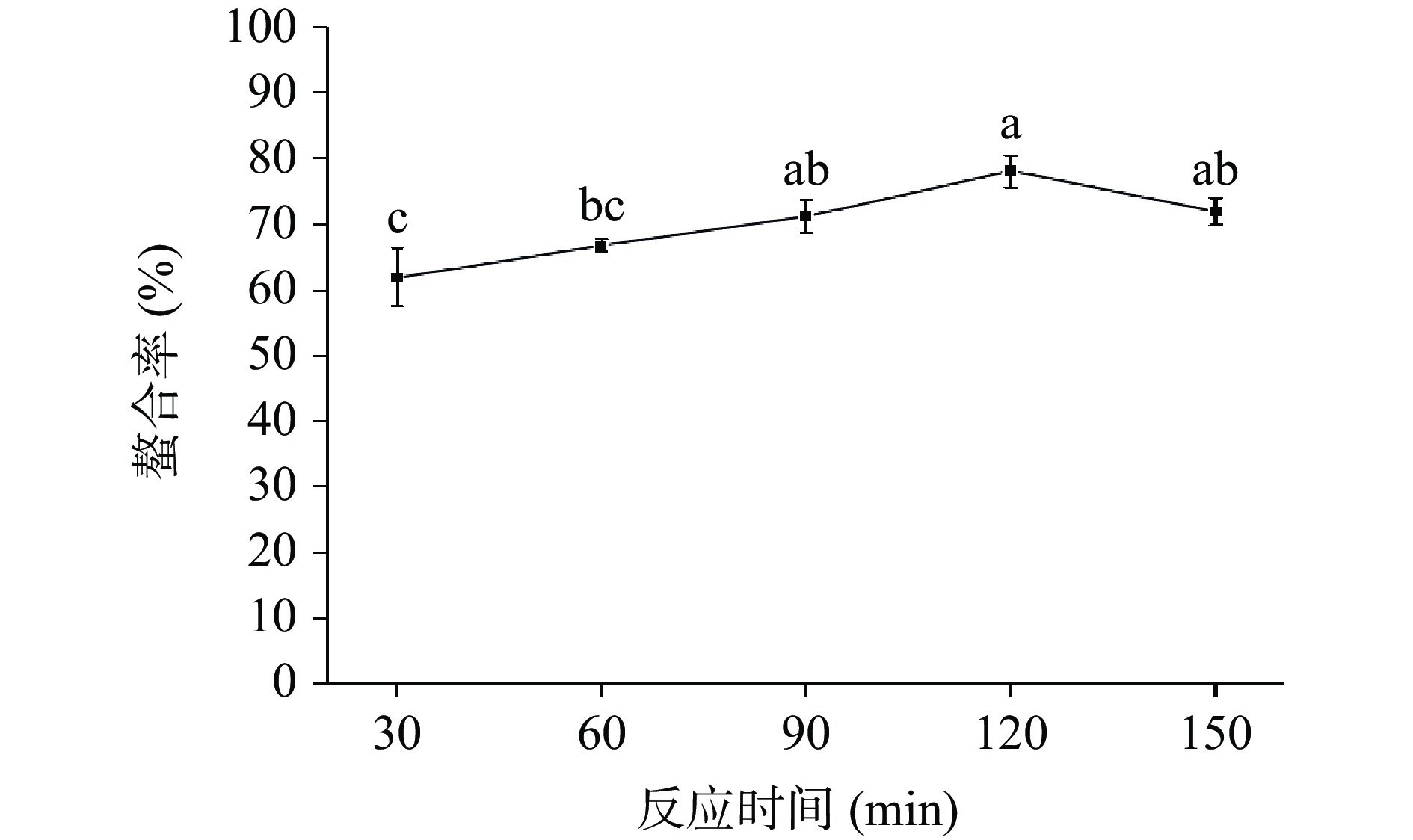
2.1.3 反应时间对螯合率的影响
如图3所示,螯合率随着反应时间的增加呈现出先上升后下降的趋势,当时间为120 min时,螯合率达到最大值78.23%。当反应时间较短时,多糖和锌离子无法充分接触,螯合率较低;随着反应时间的延长,反应体系达到平衡状态,但由于螯合物发生轻微解离,导致螯合率下降[37-38]。因此,选择反应时间90~150 min进行后续响应面试验。
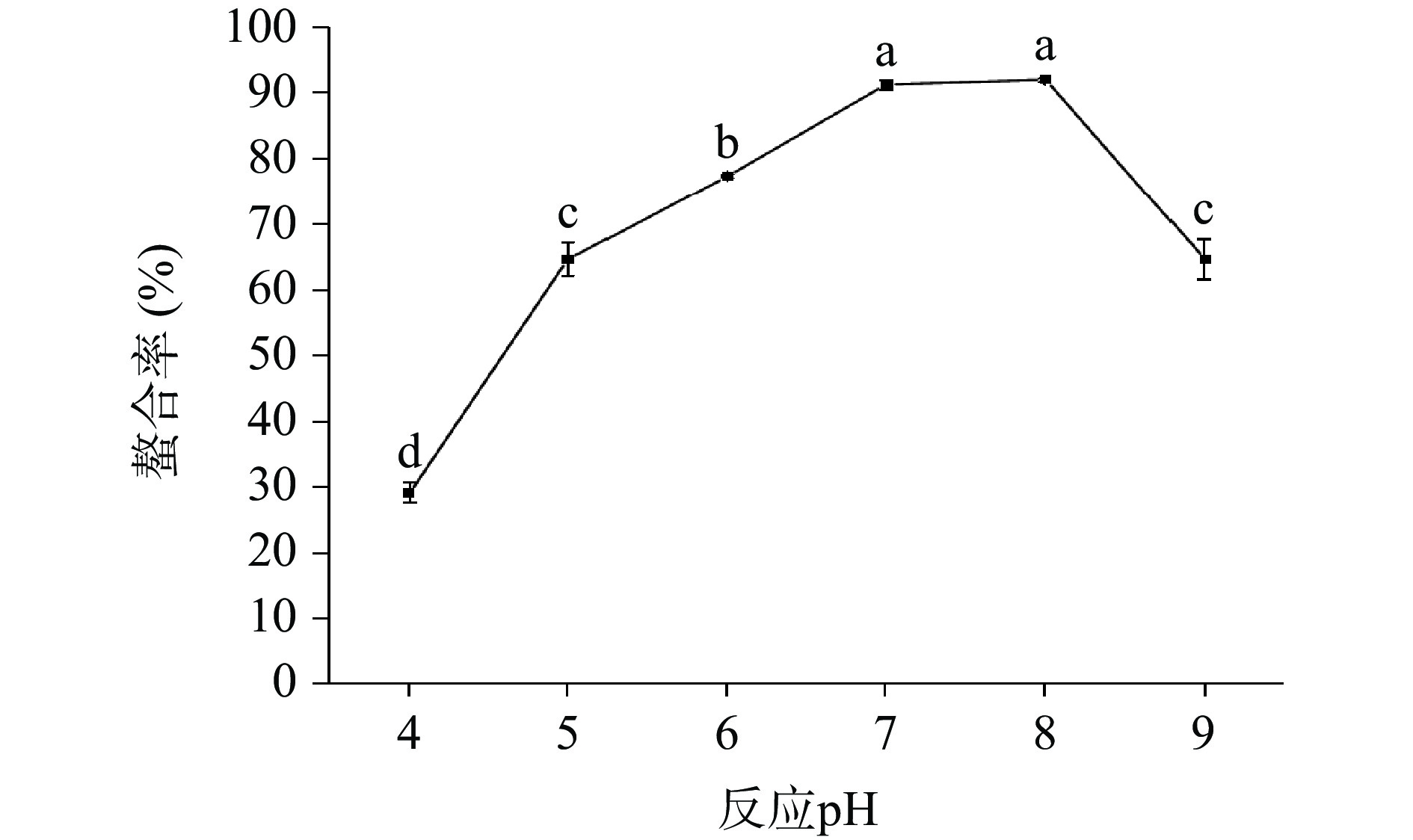
2.1.4 反应pH对螯合率的影响
如图4所示,螯合率随着反应pH的增加呈现出先上升后下降的趋势,当pH为8时,螯合率达到最大值92.12%。在酸性条件下,H+浓度高,与锌离子竞争结合位点,螯合率低;碱性条件下,OH−浓度增大,与锌离子反应,锌离子部分损失,螯合率下降,这与李文文等[23]的研究结果相似。因此,选择反应pH7~9进行后续响应面试验。
2.2 响应面试验结果
2.2.1 响应模型的建立与分析
采用Design Expert 8.0.6软件对数据进行回归分析,得到螯合率(Y)对牛蒡多糖与硫酸锌的质量比(A)、反应温度(B)、反应时间(C)和反应pH(D)的四元二次回归方程为Y=87.60+6.12A−0.61B+5.29C+5.92D−2.77AB−8.11AC−4.39AD+1.01BC−7.10BD−1.03CD−7.30A2−0.45B2−4.91C2−9.50D2。响应面试验结果见表3,方差分析结果见表4。
表 3 响应面试验结果Table 3. Response surface test results试验号 A牛蒡多糖与硫酸
锌的质量比B反应
温度C反应
时间D反应
pH螯合率
(%)1 −1 −1 0 0 71.54 2 −1 0 −1 0 56.68 3 −1 0 1 0 82.63 4 −1 0 0 1 74.40 5 −1 0 0 −1 53.17 6 −1 1 0 0 76.95 7 0 −1 −1 0 81.56 8 0 −1 0 −1 63.55 9 0 −1 0 1 90.00 10 0 −1 1 0 87.52 11 0 0 1 1 84.94 12 0 0 0 0 90.32 13 0 0 −1 −1 60.08 14 0 0 0 0 86.17 15 0 0 0 0 86.51 16 0 0 0 0 86.67 17 0 0 1 −1 76.18 18 0 0 −1 1 72.95 19 0 0 0 0 88.32 20 0 1 −1 0 74.82 21 0 1 1 0 84.82 22 0 1 0 −1 78.93 23 0 1 0 1 76.99 24 1 −1 0 0 88.99 25 1 0 −1 0 83.77 26 1 0 1 0 77.30 27 1 0 0 −1 75.87 28 1 0 0 1 79.54 29 1 1 0 0 83.33 表 4 回归模型方差分析Table 4. Analysis of variance of regression model来源 平方和 自由度 均方 F值 P值 差异性 模型 2659.37 14 189.96 45.25 <0.0001 显著 A 449.33 1 449.33 107.05 <0.0001 ** B 4.47 1 4.47 1.06 0.3198 C 336.34 1 336.34 80.13 <0.0001 ** D 420.56 1 420.56 100.19 <0.0001 ** AB 30.64 1 30.64 7.30 0.0172 * AC 262.76 1 262.76 62.60 <0.0001 ** AD 77.09 1 77.09 18.37 0.0008 ** BC 4.08 1 4.08 0.97 0.3409 BD 201.50 1 201.50 48.00 <0.0001 ** CD 4.22 1 4.22 1.01 0.3329 A2 345.57 1 345.57 82.33 <0.0001 ** B2 1.29 1 1.29 0.31 0.5887 C2 156.63 1 156.63 37.32 <0.0001 ** D2 584.82 1 584.82 139.33 <0.0001 ** 残差 58.77 14 4.20 失拟项 46.75 10 4.68 1.56 0.3556 不显著 绝对误差 12.01 4 3.00 总和 2718.14 28 注:**P<0.01,差异极显著;*P<0.05,差异显著。 由表4方差分析结果可知,失拟项P=0.3556不显著,模型P<0.0001极显著,表明该模型有意义。决定系数R2为0.9784,校正后决定系数R2Adj为0.9568,说明该回归方程拟合度和可信度较高,可利用此模型对牛蒡多糖锌的螯合能力进行预测。
一次项A、C、D,二次项A2、C2、D2,交互项AC、AD、BD对螯合作用的影响极显著(P<0.0001);交互项AB对螯合作用的影响显著(P<0.05);一次项B,二次项B2,交互项BC和CD对螯合作用影响不显著(P>0.05),可将其从回归模型中删除。最终可确定回归模型为Y=87.60+6.12A+5.29C+5.92D−2.77AB−8.11AC−4.39AD−7.10BD−7.30A2−4.91C2−9.50D2。F值越大,表明该因素对螯合率的影响越大[39]。本试验影响螯合率的因素排序为牛蒡多糖与硫酸锌的质量比>反应pH>反应时间>反应温度。
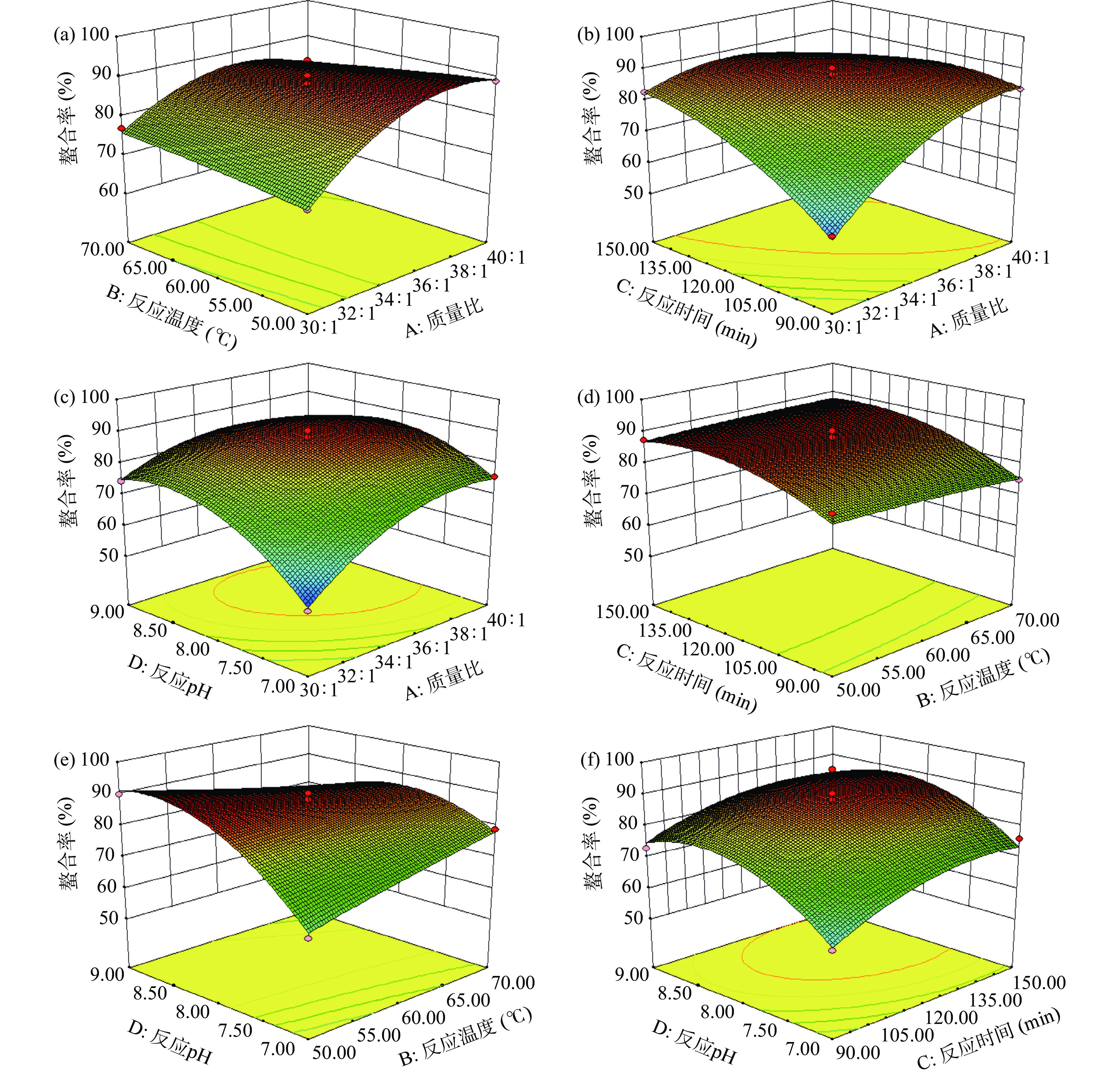
2.2.2 响应面图分析
如图5所示,响应面图均为开口向下的凸型曲面,说明螯合率存在最大值。如图5(b)、5(c)、5(e)所示,响应曲面弯曲程度较大,说明反应质量比和反应时间、反应质量比和反应pH以及反应温度和反应pH的交互作用对螯合率影响极显著。
2.2.3 回归模型验证
结合Design Expert试验设计软件,由回归模型分析方程可知:牛蒡多糖与硫酸锌的最佳螯合条件为牛蒡多糖与硫酸锌的质量比37.07:1、反应温度50 ℃、反应时间121.00 min、反应pH8.59,此时得到的预测螯合率为93.50%。为方便后续试验,选择以下条件验证:牛蒡多糖与硫酸锌的质量比37:1、反应温度50 ℃、反应时间121 min、反应pH8.6,螯合率为93.21%±0.58%,达到预测值的99.9%。ICP-MS测定锌含量为 (14.4±0.17) mg/g。因此,本试验采用响应面法所得的牛蒡多糖锌的制备优化工艺具有可靠性,可用于后续生产实践。
2.3 体外抗氧化试验结果
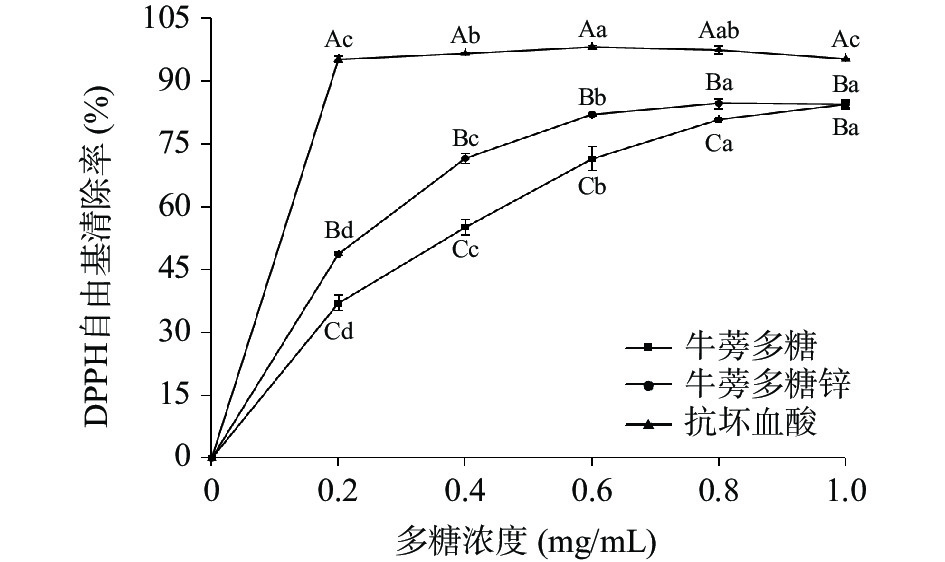
2.3.1 DPPH自由基清除试验
如图6所示,牛蒡多糖和牛蒡多糖锌均有较强的DPPH自由基清除能力,但两者的清除能力都小于抗坏血酸。当浓度为0~1.0 mg/mL时,牛蒡多糖和多糖锌的浓度与其对DPPH自由基的清除能力呈正相关,且多糖锌的清除能力优于原多糖。当浓度为1.0 mg/mL时,牛蒡多糖和牛蒡多糖锌对DPPH自由基的清除率分别为84.55%和84.59%。顾冰飞等[38]研究发现,浓度为1.0 mg/mL时,杏鲍菇多糖和多糖锌对0.1 mmol/L的DPPH溶液清除率均不足50 %,说明牛蒡多糖和多糖锌对DPPH自由基的清除能力强于杏鲍菇多糖。
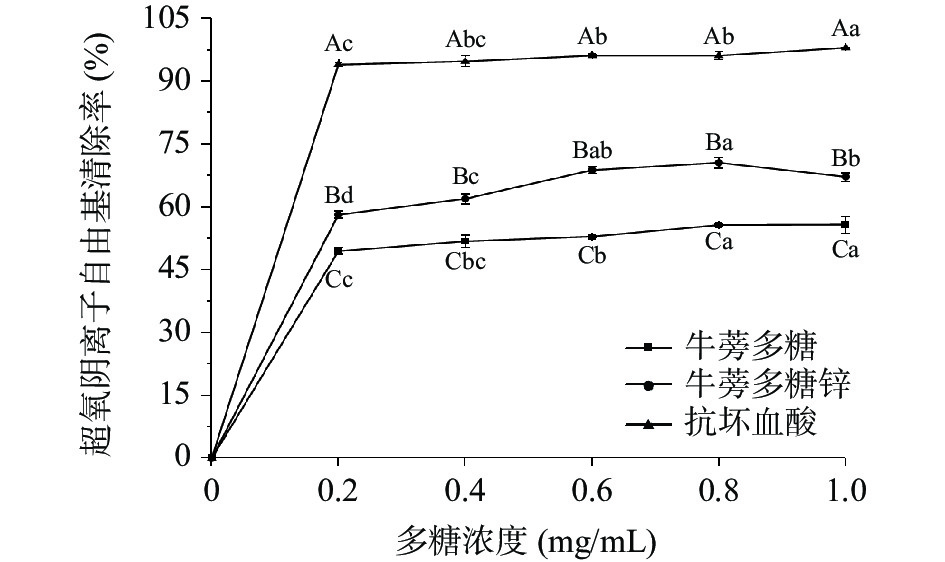
2.3.2 超氧阴离子自由基清除试验
如图7所示,牛蒡多糖和牛蒡多糖锌对超氧阴离子自由基均有一定的清除能力,但两者的清除能力都小于抗坏血酸。当浓度为0~1.0 mg/mL时,随着浓度的增加,牛蒡多糖锌对超氧阴离子自由基的清除能力呈现出先增大后变小的趋势,其清除能力始终优于原多糖。可能是因为牛蒡多糖锌与自由基反应生成的中间体更加稳定,使得其清除自由基的能力变强[40]。当浓度为1.0 mg/mL时,牛蒡多糖和牛蒡多糖锌对超氧阴离子自由基的清除率分别为55.83%和67.27%。
2.3.3 羟基自由基清除试验
如图8所示,牛蒡多糖和牛蒡多糖锌对羟基自由基均有一定的清除能力,但两者的清除能力都小于抗坏血酸。当浓度为0~1.0 mg/mL时,随着浓度的增加,牛蒡多糖对羟基自由基的清除能力先增加后稳定,牛蒡多糖锌对羟基自由基的清除能力先增大后变小,其清除率均低于15%。值得注意的是,牛蒡多糖对羟基自由基的清除能力优于牛蒡多糖锌,这可能是由于锌离子与多糖羟基上的氧结合,使游离羟基数目减少,导致多糖锌的羟基自由基清除活性减弱[41]。
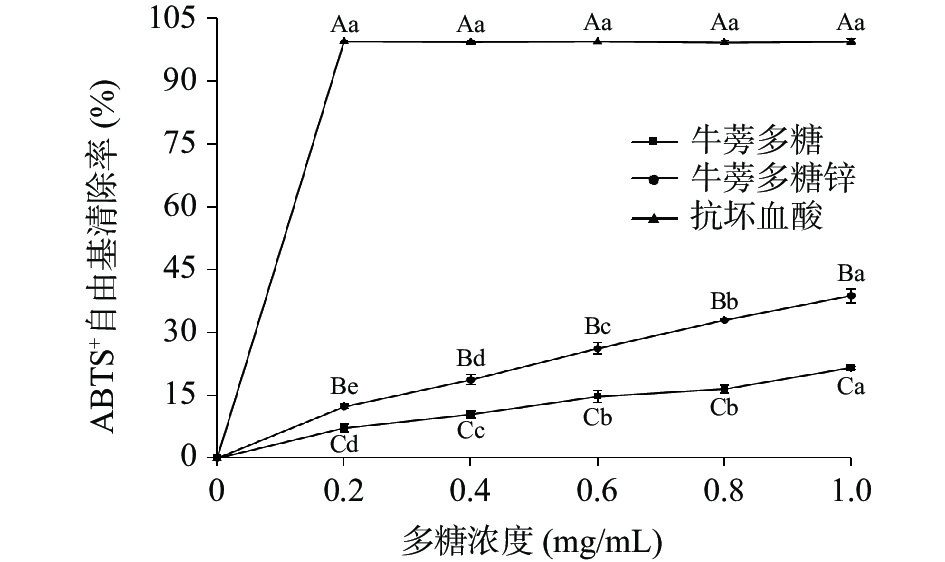
2.3.4 ABTS+自由基清除试验
如图9所示,牛蒡多糖和牛蒡多糖锌对ABTS+自由基均有一定的清除能力,但两者的清除能力都小于抗坏血酸。当浓度为0~1.0 mg/mL时,多糖和多糖锌的浓度与其对ABTS+自由基的清除能力成正相关,且多糖锌的清除能力优于原多糖。当浓度为1.0 mg/mL时,牛蒡多糖和牛蒡多糖锌对ABTS+自由基的清除率分别为21.66%和38.88%。
3. 结论
采用响应面法对牛蒡多糖锌的制备工艺进行优化,确定最佳制备工艺为:牛蒡多糖与硫酸锌的质量比37:1、反应温度50 ℃、反应时间121 min、反应pH8.6,螯合率为93.21%±0.58%。抗氧化试验表明,当浓度为1.0 mg/mL时,牛蒡多糖锌对DPPH自由基、超氧阴离子自由基和ABTS+自由基的清除率分别为84.59%±0.60%、67.27%±1.00%、38.88%±1.68%,清除能力优于牛蒡多糖,说明锌的修饰增强了牛蒡多糖的抗氧化活性。本研究为新型补锌剂的开发提供了理论依据,也为牛蒡资源的综合利用提供参考。
-
表 1 响应面试验因素与水平
Table 1 Response surface experimental factors and levels
水平 因素 A牛蒡多糖与硫酸锌
的质量比B反应温度
(℃)C反应时间
(min)D反应
pH−1 30:1 50 90 7 0 35:1 60 120 8 1 40:1 70 150 9 表 2 微波消解升温程序
Table 2 Temperature rise procedure of microwave digestion
步骤 控制温度(℃) 升温时间(min) 恒温时间(min) 1 120 5 3 2 165 5 0 3 190 10 15 表 3 响应面试验结果
Table 3 Response surface test results
试验号 A牛蒡多糖与硫酸
锌的质量比B反应
温度C反应
时间D反应
pH螯合率
(%)1 −1 −1 0 0 71.54 2 −1 0 −1 0 56.68 3 −1 0 1 0 82.63 4 −1 0 0 1 74.40 5 −1 0 0 −1 53.17 6 −1 1 0 0 76.95 7 0 −1 −1 0 81.56 8 0 −1 0 −1 63.55 9 0 −1 0 1 90.00 10 0 −1 1 0 87.52 11 0 0 1 1 84.94 12 0 0 0 0 90.32 13 0 0 −1 −1 60.08 14 0 0 0 0 86.17 15 0 0 0 0 86.51 16 0 0 0 0 86.67 17 0 0 1 −1 76.18 18 0 0 −1 1 72.95 19 0 0 0 0 88.32 20 0 1 −1 0 74.82 21 0 1 1 0 84.82 22 0 1 0 −1 78.93 23 0 1 0 1 76.99 24 1 −1 0 0 88.99 25 1 0 −1 0 83.77 26 1 0 1 0 77.30 27 1 0 0 −1 75.87 28 1 0 0 1 79.54 29 1 1 0 0 83.33 表 4 回归模型方差分析
Table 4 Analysis of variance of regression model
来源 平方和 自由度 均方 F值 P值 差异性 模型 2659.37 14 189.96 45.25 <0.0001 显著 A 449.33 1 449.33 107.05 <0.0001 ** B 4.47 1 4.47 1.06 0.3198 C 336.34 1 336.34 80.13 <0.0001 ** D 420.56 1 420.56 100.19 <0.0001 ** AB 30.64 1 30.64 7.30 0.0172 * AC 262.76 1 262.76 62.60 <0.0001 ** AD 77.09 1 77.09 18.37 0.0008 ** BC 4.08 1 4.08 0.97 0.3409 BD 201.50 1 201.50 48.00 <0.0001 ** CD 4.22 1 4.22 1.01 0.3329 A2 345.57 1 345.57 82.33 <0.0001 ** B2 1.29 1 1.29 0.31 0.5887 C2 156.63 1 156.63 37.32 <0.0001 ** D2 584.82 1 584.82 139.33 <0.0001 ** 残差 58.77 14 4.20 失拟项 46.75 10 4.68 1.56 0.3556 不显著 绝对误差 12.01 4 3.00 总和 2718.14 28 注:**P<0.01,差异极显著;*P<0.05,差异显著。 -
[1] HOU B, WANG W C, GAO H, et al. Effects of aqueous extract of Arctium lappa L. roots on serum lipid metabolism[J]. The Journal of International Medical Research,2018,46(1):158−167. doi: 10.1177/0300060517716341
[2] 刘萍. 牛蒡的开发利用现状及展望[J]. 食品研究与开发,2013,34(15):128−130. [LIU P. Processing and utilization situation of great burdock and its prospect[J]. Food Research and Development,2013,34(15):128−130. [3] 朱姗姗, 张斌, 朱文卿, 等. 牛蒡多糖特性分析及对脂多糖诱导巨噬细胞炎症的调节作用[J]. 食品工业科技,2022,43(15):272−278. [ZHU S S, ZHANG B, ZHU W Q, et al. Analysis of properties of burdock polysaccharide and its regulatory effect on lipopolysaccharide-induced macrophage inflammation[J]. Science and Technology of Food Industry,2022,43(15):272−278. [4] ZHANG N F, WANG Y, KAN J, et al. In vivo and in vitro anti-inflammatory effects of water-soluble polysaccharide from Arctium lappa[J]. International Journal of Biological Macromolecules,2019,135:717−724. doi: 10.1016/j.ijbiomac.2019.05.171
[5] 王佳佳, 刘玮, 朱静, 等. 牛蒡多糖的降血糖活性[J]. 中国药科大学学报,2013,44(5):455−459. [WANG J J, LIU W, ZHU J, et al. Hypoglycemic activity of a polysaccharide from the roots of Arctium lappa L J]. Journal of China Pharmaceutical University,2013,44(5):455−459.
[6] WATAANABE A, SASAKI H, MIYAKAWA H, et al. Effect of dose and timing of burdock (Arctium lappa) root intake on intestinal microbiota of mice[J]. Microorganisms,2020,8(2):220. doi: 10.3390/microorganisms8020220
[7] ZHANG W, LI L Y, MA Y, et al. Structural characterization and hypoglycemic activity of a novel pumpkin peel polysaccharide-chromium (III) complex[J]. Foods,2022,11(13):1821. doi: 10.3390/foods11131821
[8] XU Y, WU Y J, SUN P L, et al. Chemically modified polysaccharides: Synthesis, characterization, structure activity relationships of action[J]. International Journal of Biological Macromolecules,2019,132(1):970−977.
[9] 李玲玉, 邱志常, 朱姗姗, 等. 响应面法优化牛蒡多糖超声辅助提取工艺与抗氧化活性评价[J]. 食品科技,2020,45(11):197−204, 211. [LI L Y, QIU Z C, ZHU S S, et al. Optimization of polysaccharides from Arctium lappa L. by ultrasound-assisted extraction using response surface methodology and its antioxidant activity[J]. Food Science and Technology,2020,45(11):197−204, 211. [10] WANG Y, ZHANG N F, KAN J, et al. Structural characterization of water-soluble polysaccharide from Arctium lappa and its effects on colitis mice[J]. Carbohydrate Polymers,2019,213:89−99. doi: 10.1016/j.carbpol.2019.02.090
[11] LI L Y, QIU Z C, DONG H J, et al. Structural characterization and antioxidant activities of one neutral polysaccharide and three acid polysaccharides from the roots of Arctium lappa L.: A comparison[J]. International Journal of Biological Macromolecules,2021,182:187−196. doi: 10.1016/j.ijbiomac.2021.03.177
[12] 李卷梅. 牛蒡根多糖提取和结构特征[D]. 南昌: 南昌大学, 2019 LI J M. Extraction and structural characteristic of polysaccharides from Arctium lappa Linn. radix[D]. Nanchang: Nanchang University, 2019.
[13] 朱文卿, 朱姗姗, 何秋霞, 等. 牛蒡多糖与绿原酸对斑马鱼氧化损伤的协同抗氧化作用[J]. 中国食品学报,2022,22(4):95−103. [ZHU W Q, ZHU S S, HE Q X, et al. Synergistic antioxidant effects of burdock polysaccharide and chlorogenic acid on oxidative damage in zebrafish[J]. Journal of Chinese Institute of Food Science and Technology,2022,22(4):95−103. [14] MALINOWSKA E, KRZYCZKOWSKI W, HEROLD F, et al. Biosynthesis of selenium-containing polysaccharides with antioxidant activity in liquid culture of Hericium erinaceum[J]. Enzyme and Microbial Technology,2009,44(5):334−343. doi: 10.1016/j.enzmictec.2008.12.003
[15] 张金尧, 汪洪. 锌肥施用与人体锌素营养健康[J]. 肥料与健康,2020,47(1):11−16. [ZHANG J Y, WANG H. Zinc fertilizer application and human zinc nutrient health[J]. Fertilizer and Health,2020,47(1):11−16. [16] 袁心田, 陈华国, 赵超, 等. 锌多糖的合成方法、结构特征和生物活性研究进展[J]. 食品与发酵工业,2022,48(14):336−344. [YUAN X T, CHEN H G, ZHAO C, et al. Progress of synthesis methods, structural characteristics and biological activities of zinc polysaccharides[J]. Food and Fermentation Industry,2022,48(14):336−344. [17] SANDSTEAD H H. Subclinical zinc deficiency impairs human brain function[J]. Journal of Trace Elements in Medicine and Biology,2012,26(2/3):70−73.
[18] 姜莉媛. 水溶性大豆多糖与锌离子螯合反应机理与产物性质研究[D]. 广州: 华南理工大学, 2021 JIANG L Y. Study on the chelation mechanism of soluble soybean polysaccharides with zinc ion and the properties of the products[D]. Guangzhou: South China University of Technology, 2021.
[19] 黄靖, 邹烨, 王未, 等. 肉苁蓉多糖锌的制备、表征及抗氧化活性[J]. 化学研究,2015,26(6):584−589. [HUANG J, ZOU Y, WANG W, et al. Preparation, characterization and antioxidant activity of Cistanche tubulosa Zn2+-polysaccharide complex[J]. Chemical Research,2015,26(6):584−589. [20] MOHANTA B, SEN D J, MAHANTI B, et al. Antioxidant potential of herbal polysaccharides: An overview on recent researches[J]. Sensors International,2022,3:100158. doi: 10.1016/j.sintl.2022.100158
[21] WANG J Q, HU S Z, NIE S P, et al. Reviews on mechanisms of in vitro antioxidant activity of polysaccharides[J]. Oxidative Medicine and Cellular Longevity,2016,2016:5692852.
[22] 董淑君, 张禧庆, 刘旭龙, 等. 南瓜皮多糖锌的制备及生物利用率研究[J]. 食品工业科技,2022,43(18):200−207. [DONG S J, ZHANG X Q, LIU X L, et al. Study on preparation and bioacceptability of pumpkin skin polysaccharide-zinc complex[J]. Science and Technology of Food Industry,2022,43(18):200−207. [23] 李文文, 王丹, 董淑君, 等. 生姜皮多糖锌的制备及体外模拟消化研究[J]. 食品工业科技,2022,43(18):185−191. [LI W W, WANG D, DONG S J, et al. Preparation of ginger peel polysaccharide-zinc complex and in vitro simulated digestion study[J]. Science and Technology of Food Industry,2022,43(18):185−191. [24] 汤陈鹏, 吕峰, 王蓉琳. 孔石莼多糖锌结构表征与体外降血糖活性[J]. 食品科学,2020,41(7):52−58. [TANG C P, LÜ F, WANG R L. Structural characterization and hypoglycemic activity in vitro of Ulva pertusa polysaccharides-zinc complex[J]. Food Science,2020,41(7):52−58. [25] ZHANG M, ZHAO H, SHEN Y, et al. Preparation, characterization and antioxidant activity evaluation in vitro of Fritillaria ussuriensis polysaccharide-zinc complex[J]. International Journal of Biological Macromolecules,2020,146(1):462−474.
[26] 罗敬文, 司风玲, 顾子玄, 等. 3种木耳多糖的抗氧化活性与抑菌能力比较分析[J]. 食品科学,2018,39(19):64−69. [LUO J W, SI F L, GU Z X, et al. Antioxidant and antimicrobial activities of polysaccharides from three species ofAuricularia[J]. Food Science,2018,39(19):64−69. [27] DONG S J, ZHANG B, MA Y, et al. Pumpkin skin polysaccharide–Zn(II) complex: Preparation, characterization, and suppression of inflammation in zebrafish[J]. Foods,2022,11:2610. doi: 10.3390/foods11172610
[28] 廉雯蕾. 脱酰胺-酶解法制备米蛋白肽及其亚铁螯合物的研究[D]. 无锡: 江南大学, 2015 LIAN W L. Study on preparation of rice protein peptides with acid deamidation-enzymolysis and iron chelating[D]. Wuxi: Jiangnan University, 2015.
[29] 张浩然, 徐汀, 田恺, 等. 快速消解-电感耦合等离子体质谱法测定水产配合饲料中的铬、铜、锌、砷、镉、汞和铅[J]. 食品安全质量检测学报,2021,12(11):4365−4372. [ZHANG H R, XU T, TIAN K, et al. Determination of chromium, copper, zinc, arsenic, cadmium, mercury and lead in aquatic formula feeds by rapid digestion-inductively coupled plasma mass spectrometry[J]. Food Safety and Quality Detection Technology,2021,12(11):4365−4372. [30] 郭雷, 宋宇, 邵天舒, 等. 微波消解-电感耦合等离子体质谱法测定整蛋白型肠内营养剂中铁、锌、铜、锰元素含量[J]. 中国药业,2020,29(21):72−74. [GUO L, SONG Y, SHAO T S, et al. Content determination of Fe, Zn, Cu and Mn in intacted protein enteral nutrition powder by MAE-ICP-MS[J]. China Pharmaceuticals,2020,29(21):72−74. [31] 符玉霞, 郭欣, 魏亚博, 等. 红枣多糖羧甲基化修饰及其抗氧化活性研究[J]. 食品工业科技,2022,43(17):104−113. [FU Y X, GUO X, WEI Y B, et al. Study on carboxymethylation modification and antioxidant activity of polysaccharides from jujube[J]. Science and Technology of Food Industry,2022,43(17):104−113. [32] LI Y, ZHU C P, ZHAI X C, et al. Optimization of enzyme assisted extraction of polysaccharides from pomegranate peel by response surface methodology and their anti-oxidant potential[J]. Chinese Herbal Medicines,2018,10(4):416−423. doi: 10.1016/j.chmed.2018.08.007
[33] 阮进基, 苏帆, 云少君, 等. 杏鲍菇多糖-钙螯合物的制备及其抗氧化活性[J]. 食品工业,2022,43(2):88−93. [RUAN J J, SU F, YUN S J, et al. Preparation of Pleurotus eryngii polysaccharides-calcium chelate and its antioxidant activity research[J]. Food Industry,2022,43(2):88−93. [34] 何坤明, 王国锭, 白新鹏, 等. 山茱萸籽多糖分离纯化、结构表征及抗氧化活性[J]. 食品科学,2021,42(19):81−88. [HE K M, WANG G D, BAI X P, et al. Isolation, purification, structural characterization and antioxidant activity of Cornus officinalis seeds polysaccharides[J]. Food Science,2021,42(19):81−88. [35] 董金满, 李鸿梅, 李炳东. 罗耳阿太菌多糖锌的制备及其抗氧化活性研究[J]. 食品工业,2018,39(6):22−26. [DONG J M, LI H M, LI B D. Preparation and antioxidant activity of Athelia rolfsii polysaccharide-zinc[J]. Food Industry,2018,39(6):22−26. [36] 李兴艳, 张丙云, 尚永彪. 正交实验优化酵母多糖锌配合物的制备及其对尿素的吸附性能[J]. 食品科学,2013,34(14):57−62. [LI X Y, ZHANG B Y, SHANG Y B. Preparation of yeast polysaccharide-Zn complex and its adsorption performance for urea[J]. Food Science,2013,34(14):57−62. [37] 赵姝雯. 金针菇(Flammulina velutipes)锌多糖的制备、结构分析及其生物活性研究[D]. 南京: 南京农业大学, 2016 ZHAO S W. Preparation, characterization, antioxidant and anti-inflammatory effect of the chelate of Flammulina velutipes polysaccharide with Zn[D]. Nanjing: Nanjing Agricultural University, 2016.
[38] 顾冰飞, 赵圆圆, 陈义勇. 杏鲍菇多糖锌螯合物的制备工艺及其抗氧化活性[J]. 食品研究与开发,2019,40(4):97−103. [GU B F, ZHAO Y Y, CHEN Y Y. Preparation technology of Pleurotus eryngii polysaccharide-zinc (Ⅱ) chelate and its antioxidant activity[J]. Food Research and Development,2019,40(4):97−103. [39] 吕侠影, 姜绍通, 余振宇, 等. 苦丁-荔枝复合饮料的研制[J]. 食品工业科技,2015,36(13):225−228, 233. [LÜ X Y, JIANG S T, YU Z Y, et al. Preparation of beverage from ilex and litchi[J]. Science and Technology of Food Industry,2015,36(13):225−228, 233. [40] 吴新建, 林素英, 李荣华. 槲皮素与3d-过渡金属二价离子的配位反应研究[J]. 福建师范大学学报,2007(6):68−71. [WU X J, LIN S Y, LI R H. Research on the coordination reactions of 3d-transition metal (Ⅱ) ions with quercetin[J]. Journal of Fujian Normal University,2007(6):68−71. [41] 王元凤, 金征宇, 魏新林. 茶多糖金属络合物的制备及清除自由基活性研究[J]. 天然产物研究与开发,2009,21(3):382−387. [WANG Y F, JIN Z Y, WEI X L. Preparation and hydroxyl radical-scavenging effects of tea polysaccharides metal complexes[J]. Natural Products Research and Development,2009,21(3):382−387. -
期刊类型引用(5)
1. 王共明,黄会,丁玉竹,薛敬林,舒志强,井月欣,矫春娜,张健. 海参粉超临界CO_2萃取脱脂工艺优化及对挥发性风味物质的影响. 食品工业科技. 2025(03): 241-248 .  本站查看
本站查看
2. 李正阳,刘畅,费靖淳,周浩,韩万鑫,潘一萍,祁艳霞,赵前程. 刺参自溶肽美拉德反应产物表征及抗氧化活性研究. 食品安全质量检测学报. 2025(04): 224-233 .  百度学术
百度学术
3. 赵影,田柬昕,钟碧銮,李萌,苏可珍. 海参深加工脱腥技术研究进展. 食品工业. 2024(03): 229-235 .  百度学术
百度学术
4. 王志龙,王禹,段静瑶,苏岩峰,喻佩. 海参制品腥味化合物形成与脱腥技术研究进展. 中国调味品. 2024(06): 206-212 .  百度学术
百度学术
5. 马慧,顾雪敏,李芳,梅洁,王梓棚,孔令明. 菌酶协同处理在食品加工中的研究进展及应用. 中国调味品. 2024(07): 208-213 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:



 下载:
下载:



