Extraction Process Optimization and Antioxidant Activity Evaluation of Crude Polysaccharides from Lonicera japonica
-
摘要: 采用热水提取法提取金银花多糖,通过单因素实验考察料液比、浸提时间、浸提温度和提取次数4个因素对多糖得率的影响,在此基础上利用响应面法对提取条件进行优化。以DPPH自由基、ABTS+自由基、羟基自由基、超氧阴离子自由基清除能力和总还原力为指标评价金银花粗多糖的抗氧化活性。结果表明:金银花多糖的最佳提取工艺条件为料液比1:30(g/mL)、浸提时间120 min、浸提温度70 ℃,此条件下多糖的实际得率为6.45%±0.15%,与预测值的相对误差为1.2%。当金银花粗多糖浓度为2 mg/mL时,DPPH自由基、ABTS+自由基、羟基自由基和超氧阴离子自由基的清除率分别为88.56%、99.51%、46.40%和85.88%,总还原力为1.04。该方法制备的金银花粗多糖具有较好的抗氧化能力,这为金银花活性多糖的进一步分离、纯化及结构表征提供了理论依据。Abstract: The polysaccharides from Lonicera japonica were extracted by the hot water extraction method, and the effects of solid-liquid ratio, extraction time, extraction temperature and extraction times on the yield of polysaccharides were investigated by a single factor test. On this basis, the response surface method was used to optimize the extraction conditions. The antioxidant activity of crude polysaccharides from Lonicera japonica were evaluated by measuring DPPH free radical, ABTS+ free radical, hydroxyl free radical, superoxide anion free radical scavenging ability and total reducing power. The results showed that the optimal extraction process conditions of polysaccharides from Lonicera japonica were as follow: solid-liquid ratio of 1:30 (g/mL), extraction time of 120 min, and extraction temperature of 70 ℃. Under these conditions, the actual yield of polysaccharides from Lonicera japonica was 6.45%±0.15%, and the relative error with the predicted value was 1.2%. When the concentration of crude polysaccharides was 2 mg/mL, the maximum scavenging rates of DPPH free radical, ABTS+ free radical, hydroxyl free radical and superoxide anion free radical were 88.56%, 99.51%, 46.40% and 85.88%, respectively. Besides, the total reducing power was 1.04. The optimized crude polysaccharides had an excellent antioxidant activity, which provided a theoretical basis for further isolation, purification and characterization of active polysaccharides from Lonicera japonica.
-
金银花是忍冬科植物忍冬(Lonicera japonica Thunb.)干燥的花蕾或初开的花,属于药食同源类植物,性甘、寒,归肺、心、胃经,种植广泛,药用历史悠久,常用于清热解毒和治疗各种热性疾病[1-2]。金银花的多种功能与其含有的挥发油类[3]、有机酸类[4]、黄酮类[5]、环烯醚萜苷类[6]、三萜皂苷类[7]等多种功能性成分有关。其中,多糖是金银花中主要活性成分之一,具有抗氧化[8]、免疫调节[9]、抗炎[10]、抗胰腺癌[11]以及降血糖、降血脂[12]等良好的药理作用,在食品和医药行业有广泛的应用前景。
常见的金银花多糖的提取方法有水提法[13]、酶及复合酶提法[14]、超声波法[15]等,作为传统提取方法,水提法具有成本低、设备要求低、干扰因素少和可大量制备等优点[16]。李尔春[17]利用正交法优化水提金银花多糖工艺,得出最佳提取方案为提取温度40 ℃、提取时间为2 h、料液比为1:20(g/mL)、提取2次。Zhang等[8]利用水提法提取金银花多糖,在料液比为1:28(g/mL)、提取温度100 ℃、提取3次的提取条件下金银花多糖得率为5.3%,并经分离纯化得到5种多糖组分,对其进行结构表征和抗氧化活性研究发现,LJP-A-3多糖组分抗氧化活性最佳,对DPPH自由基、ABTS+自由基的最大清除率高于80%,对羟基自由基和超氧阴离子自由基的最大清除率约为70%。目前水提法提取金银花多糖主要采用正交法优化提取工艺,关于响应面法优化水提法提取金银花多糖的研究报道较少[18-20]。响应面法优化提取工艺,不仅可以获得高精度回归方程,而且通过合理的预测简化工艺的同时实现多变量的选择优化[21]。所以响应面结合水提法提取金银花多糖对简化工艺、提高产率和降低能耗等方面至关重要。此外,二者原材料分别来源于陕西和贵州,本实验采用的金银花来源于山东,多糖的提取率、结构和生物活性都因原材料的差异和提取条件的不同而有较大的差别。同时,二者都通过体外抗氧化实验进行研究,但评价指标既有重合又有差异,本研究通过5种指标系统评价金银花粗多糖体外抗氧化活性,避免单一抗氧化方法评价抗氧化活性的片面和不足。
本研究以金银花为原料,采用热水浸提法提取金银花多糖,在单因素实验的基础上采用Box-Behnken响应面法优化提取工艺,确定最佳提取条件;通过测定对DPPH自由基、ABTS+自由基、羟基自由基和超氧阴离子自由基的清除能力和总还原力等5项指标综合评价其抗氧化活性,为金银花多糖的提取工艺及活性评价研究提供了理论依据。
1. 材料与方法
1.1 材料与仪器
金银花 购于山东省临沂市;1,1-二苯基-2-三硝基苯肼(DPPH) 美国Sigma公司;2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(ABTS) 北京索莱宝科技有限公司;水杨酸、Tris均为分析纯 北京百拓科技有限公司;正丁醇、氯仿、无水乙醇、氢氧化钠、苯酚、浓硫酸、过硫酸钾、过氧化氢、盐酸、抗坏血酸、邻苯三酚、七水合硫酸亚铁、铁氰化钾、三氯乙酸等均为分析纯 国药集团化学试剂有限公司。
DHG-9070A型电热恒温鼓风干燥箱 上海一恒科技有限公司;SS-H6数显恒温水浴锅 江苏金怡仪器科技有限公司;HY-2A调速多用振荡器 国华电器有限公司;DDL5冷冻离心机 长沙英泰仪器有限公司;FD-304冷冻干燥机 济南骏德仪器有限公司;MD Spectramax i3酶标仪 美国Molecular Devices公司;AX224ZH电子天平 奥豪斯仪器(常州)有限公司。
1.2 实验方法
1.2.1 原料预处理
取适量干燥的金银花,置于50 ℃鼓风干燥箱中干燥24 h,粉碎,过60目筛,备用。
1.2.2 金银花多糖的提取
参照柴美玲等[22]实验方法并稍作修改提取金银花多糖。取金银花粗粉4.0 g置于烧杯中,加入一定量的去离子水,在一定温度下提取一定时间,过滤得到金银花多糖浸提液。浸提液经4倍体积的无水乙醇处理,4000 r/min离心15 min获得沉淀物。沉淀物经Sevage法除蛋白(氯仿:正丁醇=4:1,重复5次)后,冷冻干燥后得金银花粗多糖。
1.2.3 单因素实验
1.2.3.1 料液比对金银花多糖得率的影响
参照“1.2.2”进行操作,固定浸提时间120 min、浸提温度70 ℃、提取1次,考察不同料液比1:20、1:25、1:30、1:35、1:40(g/mL)对金银花多糖得率的影响。
1.2.3.2 浸提时间对金银花多糖得率的影响
参照“1.2.2”进行操作,固定料液比为1:30(g/mL)、浸提温度70 ℃、提取1次,考察不同浸提时间60、90、120、150、180 min对金银花多糖得率的影响。
1.2.3.3 浸提温度对金银花多糖得率的影响
参照“1.2.2”进行操作,固定料液比为1:30(g/mL)、浸提时间120 min、提取1次,考察不同浸提温度50、60、70、80、90 ℃对金银花多糖得率的影响。
1.2.3.4 提取次数对金银花多糖得率的影响
参照“1.2.2”进行操作,固定料液比为1:30(g/mL)、浸提时间120 min、浸提温度70 ℃,考察不同提取次数1、2、3、4、5次对金银花多糖得率的影响。
1.2.4 响应面试验设计
在单因素实验的基础上,以Box-Behnken响应面模型设计试验,选取料液比、浸提时间和浸提温度三个影响因素为自变量,以金银花多糖得率为响应值Y,进行三因素三水平的响应面试验分析,采用Design-Expert 8.0.6统计分析软件建立Box-Behnken模型,优化金银花多糖的提取工艺参数,试验因素与水平见表1。
表 1 响应面因素及水平设计Table 1. Factors and levels of response surface experiment水平 因素 A料液比(g/mL) B浸提时间(min) C浸提温度(℃) −1 1:25 90 60 0 1:30 120 70 1 1:35 150 80 1.2.5 金银花多糖含量测定
1.2.5.1 标准曲线的绘制
利用苯酚-硫酸法测定多糖含量[23]。准确称取烘干至恒重的葡萄糖10 mg,用去离子水定容至100 mL,得葡萄糖标准溶液。分别吸取0、0.2、0.4、0.6、0.8、1.0、1.2、1.4、1.6、1.8、2.0 mL的葡萄糖标准溶液于试管中,加入去离子水至2 mL,分别加入浓硫酸5 mL,5%的苯酚1 mL。混匀,沸水浴20 min,静置10 min,490 nm下测其吸光值。以葡萄糖浓度X(mg/mL)为横坐标,OD490(Y)为纵坐标,绘制葡萄糖标准曲线,得回归方程Y=5.7496X−0.0299,R2=0.9992。
1.2.5.2 多糖得率的计算
用1.2.5.1中方法测定吸光度,根据标准曲线计算金银花多糖的质量浓度[24]。按照以下公式计算金银花多糖得率:
N=C×B×VW×100 式中:N代表金银花多糖得率(%);C代表根据标准曲线计算得到的金银花多糖的质量浓度(mg/mL);B代表稀释倍数;V代表多糖浸提液体积(mL);W代表金银花质量(g)。
1.2.6 体外抗氧化活性评价
1.2.6.1 金银花粗多糖对DPPH自由基清除能力的测定
取上述方法制备的金银花粗多糖,配制成不同浓度的金银花粗多糖溶液(0、0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL),各取2 mL,加入2 mL DPPH-乙醇(0.2 mmol/L)溶液,室温避光孵育30 min。以蒸馏水为空白对照,VC为阳性对照,于517 nm下测定吸光值,重复3次[25-26]。按照以下公式计算DPPH自由基清除率:
DPPH自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为样品在溶液体系中反应后在517 nm下吸光值;A2为乙醇代替DPPH-乙醇溶液在溶液体系中反应后在517 nm下吸光值;A0为蒸馏水代替样品在溶液体系中反应后在517 nm下吸光值。
1.2.6.2 金银花粗多糖对ABTS+自由基清除能力的测定
蒸馏水配制2.45 mmol/L的过硫酸钾溶液和7 mmol/L的ABTS+溶液,等体积混合,定容至100 mL,得到ABTS+储备液,室温避光孵育12~16 h。取适量ABTS+储备液通过pH为7.4的PBS缓冲液稀释至在734 nm下的吸光值为0.7±0.02,得到ABTS+工作液。取上述方法制备的金银花粗多糖,配制成不同浓度的金银花粗多糖溶液(0、0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL),各取0.1 mL,加入1.9 mL的ABTS+工作液,摇匀后避光反应6 min。以蒸馏水为空白对照,VC为阳性对照,于734 nm下测定吸光值,重复3次[27-28]。按照以下公式计算ABTS+自由基清除率:
ABTS+自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为样品在溶液体系中反应后在734 nm下吸光值;A2为蒸馏水代替ABTS+工作液在溶液体系中反应后在734 nm下吸光值;A0为蒸馏水代替样品在溶液体系中反应后在734 nm下吸光值。
1.2.6.3 金银花粗多糖对羟基自由基清除能力的测定
取上述方法制备的金银花粗多糖,配制成不同浓度的金银花粗多糖溶液(0、0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL),各取1 mL,分别加入8.8 mmol/L的H2O2、9 mmol/L的硫酸亚铁溶液和水杨酸溶液各1 mL,摇匀后在37 ℃水浴条件下反应30 min,以蒸馏水为空白对照,VC为阳性对照,于510 nm下测定吸光值,重复3次[29-30]。按照以下公式计算羟基自由基清除率:
羟基自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为样品在溶液体系中反应后在510 nm下吸光值;A2为蒸馏水代替H2O2溶液在溶液体系中反应后在510 nm下吸光值;A0为蒸馏水代替样品在溶液体系中反应后在510 nm下吸光值。
1.2.6.4 金银花粗多糖对超氧阴离子自由基清除能力的测定
取上述方法制备的金银花粗多糖,配制成不同浓度的金银花粗多糖溶液(0、0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL),各取1 mL,分别加入4.5 mL 50 mmol/L的Tris-HCl缓冲液(pH8.2),混匀于25 ℃下反应20 min,加入0.1 mL 3 mmol/L的邻苯三酚溶液,混匀于25 ℃下反应5 min,立即加入1 mL 8 mmol/L的HCl终止反应。以蒸馏水为空白对照,VC为阳性对照,于320 nm下测定吸光值,重复3次[31-32]。按照以下公式计算超氧阴离子自由基清除率:
超氧阴离子自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为样品在溶液体系中反应后在320 nm下吸光值;A2为蒸馏水代替邻苯三酚溶液在溶液体系中反应后在320 nm下吸光值;A0为蒸馏水代替样品在溶液体系中反应后在320 nm下吸光值。
1.2.6.5 金银花粗多糖总还原力的测定
取上述方法制备的金银花粗多糖,配制成不同浓度的金银花粗多糖溶液(0、0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL),各取1 mL,分别加入1%的铁氰化钾和0.2 mol/L的磷酸缓冲液(pH6.6)各1 mL,在50 ℃水浴条件下反应20 min,迅速加入10%的三氯乙酸,8000 r/min离心5 min。取2 mL上清液,分别加入2 mL蒸馏水和0.1%的FeCl3,混匀静置10 min。以蒸馏水为空白对照,VC为阳性对照,于700 nm下测定吸光值,重复3次[33]。按照以下公式计算总还原力:
总还原力=A−A0 式中:A为样品在溶液体系中反应后在700 nm下的吸光值;A0为蒸馏水代替样品在溶液体系中反应后在700 nm下的吸光值。
1.3 数据处理
每组实验均重复3次,测定数据以平均值±标准差表示,利用Design Expert 8.0.6进行数据统计分析;采用SPSS 21.0软件对数据进行差异性显著分析(Duncan法,n=3,P<0.05);采用Origin 2017软件绘图。
2. 结果与分析
2.1 金银花多糖提取单因素实验结果
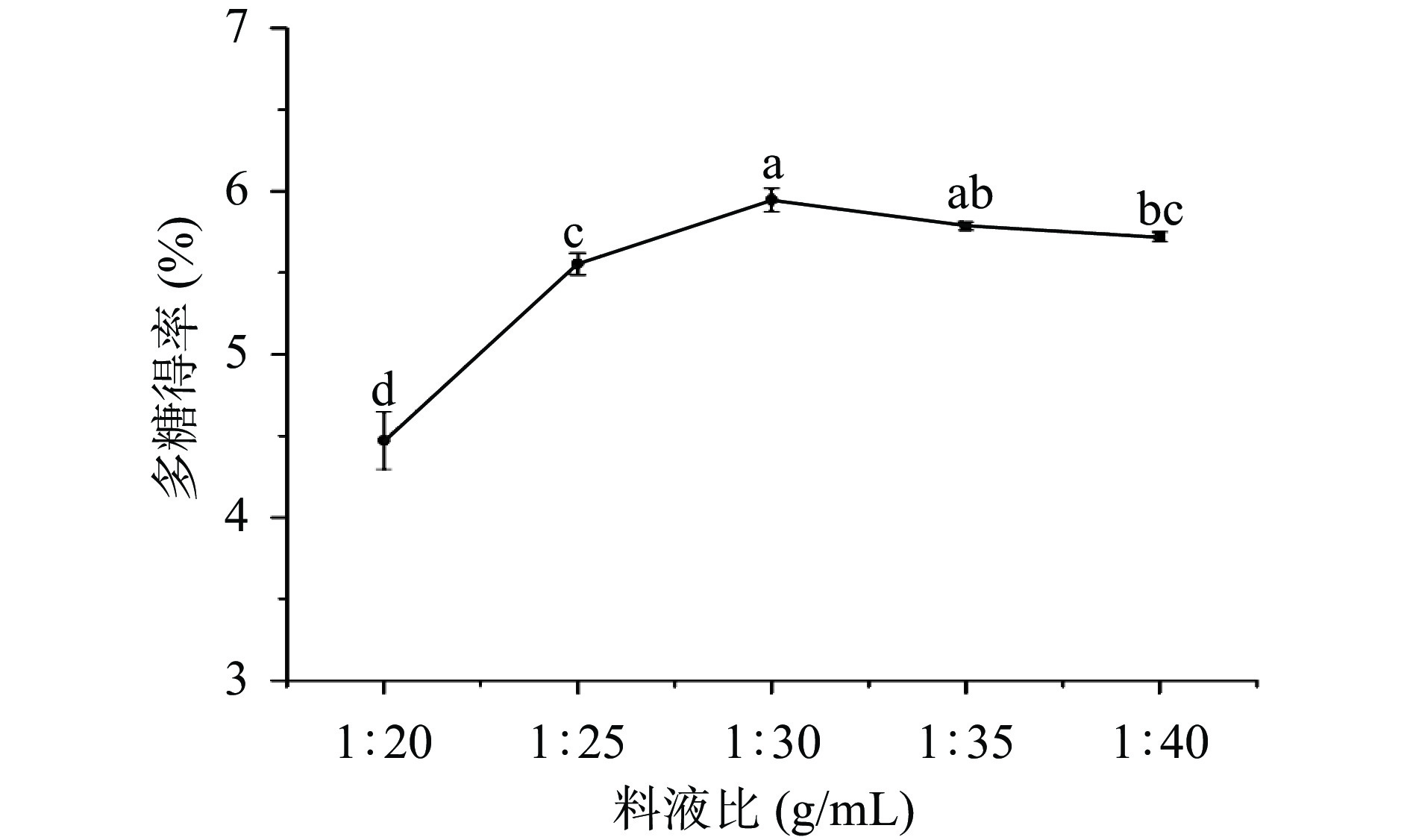
2.1.1 料液比对金银花多糖得率的影响
料液比对金银花多糖得率的影响如图1所示,料液比在1:20~1:40(g/mL)范围内,金银花多糖的得率呈现先上升后略降的趋势,当料液比为1:30(g/mL)时金银花多糖得率达到最大,为5.94%。推测原因为随着提取溶剂的增加,多糖的浸出率随之提高,但过高的料液比会溶出其他水溶物,抑制多糖释放[34-35]。结合实验结果,选择料液比1:25~1:35(g/mL)进行后续试验。
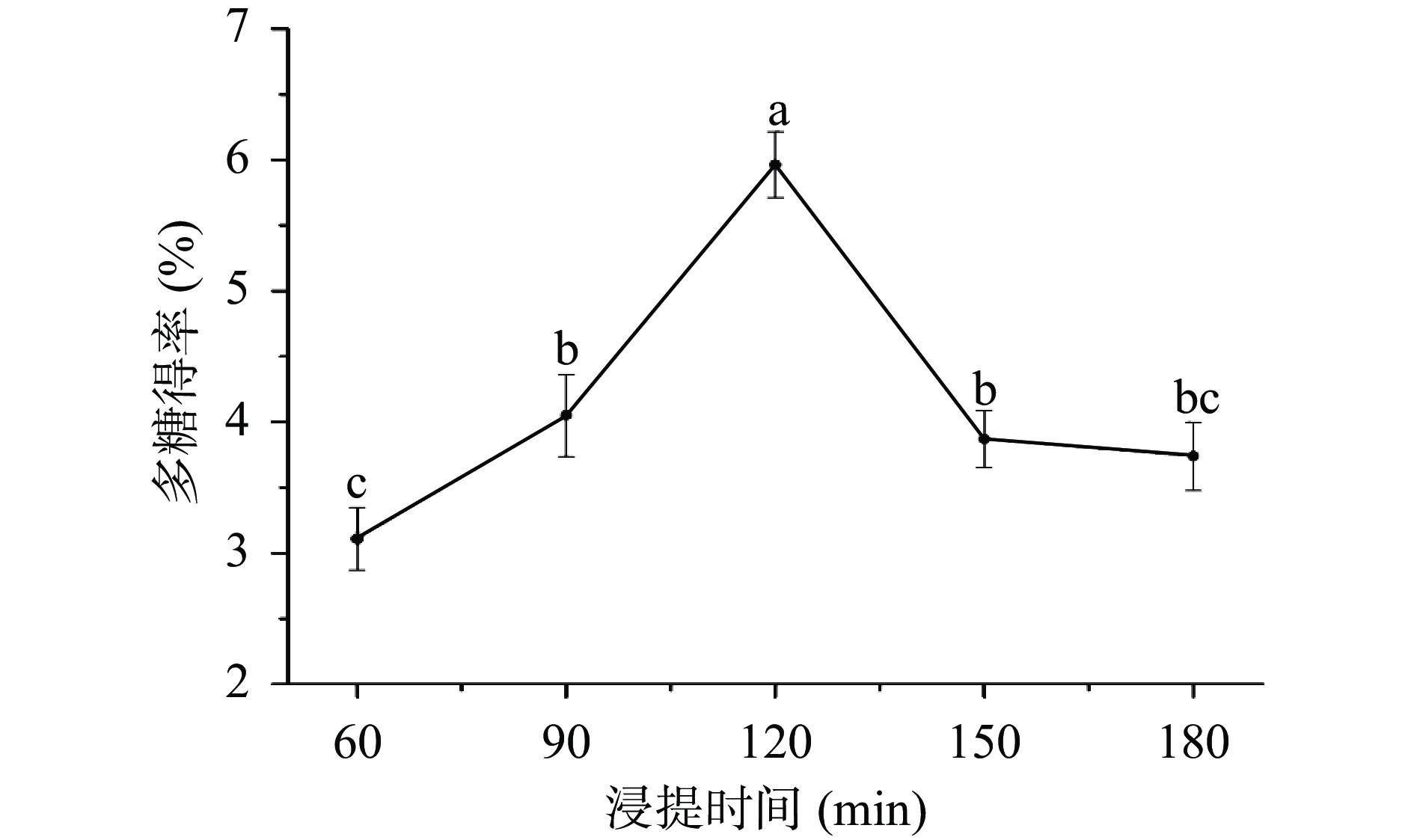
2.1.2 浸提时间对金银花多糖得率的影响
浸提时间对金银花多糖得率的影响如图2所示,浸提时间在60~180 min范围内,金银花多糖的得率呈现先上升后下降的趋势,当浸提时间为120 min时多糖得率最大,为5.96%。推测可能由于长时间高温浸提使多糖部分水解,所以浸提时间不宜过久[36]。结合实验结果,选择浸提时间90~150 min进行后续试验。
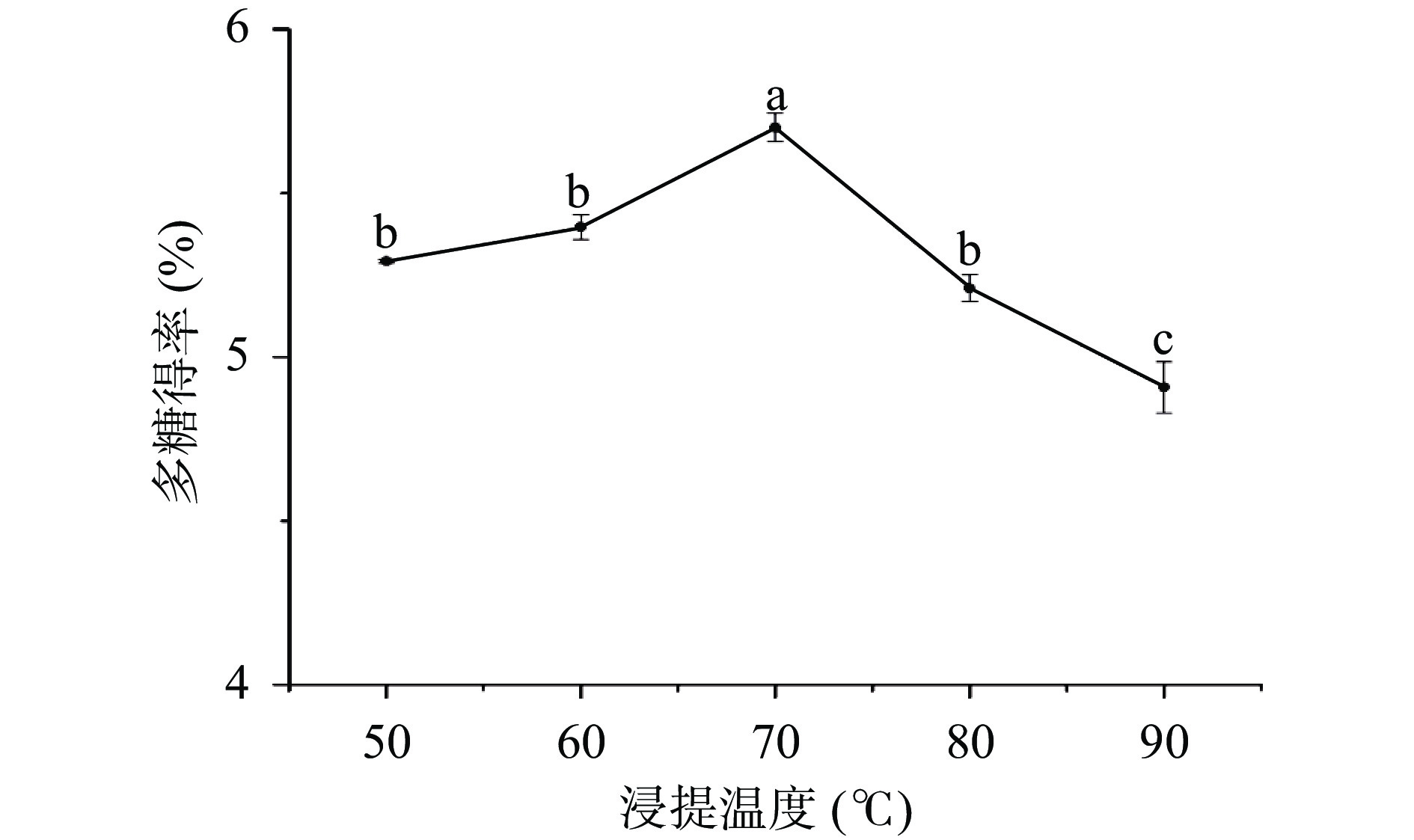
2.1.3 浸提温度对金银花多糖得率的影响
浸提温度对金银花多糖得率的影响如图3所示,浸提温度在50~90 ℃范围内,金银花多糖的得率呈现先升高后下降的趋势,在浸提温度70 ℃时多糖得率达到最大,为5.70%。推测可能是温度升高使部分多糖水解[37]。结合实验结果,选择浸提温度60~80 ℃进行后续试验。
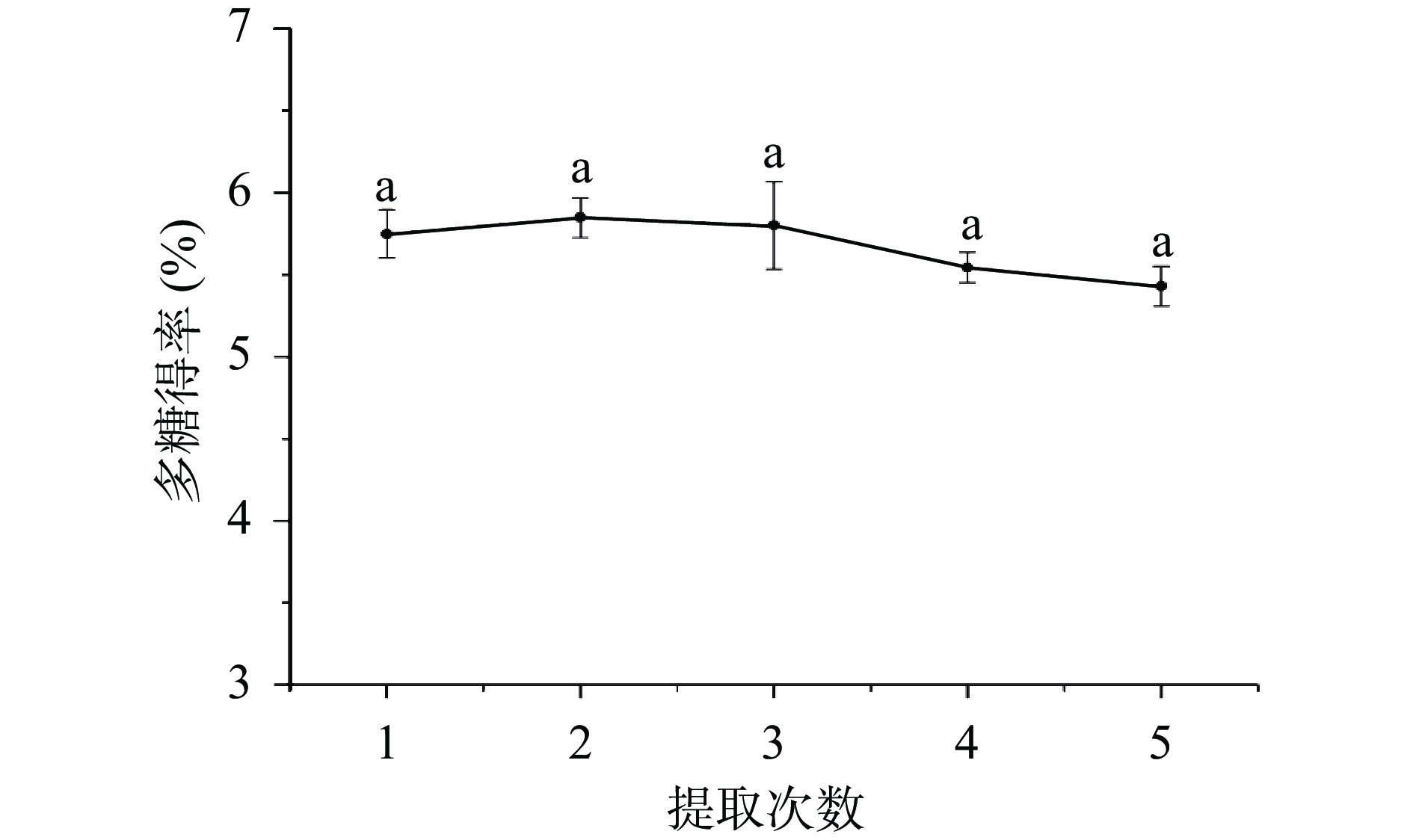
2.1.4 提取次数对金银花多糖得率的影响
提取次数对金银花多糖得率的影响如图4所示,结果显示,固定条件下(料液比为1:30(g/mL)、浸提时间120 min、浸提温度70 ℃),提取次数对金银花多糖得率影响较小,提取1~5次多糖的得率无显著性差异。金银花多糖的得率呈现先升高后下降的趋势,以提取次数2次时多糖得率最大,为5.84%;之后随着提取次数的增加多糖得率略有下降。推测原因可能是随着提取次数的增加,金银花多糖的溶出增加,但提取液体积增加,多糖提取、浓缩的损耗增加,考虑到节约成本和降低能耗,最佳提取次数选择为提取1次[38]。
2.2 金银花多糖提取条件响应面试验结果
2.2.1 响应面模型的建立与分析
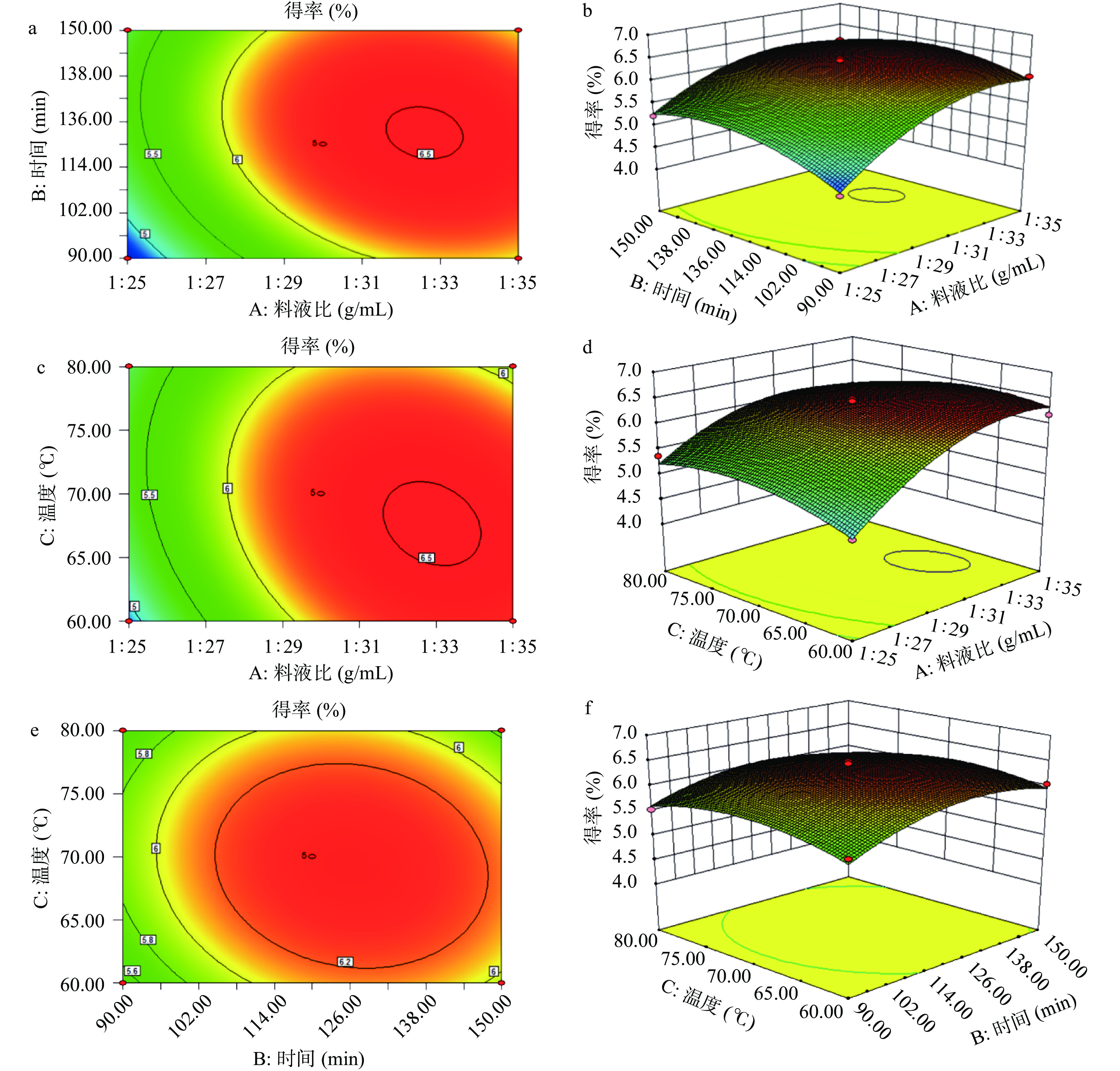
以金银花多糖得率为因变量(Y),料液比A、浸提时间B、浸提温度C为自变量,采用响应面法进行数据分析,对试验所得结果采用Design Expert 8.0.6软件进行回归分析,试验设计及结果见表2,方差分析见表3。试验数据通过Design Expert 8.0.6软件进行回归方程多项式拟合与分析,得到回归方程为:Y=6.37+0.53A+0.15B−0.027C−0.14AB−0.19AC−0.07BC−0.5A2−0.37B2−0.29C2。为了验证金银花多糖提取工艺条件的二次多项回归方程的可行性,对该回归模型进行方差分析和显著性检验,结果如表3所示:该模型差异性显著(P<0.0001),失拟项不显著(P>0.05),说明此模型拟合度较好;校正模型的相关系数R2为0.9740,校正后决定系数R2Adj为0.9405,说明选用的模型与实际情况拟合较好、误差小,可以在实际实验中反映各因素对金银花多糖得率之间的关系。由表3可知,一次项中料液比(A)对多糖得率的线性效应极显著(P<0.0001);浸提时间(B)对多糖得率的线性效应显著(P<0.05);浸提温度(C)对多糖得率的线性效应不显著(P>0.05)。二次项中,A2、B2、C2影响极显著(P<0.01),AC影响显著(P<0.05),AB、BC影响不显著(P>0.05),所以最终确定回归模型为Y=6.37+0.53A+0.15B−0.19AC−0.5A2−0.37B2−0.29C2。由F值可以得出,在试验范围内各因素对金银花多糖得率的影响大小为料液比>浸提时间>浸提温度。
表 2 响应面试验设计与结果Table 2. Experimental design and results for response surface试验号 A料液比 B浸提时间 C浸提温度 多糖得率(%) 1 1 −1 0 6.09 2 0 0 0 6.48 3 0 0 0 6.37 4 0 1 1 5.67 5 0 0 0 6.44 6 0 1 −1 6.03 7 1 0 1 5.91 8 −1 1 0 5.21 9 0 −1 1 5.53 10 0 −1 −1 5.61 11 0 0 0 6.23 12 0 0 0 6.35 13 1 1 0 6.12 14 −1 −1 0 4.61 15 1 0 −1 6.18 16 −1 0 1 5.37 17 −1 0 −1 4.88 表 3 回归模型方差分析Table 3. Analysis of variance of regression model平方和 自由度 均方 F值 P值 显著性 模型 4.86 9 0.54 29.11 <0.0001 显著 A料液比 2.24 1 2.24 120.62 <0.0001 ** B浸提时间 0.18 1 0.18 9.55 0.0176 * C浸提温度 6.050×10−3 1 6.050×10−3 0.33 0.5857 AB 0.081 1 0.081 4.38 0.0746 AC 0.14 1 0.14 7.79 0.0269 * BC 0.020 1 0.020 1.06 0.3381 A2 1.03 1 1.03 55.81 0.0001 ** B2 0.58 1 0.58 31.21 0.0008 ** C2 0.36 1 0.36 19.53 0.0031 ** 总残差 0.13 7 0.019 失拟项 0.093 3 0.031 3.35 0.1365 不显著 纯误差 0.037 4 9.230×10−3 总回归 4.99 16 R2=0.9740 R2Adj=0.9405 注:**P<0.01,差异极显著;*P<0.05,差异显著。 2.2.2 响应面图的分析
各因素之间的交互作用结果见图5。图5(a)、(b)所示,料液比对多糖得率的影响大于浸提时间,等高线近似椭圆,说明两因素交互作用对多糖得率的影响较弱;图5(c)、(d)所示,料液比对多糖得率的影响大于浸提温度,等高线呈椭圆形,说明两因素交互作用对多糖得率影响较大;图5(e)、(f)所示,浸提时间对多糖得率的影响大于浸提温度,等高线近似椭圆,说明两因素对多糖得率影响较弱。
2.2.3 回归模型的验证
通过回归模型的分析,以多糖得率为评价指标,金银花多糖的理论提取工艺条件为:料液比1:32.82(g/mL),浸提时间123.48 min,浸提温度67.56 ℃,此条件下,模型预测金银花多糖得率为6.53%。考虑实际操作简便,将工艺条件调整为料液比1:30(g/mL)、浸提时间120 min、浸提温度70 ℃,此条件下多糖得率为6.45%±0.15%,相对误差为1.2%,与预测值误差较小,表明提取工艺条件参数优化稳定可靠,可用于生产实践。
2.3 金银花粗多糖体外抗氧化能力评价
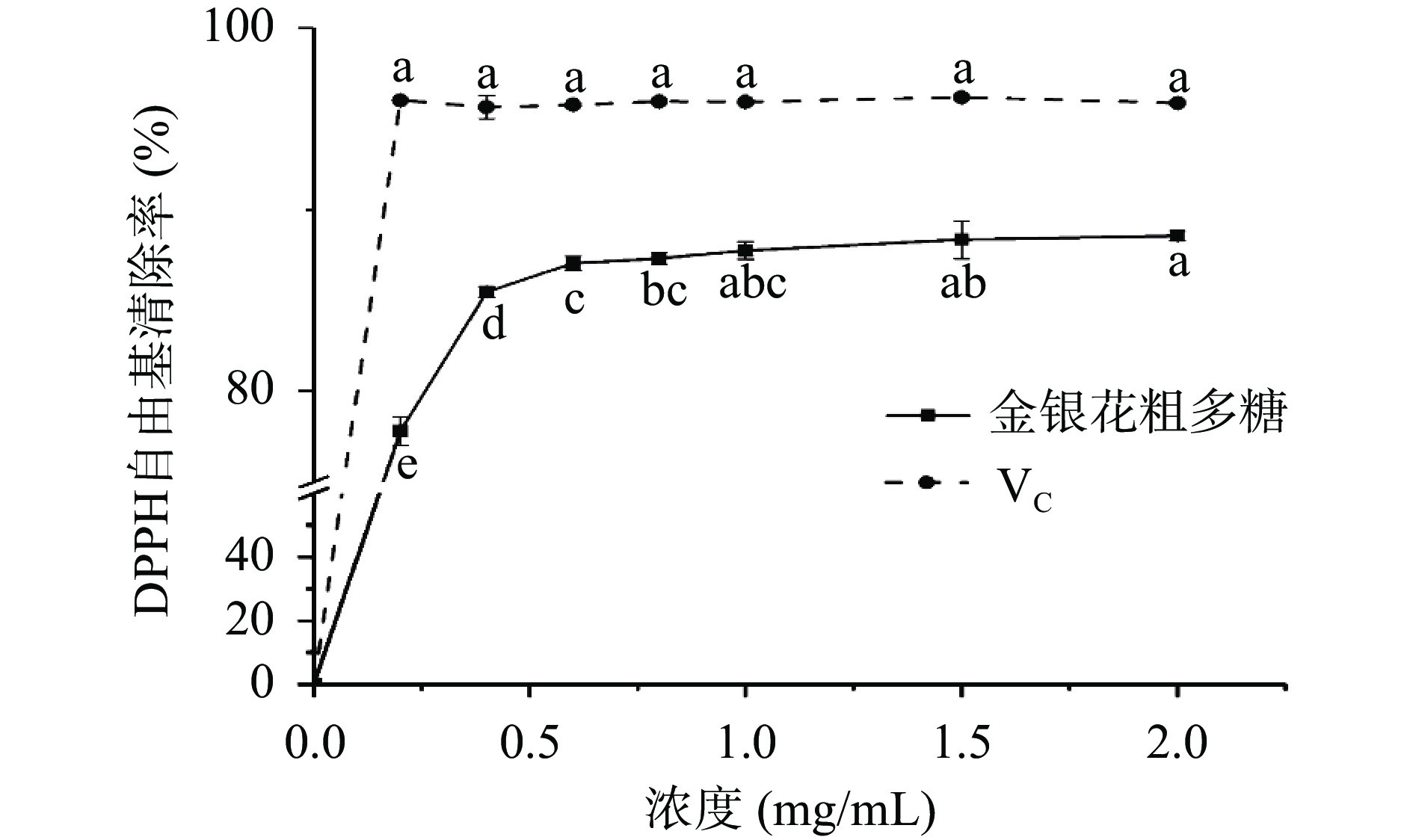
2.3.1 金银花粗多糖对DPPH自由基清除能力
如图6所示,在0~2.0 mg/mL范围内,随着金银花粗多糖质量浓度的增大,其对DPPH自由基的清除率也随之升高,当浓度达到0.4 mg/mL后,曲线趋于平缓,表明在一定浓度范围内,金银花粗多糖对DPPH自由基的清除能力与其浓度呈剂量效应关系,最大清除率为88.56%。相比之下,VC对DPPH自由基清除效果更好,在0.2~2.0 mg/mL基本不变,维持在95%~96%。此外,向佳兰等[39]研究发现超声提取金银花多糖对DPPH自由基具有较强的清除能力,在测定最大浓度0.28 mg/mL时的清除率为88.88%。本研究制备的金银花粗多糖在0.2 mg/mL时清除率为77.80%,也显示出较强的DPPH自由基清除能力。
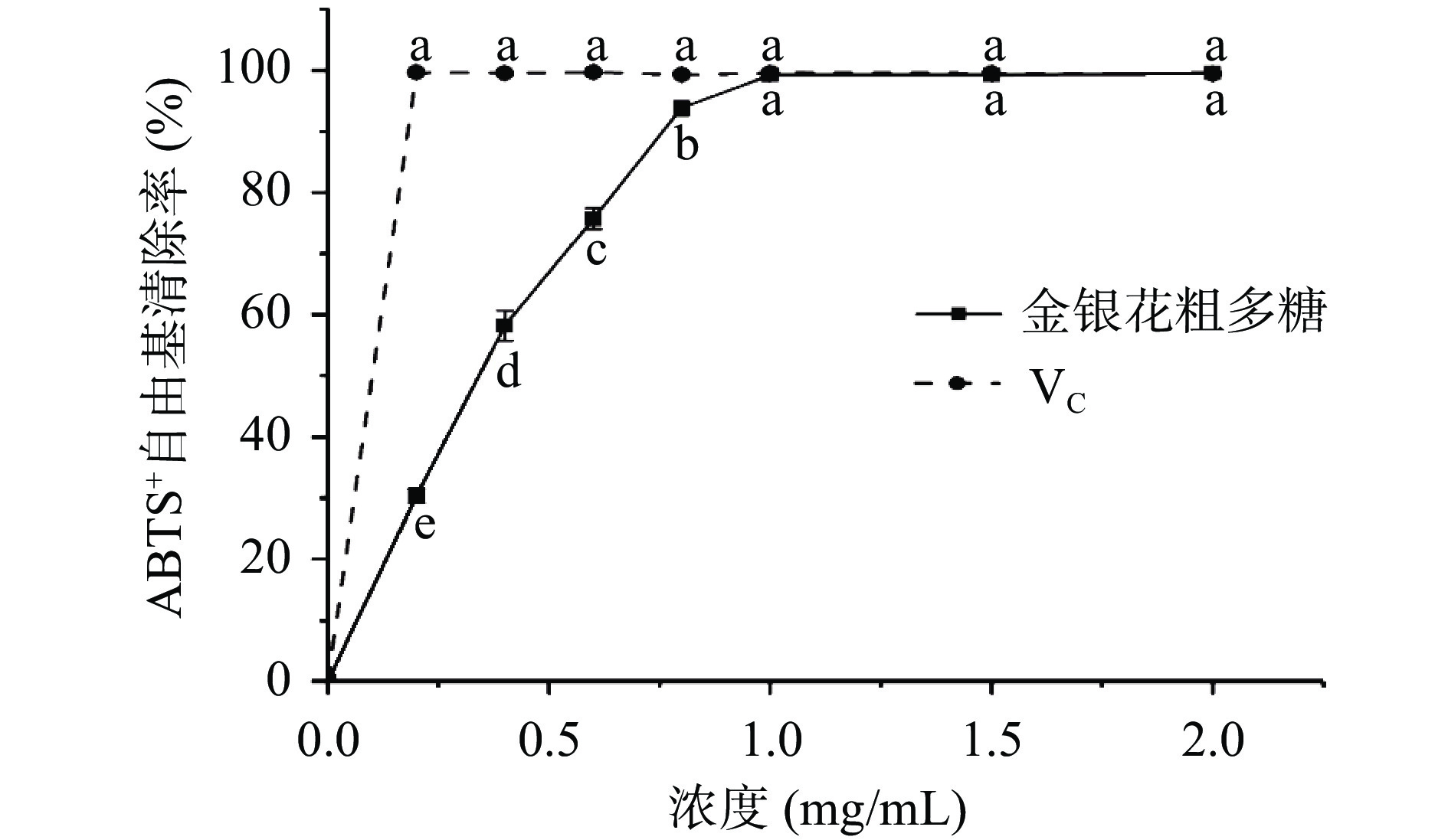
2.3.2 金银花粗多糖对ABTS+自由基清除能力
如图7示,在0~2.0 mg/mL范围内,随着金银花粗多糖质量浓度的增大,其对ABTS+自由基的清除率也随之升高,之后趋于平缓。当浓度大于1.0 mg/mL后,对ABTS+自由基的清除率接近于VC,最大清除率为99.51%。刘红萍等[40]发现金银花酸性多糖LJP-A对ABTS+自由基具有较强的清除能力,在浓度为2 mg/mL,清除率接近70%,金银花中性多糖LJP-N活性低于LJP-A,当浓度增至4 mg/mL时,对ABTS+自由基清除率不足40%。说明该方法制备的金银花粗多糖的ABTS+自由基清除能力优于LJP-A和LJP-N,这种作用效果差异可能与金银花的生长环境、品种、提取工艺等多种因素有关。
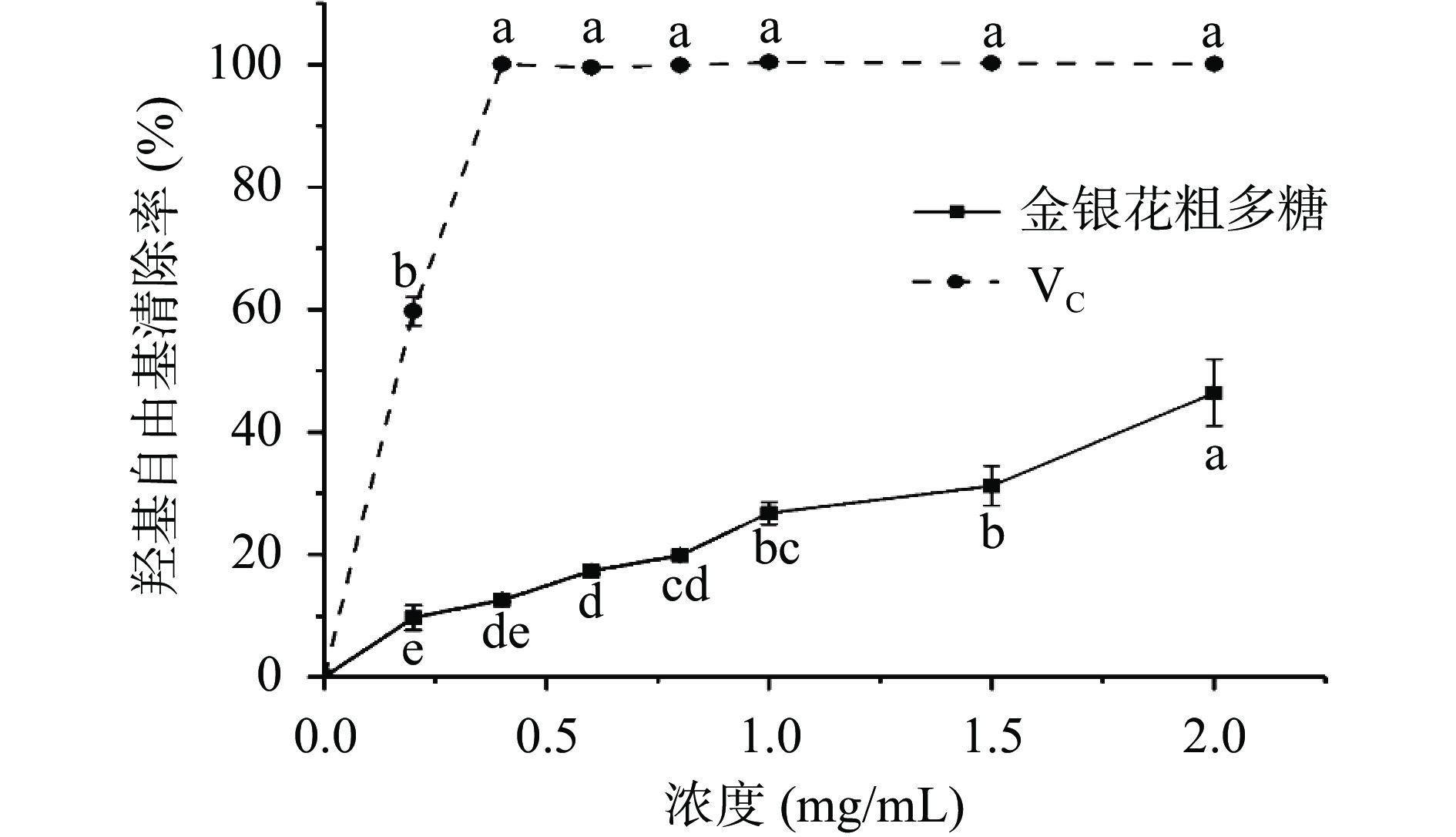
2.3.3 金银花粗多糖对羟基自由基清除能力
如图8示,在0~2.0 mg/mL范围内,随着质量浓度的增大,其对羟基自由基的清除率随之升高,从9.69%增加到46.40%,呈现一定的浓度依赖性,在相同质量浓度下清除能力显著低于VC。在刘红萍等[40]的研究中发现,在2 mg/mL的浓度下,金银花酸性多糖LJP-A和中性多糖LJP-N的羟基自由基清除率分别约为30%和10%,同等浓度下羟基自由基的清除能力均低于本研究制备的金银花粗多糖。此外,赵鹏等[41]发现经水提、柱层析法分离、羧甲基化后的金银花多糖在浓度为2 mg/mL时对羟基自由基的清除率约为60%,比未羧甲基化的金银花多糖的清除率提高了约20%,这可能由于提取分离方法不同以及衍生化过程使得多糖亲水性不同造成的。
2.3.4 金银花粗多糖对超氧阴离子自由基清除能力
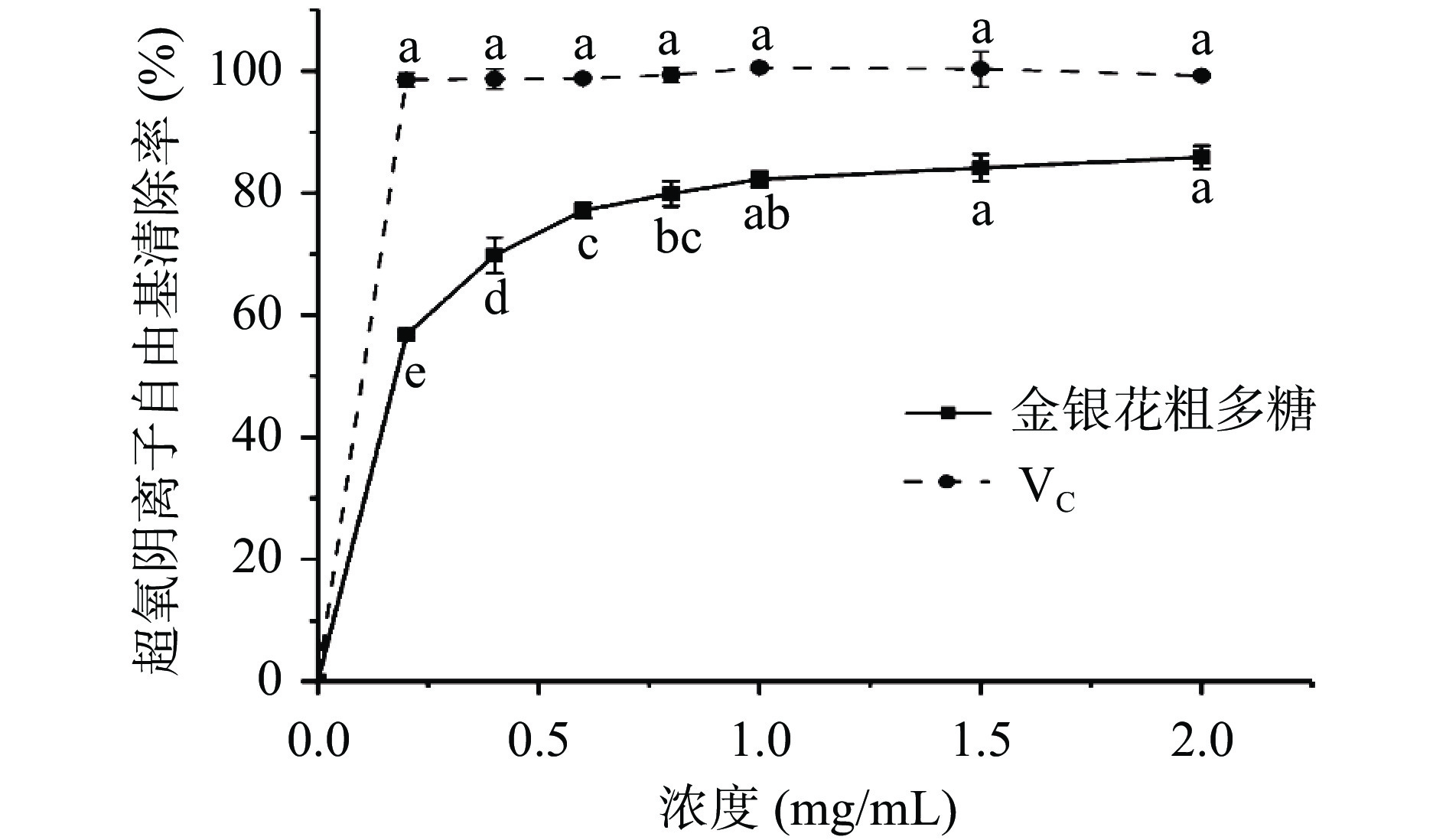
如图9所示,在0~2.0 mg/mL范围内,金银花粗多糖对超氧阴离子自由基具有较好的清除能力,并且随着浓度的增加,清除率从56.78%增加到85.88%。但是在相同质量浓度下,VC对超氧阴离子自由基的清除率基本维持在98%以上,优于金银花粗多糖的清除效果。Zhang等[8]利用热水浸提法获得金银花粗多糖并利用柱层析法获得五种金银花多糖级分,在0~2 mg/mL的多糖浓度下,超氧阴离子自由基最大清除率在40%~70%之间,低于该方法制备的金银花粗多糖对超氧阴离子自由基的清除效果。
2.3.5 金银花粗多糖总还原力测定结果
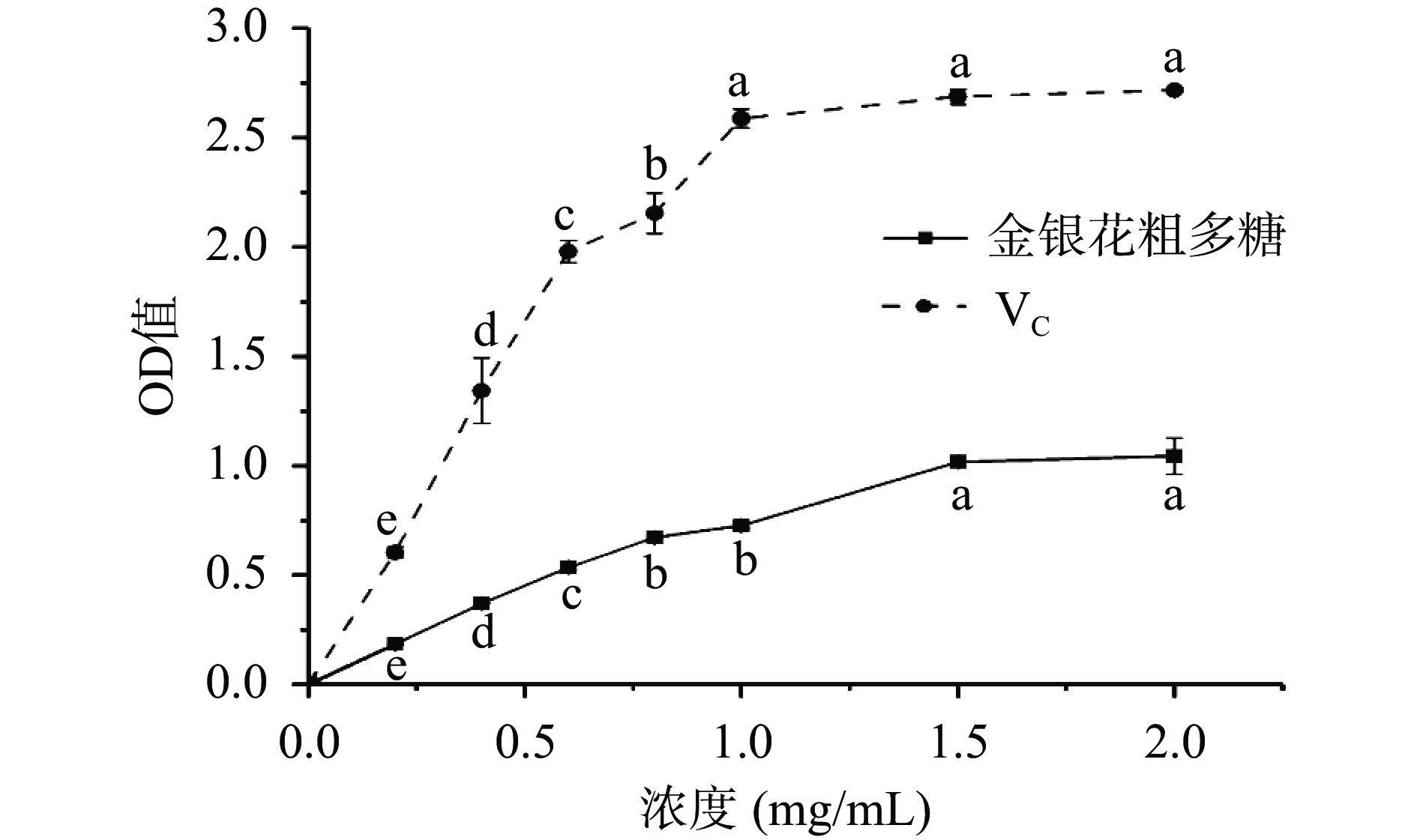
吸光度OD值越高说明金银花粗多糖的总还原能力越高。如图10所示,金银花粗多糖在0~2.0 mg/mL范围内呈现出不同程度的还原能力,且和浓度呈剂量效应关系,随着质量浓度的增加,还原力缓慢上升,当浓度到1.5 mg/mL后,还原能力趋于平缓,最大为1.04。VC在测定浓度范围内还原能力随着浓度的增加快速上升,当浓度大于1.0 mg/mL后趋于平缓,最大为2.71。相同质量浓度下,金银花粗多糖的总还原力低于VC。此外,李尔春[17]研究发现,在2 mg/mL浓度时金银花粗多糖最大总还原力低于0.5,总还原力略低于本研究制备的金银花粗多糖。
3. 结论
在单因素实验的基础上,通过响应面优化试验设计,得到金银花多糖最佳提取工艺参数:料液比1:30(g/mL),浸提时间120 min,浸提温度70 ℃,在此条件下金银花多糖的实际得率为6.45%±0.15%,与预测值差距较小,表明通过响应面优化金银花多糖的提取工艺准确可行。体外抗氧化活性结果显示:金银花粗多糖的抗氧化活性虽然低于VC,但当浓度为2 mg/mL时,对DPPH自由基的清除率为88.56%,对ABTS+自由基的清除率为99.51%,对超氧阴离子自由基的清除率为85.88%,对羟基自由基的清除率较低为46.40%,总还原力为1.04。研究结果显示,金银花粗多糖具有较好的抗氧化活性,可为金银花产品的开发和利用提供技术支持和理论依据。
-
表 1 响应面因素及水平设计
Table 1 Factors and levels of response surface experiment
水平 因素 A料液比(g/mL) B浸提时间(min) C浸提温度(℃) −1 1:25 90 60 0 1:30 120 70 1 1:35 150 80 表 2 响应面试验设计与结果
Table 2 Experimental design and results for response surface
试验号 A料液比 B浸提时间 C浸提温度 多糖得率(%) 1 1 −1 0 6.09 2 0 0 0 6.48 3 0 0 0 6.37 4 0 1 1 5.67 5 0 0 0 6.44 6 0 1 −1 6.03 7 1 0 1 5.91 8 −1 1 0 5.21 9 0 −1 1 5.53 10 0 −1 −1 5.61 11 0 0 0 6.23 12 0 0 0 6.35 13 1 1 0 6.12 14 −1 −1 0 4.61 15 1 0 −1 6.18 16 −1 0 1 5.37 17 −1 0 −1 4.88 表 3 回归模型方差分析
Table 3 Analysis of variance of regression model
平方和 自由度 均方 F值 P值 显著性 模型 4.86 9 0.54 29.11 <0.0001 显著 A料液比 2.24 1 2.24 120.62 <0.0001 ** B浸提时间 0.18 1 0.18 9.55 0.0176 * C浸提温度 6.050×10−3 1 6.050×10−3 0.33 0.5857 AB 0.081 1 0.081 4.38 0.0746 AC 0.14 1 0.14 7.79 0.0269 * BC 0.020 1 0.020 1.06 0.3381 A2 1.03 1 1.03 55.81 0.0001 ** B2 0.58 1 0.58 31.21 0.0008 ** C2 0.36 1 0.36 19.53 0.0031 ** 总残差 0.13 7 0.019 失拟项 0.093 3 0.031 3.35 0.1365 不显著 纯误差 0.037 4 9.230×10−3 总回归 4.99 16 R2=0.9740 R2Adj=0.9405 注:**P<0.01,差异极显著;*P<0.05,差异显著。 -
[1] 宋亚玲, 倪付勇, 赵祎武, 等. 金银花化学成分研究进展[J]. 中草药,2014,45(24):3656−3664. [SONG Y L, NI F Y, ZHAO Y W, et al. Research progress on chemical constituents from Lonicerae flos[J]. Chinese Herbal Medicines,2014,45(24):3656−3664. doi: 10.7501/j.issn.0253-2670.2014.24.027 [2] 吴娇, 王聪, 于海川. 金银花中的化学成分及其药理作用研究进展[J]. 中国实验方剂学杂志,2019,25(4):225−234. [WU J, WANG C, YU H C. Chemical constituents and pharmacological effect of Lonicerae Japonicae Flos[J]. Chinese Journal of Experimental Traditional Medical Formulae,2019,25(4):225−234. doi: 10.13422/j.cnki.syfjx.20190408 [3] 马勤川, 贾凯, 卢杰, 等. 亚临界R134a萃取金银花挥发油[J]. 食品工业科技,2012,33(13):197−200. [MA Q C, JIA K, LU J, et, al. Subcritical R134a extraction of volatile oil from Lonicera japonica[J]. Science and Technology of Food Industry,2012,33(13):197−200. [4] 张伟, 董红敬, 刘伟, 等. 应用离子液体逆流色谱系统分离制备金银花中的绿原酸[J]. 食品工业,2021,42(2):107−110. [ZHANG W, DONG H J, LIU W, et al. Purification of chlorogenic acid from Lonicera japonica Thunb. by high-speed counter-current chromatography using [C6min] [PF6] as the modifier of two-phase solvent system[J]. The Food Industry,2021,42(2):107−110. [5] 罗磊, 张冰洁, 韦倩倩, 等. 金银花黄酮对过氧化氢诱导RAW264.7巨噬细胞损伤的保护作用[J]. 中国食品学报,2019,19(5):18−25. [LUO L, ZHANG B J, WEI Q Q, et al. Protective effects of flavonoids from Lonicera japonica Thunb. on hydrogen peroxide induced toxicity in RAW264.7 cells[J]. Journal of Chinese Institute of Food Science and Technology,2019,19(5):18−25. [6] 杨然, 陆远, 郝昊, 等. 金银花环烯醚萜苷类化学成分和药理活性研究进展[J]. 中国中药杂志,2021,46(11):2746−2752. [YANG R, LU Y, HAO H, et al. Research progress on chemical constituents and pharmacological activities of iridoid glycosides in Lonicera japonica[J]. China Journal of Chinese Materia Medica,2021,46(11):2746−2752. [7] 朱文卿, 任汉书, 郑媛媛, 等. 金银花的功能性成分及其生物活性研究进展[J]. 食品工业科技,2021,42(13):412−426. [ZHU W Q, REN H S, ZHENG Y Y, et al. Research progress in functional components and bioactivity of honeysuckle[J]. Science and Technology of Food Industry,2021,42(13):412−426. doi: 10.13386/j.issn1002-0306.2020070411 [8] ZHANG T, LIU H P, BAI X Y, et al. Fractionation and antioxidant activities of the water-soluble polysaccharides from Lonicera japonica Thunb[J]. International Journal of Biological Macromolecules,2020,151:1058−1066. doi: 10.1016/j.ijbiomac.2019.10.147
[9] ZHOU X, DONG Q, KAN X, et al. Immunomodulatory activity of a novel polysaccharide from Lonicera japonica in immunosuppressed mice induced by cyclophosphamide[J]. PLoS One,2018,13(10):e0204152. doi: 10.1371/journal.pone.0204152
[10] WANG D, ZHAO X, LIU Y. Hypoglycemic and hypolipidemic effects of a polysaccharide from flower buds of Lonicera japonica in streptozotocin-induced diabetic rats[J]. International Journal of Biological Macromolecules,2017,102:396−404. doi: 10.1016/j.ijbiomac.2017.04.056
[11] LIN L, WANG P, DU Z, et al. Structural elucidation of a pectin from flowers of Lonicera japonica and its antipancreatic cancer activity[J]. International Journal of Biological Macromolecules,2016,88:130−137. doi: 10.1016/j.ijbiomac.2016.03.025
[12] YANG Q X, WANG Q L, DENG W W, et al. Anti-hyperuricemic and anti-gouty arthritis activities of polysaccharide purified from Lonicera japonica in model rats[J]. International Journal of Biological Macromolecules,2019,123:801−809. doi: 10.1016/j.ijbiomac.2018.11.077
[13] 宋逍, 辛亚洲, 赵鹏, 等. 响应面法优化金银花多糖乙酰化工艺[J]. 食品工业科技,2014,35(17):262−265, 342. [SONG X, XIN Y Z, ZHAO P, et al. Acetylization derivatives synthesis of polysaccharides from Lonicera japonica[J]. Science and Technology of Food Industry,2014,35(17):262−265, 342. doi: 10.13386/j.issn1002-0306.2014.17.049 [14] 周小楠, 董群. 正交试验优化酶法提取金银花多糖工艺[J]. 食品科学,2012,33(22):119−122. [ZHOU X N, DONG Q. Orthogonal array design for optimization of enzymatic extraction of polysaccharides from Flos Lonicerae[J]. Food Science,2012,33(22):119−122. [15] 赵鹏, 李稳宏, 朱骤海, 等. 响应面法优化金银花多糖超声提取工艺研究[J]. 食品科学,2009,30(20):151−154. [ZHAO P, LI W H, ZHU Z H, et al. Optimization of ultrasonic for polysaccharides from Lonicera japonica[J]. Food Science,2009,30(20):151−154. [16] HUANG H, HUANG G. Extraction, separation, modification, structural characterization, and antioxidant activity of plant polysaccharides[J]. Chemical Biology & Drug Design,2020,96(5):1209−1222.
[17] 李尔春. 金银花多糖的分离纯化与生物活性研究[D]. 西安: 陕西师范大学, 2008. LI E C. Studies on the isolation, purification and bioactivity of polysaccharides from Flos lonicerae[D]. Xi’an: Shaanxi Normal University, 2008.
[18] 殷洪梅, 吕新勇, 萧伟. 金银花多糖的制备工艺优化及免疫活性研究[J]. 中国中药杂志,2010,35(4):453−455. [YIN H M, LÜ X Y, XIAO W. Preparation process optimization and immune activity study of honeysuckle polysaccharide[J]. China Journal of Chinese Materia Medica,2010,35(4):453−455. [19] 邓庆华. 用正交试验法优化金银花多糖提取工艺[D]. 长春: 东北师范大学, 2008. DENG Q H. The research on optimizing the procedure of the extraction of Lonicera japonica Thunb with the orthogonal testing method[D]. Changchun: Northeast Teachers University, 2008.
[20] 何俊婷. 金银花多糖提取工艺优化[J]. 应用化工,2014,43(4):692−695. [HE J T. Optimization of extraction technology of Lonicera japonica polysaccharide[J]. Applied Chemical Industry,2014,43(4):692−695. [21] CHHAYA R, G. C. MAJUMDAR, SIRSHEDU D. Optimization of process parameters for water extraction of stevioside using response surface methodology[J]. Separation Science and Technology,2012,47(7):1014−1022. doi: 10.1080/01496395.2011.641055
[22] 柴美灵, 李娜, 乔宏萍, 等. Box-Behnken法优化甘草多糖提取工艺及其体外抗氧化活性分析[J]. 食品工业科技,2021,42(23):192−200. [CHAI M L, LI N, QIAO H P, et al. Application of Box-Behnken design for ultrasonic-assisted extraction of glycyrrhiza polysaccharide and its antioxidant activity analysis in vitro[J]. Science and Technology of Food Industry,2021,42(23):192−200. [23] DUBOIS M. Colorimetric method for determination of sugars and related substances[J]. Analytical Chemistry,1956,28(3):350−356. doi: 10.1021/ac60111a017
[24] 郭畅, 李超, 侯明明, 等. 荔枝草多糖的提取工艺优化及其体外抗氧化、降血糖活性分析[J]. 食品工业科技,2022,43(20):211−219. [GUO C, LI C, HOU M M et al. Extraction optimization and its inoxidizability and hypoglycemic properties in vitro of polysaccharide from Salvia plebeian R. Br[J]. Science and Technology of Food Industry,2022,43(20):211−219. [25] MOHSEN S M, AMMAR A S M. Total phenolic contents and antioxidant activity of corn tassel extracts[J]. Food Chemistry,2009,112(3):595−598. doi: 10.1016/j.foodchem.2008.06.014
[26] SUN X, HAO L, MA H, et al. Extraction and in vitro antioxidant activity of exopolysaccharide by Pleurotus eryngii SI-02[J]. Brazilian Journal of Microbiology,2014,44(4):1081−1088.
[27] DESEO M A, ELKINS A, ROCHFORT S, et al. Antioxidant activity and polyphenol composition of sugarcane molasses extract[J]. Food Chemistry,2020,314:126180. doi: 10.1016/j.foodchem.2020.126180
[28] 陈红惠, 牛念拉姆. 底圩茶多糖的超声波辅助提取及其抗氧化活性[J]. 食品工业科技,2020,41(21):179−184. [CHEN H H, NIU N L M. Ultrasonic extraction and antioxidant activity of polysaccharide from Dixu tea[J]. Science and Technology of Food Industry,2020,41(21):179−184. [29] CAILLET S, YU H, LESSARD S, et al. Fenton reaction applied for screening natural antioxidants[J]. Food Chemistry,2007,100(2):542−552. doi: 10.1016/j.foodchem.2005.10.009
[30] YU M, CHEN M, GUI J, et al. Preparation of chlorella vulgaris polysaccharides and their antioxidant activity in vitro and in vivo[J]. International Journal of Biological Macromolecules,2019,137:139−150. doi: 10.1016/j.ijbiomac.2019.06.222
[31] 王静杰, 杜鑫, 钟强, 等. 超声辅助酶法制备海参性腺多糖的结构特性及抗氧化活性[J]. 食品科学,2021,42(21):97−104. [WANG J J, DU X, ZHONG Q, et al. Structural characteristics and antioxidant activity of polysaccharides prepared from sea cucumber gonad by ultrasound-assisted enzymatic hydrolysis[J]. Food Science,2021,42(21):97−104. doi: 10.7506/spkx1002-6630-20201215-186 [32] ZHU S, YANG W, LIN Y, et al. Antioxidant and anti-fatigue activities of selenium-enriched peptides isolated from Cardamine violifolia protein hydrolysate[J]. Journal of Functional Foods,2021,79(2):104412.
[33] ZHAO C C, LI X, MIAO J, et al. The effect of different extraction techniques on property and bioactivity of polysaccharides from Dioscorea hemsleyi[J]. International Journal of Biological Macromolecules,2017,102:847−856. doi: 10.1016/j.ijbiomac.2017.04.031
[34] 任朝辉, 冯国辉, 张传博. 姬松茸深层发酵多糖提取工艺优化及抗氧化活性[J]. 食品工业科技,2017,38(14):216−222. [REN Z H, FENG G H, ZHANG C B. Optimization of extraction technology and antioxidant activity determination of polysaccharide from submerged fermentation mycelium in Agaricus blazei Murrill[J]. Science and Technology of Food Industry,2017,38(14):216−222. [35] 曹楠楠, 陈香荣, 吴艳. 苦豆子多糖的超声波提取工艺优化及理化性质研究[J]. 现代食品科技,2014,30(2):209−215, 99. [CAO N N, CHEN X R, WU Y. Optimization of ultrasonic extraction and physiochemical characteristics of polysaccharides from Sophora alopecuroides seeds[J]. Modern Food Science & Technology,2014,30(2):209−215, 99. [36] 王金华, 杜超, 梁晨, 等. 贵长猕猴桃多糖提取工艺及体外抗氧化功能[J]. 食品科学,2016,37(20):19−23. [WANG J H, DU C, LIANG C, et al. Extraction and antioxidant activity of polysaccharides from Guichang kiwifruit[J]. Food Science,2016,37(20):19−23. doi: 10.7506/spkx1002-6630-201620004 [37] 宋佳敏, 王鸿飞, 孙朦, 等. 响应面法优化金蝉花多糖提取工艺及抗氧化活性分析[J]. 食品科学,2018,39(4):275−281. [SONG J M, WANG H F, SUN M, et al. Optimization of extraction and antioxidant activity of polysaccharides from Cordyceps cicadae by response surface methodology[J]. Food Science,2018,39(4):275−281. doi: 10.7506/spkx1002-6630-201804041 [38] 李梦依, 汲德群, 李迎秋, 等. 牡丹籽多糖提取工艺及体外抗氧化活性研究[J]. 食品研究与开发,2022,43(7):104−111. [LI M Y, JI D Q, LI Y Q, et al. Peony seed polysaccharide extraction technology and antioxidant activity in vitro studies[J]. Food Research and Development,2022,43(7):104−111. [39] 向佳兰, 王茜, 谢阳, 等. 响应曲面法优化金银花多糖提取条件及抗氧化活性研究[J]. 乐山师范学院学报,2015,30(12):36−41. [XIANG J L, WANG Q, XIE Y, et al. A study of optimization of extraction conditions and antioxidant activity for polysaccharide from honeysuckle by response surface methodology[J]. Journal of Leshan Normal University,2015,30(12):36−41. doi: 10.3969/j.issn.1009-8666.2015.12.008 [40] 刘红萍, 赵琳, 龙源元, 等. 金银花多糖的组成成分与抗氧化活性[J]. 贵州农业科学,2019,47(6):107−112. [LIU H P, ZHAO L, LONG Y Y, et al. Components and antioxidant activity of Lonicera japonica polysaccharide[J]. Guizhou Agricultural Sciences,2019,47(6):107−112. doi: 10.3969/j.issn.1001-3601.2019.06.025 [41] 赵鹏, 张婷婷. 响应面法优化金银花多糖羧甲基化工艺及抗氧化性研究[J]. 天然产物研究与开发,2015,27(1):114−119, 190. [ZHAO P, ZHANG T T. Preparation of carboxymethyl Lonicera japonica polysaccharides and its antioxidant ability[J]. Natural Product Research and Development,2015,27(1):114−119, 190. -
期刊类型引用(24)
1. 于纯淼,廖贤,陈小倩,李艾欣,陈佳,于苗苗. 复合酶法提取诺丽多糖的工艺优化及其体外抗氧化活性. 食品研究与开发. 2025(03): 142-151 .  百度学术
百度学术
2. 张彪,杨晓宽. 纳豆菌发酵板栗渣工艺优化及其多糖的抗氧化性. 食品研究与开发. 2025(03): 160-166 .  百度学术
百度学术
3. 杨胜男,赵斗,刘宇桂,仇燕. 菜芙蓉花黄酮的超声协同双水相提取、成分分析及抗氧化性. 食品研究与开发. 2025(05): 102-113 .  百度学术
百度学术
4. 王红,彭励,宋乐,冯璐,李振凯,李彦青,高跳. 银柴胡多糖超声辅助提取工艺优化及抗氧化活性分析. 食品工业科技. 2024(01): 185-191 .  本站查看
本站查看
5. 张欣,刘盈,刘会平,马笑笑,李灿,张慧慧,王兵. 荠菜粗多糖提取优化及其理化功能与抗氧化性. 食品研究与开发. 2024(02): 103-111 .  百度学术
百度学术
6. 李春晓,宋庆琳,焦旭,冯慧程,陈虞超,郭生虎,张波,薛涛. 金莲花多糖提取工艺优化及其抗氧化活性评价. 药学研究. 2024(01): 24-29 .  百度学术
百度学术
7. 梁金月,周洪鑫,张雨晴,王玲娜,李佳,赵东升. 金银花多酚和多糖同步提取工艺优化及其抗氧化活性研究. 中国食品添加剂. 2024(03): 1-10 .  百度学术
百度学术
8. 任晓莉,杨璐,乔鹏,缪奕锴,杨懿昂,代秋红,张贤德. 复合酶法提取槐花多糖的工艺优化及其抗氧化活性. 食品工业科技. 2024(07): 8-14 .  本站查看
本站查看
9. 高长久,李文超,张朝立,孟令锴,王春辉. 红瑞木果多糖抗氧化活性的初步研究. 中国中医药现代远程教育. 2024(10): 139-141 .  百度学术
百度学术
10. 陈美花,黄舒喆,牛改改,蓝尉冰,覃媚. 白茅根金银花复合果冻的研制. 中国食品添加剂. 2024(08): 129-138 .  百度学术
百度学术
11. 唐一诺,章肖肖,宋文文,宋盈萱,高露,陈晓乐,郑振佳. 胭脂虫红色素口红制备工艺优化及品质分析. 中国食品添加剂. 2024(08): 139-147 .  百度学术
百度学术
12. 高昕冉,李心圆,王绍倩,沈一凡,刘克海. 石榴籽多糖的提取、纯化及体外抗氧化和降血糖活性分析. 山东农业大学学报(自然科学版). 2024(04): 516-525 .  百度学术
百度学术
13. 石云鑫,杨家,潘诗琴,曾诚,郭荣荣,李晓蝶,宋旭琴,杨剑,宋亚. 不同方法提取的山茱萸多糖品质特征. 南方农业学报. 2024(07): 2031-2043 .  百度学术
百度学术
14. 苏宁,刘志明,王海英. 木醋液型饲料添加剂储藏稳定性研究. 中国饲料. 2024(21): 67-73 .  百度学术
百度学术
15. 罗雨菲,黄秀壁,苏芬安,谭义秋,陈永,刘小玲. 姑辽茶粗多糖提取工艺优化及其免疫调节活性评价. 食品工业科技. 2024(23): 161-169 .  本站查看
本站查看
16. 王国霞,牛祎琳,牛富婷,程莹莹. 不同提取方法对密银花多糖理化性质及抗氧化活性的影响. 食品工业科技. 2024(24): 196-203 .  本站查看
本站查看
17. 吴霞,周攀,常雪婷,李耀竞,吴科锋,邓路铭. 响应面法优化羊栖菜多糖脱蛋白工艺及其抗氧化活性分析. 粮食与油脂. 2024(12): 135-141 .  百度学术
百度学术
18. 刘丽桃,傅春燕,刘诗薇,周秀娟,谢雨芊,欧阳玉珍,王彪,葛金文. 响应面法优化降脂通脉方多糖的提取工艺研究. 中医药导报. 2024(12): 58-62 .  百度学术
百度学术
19. 李梦娜,黄佳蓉,马俊炜,张泓瑞,陈博儒,曾新安,朱峰,黄燕燕. 天然多糖的提取纯化及其对食品物理特性改善的应用研究. 食品科技. 2024(12): 204-212 .  百度学术
百度学术
20. 许梦粤,曾长立,王红波. 药食同源植物多糖提取方法、结构解析和生物活性研究进展. 食品研究与开发. 2023(19): 216-224 .  百度学术
百度学术
21. 黄明浩,黄泰奇,邓丽娟. 响应面法优化白英粗多糖提取工艺及其体外抗氧化活性的分析. 食品工业科技. 2023(22): 219-225 .  本站查看
本站查看
22. 赵燕燕,房世杰,张政,祁华梅,薄学敏,魏佳,吴斌. 沙枣花多糖提取工艺优化及其对益生菌的增殖作用. 食品工业科技. 2023(22): 134-142 .  本站查看
本站查看
23. 冉俊枫,张文明,张静雯,任艳,吕露阳,曾锐. 苦竹笋多糖提取工艺优化及其抗氧化活性研究. 食品科技. 2023(10): 165-172 .  百度学术
百度学术
24. 蒋大珍,马佰诚,杨皎,罗进城,孙雪薇,李佳琳. 槲寄生多糖提取工艺优化及抗氧化活性研究. 北方农业学报. 2023(05): 84-92 .  百度学术
百度学术
其他类型引用(7)





 下载:
下载:






 下载:
下载:



