Analyzing of the Composition and Medicinal Properties of Gastrodia elata during Cooking Based on Metabonomics and Network Pharmacology
-
摘要: 目的:通过代谢组学、网络药理学及分子对接技术阐述天麻在熟制过程中成分及其药理活性变化。方法:使用LC-QTOF-MS及R语言对天麻成分进行检测和分析;通过PubChem数据库及文献查找筛选出具有生物活性的成分;使用Swiss target prediction数据库及SEA数据库对成分靶点进行预测,GeneCards数据库和OMIM数据库获取疾病靶点;通过STRING 11.5数据库及Cytoscape3.8.2软件绘制药物-化合物-靶点网络及靶点蛋白互作网络,筛选关键成分及靶点;通过DAVID数据库和OmicShare Tools对交集靶点进行GO富集和KEGG通路注释分析。结果:在熟制天麻和新鲜天麻中找出89种在含量方面具有差异的成分;分别筛选出11种具有治疗惊厥作用的成分以及410个潜在靶点,5种具有治疗糖尿病及其并发症作用的成分及698个潜在靶点;GO和KEGG富集分析发现天麻通过IL-17信号通路、cAMP信号通路、神经活性物质受体信号通路、阿尔茨海默病信号通路以及多巴胺能神经突触信号通路治疗惊厥,通过AGE-RAGE信号通路、HIF-1、VEGF以及TNF信号通路治疗糖尿病;分子对接结果显示筛选出的成分均结合在靶点蛋白的空腔中,结合自由能均小于0 kcal/mol,分子对接构象稳定。结论:熟制天麻具有更好的神经保护作用,新鲜天麻在治疗糖尿病及其引发的心血管疾病等方面具有更好的效果。Abstract: Objective: To explain the changes of composition and medicinal properties of Gastrodia elata during cooking by metabonomics, network pharmacology and molecular docking techniques. Methods: The components of Gastrodia elata were detected by LC-QTOF-MS and analyzed by R language. The bioactive ingredients were screened through PubChem database and literature. Swiss target prediction database and SEA database were used to predict the potential targets of the active ingredients, while GeneCards database and OMIM database were used to search for diseases-related targets. The STRING 11.5 database and Cytoscape3.8.2 software were used to construct drug-compound-target network and target protein interaction network. GO enrichment and KEGG pathway annotation analysis of intersection targets were performed by DAVID database and OmicShare Tools. Results: 89 Components with different contents were found in cooked Gastrodia elata and fresh Gastrodia elata. 11 Compounds were screened for the treatment of convulsion by 410 potential targets, and 5 compounds were screened for the treatment of diabetes and its complications by 698 potential targets. GO and KEGG enrichment analysis showed that Gastrodia elata treated convulsion through IL-17 signaling pathway, cAMP signaling pathway, neuroactive substance receptor signaling pathway, Alzheimer's disease signaling pathway and dopaminergic synaptic signaling pathway, while treated diabetes through AGE-RAGE signaling pathway, HIF-1, VEGF and TNF signaling pathway. The results of molecular docking showed that the selected components were all bound to the cavity of the target protein, and the binding free energy was less than 0 kcal/mol, and the molecular docking conformation was stable. Conclusion: Cooked Gastrodia elata has better neuroprotective effect, and fresh Gastrodia elata has better effect in treating diabetes mellitus and cardiovascular diseases.
-
Keywords:
- Gastrodia elata /
- cooking /
- metabonomics /
- network pharmacology /
- molecular docking
-
天麻(Gastrodia elata)为兰科(Orchidaceae)植物的块茎,又被称为赤箭、鬼督邮、神草、定风草、水洋芋等,广泛分布于云南、四川及贵州等地。贵州德江天麻,是我国传统道地药材,品质高,其天麻素含量达1.3%以上,远高于国家药典规定的0.22%[1]。2007年,德江天麻获得国家地理标志产品;2014年贵州德江被评为“中国天麻之乡”。天麻最初被记载于《神农本草经》,具有息风止痉,平抑肝阳,祛风通络的功效[2]。现代研究表明:天麻具有保护神经[3]、抗炎[4]、抗惊厥[5]以及抗氧化[6]等功效。自2018年天麻被确认为药食两用的植物,天麻的应用范围更加广泛,除了传统中药材,天麻还可作为营养健康食品用于消费者。
炮制方法对食品和药材的化学成分和生物学活性具有一定的影响。高可新等[7]研究了不同炮制方法对黄芩活性成份含量及抗氧化作用的影响,结果表明经过黄酒炮制的黄芩素和汉黄芩素含量高于生黄芩,并且酒黄芩对DPPH自由基、OH自由基以及超氧阴离子自由基的清除率高于生黄芩,表明黄酒炮制显著增强了黄芩的抗氧化能力。赵翡翠[8]研究了不同炮制方法对新疆准噶尔乌头化学组成和生物学活性的影响,研究表明加入水煮法炮制的准噶尔乌头中的乌头碱要低于生准噶尔乌头以及其他方法炮制品,表明炮制降低了准噶尔乌头的毒性,同时各种方法的炮制品均可以提高准噶尔乌头的镇痛和抗炎作用。
目前关于天麻炮制前后化学成分及生物学活性的研究较少,对新鲜天麻和熟制天麻活性成分差异以及生物功能性差异的研究还不深入,已有研究表明:蒸制天麻中的天麻素含量高于新鲜天麻,而多糖含量则相反[9],这说明炮制会对天麻化学成分产生一定影响,同时也可能对其生物活性产生一定的影响。本文以贵州德江天麻为研究对象,通过LC-QTOF-MS代谢组学技术系统且全面地分析了天麻熟制过程中的成分变化,同时通过网络药理学技术对贵州德江天麻在炮制过程中的生物活性功能变化也进行了相应的预测,为天麻产品功能性开发以及工业化生产提供科学理论依据。
1. 材料与方法
1.1 材料与仪器
天麻 由贵州德江县康奇药植开发有限责任公司提供,经德江县中药材专班邵先强高级工程师鉴定为红天麻(Gastrodia elata Bl. f. elata);甲醇 分析纯,购于国药集团化学试剂有限公司。
LC-QTOF-MS为高效液相色谱(安捷伦1260)串联飞行时间质谱(AB SCIEX TOF 5600+) 美国安捷伦科技有限公司;FD-2A真空冷冻干燥机 北京博医康实验仪器有限公司。
1.2 实验方法
1.2.1 LC-QTOF-MS分析天麻提取液
新鲜天麻置于蒸锅内蒸制30 min后得熟制天麻。将新鲜天麻(生天麻)、熟制天麻(熟天麻)冻干后,研磨成粉末。称取相同质量的天麻粉末,以甲醇为溶剂,料液比1:15 g/mL,置于摇床中以200 r/min转速振荡提取30 min,6000×g离心15 min后得天麻提取液,过0.22 μm滤膜后上样分析。
LC-QTOF-MS分析参考刘启月等[10]的方法。LC-QTOF-MS的色谱条件为:XSelect HSS T3(4.6 mm×150.0 mm,3.5 μm) 色谱柱;流动相A为0.1%甲酸/水,流动相B为乙腈;进样量为10 μL,流动相梯度洗脱程序为: 0~3.00 min,10% B;3.00~21.00 min,10%~95% B;21.00~28. 00 min,95% B;28.00~28.10 min,10% B;28.10~34. 00 min,10% B。质谱条件为:QTOF-MS 全扫描模式,质量扫描范围为m/z 50~1000;正电离模式的源电压为5500 V,负电离模式的源电压为4500 V;帘气流动压力为25 psi、雾化器流动压力为50 psi、加热气体流动压力为50 psi;碰撞能量(CE) 为30 V和−30 V。利用MS-DI-AL软件对LC-QTOF-MS数据进行分析,将实验数据与数据库进行相似性匹配来进行化合物鉴定,同时根据相同组分在不同组别之间的峰面积进行相对定量及比较。采用R语言中的(数据包)绘制主成分分析(PCA)图以及热图(heatmap)。基于生熟天麻差异代谢物,进一步通过PubChem网站(https://pubchem.ncbi.nlm.nih.gov/),Lipinski原则(类五药原则)[11]以及相关参考文献对差异代谢物进一步分析注释,筛选出具有生物活性功能的差异代谢物。
1.2.2 成分靶点预测及疾病靶点筛选
从PubChem网站获得各个成分的Smiles化学结构式,首先将Smiles化学结构式上传到Swiss Target Prediction(http://www.swissadme.ch/)网站,选择“人类”为研究物种,获得该成分可能的靶点蛋白信息。同时将Smiles化学结构式上传到SEA(Similarity ensemble approach,https://sea.bkslab.org/)网站,获得预测靶点信息,再以“人类”为研究物种,筛选出可能的靶点。最后将两个数据库得到的靶点蛋白进行去重,取并集,得到该成分的可能的作用靶点。
分别以“Convulsions”和“Diabetes”在GeneCards数据库(https://www.genecards.org/)和OMIM数据库(https://omim.org/)中进行搜索,可得到与惊厥和糖尿病相关的靶点,对得到的靶点进行去除假阳性,去除重复靶点,取并集,得到与惊厥和糖尿病相关的靶点的总和。
以成分的靶点蛋白与疾病的靶点蛋白为子集,采用Venny2.1软件绘制韦恩图,并获取交集部分成分作为活性成分治疗疾病的靶点。将活性成分与靶点进行匹配,导入Cytoscape 3.8.2中绘制成分-疾病靶点作用网络图。
1.2.3 PPI网络构建
将靶点数据导入STRING11.5数据库(https://www.string-db.org/)中,选择“人类”为研究物种,绘制蛋白质互作网络(PPI)。将结果导入Cytoscape 3.8.2中计算出该互作网络的拓扑学数据。以大于Degree值的平均值的2倍作为筛选关键靶点的标准,筛选出治疗疾病的关键靶点及其对应的活性成分。
1.2.4 GO富集分析及KEGG富集分析
参考陈钰婷等[12]的方法,将活性成分治疗疾病的靶点蛋白借助David数据库(https://david.ncifcrf.gov/)中的Gene ID Conversion工具转化为Gene ID;再利用OmicShare Tools中的GO富集分析工具及KEGG富集分析工具对靶点进行信号通路分析。
1.2.5 “成分-靶点”分子对接验证
在PDB数据库(https://www.rcsb.org/)中下载靶点蛋白的3D结构文件,在Pymol 2.5软件中进行去除水分子及配体分子后保存为受体文件;在PubChem数据库中下载成分的3D结构文件,通过OpenBabel软件进行格式转化,保存为配体文件。最后将受体蛋白和配体通过AutoDock4进行分子对接。以最低结合能为标准筛选可能的分子对接结构,最后通过Pymol 2.5软件对对接结果进行可视化处理。
1.3 数据处理
使用MS-DI-AL软件及数据库对LC-QTOF-MS数据进行分析,并使用T检验法检验各成分的相对含量差异(P<0.05)。使用Swiss target prediction数据库及SEA数据库对成分靶点进行预测,GeneCards数据库和OMIM数据库获取疾病靶点;通过STRING 11.5数据库及Cytoscape3.8.2软件绘制药物-化合物-靶点网络及靶点蛋白互作网络,筛选关键成分及靶点;通过DAVID数据库和OmicShare Tools对交集靶点进行GO富集和KEGG通路注释分析。
2. 结果与分析
2.1 代谢组学分析
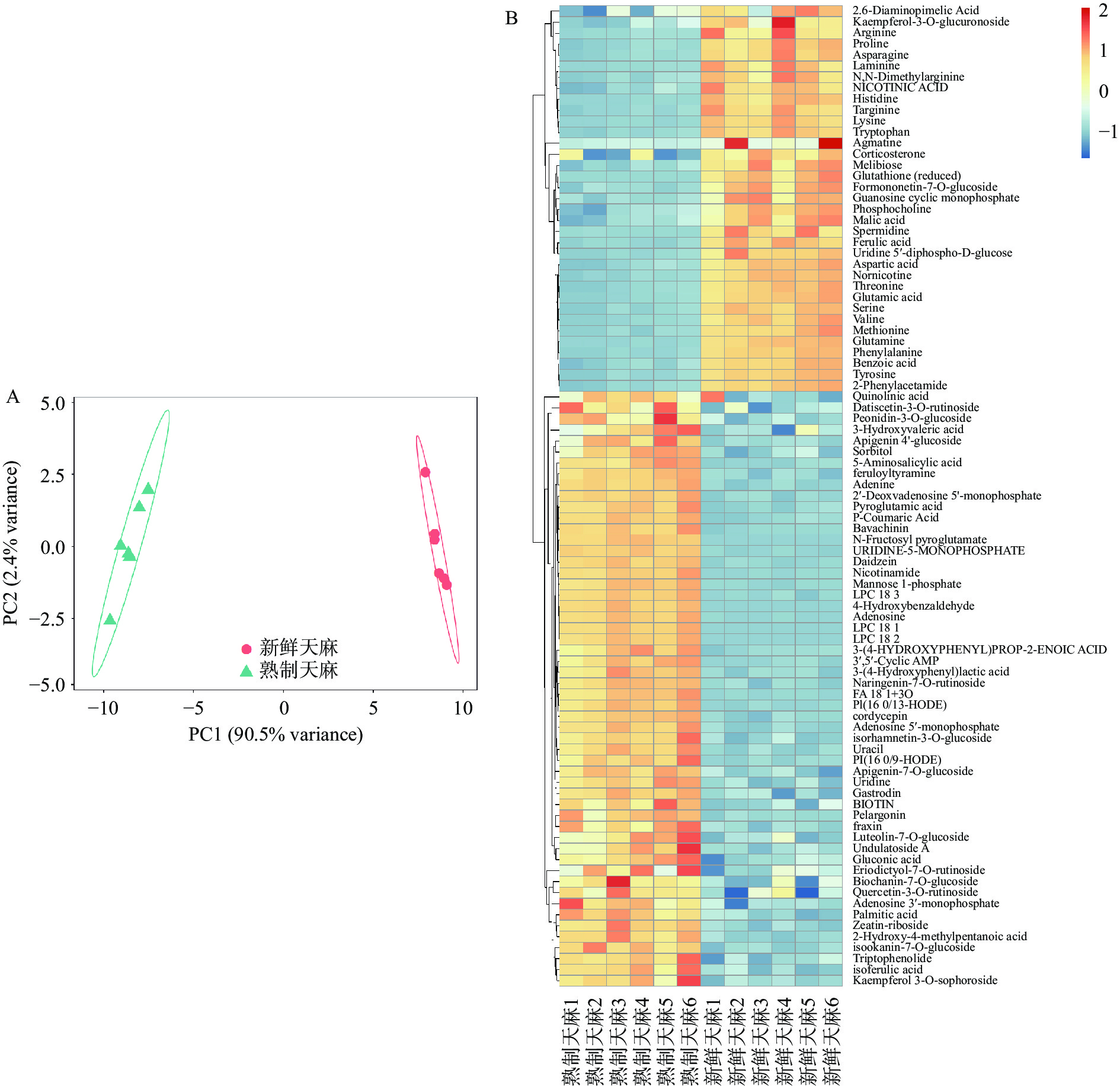
为了找出熟制天麻和新鲜天麻的化学组成及其含量上的差异,采用层次聚类分析(热图)及主成分分析(PCA)对LC-QTOF-MS数据进行判别分析。如图1(B)所示,经过对各组分在不同组别之间的峰面积大小进行T检验分析,发现熟制天麻与新鲜天麻存在89种相对含量存在明显差异的成分,其中焦谷氨酸、烟酰胺、p-香豆酸、异阿魏酸以及天麻素等54种成分在熟制天麻中的含量显著高于新鲜天麻(P<0.05),而苹果酸、烟酸、阿魏酸、谷胱甘肽以及多种氨基酸的含量在熟制天麻中的含量却显著低于新鲜天麻(P<0.05)。在图1(A)的PCA图中可以看出,熟制天麻与新鲜天麻之间表现为明显的离散型,表明熟制天麻与新鲜天麻在化学组成及其成分含量方面确实存在显著差异。这可能是因为在蒸煮过程中,存在部分水溶性物质的溶解损失[13],同时部分热不稳定成分在加热条件下分解从而导致该成分的降解成分在熟制天麻中的含量增加[14]。在新鲜天麻中,主要化学成分为氨基酸类,而熟制天麻中的主要化学成分为类黄酮类和有机酸。值得注意的是,在新鲜天麻中,存在两种不利于人体健康的物质—N,N-二甲基精氨酸和去甲烟碱。N,N-二甲基精氨酸的摄入或使人患心血管疾病的风险增加[15-16],去甲烟碱是尼古丁的代谢产物,具有一定的致癌性[17]。在蒸煮过后,这两种物质的含量显著降低(P<0.05),但是在熟制天麻中,喹啉酸含量有所增加。喹啉酸是作为N-甲基-D-天冬氨酸受体的激动剂。在大脑内部,巨噬细胞的浸润和小胶质细胞的激活会产生和释放喹啉酸,因此被认为是一种脑内源性兴奋毒素[18],摄入过多的喹啉酸会增加脑部疾病风险。
通过在PubChem数据库中查找以及参考大量文献,对89种存在相对含量差异的成分进行了筛选,找出了16种以及已报道具有活性功能的成分,其中熟制天麻占了11种,新鲜天麻占了5种。将各成分进行功能注释,并将结果汇总于表1,发现:熟制天麻成分主要具有抗惊厥以及保护神经等功能,而新鲜天麻主要表现为抗氧化以及治疗心血管疾病等功能。研究表明,导致心血管疾病的一个重要病因是糖尿病,同时心血管疾病也是糖尿病患者死亡的主要原因[19]。因此推测新鲜天麻中的成分可以通过治疗糖尿病来缓解心血管疾病。
表 1 熟制天麻及新鲜天麻的成分及功能Table 1. Ingredients and functions of cooked and fresh Gastrodia elata化合物 PubChem ID 成分 分子式 功能 熟制天麻 4-Hydroxybenzaldehyde 126 4-羟基苯甲醛 C7H6O2 降血糖[20],抗氧化[21],
抗惊厥与癫痫[22]Daidzein 5281708 大豆黄酮 C15H10O4 抗肿瘤[23],抗健忘[24],治疗2型糖尿病[25],降血压[26] Nicotinamide 936 烟酰胺 C6H6N2O 保护神经元[27],抗惊厥[28]治疗1型糖尿病[29],缓解胰岛素抵抗[30] p-Coumaric Acid 637542 p-香豆酸 C9H8O3 神经保护作用[31],抗癌[32-33],修复肝损伤[34],调节免疫及抗炎活性[35] Bavachinin 10337211 补骨脂二氢黄酮甲醚 C21H22O4 治疗哮喘[36],抗肿瘤[37-38] Cordycepin 6303 虫草素 C10H13N5O3 神经保护作用[39-40],治疗哮喘[41] Gastrodin 115067 天麻素 C13H18O7 抗健忘[42],促进记忆[43],神经保护作用[44-45],保肝护肝[46] Isoferulic acid 736186 异阿魏酸 C10H10O4 抗健忘[47] Biotin 171548 生物素 C10H16N2O3S 治疗脑损伤及记忆障碍[48],治疗糖尿病[49] Peonidin-3-O-glucoside 14311151 芍药苷-3-O-葡萄糖苷 C22H23O11+ 降血糖血脂[50],抗氧化[51] Luteolin-7-O-glucoside 5280637 木犀草素-7-O-葡萄糖苷 C21H20O11 调节免疫[52],抗炎[53] 新鲜天麻 Agmatine 199 精胺 C5H14N4 治疗脑梗塞及认知障碍[54],缓解疼痛[55] Spermidine 1102 亚精胺 C7H19N3 抗癌[56],治疗心血管疾病[57] Ferulic acid 445858 阿魏酸 C10H10O4 抗氧化[58],抗炎[59] Ononin 442813 芒柄花素-7-O-葡萄糖苷 C22H22O9 抗氧化[60],抗炎[61] Nicotinic acid 938 烟酸 C6H5NO2 治疗心血管疾病[62] 2.2 成分靶点预测及疾病靶点筛选
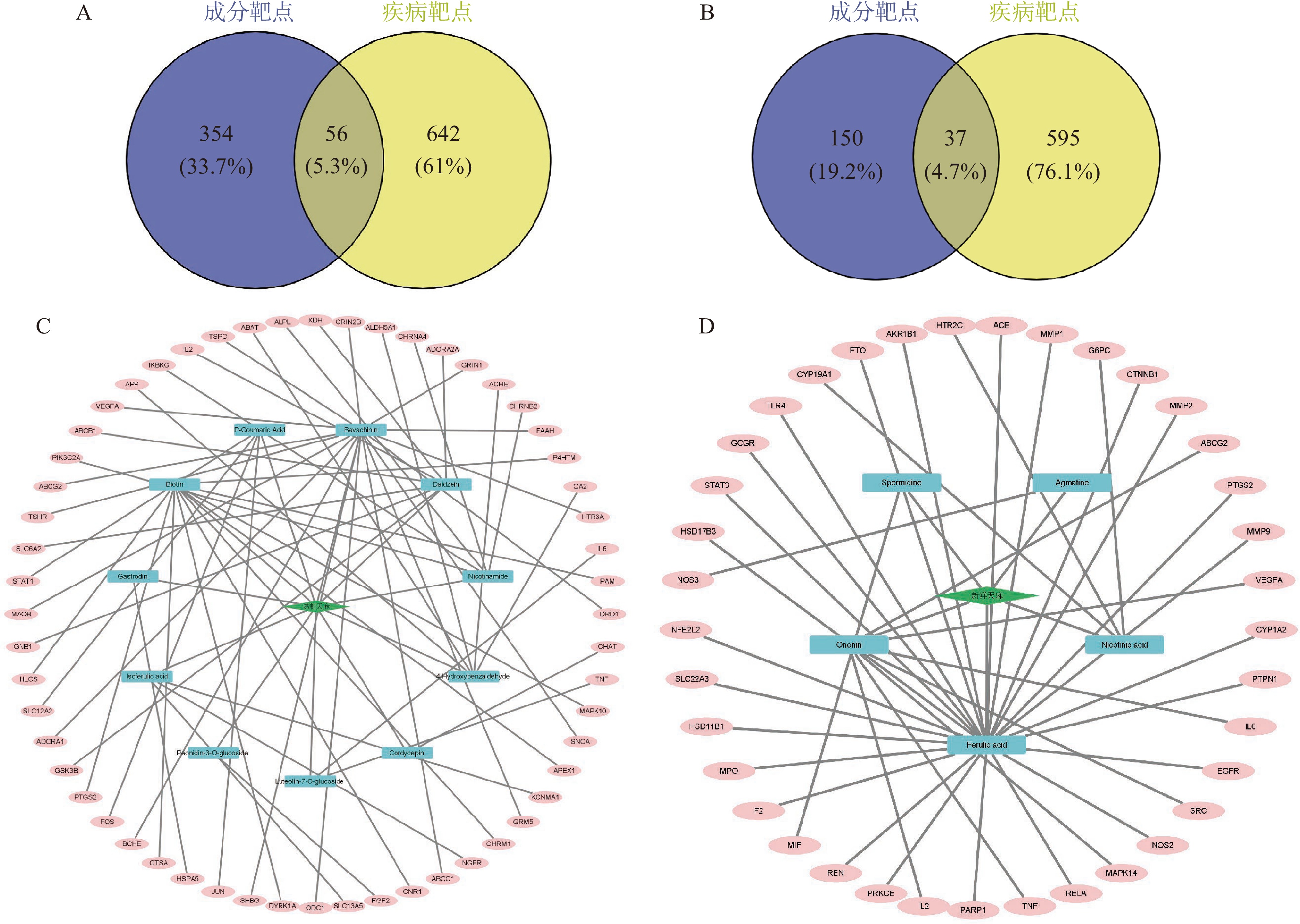
将11个熟制天麻中的活性成分的Smiles化学结构上传到Swiss Target Prediction网站和SEA网站得到预测靶点,对两个网站得到的靶点进行去重整合,得到作用靶点410个。从GeneCards、OMIM数据库中搜索与惊厥相关的靶点,经过去除假阳性及去重后,得到698个靶点,熟制天麻中的活性成分与惊厥靶点共有56个相交的靶点,如图2(A)所示。对新鲜天麻中的活性成分和糖尿病进行相同的处理,得到37个相交的靶点,如图2(B)所示。将靶点与成分信息导入Cytoscape3.8.2软件后,得到天麻-成分-靶点网络图,如图2(C)和图2(D)所示。由网络图可知,熟制天麻中,补骨脂二氢黄酮甲醚具有16个靶点,生物素有9个靶点,天麻素有7个靶点。在新鲜天麻中,阿魏酸有26个靶点,芒柄花素-7-O-葡萄糖苷有6个靶点,烟酸有3个靶点。
2.3 PPI网络构建
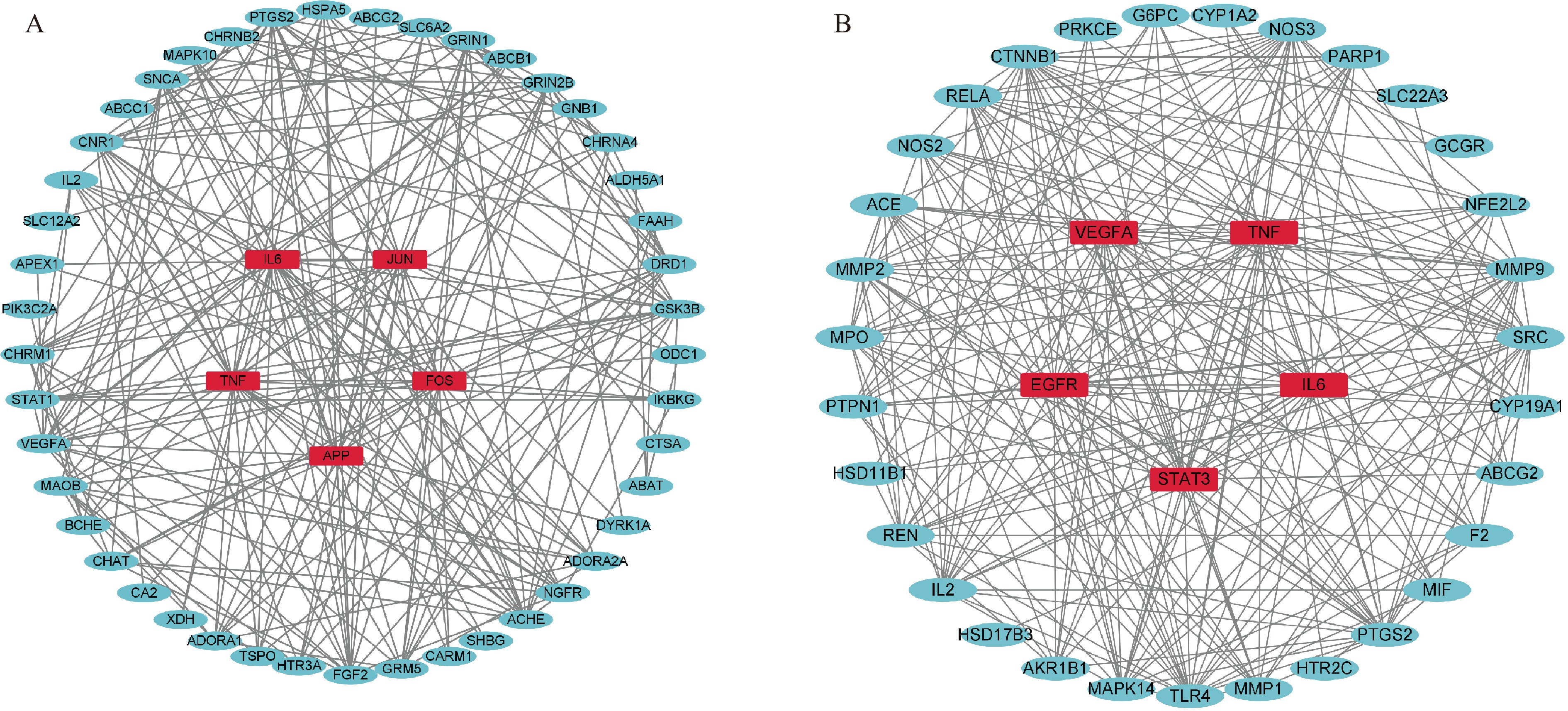
将熟制天麻成分与惊厥的共同靶点以及新鲜天麻与糖尿病的共同靶点上传至STRING11.5数据库中,得到靶点相互作用的PPI网络。将结果导入Cytoscape3.8.2软件,计算各个网络的拓扑学参数。以Degree值的平均值的2倍为筛选标准,筛选出关键靶点,重新绘制靶点相互作用网络图,见图3。图3(A)为熟制天麻成分干预下的惊厥靶点相互作用网络图,其中IL6、JUN、FOS、APP以及TNF为熟制天麻成分治疗惊厥的关键靶点。图3(B)为新鲜天麻成分干预下的糖尿病靶点相互作用网络图,其中TNF、IL6、STAT3、EGFR以及VEGFA为新鲜天麻成分治疗糖尿病的关键靶点。
2.4 GO富集分析及KEGG富集分析
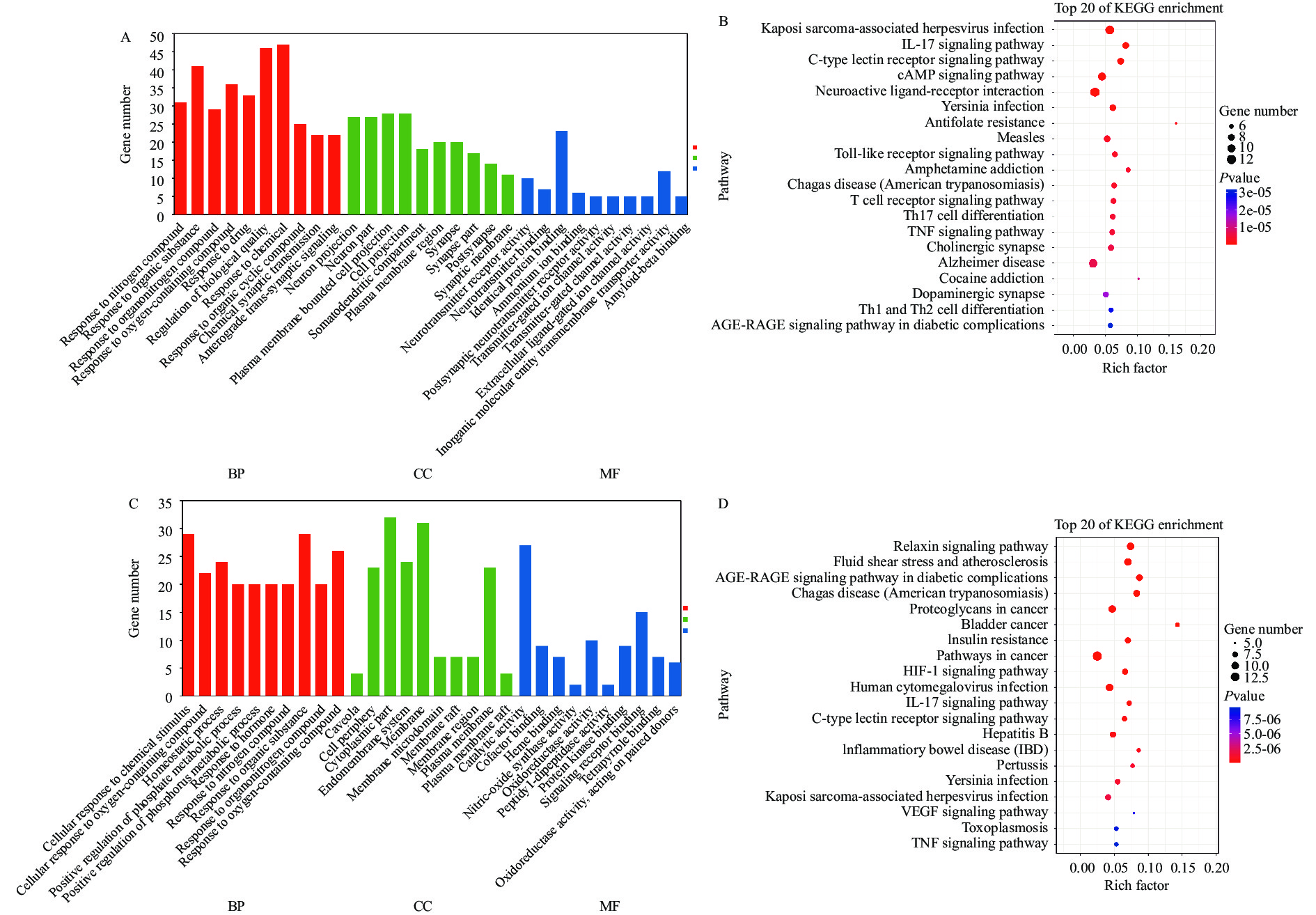
通过OmicShare Tools中的GO富集分析工具及KEGG富集分析工具对熟制天麻和新鲜天麻干预惊厥及糖尿病靶点基因进行富集分析,得到富集结果见图4。图4(A)及图4(B)为熟制天麻干预惊厥靶点基因进行富集分析结果,图4(C)及图4(D)为新鲜天麻干预糖尿病靶点基因进行富集分析结果,图4显示的富集结果均具有一定的可靠性(P<0.01)。在GO富集分析图中,竖轴为X轴,代表基因数量,横轴为Y轴,其中BP、CC及MF分别代表富集基因本体的三个方面—生物过程(Biological process)、细胞定位(Cellular components)以及分子功能(Molecular function),在制图过程中进行了XY轴颠倒。在KEGG富集分析图中,横轴表示-lg Padjust,纵轴表示富集的通路,气泡颜色的变化本质为P值的变化,反映富集结果的可靠性;气泡大小的变化代表了富集到该通路中基因数量的变化。如图4(A)可知,熟制天麻成分干预惊厥的靶点参与了对药物、含氧化合物、含氮化合物、有机物的反应过程以及生物质量调控,化学突触传递、正向突触信号传递等过程。这些靶点主要集中在神经细胞的细胞膜、细胞质以及细胞突触等部位,具有传递和转运神经递质,调控神经递质及离子运输通道活性等功能。由图4(B)可知,熟制天麻成分干预惊厥的靶点主要集中在IL-17信号通路、C型凝集素受体信号通路、cAMP信号通路、神经活性物质受体信号通路、TNF信号通路、阿尔茨海默病信号通路以及多巴胺能神经突触信号通路。同样,由图4(C)和图4(D)可知,新鲜天麻成分干预糖尿病的靶点参与了对含氧化合物、含氮化合物、有机物、激素的反应过程以及正调控磷代谢过程,这些靶点主要集中在内质网膜及细胞膜上,具有结合信号受体、催化反应、氧化还原酶活性结合蛋白激酶等活性,这些靶点主要富集在松弛素信号通路、动脉粥样硬化信号通路、糖尿病并发症中的AGE-RAGE信号通路、癌症以及癌症中蛋白多糖信号通路、胰岛素耐受性、炎症性肠病、HIF-1、VEGF以及TNF信号通路。
2.5 分子对接验证
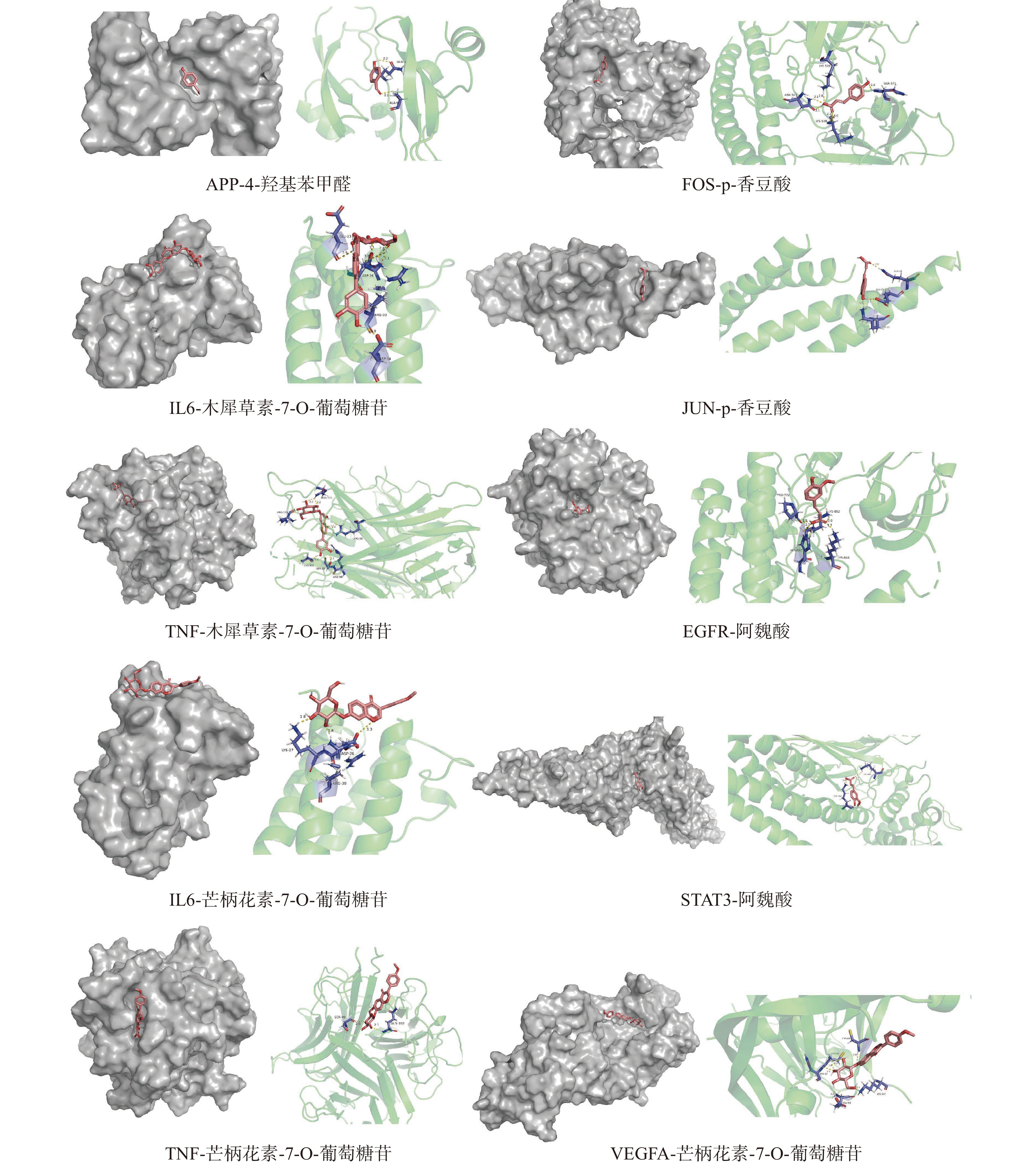
虽然在成分靶点预测中,熟制天麻中,补骨脂二氢黄酮甲醚、生物素、天麻素具有较多的靶点,但是在靶点的PPI网络图中,5个关键靶点所对应的成分为4-羟基苯甲醛、p-香豆酸以及木犀草素-7-O-葡萄糖苷,由于靶点是执行功能的主要物质,因此选择APP、FOS、IL6、JUN以及TNF所对应的成分进行分子对接验证。同时在新鲜天麻成分靶点预测以及靶点PPI网络中,预测的成分以及靶点具有一致性,因此选择EGFR、IL6、STAT3、TNF以及VEGFA所对应的阿魏酸及芒柄花素-7-O-葡萄糖苷进行分子对接验证。分子对接结果如图5所示,所有分子对接的能量均小于0 kcal/mol,同时每个成分都结合在靶点蛋白的空腔内,因此可以推测每个组分在细胞内都可以与靶点自发结合形成靶点-配体二元复合物。
3. 结论与讨论
本文通过LC-QTOF-MS技术对熟制天麻和新鲜天麻的成分进行了代谢组学分析,找出了熟制天麻与新鲜天麻中存在相对含量差异的89种代谢物,正是这种含量上的差异可能对天麻功能产生一定影响[63]。由实验结果可知,新鲜天麻含有N,N-二甲基精氨酸和去甲烟碱,熟制天麻含有喹啉酸,大量存在的N,N-二甲基精氨酸会导致高血压同时去甲烟碱和喹啉酸具有一定的神经毒性,因此在天麻食用以及加工过程中应该注意尽可能降低这些成分的含量或者与其它食物或药材进行适当的配伍。
通过数据库查询对差异成分进行了功能上的预测及比较,发现熟制天麻对神经具有更好的保护作用,而新鲜天麻可能对糖尿病以及由糖尿病引起的心血管疾病具有更好的缓解效果。在熟制天麻成分中,补骨脂二氢黄酮甲醚、生物素、天麻素具有较多的靶点,但是在关键靶点筛选中,得到的关键靶点所对应的成分为4-羟基苯甲醛、p-香豆酸以及木犀草素-7-O-葡萄糖苷。这表明补骨脂二氢黄酮甲醚、生物素、天麻素以及4-羟基苯甲醛、p-香豆酸以及木犀草素-7-O-葡萄糖苷在保护神经方面都具有一定的作用,但是4-羟基苯甲醛、p-香豆酸以及木犀草素-7-O-葡萄糖苷起到了主要的作用,而补骨脂二氢黄酮甲醚、生物素、天麻素通过促进靶点与关键靶点的相互作用来保护神经细胞。APP作为细胞表面受体,在神经元表面执行与神经突生长、神经元粘附和轴突形成相关的生理功能[64]。补骨脂二氢黄酮甲醚的靶点BCHE可以与APP相互作用来缓解阿尔茨海默症[65]。JUN是一种转录因子,能够识别并结合增强子七聚体基序5'-TGA[CG]TCA-3'[66]。FOS是一种核磷蛋白,能够与JUN/AP-1转录因子形成紧密但非共价连接的复合物[67]。因此可以推测熟制天麻中的成分通过影响基因的表达来达到保护神经细胞的功能。
VEGFA是血管中的生长因子,具有促进血管细胞和内皮细胞生长活性,诱导内皮细胞增殖,促进细胞迁移,抑制细胞凋亡,诱导血管通透[68]。EGFR是EGF家族中的酪氨酸激酶,是ATP代谢通路中的靶点,同时也可以激活NFκB信号通路[69]。和TNF、IL6、EGFR、STAT3都是与炎症相关的靶点蛋白[70]。炎症已经被确认可以减少细胞胰岛素分泌和增加胰岛素抵抗从而导致糖尿病,因此缓解炎症反应已经被认为是一种治疗糖尿病及其引发的心血管疾病的一种方法[70-72]。因此推测新鲜天麻中的成分通过影响能量代谢途径以及减轻炎症反应来缓解糖尿病及相关的心血管疾病。
综上所述,本研究通过代谢组学、网络药理学及分子对接技术对天麻熟制过程中成分的变化及药性的变化进行了系统的研究及科学的预测,为天麻的食用及加工提供了科学参考,同时为后续天麻在神经保护机制、治疗糖尿病及心血管疾病方面研究提供了新的思路。
-
表 1 熟制天麻及新鲜天麻的成分及功能
Table 1 Ingredients and functions of cooked and fresh Gastrodia elata
化合物 PubChem ID 成分 分子式 功能 熟制天麻 4-Hydroxybenzaldehyde 126 4-羟基苯甲醛 C7H6O2 降血糖[20],抗氧化[21],
抗惊厥与癫痫[22]Daidzein 5281708 大豆黄酮 C15H10O4 抗肿瘤[23],抗健忘[24],治疗2型糖尿病[25],降血压[26] Nicotinamide 936 烟酰胺 C6H6N2O 保护神经元[27],抗惊厥[28]治疗1型糖尿病[29],缓解胰岛素抵抗[30] p-Coumaric Acid 637542 p-香豆酸 C9H8O3 神经保护作用[31],抗癌[32-33],修复肝损伤[34],调节免疫及抗炎活性[35] Bavachinin 10337211 补骨脂二氢黄酮甲醚 C21H22O4 治疗哮喘[36],抗肿瘤[37-38] Cordycepin 6303 虫草素 C10H13N5O3 神经保护作用[39-40],治疗哮喘[41] Gastrodin 115067 天麻素 C13H18O7 抗健忘[42],促进记忆[43],神经保护作用[44-45],保肝护肝[46] Isoferulic acid 736186 异阿魏酸 C10H10O4 抗健忘[47] Biotin 171548 生物素 C10H16N2O3S 治疗脑损伤及记忆障碍[48],治疗糖尿病[49] Peonidin-3-O-glucoside 14311151 芍药苷-3-O-葡萄糖苷 C22H23O11+ 降血糖血脂[50],抗氧化[51] Luteolin-7-O-glucoside 5280637 木犀草素-7-O-葡萄糖苷 C21H20O11 调节免疫[52],抗炎[53] 新鲜天麻 Agmatine 199 精胺 C5H14N4 治疗脑梗塞及认知障碍[54],缓解疼痛[55] Spermidine 1102 亚精胺 C7H19N3 抗癌[56],治疗心血管疾病[57] Ferulic acid 445858 阿魏酸 C10H10O4 抗氧化[58],抗炎[59] Ononin 442813 芒柄花素-7-O-葡萄糖苷 C22H22O9 抗氧化[60],抗炎[61] Nicotinic acid 938 烟酸 C6H5NO2 治疗心血管疾病[62] -
[1] 黎荣. 国家地理标识 德江天麻[J]. 大众科学,2017,323(3):19. [LI R. National geographical indication-Dejiang Tianma[J]. China Public Science,2017,323(3):19. [2] 唐春梓, 廖朝林, 林先明, 等. 天麻的研究现状与展望[J]. 中国现代中药,2008(6):10−12,14. [TANG C Z, LIAO Z L, LIN X M. Research status and prospect of Gastrodia elata[J]. Modern Chinese Medicine,2008(6):10−12,14. doi: 10.3969/j.issn.1673-4890.2008.06.003 [3] ZHOU B, TAN J, ZHANG C, et al. Neuroprotective effect of polysaccharides from Gastrodia elata Blume against corticosterone-induced apoptosis in PC12 cells via inhibition of the endoplasmic reticulum stress-mediated pathway[J]. Molecular Medicine Reports,2017,17(1):1182−1190.
[4] YU L, LI M, XU J Z, et al. Gastrodia elata attenuates inflammatory response by inhibiting the NF-κB pathway in rheumatoid arthritis fibroblast-like synoviocytes[J]. Biomedicine & Pharmacotherapy,2017,85:177−181.
[5] LIU Y, HUANG G. The chemical composition, pharmacological effects, clinical applications and market analysis of Gastrodia elata[J]. Pharmaceutical Chemistry Journal,2017,51(3):1−5.
[6] ANHUAN S, JIAN M X, FANG Y H, et al. The phenolic components of Gastrodia elata improve prognosis in rats after cerebral ischemia/reperfusion by enhancing the endogenous antioxidant mechanisms[J]. Oxidative Medicine and Cellular Longevity,2018,2018:1−16.
[7] 高可新, 李利霞, 王小康. 不同炮制方法对黄芩活性成份含量及抗氧化作用的影响[J]. 中国合理用药探索,2021,18(9):109−113. [GAO K X, LI L X, WANG X K. Effects of different processing methods on the content of active components and antioxidant effect of Scutellaria baicalensis[J]. Chinese Journal of Rational Drug Use,2021,18(9):109−113. [8] 赵翡翠. 新疆准噶尔乌头亲缘关系、炮制毒效活性及化学成分研究[D]. 乌鲁木齐: 新疆医科大学, 2015 ZHAO F C. Studies on the phylogenetic relationship, toxic activity during processing and chemical compositions of Xingjiang Aconitum soongaricum[D]. Urumqi: Xinjiang Medical University, 2015.
[9] 李清, 谢宇璐, 许攀, 等. 基于溶剂法研究建昌帮姜天麻不同部位主成分差异[J]. 南昌工程学院学报,2020,39(4):90−95. [LI Q, XIE Y L, XU P, et al. Study on principal component difference of different parts of Jianchang Bang Gastrodia elata processed by ginger based on solvent method[J]. Journal of Nanchang Institute of Technology,2020,39(4):90−95. doi: 10.3969/j.issn.1006-4869.2020.04.017 [10] 刘启月, 李勇, 陈小龙, 等. 基于代谢组学分析桃胶中酚类化合物含量及抗氧化活性[J]. 江苏农业学报,2021,37(3):746−753. [LIU Q Y, LI Y, CHENG X L, et al. Analysis on phenolics contents and antioxidant activity in peach gum based on metabolomics[J]. Jiangsu J of Agr Sci,2021,37(3):746−753. [11] 杨二冰, 李正名. 药物分子设计中的Lipinski规则[J]. 化学通报,2006(1):16−19. [YANG E B, LI Z M. The Lipinski' s rules in drug discovery[J]. Chemistry,2006(1):16−19. doi: 10.14159/j.cnki.0441-3776.2006.01.003 [12] 陈钰婷, 王俊玲, 吴依娜. 基于网络药理学和分子对接探讨地稔治疗宫颈癌的分子机制[J]. 世界科学技术-中医药现代化,2021,23(9):10. [CHEN Y T, WANG J L, WU Y N. Study on the molecular mechanism of Melastoma dodecandrum Lour in treating cervical cancer based on network pharmacology and molecular docking[J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology,2021,23(9):10. [13] 杨飞, 王信, 马传江, 等. 天麻加工炮制、成分分析与体内代谢研究进展[J]. 中国中药杂志,2018,43(11):2207−2215. [YANG F, WANG X, MA C J, et al. Research progress of Gastrodiae rhizoma machining processing, composition analysis and in vivo metabolism[J]. China Journal of Chinese Materia Medica,2018,43(11):2207−2215. doi: 10.19540/j.cnki.cjcmm.20180322.008 [14] 田紫平, 肖慧, 冯舒涵, 等. 天麻有效成分巴利森苷的降解规律分析[J]. 中国实验方剂学杂志,2017,23(23):18−21. [TIAN Z P, XIAO H, FENG S H, et al. Analysis of degradation mechanism of parishin in Gastrodiae rhizoma[J]. Chinese Journal of Experimental Traditional Medical Formulae,2017,23(23):18−21. doi: 10.13422/j.cnki.syfjx.2017230018 [15] DOWSETT L, HIGGINS E, ALANAZI S, et al. ADMA: A key player in the relationship between vascular dysfunction and inflammation in atherosclerosis[J]. Journal of Clinical Medicine,2020,9(9):3026. doi: 10.3390/jcm9093026
[16] 李姣锋, 罗健东. 非对称二甲基精氨酸诱导大鼠心肌细胞肥大的作用[J]. 广州医学院学报,2008,159(1):5−9. [LI J F, LUO J D. Induced cardiomyocyte hypertrophy in rats by asymmetric dimethyl-arginine[J]. Academic Journal of Guangzhou Medical College,2008,159(1):5−9. [17] MIRVISH S S, SAMS J, HECHT S S. Kinetics of nornicotine and anabasine nitrosation in relation to, n’-nitrosonornicotine occurrence in tobacco and to tobacco-induced cancer 2[J]. JNCI: Journal of the National Cancer Institute,1977,59(4):1211−1213. doi: 10.1093/jnci/59.4.1211
[18] GUILLEMIN G J. Quinolinic acid, the inescapable neurotoxin[J]. FEBS J,2012(8):65−1356.
[19] STRAIN W D, PALDÁNIUS P M. Diabetes, cardiovascular disease and the microcirculation[J]. Cardiovasc Diabetol,2018(1):57.
[20] MANAHARAN T, MING C H, PALANISAMY U D. Syzygium aqueum leaf extract and its bioactive compounds enhances pre-adipocyte differentiation and 2-NBDG uptake in 3T3-L1 cells[J]. Food Chem,2012(2):354−363.
[21] KHALLOUKI F, HAUBNER R, ULRICH C M, et al. Ethnobotanical survey, chemical composition, and antioxidant capacity of methanolic extract of the root bark of Annona cuneata Oliv.[J]. Journal of Medicinal Food,2011(11):1397−1402.
[22] HA J H, LEE D U, LEE J T, et al. 4-Hydroxybenzaldehyde from Gastrodia elata B1. is active in the antioxidation and GABAergic neuromodulation of the rat brain[J]. J Ethnopharmacol,2000(1):329−333.
[23] LIAN Z, NIWA K, TAGAMI K, et al. Preventive effects of isoflavones, genistein and daidzein, on estradiol-17beta-related endometrial carcinogenesis in mice[J]. Jpn J Cancer Res,2001(7):726−734.
[24] KIM D H, JUNG H A, PARK S J, et al. The effects of daidzin and its aglycon, daidzein, on the scopolamine induced memory impairment in male mice[J]. Archives of Pharmacal Research,2010,33(10):1685. doi: 10.1007/s12272-010-1019-2
[25] SUN A P, CHOI M S, CHO S Y, et al. Genistein and daidzein modulate hepatic glucose and lipid regulating enzyme activities in C57BL/KsJ-db/db mice[J]. Life Sciences,2006,79(12):1207−1213. doi: 10.1016/j.lfs.2006.03.022
[26] CAO Y X, YANG X J, JING L, et al. Effects of daidzein sulfates on blood pressure and artery of rats[J]. Basic & Clinical Pharmacology & Toxicology,2010,99(6):425−430.
[27] NAJEEB U, YOUNG L H, IMRAN N M, et al. Nicotinamide inhibits alkylating agent-induced apoptotic neurodegeneration in the developing rat brain[J]. PloS One,2011,6(12):e27093. doi: 10.1371/journal.pone.0027093
[28] KRYZHANOVSKIĬ G N, SHANDRA A A. Effect of diazepam and nicotinamide on convulsive activity of various types[J]. Farmakologiia I Toksikologiia,1985,48(4):21.
[29] PENBERTHY W T. Pharmacological targeting of IDO-mediated tolerance for treating autoimmune disease[J]. Current Drug Metabolism,2007,8(3):245−266. doi: 10.2174/138920007780362545
[30] NEJABATI H R, SAMADI N, SHAHNAZI V, et al. Nicotinamide and its metabolite N1-methylnicotinamide alleviate endocrine and metabolic abnormalities in adipose and ovarian tissues in rat model of polycystic ovary syndrome[J]. Chemico-Biological Interactions,2020,324:109093.
[31] GUVEN M, ARAS A B, AKMAN T, et al. Neuroprotective effect of p-coumaric acid in rat model of embolic cerebral ischemia[J]. Iranian Journal of Basic Medical Sciences,2015,18(4):356.
[32] SHARMA S H, RAJAMANICKAM V, NAGARAJAN S. Antiproliferative effect of p-coumaric acid targets UPR activation by downregulating Grp78 in colon cancer[J]. Chemico-Biological Interactions,2018,291:16−28. doi: 10.1016/j.cbi.2018.06.001
[33] YAMAGUCHI M, MURATA T, RAMOS J W. The botanical component p-hydroxycinnamic acid suppresses the growth and bone metastatic activity of human prostate cancer PC-3 cells in vitro[J]. Journal of Cancer Research and Clinical Oncology,2021,147(2):339−350. doi: 10.1007/s00432-020-03405-5
[34] SABITHA R, NISHI K, GUNASEKARAN V P, et al. p-Coumaric acid attenuates alcohol exposed hepatic injury through MAPKs, apoptosis and Nrf2 signaling in experimental models[J]. Chemico-Biological Interactions,2020,321:109044. doi: 10.1016/j.cbi.2020.109044
[35] HUANG X J, YOU Y Q, XI Y, et al. p-Coumaric acid attenuates IL-1β-induced inflammatory responses and cellular senescence in rat chondrocytes[J]. Inflammation,2020,43(2):619−628. doi: 10.1007/s10753-019-01142-7
[36] ZHANG C, QIN Q, LI H. Targeted therapeutic effect of bavachinin nanospheres on pathological site of chronic asthmatic mice model[J]. Journal of Nanoscience and Nanotechnology,2021,21(2):1085−1090. doi: 10.1166/jnn.2021.18641
[37] GE L N, YAN L, LI C, et al. Bavachinin exhibits antitumor activity against non-small cell lung cancer by targeting PPARγ[J]. Molecular Medicine Reports,2019,20(3):2805−2811.
[38] ZHAO C, GHOSH B, CHAKRABORTY T, et al. Bavachinin mitigates DMH induced colon cancer in rats by altering p53/Bcl2/BAX signaling associated with apoptosis[J]. Biotechnic & Histochemistry,2021,96(3):179−190.
[39] GOVINDULA A, PAI A, BAGHEL S, et al. Molecular mechanisms of cordycepin emphasizing its potential against neuroinflammation: An update[J]. European Journal of Pharmacology,2021,908:174364−174364. doi: 10.1016/j.ejphar.2021.174364
[40] CHENG C Υ, ZHU X Y. Cordycepin mitigates MPTP-induced Parkinson's disease through inhibiting TLR/NF-κB signaling pathway[J]. Life Sciences,2019,223:120−127. doi: 10.1016/j.lfs.2019.02.037
[41] YANG X F, LI Y X, HE Y H, et al. Cordycepin alleviates airway hyperreactivity in a murine model of asthma by attenuating the inflammatory process[J]. International Immunopharmacology,2015,26(2):401−408. doi: 10.1016/j.intimp.2015.04.017
[42] WU C R, HSIEH M T, HUANG S C, et al. Effects of Gastrodia elata and its active constituents on scopolamine-induced amnesia in rats[J]. Planta Medica,1996,62(4):317−321. doi: 10.1055/s-2006-957892
[43] HSIEH M T, WU C R, CHEN C F. Gastrodin and p-hydroxybenzyl alcohol facilitate memory consolidation and retrieval, but not acquisition, on the passive avoidance task in rats[J]. Journal of Ethnopharmacology,1997,56(1):45−54. doi: 10.1016/S0378-8741(96)01501-2
[44] 李旭, 徐天娇, 刘立琨, 等. 天麻素联合异钩藤碱抑制MPP+诱导的PC12细胞凋亡的抗氧化机制[J]. 中国中药杂志,2021,46(2):420−425. [LI X, XU T J, LIU L K, et al. Antioxidant mechanism of gastrodin combined with isorhynchophylline in inhibiting MPP+-induced apoptosis of PC12 cells[J]. China Journal of Chinese Materia Medica,2021,46(2):420−425. [45] 张志龙, 郜玉钢, 臧埔, 等. 天麻素、对羟基苯甲醇对中枢神经系统作用机制研究进展[J]. 中国中药杂志,2020,45(2):312−320. [ZHANG Z L, GAO Y G, ZANG P, et al. Research progress on mechanism of gastrodin and p-hydroxybenzyl alcohol on central nervous system[J]. China Journal of Chinese Materia Medica,2020,45(2):312−320. doi: 10.19540/j.cnki.cjcmm.20190730.401 [46] QU L L, YU B, LI Z, et al. Gastrodin ameliorates oxidative stress and proinflammatory response in nonalcoholic fatty liver disease through the AMPK/Nrf2 pathway[J]. Phytotherapy Research,2016,30(3):402−11. doi: 10.1002/ptr.5541
[47] KIM S R, KANG S Y, LEE K Y, et al. Anti-amnestic activity of E-p-methoxycinnamic acid from Scrophularia buergeriana[J]. Cognitive Brain Research,2003,17(2):454−461. doi: 10.1016/S0926-6410(03)00161-7
[48] ATTIA H, ALBUHAYRI S, ALARAIDH S, et al. Biotin, coenzyme Q10, and their combination ameliorate aluminium chloride-induced Alzheimer's disease via attenuating neuroinflammation and improving brain insulin signaling[J]. Journal of Biochemical and Molecular Toxicology,2020,34(9):e22519.
[49] JEFF G M D, CDE B A, VIJAYA F A, et al. Chromium picolinate and biotin combination reduces atherogenic index of plasma in patients with type 2 diabetes mellitus: A placebo-controlled, double-blinded, randomized clinical trial[J]. American Journal of the Medical Sciences,2007,333(3):145−153. doi: 10.1097/MAJ.0b013e318031b3c9
[50] CHEN Z Q, WANG C, PAN Y X. et al. Hypoglycemic and hypolipidemic effects of anthocyanins extract from black soybean seed coat in high fat diet and streptozotocin-induced diabetic mice[J]. Food & Function,2018,9(1):426−439.
[51] CUI C, ZHANG S, YOU L, et al. Antioxidant capacity of anthocyanins from Rhodomyrtus tomentosa (Ait.) and identification of the major anthocyanins[J]. Food Chemistry,2013,139(1-4):1−8. doi: 10.1016/j.foodchem.2013.01.107
[52] SONG Y S, PARK C M. Luteolin and luteolm-7-O-glucoside strengthen antioxidative potential through the modulation of Nrf2/MAPK mediated HO-1 signaling cascade in RAW 264.7 cells[J]. Food and Chemical Toxicology:An International Journal Published for the British Industrial Biological Research,2014,65:70−75. doi: 10.1016/j.fct.2013.12.017
[53] DE S A, CAPORALI S, DI DANIELE N, et al. Anti-inflammatory and proliferative properties of luteolin-7-O-glucoside[J]. International Journal of Molecular Sciences,2021,22(3):1321. doi: 10.3390/ijms22031321
[54] NKA B, SR A, SC A, et al. Involvement of hippocampal agmatine in β 1-42 amyloid induced memory impairment, neuroinflammation and BDNF signaling disruption in mice[J]. Neurotoxicology,2020,80:1−11. doi: 10.1016/j.neuro.2020.06.002
[55] KARADAG H C, ULUGOL A, TAMER M, et al. Systemic agmatine attenuates tactile allodynia in two experimental neuropathic pain models in rats[J]. Neuroscience Letters,2003,339(1):88−90. doi: 10.1016/S0304-3940(02)01456-8
[56] FAN J, FENG Z, NING C. Spermidine as a target for cancer therapy[J]. Pharmacological Research,2020,159:104943. doi: 10.1016/j.phrs.2020.104943
[57] MADEO F, EISENBERG T, PIETROCOLA F, et al. Spermidine in health and disease[J]. Science,2018,359(6374):eaan2788. doi: 10.1126/science.aan2788
[58] ZHANG Y H, ZHOU J X, ZHANG N H, et al. Process optimization for production of ferulic acid and pentosans from wheat brans by solid-state fermentation and evaluation of their antioxidant activities[J]. ACS Food Science & Technology,2022,2(7):1114−1122.
[59] LI D, RUI Y X, GUO S D, et al. Ferulic acid: A review of its pharmacology, pharmacokinetics and derivatives[J]. Life Sciences,2021,284:119921. doi: 10.1016/j.lfs.2021.119921
[60] LEE W, CHOO S, SIM H, et al. Inhibitory activities of ononin on particulate matter-induced oxidative stress[J]. Biotechnology and Bioprocess Engineering,2021,26(2):208−215. doi: 10.1007/s12257-020-0294-0
[61] DONG L, YIN L, ZHANG Y B, et al. Anti-inflammatory effects of ononin on lipopolysaccharide-stimulated RAW 264.7 cells[J]. Molecular Immunology,2017,83:46−51. doi: 10.1016/j.molimm.2017.01.007
[62] PRIKSZ D, LAMPE N, KOVACS A, et al. Nicotinic-acid derivative BGP-15 improves diastolic function in a rabbit model of atherosclerotic cardiomyopathy[J]. British Journal of Pharmacology,2022,179(10):2240−2258. doi: 10.1111/bph.15749
[63] 戎立保, 易文. 半夏的炮制方式及其对药效的影响探析[J]. 中国社区医师,2021,37(25):11−12. [RONG L B, YI W. The processing method of Pinellia ternata and its effect on the efficacy[J]. Chinese Community Doctors,2021,37(25):11−12. doi: 10.3969/j.issn.1007-614x.2021.25.005 [64] BAUMKTTER F, SCHMIDT N, VARGAS C, et al. Amyloid precursor protein dimerization and synaptogenic function depend on copper binding to the growth factor-like domain[J]. Journal of Neuroscience,2014,34(33):11159−11172. doi: 10.1523/JNEUROSCI.0180-14.2014
[65] MIZUKAMI K, AKATSU H, ABRAHAMSON E E, et al. Immunohistochemical analysis of hippocampal butyrylcholinesterase: Implications for regional vulnerability in Alzheimer's disease[J]. Neuropathology,2015(2):45−135.
[66] JI Z, DONALDSON I J, LIU J, et al. The forkhead transcription factor FOXK2 promotes AP-1-mediated transcriptional regulation[J]. Molecular and Cellular Biology,2012,32(2):385−398. doi: 10.1128/MCB.05504-11
[67] BOSSIS G, MALNOU C E, FARRAS R, et al. Down-regulation of c-Fos/c-Jun AP-1 dimer activity by sumoylation[J]. Molecular and Cellular Biology,2005,25(16):6964−6979. doi: 10.1128/MCB.25.16.6964-6979.2005
[68] MURPHY J F, FITZGERALD D J. Vascular endothelial growth factor induces cyclooxygenase-dependent proliferation of endothelial cells via the Vegf-2 receptor[J]. Faseb Journal,2001,15(9):1667−1669. doi: 10.1096/fj.00-0757fje
[69] HABIB A A, CHATTERJEE S, PARK S K, et al. The epidermal growth factor receptor engages receptor interacting protein and nuclear factor-κB (NF-κB)-inducing kinase to activate NF-κB identification of a novel receptor-tyrosine kinase signalosome[J]. Journal of Biological Chemistry,2001,276(12):8865−8874. doi: 10.1074/jbc.M008458200
[70] YAMAMOTO T, SEKINE Y, KASHIMA K, et al. The nuclear isoform of protein-tyrosine phosphatase TC-PTP regulates interleukin-6-mediated signaling pathway through STAT3 dephosphorylation[J]. Biochemical & Biophysical Research Communications,2002,297(4):811−817.
[71] AGRAWAL N K, KANT S. Targeting inflammation in diabetes: Newer therapeutic options[J]. World J Diabetes,2014(5):697−710.
[72] TSALAMANDRIS S, ANTONOPOULOS A S, OIKONOMOU E, et al. The role of inflammation in diabetes: Current concepts and future perspectives[J]. European Cardiology,2019,14(1):50−59. doi: 10.15420/ecr.2018.33.1
-
期刊类型引用(9)
1. 方丽,江晓,李雪莹,张丽,黄嘉颖,张方圆. 气相色谱-三重四极杆质谱法同时测定乌梅中25种多环芳烃及其污染来源分析. 食品安全质量检测学报. 2024(02): 74-82 .  百度学术
百度学术
2. 王润博,刘思琪,王林山. 发酵型含乳饮料研究概况及新产品开发. 漯河职业技术学院学报. 2024(01): 34-40 .  百度学术
百度学术
3. 杨小丽,李本姣,章攀,李松,李智佳. 青梅果酒加工工艺研究进展. 南方农业. 2024(21): 130-133 .  百度学术
百度学术
4. 周丹英,姜慧洁,胡云莉,章越. 茶多酚银杏叶胶囊的研制及其辅助降血脂功能评价. 食品科技. 2023(05): 113-119 .  百度学术
百度学术
5. 郭锦荣. 中药调脂及抗动脉粥样硬化作用研究进展. 中国中医药现代远程教育. 2023(13): 200-202 .  百度学术
百度学术
6. 蒋维,舒晓燕,王玉霞,唐志康,梅国富,杨兴蓉,刘欣雨,侯大斌. 四川主产区不同品种青梅果实品质分析. 食品工业科技. 2023(16): 321-330 .  本站查看
本站查看
7. 周芳,陈文明,陈新宇,蔡嘉洛,LAU Yutong. 冬春谧阳方对高脂血症患者PPARγ/ANGPTL受体配体的影响. 陕西中医. 2023(11): 1537-1541 .  百度学术
百度学术
8. 任蓉,杜雅薇,冉隆开. 血脂异常的中医病因病机及辨证施治的研究进展. 疑难病杂志. 2023(11): 1228-1232 .  百度学术
百度学术
9. 裴占阳,韦经利,余江游,赵先游,班明政,陈福. 几种中草药饲料添加剂在动物生产中的应用研究. 现代畜牧兽医. 2022(09): 60-63 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:
 下载:
下载:
