Research Progress on Catalytic Conversion of Cellulose to Glucose and Polyols
-
摘要: 自然界中含量最丰富的纤维素,是一种清洁可再生的碳资源,可以替代石油等不可再生资源催化转化为高附加值的平台化合物。本文简要介绍了纤维素的结构,指出了纤维素水解及高效转化的关键步骤,并全面综述了纤维素转化为葡萄糖、山梨醇和乙二醇的工艺条件(如催化剂种类、反应温度、反应时间等)及催化机理,并展望了各工艺过程中催化剂的研究方向,旨在为纤维素催化转化为小分子平台化合物的生产提供参考。Abstract: As a clean and renewable carbon resource, cellulose is an alternative for non-renewable resources such as oil and can convert into high value adding molecule platform chemicals. This paper briefly overviews the structure of cellulose and points out the critical steps of cellulose hydrolysis and efficient conversion, and reviewes the process conditions and catalytic mechanism comprehensively for the conversion of cellulose into glucose, sorbitol and ethylene glycol (such as catalyst types, reaction temperature, reaction time, etc.). The research direction of catalysts in each process is prospected, which would be the reference for the catalytic conversion of cellulose into small molecule platform compounds in future.
-
Keywords:
- cellulose /
- catalytic conversion /
- glucose /
- sorbitol /
- ethylene glycol
-
目前,世界上绝大多数的燃料和化学品都是通过化石资源生产的[1]。为了缓解传统不可再生的化石资源的枯竭,寻找可代替化石资源的绿色可再生资源已经引起了人们的广泛关注[2-3]。自然界中,木质纤维素生物质资源十分丰富,且木质纤维素不易被人类消化,不会引发粮食之争。因此,木质纤维素及其衍生物的高效转化备受关注[4]。木质纤维素主要由纤维素(35%~50%)、半纤维素(20%~35%)和木质素(10%~25%)以及其他次要成分组成[5]。秸秆、废旧棉纺织品、农业废弃物等都富含纤维素,将纤维素高值化转化成为科学家们近年来不断探索的主题。本文主要针对以纤维素为原料催化制备葡萄糖、山梨醇和乙二醇的路线进行综述,重点介绍纤维素的结构及其衍生的小分子平台化合物;纤维素化学催化转化为葡萄糖、山梨醇和乙二醇的工艺方法、机理和催化剂,对未来纤维素的催化转化利用具有一定的参考价值。
1. 纤维素的结构及小分子平台化合物
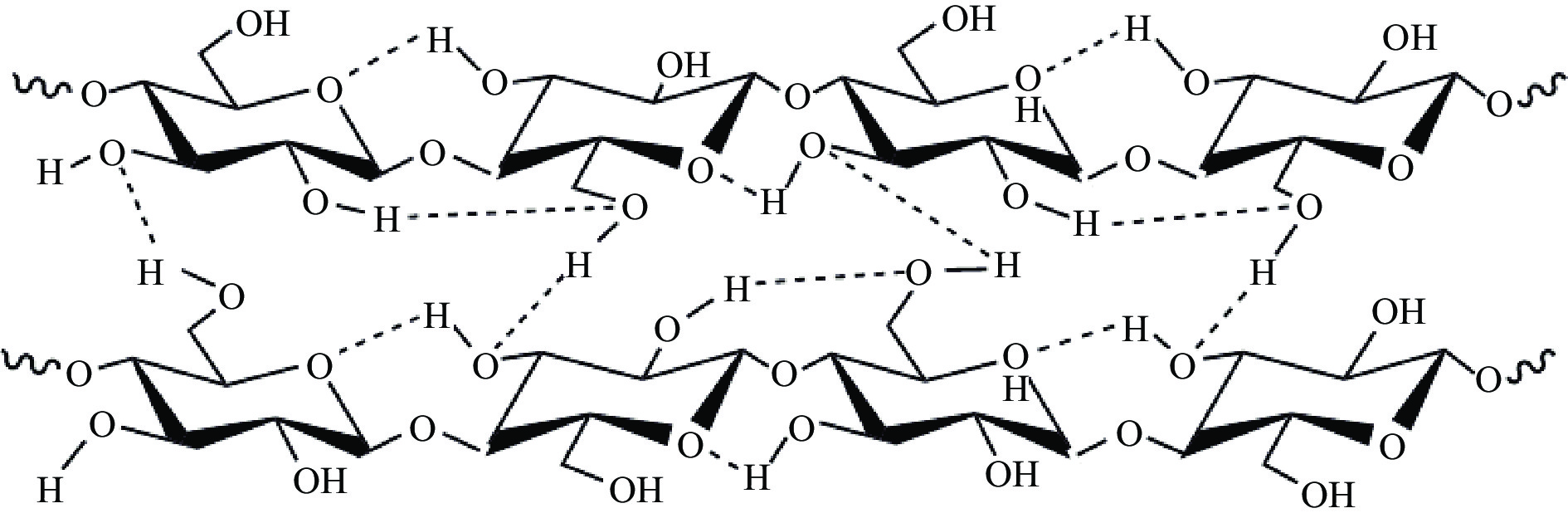
纤维素的化学式为(C6H10O5)n,由葡萄糖单元组成,聚合度在1510~5500之间[6]。纤维素中的葡萄糖单体以椅式构象存在,并通过β-1,4糖苷键连接在一起,见图1。羟基排列在赤道位置,并通过氢键与相邻的葡萄糖单元相连[7],纤维素的每一个葡萄糖环上都有三个位点的羟基极易互相吸引形成大分子内和分子间氢键,这些氢键错综交织形成丰富而致密的氢键网络结构导致其化学性质非常稳定,因此,纤维素非常难水解。这也是纤维素高效转化的主要障碍,纤维素水解的首要前提是破坏β-1,4糖苷键和氢键。
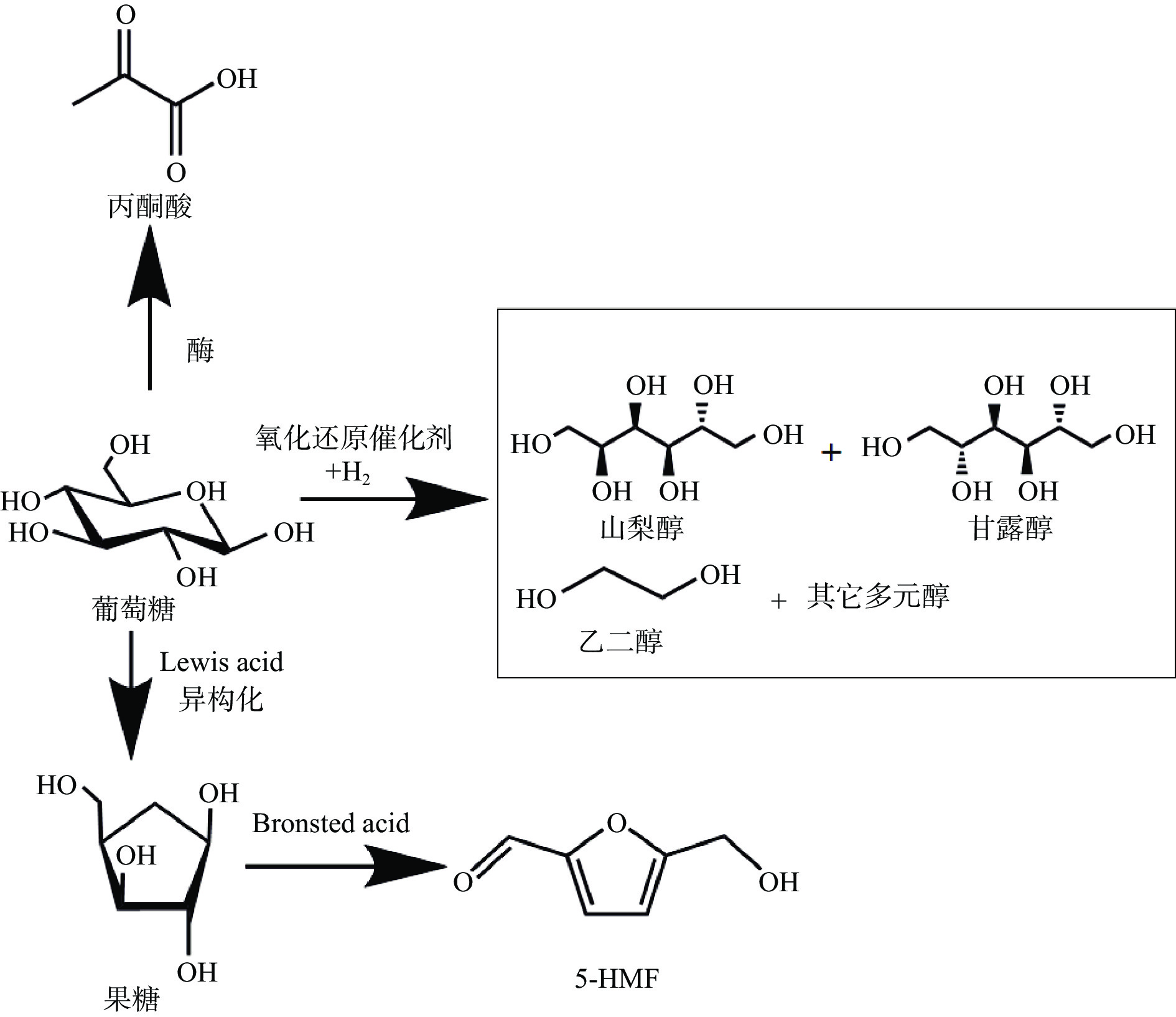
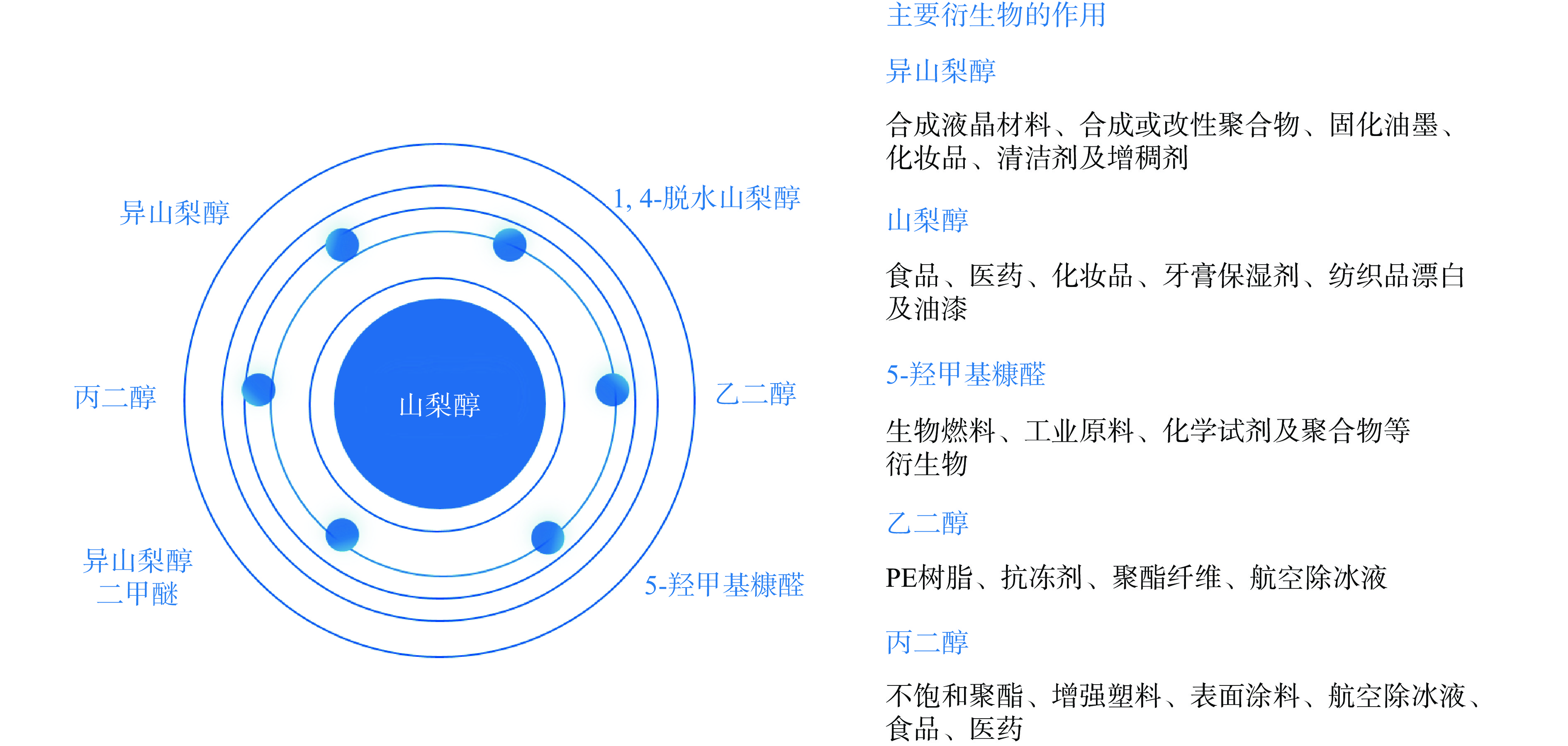
在纤维素转化的众多平台化合物(如木糖醇、山梨醇、甘油、乙酰丙酸及5-羟甲基糠醛等)中,葡萄糖作为重要的平台化合物,可以进一步转化为各种下游产品(见图2)[8],广泛应用于化工、食品及能源等行业;山梨醇能用作食品的保湿剂和保鲜剂,经过脱水、氧化、酯化等化学反应可以生产各种精细化学品[9];1,4-脱水山梨醇是工业上Span与Tween类表面活性剂的重要原料和中间体;异山梨醇作为聚合物单体用于聚醚、聚酯、聚氨酯、聚碳酸酯等聚合物的改性等;乙二醇可用于生产聚酯、乙二醛、防冻剂、乙二酸及各种表面活性剂等。我国的乙二醇长期存在供不应求的状态,而由纤维素可持续降解为乙二醇可缓解化石燃料的匮乏;5-羟甲基糠醛是一种重要的化学中间体,可以发生加氢、氧化脱氢、酯化等化学反应,同样广泛应用于医药、化学、能源等领域(见图3)。
纤维素是天然气和石油等不可再生资源最有前景的替代品之一,可以转化为多种高值化学品。将纤维素降解为小分子平台化合物的催化过程主要有四类反应:a.纤维素水解和氢化转化为糖醇;b.通过断裂相应的C-C和C-O键,将葡萄糖选择性氢解成小分子醇;c.果糖(葡萄糖异构化)进一步脱水和氢化生成HMF及其衍生物;d.通过氢解和加氢脱氧生成液态烷烃[10]。纤维素水解制备葡萄糖,加氢制备山梨醇及乙二醇等多元醇或催化转化为其他小分子平台化合物,都是纤维素资源化利用的重要途径。
2. 纤维素水解为葡萄糖
纤维素的水解主要是通过酸或酶(纤维素酶)来催化的,但是酶法存在明显的缺点,如反应速率低、价格昂贵、产物不易分离等。相反,采用酸法进行水解既经济又快速。酸法水解纤维素采用的催化剂可以分为液体酸和固体酸[11]。
2.1 液体酸催化剂
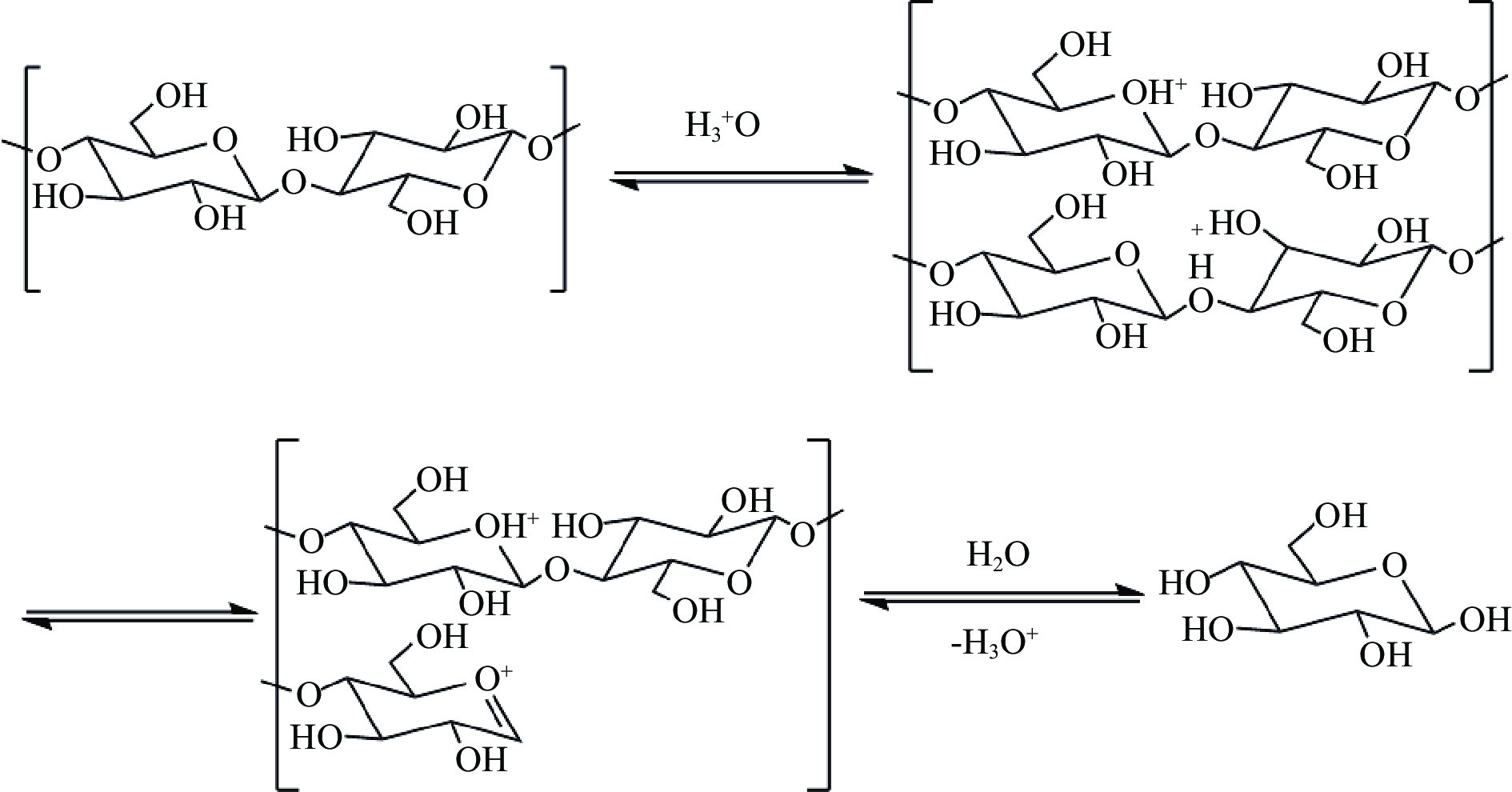
由于硫酸和盐酸等强酸对纤维素水解的活性高,自20世纪20年代以来,浓酸和稀酸就一直被用于催化纤维素水解制备葡萄糖[12]。纤维素酸解制备葡萄糖机理分为两步(见图4):在H+的作用下,纤维素糖苷键中的O原子首先被质子化,形成嗡盐离子,最后嗡盐与水发生反应得到葡萄糖。
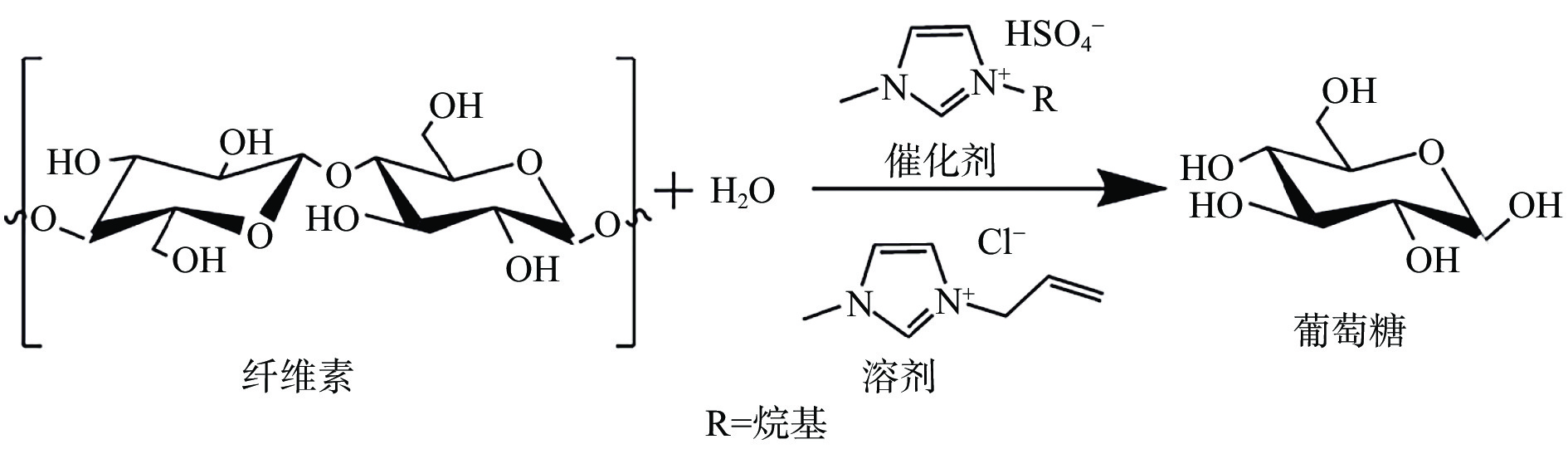
William等[13]在215 ℃、0.05%(按重量计)的硫酸下催化水解纤维素,获得的葡萄糖产率为71%;赵燕等[14]在200 ℃下用10%的稀硫酸对褐藻纤维素进行水解,反应60 min后得到还原糖产率为98.62%。Feng等[15]在离子液体中水解纤维素,葡萄糖的产率提高到90%。付霓虹等[16]以离子液体1-烯丙基-3-甲基咪唑氯盐([Amim]Cl)为溶剂,以咪唑类酸功能离子液体[Cnmim]HSO4(n=2-7)为催化剂通过微波辅助水解微晶纤维素(MCC)(水解示意图见图5),发现离子液体的酸性大小对实验结果有明显的影响,酸性越大催化效果越好。结果显示:当加入0.1 g的催化剂和70 μL的水、纤维素与催化剂的摩尔比为1:1、反应时间为40 min、反应温度为110 ℃时实验效果最好,即纤维素转化率为100%,可还原糖产率为89.94%,葡萄糖产率达到了46.24%。由此可见,和传统的液体酸催化剂相比,离子液体催化剂降解纤维素的反应温度较低,这是由于离子液体可以溶解纤维素并同时可以水解糖苷键的双重作用。
虽然液体酸在纤维素水解过程中具有良好的催化性能和反应速度快的优点,尤其是酸性离子液体在催化纤维素降解时,离子液体不仅具有溶解纤维素的能力,还作为亲核基团进攻糖苷键,降低了纤维素降解的反应温度。但是,酸催化水解存在腐蚀设备、酸回收困难及后处理会产生废水等问题。为了缓解上述问题,环境友好、不腐蚀设备、可回收的固体酸被越来越多的用于纤维素的水解。
2.2 固体酸催化剂
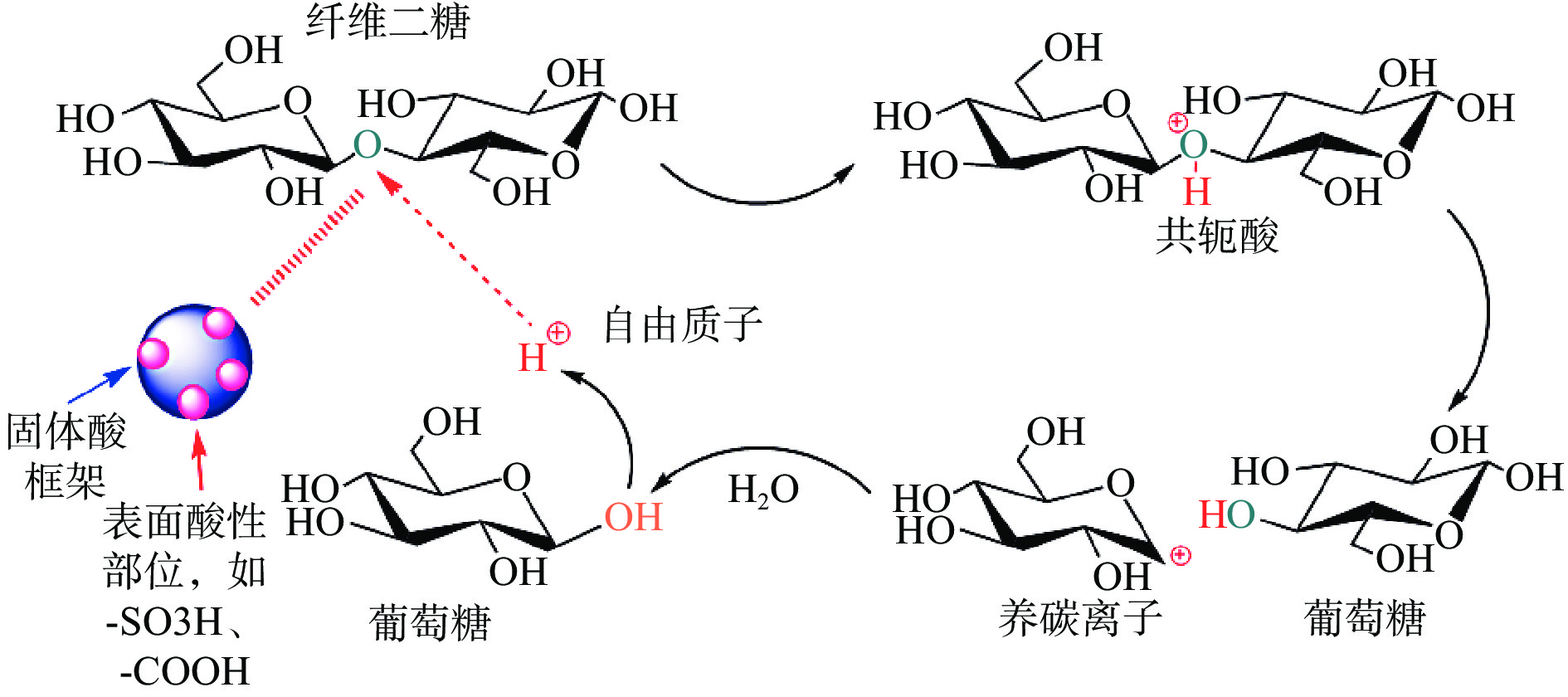
由于液体酸催化存在腐蚀反应设备、污染环境及催化剂不易回收等缺点,固体酸催化剂越来越多的用于催化纤维素生产葡萄糖及其衍生物的研究。大多数固体酸都带有Brønsted酸基,如强磺酸(SO3H)和弱羧酸(COOH)。一些固体酸,如H型沸石和金属氧化物,不仅具有很强的Brønsted酸性,催化纤维素水解时,还具有Lewis酸性。固体酸催化纤维素水解反应的机理(见图6):首先,在高温时,固体酸表面的Lewis酸性位和Brønsted酸性位的表面的水因质子化而形成氢离子,该氢离子对于纤维素水解生成纤维二糖起到了催化作用;其次,固体酸表面的酸性基团使纤维素中β-1,4糖苷键发生断裂,从而使其水解生成葡萄糖[11]。
2.2.1 含SO3H基团固体酸催化剂
磺酸(SO3H)是一种强酸性基团,可以为纤维素β-1,4糖苷键的水解提供质子。许多聚合物基固体酸、无机固体酸(如磺化二氧化硅)及磺化碳等采用SO3H作为强Brønsted酸性中心[17-18]。其中,磺化碳催化剂对纤维素具有显著的催化活性,是研究最多的固体酸催化剂。陆佳等[19]通过碳化-磺化法将玉米芯制备成碳基固体酸(CSA)催化剂,以经过NaOH/尿素冻融预处理的纤维素为原料,研究了CSA催化纤维素水解糖化的效果与条件。结果显示:在350 ℃下碳化2 h、100 ℃下磺化5 h制备的CSA催化性能最好。在CSA和纤维素的质量比为3:1、温度为200 ℃时,反应0.5 h得到纤维素水解还原糖得率与转化率分别为47.1%和63%。Qi等[20]采用一种由聚离子液体和聚磺酸链组成的多孔膜基聚合物固体酸催化剂,对麦草原料进行催化水解制备葡萄糖。在1-丁基-3-甲基咪唑氯化物([BMIM]Cl)、γ-戊内酯(GVL)和水的溶剂混合物中,以7.6:1.9:0.5的重量比,在150 ℃下反应60 min得到纤维素的转化率为83.3%,葡萄糖产率为50.7%。由此可见,催化剂酸性位点的加强,虽然可以增加纤维素水解的转化率,但目标产物葡萄糖的选择性并不高,这主要是因为在强酸存在的条件下,生成的葡萄糖又脱水转变为5-羟甲基糠醛,并进一步分解为乙酰丙酸和甲酸[21]等其他副产物。为了提高葡萄糖的选择性,可以对催化剂表面进行改性,从而减弱葡萄糖在催化剂表面的吸附性,避免葡萄糖的进一步副反应。刘阳等[22]通过苯胺的重氮化反应对自制的C-SiO2-SO3H催化剂表面枝接苯环进行改性,来降低葡萄糖在催化剂表面的吸附效果。结果表明:改性后的C-SiO2-Ben-SO3H催化剂在180 ℃下反应12 h,得到葡萄糖产率为55.11%、葡萄糖选择性为95.98%,高于未改性催化剂葡萄糖的产率(29.53%)和选择性(82.33%)。因此,通过降低葡萄糖在催化剂表面的吸附性,可以提高葡萄糖的收率,为SO3H基团固体酸催化葡萄糖进一步大规模的生产提供思路。但是由于SO3H基团在水中的高浸出性,导致催化剂很难从残余纤维素中分离出来,并且很容易失活。因此,在未来的研究中应着重开发高效、经济的再生过程,如再磺化和离子交换等。
2.2.2 含弱酸中心固体酸催化剂
研究发现,含有羧酸基(COOH)等弱酸性位点的固体酸也可以水解纤维素的β-1,4糖苷键[23]。To等[24]利用羧酸、酚羟基和内酯基团官能化得到的中孔碳(总酸度2.2 mmol/g)水解纤维素,得到葡萄糖产率为67.2%。结果表明,弱酸位点可以水解纤维素基质。此外,它们能吸附到纤维素基质上,这对纤维素的有效水解至关重要。含有COOH基团的固体酸比含SO3H基固体酸更稳定、反应更温和,但是由于酸性不强导致催化活性低、反应时间更长。
2.2.3 杂多酸催化剂
与其他固体酸相比,杂多酸(HPA)催化剂更有利于纤维素的水解。因为与无机酸(如H2SO4、HCl)相比,HPA催化剂具有经济环保、高活性、良好的热稳定性、副产物少、产生的废物也少、无毒及易于处理等独特性质[25]。最常见的HPA是Keggin型,其阴离子为[XM12O40]n−,X是杂原子(例如P、Si),M是金属离子(例如W6+、Mo6+)。其中,H3PW12O40是最常见的Keggin型HPA。此外,酸性强的H3PW12O40极易溶于水,并能完全解离质子,这有助于与异质基质接触,从而提高反应速率[26]。此外,Keggin型HPA的基本结构单元是具有良好对称性和低电荷密度的含氧四面体和八面体阴离子[27]。Sun等[28]制备了[MIMPSH]nH3−nPW(n=1,2)催化剂用于催化纤维素解聚制备葡萄糖。在反应温度为140 ℃、反应时间为5 h条件下,还原糖和葡萄糖的产率分别为40.6%和36.0%,同时纤维素的转化率为55.1%。HPA作为一种高效、环保、安全的催化剂,对纤维素的降解具有很高的催化活性;由于HPA具有的独特物理和化学性质,可以应用于均相和非均相催化反应;在反应器中分离后,可以重复使用,几乎不会失去催化活性。尽管杂多酸对纤维素降解具有一定的催化效果,但多数是在水相或有机溶剂中进行的,而且反应需要在较高的温度下才能进行,反应时间也较长。为了增强杂多酸催化水解纤维素的效果,反应一般需在微波辅助加热或以离子液体为溶剂的情况下进行。
2.2.4 金属氧化物催化剂
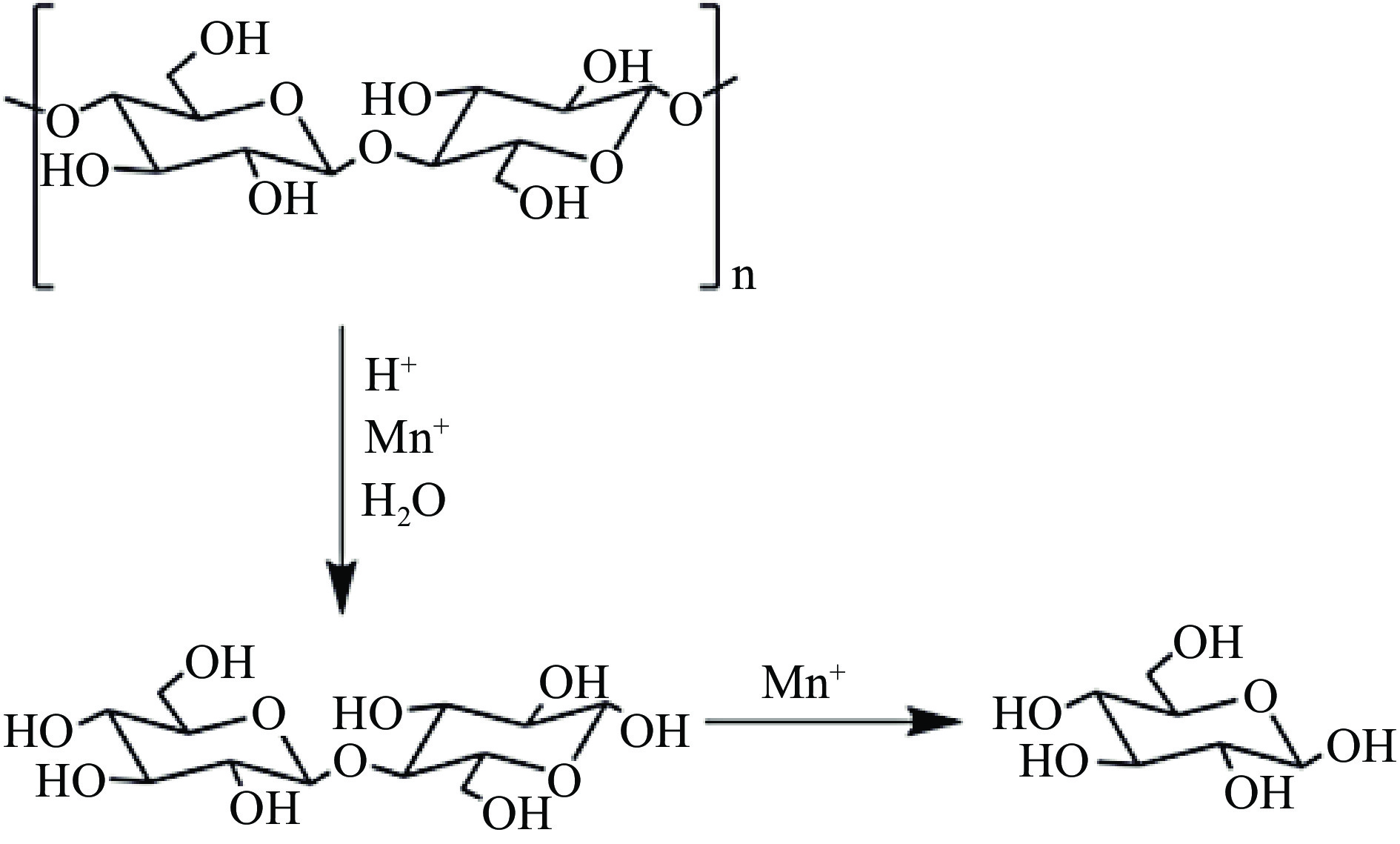
金属氧化物催化剂在水解纤维素时,一般设计并制备复合金属氧化物,使其既含B酸又含L酸。Zhang等[29]制备了固体酸催化剂CaFe2O4催化纤维素水解制备葡萄糖,实现了纤维素最大的水解率为49.8%,葡萄糖的选择性为74.1%,催化剂也可多次使用。催化剂的催化活性与其比表面积和孔结构相关,大的孔结构易于反应物进入并接触金属氧化物孔内的活性位点。Caio等[30]将介孔Nb-W氧化物及Nb2O5用于纤维二糖水解为葡萄糖的研究,结果发现Nb-W氧化物的催化性能高于Nb2O5且Nb:W为3:7的复合金属氧化物的高比表面积、介孔结构和强酸性位点使其具有最优的水解性能。隋松泉[31]制备了Mn-Fe-Al复合金属氧化物用在纤维素水解转化制备葡萄糖的反应(水解示意图见图7),在240 ℃时反应4 h得到葡萄糖的产率为48.1%,且催化剂的重复性能良好。金属氧化物不仅具有很强的Brønsted酸性,而且在催化纤维素水解时,也具有Lewis酸性。然而,具有路易斯酸位点的金属氧化物在水中通常不稳定,容易通过水配位形成金属氢氧化物,从而降低催化剂的活性。
在过去几十年里,固体酸在催化纤维素水解领域取得了重大进展。采用固体酸催化剂不仅具备了液体酸水解时带来的优点,即反应时间较短,操作工艺简单,催化剂易得且价格低廉,生产成本较低。同时避免了液体酸催化剂会腐蚀设备,不能重复利用及需要中和及后续的除盐工序,以及高温条件下容易生成副反应的缺点。但固体酸催化剂的应用还存在很多需要解决的问题:因纤维素不溶解于水和大部分溶剂,固体酸和纤维素之间的相互作用低,需进一步改善纤维素与固体酸的接触,比如添加离子液体、超声等促进纤维素的水解;催化剂的稳定性还有待提高,如还需解决固体酸上-SO3H的浸出问题;同时需要开发高效、经济的再生过程,提高固体酸催化剂的回收率。因此,还需要设计更环保、更高效的成型固体酸催化剂为纤维素水解工业化应用提供参考。
3. 纤维素一锅法制备山梨醇
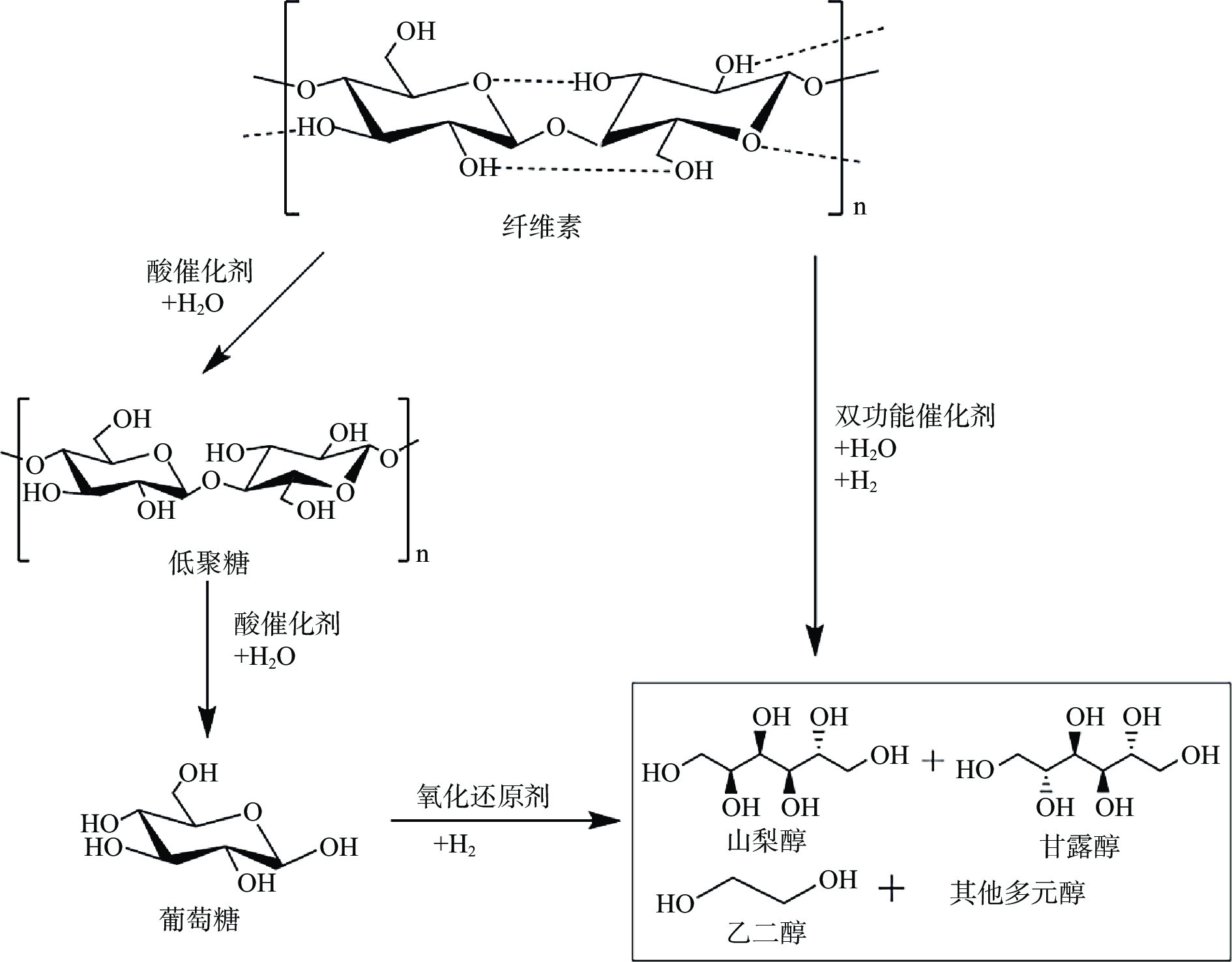
纤维素一锅法水解/加氢是指纤维素的水解与加氢在同一催化剂作用下发生,水解形成的己糖在高温和高压下加氢后生成山梨醇,工艺路线如图8所示[32]。目前研究人员对一锅法催化纤维素水解/加氢的工艺研究主要集中在催化剂的开发和工艺条件的优化等方面,近年来,研究人员开发了很多用于纤维素一锅水解/加氢的催化剂,大致可以分为:负载型催化剂、双功能催化剂和双金属催化剂[33-34]。
3.1 负载型金属催化剂
催化加氢使用的贵金属催化剂经济成本较高,将其负载于载体上,不仅能充分利用载体和金属的优势,而且有利于催化剂的回收利用,可以有效降低催化剂使用的成本。Fukuoka等[35]首先报道了负载型金属催化剂将纤维素一锅转化为山梨醇和甘露醇,他们发现在Pt/γ-Al2O3催化剂的存在下,在水溶剂中,H2压力为5 MPa、温度为463 K条件下反应24 h后,获得的糖醇产率为31%(其中山梨醇为25%,甘露醇为6%)。Luo等[36]研究了Ru/C催化剂对纤维素进行一锅加氢的影响,发现在243 ℃的热水中纤维素的转化率为85%,山梨糖醇的选择性为35%。实验证明在酸性条件下,高温可以使水产生大量质子,促进纤维素水解生成葡萄糖,再通过金属催化加氢制备六元醇。Adsuar-García等[37]采用商业炭黑制备了钌催化剂,该炭黑分别通过硫酸和(NH4)S2O8的磺化和氧化处理进行了改性,以形成酸性表面位点。该催化剂在H2压力为5 MPa、温度为190 ℃条件下反应3 h,得到山梨醇的选择性最高,此时,纤维素的转化率接近70%,山梨醇产率超过40%。此外,催化剂载体也是影响纤维素水解的一个重要因素,Matveeva等[38]比较了在超交联聚苯乙烯(HPS)MN-270及其功能化类似物NH2-HPS(MN-100)和SO3H-HPS(MN-500)的含钌催化剂存在下,纤维素在亚临界水中的一锅水解加氢过程。结果表明,含1.0%钌/MN-270的催化剂活性最高。在H2压力为6 MPa、温度为245 ℃条件下反应0.08 h,纤维素的转化率为85%,山梨醇和甘露醇的总收率平均为50%。Rey-Raap等[39]报道了葡萄糖制备的碳纳米管(CNT)作为Ru纳米颗粒的载体,该CNT具有高比表面积、丰富的微孔和低酸度,能够提高钌的分散性。在温度为205 ℃、H2压力为5 MPa条件下反应3 h,纤维素的转化率达到了100%,山梨醇的产率为64.1%。Lucília等[40]采用HNO3对CNT进行改性处理,在CNT表面上结合了不同组的氧化基团。将0.4wt%Ru负载在改性后的CNT上,在H2压力为5 MPa、温度为205 ℃条件下反应2 h,山梨醇的选择性最大达到70%。并且该催化剂在经过四次重复使用后催化效果依然稳定。载体的焙烧温度也是影响纤维素一锅法制备六元醇的因素之一,吕结等[41]制备了Pt/Al2O3催化剂,考察了载体和催化剂焙烧温度对Pt/Al2O3催化纤维素一锅转化性能的影响。研究发现,载体氧化铝经800 ℃焙烧后负载铂,再经400 ℃焙烧制得的催化剂活性最高,六元醇的选择性达到了78.5%。
在负载型金属催化剂中,Pt和Ru催化剂的山梨醇产率较高,而Ir、Pd和Ni催化剂的活性较低。反应机理表明H2解离吸附在Ru表面,氢物种可逆地溢出到载体表面。因此,纤维素水解的酸性位点不仅是由于载体中固有的酸性表面位点,而且是由H2原位生成的。酸性位点在纤维素水解为葡萄糖的过程中起着决定性的作用,然后通过Ru和H2还原葡萄糖中的C=O基团形成山梨醇[42]。除此之外,催化剂载体种类及催化剂载体的焙烧温度对纤维素的降解也会产生影响。采用负载型金属催化剂有利于促进纤维素一锅水解/加氢制备山梨醇反应,提高山梨醇的产率。
3.2 双功能催化剂
纤维素水解/加氢的双功能催化剂主要由两个主要部分组成:a.具有加氢能力的过渡金属催化剂,通常为Pt或Ru等;b.具有酸性位点的固体载体材料(如二氧化硅、氧化铝或酸性沸石等)[43-44]。Li等[45]制备了双功能催化剂Ru/CCD-SO3H(磺酸官能化碳化木薯渣负载钌),并用于纤维素一锅水解加氢制备山梨醇。在最佳条件温度为180 ℃时反应10 h,山梨醇的产率可达63.8%左右。与Fukuoka采用的Pt/γ-Al2O3催化剂相比,反应时间缩短了14 h。Lazaridis等[46]研究了负载在微/中孔活性炭上的Ru和Pt催化剂在微晶和球磨纤维素的水解氢化中的性能。在温度为180 ℃、H2压力为2 MPa条件下反应24 h,含有磺酸基和铂纳米颗粒的微/介孔活性炭催化生成的六元醇总收率为69.5%,而负载同一载体的Ru催化得到的六元醇产率只有10.9%。Palkovits等[47]将杂多酸和负载型Ru催化剂相结合制备出具有酸性和加氢性能的双功能催化剂,在压力为50 bar、温度为160 ℃下催化α-纤维素7 h,得到糖醇产率为81%,碳效率高于90%。两种催化剂在四次连续反应后均保持稳定,同时发现磺酸基数量的减少不影响山梨醇的活性和选择性。目前,含有酸中心和金属中心的双功能催化剂在纤维素一锅转化为山梨醇反应中表现出优异的性能,已成为研究人员关注的焦点[48]。双功能催化剂的使用避免了无机酸带来的环境污染、产品分离困难和腐蚀设备等问题,催化剂可以重复使用,有利于降低反应的成本。
3.3 双金属催化剂
除了负载型金属催化剂和双功能催化剂外,双金属催化剂在催化纤维素一锅水解氢化为糖醇的过程中也展示出一定的催化性能。众所周知,在加氢反应中,添加金属助催化剂可以提高负载型金属催化剂的活性。金属助催化剂一般为Ni、Fe和Sn等非贵金属,因为它们倾向于保持缺电子状态,这有助于通过使羰基极化的方式实现更高的羰基氢化活性[49]。
Ribeiro等[50]通过浸渍两种不同的载体(活性炭和碳纳米管)制备Ru-Ni双金属催化剂用于纤维素一锅转化为山梨醇。研究表明,载体对实验结果没有影响;双金属纳米颗粒中的镍由于两种金属的紧密相互作用,对催化提高纤维素的转化率和山梨醇的选择性具有促进作用。实验发现,在温度为205 ℃、H2压力为5 MPa条件下反应5 h,得到山梨醇的产率在50%~60%之间。当纤维素和催化剂一起研磨时,山梨醇产率可以进一步增加到70%以上。催化剂在连续四次反应后依然保持活性。Tathod等[51]研究了PtSn/γ-Al2O3(AL)和PtSn/C双金属催化剂中Sn的促进作用。发现在温度为130 ℃下反应120 min,采用Pt(2)Sn(0.25)/AL催化剂得到山梨醇的产率为78%,而Pt/AL催化剂条件下山梨醇产率只有20%。这说明,与不含Sn的催化剂相比,AL负载的双金属催化剂的糖醇产率显著提高,其产率比Pt/AL高1.5~3倍,这是由于Sn以离子形式(路易斯酸)存在,使糖的羰基极化,从而显示出更好的加氢活性。双金属催化剂不仅具备了负载型金属催化剂的优点,而且在催化剂中加入非贵金属可以降低贵金属的含量,既经济又高效。
4. 纤维素一锅水解/氢解制备乙二醇
乙二醇的传统制备方法是以化石资源的乙烯为原料,存在资源短缺的危机。近年来,随着生物质氢解工艺的不断发展,以生物质纤维素为原料一锅水解/氢解制备乙二醇逐渐成为研究热点,以纤维素为原料制备乙二醇的工艺路线如图9所示[52]。
纤维素一锅法水解/氢解为乙二醇的反应机理为:首先,在酸的存在下,纤维素水解后获得水溶性低聚糖和葡萄糖;然后,在钨等催化剂的催化下,通过逆羟醛缩合断裂低聚糖和葡萄糖的相应C-C键,形成乙醇醛;最后,乙醇醛由具有加氢特性的金属催化剂催化,生成目标产物乙二醇。
Ribeiro等[53]制备了W/CNT和Ru-W/CNT催化剂,考察了金属负载量、催化剂用量、催化剂载体等工艺条件对纤维素一锅法转化为乙二醇反应的影响,研究表明:Ru的加入可大大增加乙二醇的产率;采用0.8% Ru–30% W/CNT作为催化剂,在温度为205 ℃和H2压力为5 MPa及反应3 h的条件下,乙二醇的收率为40%。Wiesfeld等[54]研究了单斜晶系WO3在反应2 h后得到纤维素转化率为40%,乙二醇(EG)的选择性为30%。而b-WO3和m-WO3在反应1 h后,纤维素的转化率已经分别达到了62%和67%,EG选择性分别为61%和50%。钨矿(b-WO3)和介孔氧化钨(m-WO3)都比单斜晶系WO3更具活性和EG选择性。Li等[55]以形状良好的矩形三氧化钨纳米片为基质,研究了各种金属负载催化剂对纤维素转化为乙二醇的催化性能。结果表明,Ru/WO3更有利于乙二醇的制备,在1% Ru/WO3纳米片催化剂上,EG的最高产率为76.3%(H2压力为4 MPa、温度为513 K、反应时间为2 h)。在相同的还原条件下(NaBH4或H2),将Ru纳米颗粒嵌入WO3纳米片上会产生更多的W5+活性位点,促进葡萄糖逆羟醛缩合反应。此外,一部分Ru以无定形RuOxδ+相形式存在于Ru/WO3催化剂中,这可以进一步增加释放到水溶液中的H+,提高纤维素的可水解性。由此可见,钌钨相结合的催化剂在纤维素一锅法水解/氢解制备乙二醇中起到了特殊的作用,同时具有断裂C-C键的能力和催化加氢生成EG的能力。
双金属催化剂在一锅法制备二元醇的工艺中最具优势,它缓解了酸的溶脱带来的后处理问题。但双金属催化剂还需克服微晶纤维素的致密的网络结构以提高纤维素的可利用性;传质问题严重限制和阻碍了非均相条件下不溶于水的生物质纤维素的转化利用。因此,还有待开发多功能催化剂或新工艺用于纤维素的解聚降解或加氢还原裂解。
5. 结论与展望
纤维素是自然界最丰富的可再生生物质资源,将纤维素降解为葡萄糖及小分子醇,既缓解了石化资源短缺危机,又将纤维素高值化利用,具有十分重要的经济意义。在纤维素的酸解工艺中,固体酸催化剂不仅具备了液体酸催化剂的优点,同时避免了液体酸催化剂的诸多缺点。目前,已知固体酸催化剂的催化性能是由固体酸和纤维素的结构性质以及它们之间的有效接触和相互作用决定的。未来应着重研究解决催化剂活性、产物的选择性、催化剂稳定性等问题;纤维素一锅法加氢或氢解催化转化为六元醇或二元醇的最适催化剂为酸-金属双功能催化剂,一方面酸催化剂促进纤维素水解为葡萄糖,另一方面金属催化剂可使生成的葡萄糖进一步氢解为目标产物。此外,多功能催化剂的水热稳定性和优异的催化活性是实现纤维素充分利用的重要因素。如何提高催化剂的催化活性、稳定性及可重复利用性是未来纤维素催化转化的重点研究方向。该综述对未来纤维素催化转化的工业化应用起到一定的参考价值。
-
-
[1] 刘中海, 高赛男, 秦冬玲, 等. 改性分子筛催化果糖脱水制5-羟甲基糠醛[J]. 南京工业大学学报:自然科学版,2020,42(1):56−61. [LIU Z H, GAO S N, QIN D L, et al. Modified molecular sieves for catalytic dehydration of fructose to 5-hydroxymethylfurfural[J]. Journal of Nanjing University of Technology: Natural Science Edition,2020,42(1):56−61. [2] PARVULESCU V I, BALU A M, KUBIKA D, et al. Hydrolysis of hemicellulose and derivatives-a review of recent advances in the production of furfural[J]. Frontiers in Chemistry,2019,6:146−175.
[3] 吴仁荣, 梁金花. 秸秆基磺化碳催化制备生物柴油[J]. 南京工业大学学报:自然科学版,2020,42(2):167−172. [WU R R, LIANG J H. Preparation of biodiesel from oleic acid catalyzed by straw stalk-based sulfonated carbon[J]. Journal of Nanjing University of Technology: Natural Science Edition,2020,42(2):167−172. [4] WALTER D, SHARMA V K, MENGSHAN L, et al. Lignocellulosic biomass transformations via greener oxidative pretreatment processes: Access to energy and value-added chemicals[J]. Frontiers in Chemistry,2018,6:141−164. doi: 10.3389/fchem.2018.00141
[5] DAHMEN N, LEWANDOWSKI I, ZIBEK S, et al. Integrated lignocellulosic value chains in a growing bioeconomy: Status quo and perspectives[J]. GCB Bioenergy,2019,11:107−117. doi: 10.1111/gcbb.12586
[6] OKOLIE J A, NANDA S, DALAI A K, et al. Chemistry and specialty industrial applications of lignocellulosic biomass[J]. Waste and Biomass Valorization,2021,12:2145−2169. doi: 10.1007/s12649-020-01123-0
[7] KOBAYASHI H, HOSAKA Y, HARA K, et al. Control of selectivity, activity and durability of simple supported nickel catalysts for hydrolytic hydrogenation of cellulose[J]. Green Chemistry,2014,16(2):637−644. doi: 10.1039/C3GC41357H
[8] KANG S, FU J, ZHANG G. From lignocellulosic biomass to levulinic acid: A review on acid-catalyzed hydrolysis[J]. Renewable and Sustainable Energy Reviews,2018,94:340−362. doi: 10.1016/j.rser.2018.06.016
[9] YUAN D, ZHAO N, WANG Y, et al. Dehydration of sorbitol to isosorbide over hydrophobic polymer-based solid acid[J]. Applied Catalysis B: Environmental,2018,240:182−192.
[10] XIN H S, HU X, CAI C L, et al. Catalytic production of oxygenated and hydrocarbon chemicals from cellulose hydrogenolysis in aqueous phase[J]. Frontiers in Chemistry,2020,8:333−353. doi: 10.3389/fchem.2020.00333
[11] ZENG M, PAN X. Insights into solid acid catalysts for efficient cellulose hydrolysis to glucose: Progress, challenges, and future opportunities[J]. Catalysis Reviews,2020(1):445−490.
[12] 赵博, 胡尚连, 龚道勇, 等. 固体酸催化纤维素水解转化葡萄糖的研究进展[J]. 化工进展,2017,36(2):555−567. [ZHAO B, HU S L, GONG D Y, et al. New advances on hydrolysis of cellulose to glucose by solid acid[J]. Progress in Chemical Industry,2017,36(2):555−567. [13] WILLIAM S MOK, ANTAL M J, VARHEGYI G. Productive and parasitic pathways in dilute acid-catalyzed hydrolysis of cellulose[J]. Industrial & Engineering Chemistry Research,1992,31(1):94−100.
[14] 赵燕, 殷伟豪, 李泓泉, 等. 褐藻纤维素稀酸水解工艺优化[J]. 广东化工,2017,44(22):23−24. [ZHAO Y, YIN W H, LI H Q, et al. Optimization of hydrolysis process of algal cellulose dilute acid[J]. Guangdong Chemical Industry,2017,44(22):23−24. doi: 10.3969/j.issn.1007-1865.2017.22.010 [15] FENG D X, LI L Z, FANG Y, et al. Separation of ionic liquid [Mmim] and glucose from enzymatic hydrolysis mixture of cellulose using alumina column chromatography[J]. Applied Microbiology and Biotechnology,2011,91(2):399−405. doi: 10.1007/s00253-011-3263-x
[16] 付霓虹, 袁玉国, 王景芸, 等. 酸性离子液体催化降解纤维素的研究[J]. 应用化工,2016,45(5):908−911. [FU N H, YUAN Y G, WANG J Y, et al. Cellulose degradation catalyzed by acid ionic liquids[J]. Applied Chemical Industry,2016,45(5):908−911. doi: 10.16581/j.cnki.issn1671-3206.20160201.007 [17] MASAAKI, KITANO, DAIZO, et al. Adsorption-enhanced hydrolysis of β-1,4-glucan on graphene-based amorphous carbon bearing SO3H, COOH, and OH groups[J]. Langmuir,2009,25(9):5068−5075. doi: 10.1021/la8040506
[18] RINALDI R, PALKOVITS R, FERDI S. Depolymerization of cellulose using solid catalysts in ionic liquids[J]. Angewandte Chemie International Edition,2008,47(42):8047−8050. doi: 10.1002/anie.200802879
[19] 陆佳, 刘伟, 王欣, 等. 玉米秸秆衍生碳基固体酸的制备及其催化纤维素水解糖化[J]. 化工进展,2020,39(9):3635−3642. [LU J, LIU W, WANG X, et al. Preparation of carbon-based solid acid derived from corn stalk and its catalytic performance in hydrolysis and saccharification of cellulose[J]. Progress in Chemical Industry,2020,39(9):3635−3642. doi: 10.16085/j.issn.1000-6613.2019-1895 [20] QI B, ANH V, RANIL W S, et al. Glucose production from lignocellulosic biomass using a membrane-based polymeric solid acid catalyst[J]. Biomass and Bioenergy,2018,117:137−145. doi: 10.1016/j.biombioe.2018.07.017
[21] SHROTRI A, KOBAYASHI H, FUKUOKA A. Cellulose depolymerization over heterogeneous catalysts[J]. Accounts of Chemical Research,2018,51(3):761−768. doi: 10.1021/acs.accounts.7b00614
[22] 刘阳, 李文志. 苯改性催化剂催化纤维素水解选择性制葡萄糖[J]. 化学工程,2020,48(7):1−5. [LIU Y, LI W Z. Benzene-modified catalyst improving glucose selectivity in cellulose hydrolysis[J]. Chemical Engineering,2020,48(7):1−5. [23] CHUNG P W, CHARMOT A, OLATUNJI-OJO O A, et al. Hydrolysis catalysis of miscanthus xylan to xylose using weak-acid surface sites[J]. Acs Catalysis,2014,4(1):302−310. doi: 10.1021/cs400939p
[24] TO A T, CHUNG P W, KATZ A. Weak-acid sites catalyze the hydrolysis of crystalline cellulose to glucose in water: Importance of post-synthetic functionalization of the carbon surface[J]. Angewandte Chemie,2015,54(38):11050−11053. doi: 10.1002/anie.201504865
[25] BEECK B O D, GEBOERS J, VYVER S V D, et al. Conversion of (ligno) cellulose feeds to isosorbide with heteropoly acids and Ru on carbon[J]. ChemSusChem,2013,6(1):199−208. doi: 10.1002/cssc.201200610
[26] TIAN J, WANG J, ZHAO S, et al. Hydrolysis of cellulose by the heteropoly acid H3PW12O40[J]. Cellulose,2010,17(3):587−594. doi: 10.1007/s10570-009-9391-0
[27] LUO X X, WU H G, LI C H, et al. Heteropoly acid-based catalysts for hydrolytic depolymerization of cellulosic biomass[J]. Frontiers in Chemistry,2020,8:580146−580175. doi: 10.3389/fchem.2020.580146
[28] SUN Z, CHENG M, LI H, et al. One-pot depolymerization of cellulose into glucose and levulinic acid by heteropolyacid ionic liquid catalysis[J]. RSC Advances,2012,2(24):9058−9065. doi: 10.1039/c2ra01328b
[29] ZHANG F, FANG Z. Hydrolysis of cellulose to glucose at the low temperature of 423 K with CaFe2O4-based solid catalyst[J]. Bioresource Technology,2012,124:440−445. doi: 10.1016/j.biortech.2012.08.025
[30] CAIO T, ATSUSHI T, AI I, et al. Highly active mesoporous Nb-W oxide solid-acid catalyst[J]. Angewandte Chemie,2010,49(6):1128−1132. doi: 10.1002/anie.200904791
[31] 隋松泉. 新型Al2O3载体负载的金属和复合金属氧化物催化剂制备, 结构及其催化化性能[D]. 北京: 北京化工大学, 2016. SUI S Q. The preparation and structure of spherical γ-Al2O3 support catalysts and the study of their catalytic performance[D]. Beijing: Beijing University of Chemical Technology, 2016.
[32] MANAENKOV O V, KISLITSA O V, MATVEEVA V G, et al. Cellulose conversion into hexitols and glycols in water: Recent advances in catalyst development[J]. Frontiers in Chemistry,2019,7:834−841. doi: 10.3389/fchem.2019.00834
[33] STIJN V D V, GEBOERS J, JACOBS P A, et al. Recent advances in the catalytic conversion of cellulose[J]. ChemCatChem,2011,3:82−94.
[34] XU S, YAN X, BU Q, et al. Catalytic conversion of cellulose into polyols using carbon-nanotube-supported monometallic Pd and bimetallic Pd–Fe catalysts[J]. Cellulose,2017,24(6):2403−2413.
[35] FUKUOKA A, DHEPE P L. Catalytic conversion of cellulose into sugar alcohols[J]. Angewandte Chemie International Edition,2006,45(31):5161−5163. doi: 10.1002/anie.200601921
[36] LUO C, WANG S, LIU H C. Cellulose conversion into polyols catalyzed by reversibly formed acids and supported Ruthenium clusters in hot water[J]. Angewandte Chemie,2010,119(40):7780−7783.
[37] ADSUAR-GARCÍA M D, FLORES-LASLUISA J X, AZAR F Z. Carbon-black-supported Ru catalysts for the valorization of cellulose through hydrolytic hydrogenation[J]. Catalysts,2018,8(12):572−586. doi: 10.3390/catal8120572
[38] MATVEEVA V G, SULMAN E M, MANAENKOV O V, et al. Hydrolytic hydrogenation of cellulose in subcritical water with the use of the Ru-containing polymeric catalysts[J]. Catalysis Today,2017,280(1):45−50.
[39] REY-RAAP N, RIBEIRO L S, ÓRFÃO J J M, et al. Catalytic conversion of cellulose to sorbitol over Ru supported on biomass-derived carbon-based materials[J]. Applied Catalysis B: Environmental,2019,256:117826−117861. doi: 10.1016/j.apcatb.2019.117826
[40] LUCÍLIA S R, JUAN J D, ÓRFÃO J J M, et al. Influence of the surface chemistry of multiwalled carbon nanotubes on the selective conversion of cellulose into sorbitol[J]. ChemCatChem,2017,9(5):888−896. doi: 10.1002/cctc.201601224
[41] 吕结, 韩金玉, 王华, 等. 焙烧温度对Pt/Al2O3催化剂催化纤维素转化性能的影响[J]. 中国科技论文,2014,9(6):623−627. [LV J, HAN J Y, WANG H, et al. Effect of calcination temperature on catalytic conversion of cellulose over Pt/Al2O3 catalyst[J]. Chinese Scientific Papers,2014,9(6):623−627. doi: 10.3969/j.issn.2095-2783.2014.06.001 [42] HAN J W, LEE H. Direct conversion of cellulose into sorbitol using dual-functionalized catalysts in neutral aqueous solution[J]. Catalysis Communications,2012,19(19):115−118.
[43] 李闯. 纤维素及其平台分子催化氢化研究[D]. 合肥: 中国科学技术大学, 2020. LI C. Studies on the catalytic hydrogenation of cellulose and platform molecule[D]. Hefei: University of Science and Technology of China, 2020.
[44] 李侨光, 刘仕伟, 于世涛. 纤维素制多元醇催化技术研究进展[J]. 林产化学与工业,2015,35(4):145−150. [LI Q G, LIU S W, YU S T. Research progress on catalytic technologies for production of polyols from cellulose[J]. Forest Products Chemistry and Industry,2015,35(4):145−150. doi: 10.3969/j.issn.0253-2417.2015.04.023 [45] LI Z Y, LIU Y, LIU C F, et al. Direct conversion of cellulose into sorbitol catalyzed by a bifunctional catalyst[J]. Bioresource Technology,2018,274:190−197.
[46] LAZARIDIS P A, KARAKOULIA S A, TEODORESCU C, et al. High hexitols selectivity in cellulose hydrolytic hydrogenation over platinum (Pt) vs. ruthenium (Ru) catalysts supported on micro/mesoporous carbon[J]. Applied Catalysis B:Environmental,2017,214(5):1−14.
[47] PALKOVITS R, TAJVIDI K, RUPPERT A, et al. Heteropoly acids as efficient acid catalysts in the one-step conversion of cellulose to sugar alcohols[J]. Chemical Communications,2011,47:576−578. doi: 10.1039/C0CC02263B
[48] ROMERO A, NIETO-MÁRQUEZ A, ALONSO E, et al. Bimetallic Ru: Ni/MCM-48 catalysts for the effective hydrogenation of D-glucose into sorbitol[J]. Applied Catalysis A: General,2017,529(5):49−59.
[49] MARINELLI T, NABUURS S, PONEC V. Activity and selectivity in the reactions of substituted α, β-unsaturated aldehydes[J]. Journal of Catalysis,1995,151(2):431−438. doi: 10.1006/jcat.1995.1045
[50] RIBEIRO L S, DELGADO J J, ÓRFÃO J J M, et al. Carbon supported Ru-Ni bimetallic catalysts for the enhanced one-pot conversion of cellulose to sorbitol[J]. Applied Catalysis B: Environmental,2017,217(15):265−274.
[51] TATHOD A P, PARESH L D. Efficient method for the conversion of agricultural waste into sugar alcohols over supported bimetallic catalysts[J]. Bioresource Technology,2015,178:36−44. doi: 10.1016/j.biortech.2014.10.036
[52] PANG J F, ZHENG M Y, SUN R Y, et al. Selectivity control for cellulose to diols: Dancing on the eggs[J]. ACS Catalysis,2017,7(3):1939−1954. doi: 10.1021/acscatal.6b03469
[53] RIBEIRO L S, ÓRFÃO J, ÓRFÃO J J M, et al. Hydrolytic hydrogenation of cellulose to ethylene glycol over carbon nanotubes supported Ru-W bimetallic catalysts[J]. Cellulose,2018,25(4):2259−2272. doi: 10.1007/s10570-018-1721-7
[54] WIESFELD J J, PEROLJA P, ROLLIER F A, et al. Cellulose conversion to ethylene glycol by tungsten oxide-based catalysts[J]. Molecular Catalysis,2019,473:110400−110410. doi: 10.1016/j.mcat.2019.110400
[55] LI N X, ZHENG Y, WEI L F, et al. Metal nanoparticles supported on WO3 nanosheets for highly selective hydrogenolysis of cellulose to ethylene glycol[J]. Green Chemistry,2017,19(3):682−691. doi: 10.1039/C6GC01327A
-
期刊类型引用(2)
1. 汪小弯,余瑶琪,李瀚,季台隆,南秋利. 生物基多元醇的研究进展. 化工时刊. 2024(05): 34-38 .  百度学术
百度学术
2. 郭建军,王通,吴庆华,曾静,袁林. 镰刀菌YL2产纤维素酶液体发酵工艺优化. 湖南农业科学. 2023(11): 79-86 .  百度学术
百度学术
其他类型引用(2)





 下载:
下载:

 下载:
下载:



