Applied Research for Liquid-phase Chip Detection of Foodborne Salmonella Carrying Plasmid-mediated Quinolone Resistance Genes
-
摘要: 目的:建立应用新型液相芯片技术检测食源性沙门氏菌携带的质粒介导喹诺酮类耐药(PMQR)基因中4种基因:qnrS、aac(6')-Ib-cr、oqxA、oqxB的方法。方法:针对食源性沙门氏菌携带的qnrS、aac(6')-Ib-cr、oqxA、oqxB四种PMQR基因,设计对应引物和微球,采用液相芯片技术对7株标准菌株进行特异性实验;对4株各含1种PMQR基因的食源性沙门氏菌进行重复性和灵敏度实验;然后检测来自食源性风险监测的71株耐喹诺酮类沙门氏菌,和普通PCR进行对比实验。结果:成功建立了液相芯片技术检测食源性沙门氏菌携带的qnrS、aac(6')-Ib-cr、oqxA、oqxB四种PMQR基因的方法,携带qnrS基因的耐药株检出限为5 CFU/mL、携带aac(6')-Ib-cr基因的耐药株检出限为25 CFU/mL、携带oqxA和oqxB基因的耐药株检出限为10 CFU/mL。所有阳性判定结果荧光中位值(MFI)均≥5倍阴性对照组。重复性实验变异系数(CV)均小于5%,特异性实验结果特异性100%,阴性菌株无阳性信号反应。qnrS检出率29.6%(21/71)、aac(6')-Ib-cr 35.2%(25/71)、oqxA 28.2%(20/71)、oqxB 23.9%(17/71),方法比对的结果符合率为100%。结论:实验建立的液相芯片技术检测食源性沙门氏菌质粒介导喹诺酮类耐药基因qnrS、aac(6')-Ib-cr、oqxA、oqxB的方法具有灵敏度高、特异性好、稳定性强、结果准确的特点,可以为食源性沙门氏菌PMQR基因的检测以及耐药性的监控提供技术支撑。Abstract: Objective: To establish a method to detect four genes: qnrS, aac(6')-Ib-cr, oqxA, oqxB, among the plasmid-mediated quinolone resistance (PMQR) genes carried by foodborne Salmonella by applying a novel liquid-phase chip technique. Methods: For the four PMQR genes carried by foodborne Salmonella: qnrS, aac(6')-Ib-cr, oqxA, and oqxB, corresponding primers and microspheres were designed, and liquid-phase microarray technology was used to perform specificity experiments on seven standard strains. Reproducibility and sensitivity experiments were performed on four foodborne Salmonella strains containing one PMQR gene each. 71 quinolone resistant Salmonella strains from foodborne risk monitoring were tested, and a comparison experiment with ordinary PCR was carried out. Results: A method for the detection of four PMQR genes, qnrS, aac(6')-Ib-cr, oqxA and oqxB, in foodborne Salmonella was successfully established by liquid-phase microarray technology. The LOD (limit of detection) of qnrS, aac(6')-Ib-cr, oqxA and oqxB were 5, 25, 10 and 10 CFU/mL respectively. The median fluorescence values (MFI) of all positive determinations were ≥5 times those of the negative control group. The coefficients of variation (CV) of the repeatability experiments were less than 5%. In the specificity experiments, all quinolone resistant Salmonella strains were detected, and no cross-reactivity with other non-target bacteria was observed. The detection rate of qnrS, aac(6')-Ib-cr, oqxA and oqxB were 29.6% (21/71), 35.2% (25/71), 28.2% (20/71), 23.9% (17/71) respectively. The coincidence rate between the liquid chip technology and PCR was 100%. Conclusion: The experimentally established liquid-phase chip technique for the detection of foodborne Salmonella plasmid-mediated quinolone resistance genes qnrS, aac(6')-Ib-cr, oqxA and oqxB is characterized by high sensitivity, good specificity, stability, and accurate results, which can provide technical support for the detection of foodborne Salmonella PMQR genes and the monitoring of drug resistance.
-
近年来,食源性疾病已经成为了全球重视的公共卫生问题,随着21世纪全球化的高速发展,更为频繁的人员往来和更为快捷的物资流通等因素导致了食源性疾病的发病率显著上升[1-3]。在我国食源性疾病感染中最常见的是沙门氏菌,占到发病总数的70%~80%[4-6]。沙门氏菌(Salmonella spp.)是一种常见的人畜共患病原菌,在自然界中主要存在于鸡鸭等禽类和蛋类上,能够引起各类食源性疾病[7-9]。常用的治疗药物是由萘啶酸发展起来的喹诺酮类抗生素[10-12]。然而由于各类抗生素在农业、畜牧业和临床治疗中的滥用,沙门氏菌的耐药性正日益增长,严重影响了对患者的治疗效果[13-15]。综合国内文献报道,目前沙门菌的发展趋势是对喹诺酮及头孢类的耐药性不断增强,多重耐药性上升,耐药谱也不断增宽[16-18]。以往认为沙门氏菌对喹诺酮类的耐药主要由喹诺酮耐药决定区(Quinolone resistance-determining region,QRDR)的靶位改变和主动外排所致,两者均由染色体介导。近期研究认为,质粒介导的喹诺酮耐药(Plasmid-mediated quinolone resistance,PMQR)是沙门氏菌耐药性传播的主要途径,拥有在不同细菌中迅速水平传播的能力从而导致更大范围的流行[19-21]。现已报道的PMQR类基因主要分为3类:qnr家族、aac(6')-Ib-cr基因簇和喹诺酮类药物特异性外排泵基因oqxAB、qep系列。其中qnr家族(包含qnrA、qnrB、qnrC、qnrD、qnrS)编码QNR蛋白,该蛋白能保护DNA回旋酶和拓扑异构酶Ⅳ不受喹诺酮类的抑制;aac(6')-Ib基因编码氨基乙酰化酶,通过对喹诺酮类(诺氟沙星、环丙沙星)哌嗪环上氨基氮原子的乙酰化而介导低水平耐药;oqxA、oqxB、qepA则编码质粒介导的外排泵,通过对亲水性喹诺酮类药物的外排而介导低水平耐药[22]。由于PMQR常和其它类型的耐药基因共同存在于同一个质粒上,往往会造成携带该质粒的菌株表现出多重耐药[23-24]。所有这些都必然对人类和动物的健康造成严重威胁。
对于沙门氏菌PMQR基因的检测,主要还是使用传统的PCR方法检测[22-25]。迄今尚无标准化试剂,存在着操作复杂、步骤繁多、耗时漫长等缺点,导致实际应用受到限制。液相芯片(Liquid chip)又称为多功能悬浮阵列(Multi-analyte suspension array,MASA)或高通量悬浮阵列(High-throughput suspension array),是融合了包括激光点阵技术、免疫分析技术、流式细胞技术、荧光编码微球技术、高速数字信号处理技术及高通量分析于一体的新型生物分子检测技术。其核心技术主要包含xMAP技术[26-27]和xTAG技术[28-29]。xMAP技术是利用特定的荧光染色微球,修饰以不同的抗体或探针,可用于蛋白与核酸检测,又被称为流式荧光杂交法(Flexible multi-analyte profiling technology)。xTAG技术则是在微球上采用特定的anti-TAG标签序列修饰,与待检样本中加入的TAG序列进行特异性配对结合。因此相较传统方法具有高通量、高速度、高灵敏度等优点。
目前,使用液相芯片技术检测食源性沙门氏菌PMQR基因的研究国内尚未见报道。所以本实验室拟用以液相芯片技术为核心的Luminex 200检测平台,根据相关资料设计能够特异性捕获和扩增目标的MagPlex-TAG微球及引物,用于食源性风险监测中沙门氏菌PMQR基因的检测,并对其重复性、特异性、灵敏度进行验证,以期建立液相芯片技术检测食源性沙门氏菌PMQR基因的新方法。根据国内外相关文献PMQR类基因的检出情况,qnrA、qnrB、qnrC、qnrD、qepA检出率相对偏低[30-34],结合2012~2021年常州地区食源性风险监测沙门氏菌喹诺酮类耐药株的检测结果,最终选择常州地区实际检出率较高的qnrS、aac(6')-Ib-cr、oqxA、oqxB这4种耐药基因进行检测研究。本实验将为食源性沙门氏菌的PMQR基因和其他致病菌耐药基因的检测提供新的方法、思路和实验数据,今后也将为食源性风险监测工作以及哨点医院致病菌耐药性传播的监测提供更好的技术支持,具有重要的社会意义。
1. 材料与方法
1.1 材料与仪器
2012~2021年常州地区食源性风险监测共分离沙门菌株287株 根据江苏省食源性风险监测工作手册,菌株编号模式3204020220XX00XXX。通过药敏实验(微量肉汤法)检出71株沙门氏菌耐喹诺酮类药物(环丙沙星和(或)萘啶酸),其中来自食物样本的菌株18株,来自哨点医院腹泻病例的菌株53株。经PCR扩增耐药基因片段后送苏州金唯智生物科技有限公司测序,其中含qnrS耐药基因的有21株、含aac(6')-Ib-cr耐药基因的有25株、含oqxA耐药基因的有20株、含oqxB耐药基因的有17株。所有菌株均经过全自动微生物检测系统VITEK2生化反应确认并进行了血清分型。质控菌株大肠埃希菌(ATCC25922)、肺炎克雷伯杆菌(ATCC700603)、金黄色葡萄球菌(ATCC25923)、单核细胞增生李斯特氏菌(ATCC19114)、副溶血性弧菌(ATCC17802)、肠炎沙门氏菌(ATCC9270)、鼠伤寒沙门氏菌(ATCC14028) 由梅里埃中国有限公司提供;普通营养琼脂培养基 上海科玛嘉生物技术有限公司;QIAGEN® HotStarTaq Master Mix 凯杰核酸扩增预混液 凯杰(上海)生物科技有限公司;上述所有试剂均在有效期内,实验室的无菌室温度保持16~24 ℃,湿度保持30%~60%,孵室温度保持37 ℃。本实验室每年均通过中国疾病预防控制中心营养与食品安全所组织的实验室能力验证考核。
VITEK2 COMPACT 30 全自动微生物鉴定及药敏系统 梅里埃中国有限公司;AIM+Vizion 全自动药敏试验菌液接种判读仪、Veriti PCR 热循环仪 赛默飞世尔中国有限公司;路明克斯Luminex 200 液相芯片分析系统 美国路明克斯中国有限公司;定量质控菌株磁珠 美正生物科技有限公司。
1.2 实验方法
1.2.1 液相芯片技术引物设计和微球选择
4对耐药基因的特异性引物在Genbank数据库中下载对应的特异性靶基因序列(qnrS ID: MT335864.1、aac(6')-Ib-cr ID: JX457478.1、oqxAB ID: KM877269.1),使用引物设计软件Primer 5.0分别进行设计,选择分数较高,无引物二聚体和发夹结构的引物组。通过BLAST确保不同引物对之间没有同源关系,且基因片段大小控制在200 bp左右,在保证特异性的同时,防止片段过长而降低与微球的杂交效率。然后在设计好的特异性引物上游的5’前端添加一个和MagPlex-TAG微球互补的标签,中间用碳桥连接;下游的5’前端添加一个生物素,这样可以在保证复性温度和杂交效率的同时有效地避免不同检测物标记的微球之间的相互杂交[35-36],最后交由上海生工合成,采用HDLC纯化。
特异性的MagPlex-TAG微球选择参考国家标准GB/T 19495.9-2017转基因产品检测 植物产品液相芯片检测技术和Luminex 200检测平台的使用说明手册(4 th Edit xMAPCookbook)以及相关文献资料[37-38],采用目标特异性PCR序列检测方法(Target-Specific PCR Sequence Detection with Mag Plex-TAG Microspheres),将相应引物序列输入路明克斯公司数据库,由Luminex TagIt®设计确定,得到合适的微球编号。这些表面带有anti-标签的微球将能够和相应的扩增产物高效特异性的结合。特异性引物和微球对应编号见表1。
表 1 特异性引物和对应微球编号Table 1. Specific primers and corresponding microsphere numbers基因名称 引物序列(5’-3’) 扩增片段(bp) 微球编号 qnrS F: TTAACAACTTATACAAACACAAAC/iSp12/
ACGACATTCGTCAACTGCAAR: Biotin/CGATTACTCACTTGATGGGC 212 MTAG-A053 aac(6')-Ib-cr F: AACTTTCTCTCTCTATTCTTATTT/iSp12/
TTGCGATGCTCTATGAGTGGCTAR: Biotin/ATACCCAATCGGCTCTCCAT 170 MTAG-A043 oqxA F: TACTTCTTTACTACAATTTACAAC/iSp12/
GATCAGTCAGTGGGATAGTTTR: Biotin/GCGCGATAGGTTCTGTCATC 162 MTAG-A015 oqxB F: CTATCATTTATCTCTTTCTCAATT/iSp12/
TTCTCCCCCGGCGGGAAGTACR: Biotin/GGCAGCGACCTTATTGGGAT 162 MTAG-A072 1.2.2 液相芯片技术扩增PMQR基因
DNA提取采用热裂解法。扩增反应使用QIAGEN® HotStar Taq Master Mix,根据Mix使用说明预设,总反应体系设置为25 μL,其中Mix 12.5 μL,水8 μL,上下游引物(浓度10 μmol/L)各1.25 μL,样本DNA 2.0 μL,加样全程需在冰盒上进行以保持温度。加好样后放入Veriti PCR热循环仪,扩增条件设置:95 ℃预变性15 min;94 ℃变性30 s,退火57 ℃ 60 s,72 ℃延伸90 s,共30个循环;然后72 ℃延伸10 min,全部完成后保持4 ℃。最终得到的扩增片段产物,则进行下一步微球杂交和荧光染色。
1.2.3 液相芯片技术微球杂交和染色
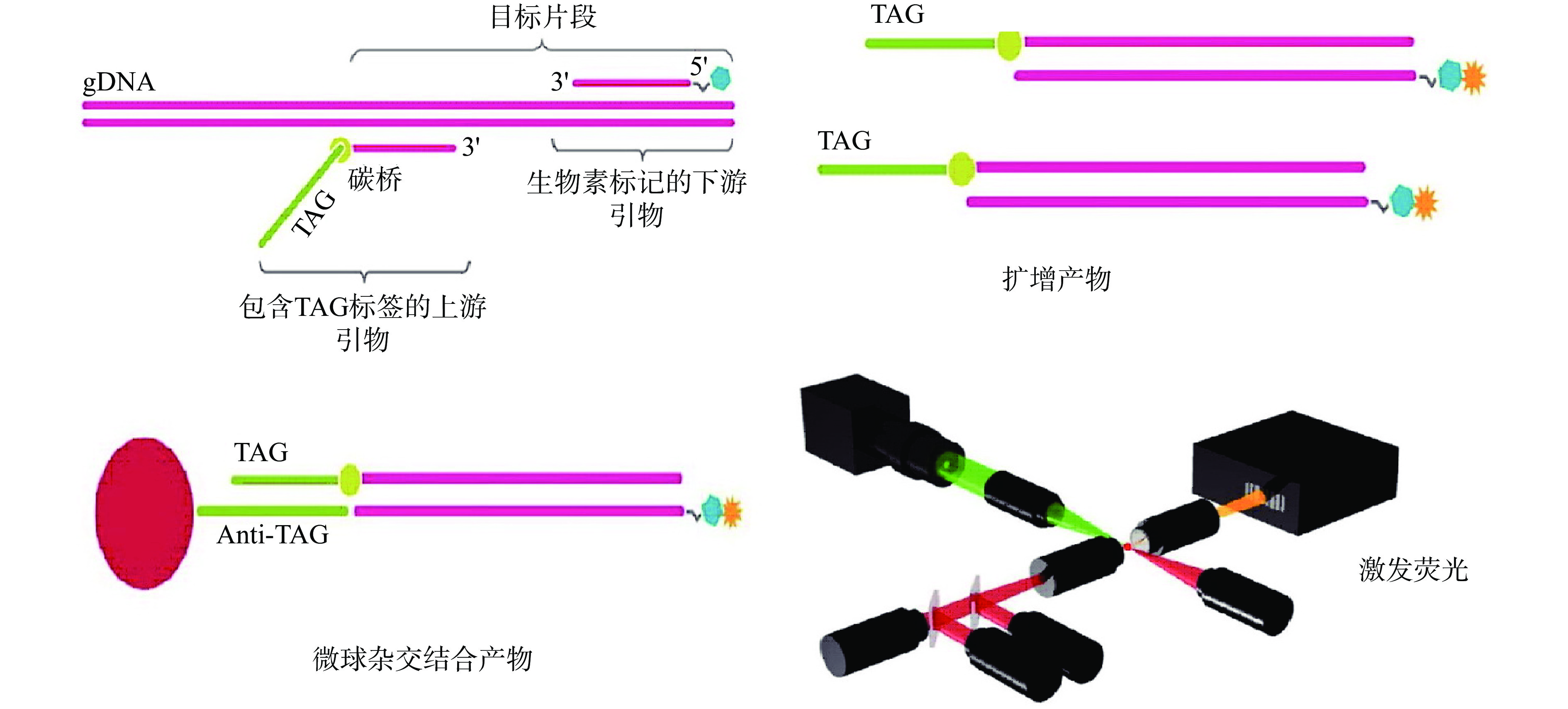
将扩增后的DNA产物和微球杂交,设置50 μL的反应体系:45 μL微球+5 μL PCR产物,同时增加一个空白阴性对照,作为检测数据的背景值。加样完成后放入Veriti PCR热循环仪,微球杂交条件设置如下:95 ℃ 5 min,52 ℃ 30 min,52 ℃ hold。杂交结束后进行荧光染色,将Luminex 200液相芯片分析系统提前预热至52 ℃。每孔样本加入50 μL链霉亲和素-R-藻红蛋白(Streptavidin, R-Phycoerythrin Conjugate, SA-PE),然后放入路明克斯Luminex 200液相芯片分析系统,保持52 ℃ 10 min,运行程序xPONENT,进行数据读取,得到中位荧光强度(MFI)。依照Luminex 200检测平台的使用说明手册,当样本的MFI值大于等于阴性背景值5倍以上时判定为阳性。其基本原理流程见图1。
1.2.4 液相芯片技术检测特异性实验
选取7株常见无PMQR基因的质控菌株:大肠埃希菌、肺炎克雷伯杆菌、金黄色葡萄球菌、单核细胞增生李斯特氏菌、副溶血性弧菌、肠炎沙门氏菌、鼠伤寒沙门氏菌。采用液相芯片技术进行检测,所有菌株检测3次。用以验证该方法对非喹诺酮类耐药菌株有无检测信号。
1.2.5 液相芯片技术检测重复性实验
采用液相芯片技术检测方法,从江苏省食源性风险监测喹诺酮类耐药菌株(见1.1)中选取4株各含单个PMQR基因的沙门氏菌:32040202201500024(qnrS阳性)、32040202201200018(aac(6')-Ib-cr阳性)、32040203201300015(oqxA阳性)、32040203201900107(oqxB阳性),进行重复性验证,每株菌检测3次,用以验证该方法的重复性和稳定性。
1.2.6 液相芯片技术检测灵敏度实验
将以上4株含PMQR基因的沙门氏菌(见1.2.5),送至美正生物科技有限公司制成BioBall定量标准菌株,然后在实验室进行目标梯度稀释。无菌操作取一粒BioBall(−30 ℃保存,100 CFU/个),置于1000 μL复苏液中,振荡5 s混匀,分别吸取10、50、100、250 μL复苏液,然后对应加入990、950、900、750 μL无菌水混匀,制成1、5、10、25 CFU/mL这4个浓度的菌悬液,同时采用ATP即时检测和平板培养计数进行平行质控,以保证菌悬液浓度正确。每个稀释度取1 mL提取模板DNA。采用液相芯片技术检测方法检测,每个稀释度需检测3次,用于验证该方法的灵敏度。
1.2.7 液相芯片技术检测对比实验
采用液相芯片技术检测与常规PCR两种方法对食源性风险监测的 71 株耐喹诺酮类沙门氏菌的上述 4 类 PMQR 基因进行对比检测,用于验证该方法与传统方法的差异。常规PCR产物测序交由苏州金唯智生物科技有限公司进行。
1.3 数据处理
特异性引物设计使用Primer 5.0软件,BLAST比对使用Genbank数据库,液相芯片荧光中位值结果的数据处理分析由系统自带的xPONENT(3.1.971.0)完成,最后结果采用Microsoft Excle 2010进行常规统计学分析处理。
2. 结果与分析
2.1 液相芯片技术检测的特异性实验结果
由表2可知,使用液相芯片技术检测7株无PMQR基因的标准菌株,结果所有样本检测的中位荧光强度(MFI)均<300,变异系数<5%,判定为阴性,证实该方法对无PMQR基因的5种常见菌株和2种不携带PMQR基因的标准沙门氏菌血清型无阳性检测信号,特异性为100%,符合国内文献报道的高特异性[39]。
表 2 液相芯片技术特异性实验结果Table 2. Experimental results of specificity of liquid chip technology菌株 目标基因(微球编码) 中位荧光强度(MFI) 平均值(m±s.d) CV(%) 背景值 大肠埃希菌(ATCC25922) qnrS(A053) 120 123 126 123.0±3.0 2 110.5 aac(6')-Ib-cr(A043) 133 141 139 137.7±4.2 3 124 oqxA(A015) 98 95 101.5 98.2±3.3 3 100.5 oqxB(A072) 107 103 111 107.0±4.0 4 99 肺炎克雷伯杆菌(ATCC700603) qnrS(A053) 219 231 238 229.3±9.6 4 230 aac(6')-Ib-cr(A043) 241 255 263 253.0±11.1 4 209 oqxA(A015) 212 230 218 220.0±9.2 4 214 oqxB(A072) 261 249 251 253.7±6.4 3 250 金黄色葡萄球菌(ATCC25923) qnrS(A053) 264 270.5 284 272.8±10.2 4 261 aac(6')-Ib-cr(A043) 266 257.5 251 258.2±7.5 3 259 oqxA(A015) 271 260 276 269.0±8.2 3 257 oqxB(A072) 255.5 263 259 259.2±3.8 1 249 单核细胞增生李斯特氏菌(ATCC19114) qnrS(A053) 218 234 229 227.0±8.2 4 203.5 aac(6')-Ib-cr(A043) 235 244 251 243.3±8.0 3 231 oqxA(A015) 253 241 260.5 251.5±9.8 4 239 oqxB(A072) 233 246.5 251 243.5±9.4 4 227 副溶血性弧菌(ATCC17802) qnrS(A053) 126 135 132 131.0±4.6 3 133.5 aac(6')-Ib-cr(A043) 133 129 140 134.0±5.6 4 129 oqxA(A015) 109 105 114 109.3±4.5 4 107 oqxB(A072) 118 125 129 124.0±5.6 4 118 肠炎沙门氏菌(ATCC9270) qnrS(A053) 132 130 124 128.7±4. 2 3 128.5 aac(6')-Ib-cr(A043) 151 160 149 153.0±5.9 4 154 oqxA(A015) 162 153.5 165 160.2±6.0 4 162.5 oqxB(A072) 137 128 135.5 133.5±4.8 4 132.5 鼠伤寒沙门氏菌(ATCC14028) qnrS(A053) 150 139 144 144.3±5.5 4 138 aac(6')-Ib-cr(A043) 147.5 150 142 146.5±4.1 3 140.5 oqxA(A015) 138 142 131 137.0±5.6 4 135 oqxB(A072) 149 155 162 155.3±6.5 4 151 2.2 液相芯片技术检测的重复性实验结果
重复性检测的实验结果见表3,阳性样本中位荧光强度(MFI)均远超液相芯片系统要求的阴性背景值5倍以上,变异系数(CV)均<5%,说明本方法具有良好的可重复性,和国内相关文献描述一致[40]。
表 3 液相芯片技术重复性实验结果Table 3. Experimental results of repeatability of liquid chip technology菌株 目标基因(微球编码) 中位荧光强度(MFI) 平均值(s.d) CV(%) 背景值 qnrS阳性沙门菌(32040202201500024) qnrS(A053) 5148.5 5259 5367 5258.2±109.3 2 170 aac(6')-Ib-cr(A043) 170 164 173.5 169.2±4.8 3 154 oqxA(A015) 153 159 148 153.3±5.5 4 139 oqxB(A072) 177 180 168 175.0±6.2 4 167 aac(6')-Ib-cr阳性沙门菌(32040202201200018) qnrS(A053) 136 132 143 137.0±5.6 4 124 aac(6')-Ib-cr(A043) 3562 3643 3709 3638.0±73.7 2 154.5 oqxA(A015) 141 154 147 147.3±6.5 4 163.5 oqxB(A072) 140 135 144 139.7±4.5 3 111 oqxA阳性沙门菌(32040203201300015) qnrS(A053) 157 161 169 162.3±6.1 4 149 aac(6')-Ib-cr(A043) 153 156 160 156.3±3.5 2 142 oqxA(A015) 4854 4717 4933 4834.7±109.3 2 162.5 oqxB(A072) 169 164 159 164.0±5.0 3 160 oqxB阳性沙门菌(32040203201900107) qnrS(A053) 159 167.5 171 165.8±6.2 4 159.5 aac(6')-Ib-cr(A043) 163.5 167.5 177 169.3±6.9 4 154 oqxA(A015) 154 157.5 148 153.2±4.8 3 145 oqxB(A072) 4329 4368 4414.5 4370.5±42.8 1 181 2.3 液相芯片技术检测的灵敏度实验结果
稀释度设定参考国内文献资料,定为25、10、5和1 CFU/mL一共4个浓度[41-42],结果见表4。qnrS检出限为5 CFU/mL、aac(6')-Ib-cr检出限为25 CFU/mL、oqxA检出限为10 CFU/mL、oqxB检出限为10 CFU/mL。目标基因的最低检出限为5 CFU/mL,比史贇学等[41]的1 CFU/mL略高,最高检出限为25 CFU/mL,比伍业健等[42]的100 CFU/mL低,总体灵敏度符合预期。
表 4 液相芯片技术灵敏度实验结果Table 4. Experimental results of sensitivity of liquid phase chip technology菌株编号 目标基因(微球编码) 菌悬液浓度(CFU/mL) 中位荧光强度(MFI) 平均值(s.d) CV(%) 背景值 qnrS阳性沙门菌
(32040202201500024)qnrS(A053) 25 5013.5 5140 5226 5126.5±106.9 2 152.5 10 3726.5 3849 3617 3730.8±116.1 3 146 5 1342 1367 1349 1352.7±12.9 1 153 1 174.5 168 181 174.5±6.5 4 147 aac(6')-Ib-cr阳性沙门菌
(32040202201200018)aac(6')-Ib-cr(A043) 25 1435 1466 1508 1469.7±36. 7 2 105 10 346.5 332 350 342.8±9.5 3 171 5 261.5 242 254 252.5±9.8 4 144 1 113.5 109 119 113.8±5.0 4 107 oqxA阳性沙门菌
(32040203201300015)oqxA(A015) 25 3956 3856 3789 3867.0±84.0 2 108.5 10 1731.5 1822 1793.5 1782.3±46.3 3 119 5 357.5 347 332 345.5±12.8 4 122 1 108.5 118 113 113.2±4.8 4 105.5 oqxB阳性沙门菌
(32040203201900107)oqxB(A072) 25 4005.5 4103 4138 4082.2±68.7 2 163.5 10 1653.5 1589 1656 1632.8±38.0 2 138 5 345.5 363 333 347.2±15.1 4 125 1 117 120 114 117.0±3.0 3 116 2.4 液相芯片技术检测的对比实验结果
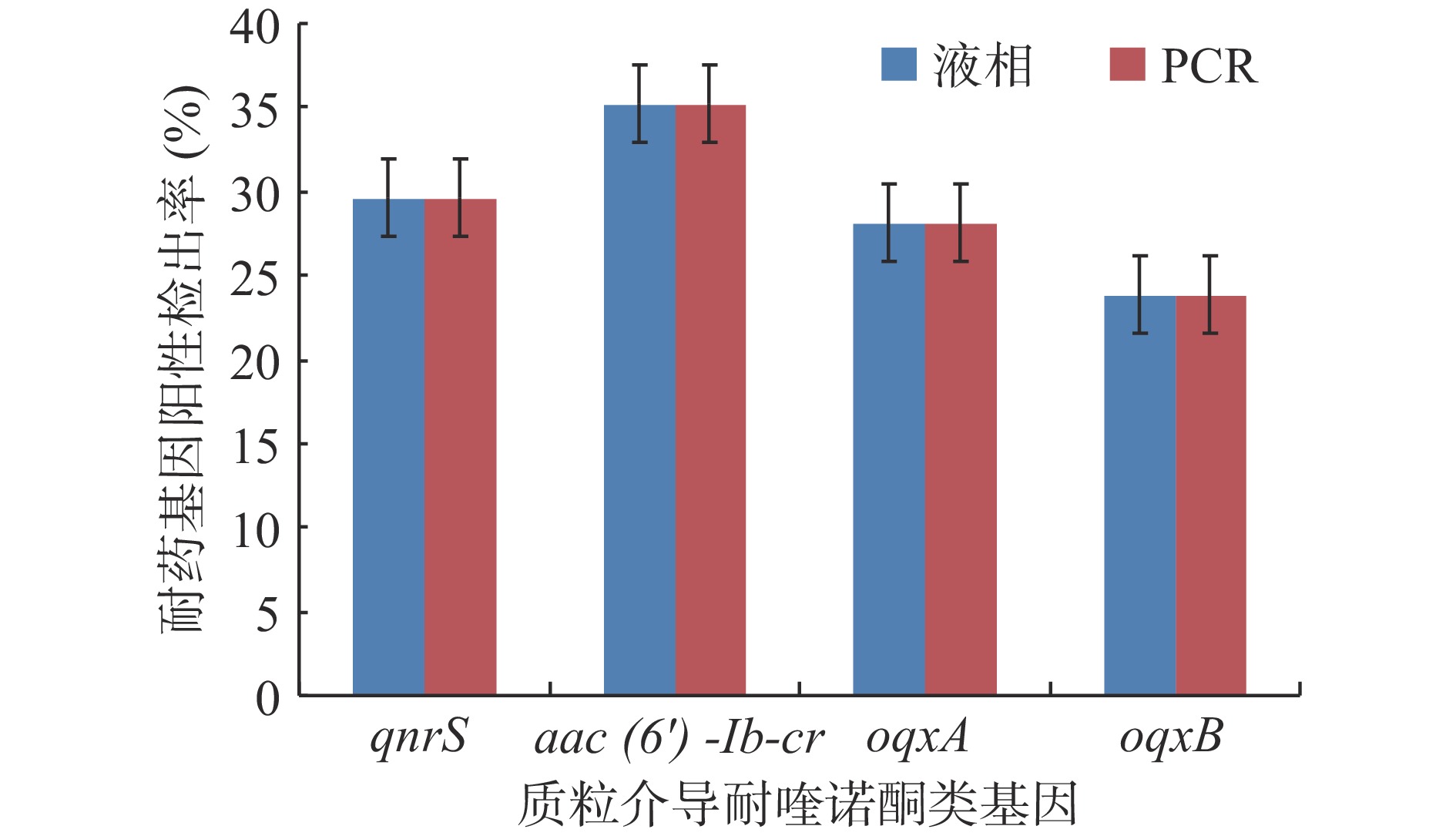
71株食源性沙门氏菌喹诺酮类耐药株的4对PMQR基因(qnrS、aac(6')-Ib、oqxA、oqxB),使用液相芯片技术检测的判定结果(MFI值大于等于阴性背景值5倍以上时判定为阳性)和普通PCR结果完全相同,qnrS检出率29.6%(21/71)、aac(6')-Ib-cr检出率35.2%(25/71)、oqxA检出率28.2%(20/71)、oqxB检出率23.9%(17/71),对目标基因以外的耐药基因无信号反应,两种方法符合率100%,见图2,达到了实验预期,也和国内报道的液相芯片技术相关应用实验数据相同[43]。
3. 讨论与结论
食源性风险监测已经成为我国食品安全保障体系的重要部分,为了保障广大人民群众的身体健康和生命安全,提高对食源性疾病的监测预警能力,迫切需要加强对食源性致病因子检测能力的建设。本次实验所使用的沙门氏菌耐药株,来源于2012~2021年间的食源性风险监测样本,种类包含生禽畜肉,养殖场环境,医院腹泻标本等,较为复杂。实验室仍主要依据风险监测手册上的传统方法如微量肉汤法进行耐药性检测,需要定时定量培养。耐药基因检测使用常规PCR,需要脉冲场凝胶电泳和测序,一定程度上存在步骤繁琐、检测困难等问题,需要进一步改进和提高。
本次实验,利用液相芯片检测技术建立了食源性沙门氏菌PMQR基因中4种常见基因qnrS、aac(6')-Ib、oqxA、oqxB的检测方法。并对新方法的特异性、重复性、灵敏度和准确性进行了验证。结果显示该方法的结果稳定、重复性好、中位荧光强度(MFI)变异系数均小于5%。特异性高,阴性样本无阳性信号,且整体实验过程中背景值信号极低,不到阳性信号值的十分之一,干扰因素对实验影响较弱,这和其他文献报道的结果一致[44-45]。因为结合了流式细胞仪技术和xMAP荧光技术及xTAG标签微球技术,检测灵敏度最高达到5 CFU/mL,已经达到《GB 4789.4食品安全国家标准 食品微生物学检验 沙门氏菌检验》的最低检出限1~10 CFU/mL要求[46]。准确性试验结果表明,和普通PCR的检测结果符合率达到100%,具有很强的实用性和可替代性。整个实验过程提取DNA+杂交+染色上机不超过6 h,且具有直观的数字结果,相对传统方法极大的提高了效率。同时新方法具有高通量的特点[47-48],可以一次检测96孔,进一步提高了速度,解决了传统检测方法存在的复杂耗时,自动化程度低的问题。这对于耐药基因的快速检测乃至食源性致病因子的大范围预防性监测,都具有重要的研究意义和广阔的发展前景。
本次实验已经证实了引物设计原理的正确性和液相芯片检测技术用于沙门氏菌PMQR基因检测的可行性,实验中所有阳性判定结果荧光中位值(MFI)均远超仪器要求的5倍阴性背景值,达到了10倍以上。方法最低检出限为携带qnrS基因菌株的5 CFU/mL,重复性实验变异系数(CV)均小于5%,特异性100%。方法比对符合率为100%,实验结果符合预期。
根据液相芯片检测技术原理和相关文献资料,它的微球上可以结合各种特异性标签,三种荧光染料最多可以分辨500种不同的微球,理论上一个样品可以实现500种独立的生物检测[49-51],因此接下来将尝试研究和优化直接从样本而非纯菌株中检测沙门氏菌多重PMQR基因的方法,进一步提高液相芯片检测技术的覆盖范围。目前液相芯片检测技术存在的缺点主要是试剂较为昂贵且依赖进口,仪器和耗材的保存条件苛刻。相信今后随着国内外液相芯片检测系统的普及[52-54]和相关仪器耗材的价格下降,该技术在食源性风险监测、哨点医院耐药菌监测、临床检验、生化分析等领域都将迎来新的发展和应用的高峰。
-
表 1 特异性引物和对应微球编号
Table 1 Specific primers and corresponding microsphere numbers
基因名称 引物序列(5’-3’) 扩增片段(bp) 微球编号 qnrS F: TTAACAACTTATACAAACACAAAC/iSp12/
ACGACATTCGTCAACTGCAAR: Biotin/CGATTACTCACTTGATGGGC 212 MTAG-A053 aac(6')-Ib-cr F: AACTTTCTCTCTCTATTCTTATTT/iSp12/
TTGCGATGCTCTATGAGTGGCTAR: Biotin/ATACCCAATCGGCTCTCCAT 170 MTAG-A043 oqxA F: TACTTCTTTACTACAATTTACAAC/iSp12/
GATCAGTCAGTGGGATAGTTTR: Biotin/GCGCGATAGGTTCTGTCATC 162 MTAG-A015 oqxB F: CTATCATTTATCTCTTTCTCAATT/iSp12/
TTCTCCCCCGGCGGGAAGTACR: Biotin/GGCAGCGACCTTATTGGGAT 162 MTAG-A072 表 2 液相芯片技术特异性实验结果
Table 2 Experimental results of specificity of liquid chip technology
菌株 目标基因(微球编码) 中位荧光强度(MFI) 平均值(m±s.d) CV(%) 背景值 大肠埃希菌(ATCC25922) qnrS(A053) 120 123 126 123.0±3.0 2 110.5 aac(6')-Ib-cr(A043) 133 141 139 137.7±4.2 3 124 oqxA(A015) 98 95 101.5 98.2±3.3 3 100.5 oqxB(A072) 107 103 111 107.0±4.0 4 99 肺炎克雷伯杆菌(ATCC700603) qnrS(A053) 219 231 238 229.3±9.6 4 230 aac(6')-Ib-cr(A043) 241 255 263 253.0±11.1 4 209 oqxA(A015) 212 230 218 220.0±9.2 4 214 oqxB(A072) 261 249 251 253.7±6.4 3 250 金黄色葡萄球菌(ATCC25923) qnrS(A053) 264 270.5 284 272.8±10.2 4 261 aac(6')-Ib-cr(A043) 266 257.5 251 258.2±7.5 3 259 oqxA(A015) 271 260 276 269.0±8.2 3 257 oqxB(A072) 255.5 263 259 259.2±3.8 1 249 单核细胞增生李斯特氏菌(ATCC19114) qnrS(A053) 218 234 229 227.0±8.2 4 203.5 aac(6')-Ib-cr(A043) 235 244 251 243.3±8.0 3 231 oqxA(A015) 253 241 260.5 251.5±9.8 4 239 oqxB(A072) 233 246.5 251 243.5±9.4 4 227 副溶血性弧菌(ATCC17802) qnrS(A053) 126 135 132 131.0±4.6 3 133.5 aac(6')-Ib-cr(A043) 133 129 140 134.0±5.6 4 129 oqxA(A015) 109 105 114 109.3±4.5 4 107 oqxB(A072) 118 125 129 124.0±5.6 4 118 肠炎沙门氏菌(ATCC9270) qnrS(A053) 132 130 124 128.7±4. 2 3 128.5 aac(6')-Ib-cr(A043) 151 160 149 153.0±5.9 4 154 oqxA(A015) 162 153.5 165 160.2±6.0 4 162.5 oqxB(A072) 137 128 135.5 133.5±4.8 4 132.5 鼠伤寒沙门氏菌(ATCC14028) qnrS(A053) 150 139 144 144.3±5.5 4 138 aac(6')-Ib-cr(A043) 147.5 150 142 146.5±4.1 3 140.5 oqxA(A015) 138 142 131 137.0±5.6 4 135 oqxB(A072) 149 155 162 155.3±6.5 4 151 表 3 液相芯片技术重复性实验结果
Table 3 Experimental results of repeatability of liquid chip technology
菌株 目标基因(微球编码) 中位荧光强度(MFI) 平均值(s.d) CV(%) 背景值 qnrS阳性沙门菌(32040202201500024) qnrS(A053) 5148.5 5259 5367 5258.2±109.3 2 170 aac(6')-Ib-cr(A043) 170 164 173.5 169.2±4.8 3 154 oqxA(A015) 153 159 148 153.3±5.5 4 139 oqxB(A072) 177 180 168 175.0±6.2 4 167 aac(6')-Ib-cr阳性沙门菌(32040202201200018) qnrS(A053) 136 132 143 137.0±5.6 4 124 aac(6')-Ib-cr(A043) 3562 3643 3709 3638.0±73.7 2 154.5 oqxA(A015) 141 154 147 147.3±6.5 4 163.5 oqxB(A072) 140 135 144 139.7±4.5 3 111 oqxA阳性沙门菌(32040203201300015) qnrS(A053) 157 161 169 162.3±6.1 4 149 aac(6')-Ib-cr(A043) 153 156 160 156.3±3.5 2 142 oqxA(A015) 4854 4717 4933 4834.7±109.3 2 162.5 oqxB(A072) 169 164 159 164.0±5.0 3 160 oqxB阳性沙门菌(32040203201900107) qnrS(A053) 159 167.5 171 165.8±6.2 4 159.5 aac(6')-Ib-cr(A043) 163.5 167.5 177 169.3±6.9 4 154 oqxA(A015) 154 157.5 148 153.2±4.8 3 145 oqxB(A072) 4329 4368 4414.5 4370.5±42.8 1 181 表 4 液相芯片技术灵敏度实验结果
Table 4 Experimental results of sensitivity of liquid phase chip technology
菌株编号 目标基因(微球编码) 菌悬液浓度(CFU/mL) 中位荧光强度(MFI) 平均值(s.d) CV(%) 背景值 qnrS阳性沙门菌
(32040202201500024)qnrS(A053) 25 5013.5 5140 5226 5126.5±106.9 2 152.5 10 3726.5 3849 3617 3730.8±116.1 3 146 5 1342 1367 1349 1352.7±12.9 1 153 1 174.5 168 181 174.5±6.5 4 147 aac(6')-Ib-cr阳性沙门菌
(32040202201200018)aac(6')-Ib-cr(A043) 25 1435 1466 1508 1469.7±36. 7 2 105 10 346.5 332 350 342.8±9.5 3 171 5 261.5 242 254 252.5±9.8 4 144 1 113.5 109 119 113.8±5.0 4 107 oqxA阳性沙门菌
(32040203201300015)oqxA(A015) 25 3956 3856 3789 3867.0±84.0 2 108.5 10 1731.5 1822 1793.5 1782.3±46.3 3 119 5 357.5 347 332 345.5±12.8 4 122 1 108.5 118 113 113.2±4.8 4 105.5 oqxB阳性沙门菌
(32040203201900107)oqxB(A072) 25 4005.5 4103 4138 4082.2±68.7 2 163.5 10 1653.5 1589 1656 1632.8±38.0 2 138 5 345.5 363 333 347.2±15.1 4 125 1 117 120 114 117.0±3.0 3 116 -
[1] 陆姣, 王晓莉, 吴林海. 国内外食源性疾病防控的研究进展[J]. 中华疾病控制杂志,2017,21(2):196−197. [LU Jiao, WANG Xiaoli, WU Linhai. The progress of foodborne disease prevention and control in the world[J]. Chinese Journal of Disease Control,2017,21(2):196−197. [2] Food Standards Agency. The FSA foodborne disease strategy 2010-15 (England)[M]. London: Food Standars Agency, 2011: 4−5.
[3] 苏丹萍, 吴云凤. 食源性致病菌风险评估研究进展[J]. 食品安全质量检测学报,2020,11(18):6515−6517. [SU Danping, WU Yunfeng. Research advances in risk assessment of food-borne pathogen[J]. Journal of Food Safety and Quality,2020,11(18):6515−6517. [4] 翁蕊, 辜依海, 张微. 食源性沙门菌流行趋势及耐药性研究进展[J]. 食品安全质量检测学报,2021,12(9):3543−3545. [WENG Rui, GU YiHai, ZHANG Wei. Research progress on epidemic trend and antimicrobial resistance research of foodborne Salmonella[J]. Journal of Food Safety and Quality,2021,12(9):3543−3545. [5] 梁莹, 杜潇利, 张妹中, 等. 综合医院食源性疾病病原学监测结果分析[J]. 中国公共卫生管理,2021,37(1):102−104. [LIANG Ying, DU Xiaoli, ZHANG Meizhong, et al. Analysis of surveillance results of foodborne disease etiology in a comprehensive hospital[J]. Chinese Journal of Public Health Management,2021,37(1):102−104. [6] 肖巍, 李想, 罗君. 2018-2020年河南省开封市儿童食源性沙门氏菌感染监测分析[J]. 河南预防医学杂志,2022,33(5):397−398. [XIAO Wei, LI Xiang, LUO Jun. Surveillance and analysis of foodborne Salmonella infection among children in Kaifeng city of Henan province from 2018 to 2020[J]. Henan Journal of Preventive Medicine,2022,33(5):397−398. [7] 毛旭建, 屠博文, 薛银刚, 等. 食源与人源性沙门氏菌的血清和耐药水平差异分析[J]. 公共卫生与预防医学,2021,32(3):63−65. [MAO Xujian, TU Bowen, XUE Yingang, et al. Analysis of serum and drug resistance levels between food source and human Salmonella[J]. Journal Public Health and Preventive Medicine,2021,32(3):63−65. doi: 10.3969/j.issn.1006-2483.2021.03.015 [8] ERKMEN O. Isolation and counting of Salmonella[J]. Microbiological Analysis of Foods and Food Processing Environments,2022:151−167.
[9] 李光辉, 高雪丽, 郭卫芸, 等. 1996—2015年间沙门氏菌食物中毒事件特征分析[J]. 食品工业,2018(5):259−261. [LI Guanghui, GAO Xueli, GUO Weiyun, et al. Analysis on characteristics of Salmonella food poisoning events from 1996 to 2015[J]. The Food Industry,2018(5):259−261. [10] 刘书宏. 鲜肉源沙门氏菌优势血清型的基因分型与喹诺酮类耐药性及其基因的研究[D]. 南宁: 广西大学, 2018 LIU Shuhong. Genotyping of predominant serotypes of Salmonella from fresh meat, quinolone resistance and its genes[D]. Nanning: Guangxi University, 2018.
[11] MD CARDOSO, SANTOS A, RODRIGUES M, et al. Salmonella spp. profiles isolated from seabird samples from the Brazilian coast[J]. Preventive Veterinary Medicine,2021,193(4):105−113.
[12] 葛琨, 武运, 杨保伟, 等. 乌鲁木齐牛羊肉源沙门氏菌对喹诺酮类药物的耐药状况及相关基因分析[J]. 食品科学,2017,38(4):107−109. [GE Kun, WU Yun, YANG Baowei, et al. Quinolone resistance characteristics and related gene analysis of Salmonella in beef and mutton retailed in Ürümqi[J]. Food Science,2017,38(4):107−109. doi: 10.7506/spkx1002-6630-201704018 [13] KIM J Y, HAN X, BAE J H, et al. Prevalence of Plasmid-mediated Quinolone Resistance (PMQR) genes in non-typhoidal Salmonella strains with resistance and reduced susceptibility to fluoroquinolones from human clinical cases in Alberta, Canada, 2009-13[J]. The Journal of Antimicrobial Chemotherapy,2016(2):55−58.
[14] 张大燕. 浅谈抗生素滥用的危害及预防对策[J]. 心理月刊,2020,15(8):238−238. [ZHANG Dayan. Talking about the harm of abuse of antibiotics and Its preventive countermeasures[J]. Psy,2020,15(8):238−238. [15] 李少博, 贺稚非, 李洪军, 等. 食源性沙门氏菌耐药机制及药敏性检测方法研究现状[J]. 食品与发酵工业,2016,42(9):257−259. [LI Shaobo, HE Zhifei, LI Hongjun, et al. Current status of research on drug resistance mechanism and drug sensitivity detection methods of foodborne Salmonella[J]. Food and Fermentation Indusries,2016,42(9):257−259. [16] 杜昕悦, 杨哲敏, 赵宇, 等. 恩诺沙星与其他氟喹诺酮类药联合对畜禽常见病原菌抑菌效果探讨[J]. 黑龙江畜牧兽医,2019(20):140−143. [DU Xinyue, YANG Zhemin, ZHAO Yu, et al. Antibacterial effect of enrofloxacin combined with other fluoroquinolones on common pathogenic bacteria of livestock and poultry[J]. Heilongjiang Animal Science and Veterinary Medicine,2019(20):140−143. [17] 胡豫杰, 刘畅, 王美美, 等. 2016年中国26个省市食源性沙门菌耐药性特征分析[J]. 中国食品卫生杂志,2018,30(5):456−461. [HU Yujie, LIU Chang, WANG Meimei, et al. Resistance characteristic analysis for foodborne Salmonella isolates from China, 2016[J]. Chinese Journal of Food Hygiene,2018,30(5):456−461. [18] 黎明, 孔喜梅, 袁齐武, 等. 成都市未成年人群腹泻沙门氏菌血清型、耐药及分子分型研究[J]. 现代预防医学,2021,48(21):3996−4000. [LI Ming, KONG Ximei, YUAN Qiwu, et al. Serotype, drug resistance and molecular typing of Salmonella among children in Chengdu[J]. Modern Preventive Medicine,2021,48(21):3996−4000. [19] TOMOVA A, IVANOVA L, BUSCHMANN A H, et al. Plasmid-mediated quinolone resistance (PMQR) genes and class 1 integrons in quinolone-resistant marine bacteria and clinical isolates of Escherichia coli from an aquacultural area[J]. Microbial Ecology,2017,75(1):1−9.
[20] 郝宏珊, 杨保伟, 师俊玲, 等. 鸡肉源沙门氏菌对喹诺酮和氟喹诺酮类抗生素耐药状况及相关基因[J]. 微生物学报,2011,51(10):1413−1420. [HAO Hongshan, YANG Baowei, SHI Junling, et al. Resistance of Salmonella from chicken to quinolone and fluoroquinolone antibiotics and related genes[J]. Acta Microbiologica Sinica,2011,51(10):1413−1420. [21] 关茹飞, 江萍, 高超, 等. 新疆乌鲁木齐市周边鸡场鸡源沙门氏菌耐药性及耐药基因的检测[J]. 中国农业科技导报,2017,19(10):28−35. [GUAN Rufei, JIANG Ping, GAO Chao, et al. In order to understand Salmonella tolerance chicken farms in Urumqi of Xinjiang and tolerance gene carrying situation[J]. Journal of Agricultural Science and Technology,2017,19(10):28−35. [22] 刘贵深, 于涛. 食源性沙门氏菌耐药性及质粒介导喹诺酮耐药基因检测[J]. 生物技术通报,2014,46(8):202−207. [LIU Guishen, YU Tao. Study on antimicrobial resistance and plasmid-mediated quinolone resistance of foodborne Salmonella isolates[J]. Biotechnology Bulletin,2014,46(8):202−207. [23] 林居纯, 覃春红, 赖婧, 等. 食品动物源沙门氏菌质粒介导喹诺酮类耐药基因的检测与分析[J]. 畜牧兽医学报,2012(5):803−809. [LIN Juchun, QIN Chunhong, LAI Jing, et al. Detection and analysis of plasmid-mediated quinolone resistance in Salmonella isolates from food animals[J]. Acta Veterinaria et Zootechnica Sinica,2012(5):803−809. [24] JONESDIAS D, MANAGEIRO V, FRANCISCO A P, et al. Assessing the molecular basis of transferable quinolone resistance in Escherichia coli and Salmonella spp. from food-producing animals and food products[J]. Veterinary Microbiology,2013,167(3−4):523−531. doi: 10.1016/j.vetmic.2013.08.010
[25] 王旭东, 王凡, 周冰倩, 等. 重庆市北碚区宠物源沙门氏菌耐药性监测及ESBL和PMQR基因检测[J]. 微生物学通报,2021,48(8):2714−2722. [WANG Xudong, WANG Fan, ZHOU Bingqian, et al. Surveillance of antimicrobial resistance and detection of ESBL and PMQR genes in pet-associated Salmonella in Beibei District, Chongqing[J]. Microbiology China,2021,48(8):2714−2722. [26] DUNBAR S A, JACOBSON J W. Quantitative, multiplexed detection of Salmonella, and other pathogens by Luminex xMAPTM suspension array[M]. Methods Mol Biol, 2007, 394: 1−19.
[27] NIKOL R, VERONIKA M, MARTIN K, et al. xMAP technology: Applications in detection of pathogens[J]. Frontiers in Microbiology,2017,8(55):32−36.
[28] 郑之北, 郑伟, 濮小英, 等. 沙门菌H抗原的xTAG法鉴定[J]. 中华微生物学和免疫学杂志,2016,36(12):942−947. [ZHENG Zhibei, ZHENG Wei, PU Xiaoying, et al. Identification of Salmonella H antigen by xTAG[J]. Chinese Journal of Microbiology and Immunology,2016,36(12):942−947. doi: 10.3760/cma.j.issn.0254-5101.2016.12.011 [29] VANWONG N, NGAMSAMUT N, HONGKAEW Y, et al. Detection of CYP2D6 polymorphism using Luminex xTAG technology in autism spectrum disorder: CYP2D6 activity score and its association with risperidone levels[J]. Drug Metab Pharmacokinet,2016:156−162.
[30] 白莉, 张秀丽, 甘辛, 等. 肉鸡养殖场中环丙沙星和头孢噻肟双重耐药沙门菌耐药机制的研究[J]. 中国食品卫生杂志,2015,27(5):487−494. [BAI Li, ZHANG Xiuli, GAN Xin, et al. Molecular characteristics of ciprofloxacin and cefotaxime co-resistant Salmonella isolates in broiler flocks[J]. Chinese Journal of Food Hygiene,2015,27(5):487−494. [31] 林亚军, 郭菲, 夏利宁, 等. 新疆乌鲁木齐市宠物源沙门氏菌耐药性及耐药基因检测[J]. 中国农业大学学报,2018,23(7):9−10. [LIN Yajun, GUO Fei, XIA Lining, et al. Detection of drug resistance and resistant genes of Salmonella from pets in Urumqi[J]. Journal of China Agricultural University,2018,23(7):9−10. doi: 10.11841/j.issn.1007-4333.2018.07.09 [32] 覃春红. 动物源沙门氏菌耐药性及质粒介导喹诺酮类耐药基因的流行病学研究[D]. 雅安: 四川农业大学, 2011 QIN Chunhong. The epidemiological study of antimicrobial resistance and plasmid-mediated quinolone resistance genes in Salmonella isolated from animals[D]. Ya'an: Sichuan Agricultural University, 2011.
[33] LEE S, PARK N YUN S J, et al. Presence of plasmid-mediated quinolone resistance (PMQR) genes in non-typhoidal Salmonella strains with reduced susceptibility to fluoroquinolones isolated from human salmonellosis in Gyeonggi-do, South Korea from 2016 to 2019[J]. Gut Pathogens,2021,13(1):714−715.
[34] DIVYA S P, CHANDRADASAN A, PRANAV P K. Prevalence of plasmid-mediated quinolone resistance (PMQR) genes and beta-lactamase genes among Salmonella, vibrio parahaemolyticus and Escherichia coli from shellfish[J]. Fishery Technology,2020(1):57.
[35] 张林杰. 基于Luminex液相芯片技术检测急性脑梗死患者炎性T细胞因子动态变化[D]. 南宁: 广西中医药大学, 2021 ZHANG Linjie. Dynamic changes of inflammatory T cytokines in patients with acute cerebral infarction were detected based on Luminex liquid chip technology[J]. Nanning: Guangxi University of Chinese Medicine, 2021.
[36] 曹广进. 利用液相芯片技术检测儿童急性呼吸道感染及感染性腹泻病原体的研究[D]. 广州: 南方医科大学, 2019 CAO Guangjin. Study on detection of the pathogens of acute respiratory tract infection and infectious diarrhea in children by using liquid-phase microarray technology[J]. Guangzhou: Southern Medical University, 2019.
[37] 肖丽, 丛峰, 朱余军, 等. 建立快速检测禽白血病病毒的液相芯片方法[J]. 实验动物科学,2017,34(5):28−30, 36. [XIAO Li, CONG Feng, ZHU Yujun, et al. Establishment of liquid chip method for rapid detection of avian leukemia virus[J]. Laboratory Animal Science,2017,34(5):28−30, 36. doi: 10.3969/j.issn.1006-6179.2017.05.006 [38] 戴莹, 雷亚克, 岳苗苗, 等. 应用液相芯片技术检测六种输入性烈性传染病病原的方法研究[J]. 中国病原生物学杂志,2019,14(11):1303−1307. [DAI Ying, LEI Yake, YUE Miaomiao, et al. Study on detection of six imported severely infectious pathogens using Luminex liquid chip technology[J]. Journal of Pathogen Biology,2019,14(11):1303−1307. [39] 郭容, 董晓妹, 别闯南, 等. 五种重要致病性弧菌高通量液相芯片检测方法的建立[J]. 中国兽医科学,2021,51(7):805−813. [GUO Rong, DONG Xiaomei, BIE Chuangnan, et al. Establishment of high throughput liquid chip for detection of five important pathogenic vibrios[J]. Veterinary Science in China,2021,51(7):805−813. [40] 叶硕, 杨元斌, 周伟艳, 等. 7种致病性弧菌xTAG液相芯片快速筛查方法的建立[J]. 中国卫生检验杂志,2020,30(20):2446−2450. [YE Shuo, YANG Yuanbin, ZHOU Weiyan, et al. A rapid screening system for the detection of seven kinds of pathogenic based on Luminex x-TAG technology[J]. Chinese Journal of Health Laboratory Technology,2020,30(20):2446−2450. [41] 史贇学. 四种食源性致病菌液相芯片xTAG技术检测方法的建立[D]. 长春: 吉林农业大学, 2019 SHI Yunxue. Establishment of a method for the simultaneous detection of four foodborne pathogens using high-throughput suspension array xTAG technology[J]. Changchun: Jilin Agricultural University, 2019.
[42] 伍业健, 吴新伟, 陶霞, 等. 应用液相芯片技术快速检测常见食源性致病菌的研究[J]. 中国卫生检验杂志,2018,28(14):1672−1675, 1679. [WU Yejian, WU Xinwei, TAO Xia, et al. Rapid detection of common food-borne pathogens with suspension array[J]. Chinese Journal of Health Laboratory Technology,2018,28(14):1672−1675, 1679. [43] 金玉娟, 陈应坚, 甘莉萍, 等. 应用液相芯片技术联合多重PCR快速检测四种常见食源性致病菌的研究[J]. 热带医学杂志,2015,15(6):735−740. [JIN Yujuan, CHEN Yingjian, GAN Liping, et al. Application of a suspension array technology and the multiplex PCR for rapid detection of four common food-borne pathogens[J]. Journal of Tropical Medicine,2015,15(6):735−740. doi: 10.3969/j.issn.1672-3619.2015.06.006 [44] BORUCKI M K, REYNOLDS J, CALL D R, et al. Suspension microarray with dendrimer signal amplification allows direct and high-throughput subtyping of Listeria monocytogenes from genomic DNA[J]. J Clin Microbiol,2005,43(7):3255−3259. doi: 10.1128/JCM.43.7.3255-3259.2005
[45] 赵莹, 屠博文, 毛旭建, 等. 液相悬浮芯片技术在沙门氏菌血清分型中的应用优势[J]. 公共卫生与预防医学,2021,32(3):75−79. [ZHAO Ying, TU Bowen, MAO Xujian, et al. Application advantages of liquid phase suspension chip technique in Salmonella serotyping[J]. Journal Public Health and Preventive Medicine,2021,32(3):75−79. doi: 10.3969/j.issn.1006-2483.2021.03.018 [46] 蔡标, 戴陈伟, 吕涵, 等. 3种快速检测沙门氏菌方法的比较分析[J]. 食品安全质量检测学报,2019,10(18):6036−6041. [CAI Biao, DAI Chenwei, LYU Han, et al. Comparative analysis of 3 rapid detection methods for Salmonella[J]. Journal of Food Safety and Quality,2019,10(18):6036−6041. [47] 毛旭建, 唐宏兵, 屠博文, 等. 液相芯片技术在沙门菌抗原缺失血清型鉴定中的应用[J]. 江苏预防医学,2019,30(3):337−339. [MAO Xujian, TANG Hongbing, TU Bowen, et al. Application of liquid chip technology in identification of Salmonella antigen deletion serotype[J]. Jiangsu Journal of Preventive Medicine,2019,30(3):337−339. [48] 董慧. 液相芯片技术分析氟西汀对抑郁大鼠趋化因子的影响[J]. 徐州医科大学学报,2022,42(2):91−96. [DONG Hui. Effect of fluoxetine on the level of serum chemokines in chronic unpredicted mild stress rats by Luminex assa[J]. Journal of Xuzhou Medical University,2022,42(2):91−96. doi: 10.3969/j.issn.2096-3882.2022.02.003 [49] 车荣飞, 白茹, 孙聪, 等. 呼吸道感染多病原检测试剂盒Luminex NxTAG~(TM)RPP与一代测序性能对比[J]. 国际病毒学杂志,2021,28(1):57−61. [CHE Rongfei, BAI Ru, SUN Cong, et al. Comparison between Luminex NxTAG~(TM) RPP and first generation sequencing performance of respiratory tract infection multi pathogen detection kit[J]. International Journal of Virology,2021,28(1):57−61. doi: 10.3760/cma.j.issn.1673-4092.2021.01.013 [50] 叶硕, 郑健, 周伟艳, 等. Luminex x-TAG技术在金黄色葡萄球菌肠毒素快速分型中的应用[J]. 中国卫生检验杂志,2020,30(21):2564−2567, 2571. [YE Shuo, ZHENG Jian, ZHOU Weiyan, et al. A rapid screening system for the detection of Staphylococcal enterotoxin based on Luminex x-TAG technology[J]. Chinese Journal of Health Laboratory Technology,2020,30(21):2564−2567, 2571. [51] POPOWITCH ELENA B, KAPLAN SAM, WU ZENGLIN, et al. Comparative performance of the Luminex NxTAG respiratory pathogen panel, GenMark eSensor respiratory viral panel, and biofire filmarray respiratory panel[J]. Microbiology Spectrum,2022:1164.
[52] KING A, KING G, WEISS C, et al. Detection of IgG antibodies to SARS-CoV-2 and neutralizing capabilities using the Luminex® xMAP® SARS-CoV-2 multi-antigen IgG assay[J]. Methods in Molecular Biology (Clifton, N. J.),2022:2511−2513.
[53] MARÍNROMERO A, TABRAUECHÁVEZ M, LÓPEZLONGARELA B, et al. Simultaneous detection of drug-induced liver injury protein and microRNA biomarkers using dynamic chemical labelling on a Luminex MAGPIX system[J]. Analytica,2021,2(4):19−24.
[54] YOO J, LEE S, LEE H W, et al. Assessment of rapid optimized 96-well tray flow cytometric crossmatch (Halifax-FCXM) with Luminex single antigen test[J]. Human Immunology,2021,82(4):234−235.
-
期刊类型引用(0)
其他类型引用(2)





 下载:
下载:
 下载:
下载:



