Effect of Homogenization Pressure on the Stability and in Vitro Digestion of Flaxseed Oil Emulsion
-
摘要: 本实验以亚麻籽油体为研究对象,通过对其进行均质处理,得到了稳定的富含α-亚麻酸的亚麻籽油体乳液,为居民在日常膳食中提高 -3不饱和脂肪酸摄入量提供了新的途径。在保持均质时间相同的条件下(3 min),对亚麻籽油体进行不同均质压力(40、80、120 MPa)与均质次数(1~3次)处理,考察均质处理对亚麻籽油体乳液的性质、环境稳定性(pH、离子强度、热、氧化稳定性)、储藏稳定性和消化特性的影响。结果表明,FOB在120 MPa下均质处理3次,电位绝对值增加,粒径显著减小(P<0.05)。均质处理后的亚麻籽油体乳液在50~90 ℃下热处理30 min,粒径、电位稳定,且表现出更好的氧化稳定性和储藏稳定性(P<0.05)。均质处理亚麻籽油体并不影响其对pH4~5和离子强度不稳定(P>0.05)。消化结果表明,均质处理后的亚麻籽油体乳液具有更快的脂肪酸释放速率(FFA)。综上,均质处理显著了减小亚麻籽油体乳液的粒径,增强了亚麻籽油体的储藏稳定性和氧化稳定性,且加快了脂肪酸释放速率。Abstract: In this study, flaxseed oil body was taken as the research object, and stable flaxseed oil body emulsion rich in α-linolenic acid was obtained through homogenization treatment, which provides a new way for residents to increase the intake of ω-3 unsaturated fatty acids in daily diet. Under the same homogenous conditions (3 min) each time, changing the homogenization pressure (40, 80, 120 MPa) and the number of times (1~3 times) of flaxseed oil emulsions, the effects of homogenization on the properties, environmental stability ( pH, ionic strength, thermal, oxidation stability) and storage stability, and digestive properties of flaxseed oil emulsions were investigated. The results showed that the absolute value of potential zeta potential increased and the particle size decreased significantly when flaxseed oil body was homogenized at 120 MPa for three times (P<0.05). After heat treatment at 50~90 ℃ for 30 min, the particle size and potential of homogenized flaxseed oil emulsions were stable, and it showed better oxidation stability and storage stability (P<0.05). With or without homogenization, flaxseed oil bodies were still unstable to pH4~5 and ionic conditions (P>0.05). The results of digestion showed that the homogenized flaxseed oil body emulsion had a higher release rate of fatty acids (FFA). In conclusion, the homogenization treatment significantly reduced the particle size of flaxseed oil emulsion, enhanced the storage stability and oxidation stability of flaxseed oil body, and accelerated the release rate of fatty acid.
-
α-亚麻酸是一种ω-3不饱和脂肪酸,具有抗癌、降血脂[1]和抗糖尿病等多种功效。人体自身无法合成,须从日常饮食中摄取[2]。亚麻籽是α-亚麻酸自然界最丰富的来源之一[3],因此,日常膳食中通过食用亚麻籽系列产品可有效提高α-亚麻酸摄入量。目前,可供人们食用的亚麻籽形式主要包括亚麻籽粉、亚麻籽食用油及部分脱脂的亚麻籽粉,应用形式单一。亚麻籽榨油后损耗较大,其营养价值无法得到充分利用。因此,亚麻籽系列产品仍具有很大的开发前景。
植物油体作为油料作物种子存储脂质的器官,富含大量不饱和脂肪酸,其主要成分[4]是中性脂(三酰甘油酯,tri-acylglycerol, TAG)、蛋白质、磷脂。与常见的油脂相比,植物油体的提取具有无需添加有机试剂[5]、乳化剂[5]和提取率高[6]等多种优势,且植物油体本身也符合人们对绿色且营养丰富产品的需求。目前,在大豆油体[7]、红花油体[8]、大麻籽油体[9]等方面有较多的研究,而关于亚麻籽油体(FOB)的研究较少,因此,以FOB为突破点,进行亚麻籽系列产品的后续开发具有较大的可行性。FOB作为一种水包油型乳液,当油相和水相之间存在着明显的密度差时,易导致液滴在容器顶部积聚,出现乳析[10]现象。同时FOB由于还含有不饱和脂肪酸,容易氧化生成氢过氧化物和二次氧化产物[11]。因此,FOB的稳定性必然是影响FOB生产应用的重要因素。李婷婷等[6]研究了牡丹油体的稳定性,发现50 ℃以上的高温对油体稳定性影响不大,pH及氯化钠浓度对牡丹油体稳定性影响显著。王智丰等[12]对芝麻油体稳定性的研究发现碱性条件、高热处理和低盐离子浓度有助于维持芝麻油体的稳定性。因此,在研究FOB乳液稳定性时,温度、离子强度、pH等因素的探究是考察其稳定性的重要指标。
高压均质是制备或稳定乳剂的一个重要过程,其可以大大减少乳剂发生乳析现象,有助于提高均匀化乳状液的物理稳定性[13]。在前期预实验中发现,FOB容易发生析水现象。这可能是由于FOB自身粒径较大且未经过任何剪切处理导致。在激光纳米粒度仪的检测中也发现样品出现不止一个波峰,且峰型较宽,表明FOB粒径大小不一。因此,针对预实验出现的问题,本研究拟采用高压均质技术处理FOB,借助高压剪切力降低FOB的粒径,并使其粒径均匀,以达到稳定乳液的目的。通过控制均质时间相同(3 min),改变均质压力(40 、80、120 MPa)与均质次数(1~3次),研究均质处理对FOB乳液的理化性质、环境稳定性(热、pH、离子强度稳定性)、氧化稳定性及消化特性的影响,为进一步开发富含α-亚麻酸的亚麻籽油体乳液产品的实际应用提供一定的理论依据。
1. 材料与方法
1.1 材料与仪器
亚麻籽 内蒙古大旭有限公司(油含量38.29%,蛋白含量21.57%);黏膜蛋白(M2378)、胃蛋白酶(P7000,酶活≥250 units/mg)、脂肪酶(L3126,酶活≥125 units/mg)、胰酶(P7545,酶活,8×USP specifications) 美国Sigma公司;1,1,3,3-四乙氧基丙烷(97%)、硫酸亚铁七水合物(ACS, ≥99.0%)、过氧化氢异丙苯(80%)、2-硫代巴比妥酸(98%)、硫氰酸铵(ACS, ≥99.0%);无水氯化钙(ACS, ≥99.0%) 上海阿拉丁生化科技有限公司;其它试剂皆为国产分析纯。
C-MAG HS 7磁力搅拌器 德国IKA集团;AL204电子分析天平 梅特勒-拉利多仪器(上海)有限公司;MH700高速纳米分散机 河北廊坊通用机械有限公司;Epoch 2酶标仪 美国Biotek Instrument有限公司;SP8激光共聚焦扫描显微镜 德国Leica公司;827pH计 梅特勒-拉利多仪器(上海)有限公司;907 TitrandopH-stat 自动电位滴定仪 瑞士万通中国有限公司;MasterSizer 3000微米粒度仪、Zetasizer Nano ZSP激光纳米粒度仪 英国马尔文公司;MJ-PB12Power311破壁机 美的集团有限公司。
1.2 实验方法
1.2.1 FOB的提取
参考Chirico等[14]的方法从亚麻籽中提取油体并进行纯化。将20.0 g亚麻籽以一定的料液比(1:13)浸泡在0.1 mol/L NaHCO3溶液中,于4 ℃过夜放置,然后倒掉浸泡液。浸泡后的亚麻籽置于相同比例的浸泡液中,使用美的破壁机以1200 W进行充分研磨。研磨后,通过三层纱布过滤,于8000 r/min 离心30 min,取上层乳膏,称为粗油体(C-OB)。为去除残留物,将上层乳膏以相同的比例悬浮于0.1 mol/L、pH9.5的NaHCO3溶液中,于8000 r/min 离心30 min,离心后取上层乳膏,重复两次,获得油体,亚麻籽油体的脂肪回收率达69.17%,并将油体于4 ℃储藏。
1.2.2 FOB的均质处理
将一定量的亚麻籽油体均匀分散在pH7.0、10 mmol/L的Tris-HCl缓冲液中,使油体乳液脂肪含量为6.25%。用高速纳米分散机均质处理FOB 1~3次,每次均质时间为3 min,处理压力分别为40、80与120 MPa。
1.2.3 FOB乳液平均粒径与平均电位测定
参考Zheng等[15]的方法,采用微米粒度仪测定FOB乳液的平均粒径。测量方法如下:遮光度为5%~8%,样品池中加入与样品相同pH的蒸馏水进行稀释,水与样品折射率分别为1.33和1.47,样品测三次,取平均值,用D3.2表示平均粒径。
参考Zhu等[16]的方法,采用激光纳米粒度仪测定乳液的ζ-电位。测量前使用与样品相同pH的蒸馏水稀释适当倍数,测定三次取平均值。
1.2.4 不同均质压力处理三次后的FOB乳液稳定性测定
1.2.4.1 pH稳定性
用0.5 mol/L HCl和0.5 mol/L NaOH将FOB乳液的pH调至2.0、3.0、4.0、5.0、6.0、7.0和8.0。每个pH的样品取5 mL分装于试管中,分别测其粒径和Zeta电位,每个样品重复3次,取平均值。
1.2.4.2 离子强度稳定性
用5 mol/L的氯化钠溶液作为母液,按比例将FOB乳液的氯化钠离子强度稀释至0、50、100、200、400 mmol/L五个梯度,每个离子强度的样品取5 mL分装于试管中,每个样品分别测量粒径和Zeta电位,重复3次,取平均值。
1.2.4.3 热稳定性
将制备好的5 mL的FOB乳液放入玻璃试管中,分别置于50、60、70、80、90 ℃的水浴条件下30 min。之后立刻取出冷却至室温,测定其粒径和Zeta电位三次,取平均值。
1.2.4.4 氧化稳定性
各取一定体积的不同均质压力处理后的FOB乳液放入离心管中,扣紧管盖。于50 ℃条件下储藏15 d,定期测定乳液氧化,平行测定三次。用初级氧化产物(POV值)与次级氧化产物(TBARs值)表示其氧化程度。
初级氧化产物(POV):FOB的POV测定参考Shantha等[17]的方法,单位mmol/kg oil。取1.5 mL异丙醇:异辛烷(体积比1:3)添加到0.3 mL FOB中,振荡(10 s,3 次)均匀,离心(1000×g,2 min),取有机层200 μL,加入甲醇:正丁醇(体积比3:1)的溶液2.8 mL,再依次加入13.94 mol/L的硫氰酸铵和氯化亚铁溶液(现配)各15 mL,暗处反应20 min,测其吸光值(波长:510 nm),根据过氧化氢异丙苯标准曲线(y=0.0761x+0.0367,R2=0.9985,其中,y为样品吸光度(abs),x为样品浓度(mmol/kg))计算FOB的POV值。
次级氧化产物(TBARs):参考Li等[18]的方法制定TBARs值的测量方法,单位μmol/kg oil。取FOB 0.2 mL与0.8 mL去氧蒸馏水混匀,再取TBA测试液(15%三氯乙酸和0.375%的TBA溶于0.25 mol/L HCl溶液)2 mL加入其中,振荡(10 s,3 次)均匀。水浴(95 ℃,15 min)后冷却至常温,离心(1000×g,2 min)取上清液,测其吸光值(波长:532 nm)。根据1,1,3,3-四乙氧基丙烷标准曲线(y=0.0479x+0.008,R2=0.9998,其中,y为样品吸光度(abs),x为样品浓度(mmol/kg))计算FOB的TBARs值。
1.2.4.5 储藏稳定性
将不同均质压力处理三次FOB乳液分别加入不同的玻璃试管中,在4 ℃下密封放置8周,然后在不同时间点(1、7、14、28、42、56 d)观察其乳析稳定性,是否出现亚麻籽油层(析油),测定其乳析指数(creaming index,CI)。
乳析指数(%)=乳液析出水相的高度/乳液总高度×100
1.2.5 FOB乳液体外消化特性研究
1.2.5.1 体外消化模型
参考Zou等[19]的方法并略作修改,依据比例配制消化液,进行消化实验。
口腔消化:取FOB 2 mL与5.5 mL蒸馏水混匀,再加入7.5 mL口腔消化液(SSF),混匀预热(37 ℃,5 min)后置于消化瓶中。用1 mol/L HCl溶液将其pH快速调至6.8,在摇床水浴(37 ℃,100 r/min,10 min)消化。
胃消化:预热(37 ℃,5 min)胃部消化液(SGF)后,取15 mL与上述口腔消化样品混匀,用1 mol/L NaOH溶液将其pH快速调至2.5,在摇床水浴(37 ℃,100 r/min,2 h)消化。
肠消化:胃消化结束后,用2 mol/L的NaOH溶液将上述胃消化样品pH迅速调至7.0。预热肠道消化液(SIF)(37 ℃,5 min)后,依次取SIF、胆盐溶液(含189 mg胆盐)、脂肪酶溶液(含60 mg脂肪酶)和胰酶溶液(含60 mg胰酶)1.5 mL、3.5 mL、2.5 mL和2.5 mL加入到上述胃消化液中,于pH-stat自动电位滴定仪中,水浴搅拌(100 r/min,37 ℃,2 h)消化,消化期间pH稳定在7.0依靠持续滴定0.1 mol/L NaOH溶液维持。
1.2.5.2 消化产物外观形貌
分别取3个阶段消化后的FOB,使用激光共聚焦显微镜(CLSM)观察其微观形态。取2 mL样品加入100 μL 0.1%尼罗红染料,激发波长为488 nm用40×和60×物镜观察样品的结构,并采集荧光图像。
1.2.5.3 FFA释放特性
参考Munoz等[20]方法略作修改测定FFA,具体方法见1.2.5.1体外消化模型-肠消化中的0.1 mol/L NaOH溶液滴定。根据pH-stat法,记录消化期间pH稳定在7.0所消耗的0.1 mol/L NaOH溶液的消耗量,根据公式(1)计算出FFA释放率(%)。
(1) 式中 :mNaOH为消耗的NaOH溶液的摩尔浓度;mlipid为的FOB质量分数(经脂肪酸组成测试发现,FOB中α-亚麻酸含量约为45.81%,其次为油酸,含量约为17.27%,亚油酸含量约为13.40%,计算得mlipid = 845.97 g/mol);Wlipid为FOB的重量(g)。
1.3 数据处理
数据的统计分析依靠SPSS17.0,平均值±标准偏差表示结果,指标间的显著性差异用不同字母表示(P<0.05)。
2. 结果与分析
2.1 不同压力处理对FOB乳液粒径与电位的影响
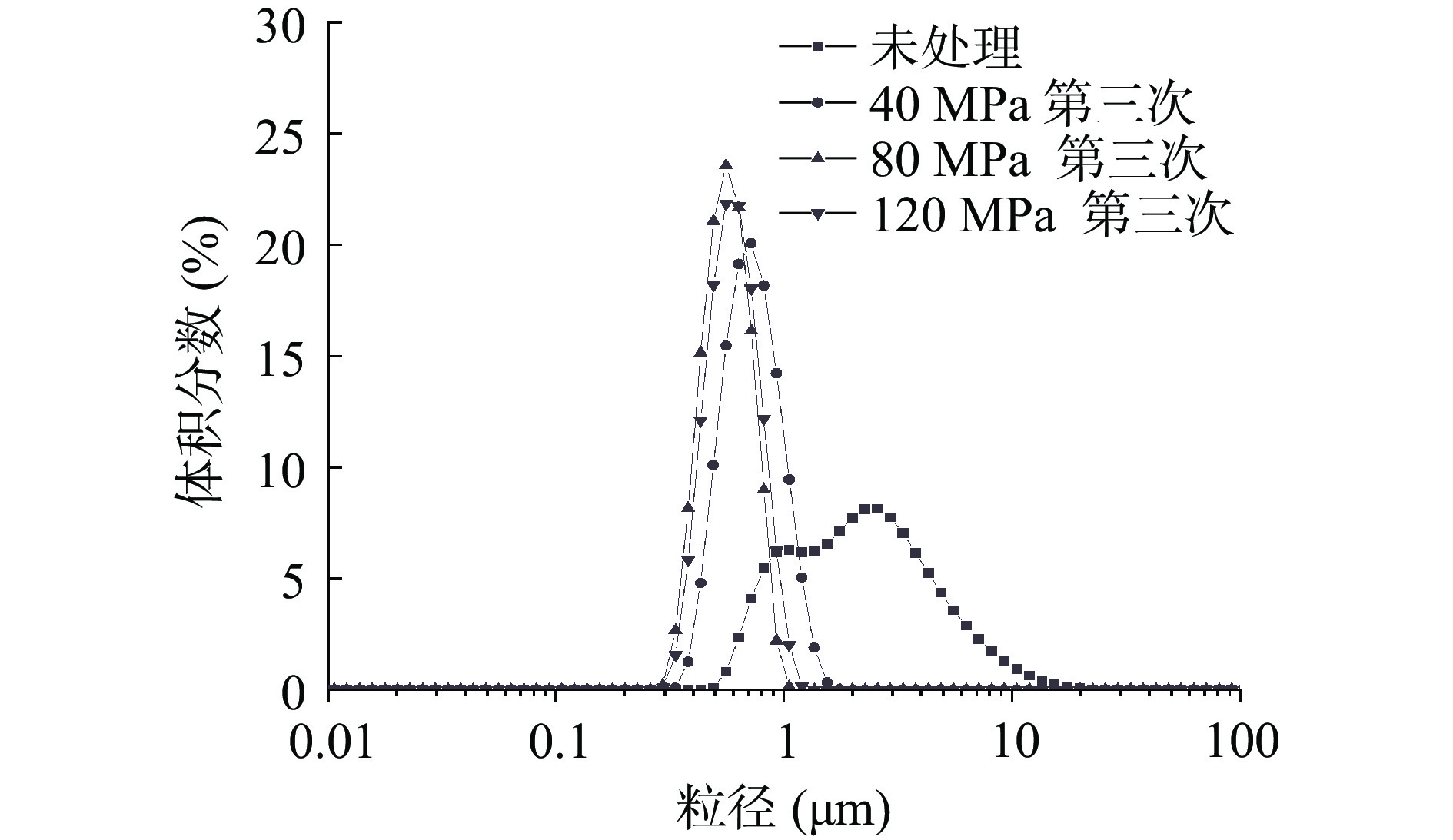
粒径分布是影响乳液物理化学和功能特性的关键特性[21]。由表1可知,在均质时间(3 min)相同的前提下,未处理的FOB体积表面平均粒径约为2 μm,40、80、120 MPa压力下处理一次后分别下降到0.85、0.87、0.77 μm,表明经过均质可显著减小FOB液滴的大小(P<0.05)。在压力不变,均质次数为1~3次时,乳液体积表面平均粒径随着处理次数增加而减小,表明增加均质次数可显著减小FOB液滴的大小(P<0.05)。在处理次数不变,均质压力为40、80、120 MPa时,乳液粒径随着压力增大而减小(P<0.05)。由图1可知,未处理的FOB粒径呈现双峰分布,说明未经过均质处理的FOB存在聚结现象,在40、80、120 MPa 压力处理三次后,乳液的粒径呈现单峰分布且粒径分布变窄,在120 MPa处理后粒度分布最窄,说明不同均质压力处理后乳液体系粒径分布更为均一。康波[22]研究发现,在100 MPa和120 MPa的条件下对花生油体处理三次,出现了乳液均质的过处理现象。本研究中在120 MPa下对FOB处理三次并未出现过乳析的现象,说明FOB可以经受高压处理且较为稳定。Yan等[23]发现,均质压力25~100 MPa的条件下,乳清蛋白和卵磷脂形成的乳液变得更加均匀。与未处理的乳液相比,高压均质处理后的FOB中蛋白簇较小,从而具有更高的乳液界面覆盖率。据报道,乳液界面处吸附蛋白之间的疏水相互作用有利于乳液的稳定性[24]。FOB高压均质后产生了更小的蛋白簇,增加了乳液界面处吸附蛋白间的相互作用力,有助于提高FOB乳液的稳定性。
表 1 不同均质压力及不同均质次数处理下亚麻籽油体的粒径和电位Table 1. Particle size, zeta potential of flaxseed oil body under different homogenization pressure and different homogenization times样品 D3.2(μm) D4.3(μm) ξ-电位(mV) 未处理 2.04±0.0115a 3.93±0.2888a −26.47±0.80a 40 MPa处理一次 0.85±0.0010c 1.08±0.0058b −32.67±1.62bc 40 MPa处理二次 0.73±0.0010e 0.80±0.0010de −32.73±1.36bc 40 MPa处理三次 0.69±0.0060g 0.75±0.0010def −34.60±1.91cd 80 MPa处理一次 0.87±0.0010b 1.15±0.0100b −31.93±0.50bc 80 MPa处理二次 0.72±0.0010f 0.88±0.0006cd −31.57±0.86bc 80 MPa处理三次 0.64±0.0010h 0.69±0.0010ef −37.16±0.11d 120 MPa处理一次 0.77±0.0006d 0.99±0.0006bc −30.33±0.12b 120 MPa处理二次 0.61±0.0006i 0.65±0.0006ef −29.97±0.75b 120 MPa处理三次 0.58±0.0006j 0.62±0.0006ef −36.33±0.75d 注:D3.2:体积表面平均粒径;D4.3:体积平均粒径;同列不同字母表示数据之间具有显著性差异(P<0.05),表2同。 液滴的ξ-电位是影响乳液稳定性的关键特性之一[25],ξ-电位绝对值越高,静电排斥力越强,因此,液滴的稳定性越高,通常认为ξ-电位的绝对值大于30 mV时液滴具有较高的稳定性,较低的电位所产生的静电斥力可能不足以抵抗范德华力而导致液滴发生聚集或絮凝[26]。由表1可知,未处理的亚麻籽油体电位绝对值为26 mV,在40 MPa下处理三次后,电位绝对值达到34 mV,当压力增大到80和120 mV,处理三次时,电位绝对值分别达到37和36 mV,表明均质处理显著性地增强了FOB乳液的电位绝对值(P<0.05),这与Cha等[27]的研究一致。高压处理可以促进蛋白质及离子基团的界面吸附从而增加分散在油滴的表面电荷[28]。因此,本研究表明高压均质处理增加了FOB乳液中油滴的表面电荷,有助于提高FOB乳液的稳定性。
2.2 pH稳定性
食品乳液在其制造、运输、储存、利用和摄入过程中可能会经历不同的酸碱环境,因此乳液的pH稳定性对其在商业中的应用至关重要。蛋白质稳定的乳液主要是通过静电斥力维持稳定,而非空间斥力。因此,蛋白质稳定的乳液对pH变化特别敏感[29]。为考察pH大小对FOB稳定性的影响,用HCl溶液或NaOH溶液将FOB的pH调至2.0~8.0,室温放置24 h,观察其平均粒径和外观变化。
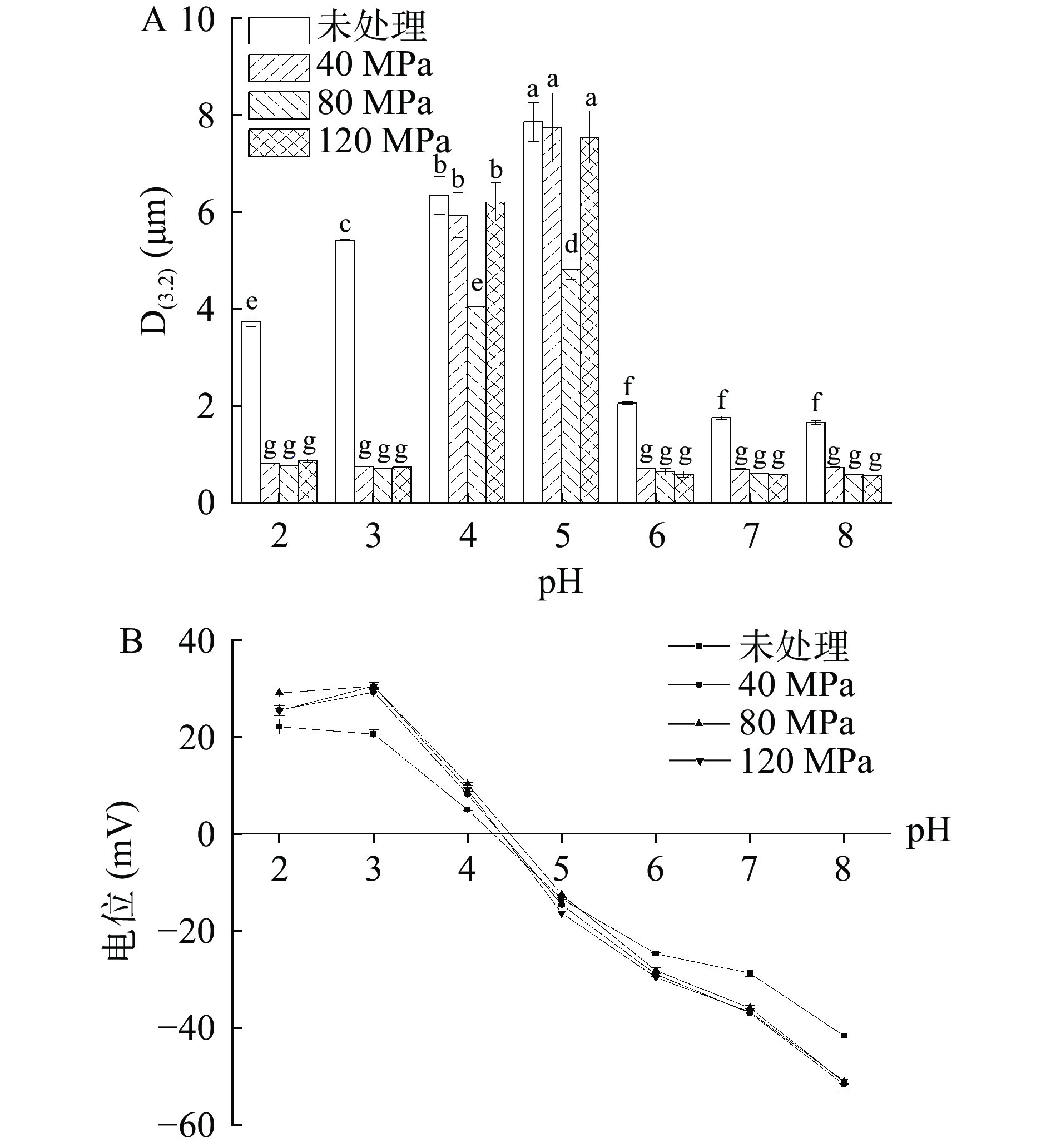
如图2、图3示,不论是否经过均质处理,当FOB的pH在4.0~5.0时,乳析现象都十分明显,D3.2明显增大,根据电位分析可知,当pH为4.0时,FOB带正电,当pH为5.0时,FOB带负电,在4.0~5.0之间(约为4.4)为其表面蛋白的等电点。当pH由4.0趋于5.0 时,FOB的表面电位逐渐趋于零,其液滴间的静电斥力也逐渐趋于零,进而导致了FOB的失稳。在等电点附近的pH条件下,油滴总体电荷所产生的排斥力不足以抵抗油滴之间疏水和范德华作用所产生的引力,因此乳液发生聚集[30],迅速失稳。据报道,不同种类(油菜、棉花、玉米、芝麻)的油体的等电点 pH 在 5.7~6.6[31],大豆油体的等电点pH 在 4.0~5.0之间[32]。随着pH的降低,乳液逐渐由负电转为正电。在低pH(2.0~3.0)的条件下,未处理和均质处理的FOB所产生的现象明显不同,在未处理的FOB中可以观察到一层乳脂层,而均质处理的FOB乳液可以维持稳定,这可能是由于均质处理导致FOB乳液表面蛋白构象发生变化,均质处理后的FOB乳液电位更大,说明其产生的静电排斥力更强,从而保持了其在pH2.0~3.0条件下的稳定。有研究报道,高压均质处理可以改变花生蛋白的微观结构,从而改善其功能特性[33]。Liu等[34]研究发现,超高压均质可以使大豆粉中的蛋白质变性。Yuan等[35]通过对表面疏水性、表面压力的分析,高压均质可以改善大豆分离蛋白的乳化性、抗冻融能力和发泡性,这些有关高压均质对蛋白结构影响的研究,进一步表明均质处理确实可能会改变FOB乳液表面蛋白构象。在高pH(6.0~8.0)条件下,未处理和均质处理的FOB均保持相对稳定。这可能是因为油滴总体电荷相互之间产生的排斥力足以抵抗油滴之间疏水和范德华作用所产生的引力,因此FOB乳液在高pH(6.0~8.0)保持稳定。
2.3 离子稳定性
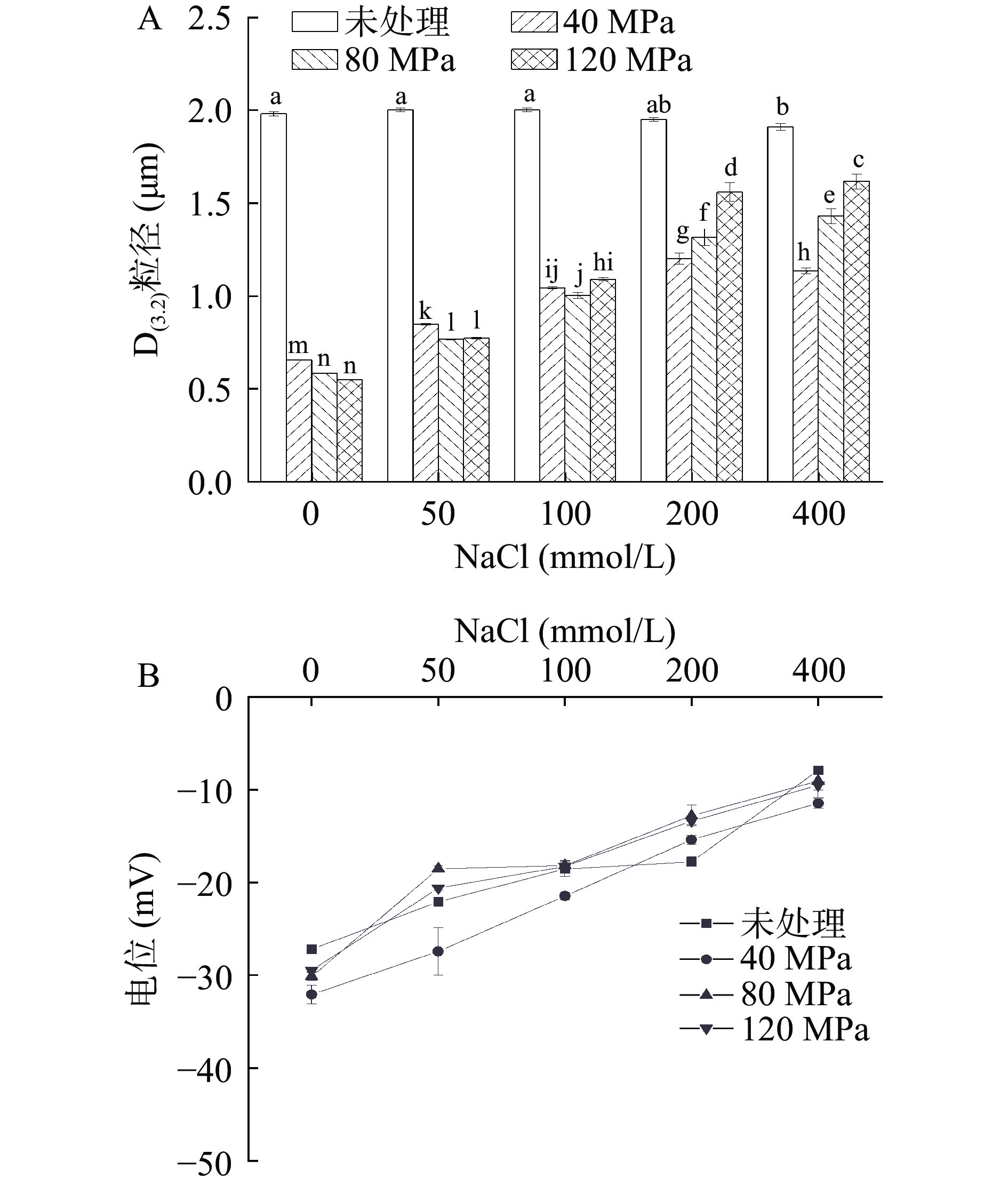
食品乳液在其应用过程中常被添加在不同盐离子浓度环境中,因此有必要了解乳液的离子稳定性。为考察离子浓度对FOB稳定性的影响,向FOB中加入不同浓度NaCl溶液,得到最终不同离子浓度的FOB,于室温下放置24 h,观察其平均粒径和外观变化。通常,随着盐离子(如NaCl)浓度在乳液中慢慢增加,由于静电的吸引,水相中的Na+倾向与蛋白质表面的负电荷集团COO−相结合,减少液滴具有的净电荷,从而影响乳剂的稳定性[36]。如图4、图5所示,所有的FOB在不同的离子浓度中均出现乳析现象,并且随着离子浓度的升高,乳膏层越厚,液滴聚集程度越强。粒径分布数据表明,随着离子浓度增加,未处理的FOB粒径基本不变,这可能是其液滴因静电屏蔽现象[37]发生聚集而并未出现合并现象,均质处理FOB的粒径逐渐增大,说明均质处理后FOB油滴不仅出现聚集还存在合并现象。高浓度的盐离子可以通过屏蔽液滴之间的静电排斥相互作用从而促进乳液中液滴聚集。在临界盐浓度以上,静电斥力不足以克服液滴之间的吸引相互作用力(范德华力和疏水作用力)。在本研究中发现,在一定浓度盐离子存在的条件下,未均质处理的FOB可以保持液滴的完整,均质处理的FOB部分液滴会结合成大油滴,出现合并现象,说明均质处理后FOB乳液对盐离子更不稳定。Hou等[38]研究发现,随着NaCl浓度的增加,大豆、花生等油体的电位绝对值显著下降,这与本文的研究一致。而其粒径方面仅略微增加,这可能是由于油体种类不同导致,FOB的表面蛋白对盐离子更敏感。Zhou等[39]研究发现花生油体的盐离子浓度小于10 mmol/L时稳定性良好,而盐离子浓度由20 mmol/L增加到100 mmol/L时,其电位绝对值显著减小,粒径显著增大,这与本文的研究结果一致。综上,FOB对盐离子较敏感,其离子稳定性较差,因此盐离子浓度在FOB稳定性中起重要作用。
2.4 热稳定性
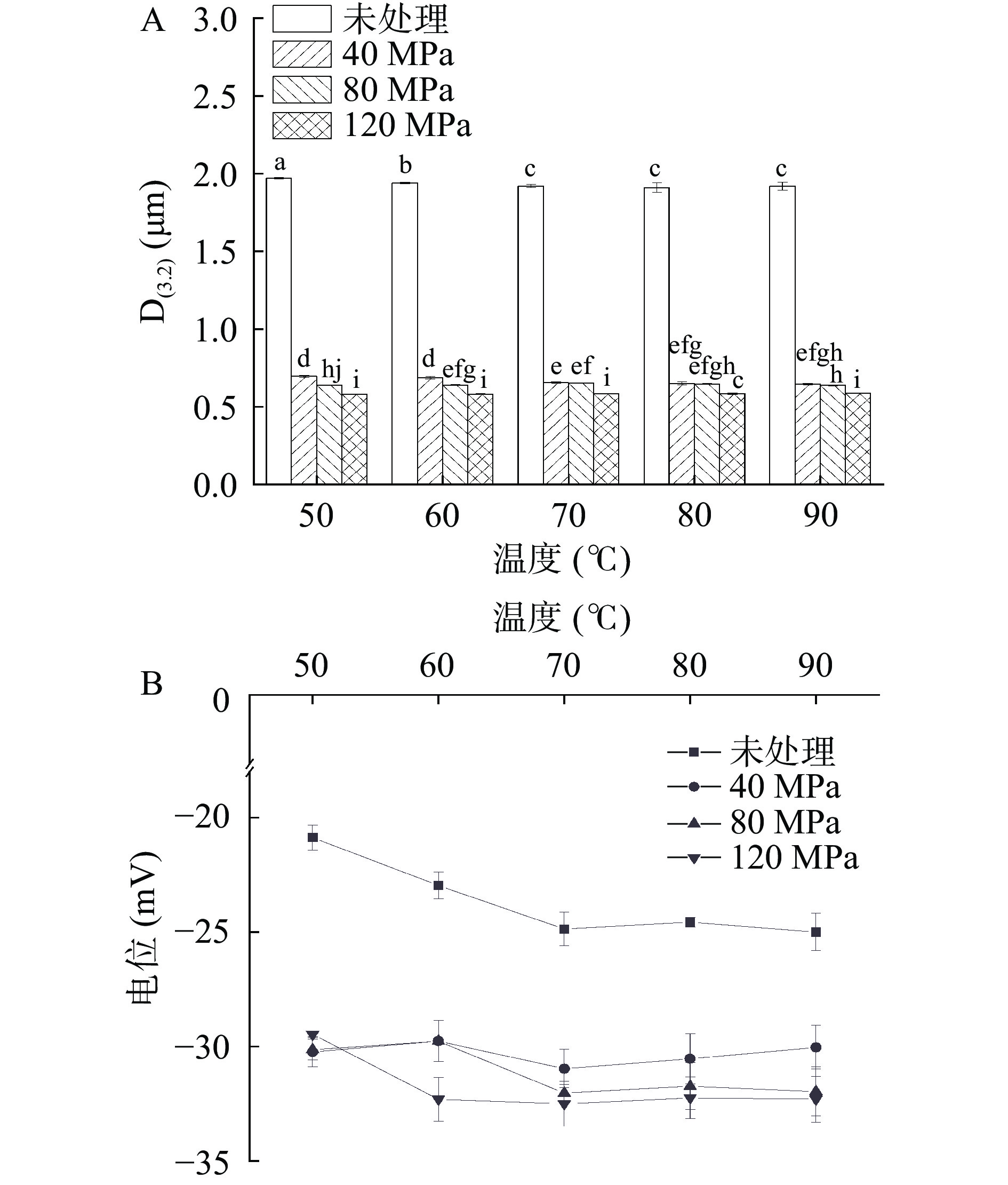
将FOB分别置于50、60、70、80、90 ℃条件下30 min,然后迅速冷却至室温,测定其粒径和观察外观变化。由图6、图7所示,不论是否对FOB进行均质处理,均未出现相分离现象,说明亚麻籽油体的热稳定性良好。由粒径结果可知,在50~90 ℃条件下处理30 min,FOB的平均粒径基本保持不变。电位结果表明,高温处理对FOB的电位影响不大,液滴在高温处理下可以维持较完整的结构,未出现聚集或合并等现象。原因可能是高温并未使与FOB结合的蛋白变性,油体蛋白仍可与FOB紧密结合[31]。油体蛋白是由疏水性中央结构域、N末端和C末端组成,疏水性中央结构嵌入TAG基质中,N/C末端暴露在外部[40]。油体蛋白这种独特的蛋白结构,可能对维持FOB的热稳定性起重要作用[41]。Iwanaga等[42]发现加热处理没有通过表面疏水作用增加蛋白与蛋白之间的相互作用。Ding等[43]在95 ℃下对豆浆加热15 min,对分离的油体粒径以及电位进行分析,发现加热对大豆油体的粒径及电位影响甚微。Chen等[44]考察了大豆油体乳液的热稳定性,大豆油体乳液在热处理后保持稳定,这与本实验研究结果相类似,说明油体乳液具有较好的热稳定性。
2.5 氧化稳定性
FOB可以为人体提供丰富的α-亚麻酸,由于其高度不饱和度而极易被氧化,而氧化产生的味道和气味,不仅会促进自由基的产生外,还会影响产品的货架寿命,这可能会对生物体造成负面的生理影响[45]。因此评估FOB的氧化稳定性对于其实际应用具有重要作用。
将FOB置于50 ℃条件下储藏15 d,通过测定初级氧化产物(过氧化氢)和次级氧化产物(丙二醛)的形成来评价FOB的氧化稳定性。如图8所示,FOB的初始过氧化值较低,这可能是油体独特的结构以及其内部存在如维生素E之类的抗氧化剂结构导致[46]。随着时间的推移,FOB的POV值逐渐上升,TBARs值先上升后下降,随着均质压力的增加,脂质氧化速率随之下降,说明高压均质有利于增强FOB的氧化稳定性。均质压力通常会影响油滴尺寸,目前,关于液滴大小对乳液中脂质氧化快慢的看法众说纷纭。在本研究中,高压均质后的FOB乳液产生的POV 和TBARs含量较低,这与 Wang等[47]的研究一致。Nakaya 等[48]研究了液滴尺寸对多不饱和脂肪酸氧化稳定性的影响,发现油滴大的乳液比油滴小的乳液氧化更快。这可能是因为高压均质处理使得蛋白在界面层快速吸附和重新排列,在油滴周围形成更致密的界面层,提高了乳液的氧化稳定性。
2.6 储藏稳定性
将制备好的FOB放置在4 ℃下储藏56 d,通过对CI和肉眼观察来评价均质对亚麻籽油体储藏稳定性的影响。由表2所示,未处理的FOB第7 d出现乳析现象,而经过均质处理的FOB乳液在14 d内都未出现乳析现象。由图9所示,第6周时,未处理的FOB出现析油现象且具有较厚的乳膏层,而均质处理的FOB乳液未出现析油现象,这说明均质处理可以极大的提高FOB的储藏稳定性。据报道,CI受多种因素影响,例如液滴粒径大小,油滴的絮凝状态以及油滴表面电荷之间的排斥力[49]。均质处理减小了FOB乳液的粒径,形成了小且均匀的液滴,而且电位的绝对值变大,也增大了液滴之间的静电斥力,因此提高了乳液的稳定性。Liang等[50]也报道过通过均质处理破坏絮凝,使得乳液油滴变得小且均匀,因此提高乳液的稳定性。FOB 乳液经过均质处理,其油滴的絮凝状态被破坏,粒径变得小且均匀,有效的提高了自身的稳定性。
表 2 亚麻籽油体储藏期间的乳析指数Table 2. Creaming index of flaxseed oil body during storage储藏天数(d) 未处理的CI(%) 40 MPa的CI(%) 80 MPa的CI(%) 120 MPa的CI(%) 1 0e 0c 0c 0c 7 2.7±0.25d 0c 0c 0c 14 7±0.25c 0c 0c 0c 28 10±0.15b 2.3±0.05b 1.6±0.15b 2.4±0.1b 42 10±0.15b(析油) 2.4±0.3b 2.6±0.15b 2.4±0.1b 56 15±0.15a(析油) 7.2±0.1a 7.3±0.1a 7. 3±0.2a 2.7 消化特性
2.7.1 消化产物的外观形貌
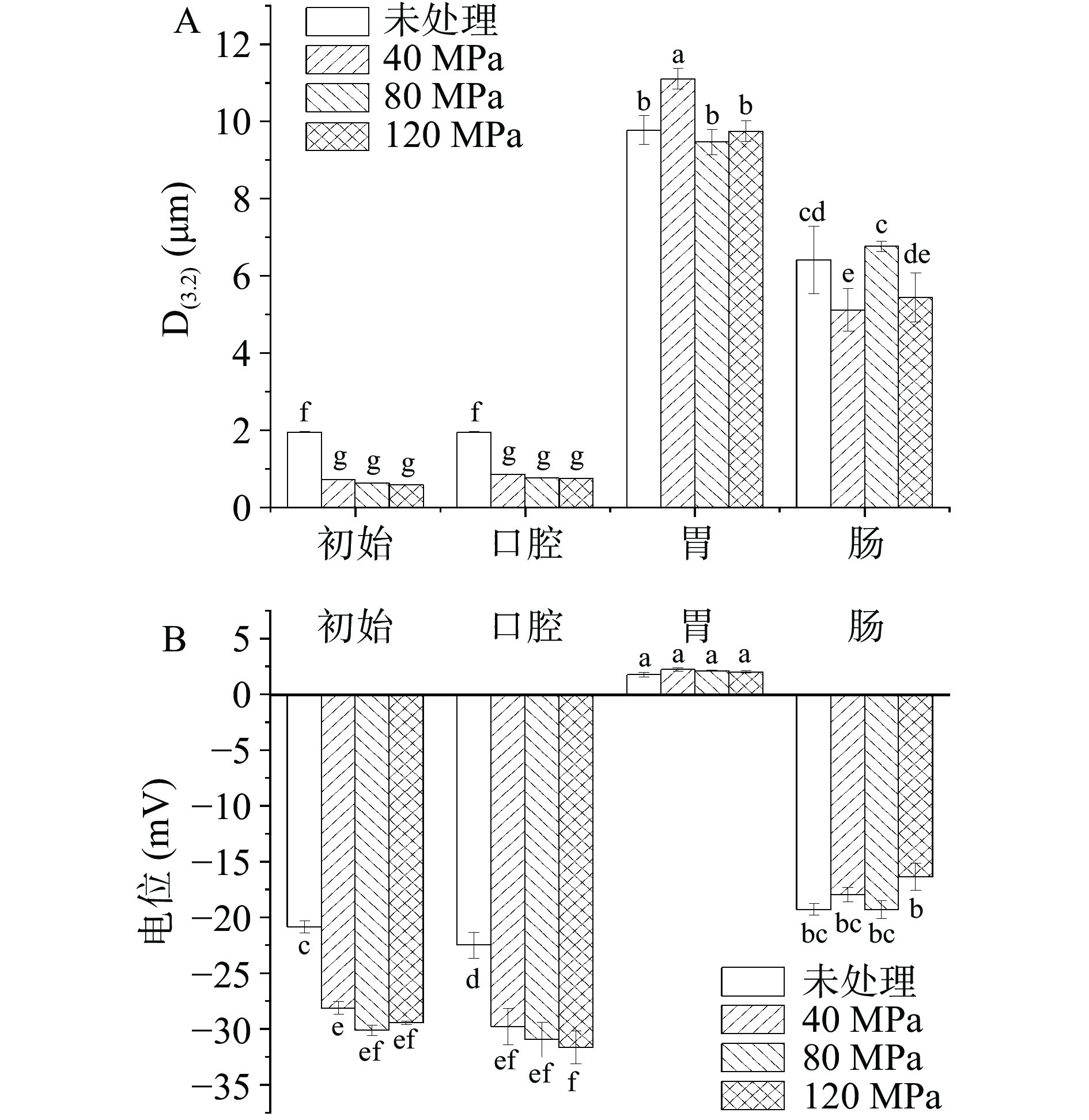
口腔阶段:由图10和图11可知,将所有的FOB暴露在模拟口腔条件下时,其平均粒径以及电位几乎没有变化,这可能是因为模拟口腔液中盐离子浓度不高,FOB可以保持其稳定状态。由共聚焦结果也表明,油滴结构依然保持独立且完整,与粒径测量的结果相符合。Zheng 等[51]也报道过大豆油体乳液在模拟口腔消化阶段保持稳定。
胃部阶段:由图10和图11可知,所有的FOB样品经过模拟胃部条件消化后,其粒径显著增大(P<0.05)。FOB的油滴表面电位均接近于0。这可能是由于在模拟胃液这种强酸性条件下,磷脂和蛋白质上的氨基被质子化,导致负电荷减少,正电荷增加。同时,胃液中的电解质也会通过静电屏蔽作用降低FOB的表面电位。共聚焦显微镜图像可以观察到大油滴的形成,这是由于胃液中的胃蛋白酶水解油体表面的蛋白质,导致FOB失稳,聚集在一起[52]。同时其电位的降低,使得液滴之间几乎没有静电斥力,在疏水作用力以及范德华作用力的吸引下,使得液滴合并成大油滴。
小肠阶段:模拟小肠消化阶段结束后,由图10和图11(A)可知,FOB样品的粒径显著减小(P<0.05),共聚焦显微镜图片也显示,在胃部观察到的大部分大颗粒被分解了,这可能是脂肪酶的作用[53]。电位结果表明,所有样品的电位都变为高负值,这可能是由于消化结束后存在各种类型的阴离子物质,如肽、游离脂肪酸、磷脂和胆盐等[54]。
2.7.2 FFA释放特性结果
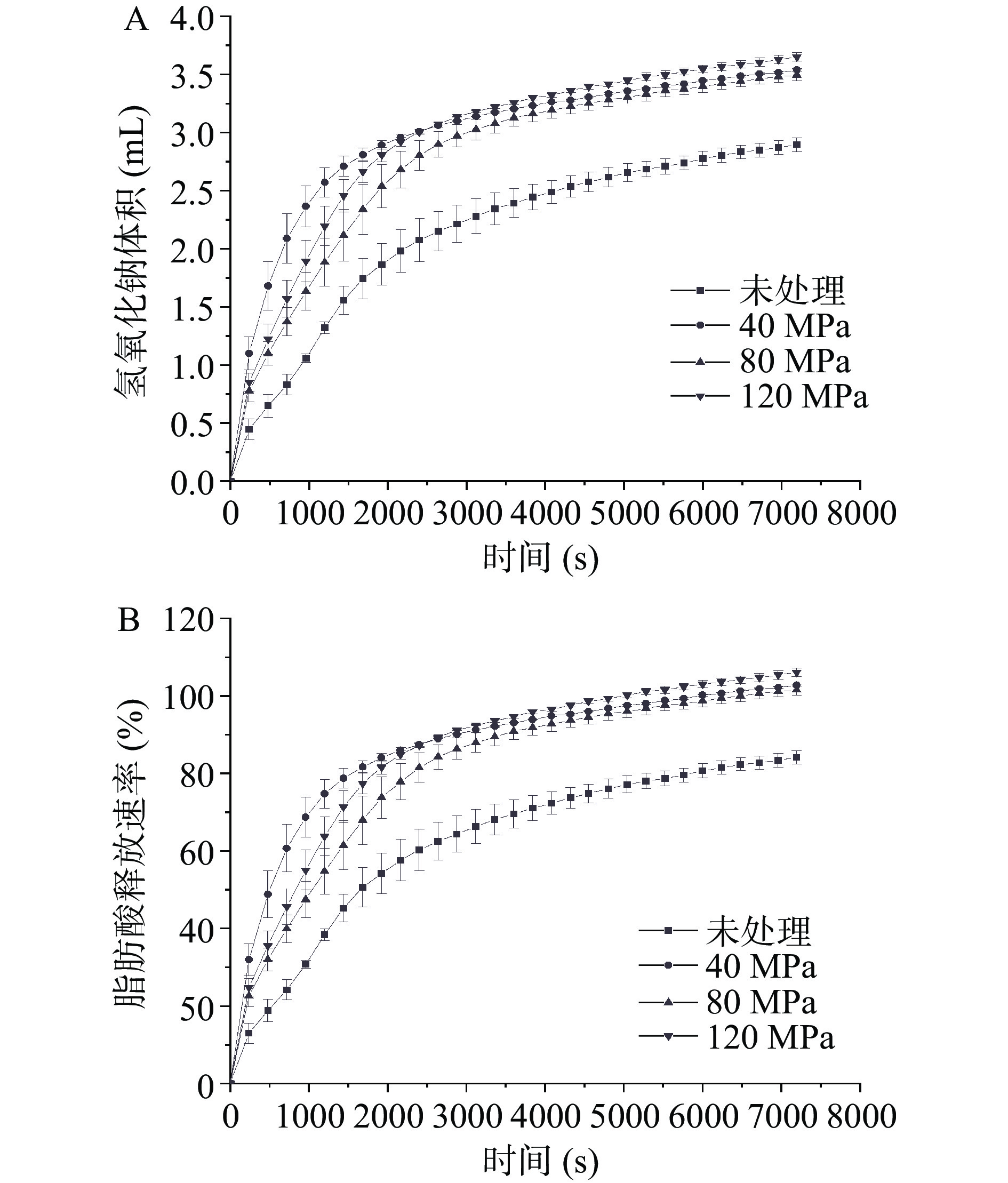
脂质的消化主要发生在小肠中,因此FFA的释放对了解FOB中亚麻籽油的消化程度具有重要作用。由图12可知,所有的FOB样品的消化曲线十分相似,在小肠消化的前30 min内,FOB均具有较高的FFA释放速率,其中均质处理后的FOB的FFA释放率较高(高达73.0%~84.0%),未处理的FOB的FFA释放速率最小,仅为54%,说明均质处理可以提高FOB的初始消化率。30 min后,FOB的FFA释放逐渐减慢,这与Zheng等[51]的报道相符合。FOB样品均具有较高的FFA释放,其中均质处理后的FOB的FFA释放约为100%,而未处理的FOB的FFA释放最低,约为80%,这表明FOB在小肠消化阶段可以较好的被水解。高压均质处理的FOB具有更快FFA释放速率,Li等[55]也报道过乳液脂质的消化速率随着液滴尺寸的减小而增加。人体摄入脂肪过多会带来诸多危害[56-57],较慢的FFA释放速率可以减缓人体对脂肪的吸收,然而对于富含PUFAs的功能性油脂来说,较快的释放速率可能带来更好的脂肪酸吸收[58],同时较快的释放速率也能减少PUFAs在肠道中的破坏。因此,高压均质可以通过改变界面表面积来调节FOB中脂质的消化过程,使其生产出可以满足不同人群营养需求的功能性食品。
3. 结论
本文在保持均质时间(3 min)相同的条件下,分析了均质压力(40、80、120 MPa)和次数(1~3次)对FOB性质的影响,探讨了不同均质压力处理对FOB乳液环境稳定性、储藏稳定性、氧化稳定性及消化特性的影响。结果表明,均质处理对FOB乳液的氧化稳定性、储藏稳定性和消化特性有较大的影响。其中,环境稳定性结果表明,FOB乳液对热处理稳定,对离子强度和pH4~5的条件不稳定,发生了严重的聚集现象。氧化稳定性结果表明,均质处理可以提高FOB乳液的氧化稳定性。对储藏稳定性而言,高压均质导致FOB乳液粒径较小,粒度分布更均匀,未处理的FOB在第7 d出现了明显的乳析现象,均质处理的FOB乳液在第28 d才出现轻微乳析,均质后的FOB乳液具有更好的储藏稳定性。在探究均质处理对FOB消化特性的影响时也发现,经过均质处理的FOB乳液FFA释放速率更快,说明均值处理后的FOB乳液可能存在更好的α-亚麻酸吸收。综上,FOB经过均质处理,乳液粒径显著减小,具有了更好的储藏稳定性和氧化稳定性,更快的脂肪酸(FFA)释放速率。均质处理对于增强FOB乳液稳定性具有显著性的作用,可以为开发稳定的富含α-亚麻酸的亚麻籽油体乳液产品提供参考依据。
-
表 1 不同均质压力及不同均质次数处理下亚麻籽油体的粒径和电位
Table 1 Particle size, zeta potential of flaxseed oil body under different homogenization pressure and different homogenization times
样品 D3.2(μm) D4.3(μm) ξ-电位(mV) 未处理 2.04±0.0115a 3.93±0.2888a −26.47±0.80a 40 MPa处理一次 0.85±0.0010c 1.08±0.0058b −32.67±1.62bc 40 MPa处理二次 0.73±0.0010e 0.80±0.0010de −32.73±1.36bc 40 MPa处理三次 0.69±0.0060g 0.75±0.0010def −34.60±1.91cd 80 MPa处理一次 0.87±0.0010b 1.15±0.0100b −31.93±0.50bc 80 MPa处理二次 0.72±0.0010f 0.88±0.0006cd −31.57±0.86bc 80 MPa处理三次 0.64±0.0010h 0.69±0.0010ef −37.16±0.11d 120 MPa处理一次 0.77±0.0006d 0.99±0.0006bc −30.33±0.12b 120 MPa处理二次 0.61±0.0006i 0.65±0.0006ef −29.97±0.75b 120 MPa处理三次 0.58±0.0006j 0.62±0.0006ef −36.33±0.75d 注:D3.2:体积表面平均粒径;D4.3:体积平均粒径;同列不同字母表示数据之间具有显著性差异(P<0.05),表2同。 表 2 亚麻籽油体储藏期间的乳析指数
Table 2 Creaming index of flaxseed oil body during storage
储藏天数(d) 未处理的CI(%) 40 MPa的CI(%) 80 MPa的CI(%) 120 MPa的CI(%) 1 0e 0c 0c 0c 7 2.7±0.25d 0c 0c 0c 14 7±0.25c 0c 0c 0c 28 10±0.15b 2.3±0.05b 1.6±0.15b 2.4±0.1b 42 10±0.15b(析油) 2.4±0.3b 2.6±0.15b 2.4±0.1b 56 15±0.15a(析油) 7.2±0.1a 7.3±0.1a 7. 3±0.2a -
[1] 韩亚男, 潘士钢, 李海英, 等. 不同产地紫苏籽含油率及α-亚麻酸含量比较[J]. 食品安全导刊,2020(18):102. [HAN Y N, PAN S K, LI H Y, et, al. Comparison of oil content andα-linolenic acid content in perilla seeds from different habitats[J]. China Food Safety Magazine,2020(18):102. [2] 沙爽, 冯启鑫, 张欣蕊, 等. 亚油酸/α-亚麻酸复合物对小鼠急性肝损伤的预防作用(英文)[J]. 食品科学,2022,18:1−18. [SHA S, FENG Q X, ZHANG X R, et, al. Preventive effect of linoleic acid/α-linolenic acid complex on acute liver injury in mice[J]. Food Science,2022,18:1−18. doi: 10.7506/spkx1002-6630-20210716-191 [3] 柏薇薇. α-亚麻酸及其分布[J]. 食品界,2017(12):82. [PAI W W. α-Linolenic acid and its distribution[J]. Food Industry,2017(12):82. [4] 刘静, 胡经纬, 周裔彬. 植物油体的提取及其乳化体系研究进展[J]. 食品工业科技,2021,42(12):422−429. [LIU J, HU J W, ZOU Y B. Advances in the extraction and emulsification system of oil bodies: A review[J]. Science and Technology of Food Industry,2021,42(12):422−429. [5] 徐泽健, 章绍兵. 植物油体制备工艺及其稳定性研究进展[J]. 中国油脂,2016,41(9):41−45. [XU Z J, ZHANG S B. Advance in preparation process and stability of plant oil body[J]. China Oils and Fats,2016,41(9):41−45. [6] 李婷婷 李志远, 孙静, 等. 牡丹油体提取及其稳定性研究[J]. 中国粮油学报,2019,34(8):98−103. [LI T T, LI Z Y, SUN J, et al. Study on extraction and stability of peony oil[J]. Journal of the Chinese Cereals and Oils,2019,34(8):98−103. doi: 10.3969/j.issn.1003-0174.2019.08.017 [7] ZAABOUL F, ZHAO Q, XU Y, et al. Soybean oil bodies: A review on composition, properties, food applications, and future research aspects[J]. Food Hydrocolloids,2022,124:107296. doi: 10.1016/j.foodhyd.2021.107296
[8] LAN X, QIANG W, YANG Y, et al. Physicochemical stability of safflower oil body emulsions during food processing[J]. Lwt,2020,132:109838. doi: 10.1016/j.lwt.2020.109838
[9] LOPEZ C, NOVALES B, RABESONA H, et al. Deciphering the properties of hemp seed oil bodies for food applications: Lipid composition, microstructure, surface properties and physical stability [J]. Food Res Int, 2021, 150(Pt A): 110759.
[10] LIZARRAGA M S, PAN L G, AñON M C, et al. Stability of concentrated emulsions measured by optical and rheological methods. Effect of processing conditions—I. Whey protein concentrate[J]. Food Hydrocolloids,2008,22(5):868−878. doi: 10.1016/j.foodhyd.2007.04.012
[11] WANG Q L, LI CUI C, JIANG L Z, et al. Oil bodies extracted from high-fat and low-fat soybeans: stability and composition during storage[J]. J Food Sci,2017,82(6):1319−1325. doi: 10.1111/1750-3841.13715
[12] 王智丰 雷帆, 武艺, 等. 芝麻油体的稳定性及油体膜蛋白结构分析[J]. 食品科技,2019,44(8):190−196. [WANG Z F, LEI F, WU Y, et al. Stability of sesame oil bodies and structure analysis of oil body proteins[J]. Food Science and Technology,2019,44(8):190−196. [13] 刘竞男 徐晔晔, 王一贺, 等. 高压均质对大豆分离蛋白乳液流变学特性及氧化稳定性的影响[J]. 食品科学,2020,41(1):80−85. [LIU J N, XU Y Y, WANG Y H, et al. Effect of high pressure homogenization on rheological properties and oxidation stability of soy protein isolate-stabilized emulsion[J]. Food Science,2020,41(1):80−85. [14] DE CHIRICO S, DI BARI V, FOSTER T, et al. Enhancing the recovery of oilseed rape seed oil bodies (oleosomes) using bicarbonate-based soaking and grinding media[J]. Food Chemistry,2018,241(15):419−426.
[15] ZHENG B, ZHANG X, LIN H, et al. Loading natural emulsions with nutraceuticals using the pH-driven method: Formation & stability of curcumin-loaded soybean oil bodies[J]. Food & Function,2019,10(9):5473−5484.
[16] ZHU Y Q, CHEN X, MCCLEMENTS D J, et al. Pickering-stabilized emulsion gels fabricated from wheat protein nanoparticles: Effect of pH, NaCl and oil content[J]. Journal of Dispersion Science and Technology,2017,39(6):826−835.
[17] SHANTHA N C, DECKER E A. Rapid, sensitive, iron-based spectrophotometric methods for determination of peroxide values of food lipids[J]. Journal of Aoac International,2020,77(2):421−424.
[18] LI R, DAI T, TAN Y, et al. Fabrication of pea protein-tannic acid complexes: Impact on formation, stability, and digestion of flaxseed oil emulsions[J]. Food Chem,2020,310:125828. doi: 10.1016/j.foodchem.2019.125828
[19] ZOU L, ZHENG B, ZHANG R, et al. Enhancing the bioaccessibility of hydrophobic bioactive agents using mixed colloidal dispersions: Curcumin-loaded zein nanoparticles plus digestible lipid nanoparticles[J]. Food Research International,2016,81(Mara):74−82.
[20] MUNOZ O, FUENTEALBA C, AMPUERO D, et al. The effect of Lactobacillus acidophilus and Lactobacillus casei on the in vitro bioaccessibility of flaxseed lignans (Linum usitatissimum L.)[J]. Food Funct,2018,9(4):2426−2432. doi: 10.1039/C8FO00390D
[21] MCCLEMENTS D J. Principles of ultrasonic droplet size determination in emulsions[J]. Langmuir,1996,12(14):3454−3461. doi: 10.1021/la960083q
[22] 康波. 花生油体乳液稳定性及乳液凝胶的研究[D]. 广州: 华南理工大学, 2010 KANG B, Rerearch on the stability of peanut oil body emulsions and the emulsion gels[D]. Guangzhou: South China University of Technology, 2010
[23] YAN B, PARK S H, BALASUBRAMANIAM V. Influence of high pressure homogenization with and without lecithin on particle size and physicochemical properties of whey protein-based emulsions[J]. Journal of Food Process Engineering,2017,40(6):e12578. doi: 10.1111/jfpe.12578
[24] TANG C H, LIU F. Cold, gel-like soy protein emulsions by microfluidization: Emulsion characteristics, rheological and microstructural properties, and gelling mechanism[J]. Food Hydrocolloids,2013,30(1):61−72. doi: 10.1016/j.foodhyd.2012.05.008
[25] DING Z, JIANG Y, LIU X. Chapter 12 - nanoemulsions-based drug delivery for brain tumors[M]//KESHARWANI P, GUPTA U. Nanotechnology-Based Targeted Drug Delivery Systems for Brain Tumors. Academic Press. 2018: 327−358.
[26] KRSTIĆ M, MEDAREVIĆ Đ, ĐURIŠ J, et al. Chapter 12-Self-nanoemulsifying drug delivery systems (SNEDDS) and self-microemulsifying drug delivery systems (SMEDDS) as lipid nanocarriers for improving dissolution rate and bioavailability of poorly soluble drugs [M]//GRUMEZESCU A M. Lipid Nanocarriers for Drug Targeting. William Andrew Publishing. 2018: 473−508.
[27] CHA Y, SHI X, WU F, et al. Improving the stability of oil-in-water emulsions by using mussel myofibrillar proteins and lecithin as emulsifiers and high-pressure homogenization[J]. Journal of Food Engineering,2019,258(OCTa):1−8.
[28] SUBIRADE M, LOUPIL F, ALLAIN A F, et al. Effect of dynamic high pressure on the secondary structure of β-lactoglobulin and on its conformational properties as determined by fourier transform infrared spectroscopy[J]. International Dairy Journal,1998,8(2):135−140. doi: 10.1016/S0958-6946(98)00034-X
[29] MCCLEMENTS D J. Protein-stabilized emulsions[J]. Current Opinion in Colloid & Interface Science,2004,9(5):305−313.
[30] NEUMANN S M, VAN DER SCHAAF U S, KARBSTEIN H P. Investigations on the relationship between interfacial and single droplet experiments to describe instability mechanisms in double emulsions[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2018,553:464−471. doi: 10.1016/j.colsurfa.2018.05.087
[31] TZEN J T, CAO Y, LAURENT P, et al. Lipids, proteins, and structure of seed oil bodies from diverse species[J]. Plant physiology,1993,101(1):267−276. doi: 10.1104/pp.101.1.267
[32] 齐家兴 廖芮莹, 李红丽, 等. 大豆油体蛋白基因家族的生物信息学分析[J]. 吉林农业大学学报,2021,43(1):51−58. [QI J X, LI H L, WANG S, et, al. Bioinformatics analysis of glycine max oleosin in soybean[J]. Journal of Jilin Agricultural University,2021,43(1):51−58. doi: 10.13327/j.jjlau.2021.4374 [33] DONG X, ZHAO M, YANG B, et al. Effect of high-pressure homogenization on the functional property of peanut protein[J]. Journal of Food Process Engineering,2011,34(6):2191−2204. doi: 10.1111/j.1745-4530.2009.00546.x
[34] LIU H H, KUO M I. Ultra high pressure homogenization effect on the proteins in soy flour[J]. Food Hydrocolloids,2016,52:741−748. doi: 10.1016/j.foodhyd.2015.08.018
[35] YUAN B, REN J, ZHAO M, et al. Effects of limited enzymatic hydrolysis with pepsin and high-pressure homogenization on the functional properties of soybean protein isolate[J]. LWT-Food Science and Technology,2012,46(2):453−459. doi: 10.1016/j.lwt.2011.12.001
[36] 张小影 齐宝坤, 孙禹凡, 等. 盐离子对大豆-乳清混合蛋白液的稳定性及界面特性的影响[J]. 食品工业科技,2021,42(6):22−28. [ZHANG X Y, QI B K, SUN Y F, et al. Effect of salt ion on the stability and interfacial adsorption characteristics of soybean-whey mixed protein emulsion[J]. Science and Technology of Food Industry,2021,42(6):22−28. [37] WANG S N , ZHAO H K, QU D N , et al. Destruction of hydrogen bonding and electrostatic interaction in soy hull polysaccharide: Effect on emulsion stability[J]. Food Hydrocolloids,2022:107304.
[38] HOU J, FENG X, JIANG M, et al. Effect of NaCl on oxidative stability and protein properties of oil bodies from different oil crops[J]. LWT,2019,113:108263. doi: 10.1016/j.lwt.2019.108263
[39] ZHOU L Z, CHEN F S, HAO L H, et al. Peanut oil body composition and stability[J]. Journal of Food Science,2019,84(10):2812−2819. doi: 10.1111/1750-3841.14801
[40] HUANG A H C. Oil bodies and oleosins in seeds[J]. Annual Review of Plant Physiology and Plant Molecular Biology,1992,43(1):177−200. doi: 10.1146/annurev.pp.43.060192.001141
[41] DELEU M, VACA-MEDINA G, FABRE J F, et al. Interfacial properties of oleosins and phospholipids from rapeseed for the stability of oil bodies in aqueous medium[J]. Colloids and Surfaces B: Biointerfaces,2010,80(2):125−132. doi: 10.1016/j.colsurfb.2010.05.036
[42] IWANAGA D, GRAY D A, FISK I D, et al. Extraction and characterization of oil bodies from soy beans: A natural source of pre-emulsified soybean oil[J]. Journal of agricultural and food chemistry,2007,55(21):8711−8716. doi: 10.1021/jf071008w
[43] DING J, WEN J, WANG J, et al. The physicochemical properties and gastrointestinal fate of oleosomes from non-heated and heated soymilk[J]. Food Hydrocolloids,2020,100:105418. doi: 10.1016/j.foodhyd.2019.105418
[44] CHEN B, MCCLEMENTS D J, GRAY D A, et al. Physical and oxidative stability of pre-emulsified oil bodies extracted from soybeans[J]. Food Chem,2012,132(3):1514−1520. doi: 10.1016/j.foodchem.2011.11.144
[45] TONON R V, GROSSO C R F, HUBINGER M D. Influence of emulsion composition and inlet air temperature on the microencapsulation of flaxseed oil by spray drying[J]. Food Research International,2011,44(1):282−9. doi: 10.1016/j.foodres.2010.10.018
[46] FISK I D, WHITE D A, LAD M, et al. Oxidative stability of sunflower oil bodies[J]. European Journal of Lipid Science and Technology,2008,110(10):962−968. doi: 10.1002/ejlt.200800051
[47] WANG Q, JIANG J, XIONG Y L. High pressure homogenization combined with pH shift treatment: A process to produce physically and oxidatively stable hemp milk[J]. Food Res Int,2018,106:487−494. doi: 10.1016/j.foodres.2018.01.021
[48] NAKAYA K , USHIO H , MATSUKAWA S, et al. Effects of droplet size on the oxidative stability of oil-in-water emulsions[J]. Lipids,2005,40(5):501. doi: 10.1007/s11745-005-1410-4
[49] CHANAMAI R, MCCLEMENTS D J. Impact of weighting agents and sucrose on gravitational separation of beverage emulsions[J]. Journal of Agricultural and Food Chemistry,2000,48(11):5561−5565. doi: 10.1021/jf0002903
[50] LIANG H N, TANG C H. pH-dependent emulsifying properties of pea [Pisum sativum (L.)] proteins[J]. Food Hydrocolloids,2013,33(2):309−319. doi: 10.1016/j.foodhyd.2013.04.005
[51] ZHENG B, ZHANG X, PENG S, et al. Impact of curcumin delivery system format on bioaccessibility: Nanocrystals, nanoemulsion droplets, and natural oil bodies[J]. Food Funct,2019,10(7):4339−4349. doi: 10.1039/C8FO02510J
[52] ZOU L, ZHENG B, ZHANG R, et al. Food-grade nanoparticles for encapsulation, protection and delivery of curcumin: Comparison of lipid, protein, and phospholipid nanoparticles under simulated gastrointestinal conditions[J]. RSC Advances,2016,6(4):3126−3136. doi: 10.1039/C5RA22834D
[53] LIANG L, ZHANG X, WANG X, et al. Influence of dairy emulsifier type and lipid droplet size on gastrointestinal fate of model emulsions:In vitro digestion study[J]. J Agric Food Chem,2018,66(37):9761−9769. doi: 10.1021/acs.jafc.8b02959
[54] SINGH H, YE A, HORNE D. Structuring food emulsions in the gastrointestinal tract to modify lipid digestion[J]. Prog Lipid Res,2009,48(2):92−100. doi: 10.1016/j.plipres.2008.12.001
[55] LI Y, HU M, MCCLEMENTS D J. Factors affecting lipase digestibility of emulsified lipids using an in vitro digestion model: Proposal for a standardised pH-stat method[J]. Food Chemistry,2011,126(2):498−505. doi: 10.1016/j.foodchem.2010.11.027
[56] CORSTENS M N, BERTON-CARABIN C C, DE VRIES R, et al. Food-grade micro-encapsulation systems that may induce satiety via delayed lipolysis: A review[J]. Crit Rev Food Sci Nutr,2017,57(10):2218−2244. doi: 10.1080/10408398.2015.1057634
[57] BRAY G A P B M. Dietary fat intake does affect obesity![J]. The American Fournal of Clinical Nutrition,1998,68(6):1157−1173. doi: 10.1093/ajcn/68.6.1157
[58] AARAK K E, KIRKHUS B, HOLM H, et al. Release of EPA and DHA from salmon oil-a comparison of in vitro digestion with human and porcine gastrointestinal enzymes[J]. Br J Nutr,2013,110(8):1402−1410. doi: 10.1017/S0007114513000664
-
期刊类型引用(8)
1. 胡泽茜,李洋,崔琢玉,黄碧飞. 冷链物流环境下时间温度指示器的制备与应用. 农业工程学报. 2023(22): 246-257 .  百度学术
百度学术
2. 钱艳峰,王娅,张明玥,杜子昂,贾靖璇,万祥龙. 用于监测食品新鲜度的时间-温度指示器研究现状. 食品工业科技. 2022(07): 10-20 .  本站查看
本站查看
3. 俞胡斐,钱静. 不可逆变色油墨的配方设计及其制备. 包装工程. 2022(07): 125-131 .  百度学术
百度学术
4. 孙若楠,张敏,夏斯璇,钱静. 胶态酶型时间温度指示器的制备研究. 包装工程. 2022(09): 115-121 .  百度学术
百度学术
5. 俞胡斐,钱静. 不可逆温敏变色油墨的显色动力学探究. 包装工程. 2022(11): 46-53 .  百度学术
百度学术
6. 张博云,张宇,李庆山,高雪峰,李娇,寇俊杰,徐凤波. 羧甲基纤维素钠/聚乙烯吡咯烷酮与独活提取物复合涂膜对柑橘果实的保鲜效果. 食品工业科技. 2022(22): 353-364 .  本站查看
本站查看
7. 刘冬青,陈朴,臧鹏,杜秉健,徐楠,向红. 时间-温度指示器在食品保质期预测中的应用. 食品工业科技. 2021(22): 1-10 .  本站查看
本站查看
8. 康峻菡,胥义. 基于扩散型TTI与鲜银耳品质关联模型的建立及验证. 中国农学通报. 2020(32): 130-139 .  百度学术
百度学术
其他类型引用(8)






 下载:
下载:






 下载:
下载:



