Simultaneous Determination of 9 Biogenic Amines in Larimichthys polyactis by UHPLC-MS/MS
-
摘要: 为快速检测水产品中精胺、亚精胺、腐胺、尸胺、组胺、色胺、章鱼胺、酪胺、2-苯乙胺9种生物胺含量,本研究以小黄花鱼为基质,优化了流动相组成和样品提取溶剂,建立了超高效液相色谱-串联三重四极杆质谱同时检测方法。样品经0.1%三氯乙酸水溶液重复提取两遍,合并上清液过0.22 μm聚四氟乙烯滤膜。以HSS T3为色谱柱,流动相A为0.1%甲酸乙腈,流动相B为10 mmol/L甲酸铵水溶液含0.2%甲酸,在电喷雾正离子电离、多反应监测模式下,9种生物胺在4 min内得到分离。根据响应强度不同,9种生物胺分成酪胺、2-苯乙胺,腐胺、尸胺、组胺、色胺、章鱼胺,精胺、亚精胺三组,以1:5:25浓度比配制多浓度混合标准中间液。该方法对三组生物胺的线性范围分别为1~40 ng/mL、5~200 ng/mL和25~1000 ng/mL;方法定量限依次为0.01、0.05和0.25 mg/kg。低、中、高三个浓度水平加标回收率分别为81.7%~111.2%、80.0%~110.3%、80.0%~99.0%;精密度(n=6)依次为1.7%~7.3%、1.3%~9.1%、0.7%~4.6%。总体而言,该方法简便、快速,具有良好的灵敏度、回收率和精密度,适用于小黄花鱼中生物胺的测定。
-
关键词:
- 生物胺 /
- 超高效液相色谱-串联质谱 /
- 小黄花鱼
Abstract: To rapidly determine 9 biogenic amines including spermine, spermidine, putrescine, cadaverine, histamine, tryptamine, octopamine, tyramine and β-phenethylamine in aquatic products, the ultra high-performance liquid chromatography-tandem mass spectrometry method was established with Larimichthys polyactis using as matrix sample, and mobile phase and extract solvents were optimized. Matrix sample was extracted by 0.1% trichloroacetic acid (TCA) in duplicate, the supernatant was combined and filtered by 0.22 μm PTFE filters, and separated by HSS T3 column in 4 min. The mobile phase A was acetonitrile containing 0.1% formic acid, while mobile phase B was 10 mmol/L ammonium formate containing 0.2% formic acid. Nine biogenic amines were divided into three groups based on their different response intensity, with a concentration range of 1 to 40 ng/mL (tyramine and β-phenethylamine), 5 to 200 ng/mL (putrescine, cadaverine, histamine, tryptamine and octopamine), and 25 to 1000 ng/mL (spermine and spermidine). Their method quantification limits (LOQs) were 0.01, 0.05 and 0.25 mg/kg, respectively. The recovery rate of low, medium and high concentrations was 81.7%~111.2%, 80.0%~110.3% and 80.0%~99.0%, respectively, with the corresponding degree of precision (n=6) of 1.7%~7.3%, 1.3%~9.1% and 0.7%~4.6%. This method is simple, fast and with good sensitivity, recovery and precision, which is suitable for the determination of biogenic amines in Larimichthys polyactis. -
黄花鱼又名黄鱼,分为大黄鱼和小黄鱼,分别为我国四大海洋渔业品种之一[1],广泛分布于南海、东海和黄海,营养丰富,肉质鲜美,深受广大消费者的喜爱[2]。除了鲜食之外,黄花鱼还可加工成鱼糜[3-4]、鱼罐头[5]、鱼露[6]、黄花鱼干[7]等系列产品,随着人们日益增长的食品安全意识,水产及其制品中生物胺、亚硝胺的安全问题越来越受到消费者的关注[8-9]。
生物胺广泛存在于生物体及多种食品中,是一类极性或半极性含氮低分子有机物[10-11]。根据分子结构特征可分为脂肪族胺、芳香族胺和杂环胺;根据氨基数目可分为单胺和多胺[12-13]。常见的生物胺有腐胺、尸胺、精胺、亚精胺、酪胺、2-苯乙胺、章鱼胺、组胺、色胺等。生物胺是生物体内蛋白质或游离氨基酸脱羧作用、醛和酮的氨基化/转氨作用等生化反应的产物[14],在人和动物消化、呼吸、循环代谢等过程中发挥重要生理作用[15]。但若在人体内累积到一定程度,将会引发头疼、高血压、发烧、皮疹、呕吐等中毒反应[16-17]。腐胺、尸胺、精胺和亚精胺还可与亚硝酸盐反应生成具有致癌毒性的亚硝胺[18-19],若不加以控制,将为下游产业水产加工制品带来风险隐患。此外,生物胺是食品新鲜程度、生产过程卫生条件重要判断指标[20-21]。现有研究集中于青皮红肉高组胺鱼类(如鲐鱼[22]、鲣鱼[23]、三文鱼[24]、鲅鱼[25]等)、腌制水产品[26-27]及发酵水产品[28]中生物胺的变化规律。而黄花鱼等白肉鱼类及其鱼鲞制品生物胺质量指标研究较为缺乏。
因此,本研究以新鲜小黄花鱼(Larimichthys polyactis)为原料,通过改变流动相组成,优化样品提取方法,建立快速简便的9种生物胺同时检测的超高效液相色谱-质谱方法,为小黄花鱼中生物胺含量的快速测定、新鲜度判断及其加工制品中亚硝胺生成风险研究提供实验基础。
1. 材料与方法
1.1 材料与仪器
新鲜小黄花鱼 购于台州市椒江区界牌农贸市场;腐胺、尸胺、精胺、亚精胺、酪胺、2-苯乙胺、组胺、色胺、章鱼胺 德国Dr.Ehrenstorfer,纯度均大于98%,供应商为上海安谱实验科技股份有限公司;乙腈 色谱级,美国Merk;甲酸、甲酸铵 AR,上海麦克林;三氯乙酸(简称TCA) AR,上海阿拉丁;试验用水 由Milli-Q Advatage A10超纯水系统制备;0.22 μm聚四氟乙烯(PTFE)过滤膜 上海迪马。
AB SCIEX QTRAP®5500超高效液相色谱-三重四极杆线性离子阱质谱仪 美国AB SCIEX;ACQUITY HSS T3 色谱柱(2.1 mm×100 mm, 1.8 µm) 美国Waters;Allegra X-30R型台式高速冷冻离心机 美国贝克曼库尔特;MQ7035X型手持式搅拌机 德国BRAUN;MS204S/01电子天平、Metrohm 809自动电位滴定仪 瑞士梅特勒-托利多;Multi Reax涡旋混合器 德国Heidolph;Milli-Q Advantage A10超纯水机 美国Millipore。
1.2 实验方法
1.2.1 标准溶液的配制
腐胺、尸胺、酪胺、2-苯乙胺、组胺、色胺和章鱼胺以8:2乙腈水(v/v)分别溶解配制成1 mg/mL单一标准储备液;精胺、亚精胺以纯水溶解配制成1 mg/mL单一标准储备液,于4 ℃避光保存。
分别准确移取0.02 mL酪胺、2-苯乙胺;0.1 mL腐胺、尸胺、组胺、色胺和章鱼胺;0.5 mL精胺、亚精胺于同一10.00 mL容量瓶中,以0.5%甲酸水溶液(v/v)[29]定容至刻度,配制成多浓度混合标准中间液。实验中根据需要配制标准工作曲线。
1.2.2 色谱条件
色谱柱:ACQUITY HSS T3 柱(2.1 mm×100 mm, 1.8 µm),柱温:40 ℃;进样量5 μL。梯度洗脱程序如表1所示。流速:0.3 mL/min;流动相A:0.1%甲酸乙腈;本实验分别考察以0.5%甲酸水溶液、5 mmol/L甲酸铵0.1%甲酸水溶液、10 mmol/L甲酸铵0.2%甲酸水溶液、20 mmol/L甲酸铵0.4%甲酸水溶液为流动相B,对9种生物胺色谱峰形及相应的影响。
表 1 流动相梯度洗脱程序Table 1. The linear gradient program of mobile phase时间(min) 流动相A(%) 流动相B(%) 0 5 95 0.3 5 95 4.5 50 50 5.0 95 5 6.5 95 5 6.6 5 95 8.0 5 95 1.2.3 质谱条件
采用电喷雾正离子扫描多反应监测;离子源温度500 ℃;气帘气压力 2.07×105 Pa;喷雾气压力3.45×105 Pa;辅助气压力3.45×105 Pa;碰撞气为氮气。9种生物胺多反应监测扫描模式质谱参数如表2所示。
表 2 九种生物胺多反应监测扫描模式的质谱参数Table 2. Parameters of MS/MS for 9 biogenic amines (BAs) MRM mode化合物 质荷比(m/z) 去簇电压(V) 碰撞电压(V) 母离子 子离子 精胺 203.2 129.1*
112.155
12025
47亚精胺 146.0 129.1*
112.140
4016
19腐胺 89.0 72.0*
30.050
5015
15尸胺 103.2 86.0*
69.143
5014
21组胺 112.2 94.7*
68.171
7025
29色胺 161.1 144.1*
117.140
4116
35章鱼胺 154.0 136.2*
91.145
3111
29酪胺 138.0 77.0*
93.043
4243
242-苯乙胺 122.0 105.2*
79.141
4219
31注:*为定量离子。 1.2.4 样品前处理
1.2.4.1 样品制备及提取
新鲜的中等大小小黄花鱼1 kg(约10条),去鳞片,去内脏,洗净,用吸水纸吸干表面水分,剥去鱼皮,取可食纯鱼肉用手持式搅拌机打成肉糜。准确称取0.5 g均质好的鱼肉样品于50.0 mL离心管中,加入10 mL提取溶液,涡旋振荡20 min,在4 ℃下8000 r/min离心5 min,重复提取两次,合并上清液定容至20 mL,涡旋混匀,取上清液过0.22 μm聚四氟乙烯滤膜,滤液待液相色谱-质谱联用仪检测。
1.2.4.2 提取液的选择
为减少样品基质干扰,同时减少有机试剂的使用,结合相关文献,本实验对比0.05% TCA水溶液、0.1% TCA水溶液和0.1% TCA水溶液:乙腈(体积比9:1)三种提取液对同一样品的提取效率,通过三个不同浓度水平加标实验考察三种提取液的回收率及精密度。
1.2.5 样品检测
在不同摊位购买小黄花鱼样品5份,编号为小黄花鱼I、小黄花鱼II、小黄花鱼III、小黄花鱼IV和小黄花鱼V,购买水潺、鲳鱼、带鱼、墨鱼、鱿鱼、南美白对虾、红虾7个新鲜水产样品及1个死后3~5 h的南美白对虾样品,对13份样品按照建立的方法开展9种不同生物胺含量的检测。
1.3 数据处理
采集的数据经Multi Quant 3.0.2软件进行定性、定量分析,小黄花鱼肉中生物胺含量数据为6次独立重复实验的平均值,以平均值±标准偏差表示。采用SPSS 22.0软件中的单因素方差分析和Duncan多次比较法进行数据统计分析,P<0.05即认为差异显著。加标回收率和精密度试验则进行6次独立重复试验。以Excel 2016整理数据及绘制图表。
2. 结果与分析
2.1 四种不同流动相中9种生物胺的峰形及响应强度
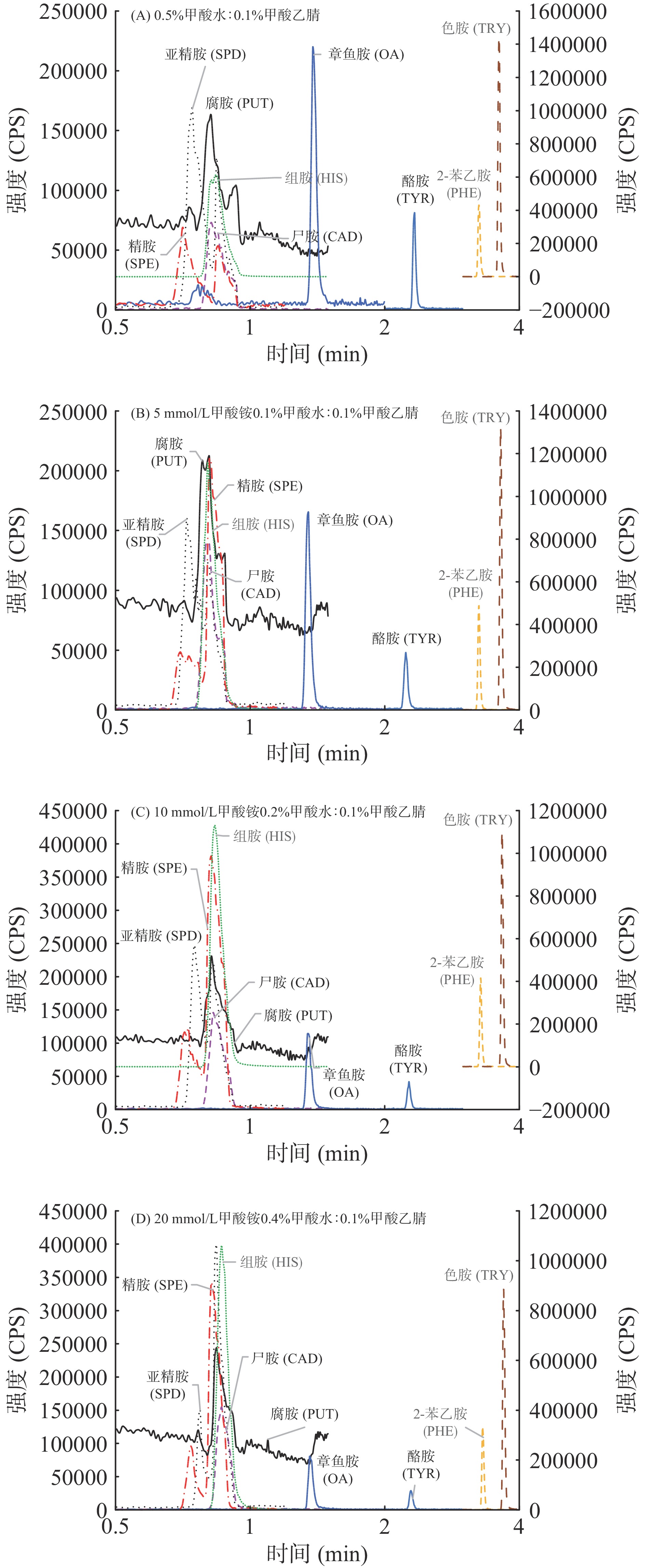
本研究中腐胺等9种生物胺均属于强极性小分子化合物,溶液pH和离子强度不仅影响化合物色谱峰形,还影响其电喷雾离子化效率,进而影响检测灵敏度。ZHANG等[30]调整进样液pH至3.0;HUANG等[31]调整pH至3.72~4.00。为此,本研究中将流动相B的pH调节至3.0附近。为获得较好地分离和响应,保持流动相A为0.1%甲酸乙腈不变,实验比较了0.5%甲酸水(pH2.26)、5 mmol/L甲酸铵0.1%甲酸水溶液(pH3.02)、10 mmol/L甲酸铵0.2%甲酸水溶液(pH3.03)及20 mmol/L甲酸铵0.4%甲酸水溶液(pH3.02)四组不同流动相B对色谱峰的影响。500 ng/mL精胺、亚精胺;50 ng/mL腐胺、尸胺、组胺、色胺和章鱼胺;5 ng/mL酪胺、2-苯乙胺在四组不同流动相中的色谱图如图1所示。
按氨基数目来分,精胺、亚精胺、腐胺和尸胺属于多胺,组胺、色胺、章鱼胺、酪胺和2-苯乙胺属于单胺。图1结果表明,增加甲酸铵浓度可改善多胺化合物峰形、增强响应,但与单胺化合物的响应强度呈负相关。流动相中不同浓度甲酸铵对组胺响应强度影响不大,但高于其在0.5%甲酸水中的响应;色胺、酪胺的响应强度随流动相中甲酸铵浓度增加而降低;章鱼胺在流动相B为0.5%甲酸水环境下响应最高,但在0.7~0.9 min有干扰,而随着甲酸铵浓度增加,章鱼胺的响应逐渐降低;2-苯乙胺在5 mmol/L甲酸铵0.1%甲酸水中响应强度最高,在20 mmol/L甲酸铵0.4%甲酸水中响应强度最低。为兼顾峰形和响应强度,本研究选用10 mmol/L甲酸铵0.2%甲酸水溶液为流动相B。
2.2 三种不同提取溶剂提取效率
生物胺类物质多为水溶性小分子,精胺、亚精胺不溶于纯乙腈。孙亚军等[32]优化提取溶剂,发现乙醇、乙腈等有机溶剂对8种生物胺提取效果均未超过50%。为此,试验分别以0.05%TCA水溶液、0.1%TCA水溶液、0.1%TCA水溶液:乙腈(9:1,v/v)作为提取溶剂,对新鲜小黄花鱼中的生物胺进行三个浓度水平加标回收试验,其中精胺、亚精胺添加水平分别为8、15、40 mg/kg;腐胺、尸胺、组胺、色胺和章鱼胺添加水平分别为1.6、3.0、8.0 mg/kg;酪胺和2-苯乙胺添加水平分别为0.32、0.60、1.60 mg/kg。每个浓度设定6个重复实验,以检验方法的精密度。
生物胺含量受实验选取的样品新鲜程度影响较大,有研究表明鲜活水产品中几乎不含生物胺,或仅含少量精胺、亚精胺[32],而本研究中购买的新鲜小黄花鱼样品中仅检出精胺、亚精胺和腐胺,结果如表3本底值所示。三种提取溶剂中,0.1%TCA水溶液对腐胺提取效果最佳;而对于精胺和亚精胺来说,0.05%TCA水溶液提取效果差。
表 3 不同提取溶剂中小黄花鱼生物胺加标回收率与精密度 (n=6)Table 3. Recoveries and precision of 9 BAs spiked in Larimichthys polyactis by different extract solvents (n=6)化合物 添加量
(mg/kg)0.05% TCA水溶液 0.1% TCA水溶液 0.1% TCA水溶液:乙腈(9:1,v/v) 本底值(mg/kg) 回收率(%) RSD(%) 本底值(mg/kg) 回收率(%) RSD(%) 本底值(mg/kg) 回收率(%) RSD(%) 精胺 8
15
400.23±0.03a 85.6
87.8
79.73.5
3.2
1.81.77±0.05c 106.2
103.8
94.31.7
9.1
1.11.52±0.05b 74.6
82.5
99.81.8
1.6
1.4亚精胺 8
15
400.35±0.01a 62.8
79.7
91.02.8
2.5
2.00.74±0.03c 111.2
110.3
99.03.6
3.8
1.30.68±0.03b 89.5
113.1
90.26.7
1.7
1.2腐胺 1.6
3.0
8.01.15±0.03b 107.4
91.9
73.31.3
1.4
0.91.38±0.08c 103.2
98.9
80.76.6
1.3
2.91.02±0.04a 102.7
92.4
75.23.1
3.3
0.8尸胺 1.6
3.0
8.078.8
72.0
72.95.3
1.1
1.190.3
83.7
80.47.3
5.7
1.680.7
73.3
72.36.0
4.1
1.9组胺 1.6
3.0
8.079.0
62.8
60.22.3
5.2
1.487.6
88.0
87.43.3
4.7
1.385.6
73.3
72.32.8
4.1
0.7色胺 1.6
3.0
8.085.4
80.2
64.55.3
4.8
2.588.1
80.5
80.25.7
7.7
4.689.2
78.8
75.23.6
1.4
1.7章鱼胺 1.6
3.0
8.057.5
56.1
59.98.6
4.5
1.185.3
80.5
80.45.6
7.0
1.670.0
70.2
70.25.9
1.1
1.2酪胺 0.32
0.60
1.6066.8
67.2
64.25.4
4.2
2.281.7
80.0
80.05.9
2.4
0.775.2
62.5
70.12.9
4.4
1.02-苯乙胺 0.32
0.60
1.6091.3
86.4
90.36.4
5.4
0.992.4
90.4
91.34.3
4.1
2.289.7
91.2
89.95.2
2.5
0.7注:不同提取溶剂对小黄花鱼中同种生物胺本底的检测结果采用Duncan’s 多重比较;同行不同小写字母表示分析结果差异显著(P<0.05)。 不同提取溶剂的加标回收率与精密度结果见表3。因小黄花鱼基质中含有精胺、亚精胺和腐胺,加标回收率以黄花鱼加标样品检测平均值(n=6)与空白基质(n=6)的差值与实际加标量的比值表示。表3结果显示,9种生物胺低、中、高三浓度水平在0.05%TCA水溶液中的加标回收率分别为57.5%~107.4%、56.1%~91.9%、59.9%~91.0%,精密度依次为1.3%~8.6%、1.1%~5.4%、0.9%~2.5%;在0.1% TCA水溶液中的加标回收率分别为81.7%~111.2%、80.0%~110.3%、80.0%~99.0%,精密度依次为1.7%~7.3%、1.3%~9.1%、0.7%~4.6%;在0.1% TCA水溶液:乙腈(9:1,v/v)中的加标回收率分别为70.0%~102.7%、62.5%~113.1%、70.1%~99.8%,精密度依次为1.8%~6.7%、1.1%~4.1%、0.7%~1.9%。综合考虑,选用0.1% TCA水溶液作为提取溶剂。
2.3 方法的线性范围、检出限和定量限
根据各化合物在仪器中的响应不同,将9种生物胺分成三组,其中酪胺和2-苯乙胺响应最高;精胺和亚精胺响应最差。配制酪胺、2-苯乙胺标准工作液浓度范围为1~40 ng/mL;精胺、亚精胺标准工作液浓度范围为25~1000 ng/mL;其余五种生物胺标准工作液浓度范围为5~200 ng/mL。以浓度为横坐标,定量离子对峰面积为纵坐标建立标准曲线。9种生物胺在相应的浓度范围内线性关系良好,相关系数r均大于0.995。以3倍信噪比(S/N=3)、10倍信噪比(S/N=10)所对应的浓度分别作为方法检出限和定量限。9种生物胺线性实验结果、检出限和定量限见表4。
表 4 九种生物胺的线性范围、回归方程、相关系数(r)、检出限和定量限Table 4. Linear range, calibration curves, correlation coefficient (r), limit of detection (LOD) and limit of quantitation (LOQ) of 9 BAs化合物 线性范围(ng/mL) 回归方程 相关系数r 检出限(mg/kg) 定量限(mg/kg) 精胺 25~1000 y=3317.9x−25504 0.9992 0.05 0.25 亚精胺 25~1000 y=2396.4x+45234 0.9988 0.05 0.25 腐胺 5~200 y=4902.3x+265395 0.9956 0.01 0.05 尸胺 5~200 y=8235x+116707 0.9954 0.01 0.05 组胺 5~200 y=67903x+530114 0.9974 0.01 0.05 色胺 5~200 y=56051x+234899 0.9987 0.01 0.05 章鱼胺 5~200 y=5197.7x+22794 0.9988 0.01 0.05 酪胺 1~40 y=22708x+1850.3 0.9999 0.003 0.01 2-苯乙胺 1~40 y=219501x+5405.5 0.9999 0.003 0.01 2.4 实际样品的检测
新鲜小黄花鱼、水潺、鲳鱼、带鱼、墨鱼、鱿鱼、南美白对虾、红虾及死后3~5 h的南美白对虾中9种生物胺含量检测结果如表5所示。数据显示,死后的南美白对虾,其体内腐胺、尸胺明显增加。
表 5 不同水产品中9种生物胺含量的测定结果(mg/kg, n=6)Table 5. The detection results of 9 BAs in different aquatic products (mg/kg, n=6)样品 精胺 亚精胺 腐胺 尸胺 组胺 色胺 章鱼胺 酪胺 2-苯乙胺 小黄花鱼I 1.64±0.14 0.67±0.04 1.26±0.05 / / / / / / 小黄花鱼II 1.79±0.05 0.63±0.11 1.38±0.21 / / / / / / 小黄花鱼III 1.54±0.19 0.52±0.03 1.42±0.16 / / / / / / 小黄花鱼IV 1.92±0.31 0.72±0.15 1.55±0.19 / / / / / / 小黄花鱼V 1.47±0.22 0.65±0.02 1.48±0.09 / / / / / / 水潺 2.02±0.21 3.21±0.24 3.69±0.12 / / / / / / 鲳鱼 1.18±0.05 0.85±0.03 3.27±0.02 0.20±0.03 / / / 0.15±0.14 / 带鱼 1.06±0.08 0.48±0.05 0.84±0.05 / / / / / / 墨鱼 7.64±0.19 1.81±0.14 1.90±0.16 3.07±0.14 / / / / / 鱿鱼 21.3±3.07 4.06±0.30 1.49±0.17 1.58±0.10 / / / / / 红虾 0.73±0.03 0.64±0.00 / 0.34±0.01 / / / 0.65±0.00 0.26±0.01 南美白对虾 0.69±0.02 0.76±0.00 / 0.57±0.01 / / / 0.75±0.04 / 死后3~5 h南美白对虾 0.71±0.01 3.16±0.36 2.34±0.17 9.80±0.16 / / / 1.01±0.03 / 注:“/”表示未检出。 3. 结论
本研究建立了超高效液相色谱-质谱法同时检测小黄花鱼中9种生物胺的非衍生化方法。9种生物胺在正离子MRM模式下经HSS T3色谱柱分离,4 min内可完成检测,其线性范围分别为酪胺、2-苯乙胺1~40 ng/mL,腐胺、尸胺、色胺、章鱼胺、组胺5~200 ng/mL,精胺、亚精胺25~1000 ng/mL。方法的定量限为0.01~0.25 mg/kg。样品以0.1%TCA溶液提取,三浓度水平加标实验中(n=6),样品的平均回收率在80.0%~111.2%,RSD在0.7%~9.1%。本研究建立的方法操作简便、检测耗时短,试剂用量少、经济成本低,灵敏度高,回收率良好。该方法为后续研究原料中生物胺含量对水产加工制品N-亚硝胺生成量的影响提供一定的基础。
-
表 1 流动相梯度洗脱程序
Table 1 The linear gradient program of mobile phase
时间(min) 流动相A(%) 流动相B(%) 0 5 95 0.3 5 95 4.5 50 50 5.0 95 5 6.5 95 5 6.6 5 95 8.0 5 95 表 2 九种生物胺多反应监测扫描模式的质谱参数
Table 2 Parameters of MS/MS for 9 biogenic amines (BAs) MRM mode
化合物 质荷比(m/z) 去簇电压(V) 碰撞电压(V) 母离子 子离子 精胺 203.2 129.1*
112.155
12025
47亚精胺 146.0 129.1*
112.140
4016
19腐胺 89.0 72.0*
30.050
5015
15尸胺 103.2 86.0*
69.143
5014
21组胺 112.2 94.7*
68.171
7025
29色胺 161.1 144.1*
117.140
4116
35章鱼胺 154.0 136.2*
91.145
3111
29酪胺 138.0 77.0*
93.043
4243
242-苯乙胺 122.0 105.2*
79.141
4219
31注:*为定量离子。 表 3 不同提取溶剂中小黄花鱼生物胺加标回收率与精密度 (n=6)
Table 3 Recoveries and precision of 9 BAs spiked in Larimichthys polyactis by different extract solvents (n=6)
化合物 添加量
(mg/kg)0.05% TCA水溶液 0.1% TCA水溶液 0.1% TCA水溶液:乙腈(9:1,v/v) 本底值(mg/kg) 回收率(%) RSD(%) 本底值(mg/kg) 回收率(%) RSD(%) 本底值(mg/kg) 回收率(%) RSD(%) 精胺 8
15
400.23±0.03a 85.6
87.8
79.73.5
3.2
1.81.77±0.05c 106.2
103.8
94.31.7
9.1
1.11.52±0.05b 74.6
82.5
99.81.8
1.6
1.4亚精胺 8
15
400.35±0.01a 62.8
79.7
91.02.8
2.5
2.00.74±0.03c 111.2
110.3
99.03.6
3.8
1.30.68±0.03b 89.5
113.1
90.26.7
1.7
1.2腐胺 1.6
3.0
8.01.15±0.03b 107.4
91.9
73.31.3
1.4
0.91.38±0.08c 103.2
98.9
80.76.6
1.3
2.91.02±0.04a 102.7
92.4
75.23.1
3.3
0.8尸胺 1.6
3.0
8.078.8
72.0
72.95.3
1.1
1.190.3
83.7
80.47.3
5.7
1.680.7
73.3
72.36.0
4.1
1.9组胺 1.6
3.0
8.079.0
62.8
60.22.3
5.2
1.487.6
88.0
87.43.3
4.7
1.385.6
73.3
72.32.8
4.1
0.7色胺 1.6
3.0
8.085.4
80.2
64.55.3
4.8
2.588.1
80.5
80.25.7
7.7
4.689.2
78.8
75.23.6
1.4
1.7章鱼胺 1.6
3.0
8.057.5
56.1
59.98.6
4.5
1.185.3
80.5
80.45.6
7.0
1.670.0
70.2
70.25.9
1.1
1.2酪胺 0.32
0.60
1.6066.8
67.2
64.25.4
4.2
2.281.7
80.0
80.05.9
2.4
0.775.2
62.5
70.12.9
4.4
1.02-苯乙胺 0.32
0.60
1.6091.3
86.4
90.36.4
5.4
0.992.4
90.4
91.34.3
4.1
2.289.7
91.2
89.95.2
2.5
0.7注:不同提取溶剂对小黄花鱼中同种生物胺本底的检测结果采用Duncan’s 多重比较;同行不同小写字母表示分析结果差异显著(P<0.05)。 表 4 九种生物胺的线性范围、回归方程、相关系数(r)、检出限和定量限
Table 4 Linear range, calibration curves, correlation coefficient (r), limit of detection (LOD) and limit of quantitation (LOQ) of 9 BAs
化合物 线性范围(ng/mL) 回归方程 相关系数r 检出限(mg/kg) 定量限(mg/kg) 精胺 25~1000 y=3317.9x−25504 0.9992 0.05 0.25 亚精胺 25~1000 y=2396.4x+45234 0.9988 0.05 0.25 腐胺 5~200 y=4902.3x+265395 0.9956 0.01 0.05 尸胺 5~200 y=8235x+116707 0.9954 0.01 0.05 组胺 5~200 y=67903x+530114 0.9974 0.01 0.05 色胺 5~200 y=56051x+234899 0.9987 0.01 0.05 章鱼胺 5~200 y=5197.7x+22794 0.9988 0.01 0.05 酪胺 1~40 y=22708x+1850.3 0.9999 0.003 0.01 2-苯乙胺 1~40 y=219501x+5405.5 0.9999 0.003 0.01 表 5 不同水产品中9种生物胺含量的测定结果(mg/kg, n=6)
Table 5 The detection results of 9 BAs in different aquatic products (mg/kg, n=6)
样品 精胺 亚精胺 腐胺 尸胺 组胺 色胺 章鱼胺 酪胺 2-苯乙胺 小黄花鱼I 1.64±0.14 0.67±0.04 1.26±0.05 / / / / / / 小黄花鱼II 1.79±0.05 0.63±0.11 1.38±0.21 / / / / / / 小黄花鱼III 1.54±0.19 0.52±0.03 1.42±0.16 / / / / / / 小黄花鱼IV 1.92±0.31 0.72±0.15 1.55±0.19 / / / / / / 小黄花鱼V 1.47±0.22 0.65±0.02 1.48±0.09 / / / / / / 水潺 2.02±0.21 3.21±0.24 3.69±0.12 / / / / / / 鲳鱼 1.18±0.05 0.85±0.03 3.27±0.02 0.20±0.03 / / / 0.15±0.14 / 带鱼 1.06±0.08 0.48±0.05 0.84±0.05 / / / / / / 墨鱼 7.64±0.19 1.81±0.14 1.90±0.16 3.07±0.14 / / / / / 鱿鱼 21.3±3.07 4.06±0.30 1.49±0.17 1.58±0.10 / / / / / 红虾 0.73±0.03 0.64±0.00 / 0.34±0.01 / / / 0.65±0.00 0.26±0.01 南美白对虾 0.69±0.02 0.76±0.00 / 0.57±0.01 / / / 0.75±0.04 / 死后3~5 h南美白对虾 0.71±0.01 3.16±0.36 2.34±0.17 9.80±0.16 / / / 1.01±0.03 / 注:“/”表示未检出。 -
[1] 李文凤, 王标诗, 余石坚, 等. 响应面法优化黄花鱼鱼鳞脱钙工艺[J]. 食品工业科技,2021,42(4):155−160. [LI W F, WANG B S, YU S J, et al. Optimization of decalcification process of yellow croaker scales by response surface methodology[J]. Science and Technology of Food Industry,2021,42(4):155−160. doi: 10.13386/j.issn1002-0306.2019100209 [2] 何淑华, 张钦发, 肖少军. 鲜黄花鱼在不同包装方式下的品质变化研究[J]. 食品工业,2014,35(5):151−153. [HE S H, ZHANG Q F, XIAO S J. Research on changes of the quality of fresh yellow croakers packed in different methods[J]. Food Industry,2014,35(5):151−153. [3] 刘丽. 小黄花鱼鱼糜制品品质的研究[J]. 农产品加工,2015,3:23−24. [LIU L. Quality of yellow croakers surimi products[J]. Farm Products Processing,2015,3:23−24. [4] 何晓萌, 黄卉, 李来好, 等. 罗非鱼与海水鱼制备混合鱼糜的凝胶特性研究[J]. 食品工业科技,2018,39(2):5−9. [HE X M, HUANG H, LI L H, et al. Research on gel properties of tilapia and sea fish mixed surimi[J]. Science and Technology of Food Industry,2018,39(2):5−9. doi: 10.13386/j.issn1002-0306.2018.02.002 [5] 杨梦奇, 刘玲玲, 李冰宁, 等. 植物油基鱼罐头中矿物油污染物高灵敏检测方法的建立[J/OL]. 食品工业科技, 2022. https://doi.org/10.13386/j.issn1002-0306.2021100291. YANG M Q, LIU L L, LI B N, et al. Establishment of highly sensitive determination method for mineral oil contaminants in vegetable oil-based canned fish products[J]. Science and Technology of Food Industry, 2022. https://doi.org/10.13386/j.issn1002-0306.2021100291.
[6] 窦少华, 赵长新, 祖国仁, 等. 黄花鱼露生产工艺的研究[J]. 食品科技,2003,10:53−55,59. [DOU S H, ZHAO C X, ZU G R, et al. Study on producing technology of yellow croaker sauce[J]. Food Science and Technology,2003,10:53−55,59. doi: 10.3969/j.issn.1005-9989.2003.06.020 [7] 陶耀宏, 汤海青, 欧昌荣, 等. 市售东海鱼鲞生物胺及相关质量指标分析[J]. 食品工业科技,2021,42(24):263−270. [TAO Y H, TANG H Q, OU C R, et al. Analysis of biogenic amines and related quality indexes of commercial dry salted fish in the east China sea[J]. Science and Technology of Food Industry,2021,42(24):263−270. doi: 10.13386/j.issn1002-0306.2021040092 [8] 丁海燕, 孙晓杰, 宁劲松, 等. 储藏温度对3种海水鱼产生生物胺的规律影响研究[J]. 食品科技,2018,43(9):177−182. [DING H Y, SUN X J, NING J S, et al. Study on the regular of biogenic amines from three marine fish stored at different temperature[J]. Food Science and Technology,2018,43(9):177−182. doi: 10.13684/j.cnki.spkj.2018.09.030 [9] 常娅妮, 马俪珍, 杨梅, 等. 不同冷冻方式对调味鱼贮藏品质的影响[J]. 食品科技,2020,45(2):137−143. [CHANG Y N, MA L Z, YANG M, et al. Effects of different freezing methods on the storage quality of seasoned channel catfish[J]. Food Science and Technology,2020,45(2):137−143. doi: 10.13684/j.cnki.spkj.2020.02.024 [10] 蒋林蓉, 徐志伟, 黄杰英, 等. 基于QuEChERS净化的液相色谱-串联质谱法分析食品中的6种生物胺[J]. 中国调味品,2017,42(8):127−132. [JIANG L R, XU Z W, HUANG J Y, et al. Determination of biogenic amines in food by modified QuEChERS method and liquid chromatography-mass spectrometry[J]. China Condiment,2017,42(8):127−132. doi: 10.3969/j.issn.1000-9973.2017.08.028 [11] 戴莹, 宋海勇, 吴曦, 等. 肉制品中生物胺的形成, 检测和控制研究进展[J]. 肉类研究,2020,34(11):89−97. [DAI Y, SONG H Y, WU X, et al. Recent progress in the formation, detection and control of biogenic amines in meat products[J]. Meat Research,2020,34(11):89−97. doi: 10.7506/rlyj1001-8123-20201005-236 [12] SANTOS M H S. Biogenic amines: Their importance in foods[J]. International Journal of Food Microbiology,1996,29:213−231. doi: 10.1016/0168-1605(95)00032-1
[13] 王光强, 俞剑燊, 胡健, 等. 食品中生物胺的研究进展[J]. 食品科学,2016,37(1):269−278. [WANG G Q, YU J C, HU J, et al. Progress in research on biogenic amines in foods[J]. Food Science,2016,37(1):269−278. doi: 10.7506/spkx1002-6630-201601046 [14] MYRSINI P, DIMITRA L, CALUM M, et al. Literature update of analytical methods for biogenic amines determination in food and beverages[J]. Trends in Analytical Chemistry,2018,98(1):128−142.
[15] 赵中辉. 水产品贮藏中生物胺的变化及组胺形成机制研究[D]. 青岛: 中国海洋大学, 2011 ZHAO Z H. Studies on changes of biogenic amines during the storage and mechanism of histamine formation in seafood[D]. Qingdao: Ocean University of China, 2011.
[16] RIO B D, REDRUELLO B, LINARES D M, et al. The biogenic amines putrescine and cadaverine show in vitro cytotoxicity at concentrations that can be found in foods[J]. Scientific Reports,2019,9(1):1−7. doi: 10.1038/s41598-018-37186-2
[17] ANAL A K, PERPETUINI G, PETCHKONGKAEW A, et al. Food safety risks in traditional fermented food from South-East Asia[J]. Food Control,2019,109:106922.
[18] BULUSHI I A, POOLE S, DEETH H C, et al. Biogenic amines in fish: Roles in intoxication, spoilage, and nitrosamine formation-A review[J]. Critical Reviews in Food Science and Nutriton,2009,49(4):369−377. doi: 10.1080/10408390802067514
[19] 白妞妞, 白锴凯, 何建林, 等. 鱼露生物胺研究进展[J]. 食品与发酵工业,2020,46(24):271−277. [BAI N N, BAI K K, HE J L, et al. Research progress of biogenic amines in fish sauce[J]. Food and Fermentation Industries,2020,46(24):271−277. doi: 10.13995/j.cnki.11-1802/ts.024673 [20] LALY S J, ANUPAMA T K, KUMAR K A, et al. Quality and freshness of fish available in supermarkets of Cochin, India based on biogenic amine content[J]. Fishery Technology,2019,56(1):212−220.
[21] COSTA C, GRAZHDAN D, FIUTOWSKI J, et al. Meat and fish freshness evaluation by functionalized cantilever-based biosensors[J]. Microsystem Technologies,2020,26(4):1−5.
[22] 赵庆志, 邓建朝, 杨贤庆, 等. 不同贮藏温度下鲐鱼生物胺变化的研究[J]. 食品工业科技,2018,39(4):260−267, 279. [ZHAO Q Z, DENG J C, YANG X Q, et al. Study on the changes of biogenic amines in mackerel under different temperatures during storage[J]. Science and Technology of Food Industry,2018,39(4):260−267, 279. doi: 10.13386/j.issn1002-0306.2018.04.048 [23] 刘洋帆, 李绪鹏, 冯阳, 等. 超高效液相色谱-串联质谱法测定鲣鱼中的生物胺[J/OL]. 食品与发酵工业. https://doi.org/10.13995/j.cnki.11-1802/ts.029408. LIU Y F, LI X P, FENG Y, et al. UPLC-MS/MS method for detection of biogenic amines in shipjack tuna[J]. Food and Fermentation Industries. https://doi.org/10.13995/j.cnki.11-1802/ts.029408.
[24] 赵冬寒, 赵楠, 梁美佳, 等. 不同贮藏温度下三文鱼鱼片生物胺和品质的变化[J]. 食品工业科技,2022,43(11):350−355. [ZHAO D H, ZHAO N, LIANG M J, et al. Change of biogenic amines and quality of salmon fillets during different storage temperature[J]. Science and Technology of Food Industry,2022,43(11):350−355. doi: 10.13386/j.issn1002-0306.2021090147 [25] 赵中辉, 林洪, 李振兴. 不同温度储藏条件下鲅鱼生物胺变化的研究[J]. 食品工业科技,2011(6):358−363. [ZHAO Z H, LIN H, LI Z X. Changes of biogenic amines in Spanish mackerel under different temperatures during the storage[J]. Science and Technology of Food Industry,2011(6):358−363. doi: 10.13386/j.issn1002-0306.2011.06.093 [26] 吴燕燕, 陈玉峰. 腌制水产品中生物胺的形成及控制技术研究进展[J]. 食品工业科技,2014,35(14):396−400. [WU Y Y, CHEN Y F. Research progress in formation and control of the biogenic amine in salted aquatic product[J]. Science and Technology of Food Industry,2014,35(14):396−400. doi: 10.13386/j.issn1002-0306.2014.14.078 [27] 陈玉峰, 吴燕燕, 邓建朝, 等. 腌制和干燥工艺对咸金线鱼中生物胺的影响[J]. 食品工业科技,2015,36(20):83−91. [CHEN Y F, WU Y Y, DENG J C, et al. Effect of pocking and drying process on biogenic amines formation in salted threadfin bream (Nemipterus hexodon)[J]. Science and Technology of Food Industry,2015,36(20):83−91. doi: 10.13386/j.issn1002-0306.2015.20.009 [28] 谢诚, 刘忠义, 周宇峰, 等. 鳙鱼糜发酵过程中生物胺的测定[J]. 食品工业科技,2010,31(7):349−351. [XIE C, LIU Z Y, ZHOU Y F, et al. Determination of biogenic amine during the fermentation of bighead carp (Aristichthys nobilis) surimi[J]. Science and Technology of Food Industry,2010,31(7):349−351. doi: 10.13386/j.issn1002-0306.2010.07.074 [29] 吴海军, 程海燕, 李立军, 等. 非衍生化LC-MS-MS法分析食品中9种生物胺[OL]. (2018-11-09).https://sciex.com/content/ dam/SCIEX/pdf/tech-notes/cn/RUO-MKT-02-8460-ZH-A.pdf WU H J, CHENG H Y, LI L J, et al. Non-derivation LC-MS/MS method for the analysis of nine biogenic amines in food[OL]. (2018-11-09).https://sciex.com/content/dam/SCIEX/pdf/tech-notes/cn/ RUO-MKT-02-8460-ZH-A.pdf.
[30] ZHANG X, FANG C, HUANG D, et al. Determination of 8 biogenic amines in aquatic products and their derived products by high-performance liquid chromatography-tandem mass spectrometry without derivatization[J]. Food Chemistry,2021,361:130044. doi: 10.1016/j.foodchem.2021.130044
[31] HUANG Y, SONG Y, CHEN F, et al. Simultaneous determination of eight biogenic amines in the traditional Chinese condiment Pixian Douban using UHPLC-MS/MS[J]. Food Chemistry,2021,353:129423. doi: 10.1016/j.foodchem.2021.129423
[32] 孙亚军, 廖建萌, 雷晓凌, 等. 液相色谱-串联质谱法同时测定虾仁中八种生物胺[J]. 食品工业,2015,36(3):273−277. [SUN Y J, LIAO J M, LEI X L, et al. Simultaneous determination of eight biogenic amines in shrimp by LC-MS/MS[J]. Food Industry,2015,36(3):273−277.





 下载:
下载:
 下载:
下载:



