Determination of Monosaccharide Composition and Content of Polysaccharide in Whey Protein Sports Nutrition Powder by Ultra Performance Liquid Chromatography-Tandem Mass Spectrometry
-
摘要: 建立了同时测定乳清蛋白运动营养粉多糖水解产物中鼠李糖、核糖、阿拉伯糖、岩藻糖、半乳糖、木糖、半乳糖醛酸、甘露醇、葡萄糖醛酸、甘露糖、葡萄糖12种糖类化合物的超高效液相色谱-串联质谱分析方法。乳清蛋白运动营养粉样品经超声辅助提取,采用Sevag法除蛋白,直至无蛋白析出,然后经酸水解进行单糖组成测定。以5 mmol/L乙酸铵+0.02%甲酸水溶液作为流动相A,甲醇作为流动相B,在电喷雾离子源负离子(electrospray ion source negative ion,ESI−)模式下,用多反应监测模式(multiple reaction monitoring,MRM)分析检测,外标法定量。结果表明,12种糖类化合物在质量浓度为0.10~6.00 μg/mL范围内,各单糖的线性关系良好,相关系数(r)均大于0.995,检出限为0.0037~0.0326 mg/g,定量限为0.0123~0.1087 mg/g。分别向样品中添加12种糖类化合物标准品浓度为40、100和160 mg/g的3个水平,其加标平均回收率为76.12%~99.12%,相对标准偏差(relative standard deviations,RSDs)为0.12%~10.01%(n=6)。应用该方法对乳清蛋白运动营养粉样品进行分析,结果发现:15份样品中的12种糖类化合物均有不同程度检出,且多种单糖在不同样品中含量差异较大。该方法的建立可为乳清蛋白运动营养粉多糖的组成及其活性提供技术支撑及基础数据。
-
关键词:
- 超高效液相色谱-串联质谱 /
- 乳清蛋白运动营养粉 /
- 多糖 /
- 单糖
Abstract: The simultaneous determination of rhamnose, ribose, arabinose, fucose, galactose, xylose, galacturonic acid, mannitol, glucuronic acid and mannose in whey protein sports nutrition powder polysaccharide hydrolyzate was established. An ultra-high performance liquid chromatography-tandem mass spectrometry method was used for the analysis of 12 sugar compounds. The samples of whey protein sports nutrition powder were extracted by ultrasound, and the protein was removed by the Sevag method until no protein was precipitated, and then the monosaccharide composition was determined by acid hydrolysis. Using 5 mmol/L ammonium acetate+0.02% formic acid aqueous solution as mobile phase A, methanol as mobile phase B, in the electrospray ion source negative ion (electrospray ion source negative ion, ESI−), in the multiple reaction monitoring mode (multiple reaction monitoring, MRM) analysis, the detection was conducted by external standard method for quantification. The results showed that in the mass concentration range of 0.10~6.00 μg/mL, the 12 sugar compounds had good linear relationship with each monosaccharide, the correlation coefficients (r) were all greater than 0.995. The detection limit was 0.0037~0.0326 mg/g. The quantitative limit was 0.0123~0.1087 mg/g. 12 sugar compounds were added to the samples at three levels with concentrations of 40, 100 and 160 mg/g, and the average recovery was 76.12%~99.12%, relative standard deviations (RSDs) 0.12%~10.01% (n=6). This method was used to analyze the samples of whey protein sports nutrition powder, and the results showed that 12 carbohydrate compounds were detected in different degrees in 15 samples, and the content of various monosaccharides in different samples was quite different. The establishment of this method could provide technical support and basic data for the structural composition and activity of whey protein sports nutrition powder polysaccharide. -
多糖是由多个单糖分子缩合、失水而成,是一类分子结构复杂且庞大的糖类物质,是生物体内重要的生物大分子[1-3]。研究表明,多糖具有特殊的生物活性[4-5],能增强免疫机制[6]、抗肿瘤[7]、降低血糖[8]、抗衰老[9]、抗辐射[10]等。多糖中单糖组成及含量不同可能导致多糖空间结构不同,从而导致生物活性不同[11-13]。乳清蛋白运动营养粉是为了满足运动人群的生理代谢、运动能力及对某些营养成分的特殊需求专门加工的运动营养食品。因此,测定乳清蛋白运动营养粉多糖的单糖组成及含量对其活性成分和质量控制具有重要意义。
多糖的测定方法主要有:苯酚-硫酸等显色反应分光光度法测定其总量[14]、离子色谱-脉冲安倍检测法[15]、衍生化的气相色谱[16]或液相色谱-紫外检测法[17]、液相色谱-蒸发光检测[18]或示差荧光检测法[19]等。上述方法尽管可以粗略测定样品中多糖的总含量,但用于测定多糖中单糖组成则存在准确度低、分离度差、操作繁琐等缺点[20-22]。近年来,色谱技术的发展为糖类化合物的分析提供了一个强有力的分析手段[23]。张璐等[24]采用高效液相色谱法测定党参中多糖的单糖组成及含量,需要对党参多糖水解液进行衍生化;王川丕等[25]建立了利用超高效液相色谱-质谱联用技术测定茶叶中8种单糖和寡糖的方法。然而,该方法检测的糖的种类偏少,此外,方法的基质也仅限于茶叶。目前,采用超高效液相色谱-串联质谱技术对样品中多糖的单糖组成及含量进行测定,无需对样品多糖水解液衍生化,只需对其单糖的特征离子进行选择扫描即可进行测定。
本文建立超高效液相色谱-串联质谱法测定乳清蛋白运动营养粉中12种单糖组成的检测方法,并对15批乳清蛋白运动营养粉中多糖的单糖组成和含量进行测定,为控制乳清蛋白运动营养粉的质量提供技术支撑及基础数据。
1. 材料与方法
1.1 材料与仪器
乳清蛋白运动营养粉15份 上海鸿志制果食品工业有限公司;D-半乳糖醛酸(批号:1110A021,CAS号:6294-16-2,纯度≥98.0%)、L(+)-阿拉伯糖(批号:1110C021,CAS号:87-72-9,纯度≥98.0%)、L- (+)-鼠李糖(批号:909A021,CAS号:6014-42-2,纯度≥98.0%)、D-核糖(批号:1026A022,CAS号:50-69-1,纯度≥98.0%)、D-(+)-甘露糖(批号:914A022,CAS号:3458-28-4,纯度≥98.0%)、D-葡萄糖醛酸(批号:1124A021,CAS号:6556-12-3,纯度≥98.0%)、L-木糖(批号:1118D0211,CAS号:609-06-3,纯度≥98.0%)、D-(+)-葡萄糖(批号:1118A021,CAS号:14431-43-7,纯度≥98.0%)、D-(-)-果糖(批号:958A358,CAS号:57-48-7,纯度≥98.0%)、D-(+)-岩藻糖(批号:2020C923,CAS号:3615-37-0,纯度≥98.0%)、D-(+)-半乳糖(批号:2020B918,CAS号:59-23-4,纯度≥98.0%)等标准品 源叶生物科技有限公司;超纯水 由Synergy UV纯水系统(德国默克密理博公司)制备,且符合GB/T 6682-2008《分析实验室用水规格和试验方法》中三级水的规定;硫酸、氢氧化钠、磷酸二氢钾、乙酸铵、三氯甲烷 分析纯,广州化学试剂有限公司;甲醇、乙腈 色谱纯,美国Sigma公司;三氟乙酸 色谱纯,上海麦克林生化科技有限公司;碳酸钠、氢氧化钠 分析纯,天津市科密欧化学试剂有限公司;0.22 μm滤膜 天津市津腾实验设备有限公司。
UHPLC-Q Exactive 超高效液相色谱-质谱联用仪 美国Thermo Fisher Scientific公司;KQ-250DB数控超声清洗器 昆山市超声仪器有限公司;Sorvall Legend23R离心机 美国赛默飞世尔科技有限公司;Synergy UV超纯水机 德国默克密理博公司;TWS-26恒温水浴锅 上海舜宇衡平科学仪器有限公司;XH-B旋涡混合器 上海精宏实验设备有限公司;DKN612 型烘箱 北京鸿运科技实验室产品有限公司;RVTR8旋转蒸发仪 武汉恒信世纪科技有限公司。
1.2 实验方法
1.2.1 工作溶液的配制
贮备液:分别称取上述12种单糖对照品0.100 g(精确至0.0001 g)于1000 mL容量瓶中,用50%乙腈水溶液定容刻度,即得浓度为0.1 mg/mL贮备液,放于4 ℃冰箱中储存备用(保存期为6个月)。
曲线工作液:分别吸取0.01、0.06、0.10、0.40和0.60 mL浓度为0.1 mg/mL贮备液于10 mL容量瓶中,用50%乙腈水溶液定容至刻度,即得浓度为0.1、0.6、1.0、4.0和6.0 μg/mL的标准工作液。
1.2.2 样品前处理
参照文献[26-27]方法,称取适量乳清蛋白运动营养粉,加入适量体积的95%乙醇90 ℃回流脱脂2 h,离心,过滤,滤渣风干得到实验样品。准确称取0.5 g(精确至0.1 mg)经脱脂处理后的乳清蛋白运动营养粉置于50 mL具塞离心管内,按照料液比1:(10~30) g/mL加入提取溶剂,在提取温度为35~75 ℃、提取功率为120~200 W的条件下提取15~55 min。提取完毕后以6000 r/min离心15 min,取其上清液,重复提取2次,合并提取液于100 mL容量瓶中,并用蒸馏水定容至刻度,即得乳清蛋白运动营养粉多糖提取液。取2 mL上述多糖提取液加入5 mL Sevag溶液(V正丁醇:V氯仿, 1:5)萃取多次除去蛋白质,直至两相间无乳白色絮状物。取上清液按照1:1(V上清液:V三氟乙酸液)加入2 mml/L三氟乙酸溶液,将其放入恒温干燥箱120 ℃水解2 h,水解液加入甲醇洗涤后氮吹,此过程重复3次将三氟乙酸去除,用1 mL水复溶后再经0.22 μm滤膜过滤,供UPLC-MS/MS分析。
1.2.3 单因素实验
按照1.2.2样品前处理的方法提取乳清蛋白运动营养粉中多糖,提取条件为:固定料液比1:10 g/mL、功率120 W、时间15 min,考察不同提取温度(35、45、55、65、75 ℃)对乳清蛋白运动营养粉中多糖得率的影响;固定提取温度为55 ℃,提取功率为120 W、提取时间为15 min,考察不同料液比(1:10、1:15、1:20、1:25、1:30 g/mL)对乳清蛋白运动营养粉中多糖得率的影响;固定提取温度为55 ℃、料液比1:20 g/mL、提取时间为15 min、考察不同提取功率(120、140、160、180、200 W)对乳清蛋白运动营养粉中多糖得率的影响;固定提取温度为55 ℃、料液比1:20 g/mL、提取功率为180 W、考察不同提取时间(15、25、35、45、55 min)对乳清蛋白运动营养粉中多糖得率的影响。
1.2.4 正交试验
在单因素实验的基础上,用提取温度(A)、料液比(B)、提取功率(C)、提取时间(D)为影响因素,采用四因素三水平设计正交试验方案,以乳清蛋白运动营养粉中多糖得率为衡量指标。正交试验因素及水平如表1。
表 1 正交试验因素水平表Table 1. Factors and levels table of orthogonal test因素 水平 1 2 3 A-提取温度(℃) 45 55 65 B-料液比(g/mL) 1:20 1:25 1:30 C-提取功率(W) 160 180 200 D-提取时间(min) 25 35 45 1.2.5 乳清蛋白运动营养粉中多糖得率的测定
采用苯酚-硫酸法,以葡萄糖为对照品,使用前将葡萄糖于105 ℃恒温烘干至恒重,准确称取0.100 g葡萄糖于1000 mL容量瓶中,加蒸馏水定容刻度,并超声溶解,即得浓度为0.1 mg/mL贮备液,放于4 ℃冰箱中储存备用。分别吸取0、0.2、0.4、0.6、0.8和1.0 mL贮备液于20 mL具塞试管中,用蒸馏水补至1.0 mL,精确加入1 mL的5%苯酚溶液,混匀后快速加入5 mL硫酸,静止10 min,使用旋涡振荡混匀,然后将试管放置30 ℃水浴锅中反应20 min,冷却后于490 nm测定吸光度,以紫外分光光度计的吸光度(Y)为纵坐标,葡萄糖质量浓度(x)为横坐标制作标准曲线,得线性回归方程:y=25.3545x−0.0214,R2=0.9998。
准确吸取1.0 mL乳清蛋白运动营养粉多糖提取液,按照标准工作曲线溶液进行显色反应后,于490 nm测定吸光度,其计算公式如下:
多糖得率(%)=C×n×VW×106×100 式中:C样品中多糖浓度,μg/mL;V样品溶液的体积,mL;n样品溶液的稀释倍数;W为样品质量,g。
1.2.6 液相色谱与质谱条件
1.2.6.1 色谱条件
色谱柱:ACQUITY BEH Amide C18(2.8 mm×150 mm,1.6 μm);流动相:5 mmol/L乙酸铵+0.02%甲酸水溶液(A)和甲醇(B);流速:0.2 mL/min;柱温:30 ℃;进样量:5 μL;梯度洗脱程序:0~7.50 min(B相90%~80%),7.50~9.50 min(B相80%~60%),9.50~25.0 min(B相60%~90%),25.0~35.0 min(B相90%)。
1.2.6.2 质谱条件
离子源:电喷雾负离子源(electron spray ionization,ESI−);离子源温度:500 ℃;雾化气GS1压力:380 kPa;辅助气GS2压力:418 kPa;毛细管喷雾电压:−5.5 kV;入口电压:−10V;出口电压:−6V;扫描方式:负离子模式。12种糖的质谱分析参数见表2。
表 2 12种糖的监测离子对、碰撞气能量和去簇电压Table 2. Monitored ion pairs, collision gas energies and declustering voltages of 12 sugars序号 化合物 保留时间(min) 母离子(m/z) 子离子(m/z) 去簇电压(eV) 碰撞能量(eV) 1 核糖 6.157 215.6 58.8*88.9149.1 −92 −26−14 2 木糖 7.357 198.8 58.8*89.2149.2 −84 −24−12 3 阿拉伯糖 8.486 218.6 58.9*89.1149.2 −88 −22−16 4 岩藻糖 9.198 196.5 58.8*89.1163.1 −86 −26−18 5 鼠李糖 11.689 208.3 58.9*103.0163.1 −84 −26−16 6 甘露醇 22.218 210.8 58.8*89.0181.1 −100 −26−18 7 甘露糖 23.389 236.5 58.8*89.1179.3 −84 −20−12 8 葡糖糖 25.895 209.8 89.1*71.1179.1 −88 −26−18 9 果糖 30.945 214.5 59.0*89.1179.2 −90 −24−12 10 半乳糖 33.989 220.7 89.1*58.6179.1 −92 −18−10 11 葡糖糖醛酸 34.898 265.8 58.8*113.2193.1 −86 −26−10 12 半乳糖醛酸 37.988 265.8 59.1*73.1193.2 −62 −24−10 注:*为定量离子。 1.3 数据处理
每组试验平行测定三次,实验数据以
¯x±s 表示,使用Microsoft office2016制图,应用SPSS20.0进行数据分析。2. 结果与分析
2.1 单因素实验结果
2.1.1 提取温度对多糖得率的影响
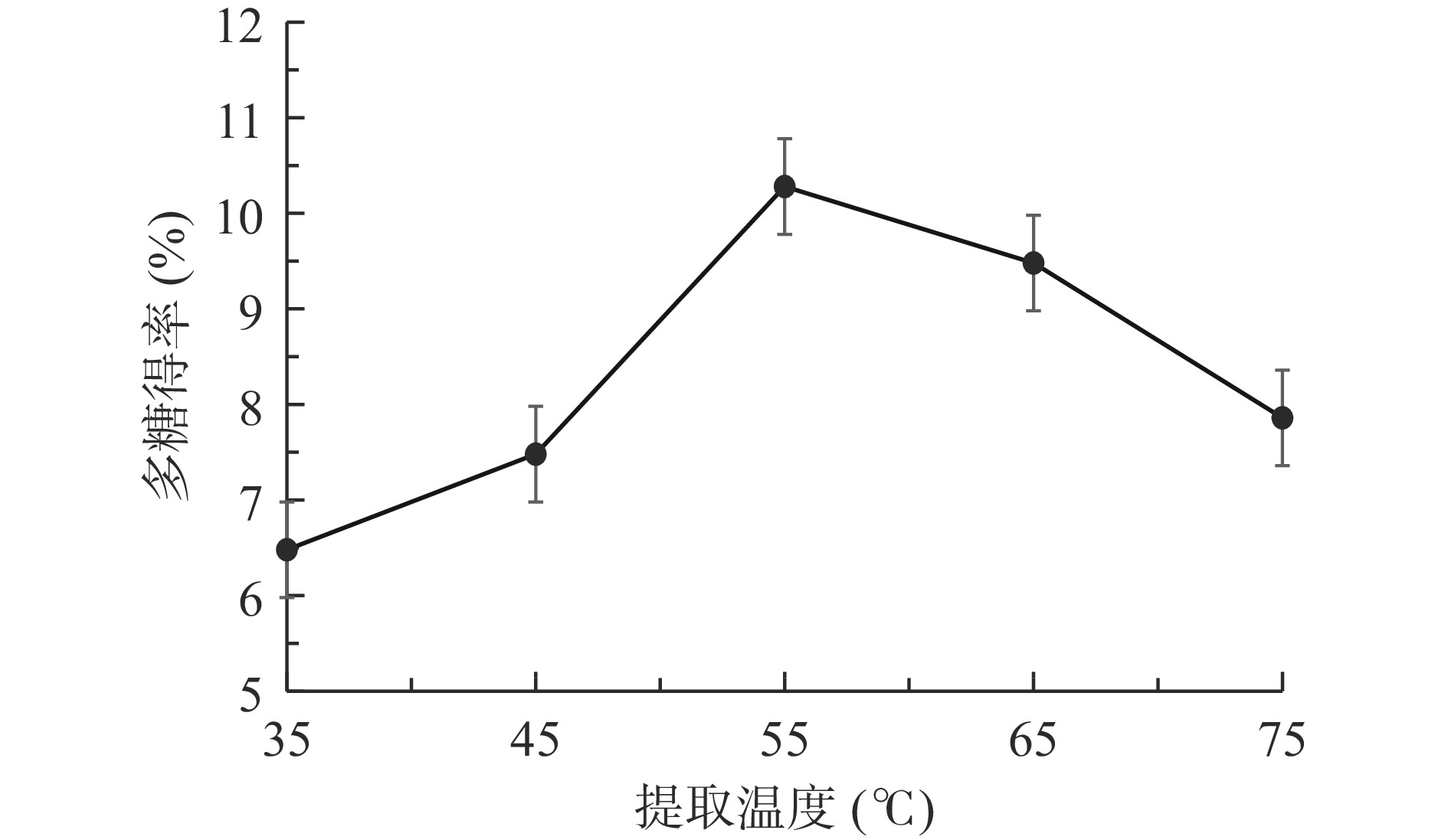
由图1可知,乳清蛋白运动营养粉中多糖的得率随着提取温度的增加呈现先增大后降低的趋势;当提取温度为35~55 ℃时,乳清蛋白运动营养粉中多糖的得率随提取温度的增加而增大;当提取温度为55 ℃时乳清蛋白运动营养粉中多糖的得率达到最大值;再次逐渐升高提取温度,乳清蛋白运动营养粉中多糖的得率反而降低。其原因可能是在一定的温度范围内,随着提取温度的升高,能降低提取溶剂与样品的粘稠度,增加乳清蛋白运动营养粉中多糖在提取溶剂中的扩散性和溶解度,有利于乳清蛋白运动营养粉中多糖从提取样品中溶出外界[28],从而使得乳清蛋白运动营养粉中多糖得率升高。当提取温度达到最佳提取温度时继续升温,高温会造成乳清蛋白运动营养粉中多糖破坏,造成乳清蛋白运动营养粉中多糖得率降低。因此,选择提取温度为45、55、65 ℃作为正交试验中提取温度的3个水平。
2.1.2 料液比对多糖得率的影响
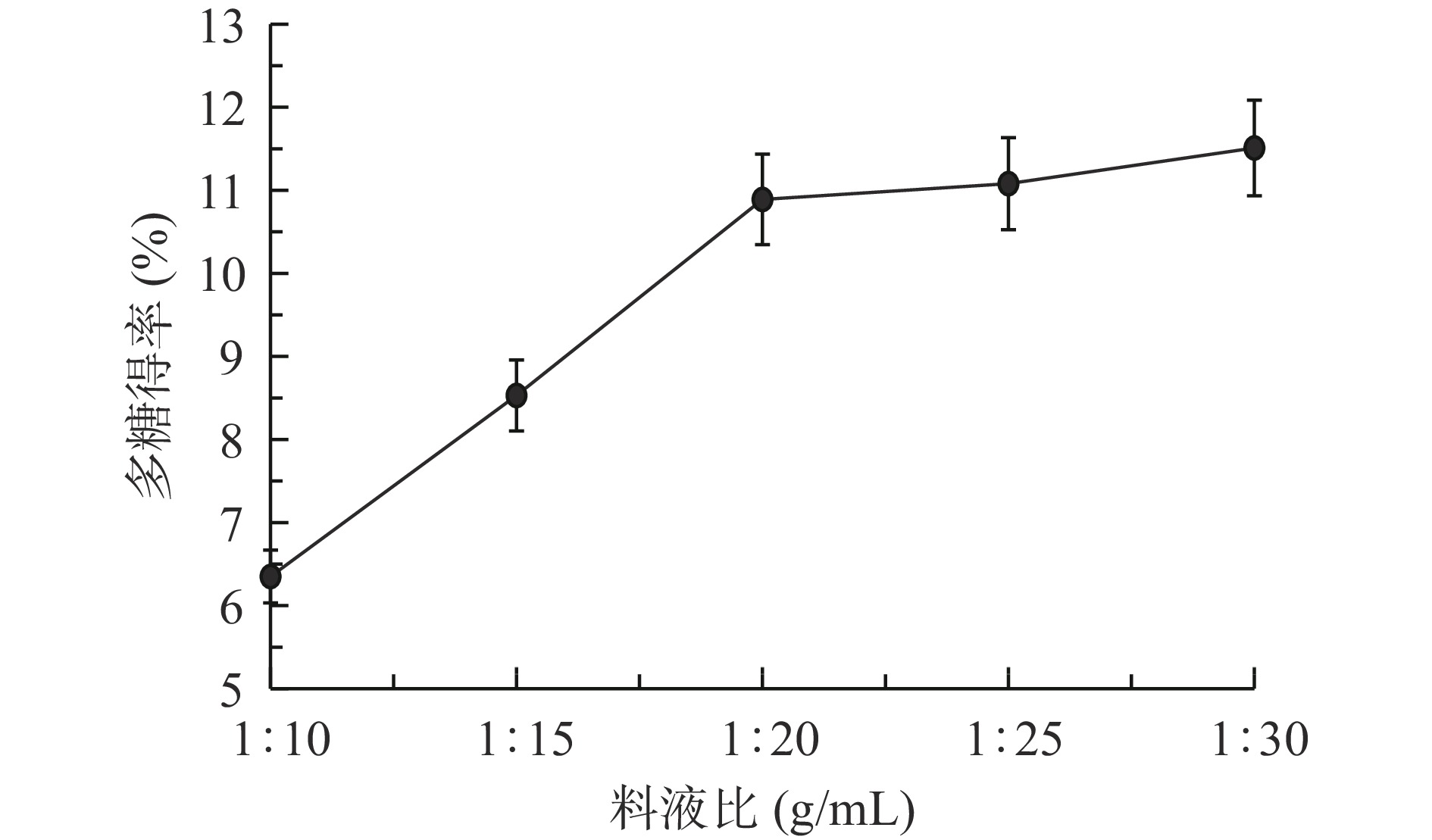
由图2可知,当料液比为1:10~1:20 g/mL范围内,随着了料液比的增加,乳清蛋白运动营养粉中多糖得率急剧增加,其原因可能是随着料液比的增大,增大了样品与提取溶剂的接触面积,有利于乳清蛋白运动营养粉中多糖的溶出,故多糖得率急剧增加[29];当料液比大于1:20 g/mL后,随着料液比的增加,乳清蛋白运动营养粉中多糖得率趋于平缓增长,其原因可能是乳清蛋白运动营养粉中多糖的溶出逐渐趋于平稳,且已大部分溶入提取溶剂中,继续增加料液比会造成其他杂质的溶出,而且还会造成提取成本的上升[30]。因此选择1:20、1:25、1:30 g/mL作为正交试验中料液比的3个水平。
2.1.3 提取功率对多糖得率的影响
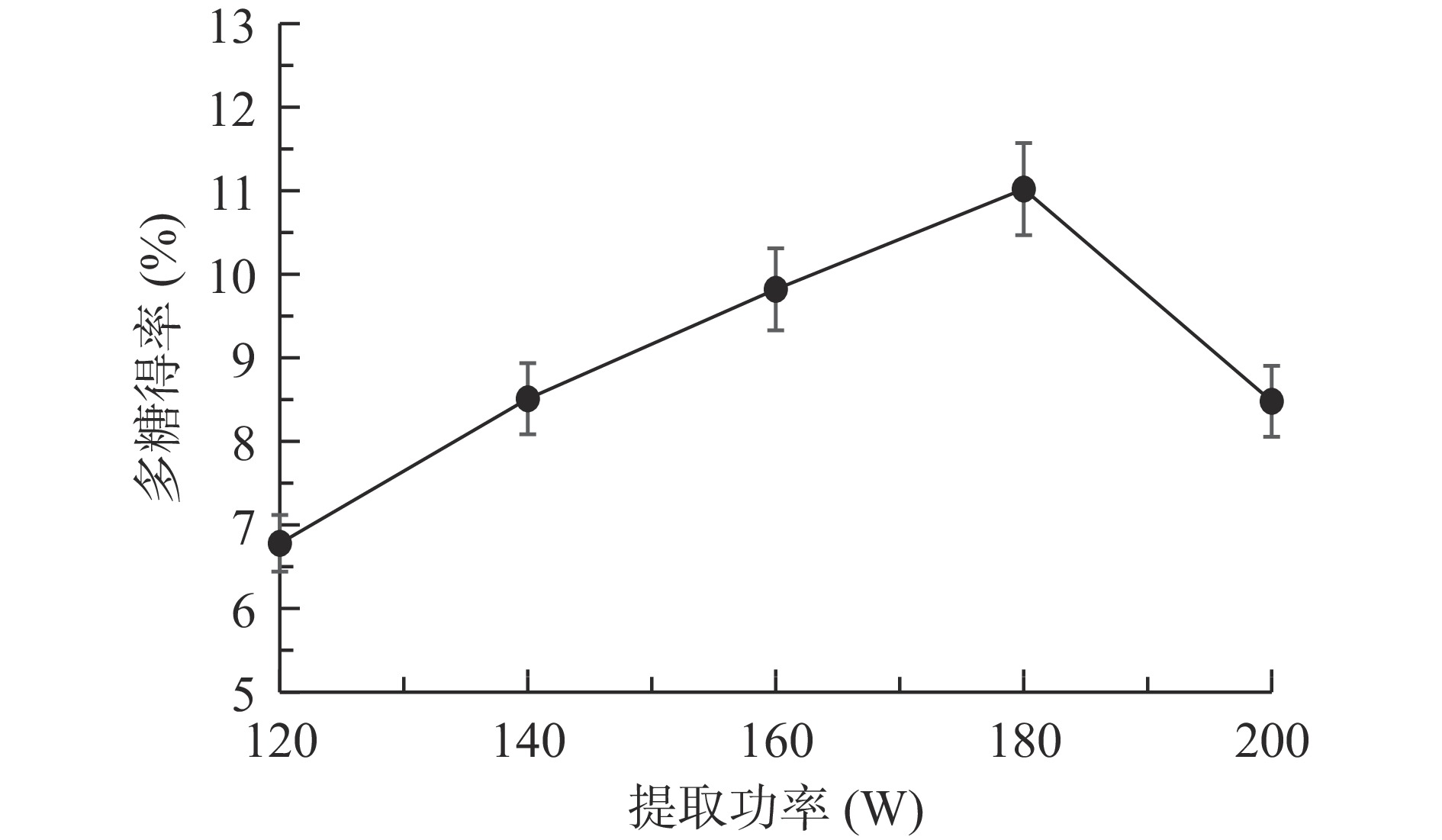
由图3可知,当超声波提取功率小于180 W时,随着提取功率逐渐增大乳清蛋白运动营养粉中多糖得率逐渐升高;当提取功率为180 W时,乳清蛋白运动营养粉中多糖得率达到最大值;当提取功率大于180 W时,乳清蛋白运动营养粉中多糖得率逐渐下降,其原因可能是超声功率达到一定强度可以产生更好的空化效果破坏细胞壁,从而有利于提取物的溶出,但随着提取功率的继续增加有可能破坏乳清蛋白运动营养粉中多糖的结构,从而使多糖得率有所下降[31]。因此选择160、180、200 W作为正交试验中提取功率的3个水平。
2.1.4 提取时间对多糖得率的影响
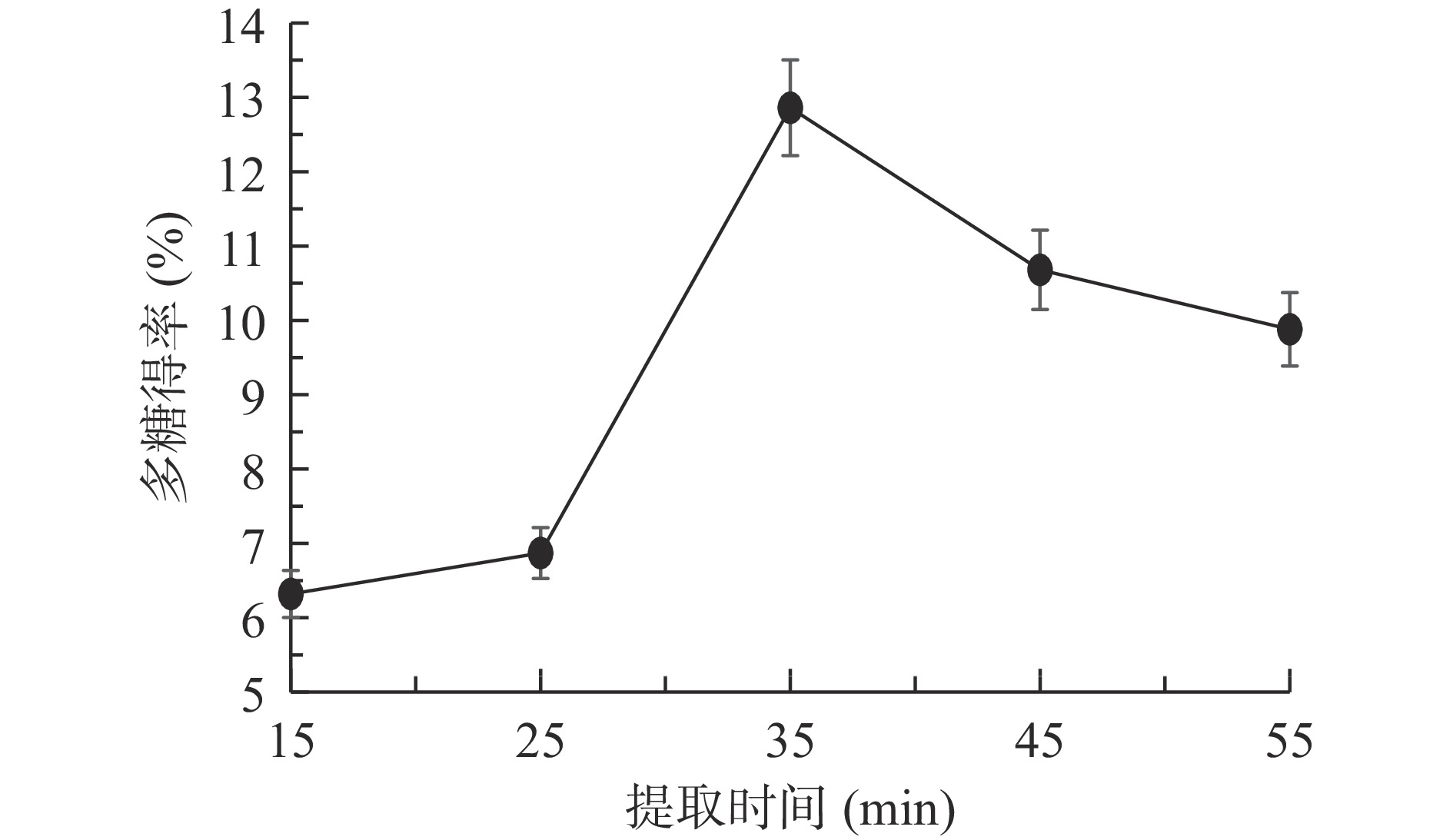
由图4可知,乳清蛋白运动营养粉中多糖得率随着提取时间的延长呈先增加后降低趋势,并在提取时间为35 min时乳清蛋白运动营养粉中多糖得率达到最大值。这表明提取时间为35 min时,乳清蛋白运动营养粉中多糖已趋于完全溶入提取溶剂中,继续延长提取时间反而会使乳清蛋白运动营养粉中多糖长时间的处于高温浸泡中,导致其分子结构破坏[32];同时,伴随样品中其他杂质的溶出。从而导致乳清蛋白运动营养粉中多糖得率下降。因此选择25、35、45 min作为正交试验中提取时间的3个水平。
2.2 正交试验结果
乳清蛋白运动营养粉中多糖提取正交试验结果,见表3。从正交试验直观分析结果可以看出,各因素对乳清蛋白运动营养粉中多糖得率的影响程度不同,四个因素对多糖得率的影响由大到小依次为提取温度﹥提取时间﹥料液比﹥提取功率。通过K值比较得到本实验最佳因素组合为A2B1C2D3不在正交表中,进行验证实验,测得乳清蛋白运动营养粉中多糖得率为12.21%,低于正交表中4实验的多糖得率13.35%,所以该正交试验的最佳条件确定为A2B1C2D2,即提取温度55 ℃、料液比1:20 g/mL、提取功率180 W、提取时间35 min。
表 3 L9(34)正交试验结果Table 3. L9(34) orthogonal test results实验号 A提取温度 B料液比 C提取功率 D提取时间(min) 多糖得率(%) 1 1 1 1 1 8.95 2 1 2 2 2 10.56 3 1 3 3 3 9.68 4 2 1 2 2 13.35 5 2 2 3 1 10.89 6 2 3 1 3 11.58 7 3 1 3 2 11.89 8 3 2 1 3 12.04 9 3 3 2 1 10.56 K1 9.73 11.40 10.86 10.13 K2 11.94 11.16 11.49 11.34 K3 11.50 10.61 10.82 11.69 R 2.21 0.79 0.67 1.56 最优组合 A2B1C2D2 2.3 仪器条件的优化
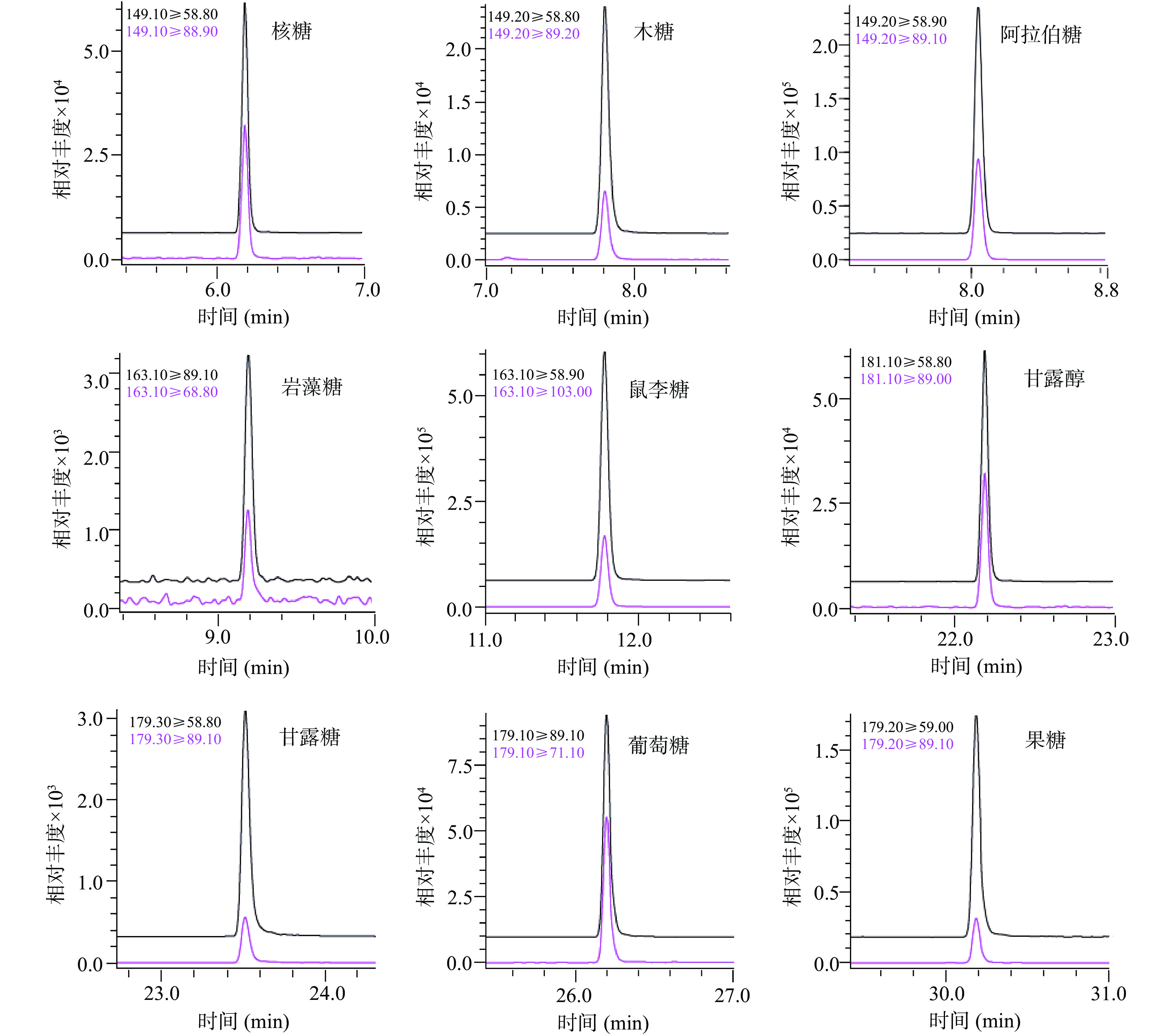
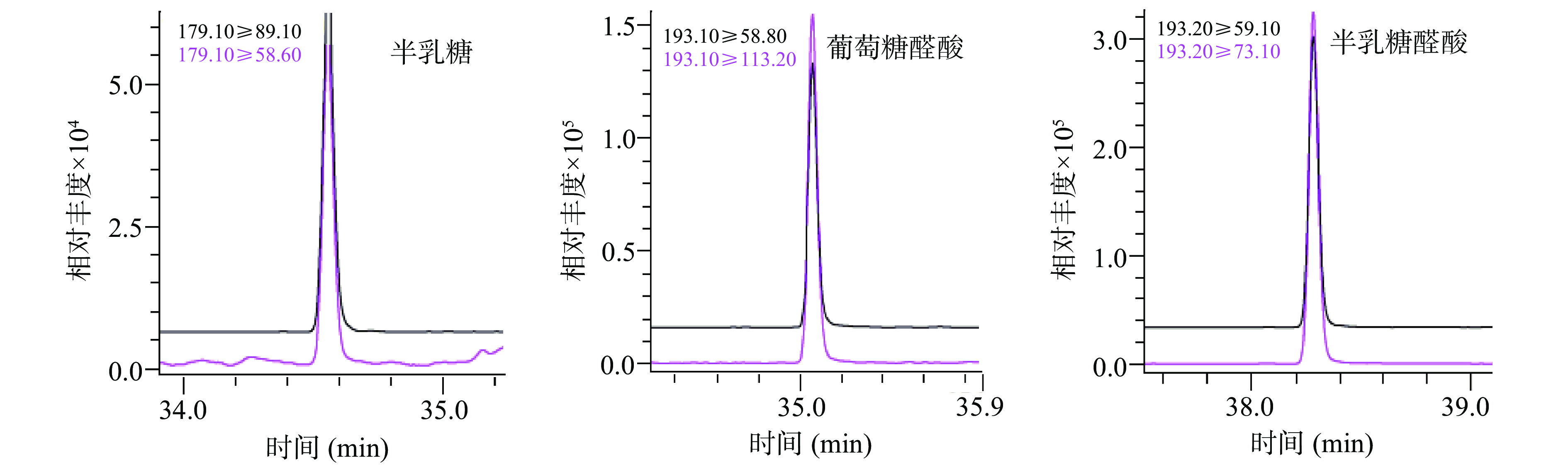
化合物的离子化效率以及出峰时间受不同流动相体系的影响较大。试验分别选择5 mmol/L乙酸铵+0.02%甲酸水溶液、纯水作为A流动相;甲醇、乙腈作为B流动相。比较2个流动相体系对分离效果的影响。结果表明,在水相(流动相A)中加入5 mmol/L乙酸铵与0.02%甲酸后,不仅可以改善色谱峰形,还可以提高目标化合物的离子化效率;流动相B中,乙腈作为流动相时,发现葡萄糖醛酸和半乳糖醛酸以及葡萄和半乳糖的分离度不好,甚至分不开;而选用甲醇作为B流动相,各目标峰分离度明显改善。因此,本试验选择5 mmol/L乙酸铵+0.02%甲酸水溶液作为流动相A,甲醇作为流动相B时12种糖类化合物在色谱上分离较好,峰形尖锐对称,结果见图5。参照文献[33]方法,根据12种糖类化合物的化学电离性质,分别在电喷雾离子源正/负模式下采用全扫描模式方式选择母离子、子离子扫描模式对子离子及碰撞能量、锥孔电压等质谱参数进行优化,发现所有糖类化合物在负离子模式下响应值均高于正离子模式,最终确定12 种糖类化合物的母离子、定性离子和定量离子参数,见表2。
2.4 方法验证
2.4.1 方法的线性回归方程、检出限及定量限
分别配制浓度为0.1、0.6、1.0、4.0、和6.0 μg/mL混合标准工作液,按上述优化好的仪器条件分析。以峰面积(Y)与目标物质量浓度(X,μg/mL)绘制标准曲线。准确称取经回流脱脂处理的0.5 g样品,向其添加适量浓度的单糖标准溶液,按照“1.2.2 样品前处理”操作,提取液按照“1.2.4液相色谱与质谱条件”上机分析,分别以信噪比(S/N)为3和10计算方法的检出限和定量限[34-36]。由表4可知,12种糖类化合物在质量浓度0.1~6.0 μg/mL范围内线性关系良好,相关系数r≥0.995,该方法的检出限范围为0.0037~0.0326 mg/g,定量限范围为0.0123~0.1087 mg/g,满足痕量需求。
表 4 12种糖类化合物的线性回归方程、检出限及定量限Table 4. Linear regression equation, detection limit and quantification limit of 15 pesticides编号 化合物 线性回归方法 相关系数(r) 线性范围(μg/mL) 检出限(mg/g) 定量限(mg/g) 1 核糖 y=6584.154x−213.04 0.998945 0.10~6.00 0.0326 0.1087 2 木糖 y=4104.356x−243.21 0.999128 0.10~6.00 0.0198 0.0660 3 阿拉伯糖 y=4987.651x+257.15 0.996787 0.10~6.00 0.0067 0.0223 4 岩藻糖 y=5312.451x−312.45 0.999154 0.10~6.00 0.0269 0.0897 5 鼠李糖 y=2135.654x−216.45 0.999784 0.10~6.00 0.0091 0.0303 6 甘露醇 y=7452.341x−451.25 0.999647 0.10~6.00 0.0105 0.0350 7 甘露糖 y=4125.351x+315.54 0.999587 0.10~6.00 0.0037 0.0123 8 葡糖糖 y=3058.458x−218.31 0.998982 0.10~6.00 0.0195 0.0650 9 果糖 y=8765.951x−378.54 0.999687 0.10~6.00 0.0058 0.0193 10 半乳糖 y=4986.481x+201.56 0.999458 0.10~6.00 0.0109 0.0363 11 葡糖糖醛酸 y=4013.261x+207.95 0.999687 0.10~6.00 0.0055 0.0183 12 半乳糖醛酸 y=4105.651x+312.45 0.999784 0.10~6.00 0.0108 0.0360 2.4.2 方法加标回收率及精密度
选取其中一种乳清蛋白运动营养粉(编号:S1)样品进行加标回收试验,分别添加3个质量浓度(40、100、160 mg/g)的待测组分混合标准溶液,每个添加水平重复6次。加标回收率及精密度(RSD%)如表5所示,回收率在76.12%~99.12%之间,精密度(RSD%)在0.12%~10.01%之间。表明该方法具有良好的回收率和精密度,符合方法学要求。
表 5 S1样品中12种糖类化合物加标回收率和RSD(n=6)Table 5. Spike recoveries and RSD of 12 carbohydrates in S1 sample (n=6)化合物 S1样品本底值(mg/g) 添加水平40 mg/g 添加水平100 mg/g 添加水平160 mg/g 回收率(%) RSD(%) 回收率(%) RSD(%) 回收率(%) RSD(%) 核糖 N.D 91.25 1.87 86.57 7.89 87.56 4.51 木糖 12.16 83.45 5.16 80.75 9.76 91.35 0.84 阿拉伯糖 8.98 86.91 3.17 98.99 6.03 84.65 9.15 岩藻糖 N.D 89.61 4.26 78.45 2.15 80.25 2.54 鼠李糖 10.26 97.56 3.09 99.12 0.86 91.64 5.16 甘露醇 N.D 86.78 8.94 86.15 0.12 76.12 2.78 甘露糖 9.66 98.68 7.56 83.59 1.78 97.56 3.01 葡糖糖 12.57 88.15 10.01 87.59 5.16 86.09 2.14 果糖 13.68 83.45 2.15 91.78 2.78 90.18 2.57 半乳糖 10.89 97.08 0.89 76.98 6.08 86.91 3.65 葡糖糖醛酸 N.D 85.91 0.59 86.95 4.13 89.45 8.15 半乳糖醛酸 9.89 86.72 2.88 87.25 0.89 81.98 5.98 注:“N.D”表示未检出。 2.5 实际样品的检测结果
以建立的方法对市售15份乳清蛋白运动营养粉进行12种糖类化合物分析检测,其检测结果如表6所示,由表6可知,15份样品中的12种糖类化合物均有不同程度检出,且多种单糖在不同样品中含量差异较大。样品编号为S2的乳清蛋白运动营养粉中12种单糖均有检出,其余14种样品中12种单糖均有不同程度检出。
表 6 15份样品中12种糖类化合物的检测结果(mg/g)Table 6. Detection results of 12 carbohydrate compounds in 15 samples (mg/g)样品编号 核糖 木糖 阿拉伯糖 岩藻糖 鼠李糖 甘露醇 甘露糖 葡糖糖 果糖 半乳糖 葡糖糖醛酸 半乳糖醛酸 S1 N.D 12.16±0.14 8.98±0.23 N.D 10.26±0.18 N.D 9.66±0.09 12.57±0.17 13.68±0.19 10.89±0.32 N.D 9.89±0.31 S2 9.98±0.21 15.68±0.19 15.47±0.16 11.66±0.36 9.45±0.11 11.45±0.09 12.01±0.17 15.65±0.24 11.25±0.28 11.77±0.17 11.56±0.26 11.22±0.31 S3 36.45±0.57 N.D 13.56±0.25 11.23±0.16 N.D 12.55±0.13 10.65±0.11 N.D 6.45±0.09 14.55±0.17 15.45±0.21 17.65±0.28 S4 18.56±0.29 11.56±0.37 N.D 16.88±0.46 11.58±0.51 N.D N.D 15.25±0.54 14.25±0.25 N.D 16.98±0.28 19.56±0.31 S5 16.87±0.18 N.D 18.65±0.27 N.D 12.47±0.14 11.78±0.22 10.11±0.14 17.21±0.24 27.56±0.37 N.D 22.45±0.19 N.D S6 13.98±0.41 25.46±0.37 N.D 17.56±0.26 N.D 14.87±0.49 21.25±0.39 N.D N.D 11.24±0.27 N.D 23.25±0.58 S7 N.D N.D 13.99±0.24 10.65±0.34 9.65±0.18 15.65±0.27 N.D 14.25±0.41 17.56±0.36 14.22±0.27 21.25±0.14 18.77±0.34 S8 14.12±0.27 16.44±0.15 10.87±0.21 N.D N.D 8.56±0.11 15.65±0.31 N.D 16.45±0.21 9.56±0.11 17.56±0.24 14.56±0.14 S9 N.D 11.23±0.17 12.77±0.34 14.25±0.26 18.77±0.29 N.D N.D 22.26±0.27 15.77±0.17 15.22±0.31 N.D N.D S10 9.65±0.31 N.D 16.66±0.54 12.55±0.84 27.89±0.69 N.D 11.44±0.37 N.D 23.14±0.25 9.65±0.31 15.47±0.24 N.D S11 13.45±0.27 15.68±0.31 N.D N.D N.D 29.65±0.69 19.65±0.56 N.D N.D 16.56±0.31 25.44±0.58 N.D S12 N.D N.D N.D 21.45±0.47 N.D 18.66±0.36 N.D 14.23±0.41 14.56±0.51 N.D 16.32±0.31 17.56±0.45 S13 N.D 11.35±0.45 18.47±0.61 N.D 24.56±0.47 N.D N.D N.D 32.44±0.41 15.33±0.31 14.35±0.31 N.D S14 17.69±0.34 10.45±0.25 N.D 12.65±0.28 N.D 11.65±0.34 15.45±0.17 N.D 19.65±0.38 17.98±0.41 N.D N.D S15 14.12±0.41 N.D 19.98±0.46 N.D 14.58±0.26 N.D 15.35±0.41 N.D N.D 12.36±0.42 N.D 23.54±0.54 注:“N.D”表示未检出。 3. 结论
本文以乳清蛋白运动营养粉为检测对象,建立最优的样品前处理及仪器分析条件对乳清蛋白运动营养粉中12种糖类化合物进行快速检测分析,通过对试验条件的选择和优化,最终采用提取温度55 ℃、料液比1:20 g/mL、提取功率180 W、提取时间35 min对乳清蛋白运动营养粉进行多糖提取,采用Sevag法除蛋白,直至无蛋白析出,然后经酸水解进行单糖组成测定。采用该方法对乳清蛋白运动营养粉中多糖的单糖组成及含量进行分析检测,样品前处理简单、准确度高、分析时间短、灵敏度高、重现性好。在质量浓度0.1~6.0 μg/mL范围内线性关系良好,相关系数r≥0.995,检出限为0.0037~0.0326 mg/g;定量限为0.0123~0.1087 mg/g,在40、100和160 mg/g的加标浓度下,其加标平均回收率为76.12%~99.12%,相对标准偏差(RSD)为0.12%~10.01%。该方法应用于乳清蛋白运动营养粉中多糖的单糖组成及含量检测结果表明,15份样品中的12种糖类化合物均有不同程度检出,且多种单糖在不同样品中含量差异较大。样品编号为S2的乳清蛋白运动营养粉中12种单糖均有检出,其余14种样品中12种单糖均有不同程度检出。该方法的建立可为乳清蛋白运动营养粉多糖的结构组成及其活性提供技术支撑及基础数据。
-
表 1 正交试验因素水平表
Table 1 Factors and levels table of orthogonal test
因素 水平 1 2 3 A-提取温度(℃) 45 55 65 B-料液比(g/mL) 1:20 1:25 1:30 C-提取功率(W) 160 180 200 D-提取时间(min) 25 35 45 表 2 12种糖的监测离子对、碰撞气能量和去簇电压
Table 2 Monitored ion pairs, collision gas energies and declustering voltages of 12 sugars
序号 化合物 保留时间(min) 母离子(m/z) 子离子(m/z) 去簇电压(eV) 碰撞能量(eV) 1 核糖 6.157 215.6 58.8*88.9149.1 −92 −26−14 2 木糖 7.357 198.8 58.8*89.2149.2 −84 −24−12 3 阿拉伯糖 8.486 218.6 58.9*89.1149.2 −88 −22−16 4 岩藻糖 9.198 196.5 58.8*89.1163.1 −86 −26−18 5 鼠李糖 11.689 208.3 58.9*103.0163.1 −84 −26−16 6 甘露醇 22.218 210.8 58.8*89.0181.1 −100 −26−18 7 甘露糖 23.389 236.5 58.8*89.1179.3 −84 −20−12 8 葡糖糖 25.895 209.8 89.1*71.1179.1 −88 −26−18 9 果糖 30.945 214.5 59.0*89.1179.2 −90 −24−12 10 半乳糖 33.989 220.7 89.1*58.6179.1 −92 −18−10 11 葡糖糖醛酸 34.898 265.8 58.8*113.2193.1 −86 −26−10 12 半乳糖醛酸 37.988 265.8 59.1*73.1193.2 −62 −24−10 注:*为定量离子。 表 3 L9(34)正交试验结果
Table 3 L9(34) orthogonal test results
实验号 A提取温度 B料液比 C提取功率 D提取时间(min) 多糖得率(%) 1 1 1 1 1 8.95 2 1 2 2 2 10.56 3 1 3 3 3 9.68 4 2 1 2 2 13.35 5 2 2 3 1 10.89 6 2 3 1 3 11.58 7 3 1 3 2 11.89 8 3 2 1 3 12.04 9 3 3 2 1 10.56 K1 9.73 11.40 10.86 10.13 K2 11.94 11.16 11.49 11.34 K3 11.50 10.61 10.82 11.69 R 2.21 0.79 0.67 1.56 最优组合 A2B1C2D2 表 4 12种糖类化合物的线性回归方程、检出限及定量限
Table 4 Linear regression equation, detection limit and quantification limit of 15 pesticides
编号 化合物 线性回归方法 相关系数(r) 线性范围(μg/mL) 检出限(mg/g) 定量限(mg/g) 1 核糖 y=6584.154x−213.04 0.998945 0.10~6.00 0.0326 0.1087 2 木糖 y=4104.356x−243.21 0.999128 0.10~6.00 0.0198 0.0660 3 阿拉伯糖 y=4987.651x+257.15 0.996787 0.10~6.00 0.0067 0.0223 4 岩藻糖 y=5312.451x−312.45 0.999154 0.10~6.00 0.0269 0.0897 5 鼠李糖 y=2135.654x−216.45 0.999784 0.10~6.00 0.0091 0.0303 6 甘露醇 y=7452.341x−451.25 0.999647 0.10~6.00 0.0105 0.0350 7 甘露糖 y=4125.351x+315.54 0.999587 0.10~6.00 0.0037 0.0123 8 葡糖糖 y=3058.458x−218.31 0.998982 0.10~6.00 0.0195 0.0650 9 果糖 y=8765.951x−378.54 0.999687 0.10~6.00 0.0058 0.0193 10 半乳糖 y=4986.481x+201.56 0.999458 0.10~6.00 0.0109 0.0363 11 葡糖糖醛酸 y=4013.261x+207.95 0.999687 0.10~6.00 0.0055 0.0183 12 半乳糖醛酸 y=4105.651x+312.45 0.999784 0.10~6.00 0.0108 0.0360 表 5 S1样品中12种糖类化合物加标回收率和RSD(n=6)
Table 5 Spike recoveries and RSD of 12 carbohydrates in S1 sample (n=6)
化合物 S1样品本底值(mg/g) 添加水平40 mg/g 添加水平100 mg/g 添加水平160 mg/g 回收率(%) RSD(%) 回收率(%) RSD(%) 回收率(%) RSD(%) 核糖 N.D 91.25 1.87 86.57 7.89 87.56 4.51 木糖 12.16 83.45 5.16 80.75 9.76 91.35 0.84 阿拉伯糖 8.98 86.91 3.17 98.99 6.03 84.65 9.15 岩藻糖 N.D 89.61 4.26 78.45 2.15 80.25 2.54 鼠李糖 10.26 97.56 3.09 99.12 0.86 91.64 5.16 甘露醇 N.D 86.78 8.94 86.15 0.12 76.12 2.78 甘露糖 9.66 98.68 7.56 83.59 1.78 97.56 3.01 葡糖糖 12.57 88.15 10.01 87.59 5.16 86.09 2.14 果糖 13.68 83.45 2.15 91.78 2.78 90.18 2.57 半乳糖 10.89 97.08 0.89 76.98 6.08 86.91 3.65 葡糖糖醛酸 N.D 85.91 0.59 86.95 4.13 89.45 8.15 半乳糖醛酸 9.89 86.72 2.88 87.25 0.89 81.98 5.98 注:“N.D”表示未检出。 表 6 15份样品中12种糖类化合物的检测结果(mg/g)
Table 6 Detection results of 12 carbohydrate compounds in 15 samples (mg/g)
样品编号 核糖 木糖 阿拉伯糖 岩藻糖 鼠李糖 甘露醇 甘露糖 葡糖糖 果糖 半乳糖 葡糖糖醛酸 半乳糖醛酸 S1 N.D 12.16±0.14 8.98±0.23 N.D 10.26±0.18 N.D 9.66±0.09 12.57±0.17 13.68±0.19 10.89±0.32 N.D 9.89±0.31 S2 9.98±0.21 15.68±0.19 15.47±0.16 11.66±0.36 9.45±0.11 11.45±0.09 12.01±0.17 15.65±0.24 11.25±0.28 11.77±0.17 11.56±0.26 11.22±0.31 S3 36.45±0.57 N.D 13.56±0.25 11.23±0.16 N.D 12.55±0.13 10.65±0.11 N.D 6.45±0.09 14.55±0.17 15.45±0.21 17.65±0.28 S4 18.56±0.29 11.56±0.37 N.D 16.88±0.46 11.58±0.51 N.D N.D 15.25±0.54 14.25±0.25 N.D 16.98±0.28 19.56±0.31 S5 16.87±0.18 N.D 18.65±0.27 N.D 12.47±0.14 11.78±0.22 10.11±0.14 17.21±0.24 27.56±0.37 N.D 22.45±0.19 N.D S6 13.98±0.41 25.46±0.37 N.D 17.56±0.26 N.D 14.87±0.49 21.25±0.39 N.D N.D 11.24±0.27 N.D 23.25±0.58 S7 N.D N.D 13.99±0.24 10.65±0.34 9.65±0.18 15.65±0.27 N.D 14.25±0.41 17.56±0.36 14.22±0.27 21.25±0.14 18.77±0.34 S8 14.12±0.27 16.44±0.15 10.87±0.21 N.D N.D 8.56±0.11 15.65±0.31 N.D 16.45±0.21 9.56±0.11 17.56±0.24 14.56±0.14 S9 N.D 11.23±0.17 12.77±0.34 14.25±0.26 18.77±0.29 N.D N.D 22.26±0.27 15.77±0.17 15.22±0.31 N.D N.D S10 9.65±0.31 N.D 16.66±0.54 12.55±0.84 27.89±0.69 N.D 11.44±0.37 N.D 23.14±0.25 9.65±0.31 15.47±0.24 N.D S11 13.45±0.27 15.68±0.31 N.D N.D N.D 29.65±0.69 19.65±0.56 N.D N.D 16.56±0.31 25.44±0.58 N.D S12 N.D N.D N.D 21.45±0.47 N.D 18.66±0.36 N.D 14.23±0.41 14.56±0.51 N.D 16.32±0.31 17.56±0.45 S13 N.D 11.35±0.45 18.47±0.61 N.D 24.56±0.47 N.D N.D N.D 32.44±0.41 15.33±0.31 14.35±0.31 N.D S14 17.69±0.34 10.45±0.25 N.D 12.65±0.28 N.D 11.65±0.34 15.45±0.17 N.D 19.65±0.38 17.98±0.41 N.D N.D S15 14.12±0.41 N.D 19.98±0.46 N.D 14.58±0.26 N.D 15.35±0.41 N.D N.D 12.36±0.42 N.D 23.54±0.54 注:“N.D”表示未检出。 -
[1] GEORGE J, SONAIANGD S, MOHANTY U, et al. Assembling and optimization of recyclable magnetite cross-linked inulinase aggregates for production of fructose syrups[J]. Materials Letters,2021,14(10):1654−1667.
[2] SAHINDE A, OBAYOMIAE O, SEYOUMR M, et al. Soil texture and properties rather than irrigation water type shape the diversity and composition of soil microbial communities[J]. Applied Soil Ecology,2021,16(11):267−278.
[3] KELLYSWE M, CFRGYTZW F, CAROLINA C, et al. Resistant starch and hydrothermal treatment of cornmeal: Factors in aflatoxins and fumonisin B1 reduction and bioaccessibility[J]. Food Control,2021,26(18):2636−2647.
[4] DRAGANA M, PAVLOVIE, SANDRAW B, et al. Preparation, physicochemical characterization and anti-proliferation of selenium nanoparticles stabilized by Polyporus umbellatus polysaccharide[J]. Bioorganic Chemistry,2021,21(11):2036−2047.
[5] 周雯, 韩丽娟, 马娜娜, 等. 黄刺浆果不同组分多糖理化性质及生物活性的比较[J]. 食品与发酵工业,2022,48(2):189−197. [ZHOU W, HAN L J, MA N N, et al. Comparison of physicochemical properties and biological activities of polysaccharides from different components of Brassica sativus[J]. Food and Fermentation Industries,2022,48(2):189−197. doi: 10.13995/j.cnki.11-1802/ts.027695 [6] 刘颖, 张金莲, 邓亚羚, 等. 黄芪多糖提取、分离纯化及其药理作用研究进展[J]. 中华中医药杂志,2021,36(10):6035−6038. [LIU Y, ZHANG J L, DENG Y L, et al. Research progress on extraction, separation and purification of Astragalus polysaccharides and their pharmacological effects[J]. China Journal of Traditional Chinese Medicine,2021,36(10):6035−6038. [7] 田颖鹏, 陈洁, 汪磊, 等. 提取方法对覆盆子多糖理化性质和体外生物活性的影响[J]. 食品工业科技,2022,43(8):1−10. [TIAN Y P, CHEN J, WANG L, et al. Effects of extraction methods on physicochemical properties and in vitro bioactivity of raspberry polysaccharide[J]. Science and Technology of Food Industry,2022,43(8):1−10. [8] ABUDETY A, NUEWDRTS R, MYQCDEF P, et al. Isolation, structural modification, characterization, and bioactivity of polysaccharides from Folium isatidis[J]. Industrial Crops & Products,2022,41(10):1540−1546.
[9] AHMEDSWA K, KOWRYUB S B, YPTWESDE Y, et al. Efficient and green sulfamic acid catalyzed synthesis of new 1,2-dihydroquinazoline derivatives with antibacterial potential[J]. Arabian Journal of Chemistry,2021,16(15):2789−2798.
[10] UAWANBG M, CARBONELL G, MAGDALRJH B, et al. Anti-herpes activity of polysaccharide fractions from Stevia rebaudiana leaves[J]. Biochemical Systematics and Ecology,2021,36(10):6035−6038.
[11] 秦丹阳, 尚贞子, 钱明雪, 等. 霍山石斛多糖理化性质与生物活性的年动态变化研究[J]. 食品工业科技,2020,41(12):29−34. [QIN D Y, SHANG Z Z, QIAN M X, et al. Study on annual dynamic changes of physicochemical properties and bioactivity of polysaccharides from Dendrobium huoshanense[J]. Science and Technology of Food Industry,2020,41(12):29−34. doi: 10.13386/j.issn1002-0306.2020.12.005 [12] 黎光富, 李刚凤, 史荣荣. 天麻多糖化学成分与药理作用研究综述[J]. 现代农业科技,2016(7):289−290,292. [LI G F, LI G F, SHI R R. A review of the chemical constituents and pharmacological effects of Gastrodia elata polysaccharides[J]. Modern Agricultural Science and Technology,2016(7):289−290,292. doi: 10.3969/j.issn.1007-5739.2016.07.178 [13] 张琪琳, 舒亚民, 潘祥林, 等. 药食同源植物多糖治疗溃疡性结肠炎的药理作用及机制研究进展[J]. 药物评价研究,2021,44(3):644−651. [ZHANG Q L, SHU Y M, PAN X L, et al. Pharmacological action and mechanism of polysaccharides from medical-food homologous plants in the treatment of ulcerative colitis[J]. Drug Evaluation Research,2021,44(3):644−651. [14] 王迎香, 唐子惟, 彭腾, 等. 苯酚-硫酸法测定酒蒸多花黄精多糖含量的优化[J]. 食品工业科技,2021,42(18):308−316. [WANG Y X, TANG Z W, PENG T, et al. Optimization of phenol-sulfuric acid method for determination of polysaccharide content in distilled Polygonatum polygonatum[J]. Science and Technology of Food Industry,2021,42(18):308−316. doi: 10.13386/j.issn1002-0306.2021010069 [15] 沈洁, 周光明, 于璐, 等. 离子色谱-脉冲安培检测法测定原桃胶中的多糖含量[J]. 食品工业科技,2016,37(5):298−301, 307. [SHEN J, ZHOU G M, YU L, et al. Determination of polysaccharide content in raw peach gum by ion chromatography-pulsed amperometric detection[J]. Science and Technology of Food Industry,2016,37(5):298−301, 307. doi: 10.13386/j.issn1002-0306.2016.05.051 [16] 黄庆华, 陈亮, 高理想, 等. 乙酸酐衍生化气相色谱法测定饲料非淀粉多糖含量时适宜称样量确定依据的研究[J]. 动物营养学报,2015,27(5):1620−1631. [HUANG Q H, CHEN L, GAO L X, et al. Study on the basis for determining the appropriate sample size for the determination of feed non-starch polysaccharide content by acetic anhydride derivatized gas chromatography[J]. Journal of Animal Nutrition,2015,27(5):1620−1631. doi: 10.3969/j.issn.1006-267x.2015.05.035 [17] 齐国敏. 高效液相色谱-紫外检测分析凉粉草多糖水解单糖组分[J]. 福建分析测试,2022,31(3):28−33. [QI G M. Analysis of hydrolyzed monosaccharide components of polysaccharide of Gazebo chinensis by high performance liquid chromatography-ultraviolet detection[J]. Fujian Analysis and Test,2022,31(3):28−33. doi: 10.3969/j.issn.1009-8143.2022.03.05 [18] 罗立梅, 陈朝银, 李时琪, 等. 高效液相色谱-蒸发光散射法测定皂荚壳多糖的单糖组分及其含量[J]. 理化检验(化学分册),2013,49(3):270−273. [LUO L M, CHEN C Y, LI S Q, et al. Determination of monosaccharide components and contents of Shitonella sinensis shell polysaccharide by high performance liquid chromatography-evaporative light scattering method[J]. Physical and Chemical Testing (Chemistry),2013,49(3):270−273. [19] WANGERD S, SWDGYUTQA Y, CQARYOHY X, et al. Cationic surfactant-modified palygorskite particles as effective stabilizer for Pickering emulsion gel formation[J]. Applied Clay Science,2019,10(17):5913−5921.
[20] HUANFWEER Z, GEWSDUYT B, DQAHFERD C, et al. Fabrication and characterization of the W/O/W multiple emulsion through oleogelation of oil[J]. Food Chemistry,2021,35(15):25968−25979.
[21] DRIRAQF M, BWQEDSEG M, Ben HLIMAYT H, et al. Improvement of Arabidopsis thaliana salt tolerance using a polysaccharidic extract from the brown algae Padina pavonica[J]. Algal Research,2021,56(16):1056−1069.
[22] 张连龙, 刁春霞, 周华生, 等. 灵硒康口服液中灵芝的鉴别及其灵芝多糖中单糖组成的测定[J]. 食品安全质量检测学报,2019,10(17):5913−5921. [ZHANG L L, DIAO C X, ZHOU H S, et al. Identification of Ganoderma lucidum in Lingsekang oral liquid and determination of monosaccharide composition in Ganoderma lucidum polysaccharides[J]. Journal of Food Safety and Quality Inspection,2019,10(17):5913−5921. doi: 10.19812/j.cnki.jfsq11-5956/ts.2019.17.058 [23] 颉东妹, 王宁丽, 刘笑笑, 等. 微波消解-离子色谱法测定枸杞多糖的含量及组成[J]. 食品安全质量检测学报,2022,13(4):1065−1072. [JIE D M, WANG N L, LIU X X, et al. Determination of content and composition of Lycium barbarum polysaccharides by microwave digestion and ion chromatography[J]. Journal of Food Safety and Quality,2022,13(4):1065−1072. doi: 10.3969/j.issn.2095-0381.2022.4.spaqzljcjs202204007 [24] 张璐, 杨莹莹. 高效液相色谱法测定党参多糖的单糖组成及含量[J]. 中国食品添加剂,2021,32(12):163−169. [ZHANG L, YANG Y Y. Determination of monosaccharide composition and content of Codonopsis polysaccharide by high performance liquid chromatography[J]. China Food Additives,2021,32(12):163−169. doi: 10.19804/j.issn1006-2513.2021.12.022 [25] 王川丕, 诸力, 刘新, 等. 超高效液相色谱-质谱联用技术测定茶叶中8种单、寡糖的含量[J]. 食品科学,2014,35(20):164−169. [WANG C P, ZHU L, LIU X, et al. Determination of 8 kinds of monosaccharides and oligosaccharides in tea by ultra-high performance liquid chromatography-mass spectrometry[J]. Food Science,2014,35(20):164−169. doi: 10.7506/spkx1002-6630-201420033 [26] 杭瑜瑜, 裴志胜, 齐丹, 等. 菠萝皮渣膳食纤维的单糖组分分析及理化性质研究[J]. 食品研究与开发,2017,38(15):26−31. [HANG Y Y, PEI Z S, QI D, et al. Analysis of monosaccharide components and physicochemical properties of dietary fiber from pineapple peel residue[J]. Food Research and Development,2017,38(15):26−31. doi: 10.3969/j.issn.1005-6521.2017.15.006 [27] 叶财发, 蔡跃辉, 曾棋平, 等. 复方首乌藤合剂的总多糖含量测定及单糖组分分析[J]. 药学实践杂志,2020,38(2):161−165. [YE C F, CAI Y H, ZENG Q P, et al. Determination of total polysaccharide content and analysis of monosaccharide component in compound Aconitum sinensis mixture[J]. Journal of Pharmaceutical Practice,2020,38(2):161−165. [28] 陈懿瑶, 罗阳, 闫燊, 等. HPAEC-PAD法测定石斛属植物单糖组分与主成分聚类分析[J]. 中国实验方剂学杂志,2018,24(15):106−111. [CHEN Y Y, LUO Y, YAN S, et al. Determination of monosaccharide components in Dendrobium by HPAEC-PAD method and cluster analysis of principal components[J]. Chinese Journal of Experimental Formulae,2018,24(15):106−111. doi: 10.13422/j.cnki.syfjx.20181046 [29] HAMZAHER N, KJELLBERG M, WUYVGFR G, et al. Assessment of the impact of hydrolysis on bound sulfonamide residue determination in honey using stable isotope dilution ultrahigh performance liquid chromatography tandem mass spectrometry[J]. Food Chemistry,2022,43(13):218−224.
[30] KWQWSVF A K, NUYTSWAD K A, ULYTRDWS B, et al. Average molecular weight, degree of hydrolysis and dry-film FTIR fingerprint of milk protein hydrolysates: Intercorrelation and application in process monitoring[J]. Food Chemistry,2020,31(10):2578−2589.
[31] PITYFERD A, FWETDFDQ V, LQAWSDEFCG M, et al. Accumulation of delphinidin derivatives and other bioactive compound in wild maqui under different environmental conditions and fruit ripening stages[J]. Industrial Crops & Products,2022,14(18):894−906.
[32] 鲁斌, 张凤明, 蔡正达, 等. 梨园块菌多糖提取工艺优化及其单糖组成分析[J]. 食品工业科技,2022,43(13):218−224. [LU B, ZHANG F M, CAI Z D, et al. Optimization of the extraction process of polysaccharide from truffles in pear orchard and analysis of its monosaccharide composition[J]. Food Industry Science and Technology,2022,43(13):218−224. doi: 10.13386/j.issn1002-0306.2021100234 [33] 张强, 韦婉珍, 罗小莉, 等. 响应面优化南酸枣叶多糖的提取工艺及其抗氧化活性[J]. 食品研究与开发,2021,42(22):150−156. [ZHANG Q, WEI W Z, LUO X L, et al. Response surface methodology to optimize the extraction process and antioxidant activity of polysaccharides from leaves of Nansuanjujube[J]. Food Research and Development,2021,42(22):150−156. doi: 10.12161/j.issn.1005-6521.2021.22.023 [34] 董超, 李晶, 杨秦, 等. 高效液相色谱-串联质谱法结合多糖衍生物手性固定相拆分氰戊菊酯[J]. 分析试验室,2020,39(4):448−453. [DONG C, LI J, YANG Q, et al. Resolution of fenvalerate by high performance liquid chromatography-tandem mass spectrometry combined with chiral stationary phase of polysaccharide derivatives[J]. Analytical Laboratory,2020,39(4):448−453. doi: 10.13595/j.cnki.issn1000-0720.2019.101703 [35] 焦健, 朱振军, 佟志晏, 等. HPLC-MS/MS法分析刺参及其制品中海参多糖的含量[J]. 中国渔业质量与标准,2020,10(5):12−17. [JIAO J, ZHU Z J, TONG Z Y, et al. Analysis of sea cucumber polysaccharide content in sea cucumber and its products by HPLC-MS/MS method[J]. China Fisheries Quality and Standards,2020,10(5):12−17. doi: 10.3969/j.issn.2095-1833.2020.05.003 [36] 郭丽, 刘斌, 温成荣, 等. HPLC-MS/MS定性分析大菱鲆不同组织中多糖成分[J]. 食品科学,2017,38(8):171−178. [GUO L, LIU B, WEN C R, et al. Qualitative analysis of polysaccharide components in different tissues of turbot by HPLC-MS/MS[J]. Food Science,2017,38(8):171−178. doi: 10.7506/spkx1002-6630-201708027 -
期刊类型引用(5)
1. 何遂庆,吴芳丽,李爱珍. 高效液相色谱法快捷测定黄原胶中D-甘露糖含量的探究. 安徽医药. 2024(06): 1109-1111 .  百度学术
百度学术
2. 陈士国,张唯希,朱凯,侯志强,叶兴乾. 食源性碳水化合物结构解析新技术前沿与展望. 中国食品学报. 2024(09): 1-17 .  百度学术
百度学术
3. 高文庆,王晴,霍志鹏,何毅. UFLC-MS/MS检测微晶纤维素中葡萄糖和纤维二糖的方法建立及其在热降解分析中的应用. 天津药学. 2024(06): 26-30 .  百度学术
百度学术
4. 王洋,刘永灵. 超高效液相色谱-串联质谱法测定4种运动饮料中多糖的单糖组成及含量. 中国食品添加剂. 2023(07): 240-247 .  百度学术
百度学术
5. 蔡肖,刘军玲,邢丽花,张晓倩,马梦真,吕家慧,冯唯一,俞年军. 霍山石斛超微粉物理特性及石斛多糖中单糖分析. 中国食品添加剂. 2023(10): 143-152 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:


 下载:
下载:



