The Interaction between Betanin and Whey Protein: Based on Multi-spectroscopy and Molecular Simulation
-
摘要: 为研究甜菜苷(Betanin)与乳清分离蛋白(Whey protein isolate, WPI)的相互作用及乳清分离蛋白对甜菜苷热稳定的影响,本文通过自组装法构建了WPI-Betanin复合物,利用紫外可见光谱验证了复合物的形成,并通过荧光光谱和圆二色谱探究了复合物形成的作用机制及蛋白质结构的变化,最后采用分子模拟技术将复合物相互作用可视化。结果表明,甜菜苷与乳清分离蛋白主要通过氢键与范德华力形成复合物,结合位点数约为1。复合物的形成导致蛋白的浊度增加,表面疏水性降低,内源荧光猝灭,且猝灭机制为静态猝灭,常温下的猝灭常数为1.78×103 L/mol。相互作用改变了乳清分离蛋白中色氨酸、酪氨酸的微环境和二级结构含量,使甜菜苷在80 ℃下加热1 h的保留率从6.17%提高到27.26%。本研究为功能性蛋白色素复合物的应用开发和甜菜苷的护色提供了理论基础。Abstract: In order to study the interaction between betanin and whey protein isolate (WPI) and the effect of whey protein isolate on the thermal stability of betanin, WPI-Betanin complex was constructed by self-assembly method. UV-vis spectroscopy was used to verify the formation of complex. The mechanism of complex formation and the changes of protein structure were investigated by fluorescence spectroscopy and circular dichroism, and the complex was visualized by molecular simulation technology. The results showed that betanin and whey protein isolate formed a complex mainly through van der Waals force and hydrogen bond, and the number of binding sites was about 1. The formation of the complex resulted in increased turbidity and decreased surface hydrophobicity of the protein, and the quenching mechanism was static, with a quenching constant of 1.78×103 L/mol at room temperature. The interaction changed secondary structure contents and the microenvironment of tryptophan and tyrosine in whey protein isolate. Moreover, the thermal stability of betanin was improved by WPI. The retention rate of betanin increased from 6.17% to 27.26% after heating at 80 ℃ for 1 h. This study provides a theoretical basis for the application and development of functional protein pigment complex and the color protection of betanin.
-
Keywords:
- betanin /
- whey protein /
- interaction /
- spectroscopy /
- molecular simulation.
-
甜菜苷(Betanin,BT)是一种天然含氮的水溶性色素,呈现玫瑰红至紫红色[1]。广泛分布于仙人掌科、陆商科、苋科等多种植物中,因最早在甜菜根中被发现而得名。甜菜苷是一类可食用天然色素,被批准用于食品和药品中的红色着色剂[2]。甜菜苷作为一种天然产物,具有抗氧化、抗癌、抗炎症、降血压、降血脂等多种益于人体健康的生物活性[3]。与花青素相比,甜菜苷能在富含维生素C和低酸性环境下维持稳定的结构和色泽[4],具有非常广阔的应用前景。然而,温度、pH、氧气等多种因素会促进甜菜苷的降解,使其从艳丽的紫红色褪为浅黄色,其抗氧化性等活性也随之下降。高温作为影响甜菜苷稳定性的最大因素,在食品加工工业中极大地限制了甜菜苷的应用。因此,寻找一种合适的保护方法至关重要。
蛋白质作为一种公认安全的可食用载体,因具有丰富营养和良好功能特性而广泛应用于食品工业中[5],可以与多种生物活性物质发生相互作用,形成复合物并扩大生物活性物质在食品工业中的应用范围。乳清蛋白是一种优质的动物全价蛋白质,营养价值高,容易消化吸收,具有多种人体必需的氨基酸[6],有优良的溶解性、乳化性、起泡性等,在食品领域应用广泛。乳清蛋白是指牛乳在pH4.6时酪蛋白沉淀后的可溶性蛋白的总称,占乳蛋白的18%~20%[7]。乳清分离蛋白(Whey protein isolate, WPI)是将蛋白质含量纯化至90%以上的乳清蛋白粉末。
目前有大量的研究表明,蛋白质能与小分子发生相互作用,形成复合物,对蛋白质的结构和功能产生影响并保护小分子的活性。蛋白质与甜菜苷相互作用的研究虽不多,却为提高甜菜苷的稳定性提供了良好的思路。大豆蛋白纤维被证明能与甜菜苷通过疏水相互作用形成聚集体,并提高甜菜苷的热稳定性[8];11S藜麦种子蛋白与甜菜苷结合并作为甜菜苷的负载体,能减少甜菜苷与氧和光的接触,从而提高甜菜苷的稳定性[9]。由此可见,蛋白可能是一类较好的主体生物聚合物,能与甜菜苷发生相互作用,从而提高甜菜苷稳定性。然而,目前关于蛋白与甜菜苷相互作用机制的研究较少,且蛋白质提高甜菜苷稳定性的机理尚不明确。因此,为探明甜菜苷与蛋白质的相互作用机制及对甜菜苷稳定性的影响,本研究以乳清分离蛋白和甜菜苷为研究对象,明确乳清分离蛋白对甜菜苷热稳定的影响以及甜菜苷对蛋白内源荧光、表面疏水性、二级结构的影响,并采用多光谱学结合分子模拟的方法探究乳清分离蛋白与甜菜苷的相互作用机制,为色素稳定的研究及功能性蛋白色素复合物的应用开发提供理论基础。
1. 材料与方法
1.1 材料与仪器
乳清分离蛋白(WPI,Hilmar 9410,纯度>90%) 美国Hilmar公司;甜菜苷(用糊精稀释的红甜菜根的提取物,CAS:S26010-25g) 上海源叶生物科技有限公司;8-苯胺-1-萘磺酸盐(ANS) 美国Sigma公司;PBS磷酸盐缓冲液 北京索莱宝科技有限公司。
UV-2450紫外可见分光光度计 日本Shimadzu公司;F-7000型荧光光度计 日本Hitachi公司;MOS-450型圆二色谱仪 法国Bio-Logic公司。
1.2 实验方法
1.2.1 乳清分离蛋白-甜菜苷复合物的制备
乳清分离蛋白粉末溶于10 mmol/L PBS 缓冲液(pH7.0),过夜搅拌以使蛋白质充分水合,在4 ℃下保存。甜菜苷溶于10 mmol/L PBS 缓冲液(pH7.0),现配现用。复合物的制备方法在Huang等[10]的基础上稍作修改。乳清分离蛋白溶液与甜菜苷溶液按一定比例混合,磁力搅拌30 min,形成乳清分离蛋白-甜菜苷混合液。
1.2.2 浊度的测定
采用紫外可见分光光度计在600 nm处测量WPI-Betanin混合液的浊度,以相应浓度的甜菜苷水溶液作为空白,通过宏观浊度的比较初步判定复合物的形成[11]。乳清分离蛋白的终浓度为20 mg/mL,乳清分离蛋白与甜菜苷的质量比分别为16:0、16:1、16:2、16:4、16:8。
1.2.3 紫外光谱测定
采用紫外光谱测定WPI-Betanin体系的紫外吸收,实验方法在Cai等[12]的方法上稍作修改,将1.6 mg/mL乳清分离蛋白母液与0.4 mg/mL甜菜苷母液按不同比例配制成具有不同甜菜苷含量的WPI-Betanin混合体系,使得体系中蛋白浓度为0.8 mg/mL、甜菜苷浓度为0.05、0.1、0.2 mg/mL。扫描WPI-Betanin混合体系在250~345 nm的紫外图谱,以甜菜苷水溶液的紫外吸收为空白,并予以扣除。
1.2.4 内源荧光光谱测定
采用F-7000荧光光谱仪测定WPI-Betanin混合体系的内源荧光。荧光光谱测量方法根据前人的研究方法[13]有所改动。将1.6 mg/mL乳清分离蛋白母液与0.4 mg/mL甜菜苷母液按不同比例配制成具有不同甜菜苷含量的WPI-Betanin混合体系,使得体系中蛋白浓度为0.8 mg/mL、甜菜苷浓度为0.025、0.05、0.075、0.1、0.125、0.15、0.175、0.2 mg/mL。在298、304、310 K温度条件下,测定WPI-Betanin混合体系的内源荧光,激发波长为280 nm,激发和发射狭缝波长均为2.5 nm,在290~480 nm处收集荧光发射光谱,扫描前分别在298、304、310 K温度条件下水浴30 min。
内源荧光猝灭数据采用Stern-Volmer方程(1)分析,WPI-Betanin复合物的结合常数与结合位点通过双对数方程(2)计算,采用Van’t Hoff方程(3)和方程(4)计算WPI-Betanin复合物结合过程中的焓变(ΔH),熵变(ΔS)和吉布斯自由能变化(ΔG),进一步推断复合物的相互作用机制[14]。
F0Fc=1+Kqτ0[BT]=1+KSV[BT] (1) 式中:F0:乳清分离蛋白起始内源荧光;Fc:添加甜菜苷之后的内源荧光;[BT]:甜菜苷浓度;KSV:Stern-Volmer猝灭常数;Kq:乳清分离蛋白猝灭速率;τ0:生物大分子猝灭平均寿命6.2×10−9 s[15]。
logF0-FcFc=logKa+nlog[BT] (2) lnKa=ΔHRT+ΔSR (3) ΔG=ΔH-TΔS (4) 式中:Ka:结合常数;通用气体常数R=8.314 J·mol−1·K−1;反应温度T=298、304、310 K。
1.2.5 表面疏水性的测定
采用F-7000荧光光度计,以8-苯胺-1-萘磺酸盐(ANS)为荧光探针测定表面疏水性[16],激发波长为390 nm,激发狭缝宽度为2.5 nm,发射狭缝宽度为5.0 nm。将16 μL 8 mmol/L ANS添加到3.2 mL WPI-Betanin混合溶液(蛋白浓度为0.8 mg/mL,甜菜苷浓度分别为0.025、0.05、0.075、0.1、0.125、0.15、0.175、0.2 mg/mL)中。相应的甜菜苷的背景荧光被扣除以矫正荧光数据,以ANS荧光强度来表示乳清分离蛋白的表面疏水性[17]。
1.2.6 圆二色谱的测定
采用圆二色谱仪测定WPI-Betanin复合体系的远紫外圆二色谱。在乳清分离蛋白浓度为0.8 mg/mL,甜菜苷浓度分别为0 (对照组)、0.1、0.2 mg/mL时,测定乳清分离蛋白在200~240 nm下的远紫外吸收。扣除相应浓度的甜菜苷背景后,根据DICHROWEB CONTIN在线的方法计算乳清分离蛋白的α-螺旋、β-折叠、β-转角、无规则卷曲含量变化[18]。
1.2.7 分子对接模拟
采用Discovery Studio 2019软件中的CDOCKER程序进行分子对接可视化地研究乳清分离蛋白与甜菜苷的相互作用。CDOCKER程序是Discovery Studio中的一种半柔性分子对接分析方法。从PDB数据库中获取了包括β-乳球蛋白(PDB: 3NPO)、α-乳白蛋白(PDB: 1HFZ)、牛血清白蛋白(PDB: 3V03)和乳铁蛋白(PDB: 1BLF)在内的乳清分离蛋白的主要蛋白结构,从PubChem数据库中获得甜菜苷分子结构。然后将甜菜苷结构及以上四种蛋白结构导入分子对接软件中,受体蛋白与配体甜菜苷赋予CHARMm力场,采用CDOCKER程序进行分子对接。在2000步的加热程序下将WPI-Betanin加热至700 K,然后在5000步的降温程序下将WPI-甜菜苷降温至298 K。保存最多10个对接结果,对接的聚类半径为0.5 Å。选择CDOCKER相互作用能(CDOCKER interaction energy)最低的对接结果为最优构象,进行相互作用分析。
1.2.8 乳清分离蛋白对甜菜苷的保护作用
为了便于观察蛋白质对甜菜苷的热保护效果,从宏观上体现乳清分离蛋白-甜菜苷复合物在加热过程中的颜色变化,本部分采用较高浓度的乳清分离蛋白与甜菜苷进行实验。分别制备WPI终浓度为5、10 mg/mL,甜菜苷终浓度为5 mg/mL的WPI-Betanin复合物,使体系中WPI与甜菜苷的质量比分别为1:1和2:1。甜菜苷溶于PBS缓冲液作为对照组。三组溶液在避光条件下80 °C水浴加热60 min。此后,将样品放入冰水中冷却,然后在设定的时间(0、10、30、60 min)进行表征。WPI-Betanin混合体系中甜菜苷含量的测量方法在Liu等[19]的基础上略加改动,将样品以2500 g(8000 r/min)离心30 min后使用紫外-可见分光光度计测定甜菜苷的浓度,根据标准曲线法在538 nm处测定甜菜苷含量。
1.3 数据处理
所有试验均重复三次或以上,采用SPSS 25.0软件进行数据的计算整理和统计分析,使用Origin 2021软件绘图。试验数据以平均数±平均偏差表示,P<0.05代表样品间存在显著性差异,在图中用不同字母表示。
2. 结果与分析
2.1 乳清分离蛋白-甜菜苷复合物的形成
通过使用紫外可见光谱法测量浊度来验证WPI-Betanin复合物的形成。当由光波的散射而形成胶体粒子时,溶液的浊度会增加。浊度增加的幅度取决于颗粒的数量、大小和折射率对比度等。因此,浊度的测量可以快速指示胶态颗粒的形成[20]。图1显示了乳清分离蛋白:甜菜苷质量比对乳清分离蛋白-甜菜苷溶液的外观和浊度的影响。当乳清分离蛋白与甜菜苷的比例从16:0增加至16:8时,浊度从0.290显著提高至0.306 cm−1(P<0.05),从外观上看,溶液变得越来越混浊,但在室温下储存一天之后,也并没有沉淀迹象。这些结果表明乳清分离蛋白与甜菜苷形成了相对较小的胶体复合物,具有较强的抗重力沉淀能力。
2.2 紫外光谱
蛋白质分子微环境中芳香族氨基酸残基的变化可能会导致蛋白质的紫外吸收发生变化,因此可以应用蛋白质的紫外光谱来分析蛋白质的结构变化。紫外光谱可反映乳清分离蛋白与甜菜苷间的相互作用,表现为紫外光谱峰值的蓝移或红移、信号的增强或减弱。图2中显示乳清分离蛋白在280 nm处有最大吸收峰,此处的吸收可能是由于色氨酸(Trp)和酪氨酸(Tyr)存在C=O键的紫外吸收[12]。乳清分离蛋白的紫外吸收随着甜菜苷浓度的增加而增加,进一步证明乳清分离蛋白与甜菜苷发生了相互作用,改变了色氨酸和酪氨酸的微环境[13]。吴云雪等[21]观察到了类似的现象,表没食子儿茶素没食子酸酯(EGCG)与乳清分离蛋白发生相互作用,蛋白的紫外吸收随着EGCG含量的增加而增加。
2.3 荧光发射光谱
于280 nm的激发波长,测定了0.6~1.2 mg/mL乳清分离蛋白的内源荧光强度。从图3A可得知,乳清分离蛋白在0.6~1.2 mg/mL的浓度范围内蛋白的荧光强度随其浓度呈现先增后减的关系,且分为两段线性关系,最大值位于0.9 mg/mL,因此选择了0.8 mg/mL的蛋白浓度进行内源荧光实验,该浓度可以避免蛋白浓度过高而引起的内滤效应,提高实验精度。图3B~D显示了在298、304、310 K温度下,不同浓度甜菜苷对乳清分离蛋白内源荧光的猝灭效果。乳清分离蛋白的色氨酸在280 nm的激发波长下在332 nm处有最大的荧光发射峰,荧光强度随着甜菜苷浓度的增加而不断下降,表明甜菜苷对乳清分离蛋白有荧光猝灭效果。此外,由图2中可知,甜菜苷在0.2 mg/mL浓度下,其紫外吸收非常低,(A280+A332)/2<0.1,这表明甜菜苷对乳清分离蛋白几乎不产生内滤效应[16],这个荧光强度的下降可能是由于甜菜苷与乳清分离蛋白发生了相互作用并形成复合物,改变了乳清分离蛋白中酪氨酸和色氨酸的微环境。类似的现象也出现在一些多酚与乳清分离蛋白的相互作用中,咖啡酸(CA)、表没食子儿茶素没食子酸酯(EGCG)与乳清分离蛋白通过非共价相互作用结合,猝灭了乳清分离蛋白的内源荧光[22]。
2.4 荧光猝灭机制及结合参数
如图4所示,在298、304、310 K温度下,Stern-Volmer方程具有良好的拟合性,表明甜菜苷猝灭为动态或静态单一猝灭类型[23]。由表1可知,在298、304、310 K温度下,WPI-Betanin的猝灭常数分别为2.06×102·mol−1、2.26×102·mol−1和2.58×102·mol−1。最小的猝灭速率常数Kq (Kq=KSV/τ0)为3.32×1010 L·mol−1·s−1明显大于各类猝灭剂对生物大分子的最大动态猝灭速率2.0×1010 L· mol−1·s−1,表明甜菜苷猝灭乳清分离蛋白内源荧光的机制为静态猝灭过程[24]。对于静态猝灭过程,可以采用双对数方程(2)计算乳清分离蛋白与甜菜苷之间的结合常数和结合位点数。从表1中可知,在不同温度下甜菜苷与乳清分离蛋白的结合常数分别为1783.16 L/mol (298 K)、672.59 L/mol(304 K)、259.81 L/mol(310 K),结合常数随温度的升高而明显降低,说明温度对乳清分离蛋白-甜菜苷相互作用的影响比较大,温度较低时结合得越紧密,这可能是因为活性小分子甜菜苷对高温较敏感。温度对结合位点数几乎没有影响,三种温度下的结合位点数均接近1,表明乳清分离蛋白与甜菜苷以1:1的比例复合。
表 1 乳清分离蛋白与甜菜苷的结合参数Table 1. Binding parameters of WPI and betanin温度
(K)KSV
(102·mol−1)Kq
(1010 L·mol−1·s−1)n Ka
(L/mol)ΔH
(kJ/mol)ΔS
(J·mol−1·K−1)ΔG
(kJ/mol)298 2.06 3.32 1.26±0.03 1783.16 − − −18.55 304 2.26 3.65 1.13±0.03 672.59 −123.28 −351.42 −16.44 310 2.58 4.16 1.00±0.04 259.81 − − −14.34 相互作用的Van’t Hoff方程为Y=14827.67X−42.27(R2=0.99),热力学参数ΔH和ΔS可由方程的斜率和截距得出。蛋白质与活性小分子之间常常通过静电作用力、疏水作用力、氢键和范德华力等非共价相互作用结合成复合物[25]。根据热力学参数的不同,可判断二者结合的作用力类型。蛋白质与小分子结合时,若ΔH>0及ΔS>0时,主要表现为疏水作用;若ΔH<0及ΔS>0,主要表现为静电作用;ΔH<0及ΔS<0,主要表现为氢键或范德华力作用[26]。由表1可知,ΔG为负值表明WPI-Betanin复合物为自发结合的过程,ΔH和ΔS均为负值表明WPI-Betanin复合物的形成为焓驱动反应,且主要相互作用为范德华力和氢键相互作用。
2.5 表面疏水性
疏水基团指示着蛋白质的三级结构,利用ANS荧光探针探究乳清分离蛋白与不同浓度甜菜苷结合后表面疏水性的变化。由图5所示,乳清分离蛋白的表面疏水性随着甜菜苷含量的增加而逐渐降低。表面疏水性的降低可能是由于从甜菜苷引入了极性基团(羧基和羟基)所致[27]。此外,甜菜苷与蛋白质表面上的疏水性氨基酸侧链基团(尤其是芳香环)结合导致荧光探针ANS可检测的表面疏水性基团减少,这两个因素都会导致疏水性降低。表没食子儿茶素没食子酸酯(EGCG)也被观察到能使乳清蛋白的表面疏水性降低,并在240 μmol/g的EGCG浓度下降低50%[28]。
2.6 圆二色谱
圆二色谱主要反映蛋白质二级结构的变化。图6显示,乳清分离蛋白的圆二色谱在216 nm附近显示了一个负峰,这是二级结构β-折叠的特征峰。如表2所示,在不存在甜菜苷的情况下,乳清分离蛋白含有12.5%的α-螺旋,31.1%的β-折叠,24.4%的β-转角和31.9%的无规则卷曲,随着甜菜苷浓度的增加,α-螺旋含量和β-转角含量分别降至10.1%和23.8%,而β-折叠含量增加至34.2%。由此可推断出,乳清分离蛋白与甜菜苷之间的相互作用可能导致了蛋白质多肽链的部分解折叠,并破坏了用于稳定螺旋结构的氢键,使得蛋白质的结构变得更加松散[29]。花青素与乳清蛋白相互作用也有类似的现象,乳清蛋白与紫薯粉花青素结合后,α-螺旋含量从20.8%下降到13.4%,花青素分子在乳清蛋白的α-螺旋区域结合,破坏了稳定螺旋结构的氢键[30]。
表 2 不同浓度甜菜苷对乳清分离蛋白二级结构的影响Table 2. Effects of different concentrations of betanin on secondary structure of WPI样品 α-螺旋(%) β-折叠(%) β-转角(%) 无规卷曲(%) 空白 12.5 31.1 24.4 31.9 0.1 mg/mL甜菜苷 10.8 33.6 24.0 31.6 0.2 mg/mL 甜菜苷 10.1 34.2 23.8 31.9 2.7 分子模拟
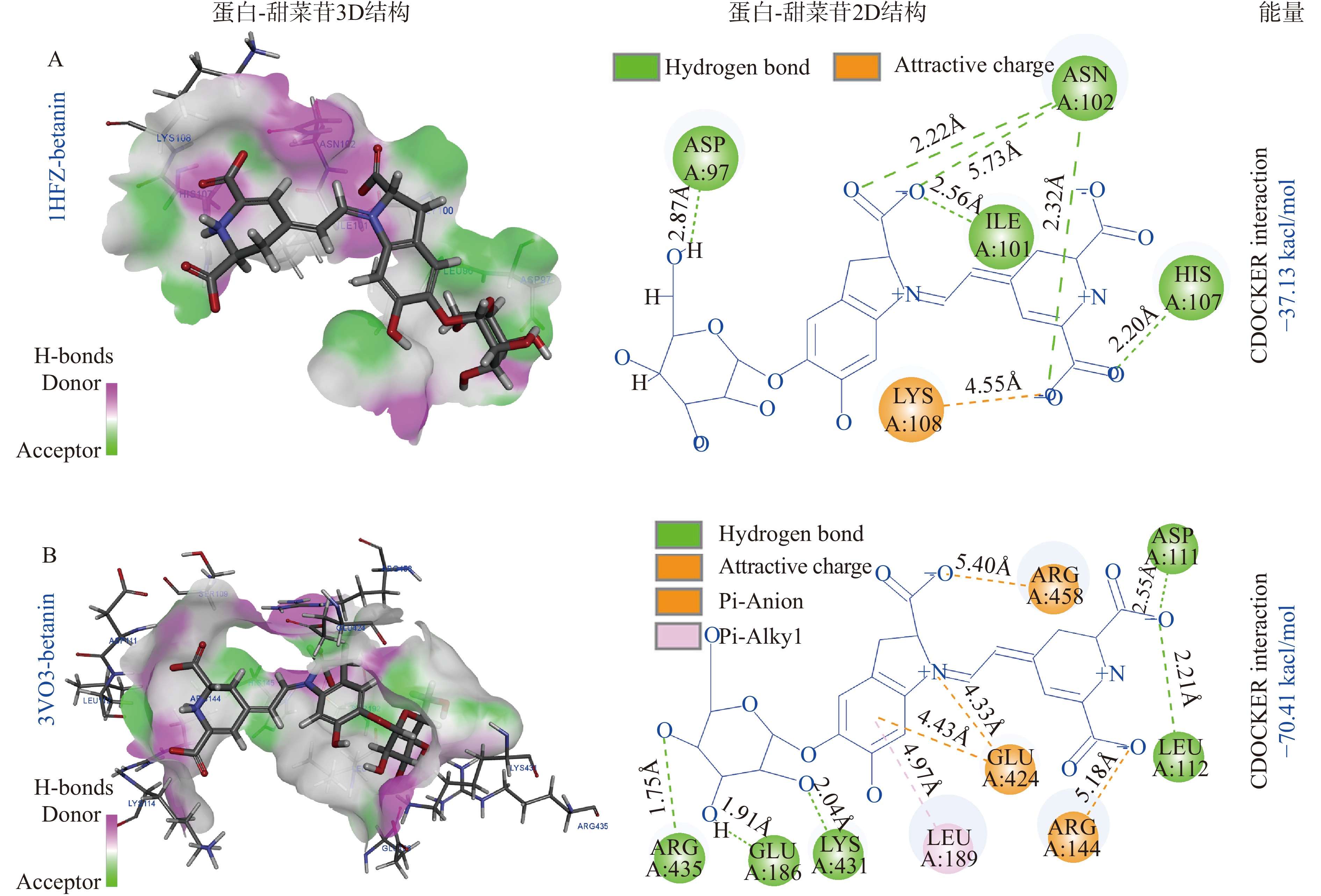
为了进一步研究乳清分离蛋白与甜菜苷之间相互作用的位置,采用CDOCHER分子对接可视化地进行对接模拟。如图7所示,甜菜苷分别与乳清分离蛋白的主要成分α-乳白蛋白(1NFZ)、牛血清蛋白(3VO3)、乳铁蛋白(1BLF)和β-乳球蛋白(3NPO)对接,甜菜苷被WPI包裹在内部。α-乳白蛋白(1HFZ)的His 107、 Asn 102、 He 101、 Asp 97与甜菜苷通过氢键相互作用结合,且Asn 102与甜菜苷形成了多个氢键(2.22 Å、5.73 Å、2.32 Å),Lys 108与甜菜苷有静电相互作用;牛血清蛋白(3V03)与甜菜苷主要通过氢键相互作用结合(Arg 435、Glu 186、 Lys 431、Arg 144、Leu 112、 Asp 111);乳铁蛋白(1BLF)的Ser 185、 His 253、Glu 187、Pro 188与甜菜苷形成氢键,Asp 197、 Glu 15、 Lys 197通过静电相互作用与甜菜苷结合;β-乳球蛋白(3NPO)主要通过氢键(Gln 120、Pro 38)和静电相互作用(Phe 105)与甜菜苷结合。总体而言,四种蛋白质与甜菜苷结合以氢键相互作用为主,与圆二色谱数据结合,可推断甜菜苷被包裹在蛋白质中,与乳清分离蛋白中α-螺旋结构中的氨基酸发生了大量的氢键相互作用,从而破坏了蛋白质α-螺旋中原有的氢键,降低了α-螺旋的含量。
2.8 乳清分离蛋白对甜菜苷的保护作用
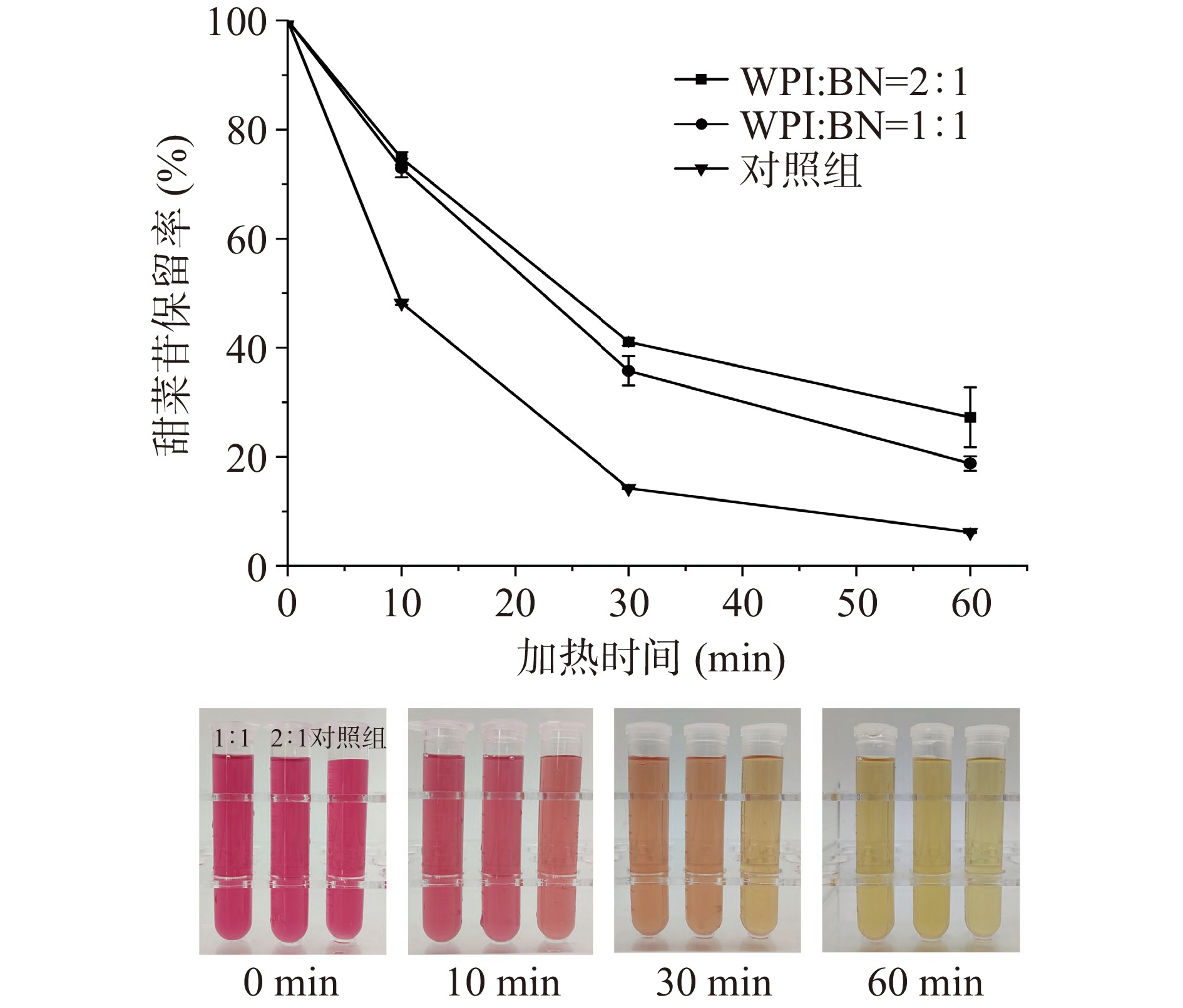
蛋白质分子可以与小分子物质通过自组装形成纳米运载体,以封装和保护某些活性物质,或改善产品的稳定性和外观[31]。如图8所示,与乳清分离蛋白形成复合物后,甜菜苷在80 ℃下的保留率提高,且随着乳清分离蛋白比例的增加而增加。加热1 h后,甜菜苷水溶液(对照组)中的甜菜苷保留率仅为6.17%,而乳清分离蛋白与甜菜苷1:1复合后,保留率增加到18.78%,二者2:1复合时,甜菜苷保留率为27.26%。表明在高温条件下,乳清分离蛋白对甜菜苷有一定的保护作用,且该保护作用依赖于蛋白质含量。结合前文相互作用及分子模拟的研究结果,推断该保护作用可能归因于甜菜苷被乳清分离蛋白包裹在内部,与蛋白中氨基酸发生了大量的非共价相互作用,在一定程度上避免了甜菜苷的热降解。
3. 结论
本文通过多光谱学和分子模拟技术研究了乳清分离蛋白与甜菜苷的相互作用,并探讨了乳清分离蛋白对甜菜苷的热稳定性影响及甜菜苷对乳清分离蛋白结构性质的影响。结果表明乳清分离蛋白对甜菜苷热稳定性的提高具有显著性影响,使甜菜苷在80 ℃下加热1 h的保留率从6.17%提高到27.26%,稳定性的提高与乳清分离蛋白-甜菜苷复合物的形成有关。乳清分离蛋白与甜菜苷通过范德华力和氢键发生相互作用以1:1的比例形成复合物,从而提升甜菜苷的热稳定性。同时,甜菜苷的加入使乳清分离蛋白表面疏水性降低,α-螺旋和β-转角的含量降低,β-折叠和无规卷曲的含量增加。本文深入探究了甜菜苷与乳清分离蛋白的相互作用,对于甜菜苷的保护、运载等方面的研究提供了思路,为功能性蛋白色素复合物的应用开发提供了理论基础。
-
表 1 乳清分离蛋白与甜菜苷的结合参数
Table 1 Binding parameters of WPI and betanin
温度
(K)KSV
(102·mol−1)Kq
(1010 L·mol−1·s−1)n Ka
(L/mol)ΔH
(kJ/mol)ΔS
(J·mol−1·K−1)ΔG
(kJ/mol)298 2.06 3.32 1.26±0.03 1783.16 − − −18.55 304 2.26 3.65 1.13±0.03 672.59 −123.28 −351.42 −16.44 310 2.58 4.16 1.00±0.04 259.81 − − −14.34 表 2 不同浓度甜菜苷对乳清分离蛋白二级结构的影响
Table 2 Effects of different concentrations of betanin on secondary structure of WPI
样品 α-螺旋(%) β-折叠(%) β-转角(%) 无规卷曲(%) 空白 12.5 31.1 24.4 31.9 0.1 mg/mL甜菜苷 10.8 33.6 24.0 31.6 0.2 mg/mL 甜菜苷 10.1 34.2 23.8 31.9 -
[1] AZEREDO H M C. Betalains: Properties, sources, applications, and stability-A review[J]. International Journal of Food Science & Technology,2009,44(12):2365−2376.
[2] ESATBEYOGLU T, WAGNER A E, SCHINI-KERTH V B, et al. Betanin a food colorant with biological activity[J]. Molecular Nutrition & Food Research,2015,59(1):36−47.
[3] GANDIA-HERRERO F, ESCRIBANO J, GARCIA-CARMONA F. Biological activities of plant pigments betalains[J]. Critical Reviews in Food Science and Nutrition,2016,56(6):937−945. doi: 10.1080/10408398.2012.740103
[4] TEIXEIRA DA SILVA D V, BAIAO D D S, SILVA F D O, et al. Betanin, a natural food additive: Stability, bioavailability, antioxidant and preservative ability assessments[J]. Molecules,2019,24:458. doi: 10.3390/molecules24030458
[5] CHEN L Y, REMONDETTO G E, SUBIRADE M. Food protein-based materials as nutraceutical delivery systems[J]. Trends in Food Science & Technology,2006,17(5):272−283.
[6] 汪姣玲. 乳清蛋白美拉德改性及其产物功能特性研究 [D]. 无锡: 江南大学, 2015. WANG J L. Study on characteristics and functional properties of Maillard reaction products from whey protein[D]. Wuxi: Jiangnan University, 2015.
[7] 倪莹宙. 乳清分离蛋白乳状液/冷凝胶制备和消化研究 [D]. 无锡: 江南大学, 2016. NI Y Z. Study on the preparation and in vitro digestion of whey protein isolate emulsions/cold-set gels[D]. Wuxi: Jiangnan University, 2016.
[8] ZHAO H S, MA Z, JING P. Interaction of soy protein isolate fibrils with betalain from red beetroots: Morphology, spectroscopic characteristics and thermal stability[J]. Food Research International,2020,135:109289. doi: 10.1016/j.foodres.2020.109289
[9] MARTÍNEZ J H, VELÁZQUEZ F, BURRIEZA H P, et al. Betanin loaded nanocarriers based on quinoa seed 11S globulin. Impact on the protein structure and antioxidant activity[J]. Food Hydrocolloids,2019,87:880−890. doi: 10.1016/j.foodhyd.2018.09.016
[10] HUANG Y, LI A J, QIU C Y, et al. Self-assembled colloidal complexes of polyphenol-gelatin and their stabilizing effects on emulsions[J]. Food & Function,2017,8(9):3145−3154.
[11] LI C H, DAI T T, CHEN J, et al. Protein-polyphenol functional ingredients: The foaming properties of lactoferrin are enhanced by forming complexes with procyanidin[J]. Food Chemistry,2021,339:128145. doi: 10.1016/j.foodchem.2020.128145
[12] CAI X, YU J N, XU L M, et al. The mechanism study in the interactions of sorghum procyanidins trimer with porcine pancreatic alpha-amylase[J]. Food Chemistry,2015,174:291−298. doi: 10.1016/j.foodchem.2014.10.131
[13] DAI T T, CHEN J, MCCLEMENTS D J, et al. Protein-polyphenol interactions enhance the antioxidant capacity of phenolics: Analysis of rice glutelin-procyanidin dimer interactions[J]. Food & Function,2019,10(2):765−774.
[14] DAI T T, LI R Y, LIU C M, et al. Effect of rice glutelin-resveratrol interactions on the formation and stability of emulsions: A multiphotonic spectroscopy and molecular docking study[J]. Food Hydrocolloids,2019,97:105234. doi: 10.1016/j.foodhyd.2019.105234
[15] LAKOWICZ J R, WEBER G. Quenching of protein fluorescence by oxygen. Detection of structural fluctuations in proteins on the nanosecond time scale[J]. Biochemistry,1973,12(21):4171−4179. doi: 10.1021/bi00745a021
[16] KATO A, NAKAI S. Hydrophobicity determined by a fluorescence probe method and its correlation with surface properties of proteins[J]. Biochimica Et Biophysica Acta,1980,624(1):13−20. doi: 10.1016/0005-2795(80)90220-2
[17] LI Y Q, CHEN Z X, MO H Z. Effects of pulsed electric fields on physicochemical properties of soybean protein isolates[J]. LWT-Food Science and Technology,2007,40(7):1167−1175. doi: 10.1016/j.lwt.2006.08.015
[18] 王晓霞, 聂智华, 李松波, 等. 多光谱法与分子对接法研究盐酸四环素与牛血清白蛋白的相互作用[J]. 光谱学与光谱分析,2018,38(8):2468−2476. [WANG X X, NIE Z H, LI S B, et al. Study on the interaction between etracycline hydrochloride and bovine serum albumin by multispectral and molecular docking[J]. Spectroscopy and Spectral Analysis,2018,38(8):2468−2476. [19] LIU H, ZHANG Y, ZHANG J B, et al. Utilization of protein nanoparticles to improve the dispersibility, stability, and functionality of a natural pigment: Norbixin[J]. Food Hydrocolloids,2022,124:107329. doi: 10.1016/j.foodhyd.2021.107329
[20] DAI T T, CHEN J, LI Q, et al. Investigation the interaction between procyanidin dimer and alpha-amylase: Spectroscopic analyses and molecular docking simulation[J]. International Journal of Biological Macromolecules,2018,113:427−433. doi: 10.1016/j.ijbiomac.2018.01.189
[21] 吴云雪, 李娟, 高晴, 等. EGCG与乳清蛋白相互作用的光谱分析[J]. 食品研究与开发,2020,41(1):7−13. [WU Y X, LI J, GAO Q, et al. Spectral analysis of the interaction between EGCG and whey protein isolate[J]. Food Research and Development,2020,41(1):7−13. doi: 10.12161/j.issn.1005-6521.2020.01.002 [22] PESSATO T B, DE MORAIS F P R, DE CARVALHO N C, et al. Protein structure modification and allergenic properties of whey proteins upon interaction with tea and coffee phenolic compounds[J]. Journal of Functional Foods,2018,51:121−129. doi: 10.1016/j.jff.2018.10.019
[23] JOYE I J, DAVIDOV-PARDO G, LUDESCHER R D, et al. Fluorescence quenching study of resveratrol binding to zein and gliadin: Towards a more rational approach to resveratrol encapsulation using water-insoluble proteins[J]. Food Chemistry,2015,185:261−267. doi: 10.1016/j.foodchem.2015.03.128
[24] ZHU J X, LI K J, WU H, et al. Multi-spectroscopic, conformational, and computational atomic-level insights into the interaction of beta-lactoglobulin with apigenin at different pH levels[J]. Food Hydrocolloids,2020,105:105810. doi: 10.1016/j.foodhyd.2020.105810
[25] 张蕊, 吴超仪, 刘宇, 等. 分子对接和荧光光谱法研究麦角甾醇与牛血清白蛋白的相互作用[J]. 食品科学,2015,36(23):38−42. [ZHANG R, WU C Y, LIU Y, et al. Studies on the interaction of ergosterol with bovine serum albumin (BSA) by fluorescence spectroscopy and molecular docking[J]. Food Science,2015,36(23):38−42. doi: 10.7506/spkx1002-6630-201523008 [26] ROSS P D, SUBRAMANIAN S. Thermodynamics of protein association reactions: Forces contributing to stability[J]. Biochemistry,1981,20:3096−3102. doi: 10.1021/bi00514a017
[27] JIANG J, ZHANG Z P, ZHAO J, et al. The effect of non-covalent interaction of chlorogenic acid with whey protein and casein on physicochemical and radical-scavenging activity of in vitro protein digests[J]. Food Chemistry,2018,268:334−341. doi: 10.1016/j.foodchem.2018.06.015
[28] CAO Y Y, XIONG Y L. Interaction of whey proteins with phenolic derivatives under neutral and acidic ph conditions[J]. Journal of Food Science,2017,82(2):409−419. doi: 10.1111/1750-3841.13607
[29] FARRELL H M, WICKHAM E D, UNRUH J J, et al. Secondary structural studies of bovine caseins: Temperature dependence of beta-casein structure as analyzed by circular dichroism and FTIR spectroscopy and correlation with micellization[J]. Food Hydrocolloids,2001,15(4-6):341−354. doi: 10.1016/S0268-005X(01)00080-7
[30] GONG S X, YANG C Y, ZHANG J H, et al. Study on the interaction mechanism of purple potato anthocyanins with casein and whey protein[J]. Food Hydrocolloids,2021,111:106223. doi: 10.1016/j.foodhyd.2020.106223
[31] JAFARI S M, MCCLEMENTS D J. Nanotechnology approaches for increasing nutrient bioavailability[J]. Advances in Food and Nutrition Research,2017,81:1−30.
-
期刊类型引用(3)
1. 许雨晗,孔宇,杨本旭,王剑锋,武淑芬. 亚麻籽水溶蛋白与红曲黄色素相互作用及其对色素稳定性的影响. 食品科学技术学报. 2024(04): 86-100 .  百度学术
百度学术
2. 王菲,车思彤,赵晓. 乳化剂与乳清蛋白包埋壁材对透明质酸微胶囊溶解性的影响. 中国乳品工业. 2024(11): 38-44 .  百度学术
百度学术
3. 胡婷,韩嘉龙,耿勤,陈军,李俶,刘成梅,何雪梅,戴涛涛. 动物蛋白与植物蛋白对甜菜苷的热保护作用机制研究. 食品工业科技. 2023(07): 10-18 .  本站查看
本站查看
其他类型引用(1)










 下载:
下载:






 下载:
下载:



