Preparation and Antioxidant Activity Analysis of Hydrolyzed Peptides from Eucommia ulmoides Seed Meal
-
摘要: 以碱提酸沉得到的杜仲籽粕蛋白为原料,以水解度和总抗氧化能力(T-AOC)为指标,在单因素实验的基础上,以酶添加量、酶解时间和底物浓度为考察因素,采用Box-Behnken法进行三因素三水平响应面试验优化设计得出杜仲籽粕水解肽的制备最佳工艺参数,并对得到的杜仲籽粕水解肽进行体外抗氧化测定。结果表明,中性蛋白酶为最优蛋白酶,最佳酶解条件为酶添加量10000 U/g,酶解时间1.50 h,底物浓度20 g/L,在该条件下的水解度为47.45%±1.50%,T-AOC为30.62±0.59 µmol/g;最佳工艺下得到的杜仲籽粕水解肽,对DPPH自由基、超氧阴离子自由基以及ABTS自由基清除率的IC50值分别为0.731、4.258、0.407 mg/mL,表现出良好的抗氧化性,为杜仲籽粕高值化利用及抗氧化肽功能产品开发提供理论依据。Abstract: Eucommia ulmoides seed meal protein prepared by alkali extraction and acid precipitation was utilized as raw material. On the basis of single factor experiment, the total evaluation value of the hydrolysis degree and total antioxidant capacity (T-AOC) as response value was used to optimize the addition of enzyme, hydrolysis time and substrate concentration. And the Box-Behnken method was used for three factors and three levels response surface test design to determine the best enzymatic preparation process of hydrolyzed peptides from Eucommia ulmoides seed meal. The antioxidant activity of the obtained hydrolyzed peptides was determined in vitro. The results showed that neutral protease was the best protease, and the best enzymatic hydrolysis condition were enzyme was 10000 U/g, hydrolysis time 1.50 h and substrate concentration 20 g/L. Under these conditions, the degree of hydrolysis and T-AOC of hydrolyzed peptides were 47.45%±1.50% and 30.62±0.59 μmol/g, separately; the IC50 for DPPH free radical, superoxide anion radical and ABTS free radical scavenging rates were 0.731, 4.258 and 0.407 mg/mL, respectively. The Eucommia ulmoides seed meal peptides prepared under these conditions had great antioxidant capacity and provided a theoretical basis for the high-value utilization of Eucommia ulmoides seed meal and the development of antioxidant peptide functional products.
-
杜仲(Eucommia ulmoides Oliv)是我国特有的名贵滋补药材和珍稀树种[1-3],主要分布在陕西、甘肃、四川、河南等秦岭以南地区[4]。杜仲籽油作为新资源食品,含有多种功能性的营养成分[5],但其在生产时,大量籽粕遭到丢弃,不仅对环境造成污染,而且导致大量营养素和功能因子的流失。杜仲籽粕的蛋白含量高达35.98%,含有18种氨基酸,人体必需氨基酸含量占总氨基酸的32.3%,是一种新型的植物蛋白来源,但其高回收价值尚未得到重视[6-8]。
目前,绿豆多肽[9]、大豆多肽[10]、鹰嘴豆多肽[11]等植物源多肽因其具有较好的抗氧化性而备受关注,并且已有较多新型的抗氧化肽,如红花籽抗氧化肽[12]、菠萝蜜种子蛋白肽[13]、木薯叶片多肽[14]等被开发出来。黄群等[15]通过酶解制备的杜仲籽粕抗氧化肽对超氧阴离子自由基清除率最高可达56.6%;葛珍珍等[16]前期发现,杜仲籽粕蛋白经消化酶体外消化的产物对DPPH·、ABTS+·和·OH的清除率分别可达63.34%、58.16%、71.11%。因此,通过不同方法制备得到的杜仲籽粕水解肽的抗氧化能力有所不同,但是否能以不同的评判指标得到抗氧化性更强的水解肽还有待进一步探究。
综上,本文以杜仲籽粕为原料,通过响应面试验优化酶解制备杜仲籽粕水解肽的工艺条件,在此工艺基础上选取DPPH、超氧阴离子以及ABTS三种自由基的清除率对杜仲籽粕水解肽的体外抗氧化性进行研究,旨在为提高杜仲籽粕附加价值,杜仲籽粕蛋白的功能性开发及其水解肽在功能性产品中的应用提供理论基础。
1. 材料与方法
1.1 材料与仪器
杜仲籽粕 中国农业科学院郑州果树研究所;酸性蛋白酶(50 U/mg)、中性蛋白酶(100 U/mg)、碱性蛋白酶(200 U/mg)、1,1-二苯基-2-三硝基苯肼(DPPH)、总抗氧化能力(T-AOC)检测试剂盒 上海源叶生物科技有限公司;2,2’-联氮双(3-乙基苯并噻唑啉-6-磺酸)二铵盐(ABTS) Sigma公司;其余试剂均为分析纯。
PHS-3C型pH计 上海仪电科学仪器股份有限公司;HC-3618R型高速冷冻离心机 安徽中科中佳科学仪器有限公司;SPARK多模式酶标仪 奥地利Tecan有限公司;RE-52AA型旋转蒸发器 上海亚荣生化仪器厂;SHB-3型循环水多用真空泵 郑州杜普仪器厂。
1.2 实验方法
1.2.1 杜仲籽粕蛋白提取
按照葛珍珍等[16]的方法提取蛋白。称取杜仲籽粕20 g,按料液比1:15(杜仲籽粕质量(g)与水体积(mL)的比例)混合均匀,用1 mol/L NaOH溶液调pH至10,在40 ℃的水浴锅中浸提1.5 h,9000 r/min离心15 min,得上清用1 mol/L HCl溶液调pH至4.2,静置30 min,9000 r/min离心15 min后,将沉淀用少量的蒸馏水复溶,调其pH至中性,冷冻干燥得到杜仲籽粕蛋白粉(纯度为70.03%)。
1.2.2 蛋白酶的筛选
选择酸性蛋白酶、中性蛋白酶和碱性蛋白酶分别对杜仲籽粕蛋白进行初步水解[17-18]。水解条件为酶添加量6000 U/g、底物质量浓度30 g/L,在不同蛋白酶的最适酶解温度和pH条件下(表1),水解3 h,以总抗氧化能力和水解度为评价指标,综合筛选出具有抗氧化且水解度相对较高的蛋白酶,进行下一步实验。
表 1 不同蛋白酶酶解试验条件Table 1. Test conditions for enzymatic hydrolysis of different proteases蛋白酶 最适温度(℃) pH 底物质量浓度(g/L) 酶添加量(U/g) 酶解时间(h) 酸性蛋白酶 40 3.5 30 6000 3 中性蛋白酶 45 7.5 30 6000 3 碱性蛋白酶 40 10.5 30 6000 3 1.2.3 酶解单因素实验
选取中性蛋白酶为最适水解酶,在该酶的最适温度(45 ℃)和pH(7.5)下,设定其单因素水解的基本条件为:酶添加量为6000 U/g,酶解时间为2.5 h,底物浓度为40 g/L。改变其中一个条件,固定其他条件并分别考察酶添加量、酶解时间及底物浓度对总抗氧化能力和水解度的影响。各个因素水平梯度分别为:酶添加量2000、4000、6000、8000、10000 U/g;酶解时间1.5、2、2.5、3、3.5 h;底物浓度10、20、30、40、50 g/L。酶解结束后,沸水浴灭酶10 min,然后离心、取上清液,测定其总抗氧化能力和水解度,通过比较确定各因素酶解工艺最适的条件。
1.2.4 响应面试验设计
在单因素实验上,根据Box-Behnken试验设计原理,以总抗氧化能力和水解度的总评归一值(OD)为响应值,选取酶添加量、酶解时间、底物浓度作为响应因子,利用Design Expert软件进行三因素三水平的Box-Behnken试验设计,试验因素及水平见表2。
表 2 Box-Behnken 试验因素水平表Table 2. Factors and levels of Box-Behnken design因素 水平 −1 0 1 A酶添加量(U/g) 6000 8000 10000 B酶解时间(h) 1.5 2 2.5 C底物浓度(g/L) 20 30 40 1.2.5 总抗氧化能力(T-AOC)测定
用T-AOC检测试剂盒进行测定。将ABTS溶液和氧化剂等体积混合配制成ABTS工作液。临用前,用蒸馏水将ABTS工作液稀释至在405 nm处的吸光度为1.4±0.05。用蒸馏水将Trolox溶液(10 mmol/L)稀释至0.05、0.15、0.3、0.6、0.9、1、1.2、1.5 mmol/L。取200 µL ABTS工作液再分别加入5 µL的酶解液,混匀,室温放置6 min,测定405 nm下的吸光值,带入标准曲线方程(y=-1.1833x+1.5175,R2=0.994)算出样品的总抗氧化能力。
1.2.6 水解度测定
参考PENAS等[19]的邻苯二甲醛法,取400 µL酶解液与3 mL邻苯二甲醛法OPA试剂迅速混匀,避光反应2 min,以未水解样品做空白对照,测定340 nm处的吸光值,按照下式计算水解度(degree of hydrolysis,DH)。
DH(%)=1.8114×ΔA×dc×100 式中:∆A为水解样品的吸光度与未水解样品的吸光度的差值;d为稀释倍数;c为蛋白质质量浓度,g/L。
1.2.7 计算总评归一值OD
以总抗氧化能力和水解度为指标,采用Hassan法[20]处理归一化,单指标评价值(d)和总评归一值(OD)按照下列公式进行换算:
d=Yi−YminYmax−Ymin OD=d1+d22 式中:d表示单指标评价值,d1表示总抗氧化能力指标评价值,d2表示水解度指标评价值,Yi表示指标中第i个值,Ymin表示指标中最小值,Ymax表示指标中最大值。
1.2.8 杜仲籽粕水解肽的体外抗氧化试验
1.2.8.1 DPPH自由基清除率测定
参考YANG等[21]的方法,并进行一定的调整。将杜仲籽粕水解物配成质量浓度分别为0.02、0.04、0.08、0.2、0.4、0.8、2、4、6、8 mg/mL的溶液。在试管中依次加入150 μL上述浓度的酶解液及150 μL的DPPH乙醇溶液(0.6 mmol/L),振荡混匀后,在室温条件下避光静置30 min,测定517 nm处的吸光值。
DPPH自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为加样品与DPPH乙醇溶液时的吸光度;A2为加样品与无水乙醇时的吸光度;A0为无水乙醇与DPPH乙醇溶液时的吸光度。
1.2.8.2 超氧阴离子自由基清除率测定
参考杨永涛[22]的方法,并进行一定的调整。配制质量浓度分别为0.2、0.4、0.8、2、4、6、8 mg/mL的样品溶液。在试管中加入4.5 mL Tris-HCl缓冲溶液(pH为8.2,浓度为0.05 mol/L),2.5 mL的蒸馏水,30 ℃水浴20 min。然后加入1.5 mL不同浓度样品溶液,以及0.5 mL的邻苯三酚溶液(25 mmol/L),快速摇匀,于30 ℃水浴反应8 min后,立即滴加0.1 mL的HCl(8 mmol/L)终止反应,测定320 nm处的吸光值。
超氧阴离子自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为加样品时的吸光度;A2为用蒸馏水代替邻苯三酚溶液时的吸光度;A0为用蒸馏水代替样品时的吸光度。
1.2.8.3 ABTS自由基清除率的测定
参考ZILIC等[23]的方法,并进行一定的调整。配制质量浓度分别为0.02、0.04、0.08、0.2、0.4、0.8、2、4、6、8 mg/mL的样品溶液。将ABTS溶液(7 mmol/L)和过硫酸钾溶液(2.45 mmol/L)按照 1:1 体积比混合均匀,避光放置12 h。取上述混合液,用无水乙醇调其吸光度在734 nm处为0.70±0.02,即得ABTS工作液。取0.4 mL样品溶液,加入ABTS工作液4.0 mL,静置反应5 min后,测定734 nm处的吸光度。
ABTS自由基清除率(%)=(1−A1−A2A0)×100 式中:A1为加样品时的吸光度;A2为用蒸馏水代替ABTS工作液时的吸光度;A0为用蒸馏水代替样品时的吸光度。
1.3 数据处理
所有试验均进行3组平行实验,数据采用平均值±标准差的形式表示,采用SPSS22.0和Origin Expert8.0.6软件对数据进行分析处理。显著性差异用单因素方差分析法(one-way ANOVA)进行表示(P<0.05)。
2. 结果与分析
2.1 蛋白酶的筛选
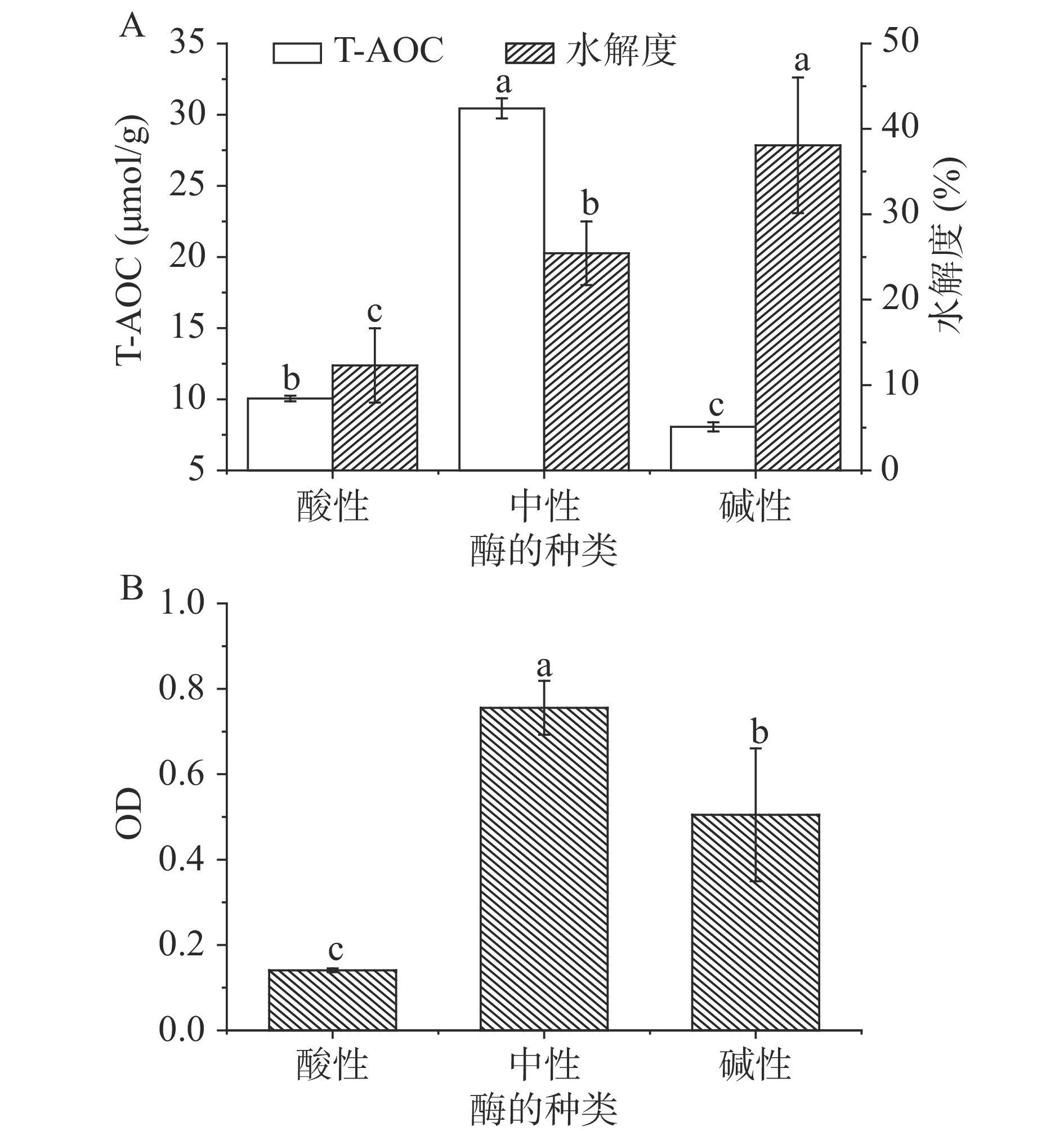
由图1可知,中性蛋白酶酶解液的总抗氧化能力最高,其次是酸性蛋白酶、碱性蛋白酶;而碱性蛋白酶对杜仲籽粕蛋白的水解度最高,其次是中性蛋白酶、酸性蛋白酶。不同的蛋白酶具有特定的酶切位点,从而得到不同肽链组成的酶解产物,所以其生物活性也存在较大差异[24]。本研究中,中性蛋白酶处理后的OD值最大,综合考虑酶解液的水解度和抗氧化活性,本实验选择中性蛋白酶为最适作用酶。
2.2 单因素实验结果
2.2.1 酶添加量的影响
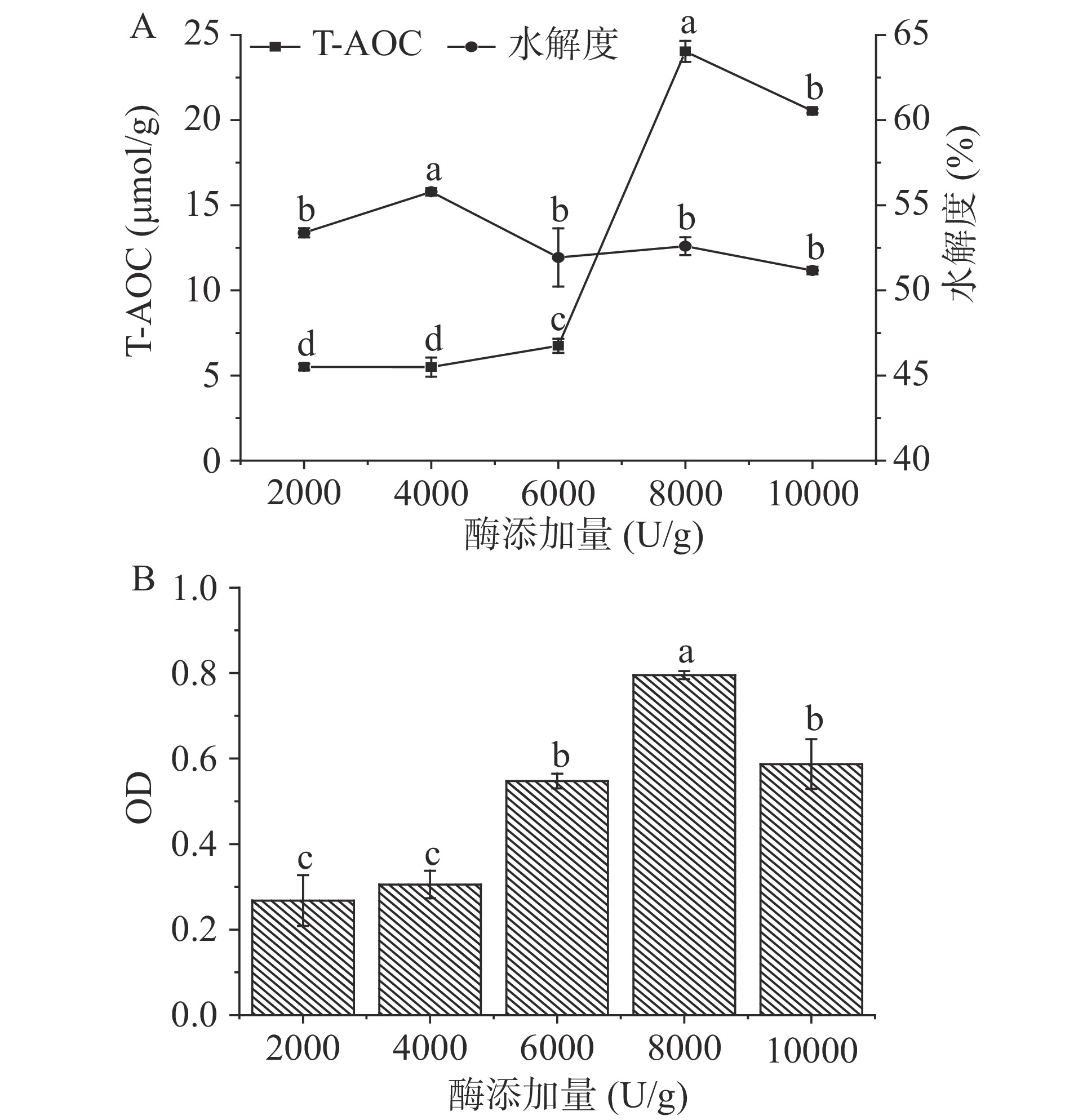
由图2可知,在测量范围内,酶解液的总抗氧化能力呈现先增大后减少的趋势。当酶添加量为8000 U/g时,总抗氧化能力达到24.03 µmol/g,达到最大值;而当酶添加量为4000 U/g时,水解度达到最大值,为55.7%。这可能是由于随着酶量的增加,酶和底物达到饱和,其水解度达到最大值,随着酶量继续增加,过多的酶将抗氧化能力较低的肽段进一步水解,从而得到抗氧化性较好的多肽[25]。综合两者得到的OD值,与总抗氧化能力呈现相同的趋势。因此,确定酶添加量为8000 U/g。
2.2.2 酶解时间的影响
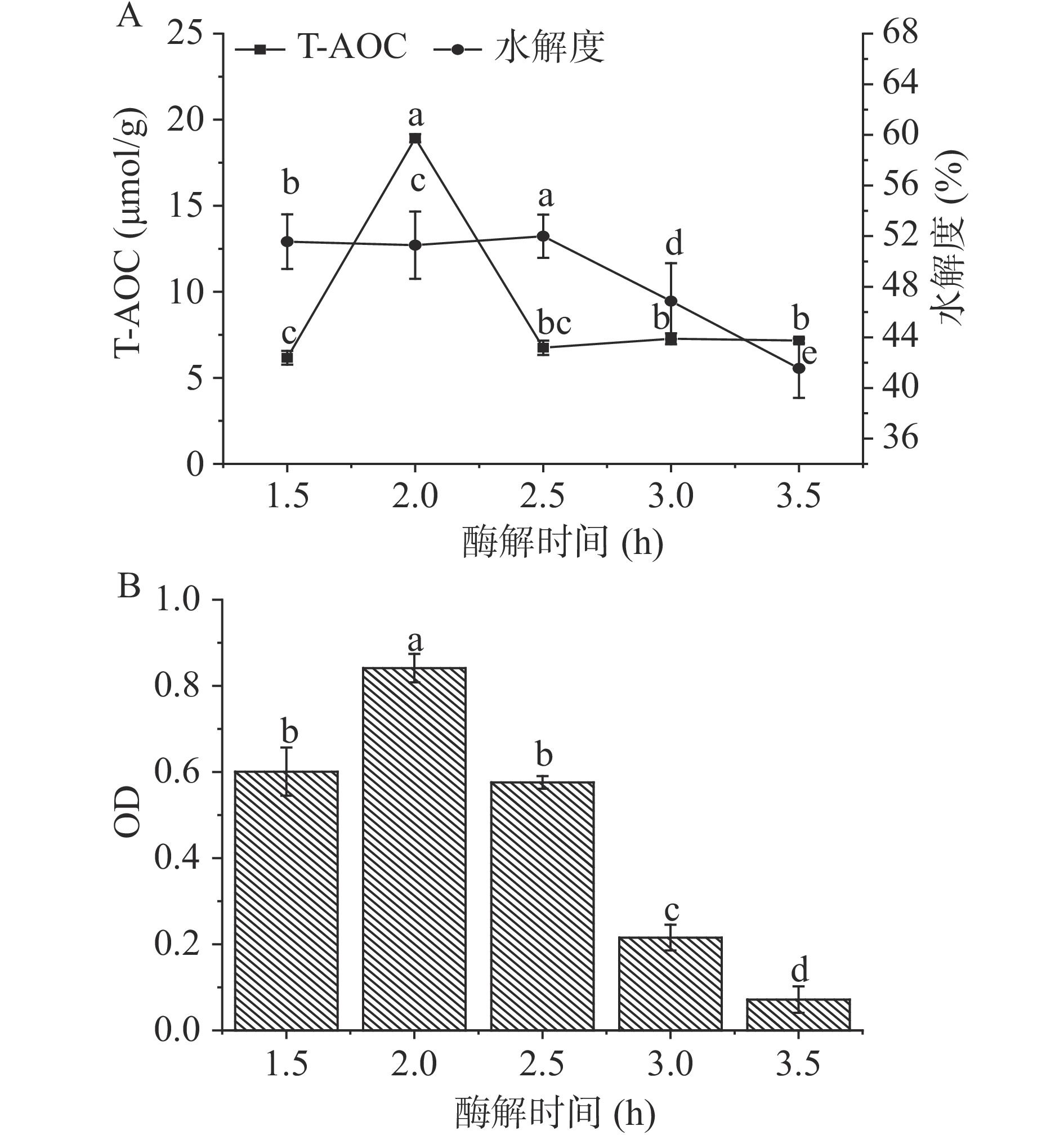
由图3可知,在酶解时间为1.5~3.5 h内,酶解液的水解度和总抗氧化能力均呈现先增大后降低的趋势。当酶解时间为2 h时,总抗氧化能力达到最大值18.92 µmol/g,继续增加酶解时间,底物逐渐被转化而导致酶解速率下降,生成的活性肽被进一步水解,从而导致酶解液的总抗氧化能力降低[26]。酶解时间为2.5 h时,其水解度达到最大值52%。综合考虑酶解液的总抗氧化能力和水解度的大小,确定酶解时间为2 h。
2.2.3 底物浓度的影响
由图4可知,随着底物浓度的增加,总抗氧化能力和水解度均先增加后降低,其中底物浓度20 g/L时,总抗氧化能力为29.3 µmol/g,达到最大值,水解度为36.4%。在底物浓度为30 g/L时其水解度为53.4%,相较前者有所增加,之后逐渐降低。这是因为在底物浓度较低时,随着底物浓度的增加,酶和底物结合速率也随之增加,当酶和底物达到饱和后,继续增加底物浓度,会对酶与底物的反应起到抑制作用[27-28]。而总抗氧化能力先增加后降低,这是因为随着水解度的增加使多肽暴露出更多的活性基团,但过高的水解度会破坏活性肽的结构,从而使总抗氧化性降低[29]。综合考虑酶解液的总抗氧化能力和水解度的大小,确定底物浓度为20 g/L。
2.3 响应面试验结果
2.3.1 中心组合试验结果
根据前述实验设计方案,选择酶添加量(A)、酶解时间(B)、底物浓度(C)三个因素为考察指标,以总抗氧化能力和水解度的总评归一值(OD)为响应值,利用Origin-Expert8.0.6软件对响应结果进行多元回归拟合,建立的二次响应面回归方程如下:OD=0.33+0.10A+0.041B−0.20C−0.10AB−0.028AC+0.078BC+0.085A2+0.10B2−0.054C2。
从实验结果(表3)和方差分析(表4)可以看出,模型极显著(P=0.0026<0.01),说明模型较为稳定,失拟项不显著(P=0.1509>0.05),说明方程拟合性良好,即回归方程模型有显著意义。决定系数R2为0.9312,即响应值的变化有93.12%与所选变量有关系,说明模型拟合程度良好,能够较准确地预测和分析实际情况[29];模型的校正决定系数R2Adj为0.8427,说明不确定因素对实验结果的干扰较小,该模型与数据拟合度良好,即回归方程模型适合杜仲籽粕多肽制备工艺的分析与预测[30]。模型的一次项A、C极显著(P<0.01),交互项AB、二次项B2差异显著(P<0.05)。对比各因素的F值大小可知,在三个因素中,按照对结果的影响排序,底物浓度(C)>酶添加量(A)>酶解时间(B)。
表 3 响应面设计及结果Table 3. Response surface design and results试验号 因素 T-AOC
(μmol/g)水解度
(%)OD A B C 1 0 0 0 26.5524 16.394 0.25721 2 −1 0 1 23.344 17.891 0.151687 3 0 −1 −1 28.9329 24.815 0.608634 4 −1 −1 0 24.9944 18.233 0.237842 5 −1 1 0 29.2255 20.129 0.487889 6 1 0 −1 31.8009 20.878 0.628496 7 1 −1 0 26.6493 33.842 0.761695 8 1 0 1 24.4468 18.509 0.183023 9 0 0 0 26.2303 19.072 0.319039 10 0 0 0 25.8923 20.511 0.344658 11 1 1 0 29.4565 23.638 0.599129 12 0 1 1 24.1479 21.984 0.31026 13 0 −1 1 20.9921 17.013 0.033119 14 0 1 −1 29.9903 21.445 0.57513 15 0 0 0 27.212 17.170 0.321057 16 −1 0 −1 27.7603 22.428 0.486 17 0 0 0 26.4726 22.242 0.415272 表 4 回归方程模型的显著性检验及方差分析Table 4. Explicitness test and variance analysis of regression equation model方差来源 平方和 自由度 均方和 F值 P值 显著性 模型 0.58 9 0.065 10.52 0.0026 ** A-酶添加量 0.082 1 0.082 13.29 0.0082 ** B-酶解时间 0.014 1 0.014 2.23 0.1792 C-底物浓度 0.33 1 0.33 53.32 0.0002 ** AB 0.043 1 0.043 6.92 0.0339 * AC 3.089E-003 1 3.089E-003 0.50 0.5015 BC 0.024 1 0.024 3.92 0.0882 A2 0.031 1 0.031 4.98 0.0607 B2 0.046 1 0.046 7.52 0.0288 * C2 0.013 1 0.013 2.03 0.1970 残差 0.043 7 6.154E-003 失拟项 0.030 3 0.010 3.09 0.1519 不显著 纯误差 0.013 4 3.244E-003 总误差 0.63 16 R2=0.9312 R2Adj=0.8427 注:*为显著(P<0.05);**为极显著(P<0.01)。 2.3.2 响应面模型验证
通过对响应面优化工艺结果拟合分析得出:中性蛋白酶酶解杜仲籽粕蛋白制备抗氧化肽的最佳工艺条件为酶添加量9999.98 U/g,酶解时间1.50 h,底物浓度20 g/L,在最佳工艺条件下,杜仲籽粕抗氧化肽的OD值为0.938。
结合实际情况将上述所得最佳条件修正为:酶添加量10000 U/g,酶解时间1.50 h,底物浓度20 g/L,在此条件下进3组验证试验,测得杜仲籽粕蛋白酶解液的总抗氧化能力为(30.62±0.59 µmol/g),水解度为47.45%±1.50%,OD值为0.932,与响应面回归模型所得到的预测值(0.938)偏差0.397%,说明这次响应面分析的回归模型可以很好地预测实际试验结果。
2.4 杜仲籽粕水解肽的体外抗氧化试验
不同质量浓度的酶解液和VC对DPPH自由基、超氧阴离子自由基以及ABTS自由基的清除率测定结果如图5所示。在测量的质量浓度范围内,酶解液和VC对自由基的清除能力均随着质量浓度的增大而逐渐增大,呈现出一定的剂量依赖性。当水解肽的浓度为0.8 mg/mL时,对DPPH自由基、超氧阴离子自由基以及ABTS自由基的清除率分别为57.4%、16.7%、75.2%;浓度为8 mg/mL时,对自由基的清除率分别为78.6%、75.4%、96.1%,而当VC的浓度为0.8 mg/mL时,对DPPH自由基、超氧阴离子自由基以及ABTS自由基的清除率分别为91.5%、94.4%、99.5%,由此可看出,杜仲籽粕水解肽对DPPH自由基、超氧阴离子自由基以及ABTS自由基的清除能力在低浓度时不如VC,但高浓度时与VC相当。本研究以水解度和总抗氧化能力为指标,在响应面优化的最佳工艺条件下制备出来的多肽,对超氧阴离子自由基的清除率可高达75.4%,且该最佳条件所需的底物质量浓度、酶添加量和酶解时间与黄群等[15]制备抗氧化肽条件相比(底物质量浓度为7.32 g/100 mL、酶用量为12292.3 U/g、酶解时间为2.59 h)更少,即此次优化得到的杜仲籽粕水解肽具有更强的抗氧化能力。
采用SPSS22.0软件进行回归拟合,计算得水解肽对DPPH自由基、超氧阴离子自由基以及ABTS自由基清除率的IC50分别为0.731、4.258、0.407 mg/mL。当某物质的IC50低于10 mg/mL时,一般说明其有较好的抗氧化活性[31],杜仲籽粕水解肽对三种自由基清除率的IC50均远小于10 mg/mL,综上,杜仲籽粕蛋白水解肽具有明显的抗氧化性。
3. 结论
本实验以杜仲籽粕为原料,通过碱提酸沉得到杜仲籽粕蛋白,利用酶解法制备多肽,通过单因素实验及响应面试验对酶添加量、酶解时间和底物浓度这三个因子进行优化,得到最佳工艺条件:酶添加量10000 U/g,酶解时间1.50 h,底物浓度20 g/L,在此条件下,酶解液的水解度为47.45%±1.50%,总抗氧化能力为(30.62±0.59 µmol/g),且随着杜仲籽粕蛋白酶解液浓度的增大,其清除DPPH自由基、超氧阴离子自由基以及ABTS自由基的能力也不断增大,表明杜仲籽粕多肽具有良好的抗氧化功能。本文仅对酶解杜仲籽粕蛋白制备多肽工艺条件及其抗氧化性进行了研究,但其抗氧化能力与结构特征间的关联性仍有待进一步探究。
-
表 1 不同蛋白酶酶解试验条件
Table 1 Test conditions for enzymatic hydrolysis of different proteases
蛋白酶 最适温度(℃) pH 底物质量浓度(g/L) 酶添加量(U/g) 酶解时间(h) 酸性蛋白酶 40 3.5 30 6000 3 中性蛋白酶 45 7.5 30 6000 3 碱性蛋白酶 40 10.5 30 6000 3 表 2 Box-Behnken 试验因素水平表
Table 2 Factors and levels of Box-Behnken design
因素 水平 −1 0 1 A酶添加量(U/g) 6000 8000 10000 B酶解时间(h) 1.5 2 2.5 C底物浓度(g/L) 20 30 40 表 3 响应面设计及结果
Table 3 Response surface design and results
试验号 因素 T-AOC
(μmol/g)水解度
(%)OD A B C 1 0 0 0 26.5524 16.394 0.25721 2 −1 0 1 23.344 17.891 0.151687 3 0 −1 −1 28.9329 24.815 0.608634 4 −1 −1 0 24.9944 18.233 0.237842 5 −1 1 0 29.2255 20.129 0.487889 6 1 0 −1 31.8009 20.878 0.628496 7 1 −1 0 26.6493 33.842 0.761695 8 1 0 1 24.4468 18.509 0.183023 9 0 0 0 26.2303 19.072 0.319039 10 0 0 0 25.8923 20.511 0.344658 11 1 1 0 29.4565 23.638 0.599129 12 0 1 1 24.1479 21.984 0.31026 13 0 −1 1 20.9921 17.013 0.033119 14 0 1 −1 29.9903 21.445 0.57513 15 0 0 0 27.212 17.170 0.321057 16 −1 0 −1 27.7603 22.428 0.486 17 0 0 0 26.4726 22.242 0.415272 表 4 回归方程模型的显著性检验及方差分析
Table 4 Explicitness test and variance analysis of regression equation model
方差来源 平方和 自由度 均方和 F值 P值 显著性 模型 0.58 9 0.065 10.52 0.0026 ** A-酶添加量 0.082 1 0.082 13.29 0.0082 ** B-酶解时间 0.014 1 0.014 2.23 0.1792 C-底物浓度 0.33 1 0.33 53.32 0.0002 ** AB 0.043 1 0.043 6.92 0.0339 * AC 3.089E-003 1 3.089E-003 0.50 0.5015 BC 0.024 1 0.024 3.92 0.0882 A2 0.031 1 0.031 4.98 0.0607 B2 0.046 1 0.046 7.52 0.0288 * C2 0.013 1 0.013 2.03 0.1970 残差 0.043 7 6.154E-003 失拟项 0.030 3 0.010 3.09 0.1519 不显著 纯误差 0.013 4 3.244E-003 总误差 0.63 16 R2=0.9312 R2Adj=0.8427 注:*为显著(P<0.05);**为极显著(P<0.01)。 -
[1] 高宏伟, 李玉萍, 李守超. 杜仲的化学成分及药理作用研究进展[J]. 中医药信息,2021,38(6):73−81. [GAO H W, LI Y P, LI S C. Study advances in chemical constituents and pharmacological effects of Eucommia ulmoides oliv[J]. Information on Traditional Chinese Medicine,2021,38(6):73−81. doi: 10.19656/j.cnki.1002-2406.210615 [2] 冯晗, 周宏灏, 欧阳冬生. 杜仲的化学成分及药理作用研究进展[J]. 中国临床药理学与治疗学,2015,20(6):713−720. [FENG H, ZHOU H Y, OUYANG D S. Research progress on chemical constituents and pharmacological effects of Eucommia ulmoides[J]. Chinese Journal of Clinical Pharmacology and Therapeutics,2015,20(6):713−720. [3] ZHU M Q, SUN R C. Eucommia ulmoides oliver: A potential feedstock for bioactive products[J]. Journal of Agricultural and Food Chemistry,2018,66(22):5433−5438. doi: 10.1021/acs.jafc.8b01312
[4] 汤诗杰, 李和平, 贺善安. 杜仲研究的现状与展望[J]. 林业科技开发,2007(2):8−12. [TANG S J, LI H P, HE S A. Present situation and prospect of Eucommia ulmoides research[J]. Journal of Forestry Engineering,2007(2):8−12. doi: 10.3969/j.issn.1000-8101.2007.02.003 [5] 武毅楠, 高梦珂, 李攀峰, 等. 杜仲籽油对2型糖尿病KKAy小鼠糖脂代谢及肠道菌群的影响[J]. 食品安全质量检测学报,2022,13(3):728−736. [WU Y N, GAO M K, LI P F, et al. Effect of Eucommia ulmoides seed oil on glycolipid metabolism and gut microbiota in KKAY mice with type 2 diabetes mellitus[J]. Journal of Food Safety & Quality,2022,13(3):728−736. doi: 10.19812/j.cnki.jfsq11-5956/ts.2022.03.004 [6] 朱莉伟, 陈素文, 蒋建新, 等. 杜仲种仁化学成分研究[J]. 中国野生植物资源,2005(2):41−42, 45. [ZHU L W, CHEN S W, JIANG J X, et al. Study on chemical constituents of Eucommia kernel[J]. Chinese Wild Plant Resources,2005(2):41−42, 45. doi: 10.3969/j.issn.1006-9690.2005.02.015 [7] 吴凡, 蒲灵操, 单旺, 等. 碱性蛋白酶提取杜仲籽粕蛋白的工艺优化[J]. 粮食科技与经济,2013,38(6):54−57. [WU F, PU L C, DAN W, et al. Optimization of alkaline protease for protein extraction from Eucommia seed meal[J]. Grain Science and Technology and Economy,2013,38(6):54−57. doi: 10.3969/j.issn.1007-1458.2013.06.020 [8] 黄诚, 尹红. 基于超声波辅助法的杜仲籽蛋白提取工艺优化[J]. 吉首大学学报(自然科学版),2014,35(1):78−82. [HUANG C, YIN H. Optimization of extraction technology of Eucommia seed protein based on ultrasonic assisted method[J]. Journal of Jishou University (Natural Sciences Edition),2014,35(1):78−82. [9] XIA J, SONG H, HUANG K, et al. Purification and characterization of antioxidant peptides from enzymatic hydrolysate of mungbean protein[J]. Journal of Food Science,2020,85(6):1735−1741. doi: 10.1111/1750-3841.15139
[10] RAYAPROLU S, HETTIARACHCHY N, HORAX R, et al. Amino acid profiles of 44 soybean lines and ACE-I inhibitory activities of peptide fractions from selected lines[J]. Journal of the American Oil Chemists Society,2015,92(7):1−11.
[11] 周丽卿. 鹰嘴豆多肽的制备及其改性研究[D]. 杨凌: 西北农林科技大学, 2012 ZHOU L Q. Study on the preparation and modification of chickpea peptide[D]. Yangling: Northwest A&F University, 2012.
[12] 刘晓艺, 周玉岩, 过利敏, 等. 不同分子量红花籽抗氧化肽稳定性研究[J/OL]. 食品工业科技: 1−14 [2022-01-11] LIU X Y, ZHOU Y Y, GUO L M, et al. Study on the stability of antioxidant peptides from safflower seeds with different molecular weights[J/OL]. Science and Technology of Food Industry: 1−14 [2022-01-11].
[13] CHAI T T, XIAO J, MOHANA DASS S, et al. Identification of antioxidant peptides derived from tropical jackfruit seed and investigation of the stability profiles[J]. Food Chemistry,2021,340:127876. doi: 10.1016/j.foodchem.2020.127876
[14] 张作达, 王琴飞, 吴若娜, 等. 木薯叶片多肽的制备与抗氧化功能研究[J/OL]. 食品与发酵工业: 1−12 [2022-01-13] ZHANG Z D, WANG Q F, WU N N, et al. Study on preparation and antioxidant function of polypeptides from cassava leaf[J/OL]. Food and Fermentation Industries: 1−12 [2022-01-13].
[15] 黄群, 杨万根, 余佶, 等. 杜仲籽粕蛋白酶解制备抗氧化肽工艺优化[J]. 食品科学,2013,34(17):205−209. [HUANG Q, YANG W G, YU J, et al. Process optimization for antioxidant peptide preparation from Eucommia seed meal protein by enzymatic hydrolysis[J]. Food Science,2013,34(17):205−209. doi: 10.7506/spkx1002-6630-201317044 [16] 葛珍珍, 王维静, 张圆圆, 等. 杜仲籽粕蛋白的分离提取及其体外消化产物的抗氧化特性研究[J]. 食品科技,2021,46(4):202−207. [GE Z Z, WANG W J, ZHANG Y Y, et al. Extraction of Eucommia ulmoides seed protein and antioxidant properties of its digested products in vitro[J]. Food Science and Technology,2021,46(4):202−207. doi: 10.13684/j.cnki.spkj.2021.04.031 [17] 贺东亮. 紫苏多肽分离纯化及其抗肿瘤活性研究[D]. 太原: 中北大学, 2019 HE D L. Study on purification and anti-cancer effects of peptides derived from perilla frutescens[D]. Taiyuan: North University of China, 2019.
[18] 郑德勇, 陈成聪, 颜阳蕾, 等. 茶树籽蛋白质微波辅助酶解制备多肽的研究[J]. 中国粮油学报,2020,35(12):135−140, 155. [ZHENG D Y, CHEN C C, YAN Y L, et al. The polypeptides preparation from Camellia sinensis seeds protein by microwave-assisted enzymolysis[J]. Journal of the Chinese Cereals and Oils Association,2020,35(12):135−140, 155. doi: 10.3969/j.issn.1003-0174.2020.12.022 [19] PENAS E, PRSTAMO G, GOMEZ R. High pressure and the enzymatic hydrolysis of soybean whey proteins[J]. Food Chemistry,2004,85(4):641−648. doi: 10.1016/j.foodchem.2003.07.025
[20] LI J C, WANG R, SHENG Z L, et al. Optimization of baicalin, wogonoside, and chlorogenic acid water extraction process from the roots of Scutellariae Radix and Lonicerae japonicae flos using response surface methodology (RSM)[J]. Processes,2019,7(11):854. doi: 10.3390/pr7110854
[21] YANG R W, LI X F, LIN S Y, et al. Identification of novel peptides from 3 to 10 kDa pine nut (Pinus koraiensis) meal protein, with an exploration of the relationship between their antioxidant activities and secondary structure[J]. Food Chemistry,2017,219:311−320. doi: 10.1016/j.foodchem.2016.09.163
[22] 杨永涛. 罗布麻总黄酮的提取、分离纯化及其抗氧化性能研究[D]. 广州: 华南理工大学, 2018 YANG Y T. Study on extraction, purification and antioxidant activity of total flavonoids from Apocynum venetum[D]. Guangzhou: South China University of Technology, 2018.
[23] ZILIC S, SERPEN A, AKILLIOGLU G, et al. Phenolic compounds, carotenoids, anthocyanins, and antioxidant capacity of colored maize (Zea mays L.) kernels[J]. Journal of Agricultural and Food Chemistry,2012,60(5):1224−1231. doi: 10.1021/jf204367z
[24] XU Z, MAO T M, HUANG L, et al. Purification and identification immunomodulatory peptide from rice protein hydrolysates[J]. Food and Agricultural Immlmology,2019,30(1):150−162. doi: 10.1080/09540105.2018.1553938
[25] 岳阳. 大米抗氧化肽的制备及其抗衰老功能研究[D]. 杭州: 浙江大学, 2021 YUE Y. Preparation of rice antioxidant peptides and its anti-aging effects[D]. Hangzhou: Zhejiang University, 2021.
[26] 郎蒙, 李燕, 蒋蔚薇, 等. 响应面优化南极磷虾粉肽制备工艺及α-葡萄糖苷酶抑制活性分析[J/OL]. 上海海洋大学学报: 1−13 [2021-11-24]. http://kns.cnki.net/kcms/detail/31.2024.S.20210601.1631.006.html. LANG M, LI Y, JIANG W W, et al. Optimization of preparation process and α-glucosidase inhibitory activity of Antarctic krill powder peptide by response surface methodology[J/OL]. Journal of Shanghai Ocean University: 1−13 [2021-11-24]. http://kns.cnki.net/kcms/detail/31.2024.S.20210601.1631.006.html.
[27] 乔晓林. 酶解小麦面筋蛋白制备抗氧化肽工艺优化[D]. 西安: 陕西科技大学, 2014 QIAO X L. Preparation of antioxidant peptides and optimization of enzymatic hydrolysis of wheat gluten[D]. Xi'an: Shaanxi University of Science & Technology, 2014.
[28] FANG X B, XIE N N, CHEN X E, et al. Optimization of antioxidant hydrolysate production from flying squid muscle protein using response surface methodology[J]. Food and Bioproducts Processing,2012,90(4):676−682. doi: 10.1016/j.fbp.2012.04.001
[29] 郭瑶. 罗非鱼皮胶原肽的制备及其抗氧化活性的研究[D]. 青岛: 中国海洋大学, 2006 GUO Y. Preparation of peptides from enzymic hydrolysates of tilapia skin collagen and its antioxidant properties[D]. Qingdao: Ocean University of China, 2006.
[30] SONG R, LIANG T, SHEN Q, et al. The optimization of production and characterization of antioxidant peptides from protein hydrolysates of Agrocybe aegerita[J]. LWT,2020,134:109987. doi: 10.1016/j.lwt.2020.109987
[31] 郑义, 邵颖, 陈安徽, 等. 益智仁总黄酮超声辅助提取工艺优化及其抗氧化活性[J]. 食品科学,2014,35(6):44−49. [ZHENG Y, SHAO Y, CHEN A H, et al. Optimization of ultrasonic-assisted extraction and antioxidant activities of total flavonoids from Alpinia oxyphylla fruits[J]. Food Science,2014,35(6):44−49. doi: 10.7506/spkx1002-6630-201406009 -
期刊类型引用(6)
1. 毕冉冉,赵圆,孙玉敬. 枸杞植物化学成分调节肠道菌群及相关生理功能的研究进展. 浙江大学学报(农业与生命科学版). 2024(01): 25-34 .  百度学术
百度学术
2. 余钟莲,王瑞,杨莉,王峥涛,石燕红. 基于熵权法和灰色关联度法评价枸杞子质量. 中成药. 2024(03): 919-926 .  百度学术
百度学术
3. 余钟莲,李薛萍,杨莉,王峥涛,刘文静,王瑞,石燕红. 宁夏道地药材枸杞子等级质量标准研究. 药学学报. 2024(05): 1399-1407 .  百度学术
百度学术
4. 黎俊威,苏君梅,胡杰,杨静,陈汉峰,刘春丽. 超高效液相色谱法测定食品中枸杞酸含量. 食品安全质量检测学报. 2024(24): 57-62 .  百度学术
百度学术
5. 夏梦琴,刘怡萍,王瑞,杨莉,王峥涛,石燕红. 枸杞子中玉米黄素双棕榈酸酯的定性与定量分析. 上海中医药杂志. 2022(05): 87-92 .  百度学术
百度学术
6. 周凌,朱吟吟,郁静华,廖勇诚,石欢,续斐,FRIES Lennart. 高效液相色谱法测定枸杞相关食品中枸杞酸和玉米黄质二棕榈酸酯的含量. 食品安全质量检测学报. 2021(20): 8141-8149 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:








 下载:
下载:



