Effects of Henna Extract Composite Gelatin Film on the Quality of Beef during Cold Chain Transport and Placement
-
摘要: 本研究调查了以墨鱼皮明胶和散沫花提取物(HAE)作为天然保鲜剂制备出的功能性涂膜对模仿冷链运输及零售1、3、6和8 d牛肉贮藏损失、颜色、菌落总数、脂质氧化以及高铁血红蛋白、血红素铁和游离氨基酸含量的影响,综合评价了散沫花提取物复合明胶膜对牛肉冷藏保鲜效果的的影响。结果表明,与未涂膜样品相比,涂膜处理有效防止了水分的流失和高铁肌红蛋白的形成,保持了肉样的持水性和颜色特性(P<0.05)。随着放置期的延长,HAE+明胶膜通过在贮藏期减少脂质氧化程度、菌落总数和嗜冷菌数,显著延长了肉的货架期(P<0.05)。此外,根据游离氨基酸含量,涂膜处理可以显著降低蛋白水解过程的速率,而未涂膜处理的样品水解速率更快(P<0.05)。主成分分析表明,样品颜色的变化与pH、血红素铁含量、脂质氧化以及微生物繁殖存在高度相关性,而HAE+明胶涂膜良好地抑制了这些因素的发展。因此,HAE+明胶涂膜可以作为有效的活性保鲜方式,用于肉类的冷藏保鲜。Abstract: In this study, the effects of functional coated films prepared with cuttlefish skin gelatine and henna extract (HAE) as natural preservation agents on the storage loss, colour, colony count, lipid oxidation and the content of haemoglobin, haemoglobin iron and free amino acids in beef mimicking cold chain transportation and retailing for 1, 3, 6 and 8 days were investigated, and the effect of scattered flowers extract composite gelatine films on beef cold storage preservation was comprehensively evaluated. The results showed that the coating treatment effectively prevented water loss and the formation of high iron myoglobin and maintained the water-holding and colour characteristics of the meat samples compared to the uncoated samples (P<0.05). As storage time increased, the HAE+gelatin film significantly extended the shelf life of the meat by reducing the degree of lipid oxidation, the total number of colonies and the number of cold-loving bacteria during storage (P<0.05). Furthermore, depending on the content of free amino acids, the coating treatment significantly reduced the rate of the protein hydrolysis process, while the uncoated samples were hydrolysed faster (P<0.05). Principal component analysis (PCA) showed a high correlation between changes in sample colour and pH, haemoglobin iron content, the occurrence of lipid oxidation and microbial reproduction, which were well inhibited by the HAE+gelatin coating. Therefore, HAE+gelatin coated films can be used as an effective active preservation method for the refrigerated fresh meat.
-
Keywords:
- henna extract /
- gelatin film /
- beef /
- lipid oxidation /
- microorganism /
- PCA
-
随着我国居民生活水平的提高,肉类生产和消费水平迅速增长,鲜肉已占包括超市在内,市场上未经加工的肉类需求量的70%以上[1]。目前,市场上鲜肉大多只是简单的保鲜膜包封或没有任何包装直接置于低温冷藏柜中。因此,相比于冷冻肉及各类肉制品,鲜肉冷藏期的稳定性极易受到当下环境的影响,导致货架期短、品质下降、甚至造成一系列安全隐患[2]。有文献指出,肉类质量下降和劣变的主要原因是由细菌引起的食品腐败、高铁肌红蛋白形成、血红素铁转化引起的色泽下降以及脂质氧化引起的风味劣变[3]。因此,控制鲜肉冷藏过程中的品质至关重要。
活性涂膜技术目前已被证明是保持食品质量的重要工具之一[2]。其中明胶作为可食用涂层的主要成分,具有较好的成膜能力和在肉类冷藏过程中防止水分流失和脂质氧化的作用[4]。然而,单一的明胶膜目前已显然无法满足肉类实际应用的要求。与其他物质结合制成的复合型明胶膜扩大了食物保鲜的应用范围。Nowzari等[5]采用壳聚糖复合明胶膜对三文鱼冷藏期间的品质变化进行了研究,发现贮藏16 d未进行任何处理的样品中,挥发性盐基氮含量(TVB-N)已接近临界值25 mg/100 g,而壳聚糖复合明胶膜组的TVB-N含量只在20 mg/100 g左右,说明壳聚糖复合明胶膜可以显著维持三文鱼的品质并延长货架期。李媛等[4]制备了含有不同质量浓度的迷迭香酸(RosA)的兔皮明胶膜对新鲜猪肉进行包装,发现使用RosA明胶膜包装可有效抑制猪肉在冷藏过程中挥发性盐基氮含量、菌落总数和pH的上升,并对脂肪氧化有一定抑制作用。然而,目前对于明胶膜的研究主要集中在其提取、性质测定以及明胶膜的制备。对于优质活性明胶膜领域的研究仍存在不足,涂膜中添加的活性物质通过释放活性剂延长产品最终的品质和保质期,且活性剂还可以改善包装产品的感官和质量特性,避免将生物活性物质直接添加到食品中[5-6]。因此,活性涂膜技术在肉类及衍生产品的保鲜和包装中具有广阔的应用前景。
散沫花(Lawsonia inermis)是近年来中草药研究较多的植物之一。它属于菊科植物,以其叶子的天然橙红色而闻名。目前已证明散沫花树叶提取物具有多种生物活性,如:抗糖尿病[7]、抗真菌[8]、抗炎症[9]和抗氧化[7,9]等功效,这是预防鲜肉质量下降的重要因素。其中抗氧化活性可以归因于几种酚类化合物[10],有报道指出含有酚类化合物提取物可以延缓脂肪氧化,延长加工肉制品的货架期[6]。然而,目前将散沫花的功效运用于保鲜领域的研究尚少。因此,设计一款保水性强、抗菌和抗氧化效果好的散沫花活性涂膜对肉类保鲜及贮藏是一种新思路。
本研究制备了一种富含大量酚类物质的散沫花提取物复合明胶膜,对模仿冷链运输及冷藏零售1、3、6、8 d的过程中牛肉品质的保鲜效果进行了分析。通过测定涂膜样品和未涂膜样品的贮藏损失率、颜色变化、菌落总数、脂质氧化程度以及高铁血红蛋白、血红素铁和游离氨基酸含量,来评价散沫花提取物复合明胶膜对牛肉冷藏保鲜效果的影响,以期为后续制备HAE+明胶复合膜在冷鲜肉贮藏中的应用提供一种新型保鲜思路和依据,也为制备一种天然抗氧化的活性包装材料提供数据参考。
1. 材料与方法
1.1 材料与仪器
新鲜墨鱼 购买于山东利洋水产有限公司,原料获得后冻藏于−20 ℃冰箱备用;牛背部最长肌 购买于江苏苏食肉品有限公司;散沫花 获得于青岛农业大学植物医学学院;尼龙筛网 购买于安平市九峰筛网制造有限公司;pH校准液(4.0、7.0、10.0)、胃蛋白酶(≥2500 U/mg dw) 均购于生工生物工程(上海)有限公司;2-硫代巴比妥酸、异硫氰酸苯酯、氨基酸标准品、去甲亮氨酸 均购于上海阿拉丁生化科技股份有限公司;盐酸、丙酮、乙腈、氢氧化钠、氯化钠、三氯乙酸、甲醇、三乙胺、乙酸钠、硫酸钾和磷酸二氢钾等其它试剂 均为分析纯,购于国药集团化学试剂有限公司。
M01研磨机 山东九阳股份有限公司;BSM分析天平 上海卓精精密仪器有限公司;CR-41型便携式色差仪 日本美能达公司;VM-370旋涡混匀器 杭州齐威仪器有限公司;BP-3 pH计 西班牙IUL公司;XFSFY-12水分活度仪 厦门精凡科技有限公司;PT-2100均质机 瑞士Kinematica公司;ST16R离心机 美国赛默飞世尔科技公司;Infinite 200 PRO多功能酶标仪 瑞士TECAN公司;G-752紫外分光光度计 上海菁海仪器有限公司;LRH-70恒温培养箱 上海一恒仪器科学有限公司;GD-SSGW3冷藏柜 佛山亿凡电器有限公司;1260高效液相色谱仪 美国安捷伦科技有限公司。
1.2 实验方法
1.2.1 散沫花提取物(HAE)的制备
参考Al-Snafi等[11]方法,散沫花洗涤后,将花叶晒干并通过研磨机粉碎成粉末,过200目尼龙筛网去除根茎组织。然后将50 g粉末与500 mL蒸馏水混合,在20 ℃室温下搅拌24 h。最后将混合物离心(10000×g,15 min,4 ℃)去除不溶性物质,收集上清液冷冻并干燥。
1.2.2 明胶提取物的制备
参考Jridi等[7]方法,新鲜墨鱼用水洗净,以消除残留物和墨水,从墨鱼外皮中提取明胶。用0.05 mol/L的氢氧化钠溶液以1:10(w/v)的比例在4 ℃环境下2 h内去除非胶原蛋白,每30 min更换一次。然后用4 ℃蒸馏水多次洗涤外皮,使其恢复到其特有的中性pH。为了提取明胶,将外皮按1:10(w/v)的比例浸泡在0.1 mol/L醋酸中,以5 U/g的比例用胃蛋白酶水解外皮,并在4 ℃下孵育48 h。为了使酶失活,用10 mol/L氢氧化钠将混合物的pH提高到7.5,并在4 ℃下搅拌1 h,然后将外皮在40 ℃下搅拌孵育18 h提取明胶,最后,样品在4 ℃下以10000×g离心30 min以除去不溶性物质。为了制备活性明胶溶液,参考Emiroğlu等[12]和Jasour等[13]方法,并根据预实验结果,确定最优的HAE和明胶提取物的浓度比例为1:100(w/v),使用混匀器使明胶和HAE形成均匀的液体,最后将制作好的明胶放在4 ℃环境下冷藏直至使用。
1.2.3 牛肉处理及贮藏
将牛背部最长肌肉均匀地分成5 cm×5 cm×2 cm左右的肉块,参考Umaraw等[2]方法,分别设置为:未处理对照组、40 ℃浸泡明胶溶液30 s组和40 ℃浸泡富含HAE明胶溶液30 s组,处理好后将样品称重,并在4 ℃无包装条件下贮藏,模拟低温运输过程中的温度环境及新鲜零售陈列环境。在第1、3、6和8 d抽取样品并进行指标测定。
1.2.4 贮藏损失率测定
肉样在第3、6、8 d的失重率分别为:
WHC(%)=(W2−W1)/W2×100 式中,W2是样品的初始重量(g);W1是同一样品在冷藏3、6、8 d的重量(g)。
1.2.5 pH、色泽和水分活度测定
使用BP-3型便携式pH计进行测定,并采用标准的三点校准(4.0、7.0、10.0)。将5 g样品在20 mL蒸馏水中均质2 min并记录数据,每个样品重复测量3次。
使用CR-41型便携式色差仪进行测定并采用标准的白板校准。记录亮度值(L*),红度值(a*),黄度值(b*),色度(c*)使用标准公式c*=(a*2+b*2)1/2,每个样品重复测量3次。
使用快速水分活度仪进行测定,用氯化钠和硫酸钾校准后,将每个样品的内部截面放入仪器中进行测定,每个样品重复测量3次。
1.2.6 菌落总数测定
参考Berghe等[14]方法,将10 g样品用90 mL 0.85%氯化钠溶液匀浆,测定不同稀释度的细菌数。用平板计数琼脂倒置平板法测定细菌总数,接种平板在37 ℃下培养2 d和在10 ℃下培养7 d测定总活菌数和嗜冷菌数,结果以lg CFU/g样品表示。
1.2.7 脂质氧化(TBARS)测定
参考姜皓等[15]方法,使用均质机将5 g样品和20 mL体积分数20%的三氯乙酸溶液在4 ℃条件下匀浆5 min,使用离心机12000×g离心10 min,取4 mL上清液与4 mL 0.02 mol/L硫代巴比妥酸混合,在100 ℃水中孵育60 min。然后4 ℃环境下以2500×g离心10 min,取上清液在532 nm和600 nm处测定吸光值。含量计算如下:TBARS含量(μmol MDA/g)=(A532−A600)/155×(1/2)×72.06×1000,其中A代表不同吸光度处的数值。
1.2.8 血红素铁含量测定
参考Rezaei等[16]方法,将2 g样品用9 mL酸化丙酮(90%丙酮、8%去离子水、2%盐酸)匀浆并25 ℃黑暗环境中放置1 h,并使用玻璃棉过滤去除杂质,滤液在640 nm处测定吸光度。含量计算如下:血红素铁含量(mg/g)=A640×680×0.0882,其中A代表640 nm处的吸光度值。
1.2.9 高铁肌红蛋白含量测定
参考Fernandez等[17]方法,将5 g样品和50 mL磷酸盐缓冲液(pH6.8)在4 ℃环境下均质15 s。然后将样品在4 ℃环境下以15000×g离心30 min,取上清液后用玻璃棉过滤,用分光光度计测定525、572和730 nm处的吸光度。含量计算如下:高铁肌红蛋白含量(%)= ((A572−A730)/(A525−A730))×100,其中A代表不同吸光度处的数值。
1.2.10 游离氨基酸测定
参考Rangaraj等[18]方法,使用均质机将5 g样品与20 mL 0.01mol/L HCl混合匀浆8 min,然后在4 ℃环境以10000×g离心20 min,取上清并用玻璃棉过滤,在-20 ℃下保存直至分析。首先,准确称取18种氨基酸标准品分别为0.1g(精确至0.0001g)于100 mL的容量瓶中,0.1 mol/L的盐酸溶液定容,混匀,得到1000 mg/L的18种氨基酸的混合标准品溶液。然后逐级稀释成50、100、200、300、400、500 mg/L的氨基酸的混合标准液。以氨基酸标准品浓度为横坐标,峰面积为纵坐标,绘制标准曲线。混合氨基酸标准储备液中各氨基酸的含量的标准公式为:Cj=mj/(Mj×250)×1000。
其中Cj代表混合氨基酸标准储备液中氨基酸的浓度(mmol/L),mj代表称取氨基酸标准品的质量(mg),Mj代表氨基酸标准品的分子量。
对于待测样品,将250 mL解冻提取物、50 mL 10 mmol/L内标去甲亮氨酸和750 mL乙腈均匀混合。混合物以12000×g离心10 min,然后将500 mL上清液在蒸发器中干燥。接着在干燥样品中加入15 mL干燥剂(甲醇:1 mol/L乙酸钠:三乙胺=2:2:1),再次干燥。然后加入15 mL异硫氰酸苯酯(PITC)溶液进行衍生化。溶液室温下放置20 min后再次干燥。分析前,样品和标准品在由5 mmol/L磷酸钠缓冲液和5%乙腈组成的300 mL稀释试剂溶液中重新配制。使用高效液相色谱和二极管阵列检测器对PITC衍生物进行反相高效液相色谱(HPLC)分析。采用PicoTag®色谱柱,流速1 mL/min,52 ℃,检测波长为254 nm。结果以mg/100 g 表示。
1.3 数据处理
结果用SPSS v.18.0专业版软件(美国IBM公司)进行分析,并以平均数±标准差的形式显示在表格中。然后进行单因素方差分析(ANOVA),最后进行邓肯检验,P<0.05代表主效应之间差异显著。使用 SIMCA v.14.1软件(法国STDM公司)进行主成分分析(PCA)。
2. 结果与分析
2.1 牛肉贮藏损失率的变化
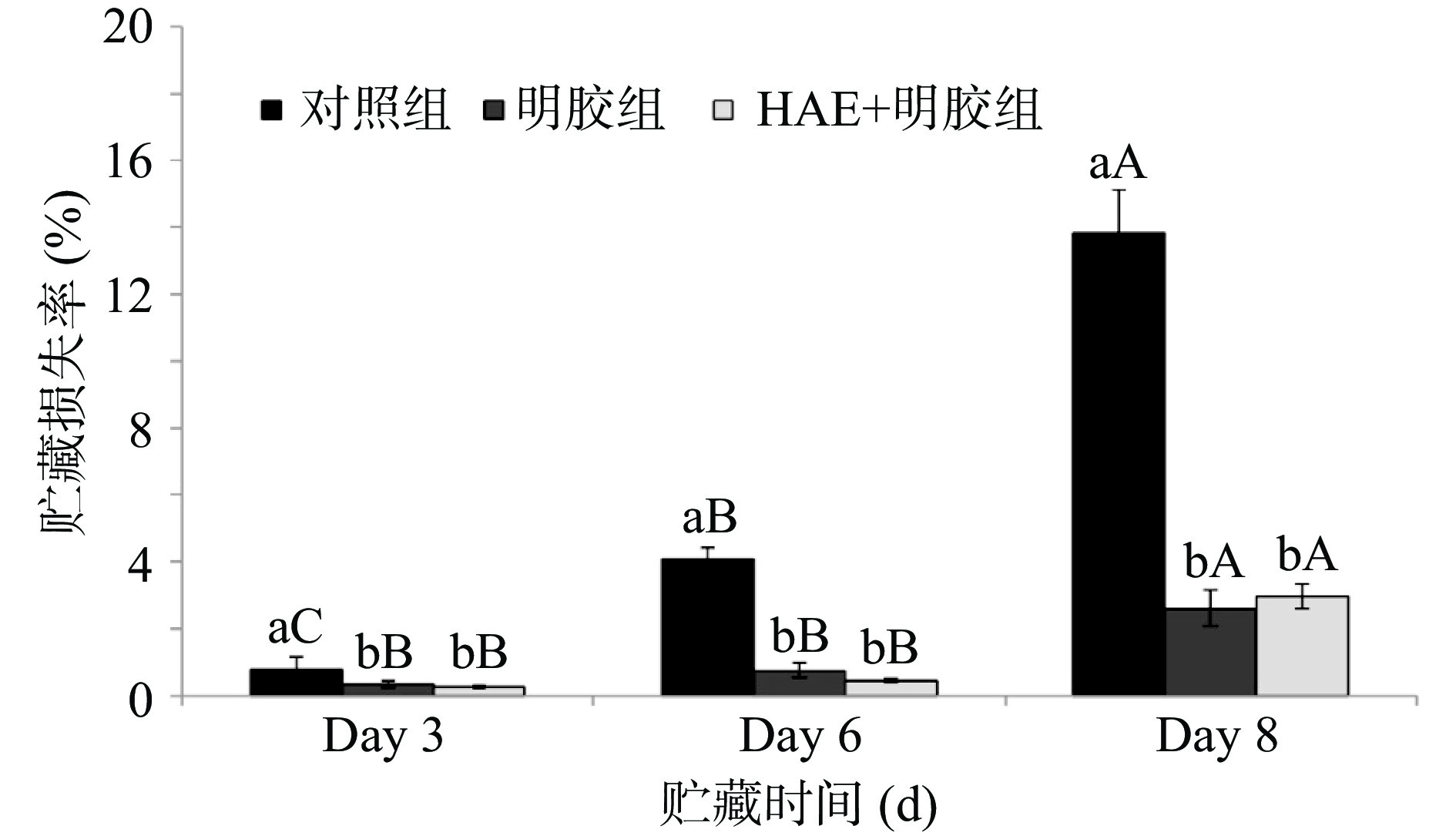
图1显示了4 ℃期间样品的贮藏损失率,对照组(未涂膜)在贮藏3、6和8 d后的损失率分别为0.8%、4%和13.8%。然而,经过明胶涂膜处理的样品显著降低了贮藏损失率,在第3、6和8 d的损失率分别为0.3%、0.75%和2.6%。添加HAE的明胶膜和未添加HAE的明胶膜样品之间的贮藏损失率差异不显著(P>0.05)。原因可能是明胶富含亲水性氨基酸和一些疏水性氨基酸,这些氨基酸能够保持水分,从而起到物理屏障防止水分流失的作用[19]。Herring等[20]研究表明,明胶涂层具有很强的保水性,并证实明胶可以减少猪肉在冷藏7 d内失水率,这与本实验的研究结果一致。
2.2 牛肉pH、水分活度和色泽的变化
表1研究了涂膜处理对牛肉贮藏期pH、水分活度(Aw)和色泽参数的影响。由表可知,对照组样品pH在贮藏6 d和8 d后显著升高。然而,明胶涂膜组样品的pH在一段时间内保持恒定,而添加HAE提取物明胶涂膜组样品在冷藏8 d后与对照组和只添加明胶组相比,pH显著降低(P<0.05)。观察结果中对照组pH在6 d和8 d增加的原因,可能是由于肉质腐败以及在碱性反应产生游离氨基酸过程中胺类物质的形成所致[21]。
表 1 贮藏1、3、6和8 d肉样的pH、水分活度和色泽的变化Table 1. Changes of pH, AW and color of meat samples at 1, 3, 6 and 8 days of storage指标 处理组 贮藏时间(d) 标准差 显著性 1 3 6 8 pH 对照组 5.79±0.08C 5.78±0.02aC 6.03±0.04aB 6.19±0.02aA 0.05 0.000 明胶组 5.79±0.08A 5.73±0.00bA 5.70±0.05cA 5.74±0.01bA 0.02 0.211 HAE+明胶组 5.79±0.08B 5.81±0.02aB 5.90±0.04bA 5.68±0.02cC 0.03 0.004 标准差 0.01 0.05 0.08 显著性 0.003 0.001 0.000 Aw 对照组 0.98±0.00A 0.98±0.00aA 0.98±0.01aA 0.98±0.00aA 0.00 0.472 明胶组 0.98±0.00A 0.99±0.00aA 0.99±0.00aA 0.98±0.00aA 0.00 0.002 HAE+明胶组 0.98±0.00A 0.99±0.00aA 0.98±0.00aA 0.97±0.01aA 0.00 0.000 标准差 0.00 0.00 0.00 显著性 0.054 0.423 0.000 L* 对照组 38.52±0.42C 39.72±0.19aB 41.24±0.59aAB 42.06±0.83aA 0.42 0.000 明胶组 38.52±0.42A 39.20±0.17aA 38.91±1.26bA 38.01±1.92bA 0.38 0.204 HAE+明胶组 38.52±0.42B 39.25±1.34aAB 41.28±1.35aA 42.05±1.25aA 0.49 0.027 标准差 0.24 0.51 0.78 显著性 0.690 0.065 0.019 a* 对照组 20.35±0.44B 22.72±0.83cA 12.43±0.27cC 5.91±0.9cD 2.45 0.000 明胶组 20.35±0.44B 25.97±1.24bA 20.74±1.44bB 15.5±1.3bC 1.15 0.000 HAE+明胶组 20.35±0.44D 27.95±0.16aA 24.89±1.27aB 22.09±0.75aC 0.89 0.000 标准差 0.80 1.86 2.37 显著性 0.001 0.000 0.000 b* 对照组 4.74±0.54A 4.32±1.15bA 3.63±0.19cAB 2.97±0.37cB 0.26 0.051 明胶组 4.74±0.54C 11.27±1.17aA 7.55±0.25bB 6.38±0.53bB 0.75 0.000 HAE+明胶组 4.74±0.54C 10.80±0.29aA 8.97±1.10aB 7.81±0.76aB 0.41 0.003 标准差 1.15 0.82 2.21 显著性 0.000 0.000 0.000 c* 对照组 20.89±0.01A 23.13±2.35cA 12.95±0.94cB 6.54±0.36cC 7.61 0.001 明胶组 20.89±0.01B 28.31±0.45bA 22.07±0.25bB 16.76±0.36bC 4.78 0.002 HAE+明胶组 20.89±0.01D 29.96±0.15aA 26.46±0.36aB 23.43±.0.19aC 3.91 0.001 标准差 3.57 6.89 8.51 显著性 0.001 0.001 0.000 注:不同小写字母表示相同贮藏时间不同处理组差异显著(P<0.05);不同大写字母表示相同处理组不同贮藏时间差异显著(P<0.05);表2同。 水分活度是控制贮藏肉品中微生物生长的一个重要因素,它可以定义为产品中存在的可用于细菌生长的游离水的量。由观察到的结果可知,在冷藏8 d中,对照组、明胶涂膜组和添加HAE明胶涂膜组的结果均没有显著差异(P>0.05)。
色泽方面,在对照组和HAE明胶组中,亮度值(L*)在冷藏期间显著增加,而红度值(a*)是牛肉贮藏期颜色变化的最大特征参数。在冷藏过程中,涂膜肉样的颜色受贮藏时间的影响,从鲜红色(新鲜状态)、浅红色到深红色。但在贮藏8 d后,未涂膜肉的颜色由鲜红色变为深棕色。根据表1可知,随着贮藏时间的延长,对照组的红度值(a*)降低,且数值明显低于明胶组和HAE+明胶组。在贮藏3、6和8 d期间,对照组的黄度值(b*)分别为4.32、3.63和2.97,而涂膜样品(明胶组和HAE+明胶组)的b*和c*显著高于对照组,肉经过涂膜处理改善了肉样的色度。此外,从红度值(a*)可以看出,与明胶涂膜相比,在明胶中添加HAE可以改善肉的颜色。这与Jridi等[7]的观点具有一致性,该文献报道,明胶涂膜显著保护了肉的色泽,且明胶涂膜对肉样中的红度值(a*)提供了良好的保护。此外,Herring等[20]研究也表明,浓度为10%的猪皮明胶涂膜在猪肉冷藏7 d内,红度值(a*)没有发生显著改变。在目前研究中,明胶中添加HAE则更加显著地改善了这一特征(P<0.05)。
2.3 牛肉菌落总数的变化
表2汇总了不同低温贮藏期的菌落总数。在放置初期(1 d),菌落总数(TVC)为3.03 lg CFU/g,这可能是由于牛肉在运输和屠宰过程中卫生条件所致。随着放置时间的延长,所有样品的TVC和PTC均显著增加,在冷藏第8 d达到最高值。根据表中结果发现,未涂膜处理的肉样菌落总数显著高于涂膜处理的肉(P<0.05),在第8 d达到最高(6.03 lg CFU/g)。而涂膜处理后的样品,可能由于表面蛋白质生物膜对氧气扩散和细菌增殖具有阻隔作用,明胶涂膜显著延缓和限制了微生物的生长[22]。在HAE明胶组样品中,与未涂膜的样品相比,TVC在放置第3 d从4.43降到3.14 lg CFU/g,第6 d从5.89降到5.57 lg CFU/g,第8 d从6.03降到5.78 lg CFU/g,而在第6 d时,与其他处理组相比,涂有HAE明胶肉类的菌落总数最低。此外,在PTC中,HAE明胶涂膜组的样品4.62 lg CFU/g,显著低于对照组5.18 lg CFU/g和明胶涂膜组5.21 lg CFU/g(P<0.05),这与TVC的趋势一致,表明添加HAE明胶组的样品在放置6 d后比没有涂膜处理的肉样贮藏效果更佳。
表 2 贮藏1、3、6和8 d肉样的总活菌数(TVC)和嗜冷菌数(PTC)Table 2. Total viable count (TVC) and cryophilic count (PTC) of meat samples at 1, 3, 6 and 8 days of storage处理组 贮藏时间(d) 标准差 显著性 1 3 6 8 TVC(lg CFU/g) 对照组 3.03±0.01D 4.43±0.05aC 5.89±0.02aB 6.03±0.02aA 0.46 0.000 明胶组 3.03±0.01C 3.09±0.06bC 5.63±0.05abB 5.9±0.01bA 0.51 0.000 HAE+明胶组 3.03±0.01C 3.14±0.01bC 5.57±0.05bB 5.78±0.03cA 0.49 0.000 标准差 0.28 0.06 0.05 显著性 0.001 0.059 0.011 PTC(lg CFU/g) 对照组 2.53±0.06D 3.95±0.02aC 5.18±0.01aB 5.78±0.02aA 0.47 0.000 明胶组 2.53±0.06D 3.56±0.04cC 5.21±0.02aB 5.69±0.04aA 0.46 0.000 HAE+明胶组 2.53±0.06D 3.75±0.02bC 4.62±0.07bB 5.62±0.1aA 0.43 0.000 标准差 0.07 0.12 0.04 显著性 0.008 0.005 0.370 目前已有报道指出,一些具有抗菌特性的物质已经从散沫花中分离出来,如没食子酸、芦荟酮1,4-萘醌等[23]。在Lorenzo等[24]报道中,合成涂膜中加入绿茶可在储存2周后将牛肉中的微生物生长减少到4 lg CFU/g。在本研究中,HAE明胶涂膜组的样品微生物数量显著减少,这可能归因于HAE的抗菌作用[8]。此外,HAE+明胶涂膜样品的冷藏保质期延长至8 d以上,尽管微生物生长的降幅不是很大,但目前的结果表明,HAE的添加与提升肉类涂膜处理的贮藏期有一定相关性。因此,如果通过提高HAE涂膜的浓度,可能可以更好抑制微生物的生长繁殖。
2.4 牛肉TBARS值的变化
脂类氧化是影响食物货架期的重要因素之一,尤其在含有高脂肪的肉类产品中[25]。通常,通过TBARS含量可以衡量肉类在贮藏过程中的脂质氧化程度。散沫花提取物以其潜在的抗氧化作用而闻名,这种作用可以抑制脂质氧化的早期阶段,并延缓氧化的过程[7]。由图2可知,在贮藏第8 d,对照组中的TBARS含量估计为0.86 μmol MDA/g,而明胶组和添加HAE+明胶组的TBARS含量分别降至0.53和0.42 μmol MDA/g。
HAE+明胶涂膜组样品中脂质氧化的减少可能归因于散沫花提取物有较强的抗氧化的作用。有报道指出,从散沫花提取物中分离出的酚苷被描述为是具有很强抗氧化活性的化合物,它可以与脂质的自由基反应,使其变得稳定,从而防止脂质氧化的发生[26]。此外,Mikhaeil等[27]的报道也指出,散沫花叶中富含的罗松酮、芹菜素、木犀草素、香豆素、对香豆酸、萘醌和蜂素,这些化合物都被认为是很好的抗氧化剂。在另一方面,明胶涂膜可以起到阻氧和降低肉脂氧化的作用[4]。Ahmad等[28]研究表明,经过明胶涂膜处理的猪肉与未涂膜处理的猪肉相比,TBARS值更低,可能归因于含有离子成分的存在,进而产生的聚合物在与肉本身的相互作用下会产生了良好的阻氧性。本实验的研究结果也表明,明胶涂膜处理有良好的阻氧效果,而添加HAE则更好地增强了明胶的抗氧能力。
2.5 牛肉血红素铁和高铁肌红蛋白含量的变化
由表3可知,对照组样品中的血红素铁水平随着时间的推移而降低,这表明在冷藏条件下,血红素铁转化为非血红素铁。有文献指出,在脂质氧化过程中,肉类和肉制品中的血红素铁可以部分转化为非血红素铁[29]。在贮藏前6 d,明胶组和HAE+明胶组的血红素含量差异不显著(P>0.05),而贮藏第8 d,与明胶处理组相比,HAE+明胶处理组显著抑制了血红素铁的转化,这可能是由于非血红素铁催化脂质氧化的能力,贮藏6 d血红素铁含量的降低可能与在相同贮藏期观察到的TBARS值的增加有关[25]。在目前研究中,除贮藏6 d后的HAE+涂膜样品外,所有样品中高铁肌红蛋白的含量随着时间推移都有所增加,这与上述脂质氧化、血红素铁含量和肉色的结果具有一致性。有文献指出,过氧化氢与高铁肌红蛋白之间的相互作用可能引发肉类发生脂质氧化[30]。此外,产生的暗红色表明高铁肌红蛋白积累可能与脂质氧化或微生物的繁殖有关[7]。在目前的研究中,明胶涂膜显著抑制了生牛肉色变和脂质氧化,而添加HAE提取物作为抗氧化剂显著改善了生牛肉的色泽劣变和脂质氧化的程度。
表 3 贮藏1、3、6和8 d肉样的高铁肌红蛋白和血红素铁含量Table 3. Contents of methemoglobin and heme iron in meat samples at 1, 3, 6, and 8 days of storage处理组 贮藏时间(d) 标准差 显著性 1 3 6 8 高铁肌红蛋白(%) 对照组 19.67±1.27D 26.7±1.99bC 61.49±2.15aB 69.01±1.50aA 5.49 0.000 明胶组 19.67±1.27C 21.84±0.75cC 37.37±3.08bB 63.12±1.12bA 4.74 0.000 HAE+明胶组 19.67±1.27C 30.7±2.49aB 26.08±3.10cB 42.98±4.48cA 2.31 0.000 标准差 1.34 4.42 3.20 显著性 0.002 0.000 0.000 血红素铁(mg/g) 对照组 5.08±0.39A 3.25±0.39bB 2.98±0.00bB 1.27±0.28cC 0.41 0.000 明胶组 5.08±0.39AB 5.70±0.82aA 5.18±0.35aAB 4.45±0.50bB 0.19 0.126 HAE+明胶组 5.08±0.39B 5.41±0.44aAB 5.77±0.45aAB 5.87±0.11aA 0.13 0.117 标准差 0.42 0.43 0.69 显著性 0.004 0.000 0.000 2.6 牛肉游离氨基酸含量的变化
在目前的研究中(图3),所有样品在4 ℃开始到贮藏8 d后,对照组中游离氨基酸的总含量分别为197.7 mg/100 g和266.6 mg/100 g,而使用明胶处理组(201.4 mg/100 g)和添加HAE+明胶处理组(209.7 mg/100 g)中的总游离氨基酸(FAA)含量无显著增加(P<0.05)。在放置到第8 d,与未处理的肉相比,明胶涂膜组和HAE明胶涂膜组的肉中只有谷氨酰胺和天冬氨酸差异不显著(P>0.05)。此外,在对照样品中,除苏氨酸、异亮氨酸和赖氨酸含量下降外,游离氨基酸总量和其余各项含量贮藏过程中均呈上升趋势。牛经屠宰后放置过程中,蛋白水解是一个缓慢的动态过程,其中内肽酶(如组织蛋白酶和钙蛋白酶)随机地作用于它们的裂解,产生复杂的多肽混合物,而外肽酶也是影响肉类新鲜度的一个重要指标,它涉及动物死后蛋白质和寡肽降解为小肽和游离氨基酸[31]。此外,肉质在腐败过程中也会导致游离氨基酸含量的增加[19]。因此,造成上述贮藏期间游离氨基酸含量的变化可能与蛋白质水解以及上述微生物的繁殖有关。
2.7 主成分分析 (PCA)
进行PCA分析来研究各指标之间的关联性以及不同处理组放置过程中牛肉品质的变化趋势。两张主成分图分别覆盖了总数据变化的84.5%和94.0%,这体现了模型的有效性。在图4a中,pH、a*、c*、血红素铁含量、TBARS、TVC、贮藏损失和水分活度处于同一象限,表明样品颜色的变化与pH、血红素铁含量、脂质氧化的发生以及微生物繁殖具有高度相关性。其中贮藏期主要颜色(a*、b*和c*)的变化与血红素铁含量的趋势高度一致,与高铁肌红蛋白含量和菌落总数含量呈反比。有文献指出,在红肉中肉色的差异与血红素铁的含量密切相关[25],而脂质氧化的产生和微生物的繁殖又会近一步影响血红素铁的形成[29],这与目前的研究结果一致。这种现象表明脂质氧化和微生物的繁殖可能在肉颜色的变化中起作用[7]。此外,有报道发现脂质氧化的发生与肉品质,包括贮藏损失率的变化也有一定的联系[31],这与主成分中观察的结果一致。在图4b中,发现PCA映射点从左向右移动,说明放置过程对牛肉的品质产生了很大的影响。在不同处理组中,随着放置期的延长,对照组PCA映射点的移动幅度最大,明胶组虽然在放置初期(3 d) PCA映射点变化不大,但随着时间的延长仍产生了显著的差异,而HAE+明胶组PCA映射点仍基本处在同一象限中。这一事实说明添加HAE的明胶涂膜可以有效控制牛肉冷藏期间的品质劣变,并延长牛肉的货架期。此外,在放置初期(1 d)时,不同处理组之间就显示出明显的距离,说明肉本身质量的差异和屠宰过程也是影响肉后期贮藏期品质的因素之一[32]。
![]() 图 4 贮藏1、3、6和8 d肉样的主成分分析注:图4b中,a、b和c分别代表三个平行。Figure 4. Principal component analysis of meat samples at 1, 3, 6 and 8 days of storage
图 4 贮藏1、3、6和8 d肉样的主成分分析注:图4b中,a、b和c分别代表三个平行。Figure 4. Principal component analysis of meat samples at 1, 3, 6 and 8 days of storage3. 结论
本研究全面调查了HAE+明胶膜对牛肉冷藏期保鲜效果的影响。主要结果是涂膜处理能有效防止牛肉中水分的流失、高铁肌红蛋白的形成以及蛋白质水解的速率,显著降低了牛肉色泽的劣变程度和贮藏损失率,维持了样品的外观,而在明胶涂层中添加HAE则更好地提高了这种保护效果。此外,与对照组相比,由于HAE的抗氧化和抗菌作用,可通过向牛肉中渗透活性成分来有效延缓pH的上升和微生物的生长,减少菌落总数和嗜冷菌数来延长肉类的保质期,并一定程度上抑制脂肪的氧化。然而,本文尚未对散沫花功能的机制做出更深层级的探究,在未来,应该把更多的精力花在对在散沫花提取物的生物活性功能上,这可以为散沫花活性保鲜材料开发提供更全面的认识,并为肉类保鲜提供更深的思路。
-
图 4 贮藏1、3、6和8 d肉样的主成分分析
注:图4b中,a、b和c分别代表三个平行。
Figure 4. Principal component analysis of meat samples at 1, 3, 6 and 8 days of storage
表 1 贮藏1、3、6和8 d肉样的pH、水分活度和色泽的变化
Table 1 Changes of pH, AW and color of meat samples at 1, 3, 6 and 8 days of storage
指标 处理组 贮藏时间(d) 标准差 显著性 1 3 6 8 pH 对照组 5.79±0.08C 5.78±0.02aC 6.03±0.04aB 6.19±0.02aA 0.05 0.000 明胶组 5.79±0.08A 5.73±0.00bA 5.70±0.05cA 5.74±0.01bA 0.02 0.211 HAE+明胶组 5.79±0.08B 5.81±0.02aB 5.90±0.04bA 5.68±0.02cC 0.03 0.004 标准差 0.01 0.05 0.08 显著性 0.003 0.001 0.000 Aw 对照组 0.98±0.00A 0.98±0.00aA 0.98±0.01aA 0.98±0.00aA 0.00 0.472 明胶组 0.98±0.00A 0.99±0.00aA 0.99±0.00aA 0.98±0.00aA 0.00 0.002 HAE+明胶组 0.98±0.00A 0.99±0.00aA 0.98±0.00aA 0.97±0.01aA 0.00 0.000 标准差 0.00 0.00 0.00 显著性 0.054 0.423 0.000 L* 对照组 38.52±0.42C 39.72±0.19aB 41.24±0.59aAB 42.06±0.83aA 0.42 0.000 明胶组 38.52±0.42A 39.20±0.17aA 38.91±1.26bA 38.01±1.92bA 0.38 0.204 HAE+明胶组 38.52±0.42B 39.25±1.34aAB 41.28±1.35aA 42.05±1.25aA 0.49 0.027 标准差 0.24 0.51 0.78 显著性 0.690 0.065 0.019 a* 对照组 20.35±0.44B 22.72±0.83cA 12.43±0.27cC 5.91±0.9cD 2.45 0.000 明胶组 20.35±0.44B 25.97±1.24bA 20.74±1.44bB 15.5±1.3bC 1.15 0.000 HAE+明胶组 20.35±0.44D 27.95±0.16aA 24.89±1.27aB 22.09±0.75aC 0.89 0.000 标准差 0.80 1.86 2.37 显著性 0.001 0.000 0.000 b* 对照组 4.74±0.54A 4.32±1.15bA 3.63±0.19cAB 2.97±0.37cB 0.26 0.051 明胶组 4.74±0.54C 11.27±1.17aA 7.55±0.25bB 6.38±0.53bB 0.75 0.000 HAE+明胶组 4.74±0.54C 10.80±0.29aA 8.97±1.10aB 7.81±0.76aB 0.41 0.003 标准差 1.15 0.82 2.21 显著性 0.000 0.000 0.000 c* 对照组 20.89±0.01A 23.13±2.35cA 12.95±0.94cB 6.54±0.36cC 7.61 0.001 明胶组 20.89±0.01B 28.31±0.45bA 22.07±0.25bB 16.76±0.36bC 4.78 0.002 HAE+明胶组 20.89±0.01D 29.96±0.15aA 26.46±0.36aB 23.43±.0.19aC 3.91 0.001 标准差 3.57 6.89 8.51 显著性 0.001 0.001 0.000 注:不同小写字母表示相同贮藏时间不同处理组差异显著(P<0.05);不同大写字母表示相同处理组不同贮藏时间差异显著(P<0.05);表2同。 表 2 贮藏1、3、6和8 d肉样的总活菌数(TVC)和嗜冷菌数(PTC)
Table 2 Total viable count (TVC) and cryophilic count (PTC) of meat samples at 1, 3, 6 and 8 days of storage
处理组 贮藏时间(d) 标准差 显著性 1 3 6 8 TVC(lg CFU/g) 对照组 3.03±0.01D 4.43±0.05aC 5.89±0.02aB 6.03±0.02aA 0.46 0.000 明胶组 3.03±0.01C 3.09±0.06bC 5.63±0.05abB 5.9±0.01bA 0.51 0.000 HAE+明胶组 3.03±0.01C 3.14±0.01bC 5.57±0.05bB 5.78±0.03cA 0.49 0.000 标准差 0.28 0.06 0.05 显著性 0.001 0.059 0.011 PTC(lg CFU/g) 对照组 2.53±0.06D 3.95±0.02aC 5.18±0.01aB 5.78±0.02aA 0.47 0.000 明胶组 2.53±0.06D 3.56±0.04cC 5.21±0.02aB 5.69±0.04aA 0.46 0.000 HAE+明胶组 2.53±0.06D 3.75±0.02bC 4.62±0.07bB 5.62±0.1aA 0.43 0.000 标准差 0.07 0.12 0.04 显著性 0.008 0.005 0.370 表 3 贮藏1、3、6和8 d肉样的高铁肌红蛋白和血红素铁含量
Table 3 Contents of methemoglobin and heme iron in meat samples at 1, 3, 6, and 8 days of storage
处理组 贮藏时间(d) 标准差 显著性 1 3 6 8 高铁肌红蛋白(%) 对照组 19.67±1.27D 26.7±1.99bC 61.49±2.15aB 69.01±1.50aA 5.49 0.000 明胶组 19.67±1.27C 21.84±0.75cC 37.37±3.08bB 63.12±1.12bA 4.74 0.000 HAE+明胶组 19.67±1.27C 30.7±2.49aB 26.08±3.10cB 42.98±4.48cA 2.31 0.000 标准差 1.34 4.42 3.20 显著性 0.002 0.000 0.000 血红素铁(mg/g) 对照组 5.08±0.39A 3.25±0.39bB 2.98±0.00bB 1.27±0.28cC 0.41 0.000 明胶组 5.08±0.39AB 5.70±0.82aA 5.18±0.35aAB 4.45±0.50bB 0.19 0.126 HAE+明胶组 5.08±0.39B 5.41±0.44aAB 5.77±0.45aAB 5.87±0.11aA 0.13 0.117 标准差 0.42 0.43 0.69 显著性 0.004 0.000 0.000 -
[1] 韩磊. 中国肉类供需形势及稳产保供对策研究[J]. 价格理论与实践,2020(7):57−61. [HAN L. Study on situation of meat supply and demand and countermeasures of ensuring stable production and supply in China[J]. Price:Theory and Practice,2020(7):57−61. HAN L. Study on situation of meat supply and demand and countermeasures of ensuring stable production and supply in China[J]. Price: Theory and Practice, 2020, (7): 57-61.
[2] UMARAW P, MUNEKATA P E S, VERMA A K, et al. Edible films/coating with tailored properties foractive packaging of meat, fish and derived products[J]. Trends in Food Science and Technology,2020,98:10−24. doi: 10.1016/j.jpgs.2020.01.032
[3] 赵娅英, 史巧, 王馨蕊, 等. 可食性膜在肉及肉制品保质中的应用研究进展[J]. 食品工业科技,2021,42(19):411−417. [ZHAO Y Y, SHI Q, WANG X R, et al. Research progress of edible film in meat and meat products[J]. Science and Technology of Food Industry,2021,42(19):411−417. ZHAO Y Y, SHI Q, WANG X R, et al. Research progress of edible film in meat and meat products[J]. Science and Technology of Food Industry, 2021, 42(19): 411-417.
[4] 李媛, 张晓洁, 马良, 等. 兔皮明胶/迷迭香酸复合膜在猪肉冷藏保鲜中的应用效果[J]. 食品科学,2019,40(19):281−287. [LI Y, ZHANG X J, MA L, et al. Application of rabbit skin gelatin/rosmarinic acid composite film in pork quality preservation during cold storage[J]. Food Science,2019,40(19):281−287. doi: 10.7506/spkx1002-6630-20180930-339 LI Y, ZHANG X J, MA L, et al. Application of rabbit skin gelatin/rosmarinic acid composite film in pork quality preservation during cold storage[J]. Food Science, 2019, 40(19): 281-287. doi: 10.7506/spkx1002-6630-20180930-339
[5] NOWZARI F, SHÁBANPOUR B, OJAGH S M. Comparison of chitosan-gelatin composite and bilayer coating and film effect on the quality of refrigerated rainbow trout[J]. Food Chemistry,2013,141(3):1667−1672. doi: 10.1016/j.foodchem.2013.03.022
[6] ALBERTOS I, AVENA-BUSTILLOS R J, MARTÍN-DIANA A B, et al. Antimicrobial olive leaf gelatin films for enhancing the quality of cold-smoked salmon[J]. Food Packaging and Shelf Life,2017,13:49−55. doi: 10.1016/j.fpsl.2017.07.004
[7] JRIDI M, SELLIMI S, LASSOUED K B, et al. Wound healing activity of cuttlefish gelatin gels and films enriched by henna (Lawsonia inermis) extract[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2017,512:71−79.
[8] 姜洪芳, 石宝俊, 张锋伦, 等. 散沫花叶总黄酮、多酚含量测定及体外抗氧化活性研究[J]. 中国野生植物资源,2015,34(5):9−13. [JIANG H F, SHI B J, ZHANG F L, et al. Determination of total flavonoids and phenolic content and antioxidant activities of ethanol extract from the leaves of Lawsonia inermis Linn[J]. Chinese Wild Plant Resources,2015,34(5):9−13. doi: 10.3969/j.issn.1006-9690.2015.05.003 JIANG H F, SHI B J, ZHANG F L, et al. Determination of total flavonoids and phenolic content and antioxidant activities of ethanol extract from the leaves of Lawsonia inermis linn[J]. Chinese Wild Plant Resources, 2015, 34(5): 9-13. doi: 10.3969/j.issn.1006-9690.2015.05.003
[9] IMAM H, MAHBUB N U, KHAN M F, et al. Alpha amylase enzyme inhibitory and anti-inflammatory effect of Lawsonia inermis[J]. Pakistan Journal of Biological Sciences:PJBS,2013,16(23):1796−1800. doi: 10.3923/pjbs.2013.1796.1800
[10] 李倩, 高文芹, 赵余庆. 散沫花化学成分和生物活性研究进展[J]. 中国中药杂志,2013,38(6):795−799. [LI Qi, GAO W Q, ZHAO Y Q. Advances in studies on chemical constituents and biological activities of Lawsonia inermis[J]. China Journal of Chinese Materia Medica,2013,38(6):795−799. LI Qi, GAO W Q, ZHAO Y Q. Advances in studies on chemical constituents and biological activities of Lawsonia inermis[J]. China Journal of Chinese Materia Medica, 2013, 38(6): 795-799.
[11] AL-SNAFI A E. A review on Lawsonia inermis: A potential medicinal plant[J]. International Journal of Current Pharmaceutical Research,2019,11(5):1−13.
[12] EMIROĞLU Z K, YEMIŞ G P, COŞKUN B K, et al. Antimicrobial activity of soy edible films incorporated with thyme and oregano essential oils on fresh ground beef patties[J]. Meat Science,2010,86(2):283−288. doi: 10.1016/j.meatsci.2010.04.016
[13] JASOUR M S, EHSANI A, MEHRYAR L, et al. Chitosan coating incorporated with the lactoperoxidase system: An active edible coating for fish preservation[J]. Journal of the Science of Food and Agriculture,2015,95(6):1373−1378. doi: 10.1002/jsfa.6838
[14] BERGHE V A, VLIETINCK A J. Screening methods for antibacterial and antiviral agents from higher plants[M]. London: Academic Press, 1991.
[15] 姜皓, 杨璐, 徐文怡, 等. 原料脂肪氧化程度对西式培根安全品质的影响[J]. 食品工业科技,2020,41(23):209−215. [JIANG H, YANG L, XU W Y, et al. Effects of different degrees of raw fat oxidation on the safety and quality of bacon[J]. Science and Technology of Food Industry,2020,41(23):209−215. JIANG H, YANG L, XU W Y, et al. Effects of different degrees of raw fat oxidation on the safety and quality of bacon[J]. Science and Technology of Food Industry, 2020, 41(23): 209-215.
[16] REZAEI M, HOSSEINI S F. Quality assessment of farmed rainbow trout (Oncorhynchus mykiss) during chilled storage[J]. Journal of Food Science,2010,73(6):H93−H96.
[17] FERNÁNDEZ-LÓPEZ J, SEVILLA L, SAYAS-BARBERÁ E, et al. Evaluation of the antioxidant potential ofhyssop (Hyssopus officinalis L.) and rosemary (Rosmarinus officinalis L.) extracts in cooked pork meat[J]. Journal of Food Science,2003,68(2):660−664. doi: 10.1111/j.1365-2621.2003.tb05727.x
[18] RANGARAJ V M, RAMBABU K, BANAT F, et al. Effect of date fruit waste extract as an antioxidant additive on the properties of active gelatin films[J]. Food Chemistry,2021,355:129631. doi: 10.1016/j.foodchem.2021.129631
[19] JAMRÓZ E, KULAWIK P, TKACZEWSKA J, et al. The effects of active double-layered furcellaran/gelatin hydrolysate film system with Ala-Tyr peptide on fresh Atlantic mackerel stored at −18 ℃[J]. Food Chemistry,2021,338:127867. doi: 10.1016/j.foodchem.2020.127867
[20] HERRING J L, JONNALONGADDA S C, NARAYANAN V C, et al. Oxidative stability of gelatin coated pork at refrigerated storage[J]. Meat Science,2010,85(4):651−656. doi: 10.1016/j.meatsci.2010.03.019
[21] BASTOS B M, FARIAS B S, CASATI M O, et al. Gelatin films from carp skin crosslinked by gallic acid and incorporated with chitosan/tuna lipid fractions[J]. Journal of Polymers and the Environment,2021,29(7):2096−2110. doi: 10.1007/s10924-020-01995-2
[22] 胡熠, 唐艳, 周伟, 等. 可食性明胶复合膜及其在食品包装上的应用研究进展[J]. 食品工业科技,2017,38(20):341−346. [HU Y, TANG Y, ZHOU W, et al. Research progress of composite edible gelatin films and its application in food packaging[J]. Science and Technology of Food Industry,2017,38(20):341−346. HU Y, TANG Y, ZHOU W, et al. Research progress of composite edible gelatin films and its application in food packaging[J]. Science and Technology of Food Industry, 2017, 38(20): 341-346.
[23] RAKHSHANDEH H, GHORBANZADEH A, NEGAH S S, et al. Pain-relieving effects of Lawsonia inermison neuropathic pain induced by chronic constriction injury[J]. Metabolic Brain Disease,2021,36(7):1709−1716. doi: 10.1007/s11011-021-00773-w
[24] LORENZO J M, SARRIÉS M V, TATEO A, et al. Carcass characteristics, meat quality and nutritional value of horsemeat: A review[J]. Meat Science,2014,96(4):1478−1488. doi: 10.1016/j.meatsci.2013.12.006
[25] AMARAL A B, SILVA M V, LANNES S C S. Lipid oxidation in meat: Mechanisms and protective factors-A review[J]. Food Science and Technology,2018,38:1−15.
[26] ZOHOURIAN T H, QUITAIN A T, SASAKI M, et al. Polyphenolic contents and antioxidant activities of Lawsonia inermis leaf extracts obtained by microwave-assisted hydrothermal method[J]. Journal of Microwave Power and Electromagnetic Energy,2011,45(4):193−204. doi: 10.1080/08327823.2011.11689814
[27] MIKHAEIL B R, BADRIA F A, MAATOOQ G T, et al. Antioxidant and immunomodulatory constituents of henna leaves[J]. Zeitschrift für Naturforschung C,2004,59(7-8):468−476.
[28] AHMAD R, ANSARI K. Chemically treated Lawsonia inermis seeds powder (CTLISP): An eco-friendly adsorbent for the removal of brilliant green dye from aqueous solution[J]. Groundwater for Sustainable Development,2020,11:100417. doi: 10.1016/j.gsd.2020.100417
[29] SOLADOYE O P, JUÁREZ M L, AALHUS J L, et al. Protein oxidation in processed meat: Mechanisms and potential implications on human health[J]. Comprehensive Reviews in Food Science and Food Safety,2015,14(2):106−122. doi: 10.1111/1541-4337.12127
[30] MIN B, AHN D U. Mechanism of lipid peroxidation in meat and meat products-A review[J]. Food Science and Biotechnology,2005,14(1):152−163.
[31] GÓMEZ I, JANARDHANAN R, IBAÑEZ F C, et al. The effects of processing and preservation technologies on meat quality: Sensory and nutritional aspects[J]. Foods,2020,9(10):1416. doi: 10.3390/foods9101416
[32] GAGAOUA M, MONTEILS V, COUVREUR S, et al. Identification of biomarkers associated with the rearing practices, carcass characteristics, and beef quality: An integrative approach[J]. Journal of Agricultural and Food Chemistry,2017,65(37):8264−8278. doi: 10.1021/acs.jafc.7b03239






 下载:
下载:



 下载:
下载:



