Determination of 14 Pesticide Residues in Tea by QuEChERS Combined with Ultra-performance Liquid Chromatography-tandem Mass Spectrometry
-
摘要: 建立了QuEChERS(Quick,Easy,Cheap,Effective,Rugged,Safe)前处理结合超高效液相色谱-串联质谱法(UPLC-MS/MS)测定茶叶中14种农药残留的方法。茶叶样品经含1%乙酸的乙腈提取,QuEChERS净化柱净化后直接进行UPLC-MS/MS测定。比较了4种QuEChERS净化柱对茶叶提取液的净化效果和农药残留的回收率,选取净化效果和回收率最好的净化柱进一步考察方法的基质效应、线性关系、回收率等。结果表明,方法的检出限为0.001~2.000 μg/L,定量限为0.003~5.000 μg/L;14种农药在相应浓度范围内呈良好的线性关系,决定系数R2为0.9926~0.9989。在100、500、800 μg/kg 3个添加水平下14种农药的回收率为71.2%~117.4%,相对标准偏差为1.1%~14.2%。该方法具有操作简单快速、灵敏度高、回收率好等优点,能够满足茶叶中多农残快速检测要求。
-
关键词:
- 超高效液相色谱-串联质谱 /
- QuEChERS前处理 /
- 有机磷农药 /
- 有机氯农药 /
- 氨基甲酸酯类农药 /
- 茶叶
Abstract: A method for the determination of 14 pesticide residues in tea was developed by QuEChERS (Quick, Easy, Cheap, Effective, Rugged, Safe) pretreatment combined with ultra-performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS). The tea samples were extracted with acetonitrile (with 1% acetic acid), purified using QuEChERS purification columns and then analyzed by UPLC-MS/MS. The effects of four purification columns on tea extracts and the recoveries of pesticide residues were compared. The column with better purification effect and recovery was selected to further investigate the matrix effect, linear relationship, and recovery of the method. The results showed that the detection limit of the method was 0.001~2.000 μg/L, and the limit of quantification was 0.003~5.000 μg/L. Reliable linear relationship within the corresponding concentration range were observed for 14 pesticides, with coefficient of determination between 0.9926 and 0.9989. The average recoveries were 71.2%~117.4% at the spiking levels of 100, 500, and 800 μg/kg with RSDs at the range of 1.1%~14.2%. This method showed its advantages of simple and fast operation, sensitivity and recovery rate, meeting the requirements for determination of multi pesticide residues in tea. -
我国是茶叶的发源地,也是茶叶生产和消费量最大的国家。由于茶树生长喜温暖潮湿环境、种植单一化、缺乏生物多样性的特点,较易发生病虫害,其规模化种植过程中离不开农药的使用,农药残留问题难以避免[1-2]。国家允许在茶叶上使用一些高效低毒的农药,在GB 2763-2021《食品安全国家标准 食品中农药最大残留限量》中规定了106项茶叶农药残留限量标准[3]。然而,由于部分商家追求利益盲目施加农药和化肥催生、茶农使用农药不科学等原因,食品安全监督检查中茶叶农残超标的情况时有发生,甚至屡有禁用高毒农药的检出,严重危害消费者安全与市场信心[4-5]。
近年来,农药残留分析方法向着快速、简单、灵敏、低成本、易普及的方向发展。液相色谱-串联质谱法和气相色谱-串联质谱法是最常用的农药多残留检测分析手段,具有高灵敏度、高通量、定量准确等优点[6-9]。由于茶叶样品基质复杂,含有大量的茶多酚、生物碱、色素和有机酸等物质,检测过程中会产生较强的基质效应,必须通过前处理净化以减弱对目标农药检测的影响[10-11]。茶叶农药残留检测中传统的样品前处理技术如固相萃取[12-13]、液液萃取[14]、基质固相分散萃取[15]等常需要多次净化步骤,操作较为繁琐和耗时。2003年美国农业部Anastasiadis等发布的QuEChERS法[16],是液液萃取法与基质分散固相萃取法相结合形成的一种前处理方法,通常使用乙腈或含1%乙酸的乙腈提取,加入无水硫酸镁(MgSO4)、氯化钠(NaCl)除水,配合使用N-丙基乙二胺(PSA)、石墨化炭黑(GCB)和十八烷基硅烷(C18)等进一步净化,对不同种类的农药均有较好的回收率,具有操作简单、快速高效、成本低廉的优点[17],在果蔬[18-20]、食用菌[21]、中药材[22]等植物源食品的多农残检测中得到了广泛的应用。本研究的主要目的是开发一种基于QuEChERS前处理技术结合UPLC-MS/MS,同时检测茶叶中14种常见农药残留的高灵敏、快速检测方法,考察提取液组分、QuEChERS净化柱等对回收率的影响,确定了最优条件,并将方法应用于30种市售茶叶样品检测,以期为高效和准确地评价茶叶的质量安全提供参考。
1. 材料与方法
1.1 材料与仪器
14种农药标准品(啶虫脒、涕灭威、克百威、内吸磷、灭线磷、吡虫啉、茚虫威、甲胺磷、灭多威、氧化乐果、甲基对硫磷、硫环磷、丙溴磷、噻虫嗪)(100 mg/L) 天津阿尔塔科技有限公司,于−20 ℃冰箱保存;30种茶叶包括不同种类绿茶(狮峰龙井、竹叶青、采花毛尖、西湖龙井、太平猴魁茶、桐城小花、绿杨春、清明茶高山绿)、红茶(武夷山红茶、祁门红茶、生态野生红茶、古树红茶、金骏眉)、白茶(牡丹王白茶、政和白茶、安吉白茶)、乌龙茶(铁观音、大红袍、老枞水仙、马头岩肉桂)、花茶(茉莉花茶、菊花茶、蒲公英玫瑰茶、玫瑰花茶)、普洱茶、青稞茶、刺五加茶等 购于当地超市和茶叶专卖店,西湖龙井和古树红茶按照《GB 23200.121-2021》所示LC-MS/MS方法检测未检出本研究涉及的14种农药,分别作为空白绿茶和红茶基质进行相关研究;QuEChERS盐包(含有6 g MgSO4,1.5 g乙酸钠) 北京绿绵科技有限公司;尼龙微孔滤膜(型号SHIMEN DISC,孔径0.22 μm) 日本SHIMADZU公司;乙腈、甲醇、甲酸 色谱纯,美国Fisher公司;甲酸铵、乙酸 分析纯,德国Merk公司;4种QuEChERS净化柱及其使用方法如表1所示。
表 1 4种QuEChERS净化柱型号、成分及使用方法Table 1. Model, component and usage of four kinds of QuEChERS purification columns生产厂家 净化柱名称 型号 成分 净化方法 天津阿尔塔
科技有限公司简单基质
针式过滤器F-QuEChERS-AOAC 3201 150 mg MgSO4
50 mg PSA在过滤器注射器端连接0.22 μm尼龙微孔滤膜,
从加样端注入1 mL前处理上清液,然后使用
柱塞杆施加正压过滤,即得待测液复杂基质
针式过滤器F-QuEChERS-AOAC 3203 150 mg MgSO4
50 mg PSA
50 mg C18
5 mg GCB北京绿绵
科技有限公司简单基质
净化柱LM806-FC-721 150 mg MgSO4
15 mg PSA
15 mg多壁碳纳米管将净化柱塞入50 mL离心管中,缓慢按压,
离心管中上层提取液经过净化柱内的阻水滤片
及填料净化后进入储液槽。取1 mL储液过
0.22 μm尼龙微孔滤膜,即得待测液茶叶专用
净化柱LM806-FC-722 120 mg MgSO4
45 mg PSA
45 mg多壁碳纳米管Q-Trap 6500质谱仪 美国AB Sciex公司;LC-30AD液相色谱仪 日本SHIMADZU公司;Centrifuge 5810R低温高速离心机 德国Eppendorf公司;QL-901涡旋仪 美国KYLIN-BELL LAB公司;破壁粉碎机 中国天喜公司。
1.2 实验方法
1.2.1 样品前处理
提取:称取1 g粉碎好的茶叶样品于50 mL离心管中,加入10 mL超纯水,涡旋振荡5 min,加入10 mL 1%乙酸-乙腈溶液,涡旋振荡30 s,加入QuEChERS盐包,涡旋振荡5 min,以9000 r/min离心5 min,得上清提取液。
净化:经过上述得到的上清液分别使用4种QuEChERS净化柱进行下一步净化处理,具体方法见表1。
1.2.2 溶液配制
混合标准溶液:取14种农药标准品溶液(100 mg/L)各100 μL于10 mL容量瓶,加入乙腈定容,得到浓度为1 mg/L的混合标准溶液,于−20 ℃冰箱保存。
空白基质溶液:称取1 g(精确至0.001 g)空白绿茶/红茶样品,按照1.2.1节进行提取和净化,得到相应的空白绿茶/红茶基质溶液,将该溶液置于−20 ℃冰箱中保存,备用。
基质混合标准溶液1:用空白基质溶液将混合标准溶液稀释得到0.001、0.005、0.01、0.02、0.05、0.1、0.5、1、2、5、10 μg/L等系列质量浓度的基质混合标准工作溶液,用于确定方法检出限和定量限。
基质混合标准溶液2:用空白基质溶液将混合标准溶液逐级稀释得到质量浓度为1、5、10、20、50、100 μg/L的系列基质混合标准工作溶液,用于做标准工作曲线,即基质匹配校准曲线。
1.2.3 色谱条件
色谱柱:SHIMAZU Shim-pack Velox Biphenyl C18色谱柱(3 mm×50 mm,2.7 μm)。分别考察乙腈-水、甲醇-水、0.1%甲酸水溶液-甲醇、0.1%甲酸水溶液-甲醇(含2 mmol/L甲酸铵)、0.1%甲酸水溶液-甲醇(含5 mmol/L甲酸铵)四种流动相对14种农药检测结果的影响。流动相洗脱程序:0~0.01 min,5% B;0.01~1.0 min,5%~40% B;1.0~3.0 min,40%~85% B;3.0~4.5 min,85%~95% B;4.5~8.0 min,95% B;8.01~10 min,95%~5% B。进样体积设置为5 μL;流速设置为0.3 mL/min;色谱柱柱温35 ℃。
1.2.4 质谱条件
离子源:ESI离子源;将14种农药混合标准溶液通过针泵进样方式进行质谱方法调谐,在ESI+和ESI−模式下进行扫描,优化各化合物的质谱条件;检测方式:多反应监测模式(multiple reaction monitoring,MRM);离子源电压:5500 V;离子源温度:500 °C;气帘气:35 psi;雾化气:65 psi;辅助加热气:55 psi。
1.2.5 方法学考察
1.2.5.1 基质效应
茶叶的基质较复杂,可能存在基质抑制或基质增强效应。分别用厂家1复杂基质净化柱处理所得的空白绿茶基质和1%乙酸-乙腈提取溶剂配制浓度为50 μg/L的14种混合农药标准溶液,重复测定3次,考察14种农药在绿茶中的基质效应。
基质效应(Matrix effect,ME)按下式计算:
式中:ME表示基质效应,%;Amatrix表示基质混合标准溶液中目标分析物的峰面积(A,peak area);Aextraction表示提取溶剂混合标准溶液中目标分析物的峰面积。
1.2.5.2 方法的线性范围、检出限、定量限
采用基质匹配标准溶液建立标准曲线。按照1.2节描述配制质量浓度为1、5、10、20、50、100 μg/L的系列基质混合标准工作液,以各个农药的峰面积为纵坐标,相应的浓度为横坐标,获得目标物农药的线性回归方程,分别以信噪比(S/N)为3和10时对应的空白样品添加浓度为检出限(Limit of detection, LOD)和定量限(Limit of quantification, LOQ)。
1.2.5.3 回收率和精密度
分别在空白绿茶和红茶样品中添加低、中、高浓度(100、500、800 μg/kg)农药进行加标回收率试验,各浓度平行试验6次,计算平均回收率及测定结果的相对标准偏差(RSD)。
1.2.5.4 实际茶样品检测
利用本文方法对市售的30种茶叶进行检测,分析其中14种目标农药的残留浓度。
1.3 数据处理
分别利用Analyst 1.7和Sciex OS 1.7.0软件进行数据采集及处理,Origin 9.0进行数据分析。
2. 结果与分析
2.1 色谱、质谱条件优化
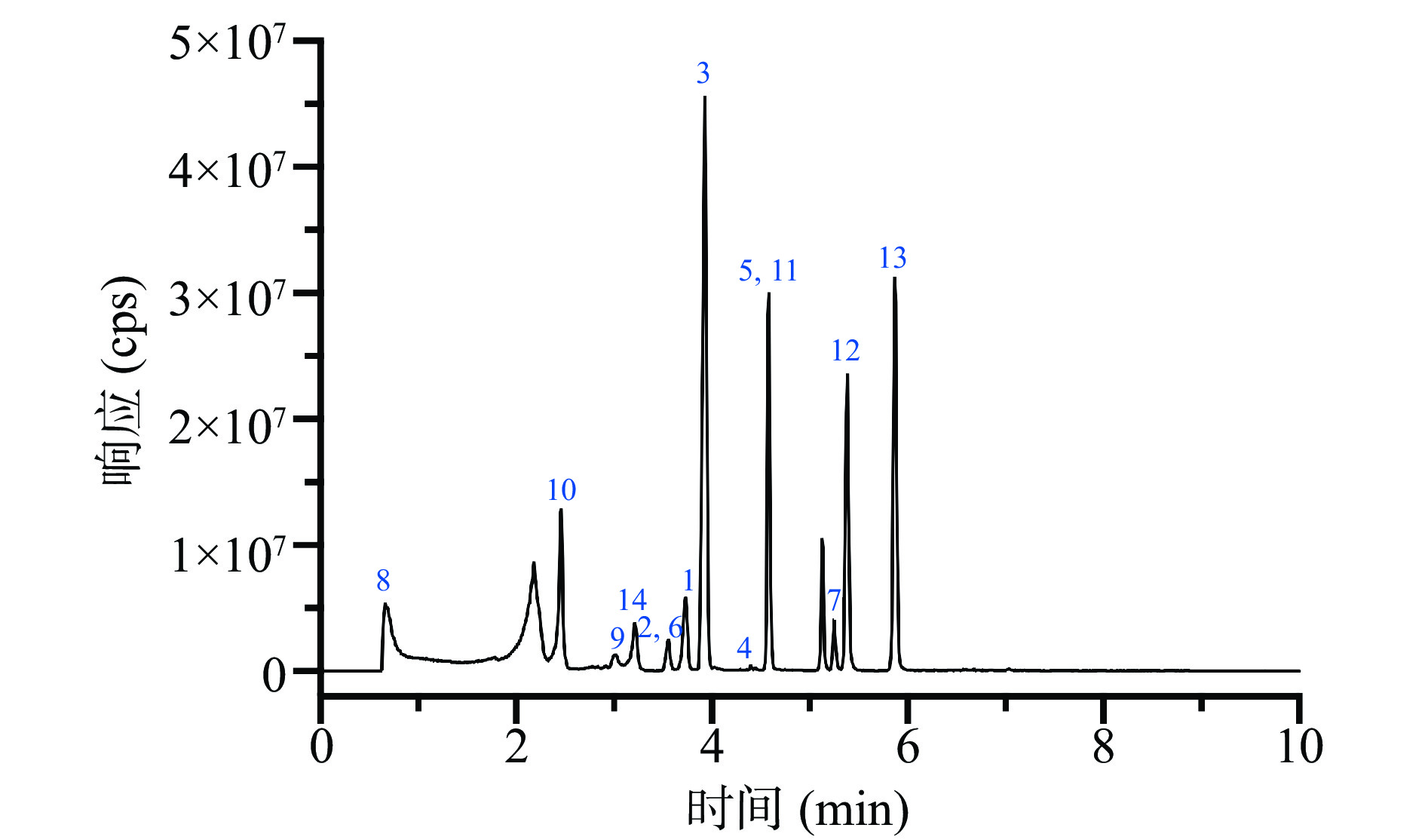
使用SHIMAZU Shim-pack Velox Biphenyl C18色谱柱(3 mm×50 mm,2.7 μm),设定流速为0.3 mL/min,分别考察了以乙腈-水、甲醇-水、0.1%甲酸水溶液-甲醇、0.1%甲酸水溶液-甲醇(含2 mmol/L甲酸铵)、0.1%甲酸水溶液-甲醇(含5 mmol/L甲酸铵)为流动相对14种农药检测结果的影响,梯度洗脱程序见1.2.3。结果表明,选用0.1%甲酸水溶液-甲醇(2 mmol/L甲酸铵)为流动相时,14种农药的响应值和峰形最好。14种农药的总离子流图见图1。
将14种农药的0.1 mg/L混合标准溶液通过针泵进样方式进行质谱方法调谐,在ESI+和ESI−模式下进行扫描。结果显示,14种农药的母离子均为[M+H]+模式。手动调谐优化14种农药母离子和子离子,选取两组灵敏度最佳的离子对作为定量离子对和定性离子对,获得最佳的碰撞电压和碰撞能量,最终得到MRM模式下14种农药优化的质谱采集参数如表2所示。
表 2 14种农药的质谱参数Table 2. MS parameters of the 14 pesticides编号 化合物名称 英文名称 母离子(m/z) 子离子(m/z) 去簇电压(V) 碰撞能量(eV) 1 啶虫脒 Acetamiprid 223 126* 65 28 223 99 65 60 2 涕灭威 Aldicarb 208 116* 20 11 208 89 20 25 3 克百威 Carbofuran 222.1 165* 70 16 222.1 123.1 70 29 4 内吸磷 Demeton 259 89* 48 22 259 61 48 45 5 灭线磷 Ethoprophos 243 97* 67 43 243 131 67 26 6 吡虫啉 Imidacloprid 256.1 175* 45 27 256.1 209 45 22 7 茚虫威 Indoxacarb 528.3 293* 57 18 528.3 249 57 23 8 甲胺磷 Methamidophos 142 94* 57 19 142 125 57 18 9 灭多威 Methomyl 163 88* 38 12 163 106 38 14 10 氧化乐果 Omethoate 214 182.9* 60 16 214 109 60 36 11 甲基对硫磷 Parathion-methyl 264 232* 78 21 264 125 78 26 12 硫环磷 Phosfolan 256.1 140* 40 30 256.1 228 40 18 13 丙溴磷 Profenofos 373 302.9* 80 25 373 345.2 80 18 14 噻虫嗪 Thiamethoxam 292 211* 30 16 292 181 30 30 注:*表示定量离子(Quantitative ion)。 2.2 提取方法选择
QuEChERS样品前处理主要由提取和净化两部分组成。在提取阶段,常用的提取溶剂有乙腈、丙酮、乙酸乙酯、甲醇、正己烷等。乙腈因最适宜于提取各种极性的农药残留,同时不会萃取出很多油性物质(如蜡、油性色素、脂肪等),且仅需加入盐便可实现与水相的分离,是目前使用最广泛的提取溶剂。研究表明,在乙腈中加入1%乙酸,并在盐析过程中加入MgSO4和缓冲盐CH3COONa可对绝大多数农药残留得到较高的回收率[23]。另外,对于含水量低的样品,通过先向样品中添加一定量的水,可弱化待分析物与样品基质之间的相互作用,使待分析物更易在萃取/分配过程中被充分提取[24]。
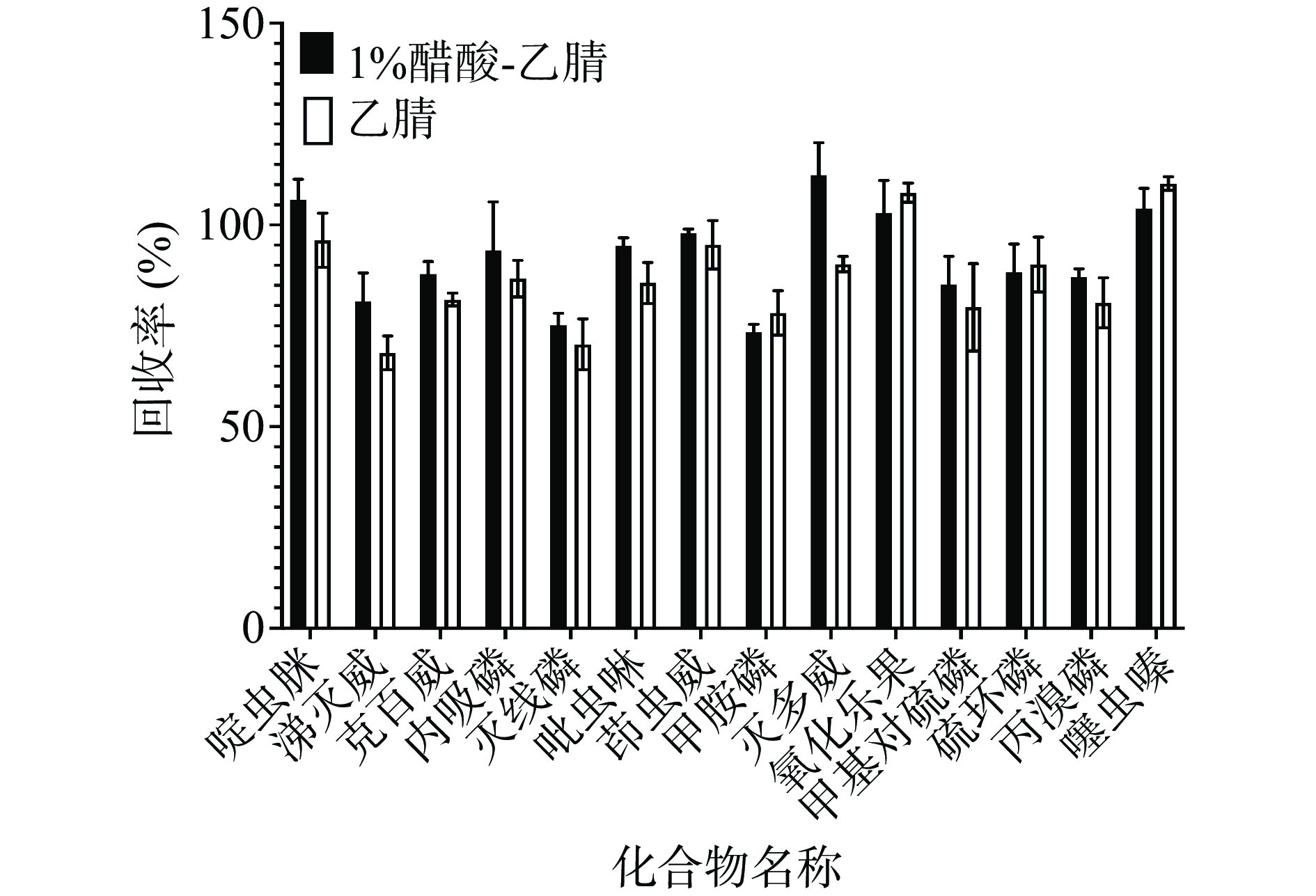
本研究首先向茶叶样品中加入适量水充分浸润,再分别使用乙腈及含1%乙酸的乙腈作为提取溶剂,震荡均匀后加入含6 g MgSO4和1.5 g CH3COONa的盐包,进行提取效果的比较,结果表明(图2),采用1%乙酸-乙腈作为提取溶剂时,其农药回收率高于乙腈作为提取溶剂,因此,本文选择1%乙酸-乙腈作为提取溶剂。
2.3 净化方式优化
茶叶样品基质复杂,其中的茶多酚、咖啡因、色素、有机酸等物质易和待测目标物共提取,干扰检测的准确性和灵敏度[6]。常见的净化剂有无水MgSO4、PSA、GCB和C18等。无水MgSO4能除去提取液的少量水分,PSA可有效去除脂肪酸、有机酸、一些极性色素和糖类,GCB能有效去除具有平面结构的甾醇和色素类杂质,C18吸附剂对油脂的去除效果十分明显[25]。另外,一些新型净化材料如多壁碳纳米管(MWCNTs)和石墨烯等因被证实能有效去除基质中色素类、糖类、氨基酸等干扰物,并在一定程度上改善GCB对部分平面结构化合物的吸附问题,也逐渐得到应用[26-27]。传统的净化方法是向提取液中加入一定量吸附剂,充分震荡使吸附剂与样品充分反应,最后离心去除吸附剂。为了使操作更加快速高效,本文使用将净化剂固相化的QuEChERS净化柱对提取液进行净化,省去震荡、涡旋和离心等步骤从而缩短了样品前处理时间。
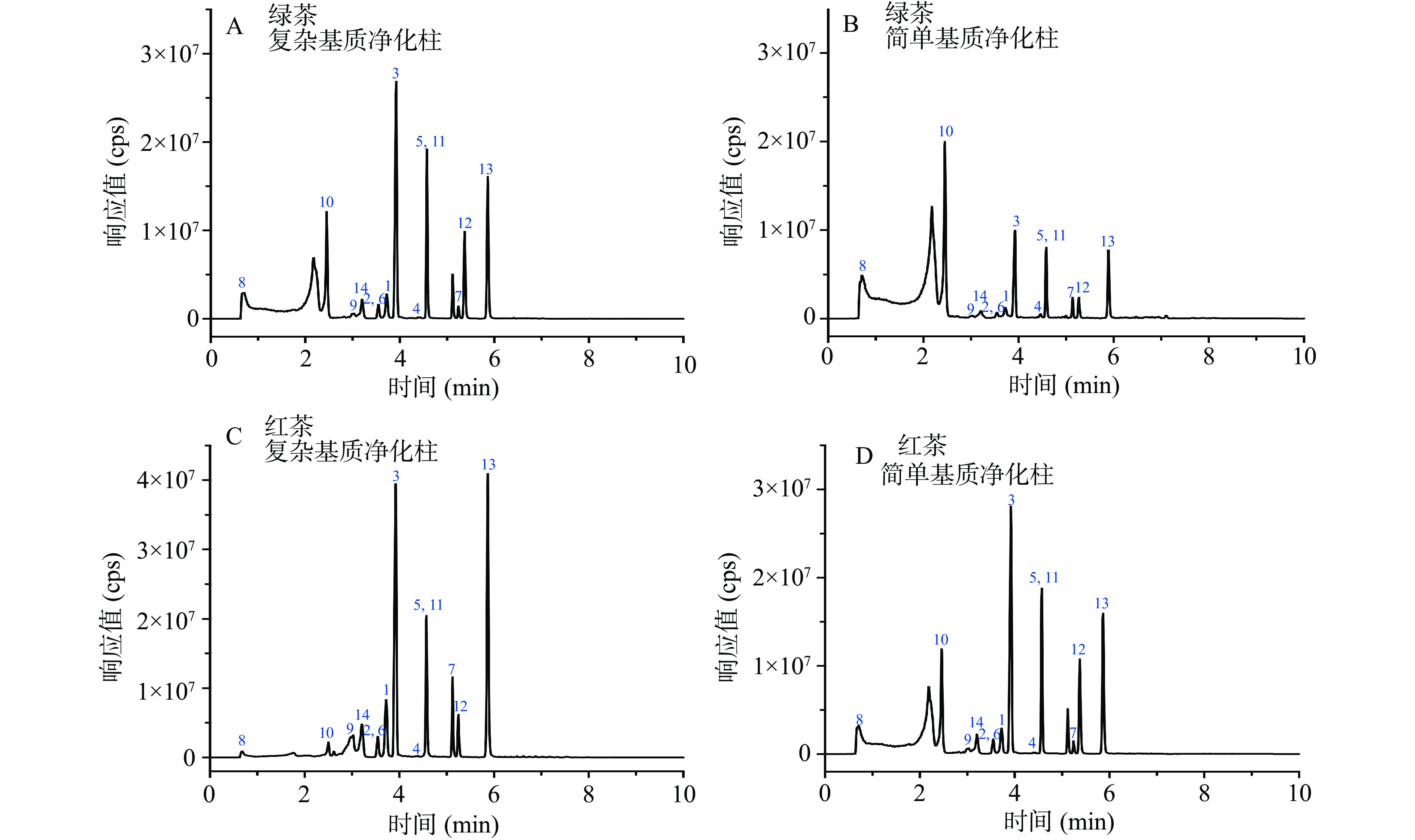
本文考察了在空白绿茶和红茶样品中添加800 μg/kg目标化合物,采用两个厂家四种商品化QuEChERS净化柱(成分及含量见表1)对茶叶提取液净化效果和农药回收率的影响。如图3所示,由茶叶提取液经不同净化柱净化后的颜色深浅可初步判断,复杂基质净化柱对于色素杂质的净化效果好于简单基质净化柱,这是因为复杂基质净化柱中的GCB或MWCNTs对色素有很好的吸附作用。根据图4可知,对于绿茶样品,厂家1简单基质净化柱对14种农药的回收率(56.3%~91.1%)整体低于厂家1复杂基质净化柱(73.4%~112.4%),且色谱图中杂峰较明显(见图5),可见含有GCB(5 mg)的复杂基质净化柱能有效吸附色素等杂质,降低提取液中高浓度杂质对目标分析物检测的影响;绿茶样品经厂家2简单基质净化柱处理后对14种农药回收率(42.7%~79.3%)和经厂家2茶叶专用柱净化后对14种农药回收率(52.7%~71.2%)整体低于厂家1净化柱,说明厂家2两种净化柱中较高含量的MWCNTs(分别为15和45 mg)对目标化合物产生了一定吸附从而导致回收率降低。对于红茶样品,采用四种净化柱处理后14种农药回收率整体高于绿茶样品,且净化后样品颜色比绿茶浅,说明绿茶和红茶在茶多酚、生物碱、色素等成分上的差异会影响净化效果和检测结果,在实际检测中应根据样品具体情况进行优化。
![]() 图 5 总离子流色谱图注:绿茶加标样品(800 μg/kg)经厂家1复杂基质(A)、简单基质(B)净化柱处理,红茶加标样品(800 μg/kg)经厂家1复杂基质(C)、简单基质(D)净化柱处理后提取液总离子流色谱图。编号1~14指代农药见表2。Figure 5. Total ion chromatograms (TIC)
图 5 总离子流色谱图注:绿茶加标样品(800 μg/kg)经厂家1复杂基质(A)、简单基质(B)净化柱处理,红茶加标样品(800 μg/kg)经厂家1复杂基质(C)、简单基质(D)净化柱处理后提取液总离子流色谱图。编号1~14指代农药见表2。Figure 5. Total ion chromatograms (TIC)综合考虑,本文使用净化效果和回收率都较好的厂家1复杂基质净化柱,进一步考察方法的基质效应、线性关系、回收率等,并对实际样品进行检测。
2.4 基质效应
茶叶中的茶多酚、生物碱、色素等易和目标物分析物共提取,难以通过净化全部去除,从而对目标分析物的离子化效率产生影响,即产生基质效应(Matrix effect,简称ME)[28-29]。我们分别用厂家1复杂基质净化柱处理所得的空白绿茶基质和1%乙酸-乙腈提取溶剂配制浓度为50 μg/L的14种混合农药标准溶液,重复测定3次,考察14种农药在绿茶中的基质效应。由表3可以看出,绿茶基质对14种农药的基质效应不同,10种农药ME>105%,为基质增强;2种农药ME<85%,为基质抑制;2种农药ME在85%~105%之间,表示无基质效应。因此,对茶叶农残检测,采用空白基质配制标准曲线进行定量分析以减弱基质效应的影响,提高定量结果的准确性。
表 3 14种农药的线性方程、决定系数、检出限、定量限、基质效应和最大残留限量Table 3. Linear equations, coefficient of determination (R2), LODs, LOQs, matrix effects and the maximum residue limits of 14 pesticides农药名称 英文名称 线性方程 R2 LOD(μg/L) LOQ(μg/L) 基质效应(%) 最大残留限量*(μg/kg) 啶虫脒 Acetamiprid y=1.51×105x+2.28×105 0.9989 0.010 0.030 96.6 10000 涕灭威 Aldicarb y=913.07x+244.27 0.9926 2.000 5.000 141.7 / 克百威 Carbofuran y=3.56×105x+1.15×105 0.9958 0.010 0.030 116.8 50 内吸磷 Demeton y=4113.33x+699.12 0.9971 0.300 1.000 198.9 50 灭线磷 Ethoprophos y=1.43×105x+2.96×104 0.9974 0.050 0.200 195.9 50 吡虫啉 Imidacloprid y=3.92×104x+7.29×104 0.9980 0.001 0.003 121.8 500 茚虫威 Indoxacarb y=2.82×104x+3.72×103 0.9982 0.300 1.000 122.6 5000 甲胺磷 Methamidophos y=2.52×104x-1.38×104 0.9962 1.000 3.000 143.1 50 灭多威 Methomyl y=1.21×104x-166.58 0.9982 0.300 1.000 74.4 200 氧化乐果 Omethoate y=1636.46x-517.30 0.9969 1.000 5.000 35.7 50 甲基对硫磷 Parathion-methyl y=3161.66x+986.90 0.9952 1.000 5.000 123.4 20 硫环磷 Phosfolan y=6.68×105x+1.75×105 0.9968 0.010 0.030 107.6 30 丙溴磷 Profenofos y=1.61×105x+9113.44 0.9981 0.100 0.500 162.4 500 噻虫嗪 Thiamethoxam y=3.61×104x+3.38×104 0.9985 0.050 0.200 91.9 10000 注:*参照GB 2763-2021《食品安全国家标准 食品中农药最大残留限量》。 2.5 线性关系、检出限、定量限
由表3可知,14种农药在相应的线性范围内线性关系良好,R2>0.99。以信噪比(S/N)为3和10时对应的空白样品添加浓度为检出限(Limit of detection, LOD)和定量限(Limit of quantification, LOQ),14种农药LOD在0.001~2.000 μg/L之间,LOQ为0.003~5.000 μg/L。根据GB 2763-2021《食品安全国家标准 食品中农药最大残留限量》,除涕灭威在茶叶中的最大残留量未做规定,其余13种农药的检出限和定量限均远低于规定的最大残留量,说明本文方法满足实际检测需求。
2.6 回收率和精密度
如表4所示,在向空白绿茶和红茶样品中添加低、中、高浓度(100、500、800 μg/kg)三个浓度水平下,方法的平均回收率为71.2%~117.4%,RSD为1.1%~14.2%,说明该方法对绿茶和红茶中14种农药残留检测的准确度和精密度良好,能够满足茶叶样品多农药残留分析的要求。
表 4 14种农药在绿茶和红茶中的加标回收率和相对标准偏差(n=6)Table 4. Recoveries and RSDs of the 14 pesticides spiked in green tea and black tea (n=6)农药名称 英文名称 绿茶 红茶 100 μg/kg 500 μg/kg 800 μg/kg 100 μg/kg 500 μg/kg 800 μg/kg 回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)啶虫脒 Acetamiprid 114.8 3.6 101.6 3.7 106.3 4.8 77.6 2.7 92.0 5.1 95.8 4.9 涕灭威 Aldicarb 93.7 9.5 81.1 8.9 81.1 7.2 88.0 13.8 87.4 4.3 99.3 7.4 克百威 Carbofuran 106.9 6.0 91.7 6.6 87.9 2.6 87.2 2.1 92.9 2.4 94.0 6.7 内吸磷 Demeton 97.0 12.4 89.2 14.1 93.9 12.3 68.9 9.0 73.5 9.1 81.7 14.2 灭线磷 Ethoprophos 80.0 5.3 74.5 5.4 75.1 1.1 82.0 1.3 85.3 1.5 87.1 6.5 吡虫啉 Imidacloprid 99.4 1.8 91.6 6.2 94.7 1.8 79.7 1.7 89.0 3.7 94.8 4.9 茚虫威 Indoxacarb 104.2 3.3 95.4 6.4 98.0 1.3 83.1 2.8 93.6 2.9 95.3 2.2 甲胺磷 Methamidophos 73.0 5.3 71.2 5.3 73.4 2.1 79.7 4.0 80.7 1.6 85.2 1.2 灭多威 Methomyl 114.4 1.9 104.3 9.6 112.3 7.5 82.8 3.4 95.2 3.2 100.4 3.1 氧化乐果 Omethoate 104.9 13.0 89.6 10.9 103.0 8.3 78.3 4.5 91.6 4.2 97.4 1.4 甲基对硫磷 Parathion-methyl 83.2 7.0 80.2 10.8 85.2 6.8 91.1 5.7 44.6 7.4 72.6 13.0 硫环磷 Phosfolan 107.3 2.0 90.4 4.5 88.3 5.6 86.6 2.7 93.2 3.1 95.4 5.8 丙溴磷 Profenofos 91.9 2.9 83.1 6.8 87.1 2.4 80.0 2.9 84.2 1.9 85.7 2.4 噻虫嗪 Thiamethoxam 117.4 10.4 99.7 4.4 104.1 4.5 83.2 3.1 96.2 5.8 101.1 2.0 2.7 实际样品检测
利用本文方法对市售的30种茶叶进行检测,如表5所示,有6种茶叶检出目标农药,其中5种茶叶检出啶虫脒,残留量为2.4~14.1 μg/kg;2种茶叶检出克百威,残留量分别为1.9、23.0 μg/kg;2种茶叶检出吡虫啉,残留量分别为1.9、33.7 μg/kg;1种茶叶检出茚虫威,残留量为3.0 μg/kg;1种茶叶检出噻虫嗪,残留量为2.4 μg/kg。上述茶叶中农药残留均未超过国家标准GB 2763-2021规定的最大残留限量值。
表 5 6种检出目标农药的茶叶中农药残留浓度(μg/kg)Table 5. Concentration of targeted pesticides detected in six tea samples目标农药 狮峰龙井 竹叶青 采花毛尖 武夷山红茶 茉莉花茶 祁门红茶 啶虫脒 14.1 8.6 2.4 ND 7.1 3.3 克百威 ND 23.0 1.9 ND ND ND 吡虫啉 1.9 33.7 ND ND ND ND 茚虫威 ND ND ND ND 3.0 ND 噻虫嗪 ND ND ND 2.4 ND ND *注:ND(not detected)表示未检出。 3. 结论
本文采用QuEChERS前处理方法结合UPLC-MS/MS技术,建立了茶叶中啶虫脒、涕灭威、克百威、内吸磷、灭线磷、吡虫啉、茚虫威、甲胺磷、灭多威、氧化乐果、甲基对硫磷、硫环磷、丙溴磷、噻虫嗪等14种农药残留的快速检测方法。通过优化提取液组分、QuEChERS净化柱种类等,14种农药的LOQ可达到0.003~5.000 μg/L,在3个添加水平下的回收率为71.2%~117.4%,能够满足茶叶农药残留限量指标的快速检测要求。对30种市售茶叶样品进行检测,其中6种茶叶检出目标农药,测得农药残留浓度均未超过国家限量标准。本文方法具有操作简便快捷、净化效果好、灵敏度和准确率高等优点,为高效和准确地评价茶叶的质量安全提供了新的参考。
-
图 5 总离子流色谱图
注:绿茶加标样品(800 μg/kg)经厂家1复杂基质(A)、简单基质(B)净化柱处理,红茶加标样品(800 μg/kg)经厂家1复杂基质(C)、简单基质(D)净化柱处理后提取液总离子流色谱图。编号1~14指代农药见表2。
Figure 5. Total ion chromatograms (TIC)
表 1 4种QuEChERS净化柱型号、成分及使用方法
Table 1 Model, component and usage of four kinds of QuEChERS purification columns
生产厂家 净化柱名称 型号 成分 净化方法 天津阿尔塔
科技有限公司简单基质
针式过滤器F-QuEChERS-AOAC 3201 150 mg MgSO4
50 mg PSA在过滤器注射器端连接0.22 μm尼龙微孔滤膜,
从加样端注入1 mL前处理上清液,然后使用
柱塞杆施加正压过滤,即得待测液复杂基质
针式过滤器F-QuEChERS-AOAC 3203 150 mg MgSO4
50 mg PSA
50 mg C18
5 mg GCB北京绿绵
科技有限公司简单基质
净化柱LM806-FC-721 150 mg MgSO4
15 mg PSA
15 mg多壁碳纳米管将净化柱塞入50 mL离心管中,缓慢按压,
离心管中上层提取液经过净化柱内的阻水滤片
及填料净化后进入储液槽。取1 mL储液过
0.22 μm尼龙微孔滤膜,即得待测液茶叶专用
净化柱LM806-FC-722 120 mg MgSO4
45 mg PSA
45 mg多壁碳纳米管表 2 14种农药的质谱参数
Table 2 MS parameters of the 14 pesticides
编号 化合物名称 英文名称 母离子(m/z) 子离子(m/z) 去簇电压(V) 碰撞能量(eV) 1 啶虫脒 Acetamiprid 223 126* 65 28 223 99 65 60 2 涕灭威 Aldicarb 208 116* 20 11 208 89 20 25 3 克百威 Carbofuran 222.1 165* 70 16 222.1 123.1 70 29 4 内吸磷 Demeton 259 89* 48 22 259 61 48 45 5 灭线磷 Ethoprophos 243 97* 67 43 243 131 67 26 6 吡虫啉 Imidacloprid 256.1 175* 45 27 256.1 209 45 22 7 茚虫威 Indoxacarb 528.3 293* 57 18 528.3 249 57 23 8 甲胺磷 Methamidophos 142 94* 57 19 142 125 57 18 9 灭多威 Methomyl 163 88* 38 12 163 106 38 14 10 氧化乐果 Omethoate 214 182.9* 60 16 214 109 60 36 11 甲基对硫磷 Parathion-methyl 264 232* 78 21 264 125 78 26 12 硫环磷 Phosfolan 256.1 140* 40 30 256.1 228 40 18 13 丙溴磷 Profenofos 373 302.9* 80 25 373 345.2 80 18 14 噻虫嗪 Thiamethoxam 292 211* 30 16 292 181 30 30 注:*表示定量离子(Quantitative ion)。 表 3 14种农药的线性方程、决定系数、检出限、定量限、基质效应和最大残留限量
Table 3 Linear equations, coefficient of determination (R2), LODs, LOQs, matrix effects and the maximum residue limits of 14 pesticides
农药名称 英文名称 线性方程 R2 LOD(μg/L) LOQ(μg/L) 基质效应(%) 最大残留限量*(μg/kg) 啶虫脒 Acetamiprid y=1.51×105x+2.28×105 0.9989 0.010 0.030 96.6 10000 涕灭威 Aldicarb y=913.07x+244.27 0.9926 2.000 5.000 141.7 / 克百威 Carbofuran y=3.56×105x+1.15×105 0.9958 0.010 0.030 116.8 50 内吸磷 Demeton y=4113.33x+699.12 0.9971 0.300 1.000 198.9 50 灭线磷 Ethoprophos y=1.43×105x+2.96×104 0.9974 0.050 0.200 195.9 50 吡虫啉 Imidacloprid y=3.92×104x+7.29×104 0.9980 0.001 0.003 121.8 500 茚虫威 Indoxacarb y=2.82×104x+3.72×103 0.9982 0.300 1.000 122.6 5000 甲胺磷 Methamidophos y=2.52×104x-1.38×104 0.9962 1.000 3.000 143.1 50 灭多威 Methomyl y=1.21×104x-166.58 0.9982 0.300 1.000 74.4 200 氧化乐果 Omethoate y=1636.46x-517.30 0.9969 1.000 5.000 35.7 50 甲基对硫磷 Parathion-methyl y=3161.66x+986.90 0.9952 1.000 5.000 123.4 20 硫环磷 Phosfolan y=6.68×105x+1.75×105 0.9968 0.010 0.030 107.6 30 丙溴磷 Profenofos y=1.61×105x+9113.44 0.9981 0.100 0.500 162.4 500 噻虫嗪 Thiamethoxam y=3.61×104x+3.38×104 0.9985 0.050 0.200 91.9 10000 注:*参照GB 2763-2021《食品安全国家标准 食品中农药最大残留限量》。 表 4 14种农药在绿茶和红茶中的加标回收率和相对标准偏差(n=6)
Table 4 Recoveries and RSDs of the 14 pesticides spiked in green tea and black tea (n=6)
农药名称 英文名称 绿茶 红茶 100 μg/kg 500 μg/kg 800 μg/kg 100 μg/kg 500 μg/kg 800 μg/kg 回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)啶虫脒 Acetamiprid 114.8 3.6 101.6 3.7 106.3 4.8 77.6 2.7 92.0 5.1 95.8 4.9 涕灭威 Aldicarb 93.7 9.5 81.1 8.9 81.1 7.2 88.0 13.8 87.4 4.3 99.3 7.4 克百威 Carbofuran 106.9 6.0 91.7 6.6 87.9 2.6 87.2 2.1 92.9 2.4 94.0 6.7 内吸磷 Demeton 97.0 12.4 89.2 14.1 93.9 12.3 68.9 9.0 73.5 9.1 81.7 14.2 灭线磷 Ethoprophos 80.0 5.3 74.5 5.4 75.1 1.1 82.0 1.3 85.3 1.5 87.1 6.5 吡虫啉 Imidacloprid 99.4 1.8 91.6 6.2 94.7 1.8 79.7 1.7 89.0 3.7 94.8 4.9 茚虫威 Indoxacarb 104.2 3.3 95.4 6.4 98.0 1.3 83.1 2.8 93.6 2.9 95.3 2.2 甲胺磷 Methamidophos 73.0 5.3 71.2 5.3 73.4 2.1 79.7 4.0 80.7 1.6 85.2 1.2 灭多威 Methomyl 114.4 1.9 104.3 9.6 112.3 7.5 82.8 3.4 95.2 3.2 100.4 3.1 氧化乐果 Omethoate 104.9 13.0 89.6 10.9 103.0 8.3 78.3 4.5 91.6 4.2 97.4 1.4 甲基对硫磷 Parathion-methyl 83.2 7.0 80.2 10.8 85.2 6.8 91.1 5.7 44.6 7.4 72.6 13.0 硫环磷 Phosfolan 107.3 2.0 90.4 4.5 88.3 5.6 86.6 2.7 93.2 3.1 95.4 5.8 丙溴磷 Profenofos 91.9 2.9 83.1 6.8 87.1 2.4 80.0 2.9 84.2 1.9 85.7 2.4 噻虫嗪 Thiamethoxam 117.4 10.4 99.7 4.4 104.1 4.5 83.2 3.1 96.2 5.8 101.1 2.0 表 5 6种检出目标农药的茶叶中农药残留浓度(μg/kg)
Table 5 Concentration of targeted pesticides detected in six tea samples
目标农药 狮峰龙井 竹叶青 采花毛尖 武夷山红茶 茉莉花茶 祁门红茶 啶虫脒 14.1 8.6 2.4 ND 7.1 3.3 克百威 ND 23.0 1.9 ND ND ND 吡虫啉 1.9 33.7 ND ND ND ND 茚虫威 ND ND ND ND 3.0 ND 噻虫嗪 ND ND ND 2.4 ND ND *注:ND(not detected)表示未检出。 -
[1] 丁亦男, 童小麟, 赖国银, 等. 国内外茶叶农药残留限量标准与出口茶叶安全研究[J]. 食品安全质量检测学报,2019,10(23):8140−8145. [DING Y N, TONG X L, LAI G Y, et al. Study on the limit standard of pesticide residue of tea and the safety of exported tea at home and abroad[J]. Journal of Food Safety & Quality,2019,10(23):8140−8145. DING Y N, TONG X L, LAI G Y, et al. Study on the limit standard of pesticide residue of tea and the safety of exported tea at home and abroad[J]. Journal of Food Safety & Quality, 2019, 10(23): 8140-8145.
[2] HAZARIKA L K, BHUYAN M, HAZARIKA B N. Insect pests of tea and their management[J]. Annual Review of Entomology,2009,54:267−284. doi: 10.1146/annurev.ento.53.103106.093359
[3] 国家卫生健康委员会, 国家市场监督管理总局, 农业农村部. 食品安全国家标准 食品中农药最大残留限量: GB 2763-2021[S]. 北京: 中国农业出版社, 2021. State Health Commission, State Market Supervision and Administration, Ministry of Agriculture and Rural Areas. National food safety standard-maximum residue limits for pesticides in food: GB 2763-2021[S]. Beijing: China Agriculture Press, 2021.
[4] 王金鑫. 基于欧盟官网通报不合格茶叶信息分析茶叶农残现状及应对措施[J]. 中国茶叶,2018,40(1):37−39. [WANG J X. Analysis of the status of tea pesticide residues and countermeasures based on the information of unqualified tea notified on the EU official website[J]. China Tea,2018,40(1):37−39. doi: 10.3969/j.issn.1000-3150.2018.01.010 WANG J X. Analysis of the status of tea pesticide residues and countermeasures based on the information of unqualified tea notified on the EU official website[J]. China Tea, 2018, 40(1): 37-39. doi: 10.3969/j.issn.1000-3150.2018.01.010
[5] 伊鋆, 杨明, 聂懿, 等. 市售茶叶中30种农药残留与风险评估[J]. 现代食品科技,2019,35(4):256−263. [YI Y, YANG M, NIE Y, et al. Monitoring and risk assessment of 30 kinds of pesticide residues in tea samples[J]. Modern Food Science and Technology,2019,35(4):256−263. YI Y, YANG M, NIE Y, et al. Monitoring and risk assessment of 30 kinds of pesticide residues in tea samples[J]. Modern Food Science and Technology, 2019, 35(4): 256-263.
[6] HUANG Y S, SHI T, LUO X, et al. Determination of multi-pesticide residues in green tea with a modified QuEChERS protocol coupled to HPLC-MS/MS[J]. Food Chemistry,2019,275:255−264. doi: 10.1016/j.foodchem.2018.09.094
[7] GAO Y X, CHEN P H, NIE D D. Determination of 53 pesticide residues in tea by gas chromatography-tandem mass spectrometry and double internal standard method[J]. Chinese Journal of Chromatography,2018,36(6):531−540.
[8] LI Y, WANG Z B, GAO F M, et al. Selection of representative matrices for the multiresidue analysis of pesticides in tea by GC-MS/MS[J]. Analytical Methods,2018,10(8):855−866. doi: 10.1039/C7AY02773G
[9] 李俊芳, 景伟文, 李德强, 等. 分散固相萃取-超高效液相色谱-串联高分辨质谱法测定新疆苹果中7种农药残留[J]. 食品科学,2018,39(8):295−301. [LI J F, JING W W, LI D Q, et al. Determination of 7 pesticide residues in Xinjiang grown apple by dispersive solid-phase extraction combined with ultra performance liquid chromatography-high resolution tandem mass spectrometry[J]. Food Science,2018,39(8):295−301. doi: 10.7506/spkx1002-6630-201808046 LI J F, JING W W, LI D Q, et al. Determination of 7 pesticide residues in Xinjiang grown apple by dispersive solid-phase extraction combined with ultra performance liquid chromatography-high resolution tandem mass spectrometry[J]. Food Science, 2018, 39(8): 295-301. doi: 10.7506/spkx1002-6630-201808046
[10] SUN R, YANG W Q, LI Y X, et al. Multi-residue analytical methods for pesticides in teas: A review[J]. European Food Research and Technology,2021,247:1839−1858. doi: 10.1007/s00217-021-03765-3
[11] 杨梅, 汪俭, 孙思, 等. 超高效液相色谱法-串联质谱法快速测定绿茶中56种农药残留[J]. 食品研究与开发,2018,39(16):134−139. [YANG M, WANG J, SUN S, et al. Determination of 56 pesticide residues in green tea by UPLC-MS/MS[J]. Food Research and Development,2018,39(16):134−139. doi: 10.3969/j.issn.1005-6521.2018.16.025 YANG M, WANG J, SUN S, et al. Determination of 56 pesticide residues in green tea by UPLC-MS/MS[J]. Food Research and Development, 2018, 39(16): 134-139. doi: 10.3969/j.issn.1005-6521.2018.16.025
[12] HUO F F, TANG H, WU X, et al. Utilizing a novel sorbent in the solid phase extraction for simultaneous determination of 15 pesticide residues in green tea by GC/MS[J]. Journal of Chromatography B,2016,1023:44−54.
[13] 曾艳, 郎红, 杨巧慧, 等. 固相萃取-GC/LC-MS/MS测定茶叶中79种农药残留[J]. 茶叶科学,2019,39(5):576−586. [ZENG Y, LANG H, YANG Q H, et al. Determination of 79 pesticide residues in tea by solid phase extraction with GC-MS/MS and LC-MS/MS[J]. Journal of Tea Science,2019,39(5):576−586. doi: 10.3969/j.issn.1000-369X.2019.05.010 ZENG Y, LANG H, YANG Q H, et al. Determination of 79 pesticide residues in tea by solid phase extraction with GC-MS/MS and LC-MS/MS[J]. Journal of Tea Science, 2019, 39(5): 576-586. doi: 10.3969/j.issn.1000-369X.2019.05.010
[14] MOINFAR S, HOSSEINI M. Development of dispersive liquid-liquid microextraction method for the analysis of organophosphorus pesticides in tea[J]. Journal of Hazardous Materials,2009,169(1-3):907−911. doi: 10.1016/j.jhazmat.2009.04.030
[15] WANG F Q, LI S H, FENG H, et al. An enhanced sensitivity and cleanup strategy for the nontargeted screening and targeted determination of pesticides in tea using modified dispersive solid-phase extraction and cold-induced acetonitrile aqueous two-phase systems coupled with liquid chromatography-high resolution mass spectrometry[J]. Food Chemistry,2019,275:530−538. doi: 10.1016/j.foodchem.2018.09.142
[16] ANASTASSIADES M, LEHOTAY S J, STAJNBAHER D, et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and “dispersive solid-phase extraction” for the determination of pesticide residues in produce[J]. Journal of Aoac International,2003,86(2):412−431. doi: 10.1093/jaoac/86.2.412
[17] MARTINEZ-PIERNAS A B, PLAZA-BOLANOS P, GILABERT A, et al. Application of a fast and sensitive method for the determination of contaminants of emerging concern in wastewater using a quick, easy, cheap, effective, rugged and safe-based extraction and liquid chromatography coupled to mass spectrometry[J]. Journal of Chromatography A,2021,1653:12.
[18] SONG L, HAN Y T, YANG J, et al. Rapid single-step cleanup method for analyzing 47 pesticide residues in pepper, chili peppers and its sauce product by high performance liquid and gas chromatography-tandem mass spectrometry[J]. Food Chemistry,2019,279:237−245. doi: 10.1016/j.foodchem.2018.12.017
[19] 邓慧芬, 张建莹, 黄科, 等. QuEChERS-液相色谱-串联质谱法测定蔬菜中105种农药残留[J]. 色谱,2018,36(12):1211−1222. [DENG H F, ZHANG J Y, HUANG K, et al. Determination of 105 pesticide residues in vegetables by QuEChERS-liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Chromatography,2018,36(12):1211−1222. doi: 10.3724/SP.J.1123.2018.09012 DENG H F, ZHANG J Y, HUANG K, et al. Determination of 105 pesticide residues in vegetables by QuEChERS-liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Chromatography, 2018, 36(12): 1211-1222. doi: 10.3724/SP.J.1123.2018.09012
[20] 刘炎, 欧阳迪庆, 叶玉凤, 等. QuEChERS结合超高效液相色谱-串联质谱法同时测定番茄中噻虫嗪、噻虫胺、螺虫乙酯及其代谢物残留[J]. 分析测试学报,2017,36(12):1431−1438. [LIU Y, OUYANG D Q, YE Y F, et al. Analysis of thiamethoxam, clothianidin and spirotetramat and their metabolites residues in tomato using QuEChERS method with ultra performance liquid chromatography-mass spectrometry[J]. Journal of Instrumental Analysis,2017,36(12):1431−1438. doi: 10.3969/j.issn.1004-4957.2017.12.003 LIU Y, OUYANG D Q, YE Y F, et al. Analysis of thiamethoxam, clothianidin and spirotetramat and their metabolites residues in tomato using QuEChERS method with ultra performance liquid chromatography-mass spectrometry[J]. Journal of Instrumental Analysis, 2017, 36(12): 1431-1438. doi: 10.3969/j.issn.1004-4957.2017.12.003
[21] 杨路平, 邵立君, 王国玲, 等. QuEChERS结合液相色谱-串联质谱法测定食用菌中13种农药残留[J]. 食品工业科技,2019,40(14):247−253. [YANG L P, SHAO L J, WANG G L, et al. Determination of thirteen pesticides in edible mushrooms by QuEChERS with UPLC MS/MS[J]. Science and Technology of Food Industry,2019,40(14):247−253. YANG L P, SHAO L J, WANG G L, et al. Determination of thirteen pesticides in edible mushrooms by QuEChERS with UPLC MS/MS[J]. Science and Technology of Food Industry, 2019, 40(14): 247-253.
[22] MIAO S, LI W, CHEN M, et al. Simultaneous determination of 508 pesticide residues in Panax notoginseng by liquid chromatography-tandem mass spectrometry[J]. Journal of Instrumental Analysis,2019,38(7):761−774.
[23] Pesticide residues in foods by acetonitrile extraction and partitioning with magnesium sulfate-gas chromatography/mass spectrometry and liquid chromatography/tandem mass spectrometry. Association of analytical communities AOAC official method 2007.01, first action 2007. 2007 AOAC INTERNATIONAL.
[24] WIEST L, BULETE A, GIROUD B, et al. Multi-residue analysis of 80 environmental contaminants in honeys, honeybees and pollens by one extraction procedure followed by liquid and gas chromatography coupled with mass spectrometric detection[J]. Journal of Chromatography A,2011,1218(34):5743−5756. doi: 10.1016/j.chroma.2011.06.079
[25] WIILKOWSKA A, BIZIUK M. Determination of pesticide residues in food matrices using the QuEChERS methodology[J]. Food Chemistry,2011,125(3):803−812. doi: 10.1016/j.foodchem.2010.09.094
[26] WANG J, DUAN H L, FAN L, et al. A magnetic fluorinated multi-walled carbon nanotubes-based QuEChERS method for organophosphorus pesticide residues analysis in Lycium ruthenicum Murr[J]. Food Chemistry,2021,338:5.
[27] LUO Y B, LI X, JIANG X Y, et al. Magnetic graphene as modified quick, easy, cheap, effective, rugged and safe adsorbent for the determination of organochlorine pesticide residues in tobacco[J]. Journal of Chromatography A,2015,1406:1−9. doi: 10.1016/j.chroma.2015.05.066
[28] 张新忠, 罗逢健, 陈宗懋, 等. 超高效液相色谱串联质谱法测定茶叶、茶汤和土壤中氟环唑、茚虫威和苯醚甲环唑残留[J]. 分析化学,2013,41(2):215−222. [ZHANG X Z, LUO F J, CHEN Z M, et al. Residue determination of epoxiconazole, indoxacarb and difenoconazole in tea, tea infusion and soil using ultra high-performance liquid chromatography coupled with tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry,2013,41(2):215−222. ZHANG X Z, LUO F J, CHEN Z M, et al. Residue determination of epoxiconazole, indoxacarb and difenoconazole in tea, tea infusion and soil using ultra high-performance liquid chromatography coupled with tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2013, 41(2): 215-222.
[29] 李淑娟, 于杰, 高玉生, 等. HPLC-MSMS测定果蔬中有机磷类农药的基质效应[J]. 食品工业科技,2017,38(6):49−53. [LI S J, YU J, GAO Y S, et al. Matrix effect of multiple organophosphorus pesticide residues detection in fruits and vegetables by HPLC-MSMS[J]. Science and Technology of Food Industry,2017,38(6):49−53. LI S J, YU J, GAO Y S, et al. Matrix effect of multiple organophosphorus pesticide residues detection in fruits and vegetables by HPLC-MSMS[J]. Science and Technology of Food Industry, 2017, 38(6): 49-53.
-
期刊类型引用(3)
1. 侯丽慧,王乐,张宇,韩文静,李旭辰,司云珊,于秀华. 一测多评法测定冰川滴丸中6个个成成分分含含量. 中国药业. 2024(10): 76-80 .  百度学术
百度学术
2. 庞敏. 线叶金雀花茶中矿物质元素含量测定及饮用安全性分析. 食品与发酵科技. 2024(05): 137-142+171 .  百度学术
百度学术
3. 张毅. 一测多评法测定胃乃安胶囊中4种异黄酮成分含量. 实用中医内科杂志. 2022(07): 42-44 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:



 下载:
下载:



