Effect of Incubation Conditions on the Protease Activity and Protein Property of Wheat Germ
-
摘要: 以脱脂小麦麦胚为原料,经微波辅助处理(600 W,10 s)后,通过改变培育温度、培育时间、培育液pH、培育液液料比,提高麦胚中内源性蛋白酶的活力,达到富集多肽的目的。研究结果表明,温度、时间、pH、液料比对麦胚中蛋白酶活力、肽含量皆有显著影响(P<0.05)。采用Box-Behnken设计对上述单因素进行响应面优化试验,发现培育温度50 ℃、培育时间6 h、培育液pH4.5和液料比10:1 mL/g为最优组合,蛋白酶活力、肽含量分别为3812.34 U/g、303.12 mg/g。实验表明,优化培育条件能够有效提高经脱脂、微波处理麦胚中蛋白酶活力及肽含量。Abstract: Degreased wheat germ, after microwave treatment (600 W, 10 s), was incubated by different conditions for enhancing the activity of its endogenous proteases and increasing the level of polypeptides, including the incubation temperature and time, pH value of incubation solutions and ratio of the solution volume to the wheat germ weight. The results showed that enzymatic activities and polypeptides contents were both significantly affected by the temperature and time, pH value and ratio (P<0.05). A response surface optimization experiment was then conducted by using a Box-Behnken assay, revealing that the highest protease activity and polypeptide level, 3812.34 U/g and 303.12 mg/g, were obtained by a combination of the incubation temperature of 50 ℃ and duration of 6 h, pH of 4.5 and ration of 10:1 mL/g. These results revealed that optimization of culture conditions of wheat germ after degreasing and microwave treatments could effectively enhance the protease activity and polypeptide amount.
-
Keywords:
- wheat germ /
- endogenous protease /
- incubation /
- protease activity /
- polypeptide content
-
小麦(Triticum aestivum)是世界上最早、最广泛栽培的粮食作物,全球约有35%~40%的人口以小麦为主食[1]。我国小麦的年产值为1.1亿吨,可产生麦胚约300万吨[2]。小麦籽粒主要由皮层、糊粉层、胚乳和胚芽四个部分组成,胚芽是营养价值最丰富的部分,占籽粒重量的1.5%~2.9%。麦胚富含碳水化合物(约53%,包括蔗糖、棉子糖、果糖和葡萄糖)、蛋白质(27.0%~30.5%)、脂肪(10%~15%)、纤维素(1.5%~4.5%)、钙、钾、镁等矿物质元素(4%)和少量维生素[3-5]。目前,利用生物技术深入加工麦胚,并研发功能性食品是研究热点,该方法既健康、环保又经济、高效[6-7]。
麦胚经过培育,多种内源性酶被激活、释放,从原来的结合状态逐渐变成了游离状态,从而促使麦胚内部发生多种生理生化反应[8]。在酶活化的过程中,蛋白酶的活化往往第一个进行。研究人员发现,麦胚中蛋白酶降解蛋白质产生的多肽具有明显的生物活性,如降血压、抗氧化活性、抗癌、降低胆固醇、抗疲劳等[9-11]。目前,已有诸多研究者报道,适度改变麦胚的培育条件,如温度、时间、pH、液料比,能够提高麦胚蛋白酶活力,达到富集功能性多肽的作用。杨润强等[12]通过响应面优化麦胚培育条件,发现时间6 h、温度49 ℃、培育液中pH3.00及液料比10:1为最优培育组合,此时麦胚中多肽含量达到88.46 mg/g,是原料麦胚的2.98倍。同样的,胡立明等[8]提出,时间4.31 h、温度45 ℃、pH4.39、液料比为30:1时,麦胚中肽含量进一步提高,达到169.04 mg/g。余南静等[13]探究了金属离子对麦胚中蛋白酶活力、多肽含量的影响,指出ZnSO4(0.60 mmol/L)、MnSO4(2.00 mmol/L)和CaCl2(1.41 mmol/L)对蛋白酶活力具有显著的正效应,酶活力达到385.44 U/g,多肽含量达到49.35 mg/g。通过优化培育条件激活麦胚内源性蛋白酶、提高肽含量的方式,仍表现出肽含量较低的缺点,限制了其应用。
近年来,物理加工方法,如微波[14]、超声波[15-17]、超临界萃取[18]等技术,可有效增强农产品的功能特性,扩大其应用范围,逐渐成为了农产品加工业发展的助推器。其中,微波技术因具有高效、节能、操作简便的优点,被广泛开发利用。王振斌等[19]研究得出,微波预处理(功率为1.33 W/mL,时间为5 min)辅助碱性蛋白酶酶解芝麻饼粕,是一种制备血管紧张素转化酶(ACE)抑制肽快速高效的方法,半数抑制剂浓度IC50值为2.81 mg/mL。微波辅助碱提可显著增大麦胚蛋白的提取率,并提高麦胚蛋白的持水/持油性、乳化性和起泡性[20]。从艳霞等[21]采用微波对压榨前的菜籽进行处理,发现菜籽油中多酚含量提高了近120倍,植物甾醇、维生素E的含量也有明显提升。微波技术在农产品加工业中发挥作用的机制主要来源于其对物料组成成分产生的热效应与非热效应。因此,将微波技术应用于麦胚培育具有研究意义。
本研究以脱脂的麦胚为原料,首先进行微波(600 W,10 s)辅助处理,然后在单因素实验基础上,利用响应面试验优化麦胚的培育条件,以提高麦胚内源性蛋白酶的活力、达到进一步提高麦胚中肽含量的目的。本文旨在为开发麦胚多肽富集产品提供新策略,从而促进功能性保健食品的开发和应用、提高麦胚资源的利用率。
1. 材料与方法
1.1 材料与仪器
小麦麦胚 丹阳市莲湖面粉有限公司;谷胱甘肽、β-疏基乙醇、酪蛋白 上海麦克林生化科技有限公司;酪氨酸、硫酸铜、酒石酸钾钠、乙二胺四乙酸、三氯乙酸、一水合柠檬酸、二水合柠檬酸三钠、氢氧化钠、磷酸氢二钠、次氯酸钠、正己烷 分析纯,国药集团化学试剂有限公司。
HWS-26型电热恒温水浴锅、DHG-9070型电热鼓风干燥箱 上海一恒科学仪器有限公司;5424-R型高速冷冻离心机 上海土森视觉科技有限公司;PHS-25型pH测试仪 上海仪电科学仪器股份有限公司;U-T3型紫外可见分光光度计 上海屹谱仪器制造有限公司;BSA124S电子分析天平 常州市幸运电子设备有限公司;ZW-bp120型变频实验微波炉 芜湖众维教研仪器研发有限公司;Vortex-m型旋涡混匀仪 上海沪析实业有限公司。
1.2 实验方法
1.2.1 麦胚脱脂处理
称取50 g麦胚原料,边搅拌边缓慢加入500 mL正己烷,25 ℃下恒温振荡12 h,离心(4000 r/min,5 min)后倒掉上清液,获得的沉淀物为脱脂麦胚,置于通风橱中风干备用。
1.2.2 单因素实验
1.2.2.1 培育温度对蛋白酶活力和肽含量的影响
称量1 g脱脂麦胚,将其放入研钵中,加入10 mL,0.1 mol/L,pH4.0的柠檬酸-柠檬酸钠缓冲液,研磨均匀后转移至离心管中,微波处理10 s(600 W,预实验结果),然后分别在30、40、50、60、70 ℃下培育6 h,测定蛋白酶活力、肽含量。
1.2.2.2 培育时间对蛋白酶活力和肽含量的影响
脱脂麦胚的处理方法同上述1.2.2.1一致,然后于50 ℃下分别培育2、4、6、8、10 h,分析蛋白酶活力、肽含量。
1.2.2.3 培育液液料比对蛋白酶活力和肽含量的影响
称量1 g脱脂麦胚,将其放入研钵中,分别加入液料比为4:1、7:1、10:1、13:1、16:1 mL/g,pH4.0的柠檬酸-柠檬酸钠缓冲液,研磨均匀,微波(600 W,10 s)处理,然后于50 ℃下培育6 h,评定蛋白酶活力及肽含量。
1.2.2.4 培育液pH对蛋白酶活力和肽含量的影响
称量1 g脱脂麦胚于研钵中,分别加入10 mL,pH3.0、pH3.6、pH4.2、pH4.8、pH5.4、pH6.0、pH6.6的柠檬酸-柠檬酸钠缓冲液,同样进行研磨、微波处理,然后于50 ℃下培育6 h,测定蛋白酶活力及肽含量。
1.2.3 响应面优化试验
在上述单因素实验基础上,以培育温度(A)、培育时间(B)、pH(C)、液料比(D)为影响因素,以蛋白酶活力、肽含量为响应值,选取响应值较高的三水平,使用Box-Behnken设计方法进行响应面试验。试验因素水平见表1。
表 1 响应面试验设计方案Table 1. Design of response surface test试验水平 试验因素 培育温度(℃) 培育时间(h) pH 液料比(mL/g) −1 40 2 4.2 4:1 0 50 4 4.8 7:1 1 60 6 5.4 10:1 1.2.4 指标的测定
1.2.4.1 蛋白酶活力的测定
蛋白酶活力的测定方法参考Harvey等[22],并作适当修改。取2.0 mL培育后的麦胚上清液,加入6.0 mL磷酸二氢钠-柠檬酸缓冲液(pH6.0,0.02 mol/L,并含5 mmol/L β-巯基乙醇、2.5 mmol/L EDTA),冰浴10 min,4 ℃下离心(4200 r/min,30 min),获得上清液,即为粗蛋白酶液;随后,取1.0 mL粗蛋白酶液,以1:1的体积比加入酪蛋白溶液(20 g/L),于40 ℃下反应10 min,沸水浴(5 min)以灭酶,然后加入2.0 mL三氯乙酸溶液(0.4 mol/L),室温下静置(15 min)以沉淀蛋白质,最后离心(4000 r/min,15 min)获得上清液,并测定上清液在275 nm下的吸光度。对照组则使用去离子水代替粗蛋白酶液,其余步骤同试验组一致。使用不同浓度酪氨酸溶液的吸光度值,并绘制标准曲线(y=0.0077x,R2=0.9991),用于定量分析样品中的酪氨酸含量。将1 mL麦胚粗蛋白酶液催化酪蛋白每分钟产生1 μg酪氨酸定义为1个酶活力单位(U)。
1.2.4.2 肽含量的测定
肽含量的测定方法参照鲁伟等[23],并作适当修改。取2.5 mL的麦胚上清液,加入2.5 mL 10%(w/v)三氯乙酸,混匀、静置10 min,离心(4000 r/min,15min)获得上清,用5%三氯乙酸定容至50 mL,然后取6.0 mL上述定容后的溶液,加入4.0 mL双缩脲试剂,混匀、静置10 min,最后离心(2000 r/min,10 min)得上清,在540 nm下测定吸光度值。对照组则使用去离子水作为麦胚上清液,其余步骤相同。使用还原型谷胱甘肽制作标准曲线(y=0.0029x,R2=0.9978),用于定量分析样品中的肽含量。
1.3 数据处理
所有试验采取3组平行,使用SPSS 20.0软件进行显著性分析(P<0.05),采用Design Expert 8.0.6软件进行Box-Behnken设计,显著性水平为P<0.05,极显著性水平为P<0.01。
2. 结果与分析
2.1 单因素实验结果
2.1.1 培育温度的影响
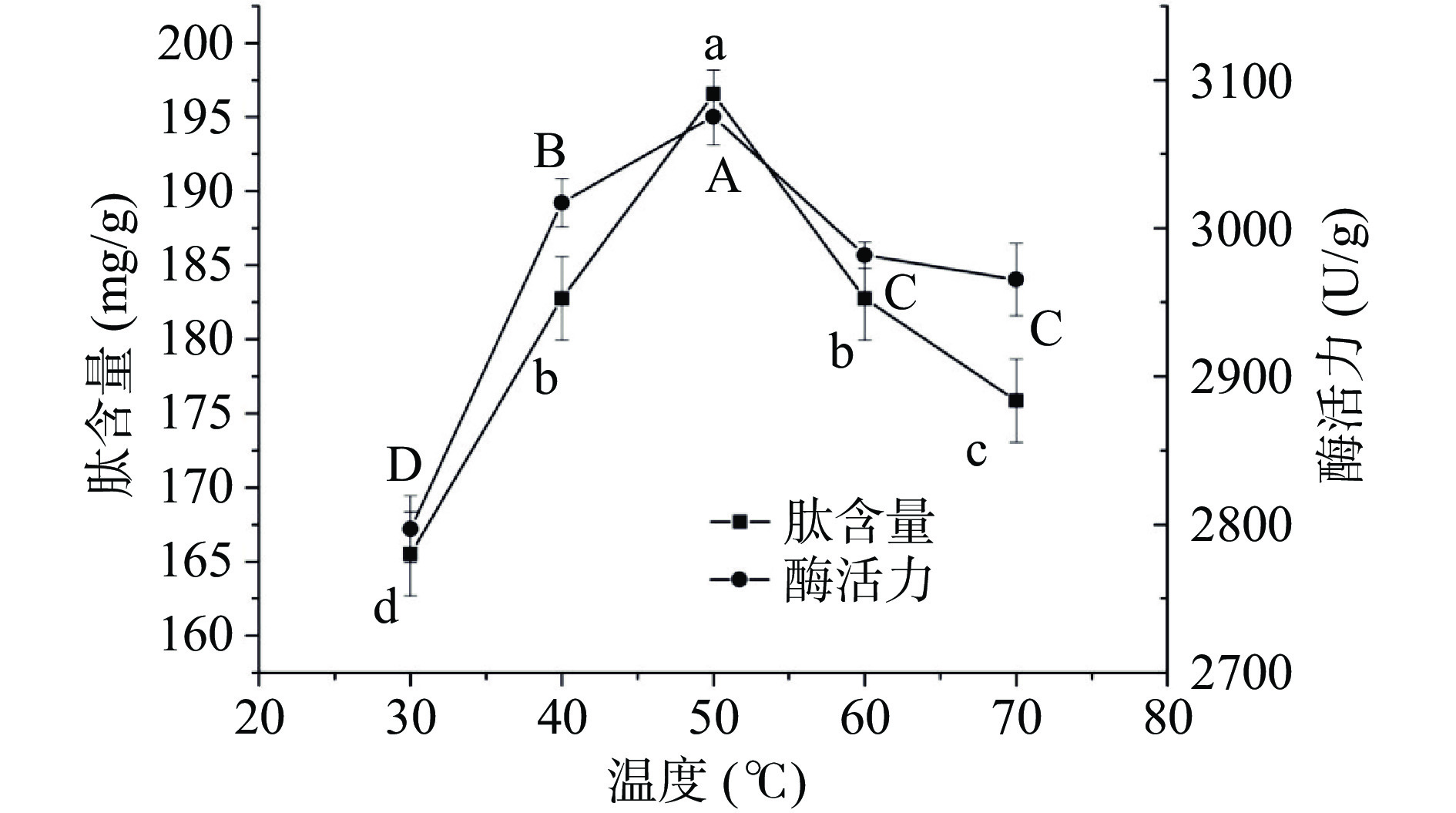
由图1可知,培育温度对麦胚蛋白酶活力及肽含量有显著影响(P<0.05)。在30~70 ℃间,酶活力呈现先上升后下降的趋势,于50 ℃达到最高酶活力(3075.32 U/g),表明适度的环境温度有利于激活麦胚中的蛋白酶,从而促使其活性提高。麦胚中含有天冬氨酸蛋白酶、半胱氨酸蛋白酶、丝氨酸蛋白酶和金属蛋白酶,其中,半胱氨酸蛋白酶、丝氨酸蛋白酶的最适反应温度均为50 ℃[24]。温度影响酶的构象,温度过高时,蛋白酶会发生变性,其活力下降。培育温度为50 ℃时,肽含量达到峰值,为196.55 mg/g,与30 ℃相比,提高了18.75%;温度提高至70 ℃时,肽含量逐渐降低至175.86 mg/g。肽含量的变化趋势也呈现先增大后减小的趋势,同蛋白酶活力的变化趋势一致,二者呈正相关关系。有诸多研究者指出,发芽处理型生物调控技术可有效增强酶促反应,从而提高生物活性物质的含量[25-28]。因此,由于麦胚中蛋白酶活性的增强,更多蛋白质被水解,从而表现为肽含量的增加。
2.1.2 培育时间的影响
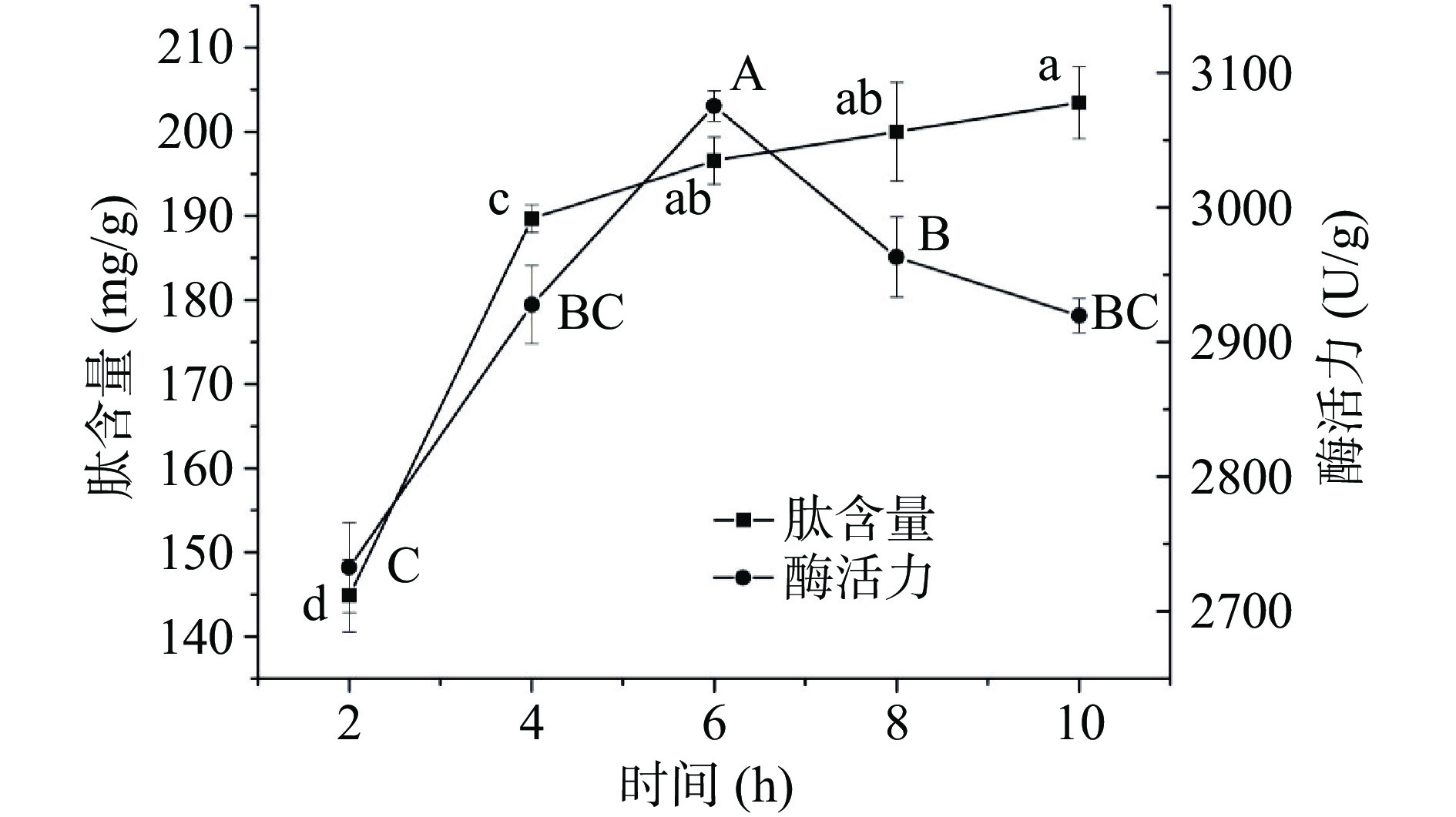
如图2所示,培育时间由2 h增加至6 h时,蛋白酶活力升高至3075.32 U/g,当培育时间延长至8 h时,蛋白酶活力明显下降,当培育时间达到10 h时,其活性继续下降,并趋于稳定。结果表明,一定培育温度下,培育时间过长时,容易导致蛋白酶失活。蛋白质的活性极易受环境影响,如酸碱处理、加热和发酵等[29-30]。Zheng等[31]提出,长时间的高温环境显著降低了一种ACE抑制六肽(来源于山茶花谷蛋白水解物)的活性。由图2可知,麦胚中肽含量随着培育时间的增加而增加。2~4 h时,肽含量显著上升(P<0.05),高于4 h时,肽含量继续上升,但上升速率趋于平缓,至10 h时,累积至203.45 mg/g。虽然蛋白酶活力在培育6 h后开始下降,但是肽的生成仍在发生。肽含量随着培育时间的增长而动态累积,最终无明显变化,达到平衡。
2.1.3 培育液液料比的影响
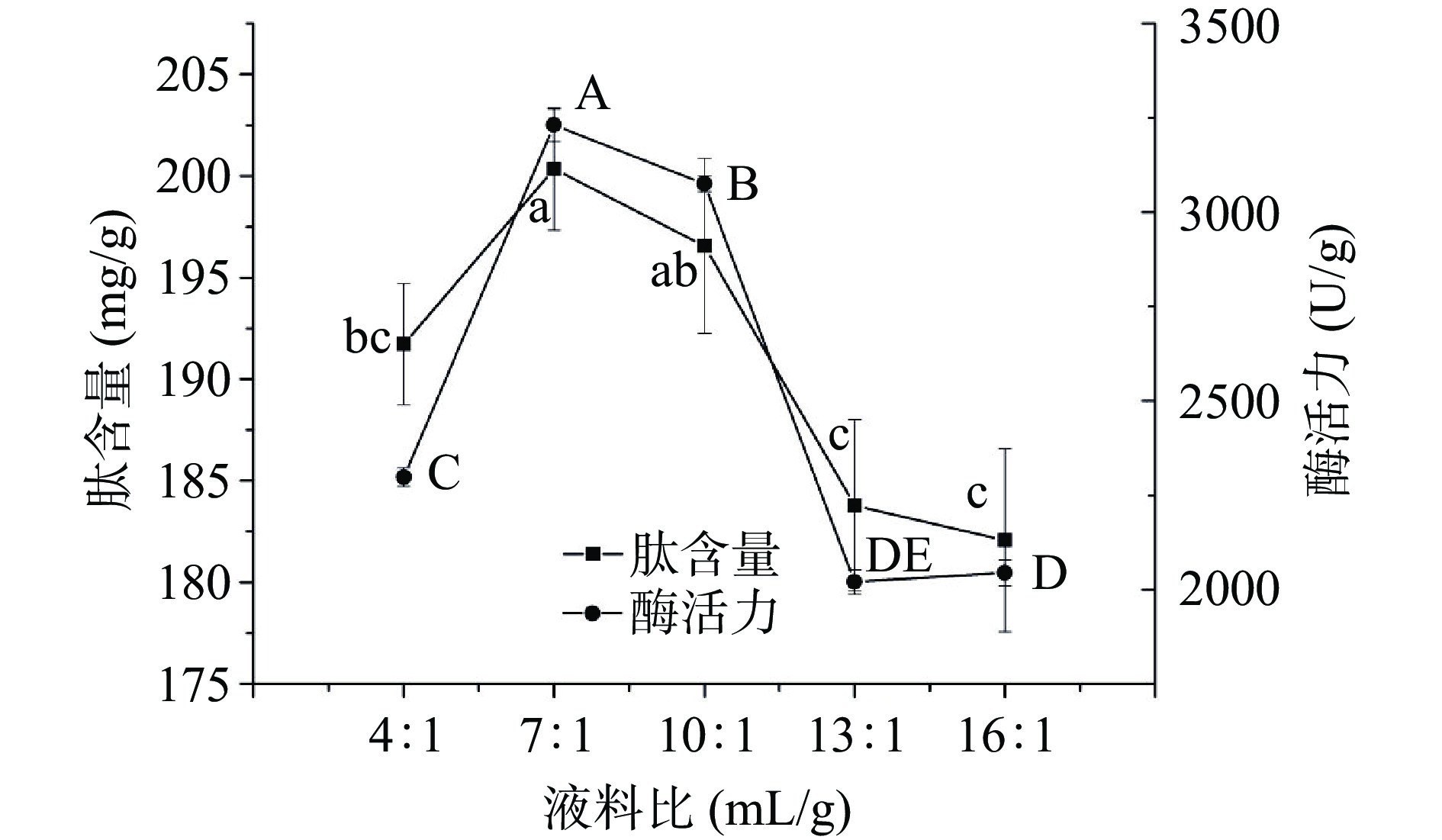
培育液液料比明显地改变了麦胚中蛋白酶的活力和肽含量。由图3可知,液料比为7:1 mL/g时,蛋白酶活力最高,肽含量也最高;液料比为4:1 mL/g时,酶活力、肽含量均较低,这可能是由于麦胚中的蛋白酶未能被充分提取。此外,提取液中蛋白质浓度过高时,也不利于酶与底物充分接触并发生反应[12]。当液料比提高至10:1、13:1、16:1 mL/g时,待培育液中蛋白酶的浓度随着料液比的增大而减小,酶活力(U/g麦胚)随之下降,肽含量也随之降低。王淑芳[32]的研究同样发现料液比7:1 mL/g下,麦胚中肽含量最高,并指出合适的酶浓度、底物浓度对酶反应至关重要。因此,合适的液料比有助于提高酶活、富集麦胚多肽。Huang等[33]开发了一种以梯度浓度加入底物牛奶蛋白的方式,大大提高了ACE抑制肽的产量。
2.1.4 培育液pH的影响
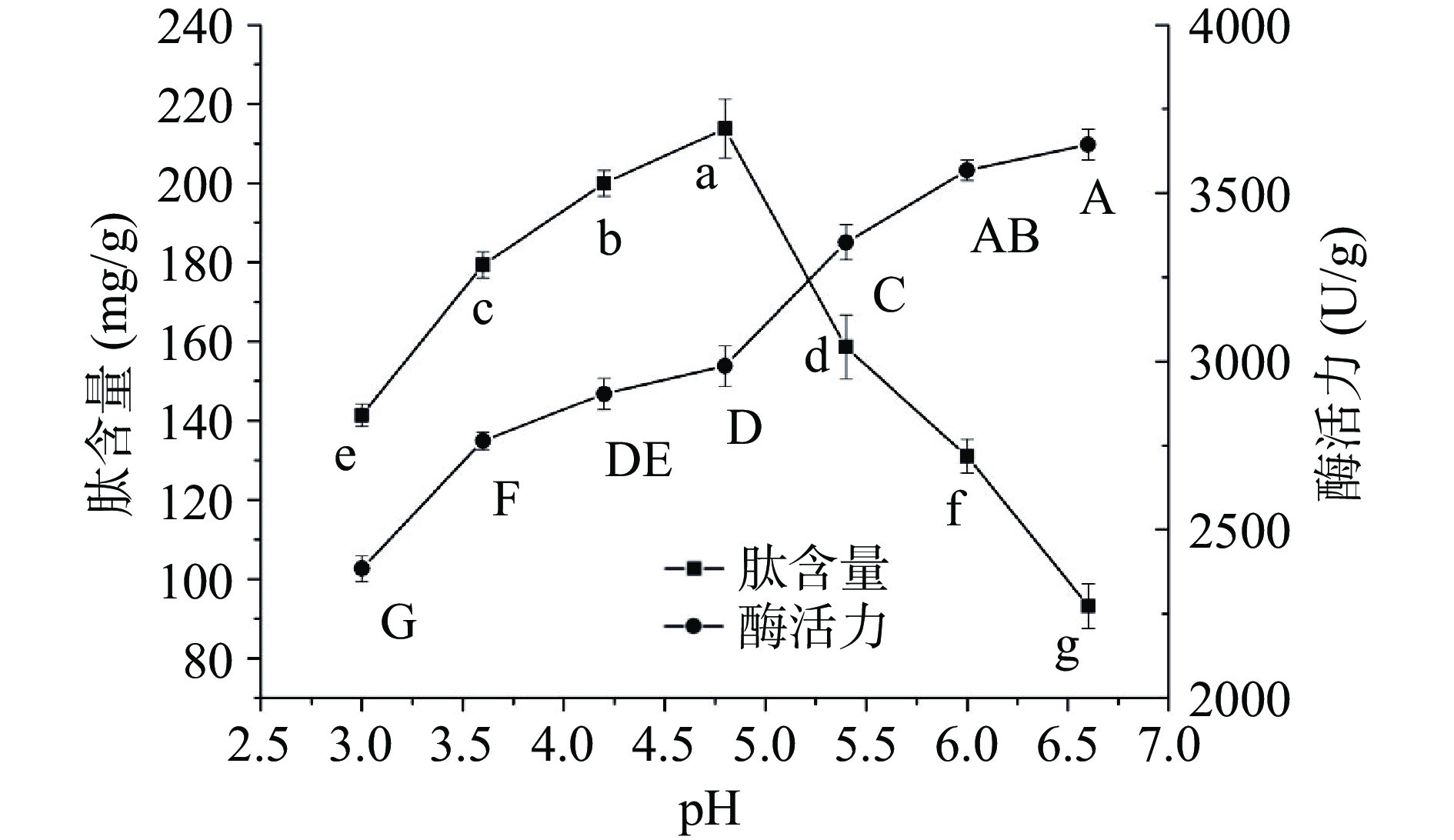
培育液的pH对麦胚蛋白酶活力及肽含量的影响如图4所示,蛋白酶活力随着pH(3.0~6.6)的升高而增加。pH4.8时,肽的含量最高,为213.79 mg/g;当pH低于4.8时,肽含量随着pH的升高而升高,而当pH高于4.8时,肽含量随着pH的升高而下降。杨润强等[12]指出,麦胚中含有较多的酸性蛋白酶,如半胱氨酸蛋白酶、天冬氨酸蛋白酶等,促使麦胚蛋白提取物在酸性环境下表现出较强的酶活。酸性环境下,可以通过提供质子以稳定酶的过渡态,达到催化反应的目的,从而促使肽的富集[32]。此外,酸性环境下,高分子量的蛋白质存在着酸降解作用。由图4可知,培育液pH接近中性时,肽含量逐渐降低,但总蛋白酶活持续地上升。麦胚裂解物具有中性蛋白酶活性[34],而麦胚中中性蛋白酶的水解能力可能低于酸性蛋白酶。
2.2 响应面试验
2.2.1 Box-Behnken设计
选用四因素三水平进行Box-Behnken试验优化,该方法设计和分析了培育温度、培育时间、培育液pH、培育液液料比四个因素对麦胚蛋白酶活力和肽含量的影响(表2)。对表2中的数据进行多元二次回归拟合,得到麦胚酶活力(Y1)及肽含量(Y2)预测值的二次多项回归方程:
表 2 Box-Behnken试验设计与试验结果Table 2. Design of Box-Behnken test and experimental results试验号 A
温度(℃)B
时间(h)C
pHD
液料比(mL/g)肽含量
(mg/g)酶活力
(U/g)1 40 6 4.8 7:1 253.09±1.14 3003.64±8.23 2 50 4 4.2 10:1 297.11±4.30 3374.55±15.30 3 50 4 4.2 4:1 216.46±6.21 1766.23±2.49 4 40 2 4.8 7:1 202.73±3.01 2904.73±11.89 5 40 4 4.2 7:1 237.78±5.21 2775.27±17.22 6 60 2 4.8 7:1 221.83±1.97 3099.64±15.32 7 50 4 5.4 4:1 187.79±0.69 1767.06±5.40 8 40 4 5.4 7:1 190.33±4.10 3066.18±7.13 9 50 2 5.4 7:1 191.34±3.01 3106.91±16.21 10 50 4 4.8 7:1 253.45±4.10 3057.45±8.97 11 60 4 4.8 10:1 254.14±5.51 4018.70±21.19 12 50 4 4.8 7:1 252.28±3.86 3058.91±10.12 13 50 2 4.8 10:1 227.21±4.29 3835.84±78.91 14 50 4 4.8 7:1 263.07±5.21 3060.36±9.56 15 50 2 4.2 7:1 202.12±3.94 2891.64±26.26 16 50 4 4.8 7:1 245.08±3.89 3064.73±8.66 17 60 4 4.2 7:1 264.79±4.26 2960.00±10.10 18 60 4 5.4 7:1 236.16±3.01 3031.27±10.38 19 50 4 4.8 7:1 250.26±4.35 3051.64±9.78 20 50 6 4.8 10:1 285.56±2.82 4170.39±9.65 21 60 6 4.8 7:1 253.19±3.94 3005.09±21.53 22 50 6 4.2 7:1 284.49±3.42 2981.82±3.56 23 50 4 5.4 10:1 234.34±3.25 4305.45±19.57 24 50 2 4.8 4:1 188.12±7.03 1801.14±2.38 25 40 4 4.8 10:1 270.97±9.89 3457.66±8.54 26 50 6 5.4 7:1 239.71±3.01 3040.00±9.59 27 40 4 4.8 4:1 165.25±0.69 1787.84±5.4 28 50 6 4.8 4:1 239.71±3.45 1763.74±4.57 29 60 4 4.8 4:1 200.29±6.89 1747.12±3.74 Y1=−3649.81+100.47A+145.68B+1197.71C−262.07D−2.42AB−9.15AC+5.01AD−32.73BC+15.49BD+129.18CD−0.75A2+4.67B2−134.98C2−23.05D2
Y2=−1123.31+14.75A+74.93B+248.17C+71.54D−0.24AB+0.78AC−0.43AD−7.08BC+0.28BD−4.74CD−0.14A2−2.19B2−26.76C2−1.29D2
2.2.2 回归方程方差分析
方差分析结果表明,蛋白酶活力的回归模型的F=101.83,P<0.0001,模型极显著,R2=0.9903,此模型可解释99.03%的变异(表3)。肽含量的回归模型的F=13.58,P<0.0001,模型极显著,R2=0.9314,此模型可解释93.14%的变异(表4)。由表3可以看出,温度对酶活力影响显著(P<0.05),而pH和液料比对酶活力的影响极显著(P<0.01),影响大小为液料比>pH>温度>时间,此外,温度和液料比、pH和液料比对蛋白酶活力有极显著的交互作用(P<0.01)。由表4可知,培育温度、培育时间、培育液pH、培育液液料比对麦胚中的肽含量皆有显著性影响(P<0.05),其中,时间、pH和液料比对肽含量的影响极显著(P<0.01),并且各因素对肽含量的影响大小为液料比>时间>pH>温度。
表 3 Box-Behnken设计中蛋白酶活力的方差分析Table 3. The variance analysis of protease activities by Box-Behnken design变异来源 平方和 自由度 均方 F值 P值 显著性 模型 1.404E 14 1.003E 101.83 <0.0001 极显著 A 62568.52 1 62568.52 6.35 0.0245 显著 B 8790.17 1 8790.17 0.89 0.3609 C 2.047E 1 2.047E 20.78 0.0004 极显著 D 1.308E 1 1.308E 1327.98 <0.0001 极显著 AB 9356.69 1 9356.69 0.95 0.3463 AC 12060.43 1 12060.43 1.22 0.2872 AD 90528.77 1 90528.77 9.19 0.0090 极显著 BC 6169.32 1 6169.32 0.63 0.4419 BD 34586.70 1 34586.70 3.51 0.0820 CD 2.163E 1 2.163E 21.95 0.0004 极显著 A2 36239.85 1 36239.85 3.68 0.0757 B2 2264.36 1 2264.36 0.23 0.6390 C2 15315.20 1 15315.20 1.55 0.2329 D2 2.791E 1 2.791E 28.33 0.0001 极显著 失拟值 1.378E 10 13782.74 608.96 0.0738 不显著 残差 90.53 4 22.63 总变异 1.418E 28 注:R2=0.9903,变异系数为3.39%;P<0.05表示显著;P<0.01表示极显著。 表 4 Box-Behnken设计中肽含量的方差分析Table 4. The variance analysis of peptide amount by Box-Behnken design变异来源 平方和 自由度 均方 F值 P值 显著性 模型 28856.89 14 2061.21 13.58 <0.0001 极显著 A 1012.92 1 1012.92 6.68 0.0217 显著 B 8661.81 1 8661.81 57.09 <0.0001 极显著 C 4147.06 1 4147.06 27.33 0.0001 极显著 D 11514.03 1 11514.03 75.88 <0.0001 极显著 AB 90.25 1 90.25 0.59 0.4534 AC 88.55 1 88.55 0.58 0.4576 AD 672.62 1 672.62 4.43 0.0538 BC 289.00 1 289.00 1.90 0.1892 BD 11.42 1 11.42 0.075 0.7878 CD 290.70 1 290.70 1.92 0.1880 A2 1202.65 1 1202.65 7.93 0.0138 显著 B2 502.06 1 502.06 3.31 0.0904 C2 601.88 1 601.88 3.97 0.0663 D2 867.79 1 867.79 5.72 0.0314 显著 失拟值 1952.04 10 195.20 4.53 0.0791 不显著 残差 172.21 4 43.05 总变异 30981.14 28 注:R2=0.9314,变异系数为5.25%。 2.2.3 响应曲面分析
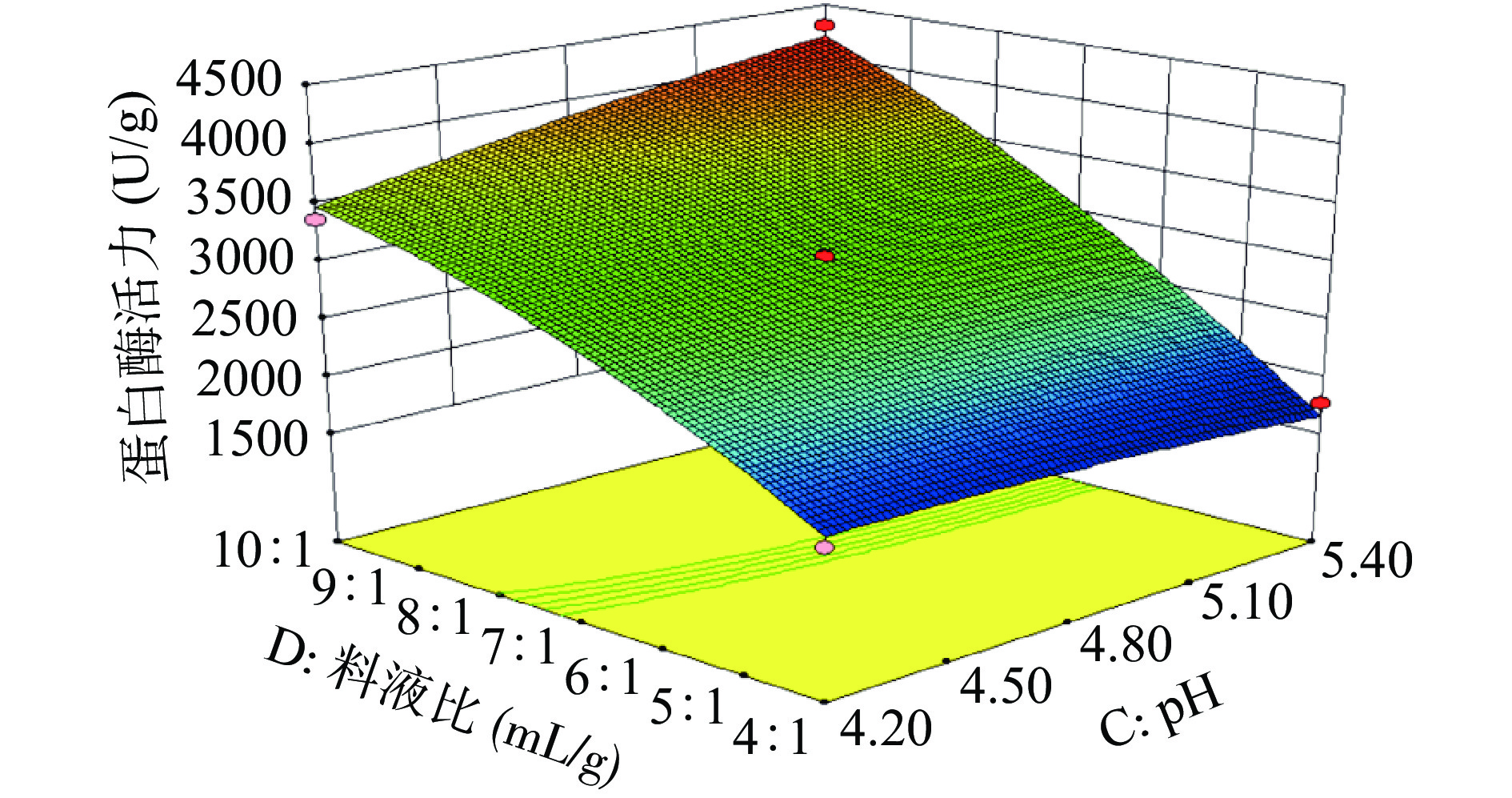
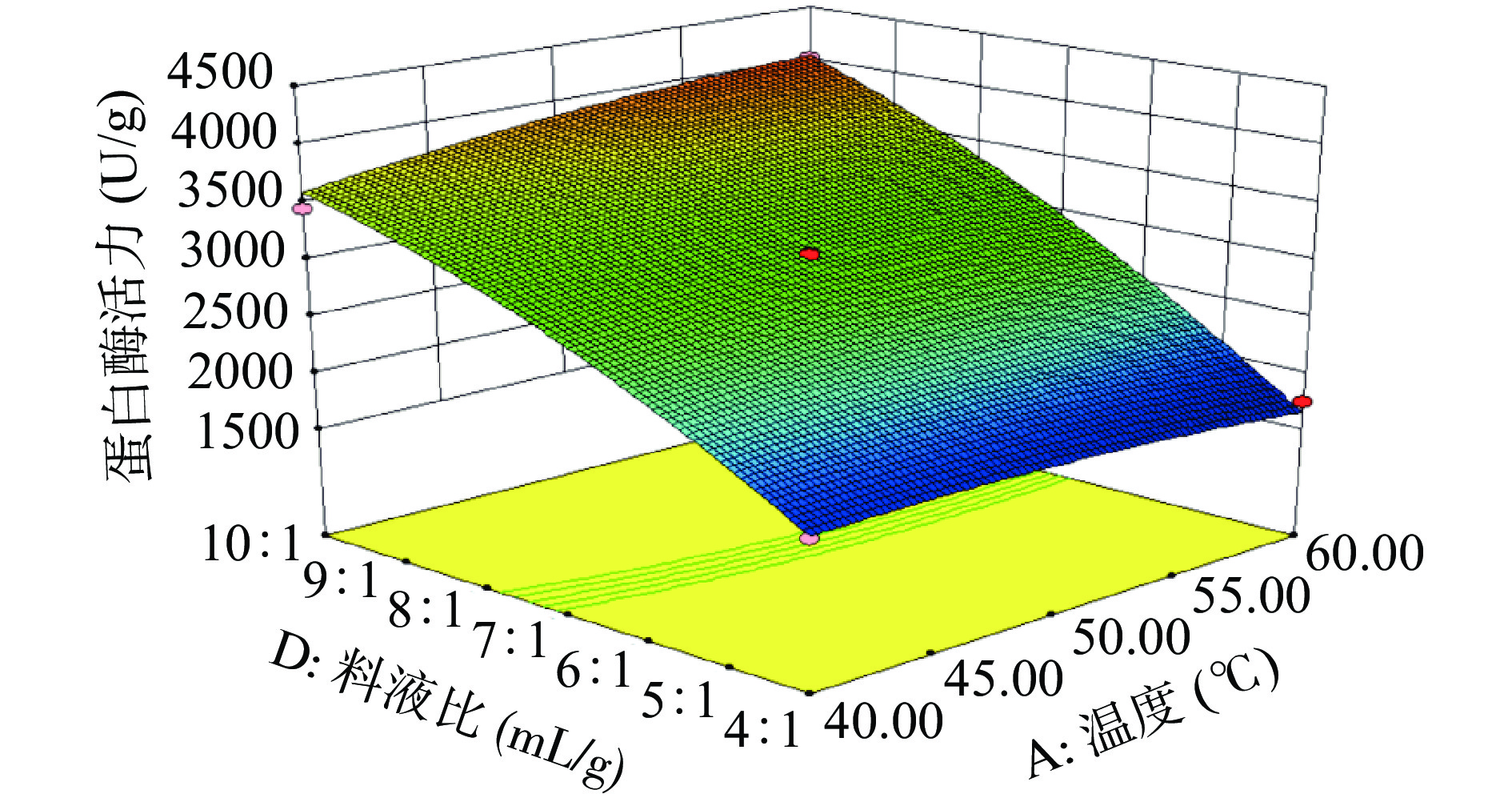
由图5可知,培育温度和时间分别固定为50 ℃、4 h,培育pH和液料比对蛋白酶活力也有明显的交互作用,不同pH下,蛋白酶活力随着液料比的升高而升高,pH为5.4、液料比10:1 mL/g时,蛋白酶活力最高,为4305.45 U/g。由图6得知,当pH、时间分别固定为4.8、4 h时,培育温度和液料比对蛋白酶活力有明显的交互作用,不同温度下,蛋白酶活力随着液料比的升高而升高,当培育温度为60 ℃、液料比为10:1 mL/g时,蛋白酶活力最高,达到4018.70 U/g。
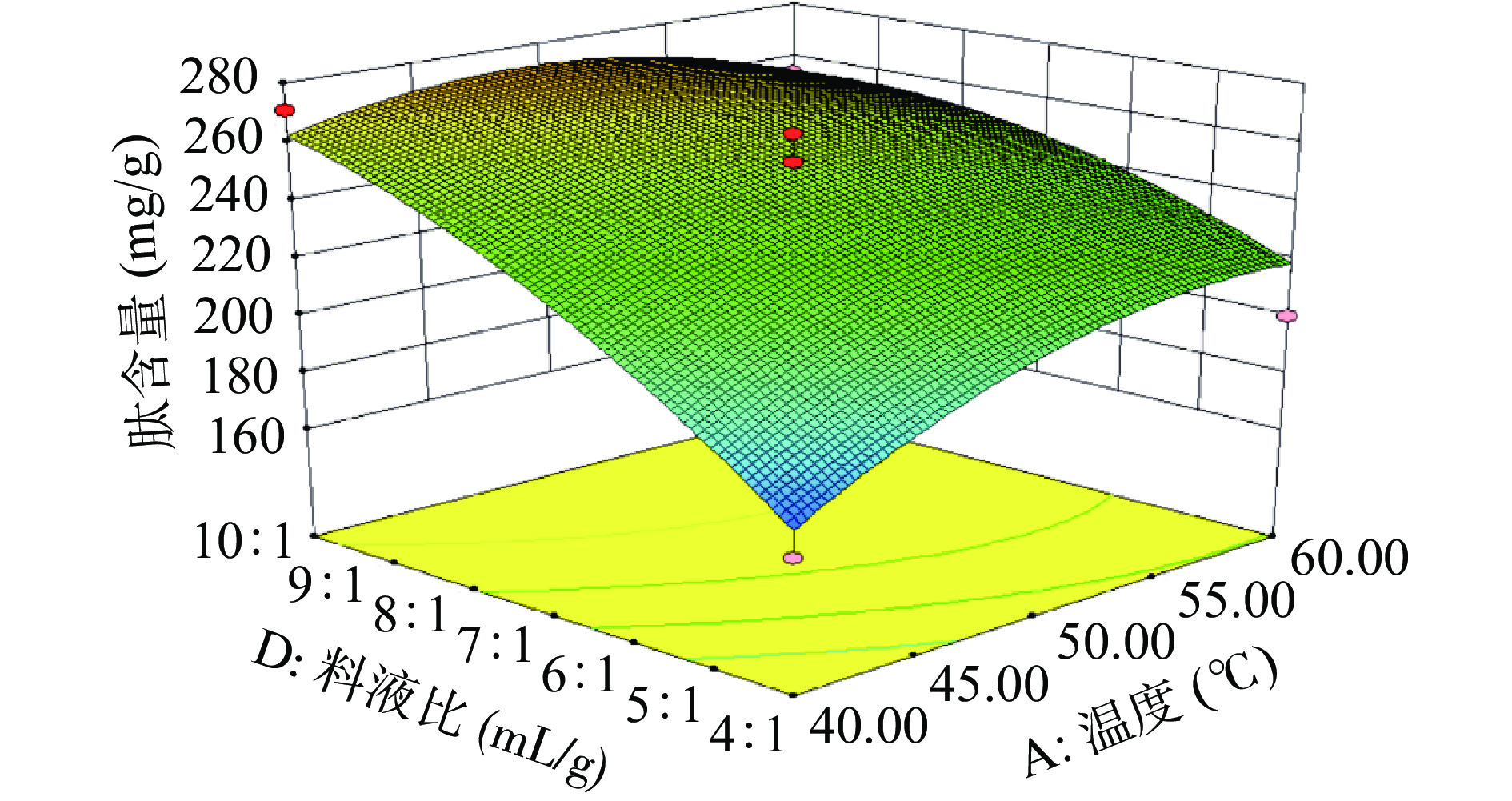
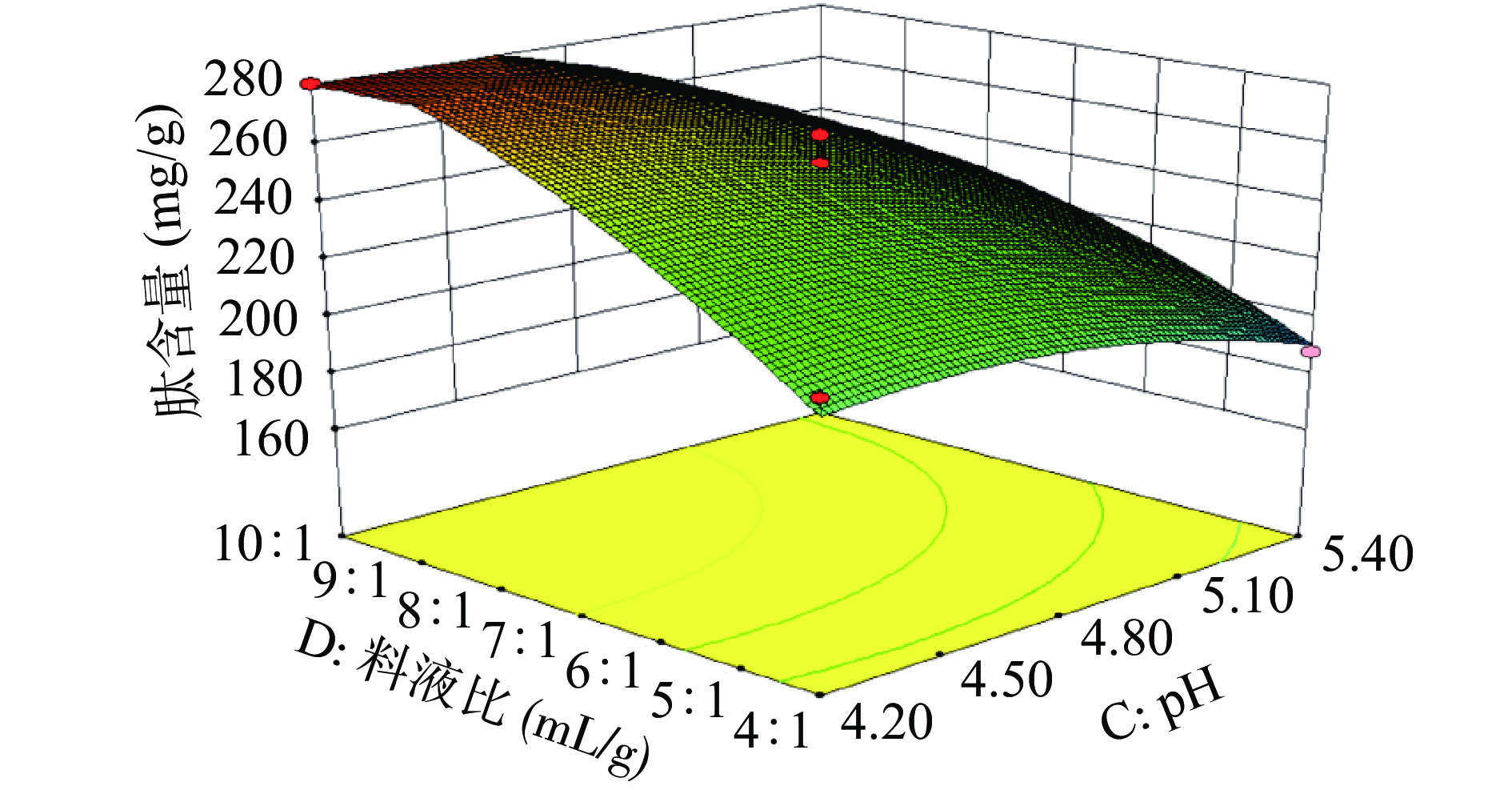
由图7可以看出,培育温度和液料比之间对麦胚肽含量的交互作用较为明显,时间和pH分别为4 h和4.8,液料比为4:1 mL/g时,培育温度升高,肽含量也升高,液料比7:1 mL/g时,随着温度升高,肽含量呈现先上升后下降的趋势,当液料比10:1 mL/g、温度50 ℃时,肽含量最高,约270 mg/g。由图8可知,当时间和温度分别为4 h和50 ℃时,培育液pH和液料比二者的交互作用较为明显,当培育液pH由4.2增加到5.4时,肽含量随着液料比的增加而提高,当培育液pH为4.2,液料比10:1 mL/g时为最高值,达到297.11 mg/g。
2.2.4 响应面模型的优化与验证
通过响应面优化得到最优培育条件为:培育温度50 ℃,时间6 h,pH4.5和液料比10:1 mL/g,通过实验验证,得到肽含量为303.12 mg/g,蛋白酶活力为3812.34 U/g。在此条件模型预测下,肽含量为307.44 mg/g,蛋白酶活力为3860.99 U/g,试验结果与预测值相接近,且显著(P<0.05)高于两组随机试验(表2试验组5、试验组24)结果(表5)。杨润强等[12]通过响应面优化得到的最高麦胚肽含量为88.46 mg/g,而本实验优化培育条件后所得到的肽含量是其3.43倍。因此,通过响应面优化培育条件,以富集麦胚肽含量,是切实可行的。
表 5 验证试验设计与结果Table 5. Validation of the test design and result处理 肽含量(mg/g) 酶活力(U/g) 最优 303.12±3.56a 3812.34±10.13a 随机1(试验组5) 237.78±5.21b 2775.27±17.22b 随机2(试验组24) 188.12±7.03c 1801.14±2.38c 注:同列不同字母表示各组间差异显著(P<0.05)。 3. 结论
优化麦胚培育条件是一种有效富集多肽、提高其应用价值的方法。本文实验结果表明,培育温度、培育时间、培育液pH及培育液液料比对麦胚蛋白酶活力及肽含量有显著影响(P<0.05)。通过响应面Box-Behnken设计得到最优的培育条件为:培育温度50 ℃、时间6 h、pH4.5及液料比10:1 mL/g,在此条件下所得的肽含量及酶活力分别为303.12 mg/g和3812.34 U/g。此外,麦胚经脱脂、微波预处理,是一种提高孵育麦胚中多肽含量的有效方法,具有进一步的研究价值。本研究为扩大麦胚的应用范围、提高其利用率提供了新的策略。
-
表 1 响应面试验设计方案
Table 1 Design of response surface test
试验水平 试验因素 培育温度(℃) 培育时间(h) pH 液料比(mL/g) −1 40 2 4.2 4:1 0 50 4 4.8 7:1 1 60 6 5.4 10:1 表 2 Box-Behnken试验设计与试验结果
Table 2 Design of Box-Behnken test and experimental results
试验号 A
温度(℃)B
时间(h)C
pHD
液料比(mL/g)肽含量
(mg/g)酶活力
(U/g)1 40 6 4.8 7:1 253.09±1.14 3003.64±8.23 2 50 4 4.2 10:1 297.11±4.30 3374.55±15.30 3 50 4 4.2 4:1 216.46±6.21 1766.23±2.49 4 40 2 4.8 7:1 202.73±3.01 2904.73±11.89 5 40 4 4.2 7:1 237.78±5.21 2775.27±17.22 6 60 2 4.8 7:1 221.83±1.97 3099.64±15.32 7 50 4 5.4 4:1 187.79±0.69 1767.06±5.40 8 40 4 5.4 7:1 190.33±4.10 3066.18±7.13 9 50 2 5.4 7:1 191.34±3.01 3106.91±16.21 10 50 4 4.8 7:1 253.45±4.10 3057.45±8.97 11 60 4 4.8 10:1 254.14±5.51 4018.70±21.19 12 50 4 4.8 7:1 252.28±3.86 3058.91±10.12 13 50 2 4.8 10:1 227.21±4.29 3835.84±78.91 14 50 4 4.8 7:1 263.07±5.21 3060.36±9.56 15 50 2 4.2 7:1 202.12±3.94 2891.64±26.26 16 50 4 4.8 7:1 245.08±3.89 3064.73±8.66 17 60 4 4.2 7:1 264.79±4.26 2960.00±10.10 18 60 4 5.4 7:1 236.16±3.01 3031.27±10.38 19 50 4 4.8 7:1 250.26±4.35 3051.64±9.78 20 50 6 4.8 10:1 285.56±2.82 4170.39±9.65 21 60 6 4.8 7:1 253.19±3.94 3005.09±21.53 22 50 6 4.2 7:1 284.49±3.42 2981.82±3.56 23 50 4 5.4 10:1 234.34±3.25 4305.45±19.57 24 50 2 4.8 4:1 188.12±7.03 1801.14±2.38 25 40 4 4.8 10:1 270.97±9.89 3457.66±8.54 26 50 6 5.4 7:1 239.71±3.01 3040.00±9.59 27 40 4 4.8 4:1 165.25±0.69 1787.84±5.4 28 50 6 4.8 4:1 239.71±3.45 1763.74±4.57 29 60 4 4.8 4:1 200.29±6.89 1747.12±3.74 表 3 Box-Behnken设计中蛋白酶活力的方差分析
Table 3 The variance analysis of protease activities by Box-Behnken design
变异来源 平方和 自由度 均方 F值 P值 显著性 模型 1.404E 14 1.003E 101.83 <0.0001 极显著 A 62568.52 1 62568.52 6.35 0.0245 显著 B 8790.17 1 8790.17 0.89 0.3609 C 2.047E 1 2.047E 20.78 0.0004 极显著 D 1.308E 1 1.308E 1327.98 <0.0001 极显著 AB 9356.69 1 9356.69 0.95 0.3463 AC 12060.43 1 12060.43 1.22 0.2872 AD 90528.77 1 90528.77 9.19 0.0090 极显著 BC 6169.32 1 6169.32 0.63 0.4419 BD 34586.70 1 34586.70 3.51 0.0820 CD 2.163E 1 2.163E 21.95 0.0004 极显著 A2 36239.85 1 36239.85 3.68 0.0757 B2 2264.36 1 2264.36 0.23 0.6390 C2 15315.20 1 15315.20 1.55 0.2329 D2 2.791E 1 2.791E 28.33 0.0001 极显著 失拟值 1.378E 10 13782.74 608.96 0.0738 不显著 残差 90.53 4 22.63 总变异 1.418E 28 注:R2=0.9903,变异系数为3.39%;P<0.05表示显著;P<0.01表示极显著。 表 4 Box-Behnken设计中肽含量的方差分析
Table 4 The variance analysis of peptide amount by Box-Behnken design
变异来源 平方和 自由度 均方 F值 P值 显著性 模型 28856.89 14 2061.21 13.58 <0.0001 极显著 A 1012.92 1 1012.92 6.68 0.0217 显著 B 8661.81 1 8661.81 57.09 <0.0001 极显著 C 4147.06 1 4147.06 27.33 0.0001 极显著 D 11514.03 1 11514.03 75.88 <0.0001 极显著 AB 90.25 1 90.25 0.59 0.4534 AC 88.55 1 88.55 0.58 0.4576 AD 672.62 1 672.62 4.43 0.0538 BC 289.00 1 289.00 1.90 0.1892 BD 11.42 1 11.42 0.075 0.7878 CD 290.70 1 290.70 1.92 0.1880 A2 1202.65 1 1202.65 7.93 0.0138 显著 B2 502.06 1 502.06 3.31 0.0904 C2 601.88 1 601.88 3.97 0.0663 D2 867.79 1 867.79 5.72 0.0314 显著 失拟值 1952.04 10 195.20 4.53 0.0791 不显著 残差 172.21 4 43.05 总变异 30981.14 28 注:R2=0.9314,变异系数为5.25%。 表 5 验证试验设计与结果
Table 5 Validation of the test design and result
处理 肽含量(mg/g) 酶活力(U/g) 最优 303.12±3.56a 3812.34±10.13a 随机1(试验组5) 237.78±5.21b 2775.27±17.22b 随机2(试验组24) 188.12±7.03c 1801.14±2.38c 注:同列不同字母表示各组间差异显著(P<0.05)。 -
[1] KHAN K. Wheat: Chemistry and technology[M]. 4Thed. USA: Woodhead Publishing and AACC International Press, 2009: 1−17.
[2] 河南省农业科学院农副产品加工研究中心. 小麦胚芽综合利用加工技术[EB/OL]. (2010-05-14). http://www.hnagri.org.cn/nfcp/article-15708.html Agricultural and Sideline Products Processing Research Center, Henan Academy of Agricultural Sciences. Processing technology on comprehensive utilization of wheat germ[EB/OL]. (2010-05-14). http://www.hnagri.org.cn/nfcp/article-15708.html.
[3] 胡莉丽. 麦胚清蛋白的酶法水解及其产物的抗氧化性研究[D]. 合肥: 合肥工业大学, 2017. HU L L. Proteolysis of wheat germ albumin and antioxidant activity of the hydrolysate[D]. Hefei: Hefei University of Technology, 2017.
[4] 李建军, 黄开红, 单成俊. 小麦胚蛋白质的研究进展[J]. 粮食与饲料工业,2010(5):7−9. [LI J J, HUANG K H, SHAN C J. Advances in research on wheat germ proteins[J]. Cereal and Feed Industry,2010(5):7−9. doi: 10.3969/j.issn.1003-6202.2010.05.003 [5] BRANDOLINI A, HIDALGO A. Wheat germ: Not only a by-product[J]. International Journal of Food Sciences and Nutrition,2012,63(S1):71−74.
[6] ZHANG Y, HE S D, BONNEIL É, et al. Generation of antioxidative peptides from Atlantic sea cucumber using alcalase versus trypsin: In vitro activity, de novo sequencing, and in silico docking for in vivo function prediction[J]. Food Chemistry,2020,306:125581. doi: 10.1016/j.foodchem.2019.125581
[7] KARAMI Z, PEIGHAMBARDOUST S H, HESARI J, et al. Antioxidant, anticancer and ACE-inhibitory activities of bioactive peptides from wheat germ protein hydrolysates[J]. Food Bioscience,2019,32:100450. doi: 10.1016/j.fbio.2019.100450
[8] 胡立明, 宋瑞雪, 陈玉霞. 响应面法优化孵育麦胚功能肽研究[J]. 食品科技,2011,36(12):174−178. [HU L M, SONG R X, CHEN Y X. Optimization of functional peptide incubation from wheat germ by response surface method[J]. Food Science and Technology,2011,36(12):174−178. [9] 辛志宏, 吴守一, 马海乐, 等. 从麦胚蛋白质中制备降血压肽的研究[J]. 食品科学,2003,24(10):120−123. [XIN Z H, WU S Y, MA H L, et al. Study on preparation of antihypertensive peptide from wheat germ protein[J]. Food Science,2003,24(10):120−123. doi: 10.3321/j.issn:1002-6630.2003.10.029 [10] 代卉, 施用晖, 韩芳, 等. 小麦肽免疫活性及抗氧化作用的研究[J]. 天然产物研究与开发,2009,21(3):473−476. [DAI H, SHI Y H, HAN F, et al. Study on wheat peptides on immune modulating and antioxidant effect[J]. Research and Development of Natural Products,2009,21(3):473−476. doi: 10.3969/j.issn.1001-6880.2009.03.028 [11] 程云辉, 王璋, 许时婴. 酶解麦胚蛋白制备抗氧化肽的研究[J]. 食品科学,2006,27(6):147−151. [CHENG Y H, WANG Z, XU S Y. Preparation of antioxidant peptide from wheat germ protein by enzymatic hydrolysis[J]. Food Science,2006,27(6):147−151. doi: 10.3321/j.issn:1002-6630.2006.06.030 [12] 杨润强, 龚小峰, 顾振新, 等. 孵育法富集麦胚多肽工艺参数优化[J]. 食品科学,2010,31(14):22−25. [YANG R Q, GONG X F, GU Z X, et al. Optimization of incubation conditions for polypeptide-enriched wheat germ[J]. Food Science,2010,31(14):22−25. [13] 余南静, 杨润强, 曹晓虹, 等. 孵育液组分对麦胚蛋白酶活力与ACE抑制率的影响[J]. 中国粮油学报,2011,26(12):11−15. [YU N J, YANG R Q, CAO X H, et al. Effect of incubation medium on protease activity and angiotensin I-converting enzyme inhibitory activity of incubated wheat germ[J]. Journal of the Chinese Cereals and Oils Association,2011,26(12):11−15. [14] 黄纪民, 李秉正, 师德强, 等. 微波技术在农产品加工领域的应用研究进展[J]. 广西科学院学报,2020,36(3):293−299. [HUANG J M, LI B Z, SHI D Q, et al. Application of microwave technology in processing of agro-products: A review[J]. Journal of Guangxi Academy of Science,2020,36(3):293−299. [15] 任晓锋, 马海乐, 贾俊强, 等. 扫频超声波预处理对麦胚蛋白制备ACE抑制肽的影响[J]. 中国食品学报,2015,15(8):101−107. [REN X F, MA H L, JIA J Q, et al. Effect of swept ultrasound pretreatment on preparation of ACE inhibitory peptides by wheat germ protein[J]. Journal of Chinese Institute of Food Science and Technology,2015,15(8):101−107. [16] JIA J Q, MA H L, ZHAO W R, et al. The use of ultrasound for enzymatic preparation of ACE-inhibitory peptides from wheat germ protein[J]. Food Chemistry,2010,119(1):336−342. doi: 10.1016/j.foodchem.2009.06.036
[17] 颜辉, 蔡豪, 贾俊强, 等. 超声酶解制备牡丹籽降血糖肽的响应面优化研究[J]. 食品工业科技,2016,37(17):220−224,231. [YAN H, CAI H, JIA J Q, et al. Optimization of ultrasonic-assisted enzymatic preparation of peony seed hypoglycemic polypeptide by response surface methodology[J]. Science and Technology of Food Industry,2016,37(17):220−224,231. [18] 张海晖, 李长征, 罗孝平, 等. 亚临界水萃取麦胚蛋白及其功能特性的研究[J]. 食品工业科技,2016,37(23):193−198,205. [ZHANG H H, LI C Z, LUO X P, et al. Study on the extraction of wheat germ protein by subcritical water and its functional properties[J]. Science and Technology of Food Industry,2016,37(23):193−198,205. [19] 王振斌, 陈兵兵, 刘加友, 等. 超声波和微波技术在芝麻饼粕ACE抑制肽制备中的应用[J]. 中国粮油学报,2015,30(10):100−106. [WANG Z B, CHEN B B, LIU J Y, et al. The application of ultrasonic and microwave technology in ACE inhibitory peptide preparation of sesame cake[J]. Journal of the Chinese Cereals and Oils Association,2015,30(10):100−106. doi: 10.3969/j.issn.1003-0174.2015.10.019 [20] 李永恒, 田双起, 赵仁勇, 等. 微波辅助碱法提取麦胚蛋白及其功能特性的研究[J]. 河南工业大学学报(自然科学版),2018,39(4):14−19. [LI Y H, TIAN S Q, ZHAO R Y, et al. Microwave-assisted alkaline extraction of wheat germ protein and its functional properties[J]. Journal of Henan University of Technology (Natural Science Edition),2018,39(4):14−19. [21] 从艳霞, 郑明明, 郑畅, 等. 微波技术对油菜籽品质影响研究进展[J]. 中国油料作物学报,2019,41(1):151−156. [CONG Y X, ZHENG M M, ZHENG C, et al. Effect of microwave technology on qualities of rapeseed[J]. Chinese Journal of Oil Crop Sciences,2019,41(1):151−156. [22] HARVEY B M R, OAKS A. Characteristics of an acid protease from maize endosperm[J]. Plant Physiology,1974,53(3):449−452. doi: 10.1104/pp.53.3.449
[23] 鲁伟, 任国谱, 宋俊梅. 蛋白水解液中肽含量的测定方法[J]. 食品科学,2005,26(7):169−172. [LU W, REN G P, SONG J M. Determination of content of peptides in protein hydrolysates[J]. Food Science,2005,26(7):169−172. doi: 10.3321/j.issn:1002-6630.2005.07.039 [24] 杨润强, 王淑芳, 顾振新. 麦胚内源蛋白酶主要特性研究[J]. 中国粮油学报,2015,30(9):1−5,12. [YANG R Q, WANG S F, GU Z X. Main properties of wheat germ endogenous protease[J]. Journal of the Chinese Cereals and Oils Association,2015,30(9):1−5,12. doi: 10.3969/j.issn.1003-0174.2015.09.001 [25] XU L, CHEN L, BARKAT A, et al. Impact of germination on nutritional and physicochemical properties of adlay seed (Coixlachrymajobi L.)[J]. Food Chemistry,2017,229:312−318. doi: 10.1016/j.foodchem.2017.02.096
[26] 罗旭, 方芳, 李倩倩, 等. 4种中国大豆萌芽过程活性物质及抗氧化能力变化规律[J]. 核农学报,2018,32(5):952−958. [LUO X, FANG F, LI Q Q, et al. Changes of functional components and antioxidant activities of four Chinese soybean cultivars during germination[J]. Journal of Nuclear Agricultural Sciences,2018,32(5):952−958. doi: 10.11869/j.issn.100-8551.2018.05.0952 [27] LIMMONGKON A, NOPPRANG N, CHAIKEANDEE P, et al. LC-MS/MS profiles and interrelationships between the anti-inflammatory activity, total phenolic content and antioxidant potential of Kalasin 2 cultivar peanut sprout crude extract[J]. Food Chemistry,2018,239:569−578. doi: 10.1016/j.foodchem.2017.06.162
[28] 朱云辉, 郭元新. 响应面法优化发芽苦荞富集γ-氨基丁酸的培养条件[J]. 西北农林科技大学学报(自然科学版),2016,44(11):141−148. [ZHU Y H, GUO Y X. Optimizing culture conditions for GABA accumulation in germinated tartary buckwheat based on response surface methodology[J]. Journal of Northwest Agriculture and Forestry University (Natural Science Edition),2016,44(11):141−148. [29] TYL C, MARTI A, ISMAIL B P. Changes in protein structural characteristics upon processing of gluten-free millet pasta[J]. Food Chemistry,2020,327:127052. doi: 10.1016/j.foodchem.2020.127052
[30] WANG K, LUO Q W, HONG H, et al. Novel antioxidant and ACE inhibitory peptide identified from arthrospira platensis protein and stability against thermal/pH treatments and simulated gastrointestinal digestion[J]. Food Research International,2021,139:109908. doi: 10.1016/j.foodres.2020.109908
[31] ZHENG Y J, SHI P Q, LI Y, et al. A novel ACE-inhibitory hexapeptide from camellia glutelin-2 hydrolysates: Identification, characterization and stability profiles under different food processing conditions[J]. LWT-Food Science and Technology,2021,147:111682. doi: 10.1016/j.lwt.2021.111682
[32] 王淑芳. 麦胚蛋白酶特性与ACE抑制肽制备及其面包研制[D]. 南京: 南京农业大学, 2015. WANG S F. Protease properties and ACE inhibitory peptide preparation from wheat germ and development of bread[D]. Nanjing: Nanjing Agricultural University, 2015.
[33] HUANG S F, GONG Y, LI Y L, et al. Preparation of ACE-inhibitory peptides from milk protein in continuous enzyme membrane reactor with gradient dilution feeding substrate[J]. Process Biochemistry,2020,92:130−137. doi: 10.1016/j.procbio.2020.02.030
[34] MUMFORD R A, PICKETT C B, ZIMMERMAN M, et al. Protease activities present in wheat germ and rabbit reticulocyte lysates[J]. Biochemical and Biophysical Research Communications,1981,103(2):565−572. doi: 10.1016/0006-291X(81)90489-7
-
期刊类型引用(1)
1. 郭元新,郭宇,朱凤,张瑶,王东旭,叶华,俞玥. 微波联合金属离子对麦胚中肽的富集研究. 食品工业科技. 2023(01): 217-223 .  本站查看
本站查看
其他类型引用(2)





 下载:
下载:
 下载:
下载:



