Effect of Stable Chlorine Dioxide Combined with Vacuum Packaging on the Quality of Pike Eel (Muraenesox cinereus) during Frozen Storage
-
摘要: 比较分析3种包装形式对冻藏海鳗品质特性的影响。将新鲜海鳗去除内脏,洗净后切块,分别进行简单封口袋包装(SP)、真空包装(VP)和0.05 g/L稳定态二氧化氯结合真空包装(CP)处理10 min,然后在−18 ℃下冻藏120 d,每20 d取样1次,测定其菌落总数、总挥发性盐基氮(total volatile base nitrogen, TVB-N)含量、色差、肌原纤维蛋白小片化指数(myofibril fragmentation index, MFI)、Ca2+-ATPase活性、羰基含量、过氧化值和丙二醛含量等指标,综合分析不同包装处理对冻藏海鳗品质特性影响。结果表明:随着贮藏时间增加,各组鱼肉中菌落总数、TVB-N含量、MFI值、羰基含量、过氧化值和丙二醛含量均随之升高,SP组增长速率显著高于其他两组,从保鲜效果得知CP组的品质保持效果显著优于其他两组;稳定态二氧化氯结合真空包装处理可有效减缓海鳗冻藏期间的色泽变化;肌原纤维蛋白Ca2+-ATPase活性,随着贮藏时间延长而不断下降,且CP组的下降趋势明显小于其他两组。综上,稳定态二氧化氯结合真空包装处理,对抑制海鳗中微生物的生长繁殖、维持鱼块新鲜度及肌肉品质效果更佳。Abstract: Comparison and analysis of the effects of three types of packaging treatments on the quality characteristics of pike eels during frozen storage. Pike eel were removed from the internal organs, cleaned and cut into pieces, then simply sealed bag packaging, vacuum packaging, soaked in 0.05 g/L stable chlorine dioxide solution for 10 minutes, then dried up and vacuum packaging treatment, which were recorded as simple packaging group, vacuum packaging group and antibacterial vacuum packaging group, respectively. The samples were stored at −18 ℃ for 120 days and sampled every 20 days. The total number of colonies, total volatile base nitrogen(TVB-N), color difference, myofibril fragmentation index(MFI), Ca2+-ATPase activity, carbonyl content, peroxide value and malondialdehyde content were measured. The effects of different packaging treatments on the quality characteristics of frozen pike eel were analyzed. The results showed that with the increase of storage time, the total number of colonies, TVB-N content, MFI value, carbonyl content, peroxide value and malondialdehyde content in each group increased, and the growth rate of the simple packaging group was significantly higher than the other two groups, and the preservation effect of the antibacterial vacuum packaging group was significantly better than the other two groups; the antibacterial vacuum packaging could effectively slow down the color change of pike eel during freezing; the Ca2+-ATPase activity of myogenic fibrin decreased with the extension of storage time, and the decreasing trend of the antibacterial vacuum packaging group was significantly smaller than the other two groups. In summary, the stable state chlorine dioxide combined with vacuum packaging treatment had a better effect on inhibiting the growth and reproduction of microorganisms in pike eels, and maintaining the freshness of fish pieces and muscle quality.
-
Keywords:
- pike eel /
- vacuum packaging /
- frozen storage /
- stable chlorine dioxide /
- quality characteristics
-
海鳗(Muraenesox cinereus),别名勾鱼、狼牙鱼,是海鳗科海鳗属鱼类,其肉厚质细、味道鲜美,营养丰富,为我国重要的上等海洋食用鱼类。海鳗广泛分布于非洲东部、印度洋及西北太平洋,在我国沿海海域也有生产,其中,以东海为主要产区。海鳗鱼体内含有丰富的蛋白质和脂肪,在贮藏及流通时极易发生氧化和微生物污染,导致鱼肉品质劣变。目前,市面上通常使用冷冻方式保存处理海鳗鱼,冻藏可抑制部分微生物繁殖,减缓肌肉中脂肪和蛋白质氧化,保持鱼肉的营养和特有风味。但长时间冻藏会使鱼肉蛋白质和脂肪发生部分氧化[1]。
真空包装处理可将水产品与空气隔绝,抑制部分微生物生长繁殖和氧化反应,保鲜效果好。其中,李伟丽等[2]研究发现,采用气调结合冷藏可延长三文鱼货架期,且真空包装效果更好;王康宇等[3]发现真空包装结合α-生育酚处理复合鲟鱼糜,可有效抑制鱼糜冻藏期间的脂肪和蛋白质氧化。稳定态二氧化氯作为一种安全高效的抑菌剂,近年来广泛应用于水产品及果蔬的保鲜领域。其中,李蓓蓓等[4]研究发现,稳定态二氧化氯结合冰藏,能较好地保持鲈鱼品质,延长货架期。据GB 2760-2014《食品安全国家标准食品添加剂使用标准》[5]规定,稳定态二氧化氯可用于水产品及其制品(仅限鱼类加工)中,最大使用量为0.05 g/kg。杨贤庆等[6]研究发现二氧化氯不但杀菌效果好,且能抗氧化,也不会对罗非鱼鱼丸外观品质造成破坏。目前,关于稳定态二氧化氯结合真空包装处理对鱼类及其制品的保鲜效果的研究报道较少。本研究以海鳗为研究对象,比较了普通包装、真空包装及稳定态二氧化氯结合真空包装三种包装方式,研究其对海鳗鱼冻藏期间品质影响,旨在为海鳗鱼保鲜技术研究提供一定的理论参考。
1. 材料与方法
1.1 材料与仪器
新鲜海鳗鱼 舟山国际水产城,质量约为2.0 kg/尾;稳定态二氧化氯 山东华实药业有限公司;平板计数琼脂(PCA) 青岛海博生物技术有限公司;超微量Ca2+-ATP酶测试盒、丙二醛(MDA)测定试剂盒 南京建成生物工程研究所;氧化镁、硼酸、盐酸、石油醚、冰乙酸、三氯甲烷、乙二胺四乙酸(EDTA)、三氯乙酸、二硝基甲肼(DNPH)、硫代硫酸钠、碘化钾 国药集团化学试剂有限公司;无特殊说明以上试剂均为分析纯。
CF16RN型高速冷冻离心机 日本日立公司;LDZF-50L-I型立式高压蒸汽灭菌器 上海申安医疗器股份有限公司;CS-210型精密色差仪 杭州彩谱科技有限公司;UV-2600型紫外可见分光光度计 上海龙尼柯仪器有限公司;KDN-520型全自动凯氏定氮仪 上海邦亿精密量仪有限公司;SZF-06C型脂肪测定仪 上海力辰邦西仪器科技有限公司。
1.2 实验方法
1.2.1 样品处理及分组
参考李蓓蓓等[4]的方法,并适当修改。将新鲜海鳗去头,解剖去内脏后,清洗干净,切成大小为7 cm×6 cm×3 cm的鱼块,分别用无菌水或稳定态二氧化氯溶液浸泡处理海鳗鱼块10 min后,纱布拭去表面水分后将其分装。实验分组如下:简单包装组:无菌水浸泡后封口袋包装,标注为SP;真空包装组:无菌水浸泡后PE袋抽真空包装,标注为VP;抑菌真空包装组:0.05 g/L稳定态二氧化氯溶液浸泡后PE袋抽真空包装,标注为CP。(在预实验中,设计的抑菌简包组即稳定态二氧化氯结合简单包装处理,在贮藏中效果不佳,为使实验结果清晰,未加入文中对比)各组样品处理后冻藏于−18 ℃冰箱中120 d,期间每隔20 d取样,进行各项指标测定。
1.2.2 菌落总数测定
根据GB/T 4789.2-2016《食品安全国家标准食品微生物学检验菌落总数测定》[7],采用平板计数法进行菌落总数测定。
1.2.3 色差测定
采用色差仪进行色差分析,每组鱼块样品平行测定3次,取平均值为最终测试结果。根据国际标准CIE规定的L*、a*、b*值所表示的色泽,对鱼块肌肉色差结果进行分析。参数中L*代表亮度、a*代表红度值、b*代表黄度值。
1.2.4 TVB-N含量测定
称取10 g切碎的鱼肉于蒸馏管中,加入75 mL水振荡摇匀,浸渍30 min后,参照GB 5009.228-2016《食品安全国家标准食品挥发性盐基氮的测定》[8],使用自动凯氏定氮仪测定。
1.2.5 肌原纤维蛋白提取
参照SUN等[9]法提取海鳗鱼的肌原纤维蛋白。取3 g海鳗鱼肉,切碎加入5倍体积Tris-HCl缓冲液(10 mmol/L,pH7.2),均质4次,每次20 s;6000 r/min离心10 min,取沉淀重复上述操作2次,向沉淀中加入5倍体积的Tris-HCl缓冲液(10 mmol/L,含0.6 mol/L NaCl,pH7.2),均质4次,每次20 s;8000 r/min离心15 min,上清液为肌原纤维蛋白。
1.2.6 肌原纤维蛋白小片化指数(MFI)
参照LI等[10]方法略作修改。称取2 g鱼肉,加入20倍体积预冷缓冲液(4 ℃;含100 mmol/L KCl,11.2 mmol/L K2HPO4,8.8 mmol/L KH2PO4,1 mmol/L EDTA,1 mmol/L MgCl2),在4 ℃下匀浆(8000 r/min,1 min,每20 s静置10 s),纱布过滤去除结缔组织后,进行10000 r/min离心15 min(4 ℃);向离心沉淀中再加入20倍体积预冷缓冲液,重复上述离心条件,去上清液保留沉淀。用以上缓冲液将沉淀制成浓度为0.5 mg/mL肌原纤维蛋白悬浊液,采用双缩脲法在540 nm波长处测定吸光度乘以200即为肌原纤维蛋白MFI值。
1.2.7 Ca2+-ATPase活性测定
根据超微量Ca2+-ATP酶测试盒说明书进行Ca2+-ATPase活性测定。
1.2.8 羰基含量测定
参考XIA等[11]的方法,略作修改。取1 mL肌原纤维蛋白稀释液于试管中,加入1 mL 10 mmol/L DNPH溶液,混匀后置于暗处反应1 h,每10 min进行1次涡旋;反应结束后,加入3 mL 20%三氯乙酸,10000 r/min离心15 min去上清液;沉淀用体积比为1:1的乙酸乙酯和无水乙醇混合溶液洗涤3次,向沉淀中加入3 mL 6 mol/L盐酸胍溶液,37 ℃水浴加热15 min使沉淀溶解;10000 r/min离心10 min,取上清液在370 nm处测OD值,计算肌原纤维蛋白羰基含量。
羰基含量(nmol/mgprot)=A×106ϵ×c 式中:A为吸光度值;
ϵ 为摩尔消光系数,22000 L(mol·cm)−1;c为样品蛋白浓度,mg prot/L。1.2.9 过氧化值含量(Peroxide value,POV)测定
鱼肉样品先经浸提、过滤、旋蒸制得待测试样。根据国标GB 5009.227-2016《食品安全国家标准食品中过氧化值的测定》[12]进行测定。
1.2.10 丙二醛(Malondialdehyde,MDA)含量测定
采用丙二醛试剂盒说明书提供的方法,对海鳗鱼丙二醛含量进行测定。
1.3 数据处理
利用SPSS 20.0软件对数据进行单因素方差分析,采用Origin 2019软件进行绘图,所有实验结果均选取三次重复实验测定的平均值。
2. 结果与分析
2.1 冻藏过程中海鳗鱼菌落总数的变化
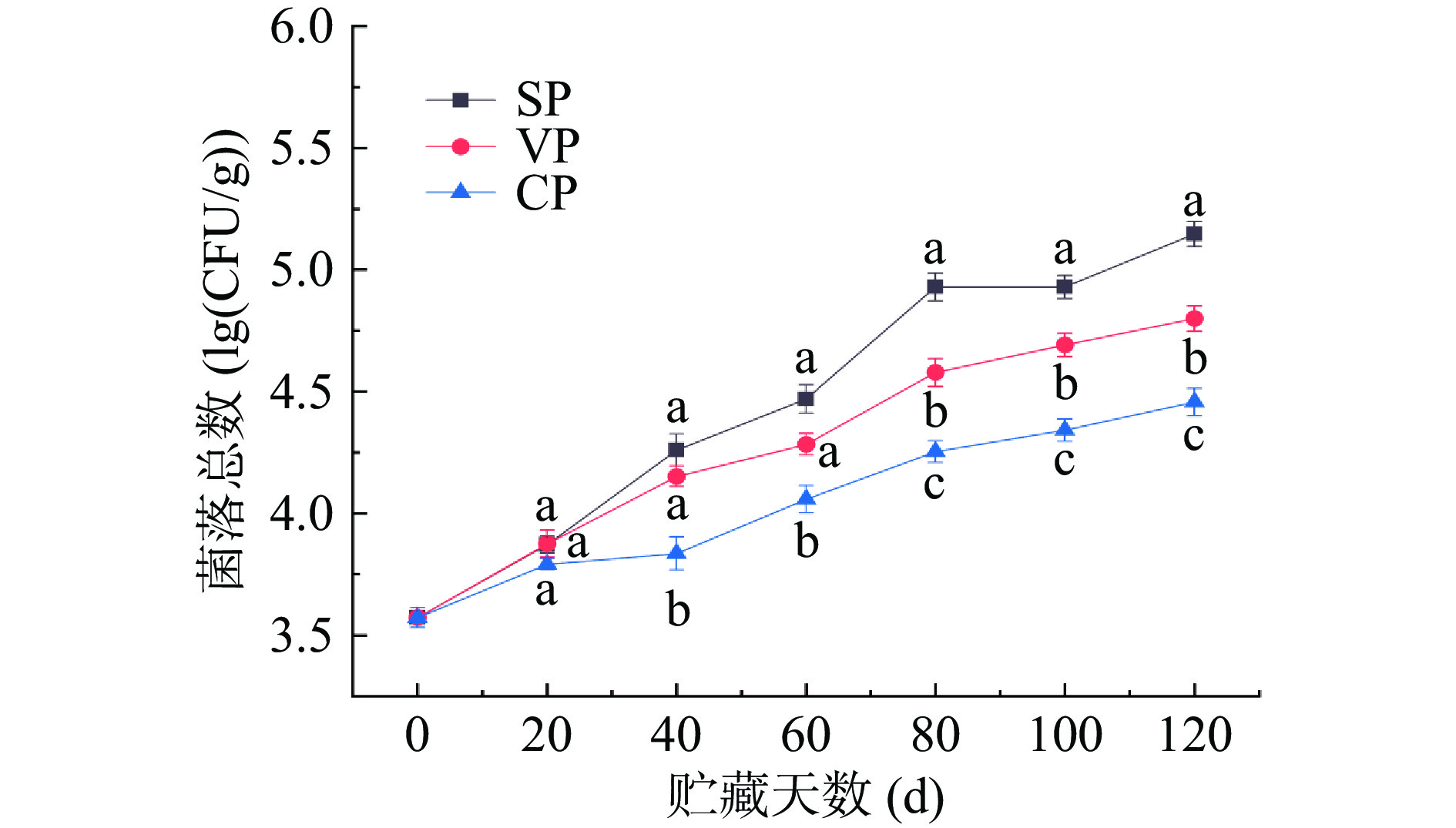
微生物会在海水鱼的捕捞和运输过程中进入其组织肌肉,分解利用鱼体中的蛋白质、脂质等营养物质,并生成腐胺化合物、醛类、醇类等不良风味物质[13]。微生物作用是导致鱼体腐败的重要原因之一,因此可通过微生物指标来判定水产品品质的优劣[14]。由图1可知,新鲜海鳗鱼的菌落总数对数值为(3.57±0.09)lg(CFU/g),肌肉切面鲜亮,富有光泽,有清新的鱼鲜味。随着贮藏时间的延长,各组样品的菌落总数均随之升高。在贮藏前期时(0~20 d),三组样品菌落总数增长缓慢,由于低温环境对微生物的影响,抑制了微生物的生长繁殖,三组样品无显著性差异(P>0.05)。从60 d开始,SP组的细菌增长速率,明显快于VP组和CP组,在60 d时,SP样品肌肉切面稍暗淡,稍有光泽,鱼鲜味较淡;VP和CP组样品肌肉切面较亮,有光泽,较清新鱼鲜味。在贮藏120 d时,SP组样品菌落总数的对数值为(5.16±0.10)lg(CFU/g),肌肉切面暗淡,无光泽,鱼鲜味消失腥味凸显;VP组为(4.80±0.08)lg(CFU/g),肌肉切面稍暗淡,稍有光泽,鱼鲜味变淡;CP组为(4.46±0.06)lg(CFU/g),肌肉切面较亮,稍有光泽,稍有鱼鲜味,无腥味。可见,抑菌结合真空处理的减菌效果较其他两组更显著(P<0.05)。
2.2 冻藏过程中海鳗鱼色差变化
水产品在冻藏过程中,肌肉色泽会发生一定的变化,通过观察色泽变化,可以衡量水产品的品质[15]。由表1可知,随着冻藏时间的增加,三组L*值和b*值均有上升,且差异显著(P<0.05)。a*值则呈现下降趋势,此结果与TIRONI等[16]对黑鲈鱼贮藏色泽变化的研究结果一致。本研究中,各组肌肉L*值的上升,主要由于冻藏过程中形成的冰晶破坏了肌肉组织,自由水增加浮于肌肉表面导致肌肉表面光亮反射,亮度值增加[17]。此外,CP组中的稳定态二氧化氯具有一定的漂白性,也可能是导致肌肉L*值上升的原因之一。海鳗鱼肌肉a*值的下降,可能由于肌肉中肌红蛋白发生氧化,导致鱼体颜色加深[18]。鱼肉b*值在冻藏过程中呈显著上升趋势(P<0.05),表明海鳗肌肉色泽逐渐向黄色过度,可能由于冻藏过程中的脂肪氧化导致,且色素降解反应也会引起b*值的增加[19]。从b*值上升的速度来看,VP组和CP组明显低于简单包装组,表明两种处理均能对鱼肉脂肪氧化起到良好的抑制作用。该结果与随后的肌肉脂质氧化测定结果一致。
表 1 不同处理方式对冻藏过程中海鳗鱼色泽的影响Table 1. Effect of different treatment methods on the color of pike eel during frozen storage指标 贮藏时间(d) SP组 VP组 CP组 L* 0 43.62±0.33dA 43.62±0.33cdA 43.62±0.33cdA 20 47.50±0.32bcA 40.82±1.01dB 45.95±0.96bA 40 46.12±0.55cdB 50.50±0.70aA 43.34±0.43dC 60 50.98±2.03aA 44.02±0.26cB 45.51±0.94bcB 80 48.98±0.50abcAB 50.23±1.61aA 46.17±0.40bB 100 48.10±0.19abcA 46.01±1.83bcA 48.36±0.59aA 120 49.38±0.28abA 48.45±0.45abA 48.84±0.44aA a* 0 −0.77±0.02aA −0.77±0.02aA −0.77±0.02abA 20 −1.55±0.02dC −1.28±0.01bB −0.87±0.08abA 40 −1.25±0.07bB −1.34±0.07bB −0.99±0.02bcA 60 −1.50±0.10cdB −1.39±0.04bB −0.89±0.21abA 80 −1.32±0.08bcB −1.29±0.20bB −0.67±0.14aA 100 −1.55±0.01dB −1.49±0.06bAB −1.23±0.12cA 120 −2.50±0.07eB −1.37±0.12bA −1.26±0.04cA b* 0 −1.79±0.01cA −1.79±0.01eA −1.79±0.01eA 20 −1.29±0.20bA −1.63±0.07cdA −1.31±0.01dA 40 −1.21±0.07bA −1.32±0.36cA −0.85±0.11cA 60 −1.03±0.13bB −1.44±0.25cdC −0.54±0.18abA 80 0.57±0.18aA −0.83±0.27bB −0.69±0.26bcB 100 0.47±0.14aA −0.43±0.18bB −0.39±0.17aB 120 0.39±0.01aA 0.16±0.08aB −0.26±0.04aC 注:同列不同小写字母表示差异显著(P<0.05);同行不同大写字母表示差异显著(P<0.05)。 2.3 冻藏过程中海鳗鱼TVB-N含量变化
TVB-N是指动物性食品在酶和细菌作用下,蛋白质分解而产生的氨以及胺类碱性化合物,其含量可作为衡量水产品品质的重要指标[20]。根据我国水产品行业标准SC/T 3106-2010规定,TVB-N含量在≤15 mg/100 g时为一级品,TVB-N值≤30 mg/100 g时为合格品。由图2可知,新鲜海鳗鱼肌肉TVB-N值为(6.71±0.08) mg/100 g,在冻藏120 d期间,TVB-N含量不断上升。三组样品在120 d贮藏期间均保持一级鲜度,TVB-N值上升幅度不大。在海鳗鱼贮藏前期,SP组和VP组相比较TVB-N值几乎无变化,差异并不显著(P>0.05)。而CP组上升速度缓慢,显著低于其他两组(P<0.05)。以上结果表明,在低温冻藏条件下,微生物不易生长,TVB-N值上升较小;但受低温环境影响,鱼肉中部分内源性蛋白酶发挥作用可能导致部分蛋白质变性,造成TVB-N含量小幅上升[21]。而稳定态二氧化氯的抑菌作用,减少了产酶微生物的总量,抑制内源酶的活性,降低了蛋白质分解速度[22]。由上,稳定态二氧化氯结合真空包装,能有效延缓海鳗冻藏期间的品质劣变,其结果与菌落总数分析结果一致。
2.4 冻藏过程中海鳗鱼肌原纤维蛋白MFI值变化
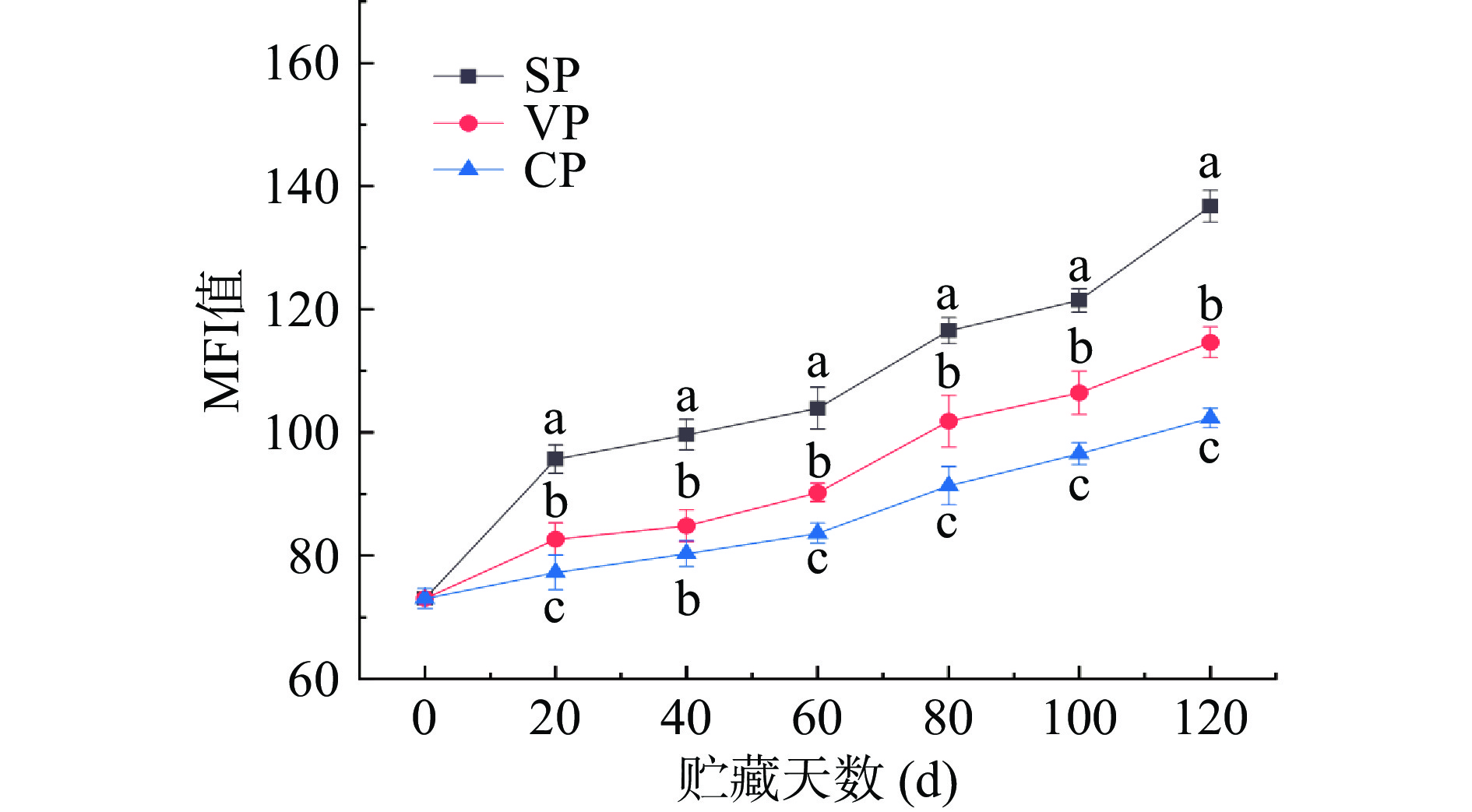
肌原纤维由于蛋白质降解而断裂形成较小片段的现象称作肌原纤维小片化,可用肌原纤维小片化指数(MFI)值表示肌原纤维的受损程度,MFI值越大,肌原纤维内部结构破坏程度越严重[23]。由图3可知,在冻藏期间所有样品的MFI值均保持持续不断上升趋势。SP组的MFI值随着冻藏时间的增加显著上升,第0 d为(73.00±1.61),第20 d则升至(95.60±2.32),与VP组和CP组(82.60±2.64、77.20±2.85)相比较差异显著(P<0.05)。鱼体肌原纤维蛋白MFI值的增加,主要是由于冻藏过程中冰晶的物理损伤所致;此外,在贮藏过程中肌肉中内钙蛋白酶造成部分肌原纤维蛋白发生降解,也使肌原纤维发生断裂[24]。而真空包装和稳定态二氧化氯处理,很好地延缓了肌原纤维内部结构的破坏。张喜才[25]研究发现,与空气包装相比,气调和真空包装在冷藏石斑鱼期间延缓了肌原纤维内部结构被破坏的速率,使MFI值上升较慢。这与本研究结果相一致。
2.5 冻藏过程中海鳗鱼肌原纤维蛋白Ca2+-ATPase活性变化
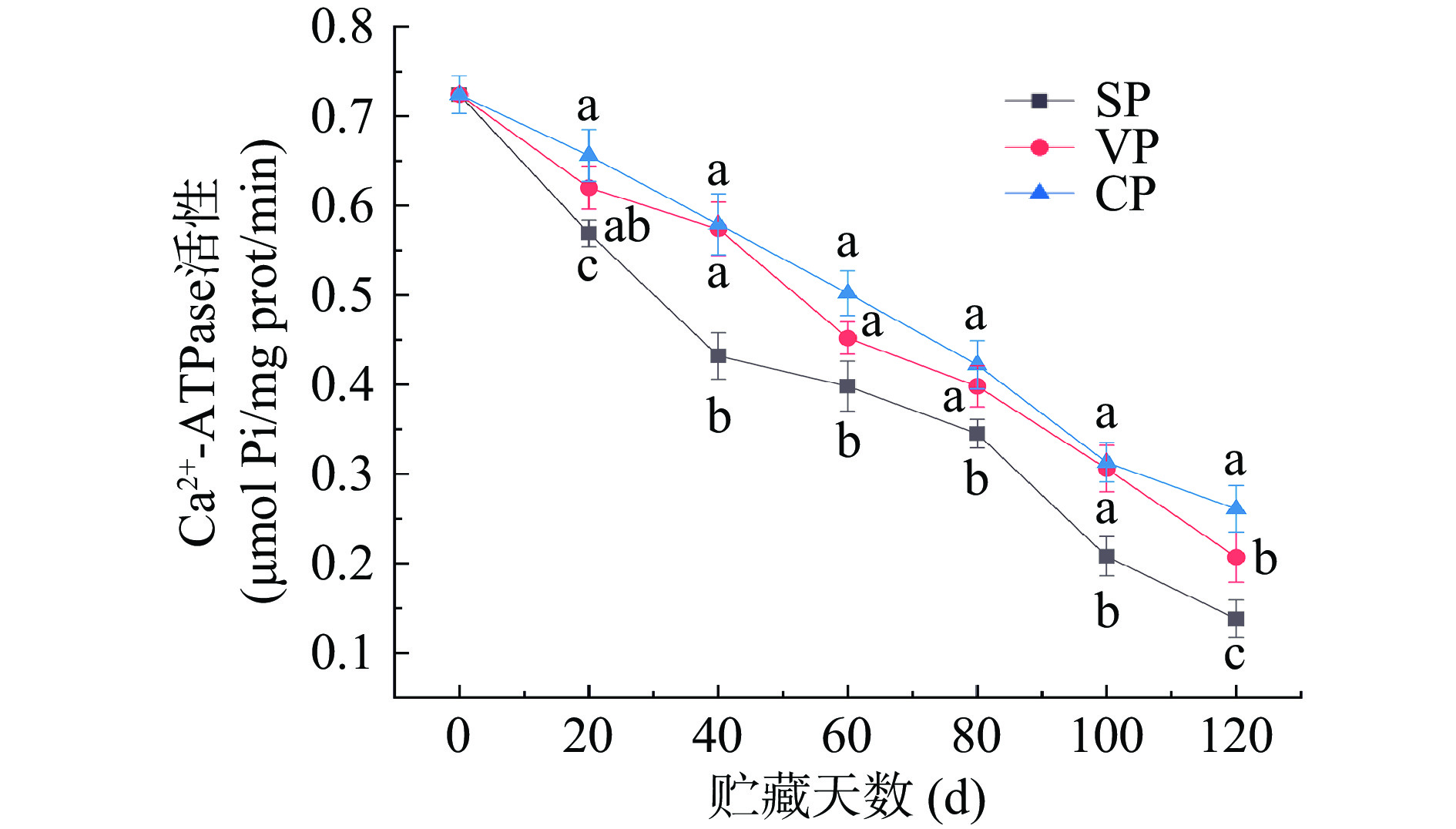
Ca2+-ATPase主要分布在肌球蛋白分子的头部位置,其活性可直接反映肌球蛋白或肌原纤维蛋白分子的完整性,常被用来评估肌原纤维蛋白变性程度[26]。通过测定单位时间内ATPase催化ATP分解生成的无机磷酸含量,来判断海鳗的Ca2+-ATPase活性,结果如图4所示。随着海鳗冻藏时间的增加,三组样品肌原纤维蛋白Ca2+-ATPase活性均呈下降趋势。新鲜海鳗肌原纤维蛋白Ca2+-ATPase活性为(0.72±0.02)μmol Pi/mg prot/min,冻藏40 d时,VP和CP组Ca2+-ATPase活性分别为(0.57±0.03)和(0.58±0.03)μmol Pi/mg prot/min,显著优于SP组(0.43±0.02)μmol Pi/mg prot/min (P<0.05)。贮藏第120 d时,CP组Ca2+-ATPase活性下降了63.95%,VP组下降了71.41%,而SP组则下降了80.94%。在冻藏过程中产生的冰晶会对肌原纤维蛋白结构产生破坏,致使Ca2+-ATPase活性下降[27]。闫春子等[28]研究认为,巯基氧化形成二硫键导致的分子聚合,也是肌原纤维蛋白Ca2+-ATPase酶活性下降的主因之一。本次研究中,VP组和CP组肌原纤维蛋白Ca2+-ATPase活性变化不大,进一步表明真空包装和稳定态二氧化氯能减缓肌肉蛋白质的降解,减少巯基氧化,保持肌肉肌原纤维蛋白的相对稳定。
2.6 冻藏过程中海鳗肌原纤维蛋白羰基含量变化
蛋白质氧化可使部分氨基酸转化成羰基衍生物,羰基可用于表征蛋白质的氧化程度[29]。如图5所示,随着冻藏时间的延长,三组样品的羰基含量均呈上升趋势,新鲜海鳗鱼的羰基含量为(1.34±0.12)nmol/mg prot,在贮藏60 d时,VP组的羰基含量为(2.03±0.13)nmol/mg prot,CP组为(1.93±0.07)nmol/mg prot,两组在贮藏前期间羰基含量上升趋势相对缓慢,60 d内二者之间无显著性差异(P>0.05);贮藏120 d时,VP组和CP组羰基含量分别为(3.27±0.08)和(2.98±0.12)nmol/mg prot,而SP组在120 d时羰基含量为(3.88±0.11)nmol/mg prot,贮藏期间速率显著上升(P<0.05),明显高于VP组和CP组。结果表明,长时间冻藏肌肉蛋白质发生氧化,而真空和稳定态二氧化氯均可有效地抑制蛋白质氧化,阻止其变性,减少羰基化合物的生成。从羰基化合物的生成来看,稳定态二氧化氯结合真空包装对减缓氧化、保持肌肉鲜度效果更好。
2.7 冻藏过程中海鳗鱼肌肉中过氧化值变化
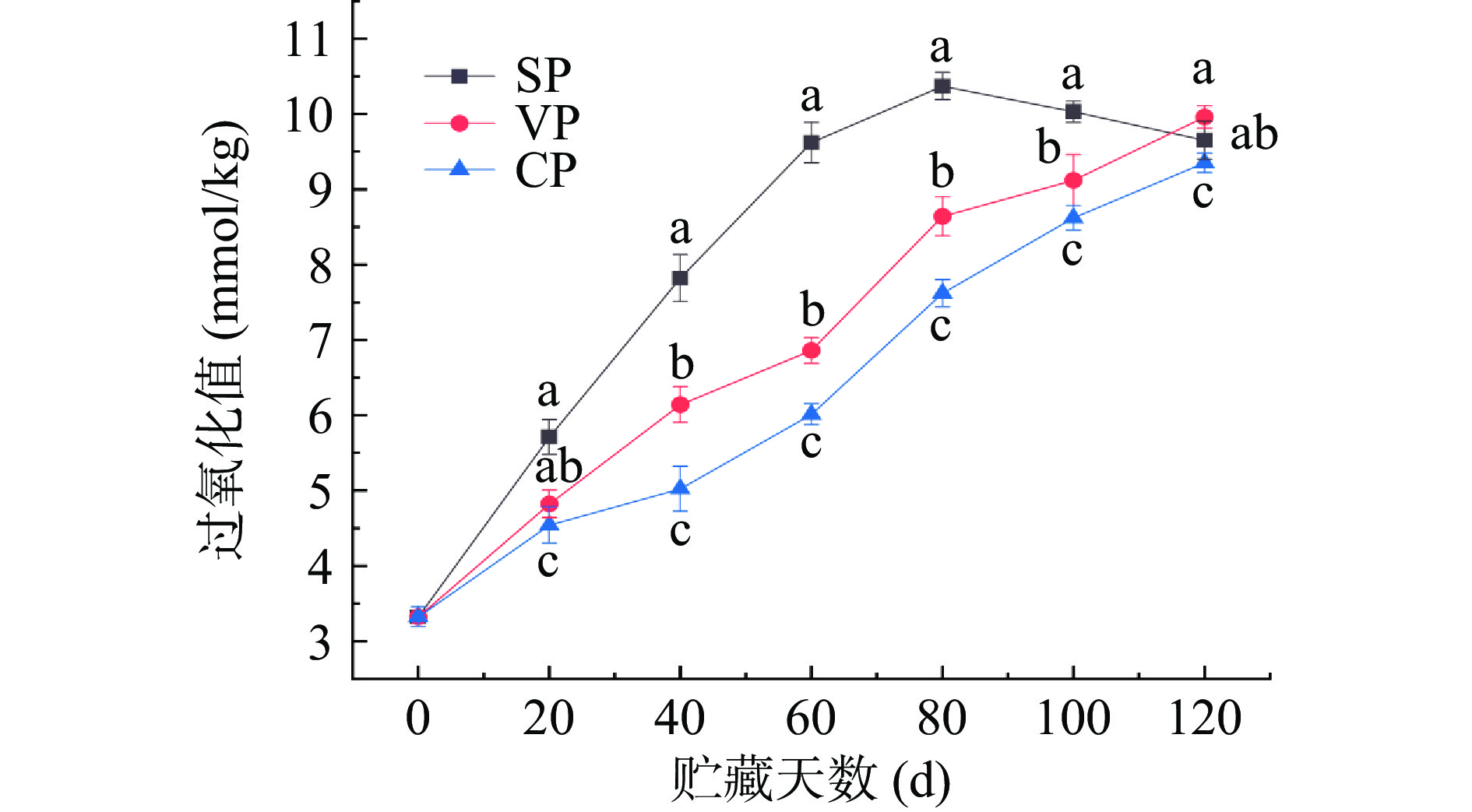
过氧化值(peroxide value,POV)是表征鱼肉脂肪氧化程度的重要指标,通过POV值可判断鱼肉的酸败程度。鱼肉在贮藏过程中脂质会发生氧化,产生酮、醛类等化合物,伴随着难闻的臭味和酸味,严重影响产品品质[30]。冻藏过程中不同处理对海鳗鱼POV值的影响,如图6所示。新鲜海鳗鱼的POV初始值为(3.32±0.13) mmol/kg,随着冻藏时间的延长,过氧化值不断增加,表明各组样品脂质均发生了不同程度的氧化,且初级氧化产物的形成速率高于分解速率。SP组的POV值迅速上升,显著高于VP和CP组(P<0.05),并在第80 d达到最大值(10.37±0.18) mmol/kg;此外,在80 d后开始出现下降趋势,可能由于在贮藏后期,作为初级脂肪氧化产物的过氧化物极其不稳定,容易进一步分解,致使贮藏后期的过氧化物含量不断降低[31];这与FIDALGO等[32]的研究结果一致。而VP组和CP组的POV值,前期缓慢上升,在第60 d开始加快上升速度,到120 d时POV值仍在增加,这是因为真空包装使鱼肉样品避免与氧气接触,但脂肪通过内源酶和微生物的作用仍在进行氧化[33]。由图可知,CP组POV值上升最慢,可能是由于二氧化氯协同发挥作用抑制了氢过氧化物的降解作用造成的。由上,稳定态二氧化氯结合真空包装可在一定程度上减缓贮藏鱼肉中脂肪的酸败进程。
2.8 冻藏过程中海鳗鱼肌肉中丙二醛含量变化
海鳗鱼体内含有丰富的不饱和脂肪酸,在自身和酶的作用下易于氧化成醛、酮、酸等物质[34]。丙二醛(malondialdehyde,MDA)作为脂质氧化的次级产物,其含量可用于表征脂质氧化程度[35]。MDA的含量越高,表明脂质氧化程度越大。根据图7可知,新鲜海鳗鱼鱼肉中MDA初始值为(0.19±0.01) nmol/mg prot。随着贮藏时间的延长,三组MDA含量均逐渐增长,其中以SP组MDA值增长最快,在贮藏120 d时为(0.60±0.02) nmol/mg prot,显著高于其他两组(P<0.05)。VP和CP组,在贮藏前期MDA含量缓慢上升,这可能是因为脂质氧化产生的氢过氧化物,进一步氧化分解生成醛类物质所致。冻藏120 d时,VP组和CP组的MDA值分别为(0.50±0.02)和(0.39±0.02) nmol/mg prot,与SP组相比,分别减少了17.03%和35.23%。由此可说明,在脂质氧化程度上,SP组>VP组>CP组。真空包装隔绝了氧气可有效地缓解脂质氧化,而稳定态二氧化氯结合真空包装效果更优。
3. 结论
研究了简单包装(SP)、真空包装(VP)和稳定态二氧化氯结合真空包装(CP)等三种方式,对海鳗鱼冻藏期间品质的变化影响。结果表明,三组处理在冻藏120 d内菌落总数和TVB-N值均呈现上升趋势,但CP组上升速率明显低于另外两组;在色差变化中,各组肌肉表面L*值和b*均增加,a*值显著下降(P<0.05);随着冻藏时间延长,MFI值和羰基含量不断上升,CP组上升速率最慢;肌原纤维蛋白Ca2+-ATPase活性随着贮藏时间的延长不断下降,且CP组与另两组相比下降速率最小;POV值和MDA含量不断升高,且SP组增长速率明显高于其他两组。由上,稳定态二氧化氯结合真空包装处理可有效抑制蛋白质和脂质氧化,降低微生物影响,保持海鳗鱼在冻藏期间的优良品质。
-
表 1 不同处理方式对冻藏过程中海鳗鱼色泽的影响
Table 1 Effect of different treatment methods on the color of pike eel during frozen storage
指标 贮藏时间(d) SP组 VP组 CP组 L* 0 43.62±0.33dA 43.62±0.33cdA 43.62±0.33cdA 20 47.50±0.32bcA 40.82±1.01dB 45.95±0.96bA 40 46.12±0.55cdB 50.50±0.70aA 43.34±0.43dC 60 50.98±2.03aA 44.02±0.26cB 45.51±0.94bcB 80 48.98±0.50abcAB 50.23±1.61aA 46.17±0.40bB 100 48.10±0.19abcA 46.01±1.83bcA 48.36±0.59aA 120 49.38±0.28abA 48.45±0.45abA 48.84±0.44aA a* 0 −0.77±0.02aA −0.77±0.02aA −0.77±0.02abA 20 −1.55±0.02dC −1.28±0.01bB −0.87±0.08abA 40 −1.25±0.07bB −1.34±0.07bB −0.99±0.02bcA 60 −1.50±0.10cdB −1.39±0.04bB −0.89±0.21abA 80 −1.32±0.08bcB −1.29±0.20bB −0.67±0.14aA 100 −1.55±0.01dB −1.49±0.06bAB −1.23±0.12cA 120 −2.50±0.07eB −1.37±0.12bA −1.26±0.04cA b* 0 −1.79±0.01cA −1.79±0.01eA −1.79±0.01eA 20 −1.29±0.20bA −1.63±0.07cdA −1.31±0.01dA 40 −1.21±0.07bA −1.32±0.36cA −0.85±0.11cA 60 −1.03±0.13bB −1.44±0.25cdC −0.54±0.18abA 80 0.57±0.18aA −0.83±0.27bB −0.69±0.26bcB 100 0.47±0.14aA −0.43±0.18bB −0.39±0.17aB 120 0.39±0.01aA 0.16±0.08aB −0.26±0.04aC 注:同列不同小写字母表示差异显著(P<0.05);同行不同大写字母表示差异显著(P<0.05)。 -
[1] JIANG Q Q, NAKAZAWA N, HU Y Q, et al. Evolution of tissue microstructure, protein properties, and oxidative stability of salted bigeye tuna(Thunnus obesus) meat during frozen storage[J]. LWT-Food Science and Technology,2021,149:111848. doi: 10.1016/j.lwt.2021.111848
[2] 李伟丽, 伍小宇, 王庆慧, 等. 不同包装处理对三文鱼冷藏货架寿命的影响[J]. 西华大学学报(自然科学版),2018,37(2):40−45. [LI W L, WU X Y, WANG Q H, et al. Effects of various packaging on the shelf-life of salmon slice during the cold storage[J]. Journal of Xihua University(Natural Science Edition),2018,37(2):40−45. doi: 10.3969/j.issn.1673-159X.2018.02.008 [3] 王康宇, 王瑞红, 李钰金, 等. α-生育酚处理与真空包装对复合鲟鱼糜冻藏期间品质的影响[J]. 食品科学,2021,42(11):195−204. [WANG K Y, WANG R H, LI Y J, et al. Effects of α-tocopherol and vacuum packaging on the quality of sturgeon surimi incorporated with chicken meat during frozen storage[J]. Food Science,2021,42(11):195−204. doi: 10.7506/spkx1002-6630-20200527-326 [4] 李蓓蓓, 刘书来, 丁玉庭. 二氧化氯减菌处理对鲈鱼品质的影响[J]. 食品科技,2010,35(10):176−179. [LI B B, LIU S L, DING Y T. Effects of chlorine dioxide bacteria reduction treatment on the quality of perch[J]. Food Science and Technology,2010,35(10):176−179. [5] 中华人民共和国家卫生和计划生育委员会. 食品安全国家标准食品添加剂使用标准 GB 2760-2014[S]. 2014: 91−92. National Health and Family Planning Commission, PRC. National food safety standards food additive use standards GB 2760-2014[S]. 2014: 91−92.
[6] 杨贤庆, 张晓丽, 马海霞, 等. 稳定态二氧化氯对罗非鱼鱼丸品质变化的影响[J]. 食品工业科技,2017,38(10):337−340. [YANG X Q, ZHANG X L, MA H X, et al. Effect of stable chlorine dioxide on preservation of tilapia fish-ball[J]. Science and Technology of Food Industry,2017,38(10):337−340. [7] 中华人民共和国家卫生和计划生育委员会. 食品安全国家标准食品微生物学检验菌落总数测定 GB 4789.2-2016[S]. 2016: 1−5. National Health and Family Planning Commission, PRC. National food safety standards food microbiology test determination of the total number of bacteria GB 4789.2-2016[S]. 2016: 1−5.
[8] 中华人民共和国家卫生和计划生育委员会. 食品安全国家标准食品挥发性盐基氮的测定 GB 5009.228-2016[S]. 2016: 3−5. National Health and Family Planning Commission, PRC. National food safety standards determination of volatile salt nitrogen in food GB 5009.228-2016[S]. 2016: 3−5.
[9] SUN F Y, HUANG Q L, HU T, et al. Effects and mechanism of modified starches on the gel properties of myofibrillar protein from grass carp[J]. International Journal of Biological Macromolecules,2014,64(5):17−24.
[10] LI D Y, LIU Z Q, LIU B, et al. Effect of protein oxidation and degradation on texture deterioration of ready-to-eat shrimps during storage[J]. Journal of Food Science,2020,85(9):427−432.
[11] XIA X F, KONG B H, LIU Q, et al. Physicochemical change and protein oxidation in porcine longissimus dorsi as influenced by different freeze thaw cycles[J]. Meat Science,2009,83(2):239−245. doi: 10.1016/j.meatsci.2009.05.003
[12] 中华人民共和国家卫生和计划生育委员会. 食品安全国家标准食品中过氧化值的测定GB 5009.227-2016[S]. 2016: 1−5. National Health and Family Planning Commission, PRC. National food safety standards determination of peroxide value in food GB 5009.227-2016[S]. 2016: 1−5.
[13] 励建荣. 海水鱼类腐败机制及其保鲜技术研究进展[J]. 中国食品学报,2018,18(5):1−12. [LI J R. Research progress on spoilage mechanism and preservation technology of marine fishes[J]. Journal of Chinese Institute of Food Science and Technology,2018,18(5):1−12. [14] 冯豪杰, 蓝蔚青, 刘大勇, 等. 不同减菌化处理方式对暗纹东方鲀冷藏期间品质变化的影响[J]. 食品科学,2020,41(7):210−217. [FENG H J, LAN W Q, LIU D Y, et al. Effects of different sterilization treatments on the quality of puffer fish(Takifugu obscurus) during refrigerated storage[J]. Food Science,2020,41(7):210−217. doi: 10.7506/spkx1002-6630-20190324-308 [15] TOMAC A, MALLO S R, PEREZ S, et al. Vacuum impregnation in Merluccius hubbsi hake fillets brining. Effect on mass transfer kinetics, texture and colour[J]. LWT-Food Science and Technology,2020,119:108892. doi: 10.1016/j.lwt.2019.108892
[16] TIRONI V, LAMBALLERIE M D, LEB A. Quality changes during the frozen storage of sea bass(Dicentrarchus labrax) muscle after pressure shift freezing and pressure assisted thawing[J]. Innovative Food Science & Emerging Technologies,2010,11(4):565−573.
[17] KANNER J, HAREL S. Desferrioxamine as an electron donor. Inhibition of membranal lipid peroxidation initiated by H2O2-activated metmyoglobin and other peroxidizing systems[J]. Free Radical Research Communications,2009,3(5):309−317.
[18] 黄卉, 郑陆红, 李来好, 等. 不同预冷温度对鲈鱼冰藏期间质构和色差的影响[J]. 食品工业科技,2018,39(24):302−308. [HANG H, ZHENG L H, LI L H, et al. Effects of different precooling temperature on texture and color of Micropterus salmoides during ice storage[J]. Science and Technology of Food Industry,2018,39(24):302−308. [19] 黄涵, 徐云强, 熊光权, 等. 冻融循环对鮰鱼片品质的影响[J]. 食品科技,2019,44(6):126−132. [HANG H, XU Y Q, XIONG G Q, et al. Effect of repeated freezing and thawing on the quality of catfish[J]. Food Science and Technology,2019,44(6):126−132. [20] YU D W, JIANG Q X, XU Y H, et al. The shelf life extension of refrigerated grass carp(Ctenopharyngodon idellus) fillets by chitosan coating combined with glycerol monolaurate[J]. International Journal of Biological Macromolecules,2017,101:448−454. doi: 10.1016/j.ijbiomac.2017.03.038
[21] 葛黎红. 内源蛋白酶在低温保鲜草鱼质构劣化中的作用与控制研究[D]. 无锡: 江南大学, 2017: 32−36. GE L H. Effect and control of endogenous protease on texture deterioration of grass carp at low temperature[D]. Wuxi: Jiangnan University, 2017: 32−36.
[22] 季晓彤, 年益莹, 薛鹏, 等. 二氧化氯对鲳鱼微冻贮藏品质的影响[J]. 肉类研究,2018,32(2):46−51. [JI X T, NIAN Y Y, XUE P, et al. Effect of chlorine dioxide on pomfret quality during superchilled storage[J]. Meat Research,2018,32(2):46−51. [23] 田园, 孙志昶, 余群力, 等. 低压电刺激对牦牛肉宰后成熟过程中嫩度及肌纤维超微结构的影响[J]. 食品科学, 2014, 35(7): 43−47. TIAN Y, SUN Z C, YU Q L, et al. Effect of low voltage electrical stimulation on tenderness and myofibrillar microstructure of yak during postmortem aging[J]. Food Science, 2014, 35(7): 43−47.
[24] 孙天利, 张秀梅, 张平, 等. 冰温结合真空包装处理对牛肉组织结构变化的影响[J]. 食品科学,2013,34(22):327−331. [SUN T L, ZHANG X M, ZHANG P, et al. Effect of controlled freezing point storage combined with vacuum packaging on texture and histological structure of beef[J]. Food Science,2013,34(22):327−331. [25] 张喜才. 石斑鱼冷藏过程中品质评价、蛋白变化以及内源性蛋白酶作用机制研究[D]. 上海: 上海海洋大学, 2020: 40−51. ZHANG X C. Study on quality evaluation, protein changes and mechanism of endogenous protease of grouper (Epinephelus coioides) during refrigerated storage[D]. Shanghai: Shanghai Ocean University, 2020: 40−51.
[26] 胡佳慧, 熊光权, 乔宇, 等. 微冻贮藏过程中能量代谢酶活性和蛋白质氧化降解对鲈鱼质构特性的影响[J]. 食品科学,2018,39(23):227−234. [HU J H, XIONG G Q, QIAO Y, et al. Effects of energy metabolism-related enzyme activities and protein oxidation on texture properties of perch(Micropterus salmoides) during superchilled storage[J]. Food Science,2018,39(23):227−234. doi: 10.7506/spkx1002-6630-201823034 [27] SIDDAIAH D, REDDY G V S, RAJU C V. Changes in lipids, proteins and kamaboko forming ability of silver carp(Hypophthalmichthys molitrix) mince during frozen storage[J]. Food Research International,2001,34(1):47−53. doi: 10.1016/S0963-9969(00)00127-7
[28] 闫春子, 夏文水, 许艳顺. 超高压对草鱼肌原纤维蛋白结构的影响[J]. 食品与生物技术学报,2018,37(4):424−428. [YAN C Z, XIA W S, XU Y S. Effect of high hydrostatic pressure processing on myofibril protein structure of grass carp fillets[J]. Journal of Food Science and Biotechnology,2018,37(4):424−428. doi: 10.3969/j.issn.1673-1689.2018.04.014 [29] STADTMAN E R, LEVINE R L. Free radical-mediated oxidation of free amino acids and amino acid residues in proteins[J]. Amino Acids,2003,25(3):207−209.
[30] 武华, 洪惠, 罗永康, 等. 冻藏温度对鳙鱼片脂质特性变化的影响[J]. 中国农业大学学报,2014,19(6):173−178. [WU H, HONG H, LUO Y K, et al. Effects of freezing storage temperature on lipid changes of bighead carp fillets[J]. Journal of China Agricultural University,2014,19(6):173−178. doi: 10.11841/j.issn.1007-4333.2014.06.24 [31] 张皖君, 蓝蔚青, 胡旭敏, 等. 竹叶提取物流化冰与迷迭香提取物流化冰处理对鲈鱼贮藏期间抗氧化活性及微生物作用影响[J]. 中国食品学报,2020,20(7):151−159. [ZHANG W J, LAN W Q, HU X M, et al. Effects of bamboo leaf extraction and rosemary extraction and icing treatment on antioxidant activity and microbial action of perch during storage[J]. Journal of Chinese Institute of Food Science and Technology,2020,20(7):151−159. [32] FIDALGO L G, LEMOS A T, DELGADILLO I, et al. Microbial and physicochemical evolution during hyperbaric storage at room temperature of fresh Atlantic salmon(Salmo salar)[J]. Innovative Food Science and Emerging Technologies,2018,45(10):264−272.
[33] 姚桂晓. 低温下真空包装对水产品营养品质影响的研究[D]. 西安: 西安理工大学, 2020: 55−56. YAO G X. Effect of low-temperature vacuum storage packaging on the nutritional quality of aquatic products[D]. Xi'an: Xi'an University of Technology, 2020: 55−56.
[34] KRIVOSHIK S R, GUARNACCIA A M, FRIED D B, et al. Disrupting fluorescence by mutagenesis in a green fluorescent fatty acid ainding protein from a marine eel[J]. Protein Journal,2020,39(2):34−38.
[35] 王雪松, 谢晶. 不同解冻方式对冷冻竹荚鱼品质的影响[J]. 食品科学,2020,41(23):137−143. [WANG X S, XIE J. Effects of different thawing methods on the quality of frozen horse mackerel[J]. Food Science,2020,41(23):137−143. doi: 10.7506/spkx1002-6630-20191105-050 -
期刊类型引用(8)
1. 胡泽茜,李洋,崔琢玉,黄碧飞. 冷链物流环境下时间温度指示器的制备与应用. 农业工程学报. 2023(22): 246-257 .  百度学术
百度学术
2. 钱艳峰,王娅,张明玥,杜子昂,贾靖璇,万祥龙. 用于监测食品新鲜度的时间-温度指示器研究现状. 食品工业科技. 2022(07): 10-20 .  本站查看
本站查看
3. 俞胡斐,钱静. 不可逆变色油墨的配方设计及其制备. 包装工程. 2022(07): 125-131 .  百度学术
百度学术
4. 孙若楠,张敏,夏斯璇,钱静. 胶态酶型时间温度指示器的制备研究. 包装工程. 2022(09): 115-121 .  百度学术
百度学术
5. 俞胡斐,钱静. 不可逆温敏变色油墨的显色动力学探究. 包装工程. 2022(11): 46-53 .  百度学术
百度学术
6. 张博云,张宇,李庆山,高雪峰,李娇,寇俊杰,徐凤波. 羧甲基纤维素钠/聚乙烯吡咯烷酮与独活提取物复合涂膜对柑橘果实的保鲜效果. 食品工业科技. 2022(22): 353-364 .  本站查看
本站查看
7. 刘冬青,陈朴,臧鹏,杜秉健,徐楠,向红. 时间-温度指示器在食品保质期预测中的应用. 食品工业科技. 2021(22): 1-10 .  本站查看
本站查看
8. 康峻菡,胥义. 基于扩散型TTI与鲜银耳品质关联模型的建立及验证. 中国农学通报. 2020(32): 130-139 .  百度学术
百度学术
其他类型引用(8)







 下载:
下载:



 下载:
下载:



