Characterization and Antioxidant Activity Analysis of Daylily Polysaccharides
-
摘要: 黄花菜是我国传统特色蔬菜干制品。为了挖掘黄花菜功能成分,采用硝酸调节水pH至1.8,提取黄花菜多糖,用Sevag法脱除蛋白,对黄花菜多糖基本特性、理化性质和体外抗氧化活性进行了分析。结果表明:脱除蛋白后黄花菜多糖得率为0.72%,多糖含量为34.91%,半乳糖醛酸含量为26.42%。黄花菜多糖含有高酯果胶,甲酯化程度值为96.13%±0.3%。黄花菜多糖中性糖分主要由半乳糖、葡萄糖、木糖组成,其摩尔比为62.50:17.31:11.30。显微观察发现,黄花菜多糖有絮状结构,表面不平整、不连续。傅里叶变换红外光谱(Fourier transform infrared,FTIR)表明,黄花菜多糖中含有较多的酯键。流变学特性分析表明,随着剪切速率增加,黄花菜多糖溶液的表观黏度先快速下降随后维持在较低水平;在各浓度下,其G'均大于G''。黄花菜多糖峰 1分子量较高,Mw为1310.32 kDa;峰 2分子量相对小很多,Mw为83.81 kDa。抗氧化分析表明黄花菜多糖具有较强的2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸自由基(2,2'-Azinobi-(3-ethylbenzthiazoline-6-sulphonate) radical,ABTS+·)清除能力和铁离子还原能力(Ferric reducing antioxidant power,FRAP)。研究结果为深入了解黄花菜多糖理化性质及其生物活性的开发利用提供了依据。Abstract: Daylily is a traditional and typical dry product in our country. In order to explore the functional components from daylily, daylily polysaccharides were extracted with water adjusted to pH1.8 using nitric acid. Proteins were removed by the Sevag method. The basic characteristics, physical and chemical properties and in vitro antioxidant activity of the daylily polysaccharides were analyzed. The results showed that the yield of daylily polysaccharides after protein removal was 0.72%, the polysaccharide content was 34.91%, and the galacturonic acid content was 26.42%. Daylily polysaccharide contains high-ester pectin, and the degree of methyl esterification was 96.13%±0.3%. The neutral sugar of daylily polysaccharide was mainly composed of galactose, glucose and xylose, and its molar ratio was 62.50:17.31:11.30. Microscopic observation revealed that the daylily polysaccharide had a flocculent structure, and the surface was uneven and discontinuous. The Fourier transform infrared (FTIR) diagram showed that the daylily polysaccharides contained more ester bonds. Analysis of the rheological properties showed that as the shear rate increased, the apparent viscosity of the daylily polysaccharide solution decreased rapidly and then maintained at a low level. At each concentration, its G' was greater than G''. The molecular weight of daylily polysaccharide peak 1 was relatively high, with Mw of 1310.32 kDa. Peak 2 molecular weight was relatively small, with Mw of 83.81 kDa. The rheological properties of the daylily polysaccharide solution showed that the apparent viscosity of the polysaccharide decreased rapidly as the shear rate increased, its G' was greater than G" at all concentrations. Results from antioxidant analysis showed that daylily polysaccharides possessed strong 2,2'-azinobi-(3-ethylbenzthiazoline-6-sulphonate) radical (ABTS+·) scavenging ability and Ferric reducing antioxidant power (FRAP) ability. This study could provide a profound understanding on the physical and chemical properties of daylily polysaccharides and provide a basis for the development and utilization of their biological activities.
-
黄花菜(Hemerocallis citrina Baroni)为阿福花科萱草属植物,在我国南北各地均有栽培。黄花菜营养丰富,含有多糖、类胡萝卜素、类黄酮和维生素等多种生物活性物质,具有抗氧化、抗衰老、抗肿瘤、抗氧化等活性[1]。
目前,对黄花菜多糖的研究引起了学者的广泛关注。黄花菜多糖可采用水提醇沉法、微波提取法、超声波提取法、微波处理-水提醇沉法和超声波处理-水提醇沉法等进行提取,以微波提取法效果最佳[2]。紫外扫描结果表明多糖几乎不含核酸和蛋白质,红外光谱显示黄花菜多糖粗品主要为杂果聚糖[3]。黄花菜多糖具有较强的体内抗肿瘤活性[4],其机制可能与多糖能够提高机体的免疫功能有关。黄花菜粗多糖含量随乙醇提取浓度的升高而增加,对H2O2和·OH自由基的清除效果也明显增强[5]。黄花菜粗多糖是一种具有α-型吡喃糖苷结构的水溶性杂多糖,对金黄色葡萄球菌、铜绿假单胞菌、大肠杆菌具有明显的抑制作用[6]。这些研究表明黄花菜多糖具有较高的应用价值,但是,对黄花菜多糖的组成和特征仍缺乏系统的研究。
基于此,拟采用硝酸调节水pH至1.8从干黄花菜中提取多糖,研究黄花菜多糖的组成、微观结构、分子表征,并系统分析其抗氧化能力,以期为黄花菜多糖功能产品的开发利用提供理论依据。
1. 材料与方法
1.1 材料与仪器
干黄花菜 产于湖南祁东,将干黄花菜在80 ℃烘干约8 h至恒重,粉碎,黄花菜粉末保存于干燥器内待用;透析袋 截留分子量为10 kDa,购于美国MYM生物科技有限公司;1, 1-二苯基-2-三硝基苯肼(DPPH)、2, 2-联氮-二( 3-乙基-苯并噻唑-6-磺酸)(ABTS)、2, 4, 6-三吡啶基-S-三嗪(TPTZ) 美国Sigma试剂公司;优级纯的硝酸等常规试剂 北京试剂公司;牛血清蛋白、考马斯亮蓝 G-250等 北京化学试剂公司;葡萄糖、半乳糖、阿拉伯糖、鼠李糖、果糖、甘露糖、岩藻糖、氢氧化钠、乙酸钠、葡聚糖标准品 色谱纯,Sigma公司。
LGJ-10B 冷冻干燥机 北京四环科学仪器厂有限公司;YB-300 高速多功能粉碎机 永康市速锋工贸有限公司;AgiLent TechnoLogies 1260体积排阻色谱 美国AgiLent科技有限公司;PE-SP100红外光谱仪 美国PerkinELmer公司;YP-2 压片机及模具 上海山岳科学仪器有限公司;S-3400N 扫描电子显微镜 日本Hitachi公司;IB-3溅射镀膜仪 日本Eiko公司;TA60W差热-热重同步分析仪 日本岛津公司;AR 1500流变仪 美国TA仪器公司。
1.2 实验方法
1.2.1 多糖的提取与制备
1.2.1.1 多糖的提取
参考宋贤良等[7]的方法略有修改。量取475 mL蒸馏水,用GR优级纯的硝酸调节pH至1.8,加入25 g黄花菜粉,在75 ℃下振荡提取3.5 h。在8000 r/min离心10 min,收集上清液。用4~5倍的95%乙醇和上清液混合至乙醇终浓度为80%得到絮状沉淀。将絮状沉淀用95%乙醇洗涤沉淀两次,再用丙酮洗涤两次除去脂肪和色素类物质。最后将洗涤后的沉淀用真空干燥箱在40 ℃下干燥即可得粗多糖,测定、计算粗多糖的得率。
粗多糖得率(%)=粗多糖质量(g)黄花菜干粉的质量(g)×100 (1) 1.2.1.2 Sevag法脱除蛋白
用60 ℃热水将得到的粗多糖配成10 mg/mL的溶液,磁力搅拌30 min后,置于4 ℃下过夜,使样品充分溶解。加入等体积的Sevag试剂(V氯仿:V正丁醇=4:1),充分振摇25 min。在4000 r/min离心10 min,弃去下层变性蛋白沉淀,重复3次。把得到的上清液用截留量为10 kDa的透析袋透析3 d,在−40 ℃真空冷冻干燥,得脱除蛋白的多糖,在干燥器内保存备用,用于组分分析、表征和抗氧化活性的研究。
1.2.2 多糖组成分析
1.2.2.1 多糖含量测定
采用蒽酮比色法测定[8]。多糖含量以每克多糖组分所含有的葡萄糖毫克数表示,重复3次。
1.2.2.2 半乳糖醛酸含量测定
采用咔唑比色法测定[8]。GalUA含量以每克多糖组分中所含有的GalUA毫克数表示,重复3次。
1.2.2.3 蛋白质含量测定
采用考马斯亮蓝染色法[9]。蛋白质含量以每克多糖组分所含有的蛋白质毫克数表示,重复3次。
1.2.2.4 甲酯化程度测定
参考Virk等[10]的方法略有修改。量取20 mL 0.5%(w/v)的多糖溶液,加入80 mL去CO2水,充分溶解。以酚酞试剂作为指示剂,用0.05 mol/L NaOH滴定至颜色变成粉红色时,向溶液中再加入15 mL 0.25 mol/L NaOH,在室温下搅拌30 min以水解酯键。再加入15 mL 0.25 mol/L盐酸以中和溶液。然后,用0.05 mol/L NaOH再次滴定至粉红色,重复3次。DM的计算公式为:
DM(%)=(V2V1+V2)×100 (2) 式中:DM为甲酯化程度,%;V1为第一次所用NaOH的体积,mL;V2为第二次所用NaOH的体积,mL。
1.2.2.5 单糖组成分析
采用高效阴离子交换色谱分析法[11]。称取黄花菜多糖10 mg置于水解管中,加入4 mL 2 mol/L的三氟乙酸,充氮1 min以排出管内空气,旋紧螺旋盖,于120 ℃水解1 h,待冷却后用氮气吹干水解液,以除去过量的三氟乙酸,加超纯水定容至10 mL。稀释后,用0.2 μm滤膜过滤,进离子色谱仪分析。
色谱条件:分析柱:Carbo PacTMPA10 4×250 mm analytical;洗脱液:200 mol/L NaOH和1 mol/L NaAc;流速:1 mL/min;进样体积:10 μL;柱温:35 ℃;检测器:脉冲安培检测器,金电极。梯度洗脱条件:A为水,B为200 mol/L NaOH,C为1 mol/L NaAc;0~20 min, 91% A,9% B,0% C;20~20.1 min,86% A,9% B,5% C;20.1~35 min,71% A,9% B,20% C。用5 mg/L的混合单糖通过外标法制作标准曲线,单糖含量以μg/mL表示,重复3次。
1.2.3 多糖结构与表征
1.2.3.1 扫描电镜观察
将黄花菜多糖粘在双面胶台上,用溅射镀膜仪在样品上镀上金膜,扫描电镜观察。
1.2.3.2 FTIR分析
将溴化钾于105 ℃干燥6 h,取200 mg溴化钾于玛瑙研钵中作空白样,充分研磨,置于压片模具中,用压片机压制,压力在25 MPa左右保持60 s,将压好的片固定于检测室中,PE-SP100红外光谱仪设置参数如下:开始:4000 cm−1, 结束:400 cm−1,扫描: T%,扫描次数:16,选定“T%”为测定指标,点击“基底”扫描空白样品作为背景。再取2 mg样品与198 mg溴化钾一起置于研钵中研磨,然后压片、固定,扫描得到样品光谱图,重复3次。
1.2.3.3 流变特性分析
参考Wang等[12]的方法略有修改。用60 ℃热水配制1.0%和2.0%多糖溶液,用磁力搅拌30 min后,置于4 ℃下过夜,使样品充分水合溶解。选择流变仪的流动扫描模式,测定剪切速率范围为0.1~100 s−1,温度为25 ℃,测定表观粘度,绘制流变曲线;再选择流变仪的振荡幅度模式,使振荡频率恒定在1 Hz,在25 ℃下对应变进行扫描(0.01%~10%),复合模量稳定的应变区则为线性黏弹区;在线性黏弹区内选定一恒定应变,选择流变仪的振荡频率模式,在25 ℃下对振荡频率进行扫描(0.1~10 Hz),测定储能模量(G')和损耗模量(G''),重复3次。
1.2.3.4 多糖分子量测定
参照Wang等[12]的方法略有修改,利用高效体积排阻色谱法测定,配制2 mg/mL的多糖溶液,过0.22 µm水相膜,分析前超声排气30 min。取20 μL溶液注入SEC系统进行分析。色谱条件:色谱柱:Agilent PL aquageL-OH MIXED-M 8μm;检测器:Agilent G7801A示差折光检测器;流动相:NaNO3溶液;流速:1 mL/min;柱温:30 ℃;检测器温度:30 ℃;流动泵:Agilent G1311B四元泵;最大压力值:130 Bar。标准品为Mw为135.35、64.65、368、13.05、9.75、5.25和2.7 kDa的葡聚糖,浓度为2 mg/mL。
1.2.4 抗氧化活性测定
1.2.4.1 ABTS+·清除能力测定
参照Li等[13]的方法略有修改。将5 mL 7 mmol/L ABTS溶液与5 mL 2.45 mmol/L过硫酸钾溶液混合,在室温下避光反应16 h,作为ABTS贮液。测定前,用蒸馏水稀释贮液,使其在波长734 nm处的吸光度值为0.70±0.02,作为工作液。然后向3 mL工作液中加入0.4 mL不同浓度的样品,剧烈摇晃30 s,避光静置6 min后,在相同波长处测定吸光度值。重复3次。ABTS·+清除率按照下式计算:
ABTS+⋅清除率(%)=(1−A1A0)×100 (3) 式中,A0为对照的吸光度值,A1为样品的吸光度值。
1.2.4.2 FRAP测定
参照Liu等[14]的方法略有修改。将10 mmol/L TPTZ的盐酸溶液(盐酸摩尔浓度为40 mmol/L)、20 mmol/L FeCl3·6H2O溶液和0.3 mol/L的乙酸钠缓冲溶液(pH3.6)按照1:1:10(v/v/v)混合得到FRAP溶液,并且于37 ℃水浴中温浴保存,此溶液现配现用。在120 μL不同浓度的样品溶液中加入360 μL蒸馏水和3.6 mL FRAP溶液。混匀后于37 ℃水浴保温60 min,取出,于波长593 nm处测定吸光度值,以每毫升不同浓度样品的铁离子还原能力以反应液中FeSO4的摩尔质量表示,重复3次。
1.3 数据处理
使用Excel 2016和Origin 9.0对所有数据进行统计,计算平均值和标准误差并制图;用SPSS Statistics 21.0对所有数据进行方差分析,并进行Duncans’差异显著性分析,P<0.05表示差异显著。
2. 结果与分析
2.1 多糖组成分析
2.1.1 脱除蛋白对黄花菜多糖组分的影响
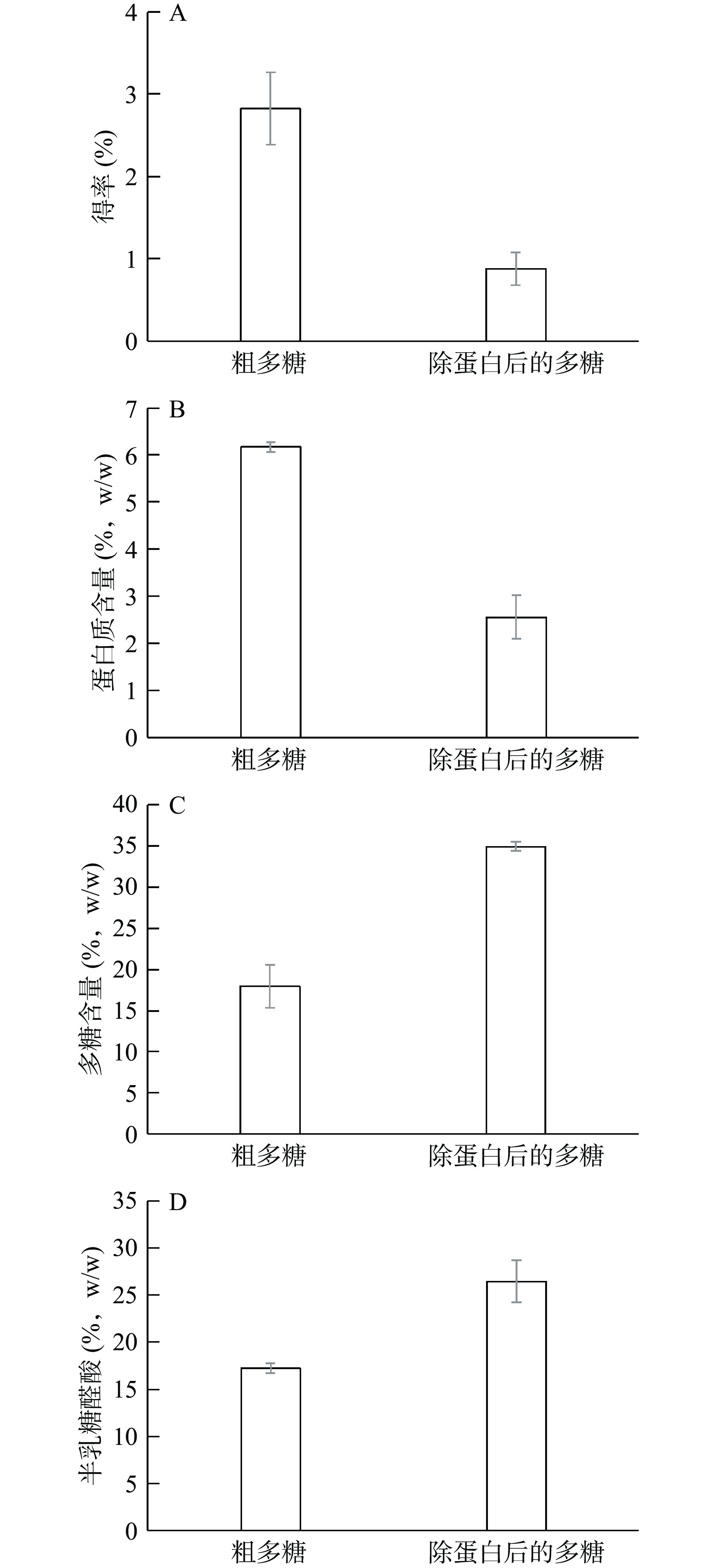
多糖常与蛋白共存或形成糖蛋白复合物。Sevag法可利用有机溶剂使溶液中的蛋白质变性而分离清除蛋白质[11]。结果表明,黄花菜粗多糖得率、蛋白质、多糖、半乳糖醛酸含量分别为2.82%、6.17%、17.93%、17.21%,见图1。脱除蛋白后多糖得率、蛋白质、多糖、半乳糖醛酸含量分别为0.72%、2.55%、34.91%、26.42%。脱除蛋白可以提高多糖的纯度,多糖含量和半乳糖醛酸含量分别提高了16.98%和9.21%。DM为被甲酯化羧基数目占全部羧基数目的百分比,黄花菜多糖DM值为96.13%±0.3%,属高酯果胶,适合用作增稠剂和胶凝剂,可用来改善产品口感。
2.1.2 单糖组成分析
分析黄花菜多糖中的单糖组成,将不同保留时间对应的峰值与标准品进行比较,进而确定单糖种类及相对含量。通过与标准品对照得知,黄花菜多糖中半乳糖醛酸、葡萄糖、半乳糖、木糖含量较高,其他种类糖的含量较低(图2)。黄花菜多糖的单糖组成摩尔比结果见表1。黄花菜多糖主要由半乳糖、葡萄糖、木糖和阿拉伯糖组成,其中半乳糖为主要成分。黄花菜多糖中半乳糖、葡萄糖、木糖摩尔比为62.50:17.31:11.30。这与周纪东等[6]发现的黄花菜粗多糖是一种具有吡喃糖环结构的水溶性杂多糖,且可能是一种与蛋白质或多肽以共价键结合的糖复合物类似。
表 1 黄花菜多糖中单糖组成Table 1. Monosaccharide composition of daylily polysaccharides组分 L-岩藻糖 L-鼠李糖 L-阿拉伯糖 D-半乳糖 D-葡萄糖 D-木糖 D-半乳糖醛酸 D-葡萄糖醛酸 摩尔比(%) 0.17±0.07 2.45±0.37 6.36±0.50 55.90±2.04 18.66±1.15 13.46±0.79 1.85±0.41 1.15±0.05 2.2 多糖的微观结构与表征分析
2.2.1 扫描电镜微观结构
SEM图像提供了黄花菜多糖的表面形貌特征[15]。SEM结果表明,黄花菜多糖有疏松片状结构,相互交叉连接[16](图3A)。放大200倍观察发现多糖极易破裂形成小孔,可能是多糖分子间存在相互排斥力,分子间吸引力较弱,导致片状结构断裂(图3B)。放大2000倍后看到部分丝状物质相互缠绕成非均匀的网状结构,还有少量颗粒物质附着杆状物质表面,使多糖呈现蓬松质轻的表观形态,分子的规整性不强,多糖结构中存在较多支链,且结构中存在较强的分子间相互作用力[17](图3C)。4000倍条件下,可看到表面不平整,有凹陷存在,孔径四周厚度不均一,呈不规则的形状(图3D)。王帅等[18]研究表明多数多糖表面具有孔状的疏松片状结构。Zhu等[19]研究发现,在高倍放大倍数下,多糖表面呈现不均匀的鳞片结构和少量的凹陷。
2.2.2 FTIR分析
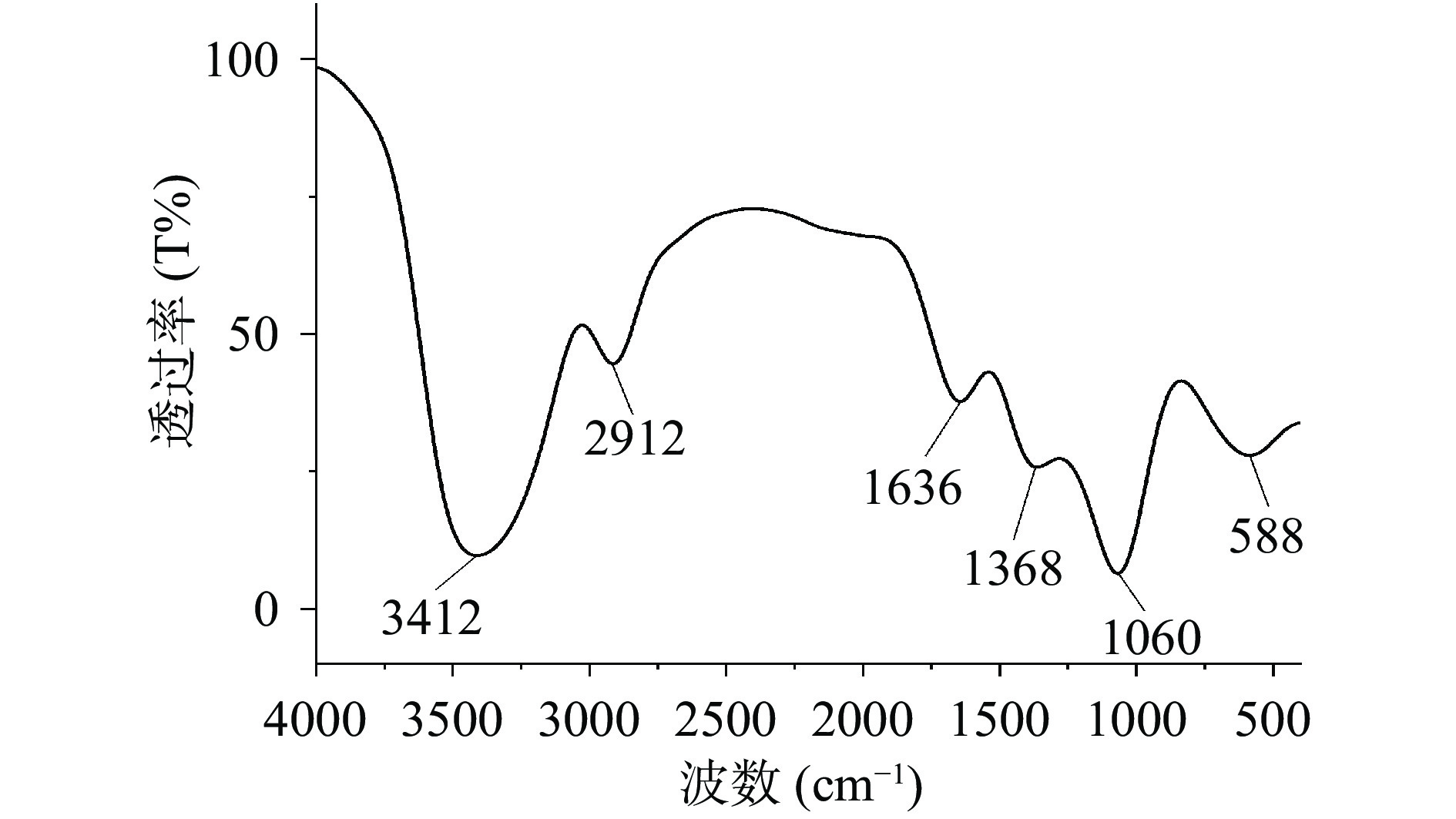
傅里叶变换红外吸收光谱谱图是化合物分子的“指纹图”,可以了解化合物的结构信息。黄花菜多糖的FTIR光谱图(图4)显示其具有多糖的一般结构特征[20]。在3412、2912、1368 cm−1这三个波段的吸收峰,即为糖类化合物的特征吸收峰[21]。最宽的吸收发生在3226~3417 cm−1,它是由O-H的伸缩振动引起的[13,22-23]。2912 cm−1是由C-H产生的伸缩振动峰。在1636 cm−1有吸收,这是由酯化C=O伸缩振动引起的[24],表明多糖中含有较多的酯键,为高酯多糖,这与前文DM值结果一致。1368 cm−1处为C-H弯曲振动吸收峰[20],1013~1120 cm−1由C-OH、C-O-C和C-C伸缩振动引起,1060 cm−1处的峰证实了吡喃环构象的存在[21],表明了多糖中存在吡喃环[23]。以上结果表明,脱除蛋白后多糖具备碳水化合物典型吸收峰,且存在吡喃糖环结构[15]。
2.2.3 流变特性分析
黏度是多糖最明显的乳化特征之一[24]。在剪切速率0.1~10 s−1范围内,随着剪切速率逐渐增大,2%和1%多糖溶液的黏度均迅速下降,溶液呈剪切减薄状态(图5A)。当剪切速率大于10 s−1时,溶液的黏度逐渐趋于稳定。黄花菜多糖溶液显示出典型的“假塑性流体”行为,这是由于剪切力使溶液内部卷曲连接的分子结构被拉直,缠结点减少,从而表现为黏度下降[24]。为了进一步探究黄花菜多糖溶液的粘弹性,在恒定频率1 Hz条件下进行应变扫描,以确定线性粘弹区。2%和1%浓度的黄花菜多糖溶液 G*值变化都比较明显图5B),最终确定将黄花菜多糖在应变为0.1%的条件下进行动态振荡实验。
储能模量G'指粘弹性材料在交变应力作用下一个周期内储存能量的能力,通常指弹性;耗能模量G''指在一个变化周期内所消耗能量的能力,通常指粘性[25]。黄花菜多糖溶液浓度为1.0%和2.0%时的储能模量(G')随着振荡频率的增大均增大,在振荡频率为1 Hz之前浓度为1.0%和2.0%时损耗模量(G'')均有小幅度的波动变化,随后随着振荡频率的增大均增大(图5C)。在各浓度下,其G'均大于G''[25-26],表明在0.1~10 Hz整个频率范围内,多糖溶液表现出弹性行为,呈现凝胶性质[25]。
2.2.4 分子量分布
黄花菜多糖的分子量分布较宽,有两个峰(图6)。表2详细列出了多糖组分的分子量分布情况,组分的分子量较大,重均分子量(Mw)更适合表征它们的分子量[27]。黄花菜多糖峰 1分子量较高,Mw为1310.32 kDa,黄花菜多糖半乳聚糖、阿拉伯聚糖等中性糖侧链含量最为丰富,较高的分支化程度使得其拥有较高的Mw[28];分散性也很大,PD为2.24。黄花菜多糖峰 2分子量相对小很多,Mw为83.81 kDa。多糖来源和制备方法的不同会导致单糖组成和分子量的较大差异,从而影响其生物功能活性[29]。同一来源的多糖由于其分子量的不同,往往具有不同的功能活性,较高分子量的多糖具有更为复杂的结构,其表现出的生物活性也更为广泛,分子量过低,难以形成具有活性的聚合结构 [30]。
表 2 黄花菜多糖的分子量分布情况Table 2. Molecular weight distribution of daylily polysaccharide组成 数均分子量(kDa) 重均分子量(kDa) Z均分子量(kDa) 粘均分子量(kDa) 多分散性(PD) 峰面积比(%) 峰 1 586.19±16.8 1310.32±106.46 7188.11±1381.28 5623.67±1169.17 2.24±0.925 47.48±8.39 峰 2 38.208±0.35 83.81±2.89 129.29±6.09 124.08±5.75 2.19±0.09 52.52±8.39 2.3 多糖的抗氧化活性
随着黄花菜多糖溶液浓度的增加ABTS+·清除能力整体呈逐渐增加的趋势,在5 mg/mL时ABTS+·清除能力达到78.99%(图7A)。FRAP法可作为样品中的总抗氧化能力的指标[31]。黄花菜多糖的FRAP能力在低浓度时随浓度增大变化幅度较小,当浓度大于0.1 mg/mL,黄花菜多糖的FRAP能力随浓度增大而增大,在5 mg/mL时FRAP值达732.75 mmol FeSO4/mL。可见,黄花菜多糖的铁离子还原能力与浓度成正相关(图7B),表明黄花菜多糖具有较好的抗氧化能力,这可能与多糖的单糖组成相关[18]。此外,有研究报道,分子量也是影响多糖抗氧化性的一方面因素[32],分子量高的多糖,生物活性往往较高[18]。多糖的活性还与糖苷键、空间构象等有密切关系,但需要进一步的研究[32]。
3. 结论
探讨了脱除蛋白后黄花菜多糖的结构特性和抗氧化活性,探索了多糖在食品工业中的潜在应用。结果表明,黄花菜中提取多糖得率为0.72%,纯度为34.91%。扫描电镜观察到黄花菜多糖呈絮状结构,互相连接。黄花菜多糖含有高甲酯程度,为大分子量多糖;黄花菜多糖主要由半乳糖、葡萄糖、木糖和阿拉伯糖组成,其中半乳糖为主要成分。FTIR分析表明多糖含有明显的酯键,且存在吡喃糖环结构。黄花菜多糖溶液显示出典型的“假塑性流体”行为,具有凝胶性质。体外抗氧化活性表明,黄花菜多糖对ABTS+·的清除效果和FRAP能力较明显。该研究表明,黄花菜多糖是一种潜在的天然抗氧化剂和胶凝剂,在营养健康产业具有一定的开发应用前景。
-
表 1 黄花菜多糖中单糖组成
Table 1 Monosaccharide composition of daylily polysaccharides
组分 L-岩藻糖 L-鼠李糖 L-阿拉伯糖 D-半乳糖 D-葡萄糖 D-木糖 D-半乳糖醛酸 D-葡萄糖醛酸 摩尔比(%) 0.17±0.07 2.45±0.37 6.36±0.50 55.90±2.04 18.66±1.15 13.46±0.79 1.85±0.41 1.15±0.05 表 2 黄花菜多糖的分子量分布情况
Table 2 Molecular weight distribution of daylily polysaccharide
组成 数均分子量(kDa) 重均分子量(kDa) Z均分子量(kDa) 粘均分子量(kDa) 多分散性(PD) 峰面积比(%) 峰 1 586.19±16.8 1310.32±106.46 7188.11±1381.28 5623.67±1169.17 2.24±0.925 47.48±8.39 峰 2 38.208±0.35 83.81±2.89 129.29±6.09 124.08±5.75 2.19±0.09 52.52±8.39 -
[1] 张运晖, 赵瑛, 欧巧明. 黄花菜采后加工及药用机理研究进展[J]. 安徽农业科学,2020,48(20):6−8. [ZHANG Y H, ZHAO Y, OU Q M. Research progress on postharvest processing and medicinal mechanism of day lily[J]. Journal of Anhui Agricultural Sciences,2020,48(20):6−8. doi: 10.3969/j.issn.0517-6611.2020.20.002 ZHANG Y H, ZHAO Y, OU Q M. Research progress on postharvest processing and medicinal mechanism of day lily[J]. Journal of Anhui Agricultural Sciences, 2020, 48(20): 6-8. doi: 10.3969/j.issn.0517-6611.2020.20.002
[2] 周纪东, 李余动. 黄花菜多糖的不同提取方法及其含量测定的研究[J]. 温州职业技术学院学报,2015,15(1):69−72,88. [ZHOU J D, LI Y D. Study on different extraction methods and their content determination of daylily polysaccharides[J]. Journal of Wenzhou Vocational and Technical College,2015,15(1):69−72,88. ZHOU J D, LI Y D. Study on different extraction methods and their content determination of daylily polysaccharides[J]. Journal of Wenzhou Vocational and Technical College, 2015, 15(1): 69-72, 88.
[3] 丁常泽, 林世家. 黄花菜多糖的提取分离分析[J]. 湖南人文科技学院学报,2009(2):21−23. [DING C Z, LIN S J. Extraction and isolation analysis of daylily polysaccharides[J]. Journal of Hunan Institute of Humanities and Technology,2009(2):21−23. doi: 10.3969/j.issn.1673-0712.2009.02.007 DING C Z, LIN S J. Extraction and isolation analysis of daylily polysaccharides[J]. Journal of Hunan Institute of Humanities and Technology, 2009(2): 21-23. doi: 10.3969/j.issn.1673-0712.2009.02.007
[4] 欧丽兰, 余昕, 张椿, 等. 黄花菜多糖的提取工艺及抗肿瘤活性研究[J]. 四川农业大学学报,2016,34(2):201−205. [OU L L, YU X, ZHANG C, et al. Study on the extraction technology and anti-tumor activity of daylily polysaccharides[J]. Journal of Sichuan Agricultural University,2016,34(2):201−205. OU L L, YU X, ZHANG C, et al. Study on the extraction technology and anti-tumor activity of daylily polysaccharides[J]. Journal of Sichuan Agricultural University, 2016, 34(2): 201-205.
[5] 张宁, 武永福. 黄花菜粗多糖梯度乙醇提取工艺及其抗氧化活性研究[J]. 中国食物与营养,2014,20(11):60−62. [ZHANG N, WU Y F. Study on extraction process and antioxidant activity of crude polysaccharides from daylily by gradient ethanol[J]. Food and Nutrition in China,2014,20(11):60−62. doi: 10.3969/j.issn.1006-9577.2014.11.015 ZHANG N, WU Y F. Study on extraction process and antioxidant activity of crude polysaccharides from daylily by gradient ethanol[J]. Food and Nutrition in China, 2014, 20(11): 60-62. doi: 10.3969/j.issn.1006-9577.2014.11.015
[6] 周纪东, 李余动. 黄花菜多糖的提取、结构性质及抑菌活性[J]. 食品科学,2015,36(8):61−66. [ZHOU J D, LI Y D. Extraction, structural properties and antibacterial activity of daylily polysaccharide[J]. Food Science,2015,36(8):61−66. doi: 10.7506/spkx1002-6630-201508011 ZHOU J D, LI Y D. Extraction, structural properties and antibacterial activity of daylily polysaccharide[J]. Food Science, 2015, 36(8): 61-66. doi: 10.7506/spkx1002-6630-201508011
[7] 宋贤良, 张星启, 蔡纯, 等. 菠萝蜜皮果胶酸提醇沉工艺优化及其结构分析[J]. 南方农业学报,2015,46(4):664−668. [SONG X L, ZHANG X Q, CAI C, et al. Optimization and structure analysis of pectin extraction and alcohol precipitation from jackfruit peel[J]. Journal of Southern Agriculture,2015,46(4):664−668. doi: 10.3969/j.issn.2095-1191.2015.4.664 SONG X L, ZHANG X Q, CAI C, et al. Optimization and structure analysis of pectin extraction and alcohol precipitation from jackfruit peel[J]. Journal of Southern Agriculture, 2015, 46(4): 664-668. doi: 10.3969/j.issn.2095-1191.2015.4.664
[8] 曹建康, 姜微波, 赵玉梅. 果蔬采后生理生化实验指导[M]. 北京: 中国轻工业出版社, 2007: 59-85. CAO J K, JIANG W B, ZHAO Y M. Guidance on postharvest physiological and biochemical experiments of fruits and vegetables[M]. Beijing: China Light Industry Press, 2007: 59-85.
[9] BRADFORD M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J]. Academic Press,1976,72(1−2):248−254.
[10] VIRK B S, SOGI D S. Extraction and characterization of pectin from apple (Malus Pumila. Cv Amri) Peel Waste[J]. International Journal of Food Properties,2004,7(3):693−703. doi: 10.1081/JFP-200033095
[11] 李梦钰, 刘会平, 贾琦, 等. 天冬多糖理化性质和流变学特性研究[J]. 食品与发酵工业,2021,47(5):48−56. [LI M Y, LIU H P, JIA Q, et al. Study on physicochemical properties and rheological properties of polysaccharides from asparaginus[J]. Food and Fermentation Industries,2021,47(5):48−56. LI M Y, LIU H P, JIA Q, et al. Study on physicochemical properties and rheological properties of polysaccharides from asparaginus[J]. Food and Fermentation Industries, 2021, 47(5): 48-56.
[12] WANG L, ZHANG B, XIAO J, et al. Physicochemical, functional, and biological properties of water-soluble polysaccharides from Rosa roxburghii Tratt fruit[J]. Food Chemistry,2018,249:127−135. doi: 10.1016/j.foodchem.2018.01.011
[13] LI C, HUANG Q, FU X, et al. Characterization, antioxidant and immunomodulatory activities of polysaccharides from Prunella vulgaris linn[J]. International Journal of Biological Macromolecules,2015,75:298−305. doi: 10.1016/j.ijbiomac.2015.01.010
[14] LIU H, CAO J, JIANG W. Evaluation and comparison of vitamin c, phenolic compounds, antioxidant properties and metal chelating activity of pulp and peel from selected peach cultivars[J]. LWT-Food Science and Technology,2015,63(2):1042−1048. doi: 10.1016/j.lwt.2015.04.052
[15] 韦志, 阮心眉, 戴涛涛, 等. 碱提砂仁多糖的结构表征及其抗氧化活性研究[J]. 食品工业科技,2021,42(24):87−93. [WEI Z, RUAN X M, DAI T T, et al. Study on structure characterization and antioxidant activity of amomum amomum polysaccharide extracted by alkali[J]. Food Industry Science and Technology,2021,42(24):87−93. WEI Z, RUAN X M, DAI T T, et al. Study on structure characterization and antioxidant activity of amomum amomum polysaccharide extracted by alkali[J]. Food Industry Science and Technology, 2021, 42(24): 87-93.
[16] ZAVASTIN D E, BILIUTĂ G, DODI G, et al. Metal content and crude polysaccharide characterization of selected mushrooms growing in Romania[J]. Journal of Food Composition and Analysis,2018,67(2):149−158.
[17] 徐铮铮. 草菇多糖的分离纯化、生物活性研究及结构分析[D]. 扬州: 扬州大学, 2015. XU Z Z. Isolation, purification, biological activity and structure analysis of Volvulus polysaccharides[D]. Yangzhou: Yangzhou University, 2015.
[18] 王帅, 赵冬雪, 韩成凤, 等. 6种活性多糖的结构、性质及其抗氧化活性的比较研究[J]. 食品研究与开发,2021,42(16):7−15. [WANG S, ZHAO D X, HAN C F, et al. Comparative study on the structure, properties and antioxidant activities of the six active polysaccharides[J]. Food Research and Development,2021,42(16):7−15. WANG S, ZHAO D X, HAN C F, et al. Comparative study on the structure, properties and antioxidant activities of the six active polysaccharides[J]. Food Research and Development, 2021, 42(16): 7-15.
[19] ZHU Y, WANG X, ZHANG C, et al. Characterizations of glucose-rich polysaccharides from Amomum longiligulare T. L. Wu fruits and their effects on immunogenicities of infectious bursal disease virus VP2 protein[J]. International Journal of Biological Macromolecules,2021,183:1574−1584. doi: 10.1016/j.ijbiomac.2021.05.138
[20] 张悦, 陈莹, 郭怡博, 等. 基于化学计量学的金钗石斛不同加工品和干燥品的红外光谱分析[J]. 中南药学,2021,19(3):431−438. [ZHANG Y, CHEN Y, GUO Y B, et al. Infrared spectrum analysis of different processed and dried products of Dendrobium nobile based on stoichiometry[J]. Central South Pharmacy,2021,19(3):431−438. ZHANG Y, CHEN Y, GUO Y B, et al. Infrared spectrum analysis of different processed and dried products of Dendrobium nobile based on stoichiometry[J]. Central South Pharmacy, 2021, 19(3): 431-438.
[21] 黄文利, 欧阳耀铭, 卢玲, 等. 粗壮脉纹孢菌发酵前后豆渣多糖理化性质和结构特性[J]. 食品工业科技,2022,43(3):26−32. [HUANG W L, OU YANG Y M, LU L, et al. Pollycorochemical properties and structural properties of bean residue before and after fermentation[J]. Science and Technology of Food Industry,2022,43(3):26−32. HUANG W L, OU YANG Y M, LU L, et al. Pollycorochemical properties and structural properties of bean residue before and after fermentation[J]. Food Industry Science and Technology, 2022, 43(3): 26-32.
[22] GAO Y F, ZHOU Y B, ZHANG Q, et al. Hydrothermal extraction, structural characterization, and inhibition HeLa cells proliferation of functional polysaccharides from Chinese tea Zhongcha[J]. Journal of Functional Foods,2017,39:1−8. doi: 10.1016/j.jff.2017.09.057
[23] 王艺. 黄精、滇黄精多糖的结构表征与降血糖活性分析[D]. 西安: 陕西师范大学, 2019. WANG Y. The structure characterization and hypoglycemic activity analysis of Polygonatum odoratum and Polygonatum yunnanensis polysaccharides[D]. Xi'an: Shaanxi Normal University, 2019.
[24] 吴潇霞, 陈楠, 白冰瑶, 等. 大果白刺多糖的物理特性及抗氧化活性研究[J]. 食品工业科技,2021,42(23):87−94. [WU X X, CHEN N, BAI B Y, et al. Study on physical properties and antioxidant activity of polysaccharide[J]. Science and Technology of Food Industry,2021,42(23):87−94. WU X X, CHEN N, BAI B Y, et al. Study on physical properties and antioxidant activity of polysaccharide[J]. Food Industry Science and Technology, 2021, 42(23): 87-94.
[25] 马之原, 朱科学, 吴桂萍, 等. 菠萝蜜多糖流变学特性的研究[J]. 食品工业科技,2021,42(23):81−86. [MA Z Y, ZHU H X, WU G P, et al. Rheological properties of jackfruit polysaccharide research[J]. Science and Technology of Food Industry,2021,42(23):81−86. MA Z Y, ZHU H X, WU G P, et al. Rheological properties of jackfruit polysaccharide research[J]. Food Industry Science and Technology, 2021, 42(23): 81-86.
[26] 杨诗沅, 邹宇晓, 黎尔纳, 等. 桑枝多糖与桑枝低聚糖的流变学特性[J]. 食品研究与开发,2021,42(8):1−6. [YANG S Y, ZOU Y X, LI E N, et al. Rheological properties of mulberry branch polysaccharides and mulberry branch oligosaccharides[J]. Food Research and Development,2021,42(8):1−6. YANG S Y, ZOU Y X, LI E N, et al. Rheological properties of mulberry branch polysaccharides and mulberry branch oligosaccharides[J]. Food Research and Development, 2021, 42(8): 1-6.
[27] LI Q Q, LI J, LI H, et al. Physicochemical properties and functional bioactivities of different bonding state polysaccharides extracted from tomato fruit[J]. Carbohydrate Polymers,2019,219:181−190. doi: 10.1016/j.carbpol.2019.05.020
[28] 孙玮璇, 田金虎, 陈健乐, 等. 提取方法对马铃薯渣果胶多糖组成及分子链构象的影响[J]. 中国食品学报,2021,21(7):216−224. [SUN W X, TIAN J H, CHEN J L, et al. Effects of extraction methods on the composition and molecular chain conformation of pectin polysaccharide from potato residue[J]. Chinese Journal of Food Science and Technology,2021,21(7):216−224. SUN W X, TIAN J H, CHEN J L, et al. Effects of extraction methods on the composition and molecular chain conformation of pectin polysaccharide from potato residue[J]. Chinese Journal of Food Science and Technology, 2021, 21(7): 216-224.
[29] WEN Y, GAO L, ZHOU H, et al. Opportunities and challenges of algal fucoidan for diabetes management[J]. Trends in Food Science & Technology,2021,111:628−641.
[30] JIAN H, QIAO F, CHEN J, et al. Physicochemical characterisation of polysaccharides from the seeds and leaves of miracle fruit (Synsepalum dulcificum) and their antioxidant α-glucosidase inhibitory activities in vitro[J]. Journal of Chemistry,2017:1−9.
[31] 羌宇. 类胡萝卜素体外抗氧化、抗肿瘤活性及其构效关系初步研究[D]. 南昌: 南昌大学, 2020. QIANG Y. Preliminary study on in vitro antioxidant and anti-tumor activity of carotenoids[D]. Nanchang: Nanchang University, 2020.
[32] 文愉熙, 黄晓舟, 林晓思. 裸藻非水溶性和水溶性多糖的化学组成及抗氧化活性分析[J]. 食品工业科技,2022,43(5):105−113. [WEN Y X, HUANG X Z, LIN X S. Chemical composition and antioxidant activity analysis of nonwater-soluble and water-soluble polysaccharides in naked algae[J]. Food Industry Science and Technology,2022,43(5):105−113. WEN Y X, HUANG X Z, LIN X S. Chemical composition and antioxidant activity analysis of nonwater-soluble and water-soluble polysaccharides in naked algae[J]. Food Industry Science and Technology, 2022, 43(5): 105-113.
-
期刊类型引用(3)
1. 龙正玉,邹金浩,杨怀谷,任国谱,曹清明,唐道邦. 肉制品发酵技术对肉品品质的调控及应用研究进展. 食品工业科技. 2024(03): 354-362 .  本站查看
本站查看
2. 白婷,王卫,吉莉莉,张佳敏,刘达玉. 浅发酵香肠产品特性及其与中式香肠和西式发酵肠的比较. 成都大学学报(自然科学版). 2022(02): 137-145 .  百度学术
百度学术
3. 张佳敏,袁波,王卫,叶富云,唐春,翁德晖. 品质改良剂对浅发酵腊肠产品特性的影响及主成分分析. 食品工业科技. 2021(18): 244-251 .  本站查看
本站查看
其他类型引用(2)








 下载:
下载:





 下载:
下载:



