Simultaneous Determination of 24 Sulfonamide Antibiotics in Fish Products by QuEChERS with Ultra Performance Liquid Chromatography-Tandem Mass Spectrometry
-
摘要: 采用QuEChERS结合超高效液相色谱-串联质谱(ultra performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)法建立了同时测定鱼肉制品中磺胺二甲嘧啶、磺胺脒、结晶磺胺等24种磺胺类抗生素的分析方法。通过对色谱、质谱条件和QuEChERS前处理技术的优化,确定了最佳的实验条件。样品采用乙腈超声提取,上清液经C18和无水硫酸镁净化,过0.20 μm滤膜后经UPLC-MS/MS检测。以乙腈−0.1%甲酸水溶液为流动相,经Eclipse XDB-C18色谱柱(4.6 mm × 100 mm,1.8 μm)进行分离,在电喷雾电离源(electrospray ionization source,ESI)正离子模式下,进行多反应监测(multiple reaction monitoring,MRM),基质匹配外标法定量。结果表明,在各自线性范围内24种磺胺类抗生素具有良好的线性关系,相关系数(r)大于0.999,在5、10、50 µg/kg 3个加标浓度水平下的平均加标回收率为80.0%~116.4%,相对标准偏差(relative standard deviation,RSD)为0.8%~9.4%(n=7)。方法检出限为0.01~0.48 µg/kg,定量限为0.02~1.59 µg/kg,所测样品均未检出磺胺类抗生素。该方法简单快速、选择性好、灵敏度高,适用于鱼肉制品中24种磺胺类抗生素的高通量检测。
-
关键词:
- 鱼肉制品 /
- 超高效液相色谱-串联质谱 /
- 磺胺类抗生素 /
- QuEChERS
Abstract: A method for the simultaneous determination of 24 sulfonamide antibiotics including sulfamethazine, sulfaguanidine, sulfanilamide and so on in fish products was established by QuEChERS coupled with ultra performance liquid chromatography-tandem mass spectrometry(UPLC-MS/MS). The optimal experimental conditions were determined by optimizing the chromatographic and mass spectrometric conditions and the QuEChERS pre-treatment technique. The samples were extracted by acetonitrile under ultrasonication, and then purified by C18 and anhydrous MgSO4. The solvent was detected by UPLC-MS/MS after filtering through 0.20 μm microporous membrane. The separation was performed on an Eclipse XDB-C18 column (4.6 mm × 100 mm, 1.8 μm) using acetonitrile −0.1% formic acid aqueous solution as the mobile phase, and determined with positive ion mode of electrospray ionization (ESI) under multiple reaction monitoring (MRM). Then the matrix matching external standard method was used for quantitative analysis. The results indicated that the 24 sulfonamide antibiotics showed good linearity in the respective linear range with the correlation coefficients (r) higher than 0.999. The average recoveries at three spiked levels of 5, 10 and 50 µg/kg ranged from 80.0% to 116.4% with the relative standard deviation (RSD) of 0.8%~9.4% (n=7). Moreover, the limits of detection (LOD) were 0.01~0.48 µg/kg and the limits of quantification (LOQ) were 0.02~1.59 µg/kg. The method was simple, rapid, selective and sensitive for the high-throughput detection of 24 sulfonamide antibiotics in fish products. -
磺胺类抗生素是一类具有对位氨基苯磺酰胺结构的抗生素总称[1-2],具有较强的抗菌能力,被广泛应用于预防和控制水产养殖过程中的各种动物疾病,除此之外,还被认为是一种饲料添加剂以促进水产养殖动物生长[3-4]。其作用原理是通过竞争性阻抑叶酸循环过程中的对氨基苯甲酸来达到减少和杀灭细菌核蛋白的目的[5]。此类人工合成的抗生素具有价格低、抗菌范围广、高效、不易分解[6]等特点,但其在动物体内具有作用时间较长、较慢代谢速率等问题,一部分会在动物体内残留,另一部分会随排泄物以原型或代谢物的形式排出体外[7-8]。过量使用磺胺类抗生素会对环境造成一定程度的污染,进而通过食物链在人体内蓄积从而对人体健康造成潜在威胁[9]。磺胺类抗生素长期存在于人类体内会引起急性或慢性中毒,还会影响机体的泌尿、免疫系统,破坏人体的造血系统或产生耐药性等[10-11]。针对动物组织及牛奶中的磺胺类抗生素,欧盟规定其最大残留量为100 µg/kg[12]。我国国家标准GB 31650-2019制订了在动物性食品中磺胺二甲嘧啶的限量为25~100 µg/kg,其他磺胺类抗生素残留总和为100 µg/kg[13]。
目前,对鱼肉中磺胺类抗生素的检测多为其中一种或几种,同时对20种以上磺胺类抗生素的检测报道较少。而且与文献报道的检测鱼肉中磺胺类抗生素的液液萃取法[14]、加速溶剂萃取法[4]、固相萃取法[15-17]等前处理技术相比,QuEChERS法具有操作简便、无需昂贵的仪器、试验成本低、应用范围广等优点。近年来,磺胺类抗生素的检测方法主要有高效液相色谱法(HPLC)[18-20]、液相色谱-串联质谱法(LC-MS/MS)[21-24]、毛细管电泳法[24-25]等。其中,液相色谱-串联质谱法具有灵敏度高、准确度好、能同时分析多种痕量物质等优点[26],适用于多种磺胺类抗生素的检测。如:HOFF等[27]基于液相色谱-串联质谱技术发展了一种测定牛肝中6种磺胺类抗生素的新方法;WANG等[28]建立了超高效液相色谱-串联质谱法分析了畜禽粪便中17种磺胺类抗生素;MARTINS等[29]发展了液相色谱串联质谱法测定牛奶中11种磺胺类抗生素的检测新方法。
鱼作为营养丰富、价格低廉的水产品之一,其组织中磺胺类抗生素的残留检测方法已有报道,而关于基质更加复杂的鱼肉制品中磺胺类抗生素的检测却鲜有报道,因此本文开展鱼肉制品中磺胺类抗生素的检测研究,对完善食品安全监测体系具有重要意义。为此,本研究通过优化QuEChERS前处理方法、色谱和质谱条件,开发了超高效液相色谱-串联质谱(UPLC-MS/MS)测定鱼肉制品中24种磺胺类抗生素的检测方法,为开展鱼肉制品中磺胺类抗生素的残留监测及风险评估提供技术支撑。
1. 材料与方法
1.1 材料与仪器
磺胺脒 纯度>99.0%,美国International L-aboratory公司;其余磺胺类抗生素标准品 纯度>97.0%,德国Dr. Ehrenstorfer Gmb H公司;甲酸、乙酸铵 色谱纯,美国Dikma公司;甲醇 色谱纯,美国Fisher公司;乙腈 色谱纯,德国Merck公司;N-丙基乙二胺(PSA) 美国Dikma公司;C18(40~50 μm) 美国Welch公司;无水硫酸镁、氯化钠 分析纯,天津永大化学试剂有限公司;ZORBAX Eclispse XDB-C18(4.6×100 mm,1.8 μm)、ZORBAX SB-Aq(2.1×150 mm,3.5 μm)、ZORBAX Eclispse Plus C18(2.1×100 mm,1.8 μm) 美国Agilent公司;鱼肉罐头、鱼豆腐、鱼肠、鱼丸和鱼皮等鱼肉制品 当地超市。
AB SCIEX Exion超高效液相色谱仪、TRIPLE QUAD 5500三重四级杆串联质谱仪(配电喷雾源(ESI)及AB SCIEX数据处理软件) 美国AB SCIEX公司;EVAP-12氮吹仪 美国Organomation公司;VXMNAL涡旋振荡器 美国OHAUS公司;T-460/H超声清洗器 德国Elma公司;Milli-Q超纯水机 美国Millipore公司;CR21N高速冷冻离心机 日本日立公司;AE240(精度1/105)电子天平 瑞士Mettler Toledo公司;GM 200研磨机 德国Retsch公司。
1.2 实验方法
1.2.1 标准溶液的配制
称取适量的磺胺类抗生素标准品采用乙腈溶解,配制成1 g/L的单一标准储备液,于−20 ℃冰箱中密封储存。取适量的各标准储备液,以乙腈定容,得到1 mg/L的混合标准溶液[30]。采用鱼肉罐头空白溶液逐级稀释配成各标准物质浓度均为0.1、0.2、0.5、1、2、5、10、20、50、100 µg/L的系列混合标准工作溶液。
1.2.2 样品前处理
准确称取粉碎后的样品1.0 g(精确至0.01 g),放入50 mL离心管中,加入超纯水2 mL和乙腈10 mL,充分涡旋混匀,超声5 min后加入NaCl 1.5 g,涡旋30 s,以8000 r/min在4 ℃下离心5 min。移取7.5 mL上清液至盛有C18 0.3 g和无水MgSO4 0.4 g的离心管中,涡旋混匀30 s,以8000 r/min离心5 min,取上层乙腈5 mL,在40 ℃下氮吹浓缩至近干,用1.0 mL初始流动相复溶,经0.20 µm滤膜过滤,供UPLC-MS/MS测定。
1.2.3 液相色谱条件
ZORBAX Eclipse XDB-C18色谱柱(4.6 mm × 100 mm,1.8 μm);柱温:40 ℃;流速:0.3 mL/min;进样量:2 μL;流动相:A为0.1%甲酸水溶液,B为乙腈;梯度洗脱程序:0.0~7.5 min,21% B;7.5~7.6 min,21%~40% B;7.6~11.0 min,40% B;11.0~11.1 min,40%~75% B;11.1~15.0min,75% B;15.1~18.0min,21% B。
1.2.4 质谱条件
离子源:电喷雾电离源(ESI);扫描方式:正离子扫描;检测方式:多反应监测(MRM);离子化电压:5500 V;离子源温度:550 ℃;气帘气:40 psi;喷雾气:50 psi;辅助气:50 psi。24种磺胺类抗生素的详细质谱参数见表1。
表 1 24种磺胺类抗生素的质谱参数Table 1. Mass spectrometric (MS) parameters for 24 sulfonamides序
号磺胺类抗生素 保留时间
(min)母离子
(m/z)子离子
(m/z)去簇电压
(V)碰撞能
(eV)1 磺胺脒 3.36 215.2 156.0*/108.1 58.1/71.2 20.3/30.9 2 结晶磺胺 3.99 173.0 93.0*/108.1 136.2/106.9 30.2/22.0 3 磺胺二甲
基异嘧啶4.00 279.2 124.2*/186.0 81.8/78.1 27.5/23.0 4 甲氧苄啶 4.46 291.2 230.1*/261.1 77.0/60.3 31.5/34.8 5 磺胺醋酰 5.26 215.1 92.0*/156.1 103.9.116.0 29.0/14.6 6 磺胺噻唑 5.51 256.1 156.1*/108.2 83.8/83.8 21.0/31.8 7 磺胺嘧啶 5.64 251.1 156.2*/108.0 59.7/48.9 22.0/33.0 8 磺胺吡啶 6.24 250.1 156.0*/184.2 73.3/82.1 23.0/23.9 9 磺胺甲基嘧啶 7.10 265.1 156.1*/172.0 40.3/61.1 23.1/23.0 10 磺胺二甲恶唑 7.18 268.2 156.2*/108.0 88.0/81.0 23.7/33.4 11 磺胺甲噻二唑 8.23 271.0 156.0*/108.2 49.2/45.1 20.8/31.3 12 磺胺甲氧哒嗪 8.61 279.2 124.1*/186.2 85.1/77.0 32.1/24.1 13 磺胺二甲嘧啶 8.79 281.0 156.2*/92.1 83.2/77.9 24.0/37.9 14 磺胺对甲氧嘧啶 9.10 281.1 156.1*/108.2 55.0/61.1 24.9/33.2 15 磺胺间甲氧嘧啶 11.26 281.1 156.2*/108.2 56.9/18.1 24.2/35.1 16 磺胺氯达嗪 12.17 285.1 156.2*/108.1 82.0/83.1 21.6/34.0 17 周效磺胺 12.58 311.1 156.0*/108.1 82.1/73.1 24.1/33.0 18 磺胺甲恶唑 12.62 254.1 156.1*/108.2 106.9/84.9 22.3/31.9 19 磺胺二甲异唑 13.04 268.0 156.2*/113.0 87.7/100.2 19.6/21.8 20 苯甲酰磺胺 13.98 277.1 156.1*/92.0 72.9/76.9 17.8/38.8 21 磺胺喹恶啉 14.18 301.1 156.0*/92.1 38.0/47.9 23.2/39.7 22 磺胺地索辛 14.25 371.2 156.2*/108.1 55.0/39.8 27.4/37.9 23 磺胺苯吡唑 14.58 315.2 156.2*/108.2 90.1/93.5 27.7/38.1 24 磺胺硝苯 15.16 336.3 156.2*/294.0 155.2/153.8 17.1/16.9 注:*为定量离子。 1.3 数据处理
采用Analyst软件1.6.3控制仪器、采集数据,MultiQuant 3.0.2软件进行数据处理和标准曲线建立。回收率及信噪比采用Microsoft Office Excel 2007软件计算。提取剂优化和净化剂优化中的回收率的计算均采用两个平行样品取平均值计算,各个条件下回收率的比较采用Origin 2018软件进行分析。精密度选择低、中、高三个浓度,每个浓度梯度取连续采集7针数据的峰面积进行相对标准偏差RSD值的计算。
2. 结果与分析
2.1 质谱条件优化
磺胺类抗生素的结构中含有氨基,容易结合H+,因此,采用正离子模式,以针泵连续进样,首先得到24种磺胺类化合物的各个母离子,分别对其单标标准溶液(50 ng/mL)进行一级质谱扫描(Q1 MS)得到其母离子,然后对其进行子离子全扫描,选择出两个响应信号较强的碎片离子,其中响应值较高的为定量离子,另一个为定性离子,再将母离子和这两个碎片离子组成检测离子对,在MRM模式下优化去簇电压(DP)和碰撞能(CE),优化结果如表1所示。
2.2 色谱条件优化
2.2.1 色谱柱选择
比较了ZORBAX Eclispse XDB-C18(4.6 mm×100 mm,1.8 μm)、ZORBAX SB-Aq(2.1 mm×150 mm,3.5 μm)、ZORBAX Eclispse Plus C18(2.1 mm×100 mm,1.8 μm)3款色谱柱对24种目标物的分离效果。实验结果显示,24种磺胺类抗生素在ZORBAX Eclispse Plus C18和ZORBAX SB-Aq色谱柱上分离度较差;相比而言,在ZORBAX Eclispse XDB-C18色谱柱上具有较好的分离效果且峰形尖锐,因此,选择ZORBAX Eclispse XDB-C18色谱柱分离24种磺胺类抗生素。
2.2.2 流动相优化
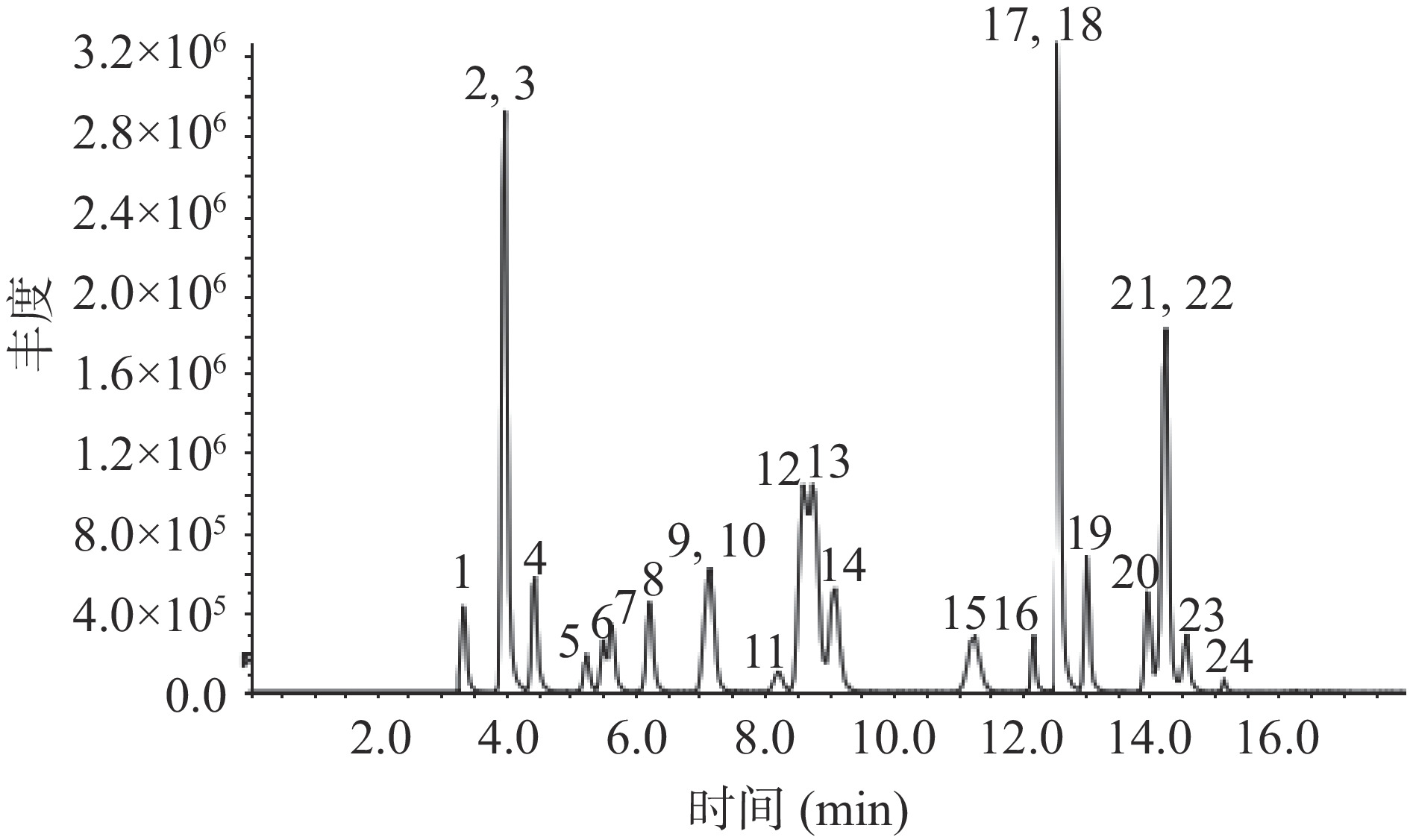
流动相对目标物的保留时间和峰形存在一定的影响。考察了有机相为甲醇、乙腈,水相为水、0.1%甲酸水和2 mmol/L乙酸铵溶液(含0.1%甲酸)时的色谱分离效果。试验结果显示,乙腈相对于甲醇而言具有较好的分离度。当有机相和水相分别为乙腈、纯水时,24种目标物的出现分裂缝且峰形较宽;加入甲酸后,峰形改善且分裂峰减少;而引入乙酸铵后导致磺胺硝苯的响应降低,因此,乙腈-0.1%甲酸水为最优流动相。图1为24种磺胺类抗生素的总离子流色谱图(TIC)。
![]() 图 1 24种磺胺类抗生素标准品的总离子流色谱图(50 μg/L)注:1.磺胺脒;2.结晶磺胺;3.磺胺二甲基异嘧啶;4.甲氧苄啶;5.磺胺醋酰;6.磺胺噻唑;7.磺胺嘧啶;8.磺胺吡啶;9.磺胺甲基嘧啶;10.磺胺二甲恶唑;11.磺胺甲噻二唑;12.磺胺甲氧哒嗪;13.磺胺二甲嘧啶;14.磺胺对甲氧嘧啶;15.磺胺间甲氧嘧啶;16.磺胺氯达嗪;17.周效磺胺;18.磺胺甲恶唑;19.磺胺二甲异唑;20.苯甲酰磺胺;21.磺胺喹恶啉;22.磺胺地索辛;23.磺胺苯吡唑;24.磺胺硝苯。Figure 1. Total ion chromatograms of 24 kinds of sulfonamides standards (50 μg/L)
图 1 24种磺胺类抗生素标准品的总离子流色谱图(50 μg/L)注:1.磺胺脒;2.结晶磺胺;3.磺胺二甲基异嘧啶;4.甲氧苄啶;5.磺胺醋酰;6.磺胺噻唑;7.磺胺嘧啶;8.磺胺吡啶;9.磺胺甲基嘧啶;10.磺胺二甲恶唑;11.磺胺甲噻二唑;12.磺胺甲氧哒嗪;13.磺胺二甲嘧啶;14.磺胺对甲氧嘧啶;15.磺胺间甲氧嘧啶;16.磺胺氯达嗪;17.周效磺胺;18.磺胺甲恶唑;19.磺胺二甲异唑;20.苯甲酰磺胺;21.磺胺喹恶啉;22.磺胺地索辛;23.磺胺苯吡唑;24.磺胺硝苯。Figure 1. Total ion chromatograms of 24 kinds of sulfonamides standards (50 μg/L)2.3 前处理方法优化
2.3.1 提取剂的优化
由于样品基质的复杂性,提取剂应满足既能很好地溶解目标化合物,又能减少对杂质的萃取。乙腈和丙酮是QuEChERS法常用的提取剂,此外酸化乙腈对许多分析物具有良好的萃取效率[31],因此,本实验考察了3种提取剂(乙腈、0.5%酸化乙腈和丙酮)对24种磺胺类抗生素的提取效率。由图2可知,相比于其他两种提取剂,乙腈对24种磺胺类抗生素的回收率均能达到75.5%以上,而且乙腈可以很好地分离蛋白质和脂肪,降低杂质的干扰,因此,最终选择乙腈作为提取剂。
2.3.2 净化剂的优化
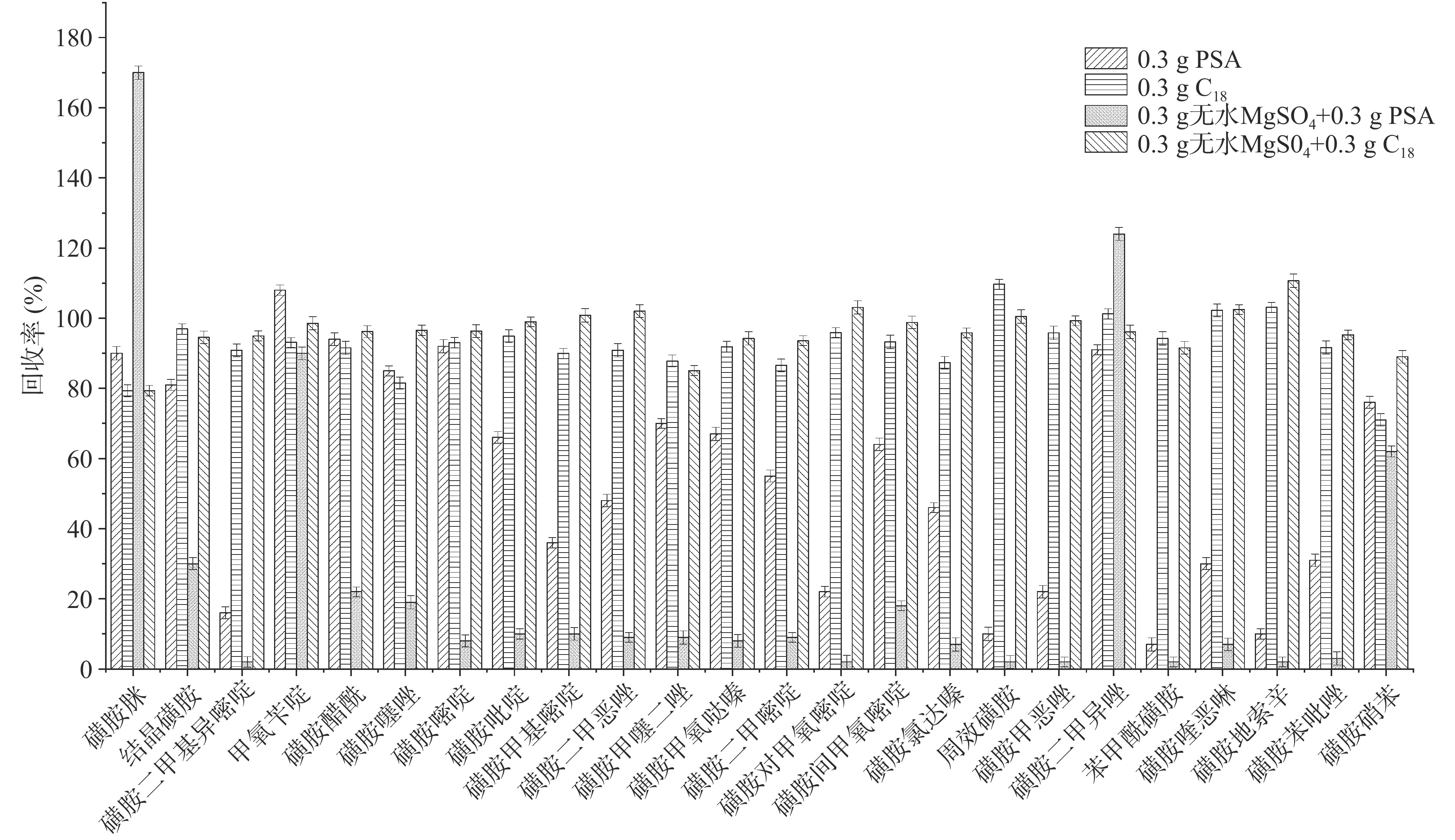
QuEChERS法是利用吸附剂填料与基质中的杂质相互作用,吸附杂质从而达到除杂净化的目的,其操作简便、效率高、试验成本低。QuEChERS法常用的净化剂有PSA、C18、石墨化碳黑等。PSA可用于去除脂肪酸、糖类、有机酸和脂类等一些杂质,而C18能有效去除脂类[32]。本文比较了0.3 g PSA、0.3 g C18、0.3 g无水MgSO4+0.3 g PSA、0.3 g无水MgSO4+0.3 g C18对样品的净化效果(见图3)。试验数据显示,以PSA或无水MgSO4+PSA作为净化剂净化时,15种磺胺类抗生素的回收率低于70.0%,特别是苯甲酰磺胺的回收率为7.3%,可能由于PSA对苯甲酰磺胺有较强的吸附作用。而以C18为净化剂时,24种磺胺类抗生素的回收率整体较高,且无水MgSO4的加入能使24种目标物的回收率达到78%以上。在上述基础上,进一步优化了C18和无水MgSO4的用量,当无水MgSO4为0.3 g时,比较了C18为0.2、0.3、0.4 g时对目标物回收率的影响。结果显示,相比于其它用量,当C18为0.3 g时,24种磺胺类抗生素回收率较好,在79.0%~112.8%之间。固定C18用量为0.3 g,考察了0.2、0.3、0.4、0.5 g无水MgSO4对目标物回收率的影响。随无水MgSO4用量的增加,24种磺胺类抗生素的回收率出现先升高再降低的趋势,当加入无水MgSO4 0.4 g时,24种目标物的回收率最好。综合上述结果,选择0.3 g C18和0.4 g无水MgSO4作为净化剂,24种磺胺类抗生素的回收率能达到84.2%~110.5%之间。
2.4 基质效应
标准曲线分别以基质空白和溶剂配制,根据基质效应计算公式:基质效应=基质标准曲线斜率/溶剂标准曲线斜率×100[33],当基质效应计算值在80.0%~120.0%时,可认为基质效应较弱,可忽略。结果表明,磺胺脒、磺胺二甲基异嘧啶、甲氧苄啶、磺胺醋酰、磺胺甲氧哒嗪、磺胺地索辛、磺胺苯吡唑的基质效应为41.5%~77.6%,具有明显的基质抑制作用,而其它17种磺胺类抗生素的基质效应在82.0%~100.9%之间,基质效应较弱。为了能精准的定量分析,标准曲线采用基质空白提取液配制,以减少因基质效应引起的误差。
2.5 方法学验证
2.5.1 标准曲线、检出限和定量限
在优化的色谱和质谱条件下测定前述1.2部分配制基质匹配标准工作液,标准曲线的横坐标为各目标化合物的浓度,纵坐标为定量离子对峰面积,得到线性回归方程及相关系数(r),检出限(LOD)和定量限(LOQ)分别以3倍和10倍的信噪比计算,见表2。这24种磺胺类抗生素的相关系数(r)均在0.999以上,线性关系良好,LOD和LOQ分别为0.01~0.48 µg/kg和0.02~1.59 µg/kg,能够满足定量分析的要求。
表 2 24种磺胺类抗生素的线性范围、线性回归方程、相关系数、检出限和定量限Table 2. Linear ranges, regression equations, correlation coefficients, limits of detection (LOD) and limits of quantification (LOQ) for detection of 24 kinds of sulfonamides磺胺类抗生素 线性范围(μg/L) 线性方程 相关系数(r) LOD(μg/kg) LOQ(μg/kg) 磺胺脒 0.5~100 Y=38706.0X+1285.6 0.9999 0.48 1.59 结晶磺胺 0.1~100 Y=50961.8X+429.2 0.9998 0.07 0.22 磺胺二甲基异嘧啶 0.1~100 Y=297084.0X+227232.0 0.9997 0.01 0.03 甲氧苄啶 0.5~100 Y=143071.0X+114250.0 0.9991 0.46 1.54 磺胺醋酰 0.1~100 Y=31022.4X+16145.0 0.9991 0.13 0.44 磺胺噻唑 0.1~100 Y=158857.0X+18768.8 0.9991 0.02 0.08 磺胺嘧啶 0.1~100 Y=162054.0X+55211.6 0.9999 0.01 0.02 磺胺吡啶 0.1~100 Y=240612.0X+145528.0 0.9998 0.01 0.03 磺胺甲基嘧啶 0.1~100 Y=171866.0X+89013.4 0.9993 0.01 0.02 磺胺二甲恶唑 0.1~100 Y=176961.0X+10432.8 0.9995 0.02 0.07 磺胺甲噻二唑 0.1~100 Y=87403.6X+668.0 0.9995 0.05 0.15 磺胺甲氧哒嗪 0.1~100 Y=108254.0X+94216.9 0.9996 0.03 0.09 磺胺二甲嘧啶 0.1~100 Y=148426.0X+103685.0 0.9991 0.01 0.03 磺胺对甲氧嘧啶 0.1~100 Y=137057.0X+11984.6 0.9992 0.04 0.13 磺胺间甲氧嘧啶 0.1~100 Y=84598.9X+17802.8 0.9999 0.02 0.08 磺胺氯达嗪 0.1~100 Y=94606.8X+19310.5 0.9997 0.08 0.28 周效磺胺 0.1~100 Y=596140.0X+619509.0 0.9991 0.01 0.02 磺胺甲恶唑 0.1~100 Y=147442.0X+60190.4 0.9991 0.02 0.05 磺胺二甲异唑 0.1~100 Y=128310.0X+9993.8 0.9993 0.01 0.02 苯甲酰磺胺 0.1~100 Y=263456.0X+170164.0 0.9990 0.01 0.02 磺胺喹恶啉 0.1~100 Y=119085.0X+80723.1 0.9996 0.02 0.07 磺胺地索辛 0.1~100 Y=500130.0X+575174.0 0.9992 0.01 0.04 磺胺苯吡唑 0.2~100 Y=65902.4X+52926.6 0.9994 0.26 0.86 磺胺硝苯 0.5~100 Y=11686.6X+2465.5 0.9998 0.40 1.33 2.5.2 加标回收率和精密度
在3个加标浓度分别为5、10和50 µg/kg下对空白样品进行加标回收实验,结果列于表3。24种待测物的平均回收率在80.0%~116.4%范围内,相对标准偏差(RSD)为0.8%~9.4%,适用于鱼肉制品中24种磺胺类抗生素残留的同步快速检测。
表 3 24 种磺胺类抗生素的加标回收率及相对标准偏差(n=7)Table 3. Spiked recoveries and RSD of 24 sulfonamides (n=7)磺胺类抗生素 加标水平(µg/kg) 5 10 50 回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)磺胺脒 82.4 9.1 83.9 6.3 109.3 4.3 结晶磺胺 84.0 7.2 81.0 6.6 94.5 1.8 磺胺二甲基异嘧啶 81.3 4.4 85.0 4.8 108.7 1.9 甲氧苄啶 88.9 4.6 87.5 4.4 103.2 2.5 磺胺醋酰 83.8 7.7 80.4 3.7 104.1 2.1 磺胺噻唑 83.1 3.9 83.0 3.1 93.2 3.5 磺胺嘧啶 83.2 4.5 94.6 3.0 114.0 2.3 磺胺吡啶 83.9 4.4 87.9 3.8 92.6 4.2 磺胺甲基嘧啶 80.4 1.7 81.8 5.7 101.6 2.7 磺胺二甲恶唑 85.7 3.1 93.3 7.1 103.6 5.4 磺胺甲噻二唑 80.7 2.2 81.0 4.1 86.5 4.8 磺胺甲氧哒嗪 80.2 2.6 84.2 7.6 116.4 6.3 磺胺二甲嘧啶 83.3 2.7 85.2 5.8 105.8 3.0 磺胺对甲氧嘧啶 81.6 4.2 89.5 6.4 100.8 3.8 磺胺间甲氧嘧啶 84.6 7.8 96.9 4.6 101.8 3.5 磺胺氯达嗪 80.0 6.1 81.1 9.4 100.9 3.3 周效磺胺 83.6 7.5 84.0 5.4 109.2 1.4 磺胺甲恶唑 85.2 5.9 88.4 4.2 107.3 1.7 磺胺二甲异唑 94.0 2.7 98.0 1.2 112.9 2.5 苯甲酰磺胺 81.8 4.8 84.2 0.8 101.0 2.7 磺胺喹恶啉 88.6 7.9 95.4 4.3 113.0 4.8 磺胺地索辛 85.2 6.3 99.0 7.0 114.0 6.0 磺胺苯吡唑 84.5 4.2 87.1 7.4 90.3 5.6 磺胺硝苯 91.0 6.2 89.4 6.2 106.3 2.4 2.6 实际样品测定
在市内超市采集4份鱼罐头、2份鱼肠、5份鱼豆腐、4份鱼丸、1份鱼皮等16份实际样品,利用本文所建立的超高效液相色谱-串联质谱法对上述样品中24种磺胺类抗生素残留进行检测,16份实际样品均未检出磺胺类抗生素。
3. 结论
采用QuEChERS前处理技术,首次建立了鱼肉制品中24种磺胺类抗生素的超高效液相色谱-串联质谱法检测新方法。24种目标物在各自线性范围内具有良好的线性关系,相关系数均大于0.999,在3个加标浓度水平下的平均加标回收率为80.0%~116.4%,相对标准偏差(RSD)为0.8%~9.4%,检出限和定量限分别为0.01~0.48 µg/kg和0.02~1.59 µg/kg。本方法前处理简便、准确度和精密度高、灵敏度好,适用于鱼肉制品中24种磺胺类抗生素的同步快速检测,为开展鱼肉制品中磺胺类抗生素的监测提供了技术支持,进一步保障了鱼肉制品的质量。
-
图 1 24种磺胺类抗生素标准品的总离子流色谱图(50 μg/L)
注:1.磺胺脒;2.结晶磺胺;3.磺胺二甲基异嘧啶;4.甲氧苄啶;5.磺胺醋酰;6.磺胺噻唑;7.磺胺嘧啶;8.磺胺吡啶;9.磺胺甲基嘧啶;10.磺胺二甲恶唑;11.磺胺甲噻二唑;12.磺胺甲氧哒嗪;13.磺胺二甲嘧啶;14.磺胺对甲氧嘧啶;15.磺胺间甲氧嘧啶;16.磺胺氯达嗪;17.周效磺胺;18.磺胺甲恶唑;19.磺胺二甲异唑;20.苯甲酰磺胺;21.磺胺喹恶啉;22.磺胺地索辛;23.磺胺苯吡唑;24.磺胺硝苯。
Figure 1. Total ion chromatograms of 24 kinds of sulfonamides standards (50 μg/L)
表 1 24种磺胺类抗生素的质谱参数
Table 1 Mass spectrometric (MS) parameters for 24 sulfonamides
序
号磺胺类抗生素 保留时间
(min)母离子
(m/z)子离子
(m/z)去簇电压
(V)碰撞能
(eV)1 磺胺脒 3.36 215.2 156.0*/108.1 58.1/71.2 20.3/30.9 2 结晶磺胺 3.99 173.0 93.0*/108.1 136.2/106.9 30.2/22.0 3 磺胺二甲
基异嘧啶4.00 279.2 124.2*/186.0 81.8/78.1 27.5/23.0 4 甲氧苄啶 4.46 291.2 230.1*/261.1 77.0/60.3 31.5/34.8 5 磺胺醋酰 5.26 215.1 92.0*/156.1 103.9.116.0 29.0/14.6 6 磺胺噻唑 5.51 256.1 156.1*/108.2 83.8/83.8 21.0/31.8 7 磺胺嘧啶 5.64 251.1 156.2*/108.0 59.7/48.9 22.0/33.0 8 磺胺吡啶 6.24 250.1 156.0*/184.2 73.3/82.1 23.0/23.9 9 磺胺甲基嘧啶 7.10 265.1 156.1*/172.0 40.3/61.1 23.1/23.0 10 磺胺二甲恶唑 7.18 268.2 156.2*/108.0 88.0/81.0 23.7/33.4 11 磺胺甲噻二唑 8.23 271.0 156.0*/108.2 49.2/45.1 20.8/31.3 12 磺胺甲氧哒嗪 8.61 279.2 124.1*/186.2 85.1/77.0 32.1/24.1 13 磺胺二甲嘧啶 8.79 281.0 156.2*/92.1 83.2/77.9 24.0/37.9 14 磺胺对甲氧嘧啶 9.10 281.1 156.1*/108.2 55.0/61.1 24.9/33.2 15 磺胺间甲氧嘧啶 11.26 281.1 156.2*/108.2 56.9/18.1 24.2/35.1 16 磺胺氯达嗪 12.17 285.1 156.2*/108.1 82.0/83.1 21.6/34.0 17 周效磺胺 12.58 311.1 156.0*/108.1 82.1/73.1 24.1/33.0 18 磺胺甲恶唑 12.62 254.1 156.1*/108.2 106.9/84.9 22.3/31.9 19 磺胺二甲异唑 13.04 268.0 156.2*/113.0 87.7/100.2 19.6/21.8 20 苯甲酰磺胺 13.98 277.1 156.1*/92.0 72.9/76.9 17.8/38.8 21 磺胺喹恶啉 14.18 301.1 156.0*/92.1 38.0/47.9 23.2/39.7 22 磺胺地索辛 14.25 371.2 156.2*/108.1 55.0/39.8 27.4/37.9 23 磺胺苯吡唑 14.58 315.2 156.2*/108.2 90.1/93.5 27.7/38.1 24 磺胺硝苯 15.16 336.3 156.2*/294.0 155.2/153.8 17.1/16.9 注:*为定量离子。 表 2 24种磺胺类抗生素的线性范围、线性回归方程、相关系数、检出限和定量限
Table 2 Linear ranges, regression equations, correlation coefficients, limits of detection (LOD) and limits of quantification (LOQ) for detection of 24 kinds of sulfonamides
磺胺类抗生素 线性范围(μg/L) 线性方程 相关系数(r) LOD(μg/kg) LOQ(μg/kg) 磺胺脒 0.5~100 Y=38706.0X+1285.6 0.9999 0.48 1.59 结晶磺胺 0.1~100 Y=50961.8X+429.2 0.9998 0.07 0.22 磺胺二甲基异嘧啶 0.1~100 Y=297084.0X+227232.0 0.9997 0.01 0.03 甲氧苄啶 0.5~100 Y=143071.0X+114250.0 0.9991 0.46 1.54 磺胺醋酰 0.1~100 Y=31022.4X+16145.0 0.9991 0.13 0.44 磺胺噻唑 0.1~100 Y=158857.0X+18768.8 0.9991 0.02 0.08 磺胺嘧啶 0.1~100 Y=162054.0X+55211.6 0.9999 0.01 0.02 磺胺吡啶 0.1~100 Y=240612.0X+145528.0 0.9998 0.01 0.03 磺胺甲基嘧啶 0.1~100 Y=171866.0X+89013.4 0.9993 0.01 0.02 磺胺二甲恶唑 0.1~100 Y=176961.0X+10432.8 0.9995 0.02 0.07 磺胺甲噻二唑 0.1~100 Y=87403.6X+668.0 0.9995 0.05 0.15 磺胺甲氧哒嗪 0.1~100 Y=108254.0X+94216.9 0.9996 0.03 0.09 磺胺二甲嘧啶 0.1~100 Y=148426.0X+103685.0 0.9991 0.01 0.03 磺胺对甲氧嘧啶 0.1~100 Y=137057.0X+11984.6 0.9992 0.04 0.13 磺胺间甲氧嘧啶 0.1~100 Y=84598.9X+17802.8 0.9999 0.02 0.08 磺胺氯达嗪 0.1~100 Y=94606.8X+19310.5 0.9997 0.08 0.28 周效磺胺 0.1~100 Y=596140.0X+619509.0 0.9991 0.01 0.02 磺胺甲恶唑 0.1~100 Y=147442.0X+60190.4 0.9991 0.02 0.05 磺胺二甲异唑 0.1~100 Y=128310.0X+9993.8 0.9993 0.01 0.02 苯甲酰磺胺 0.1~100 Y=263456.0X+170164.0 0.9990 0.01 0.02 磺胺喹恶啉 0.1~100 Y=119085.0X+80723.1 0.9996 0.02 0.07 磺胺地索辛 0.1~100 Y=500130.0X+575174.0 0.9992 0.01 0.04 磺胺苯吡唑 0.2~100 Y=65902.4X+52926.6 0.9994 0.26 0.86 磺胺硝苯 0.5~100 Y=11686.6X+2465.5 0.9998 0.40 1.33 表 3 24 种磺胺类抗生素的加标回收率及相对标准偏差(n=7)
Table 3 Spiked recoveries and RSD of 24 sulfonamides (n=7)
磺胺类抗生素 加标水平(µg/kg) 5 10 50 回收率
(%)RSD
(%)回收率
(%)RSD
(%)回收率
(%)RSD
(%)磺胺脒 82.4 9.1 83.9 6.3 109.3 4.3 结晶磺胺 84.0 7.2 81.0 6.6 94.5 1.8 磺胺二甲基异嘧啶 81.3 4.4 85.0 4.8 108.7 1.9 甲氧苄啶 88.9 4.6 87.5 4.4 103.2 2.5 磺胺醋酰 83.8 7.7 80.4 3.7 104.1 2.1 磺胺噻唑 83.1 3.9 83.0 3.1 93.2 3.5 磺胺嘧啶 83.2 4.5 94.6 3.0 114.0 2.3 磺胺吡啶 83.9 4.4 87.9 3.8 92.6 4.2 磺胺甲基嘧啶 80.4 1.7 81.8 5.7 101.6 2.7 磺胺二甲恶唑 85.7 3.1 93.3 7.1 103.6 5.4 磺胺甲噻二唑 80.7 2.2 81.0 4.1 86.5 4.8 磺胺甲氧哒嗪 80.2 2.6 84.2 7.6 116.4 6.3 磺胺二甲嘧啶 83.3 2.7 85.2 5.8 105.8 3.0 磺胺对甲氧嘧啶 81.6 4.2 89.5 6.4 100.8 3.8 磺胺间甲氧嘧啶 84.6 7.8 96.9 4.6 101.8 3.5 磺胺氯达嗪 80.0 6.1 81.1 9.4 100.9 3.3 周效磺胺 83.6 7.5 84.0 5.4 109.2 1.4 磺胺甲恶唑 85.2 5.9 88.4 4.2 107.3 1.7 磺胺二甲异唑 94.0 2.7 98.0 1.2 112.9 2.5 苯甲酰磺胺 81.8 4.8 84.2 0.8 101.0 2.7 磺胺喹恶啉 88.6 7.9 95.4 4.3 113.0 4.8 磺胺地索辛 85.2 6.3 99.0 7.0 114.0 6.0 磺胺苯吡唑 84.5 4.2 87.1 7.4 90.3 5.6 磺胺硝苯 91.0 6.2 89.4 6.2 106.3 2.4 -
[1] 张婧, 吴剑平, 贡松松, 等. 超高效液相色谱-四级杆-静电场轨道肼高分辨质谱同时快速筛查与确证猪粪中33种磺胺类及四环素类药物[J]. 上海畜牧兽医通讯,2019(6):28−32. [ZHANG J, WU J P, GONG S S, et al. Simultaneous rapid screening and confirmation of 33 sulfonamides and tetracyclines in swine manure by ultra performance liquid chromatography-quadruple rod-electrostatic field orbital hydrazine high resolution mass spectrometry[J]. Shanghai J Animal Husbandry Veterinary Med,2019(6):28−32. [2] 王乐, 李海琴, 王美玲, 等. 基于纳米金-适体结构的智能手机补色波长法检测磺胺二甲嘧啶[J]. 分析测试学报,2018,37(8):967−971. [WANG L, LI H Q, WANG M L, et al. Rapid detection of sulfadimethoxine using a smartphone digital colorimetric method based on aptamer/aunps structure[J]. Instrum Anal,2018,37(8):967−971. doi: 10.3969/j.issn.1004-4957.2018.08.017 [3] CHEN Y, XIA S, HAN X, et al. Simultaneous determination of malachite green, chloramphenicols, sulfonamides, and fluoroquinolones residues in fish by liquid chromatography-mass spectrometry[J]. J Anal Methods Chem,2020,2020:3725618.
[4] 赵巧灵, 张薇英, 汤海凤, 等. 快速溶剂萃取-超高效液相色谱-串联质谱法测定养殖鱼肌肉中19种磺胺类药物残留[J]. 食品科技,2019,44(12):335−341. [ZHAO Q L, ZHANG W Y, TANG H F, et al. Determination of 19 sulfonamides residues in cultured fish muscle with accelerated solvent extraction by high performance liquid chromatography-tandem mass spectrometry[J]. Food Sci Technol,2019,44(12):335−341. [5] 李丹, 沈昕, 张玉洁, 等. 高效液相色谱法测定鸡肉中5种磺胺类药物及乙氧酰胺苯甲酯增效剂残留量[J]. 食品安全质量检测学报,2020,11(1):202−208. [LI D, SHEN X, ZHANG Y J, et al. Determination of 5 kinds of sulfonamides and ethopabate resid-usin chicken by high performance liquid chromatography[J]. J Food Saf Qual,2020,11(1):202−208. [6] 刘桂英, 宋广军, 王召会, 等. 固相萃取-超高效液相色谱串联质谱法测定水产品中磺胺类药物残留[J]. 食品安全质量检测学报,2019,10(8):2240−2246. [LIU G Y, SONG G J, WANG Z H, et al. Determination of sulfonamide drugs residues in aquatic product by solid phase extraction-ultra performance liquid chromatography tandem mass spectrometry[J]. J Food Saf Qual,2019,10(8):2240−2246. doi: 10.3969/j.issn.2095-0381.2019.08.024 [7] 高振刚, 梁延鹏, 曾鸿鹄, 等. 固相萃取-超高效液相色谱-三重四极杆质谱法测定水中15种抗生素残留[J]. 分析试验室,2021,40(8):875−880. [GAO Z G, LIANG Y P, ZENG H H, et al. Detection of 15 antibiotics in water by solid phase extraction-ultra-high performance liquid chromatography-triple quadrupole tandem mass spectrometry[J]. Chin J Anal Lab,2021,40(8):875−880. [8] 宋焕杰, 谢卫民, 王俊, 等. SPE-UPLC-MS/MS同时测定水环境中4大类15种抗生素[J]. 分析试验室, 2022, 41(1):50-54. SONG H J, XIE W M, WANG J, et al. SPE-UPLC-MS/MS simultaneous determination of 15 antibiotics in four categories in water environment[J]. Chin J Anal Lab, 2022, 41(1):50-54..
[9] ZHOU X, CHEN W Q, DING Y Q, et al. Rapid determination of sulfonamides in chicken using two-dimensional online cleanup mode with three columns coupled to liquid chromatography-tandem mass spectrometry[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2019,1114−1115:110−118. doi: 10.1016/j.jchromb.2019.03.015
[10] DI X, WANG X, LIU Y, et al. Microwave assisted extraction in combination with solid phase purification and switchable hydrophilicity solvent-based homogeneous liquid-liquid microextraction for the determination of sulfonamides in chicken meat[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2019,1118−1119:109−115. doi: 10.1016/j.jchromb.2019.04.036
[11] 高洁, 陈达炜, 丁宇琦, 等. 固相萃取-超高效液相色谱-串联质谱法测定畜产品中残留的22种磺胺类药物[J]. 中国食品卫生杂志,2018,30(1):28−34. [GAO J, CHEN D W, DING Y Q, et al. Determination of 22 sulfonamides in livestock products by ultra high performance liquid chromatography-tandem mass spectrometry coupled with solid phase extraction[J]. Chin J Food Hyg,2018,30(1):28−34. [12] SAXENA S K, RANGASAMY R, KRISHNAN A A, et al. Simultaneous determination of multi-residue and multi-class antibiotics in aquaculture shrimps by UPLC-MS/MS[J]. Food Chem,2018,260:336−343. doi: 10.1016/j.foodchem.2018.04.018
[13] 国家市场监督管理总局. GB/T 31650—2019 食品安全国家标准 食品中兽药最大残留限量[S]. 北京: 中国农业出版社, 2019. State Administration of Market Supervision. GB/T 31650—2019 National food safety standard. Maximum residue limits for veterinary drugs in food[S]. Beijing: China Agriculture Press, 2019.
[14] GUIDI L R, SANTOS F A, RIBEIRO A C, et al. A simple, fast and sensitive screening LC-ESI-MS/MS method for antibiotics in fish[J]. Talanta,2017,163:85−93. doi: 10.1016/j.talanta.2016.10.089
[15] HELA W , BRANDTNER M , WIDEK R , et al. Determination of sulfonamides in animal tissues using cation exchange reversed phase sorbent for sample cleanup and HPLC-DAD for detection[J]. Food Chemistry,2003,83(4):601−608. doi: 10.1016/S0308-8146(03)00254−1
[16] 张林田, 陆奕娜, 黄学泓, 等. 通过式净化-高效液相色谱-串联质谱法测定动物源性食品中42种兽药残留[J]. 分析科学学报,2020,36(1):81−87. [ZHANG L T, LU Y N, HUANG X H, et al. Determination of 42 kinds of veterinary drug residues in animal-derived products by passing purification-high performance liquid chromatography-tandem mass spectrometry[J]. J Anal Sci,2020,36(1):81−87. doi: 10.2116/analsci.19SAP01 [17] 区敏霞. 高效液相色谱同时测定水产品中7种磺胺类药物残留的方法改进[J]. 食品安全导刊,2017(21):133−135. [QU M X. Improved method for simultaneous determination of 7 sulfonamides residues in aquatic products by high performance liquid chromatography[J]. Chin Food Saf Mag,2017(21):133−135. doi: 10.3969/j.issn.1674-0270.2017.21.097 [18] ZHANG Y, LIAO W, DAI Y, et al. Covalent organic framework Schiff base network-1-based pipette tip solid phase extraction of sulfonamides from milk and honey[J]. J Chromatogr A,2020,1634:461665. doi: 10.1016/j.chroma.2020.461665
[19] 李清雪, 孙王茹, 汪庆. SPE-HPLC测定水中β-内酰胺类、喹诺酮类、磺胺类抗生素[J]. 中国给水排水,2019,35(18):118−122. [LI Q X, SUN W R, WANG Q. Determination of β-lactams, quinolones and sulfonamides antibiotics in water by SPE-HPLC[J]. Chin Water & Wastewater,2019,35(18):118−122. [20] HERRERA-HERRERA A V, HERNANDEZ-BORGES J, AFONSO M M, et al. Comparison between magnetic and non magnetic multi-walled carbon nanotubes-dispersive solid-phase extraction combined with ultra-high performance liquid chromatography for the determination of sulfonamide antibiotics in water samples[J]. Talanta,2013,116:695−703. doi: 10.1016/j.talanta.2013.07.060
[21] MA J, FAN S, SUN L, et al. Rapid analysis of fifteen sulfonamide residues in pork and fish samples by automated on-line solid phase extraction coupled to liquid chromatography-tandem mass spectrometry[J]. Food Science and Human Wellness,2020,9(4):363−369. doi: 10.1016/j.fshw.2020.05.002
[22] ABAFE O A, GATYENI P, MATIKA L. A multi-class multi-residue method for the analysis of polyether ionophores, tetracyclines and sulfonamides in multi-matrices of animal and aquaculture fish tissues by ultra-high performance liquid chromatography tandem mass spectrometry[J]. Food Addit Contam Part A Chem Anal Control Expo Risk Assess,2020,37(3):438−450. doi: 10.1080/19440049.2019.1705399
[23] 庞昕瑞, 曾鸿鹄, 梁延鹏, 等. 固相萃取-超高效液相色谱-串联质谱法测定地表水中10种磺胺类抗生素残留[J]. 分析科学学报,2019,35(4):461−466. [PANG X R, ZENG H H, LIANG Y P, et al. Determination of 10 sulfonamide antibiotic residues in surface water by solid phase extraction-ultra-high performance liquid chromatography-tandem mass spectrometry[J]. J Anal Sci,2019,35(4):461−466. doi: 10.2116/analsci.18N023 [24] XU X, XU X, HAN M, et al. Development of a modified QuEChERS method based on magnetic multiwalled carbon nanotubes for the simultaneous determination of veterinary drugs, pesticides and mycotoxins in eggs by UPLC-MS/MS[J]. Food Chem,2019,276:419−426. doi: 10.1016/j.foodchem.2018.10.051
[25] 谭韬, 刘应杰, 唐倩, 等. 毛细管电泳对水体中多类抗生素的同时分离检测[J]. 重庆医学,2018,47(35):4530−4533. [TAN T, LIU Y J, TANG Q, et al. Simultaneous separation and detection of multiple classes of antibiotics in water by capillary electrophoresis[J]. Chongqing Med,2018,47(35):4530−4533. doi: 10.3969/j.issn.1671-8348.2018.35.023 [26] WEN Y, LI J, ZHANG W, et al. Dispersive liquid-liquid microextraction coupled with capillary electrophoresis for simultaneous determination of sulfonamides with the aid of experimental design[J]. Electrophoresis,2011,32(16):2131−2138. doi: 10.1002/elps.201100142
[27] HOFF R. Analysis of sulfonamide residues in bovine liver by liquid chromatography-tandem mass spectrometry without chemical extraction or clean-up procedures[J]. Anal Biochem,2020,611:114011. doi: 10.1016/j.ab.2020.114011
[28] WANG J, XU J, JI X, et al. Determination of veterinary drug/pesticide residues in livestock and poultry excrement using selective accelerated solvent extraction and magnetic material purification combined with ultra-high-performance liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A, 2020, 1617.
[29] MARTINS M T, BARRETO F, HOFF R B, et al. Multiclass and multi-residue determination of antibiotics in bovine milk by liquid chromatography-tandem mass spectrometry: Combining efficiency of milk control and simplicity of routine analysis[J]. International Dairy Journal,2016,59:44−51. doi: 10.1016/j.idairyj.2016.02.048
[30] 吴利军, 何斌, 周源, 等. 固相萃取-高效液相色谱法同时检测奶牛粪污中5种磺胺类抗生素[J]. 中国兽药杂志,2020,54(10):24−29. [WU L J, HE B, ZHOU Y, et al. Simultaneous determination of five sulfonamide antibiotics in excrement and sewage of dairy farm using solid phase extraction and high performance liquid chromatograph[J]. Chin J Veterinary Drug,2020,54(10):24−29. [31] WANG K, ZHAO L, ZHANG C, et al. Determination of 12 insect growth regulator residues in foods of different matrixes by modified QuEChERS and UPLC-MS/MS[J]. RSC Advances,2021,11(20):12162−12171. doi: 10.1039/D1RA00046B
[32] 扈斌, 谢瑜杰, 蒋康丽, 等. QuEChERS结合高效液相色谱三重四极杆串联质谱法测定花椒中191种农药残留[J]. 分析试验室,2021,40(10):1154−1165. [HU B, XIE Y J, JIANG K L, et al. Quechers combined with high performance liquid chromatography-triple quadrupole tandem mass spectrometry for the determination of 191 pesticide residues in zanthoxylum bungeanum maxim[J]. ChinJ Anal Lab,2021,40(10):1154−1165. [33] 童兰艳, 肖昭竞, 李根容, 等. 超高效液相色谱-三重四极杆质谱法测定化妆品中14种美白活性成分[J]. 分析试验室,2022,41(1):96−102. [TONG L Y, XIAO Z J, LI G R, et al. Determination of 14 whitening active components in cosmetics by ultra-high performance liquid chromatography triple quadrupole mass spectrometry[J]. Chin J Anal Lab,2022,41(1):96−102.





 下载:
下载:

 下载:
下载:



