Analysis of Volatile Flavor Components in Three Onion by Headspace Solid Phase Microextraction Combined with Gas Chromatography-Mass Spectrometry
-
摘要: 为研究洋葱挥发性成分,利用顶空固相微萃取法提取洋葱的挥发性风味成分,通过气相色谱-质谱联用法分析测定,以总峰面积和化合物个数为指标考察萃取纤维头、萃取温度、萃取时间和解吸时间4个因素对萃取效果的影响,得出最优萃取条件为:萃取纤维头50/30 μm DVB/CAR/PDMS,萃取温度60 ℃,萃取时间60 min,解吸时间5 min。利用最优萃取条件对三种色泽洋葱挥发性风味成分进行分析鉴定。结果表明:三种色泽洋葱共鉴定得到挥发性风味物质61种,其中白皮、红皮、黄皮洋葱分别测到37、40、49种挥发性成分,相对含量分别占流出组分总量的70.29%、81.92%、79.03%。61种挥发性成分中含硫化合物27种、醛类13种、醇类13种、酮类4种,其他4种。三种色泽洋葱的共有挥发性成分有22种,其中含硫化合物占比较大,特别是二异丙基二硫醚和(E)-1-丙烯基-2-丙烯基二硫醚相对含量的总和在三种色泽洋葱的挥发性成分中占比率都超过了20%,对形成洋葱特征风味贡献较大。红皮和黄皮洋葱的含硫化合物的相对含量远高于白皮洋葱,红皮洋葱中2-甲基-2-戊烯醛相对含量高于白皮和黄皮洋葱。
-
关键词:
- 洋葱 /
- 顶空固相微萃取 /
- 气相色谱-质谱联用法 /
- 挥发性风味成分
Abstract: In order to study the volatile composition of onion, the volatile flavoring substances of the onion were extracted by headspace solid phase microextraction and determined by gas chromatography-mass spectrometry. The effects of extraction fiber head, extraction temperature, extraction time and desorption time on the total peak area and the number of effective compounds were investigated. The optimum extraction conditions were determined as follows: Extraction fiber 50/30 μm DVB/CAR/PDMS, extraction temperature 60 ℃, extraction time 60 min and desorption time 5 min. Under the optimum experimental conditions, the volatile compounds of onion with three different colors were analyzed and identified. The results showed that a total of 61 kinds of volatile flavor compounds were identified. A total of 37, 40 and 49 volatile flavor compounds were detected in the white, red, and yellow onions, respectively, and the peak area content of these volatile flavor compounds accounted for 70.29%, 81.92% and 79.03% of the total volatile components, respectively. In the 61 volatile flavor compounds, 27 were sulfur compounds, 13 were aldehydes, 13 were alcohols, 4 were ketones and 4 were others. There were 22 kinds of volatile components in the three color onions, of which sulfur-containing compounds account for a relatively large proportion, especially the relative content of diisopropyl disulfide and (E)-1-propenyl-2-propenyl disulfide. The sum of the volatile components of the three color onions accounted for more than 20%, which contributed a lot to the formation of the characteristic flavor of onions. The relative content of sulfur compounds in red and yellow onions was much higher than that of white onions. The relative content of 2-methyl-2-pentenoaldehyde in red onions was higher than that of white and yellow onions. -
洋葱(Allium cepa L.)是葱科最广泛种植和食用的蔬菜之一,因其具有特殊的风味和辛辣的口感,被用作香料和食品配料。洋葱含有的营养成分有蛋白质、碳水化合物、维生素、矿物质、膳食纤维、半胱氨酸衍生物和酚类化合物等[1],除此之外还具抗真菌、抗病毒、抗炎、抗高血压、抗糖尿病、抗过敏和降血脂等多方面的药理与抗菌特性[2-3]。
洋葱的所有药用特性主要与其挥发性化合物有关,而这些挥发性化合物主要是以半胱氨酸衍生物形式存在的含硫化合物[4-5]。洋葱的含硫化合物大多数具有挥发性,因此洋葱含有的挥发性成分的种类和含量是洋葱的主要品质特征之一,更是洋葱商品价值的重要参考[6]。Colina-Coca等[7]分析了洋葱的挥发性成分,发现洋葱的主要挥发性成分为二硫化物、三硫化物和醛类化合物。Choi等[8]利用HS-SPME-GC-MS联用法对洋葱的挥发性化合物进行了分析,得知新鲜洋葱中的主要挥发性化合物为二丙基二硫。孙雪君等[9]利用HS-SPME-GC-MS联用法对不同品种洋葱的挥发性化合物进行了分析对比,发现红皮鲜洋葱和白皮鲜洋葱的挥发性成分主要是含硫化合物、醛类、醇类。但是,到目前为止,对洋葱挥发性成分的固相微萃取条件的优化还未见有相关文献报道,对三种不同色泽洋葱挥发性成分分析和对比的研究相对较少。
顶空固相微萃取(headspsce-solid-phase microextraction,HS-SPME)是近年来新兴的一种集样品采集、富集、进样为一体的挥发性成分提取方法,样品处理过程快速、简便,不需要加入提取溶剂,属于环境友好型样品处理方法[10],该方法已经被广泛用于食品[11-13]、环境[14]、医药[15]等样品中挥发性成分的前处理。本文就影响固相微萃取效率的萃取纤维头、萃取温度、萃取时间、解吸时间等因素进行了优化,利用较优的固相微萃取条件,分析测定三种不同色泽洋葱中的挥发性化合物,对比分析三种色泽洋葱挥发性成分的差异,为洋葱精深加工提供一定的理论依据。
1. 材料与方法
1.1 材料与仪器
白皮洋葱(品种为白碧龙)、红皮洋葱(品种为红优1号)、黄皮洋葱(品种为金稞7号) 三种色泽洋葱均于2021年8月采集于甘肃省酒泉市肃州区《地理标志产品 酒泉洋葱》地理标志产品保护范围内;NaCl(分析纯) 北京北化精细化学品有限公司。
CMS-QP2010 PLUS气相色谱质谱联用仪 日本岛津公司;HP-INNOWAX色谱柱(60 m×0.25 mm×0.5 μm) 美国安捷伦公司;顶空固相微萃取进样手柄,50/30 μm二乙烯基苯/碳分子筛/聚二甲基硅氧烷(divinylbenzene/carboxen/polydimethylsiloxane,DVB/CAR/PDMS)、100 μm聚二甲基硅氧烷(polydimethylsiloxane,PDMS)、85 μm Polyacrylate、60 μm PEG、75 μm碳分子筛/聚二甲基硅氧烷(carboxen/polydimethylsiloxane,CAR/PDMS)固相微萃取纤维头 美国Supelco公司;加热型磁力搅拌器 美国TALBOYS公司。
1.2 实验方法
1.2.1 样品准备
选择无损伤、无腐烂的洋葱,洗净后剥皮、切分,取50 g左右洋葱粒于研钵中,加液氮迅速研磨成粉末后置于−4 ℃冰箱冷冻备用。
1.2.2 萃取过程
参照Fernandes等[16]的方法,准确取10 g洋葱粉末于顶空瓶中,加入饱和NaCl溶液5 mL,放入磁力搅拌子,封盖后摇匀,将顶空瓶置于磁力搅拌仪上,在1600 r/min的转速下搅拌和加热,恒温20 min,使挥发性物质在顶空瓶的样品上方达到平衡。将老化处理的萃取头插入顶空瓶中,推出纤维头,在一定温度条件下吸附一定时间,抽回纤维头并拔出萃取头,迅速将萃取头插入气相色谱仪进样口,推出纤维头,在250 ℃条件下解析一定时间,抽回纤维头后拔出萃取头,同时启动仪器采集数据。
1.2.3 HS-SPME条件优化
1.2.3.1 萃取纤维头优化
萃取纤维头每次使用前需要老化,利用进样手柄分别将50/30 μm DVB/CAR/PDMS、100 μm PDMS、75 μm CAR/PDMS、60 μm PEG、85 μm Polyacrylate萃取纤维头在进样口温度为260、250、300、280、250 ℃条件下老化1、0.5、1、1、0.5 h。将老化好的萃取头插入顶空瓶中样品上方,推出纤维头,在40 ℃条件下吸附40 min,萃取完成后,将萃取纤维头置于气相色谱仪进样口解吸5 min时间,同时启动仪器采集数据。每次实验至少重复3 次。
1.2.3.2 萃取条件优化
在顶空瓶中称取10 g样品,加入饱和NaCl溶液5 mL,将老化好的5种不同涂层的萃取纤维头分别插入平衡后的顶空瓶中萃取,60 ℃加热条件下萃取60 min,将萃取头插入仪器进行分析,根据总离子流色谱图确定总峰面积和化合物个数,选择最佳的萃取纤维头。然后经单因素实验考察萃取时间、萃取温度、解吸时间,考察范围分别为萃取时间10~80 min、萃取温度20~80 ℃、解吸时间3~7 min,以总峰面积与化合物个数为指标,确定各因素最佳水平。每次实验至少重复3 次。
1.2.4 GC-MS条件
GC条件:色谱柱为HP-INNOWAX型号的毛细管柱,规格为60 m×0.250 mm×0.5 μm;气相色谱仪进样口温度为250 ℃;程序升温条件:初始温度60 ℃,保持1 min,以2 ℃/min的速率升温至180 ℃,不保持,再以20 ℃/min的速率升温至230 ℃,保持5 min;载气为高纯氦气(纯度≥99.999%);柱流量0.98 mL/min;分流比20:1。
MS条件:电子轰击离子源;电子能量70 eV;传输线温度230 ℃;离子源温度230 ℃;扫描模式:全离子扫描(Full San);离子质量扫描范围:m/z 25~500 u。
1.3 数据处理
样品中各挥发性成分的定性由计算机检索与NIST标准质谱库匹配求得;挥发性成分的定量由计算机数据处理系统,按照峰面积的归一化方法进行定量分析,计算相对含量。采用利用Excel 2010作图,IBM SPSS Statistics 20软件分析数据。
2. 结果与分析
2.1 HS-SPME纤维头的选择
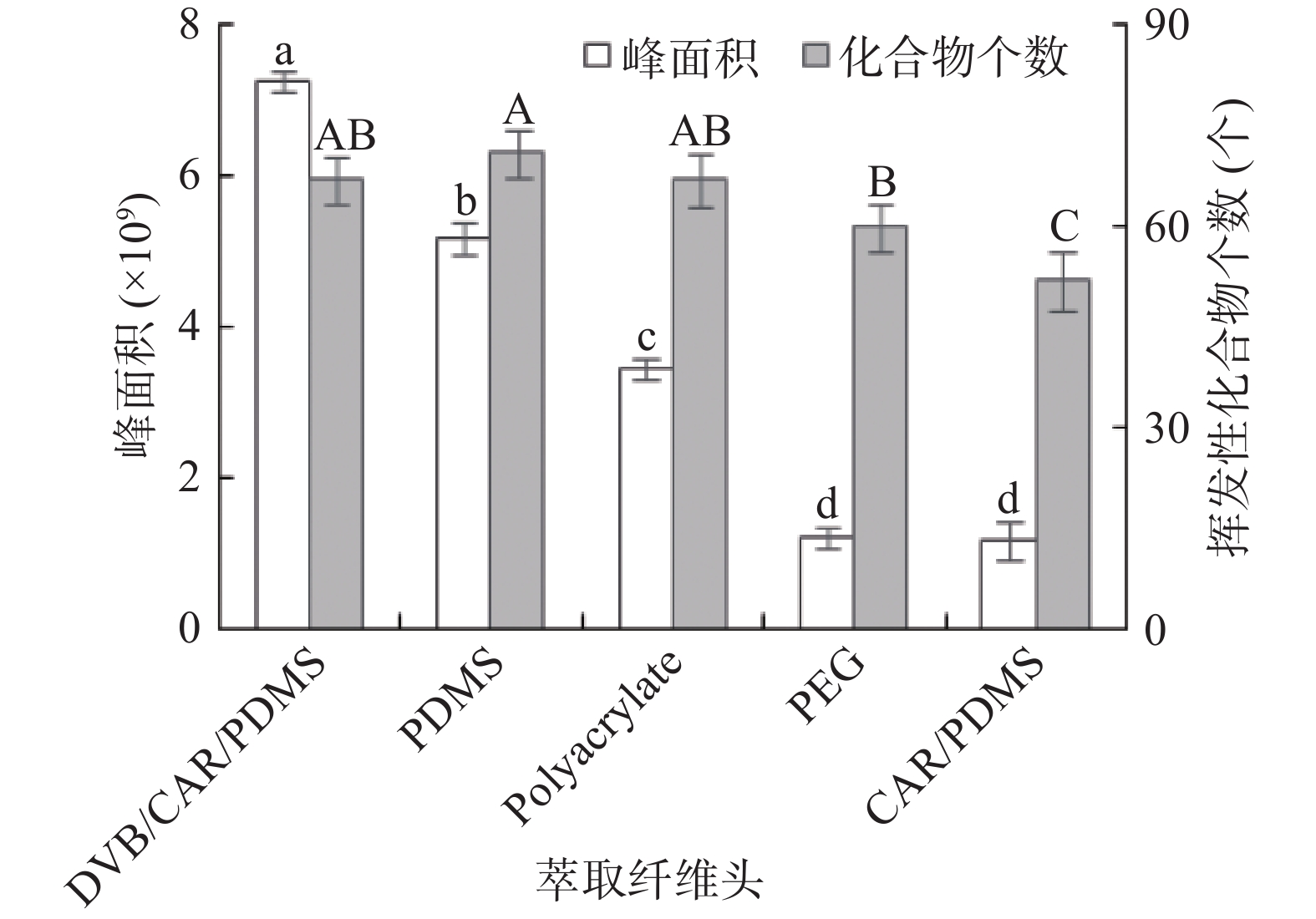
本文选择5种不同极性的萃取头对洋葱的挥发性成分进行测定,经GC-MS分离检测,如图1所示,5种萃取头对洋葱挥发性成分萃取效果有明显差异,100 μm PDMS、85 μm Polyacrylate、60 μm PEG和50/30 μm DVB/CAR/PDMS萃取头对洋葱样品挥发性物质的萃取效果明显优于75 μm CAR/PDMS,前四者化合物个数明显多于CAR/PDMS萃取头,且相互之间无明显差异,DVB/CAR/PDMS、PDMS、Polyacrylate、PEG峰面积逐渐递减,DVB/CAR/PDMS萃取的化合物峰面积最大,表明DVB/CAR/PDMS对洋葱挥发性化合物的萃取最有效。这可能是由于DVB/CAR/PDMS是三相萃取纤维头,包含了极性和非极性材料,能够更全面地分析挥发性化合物[17]。综合考虑,本实验确定50/30 μm DVB/CAR/PDMS萃取纤维头进行后续实验。
2.2 HS-SPME单因素实验结果
2.2.1 解析时间的选择
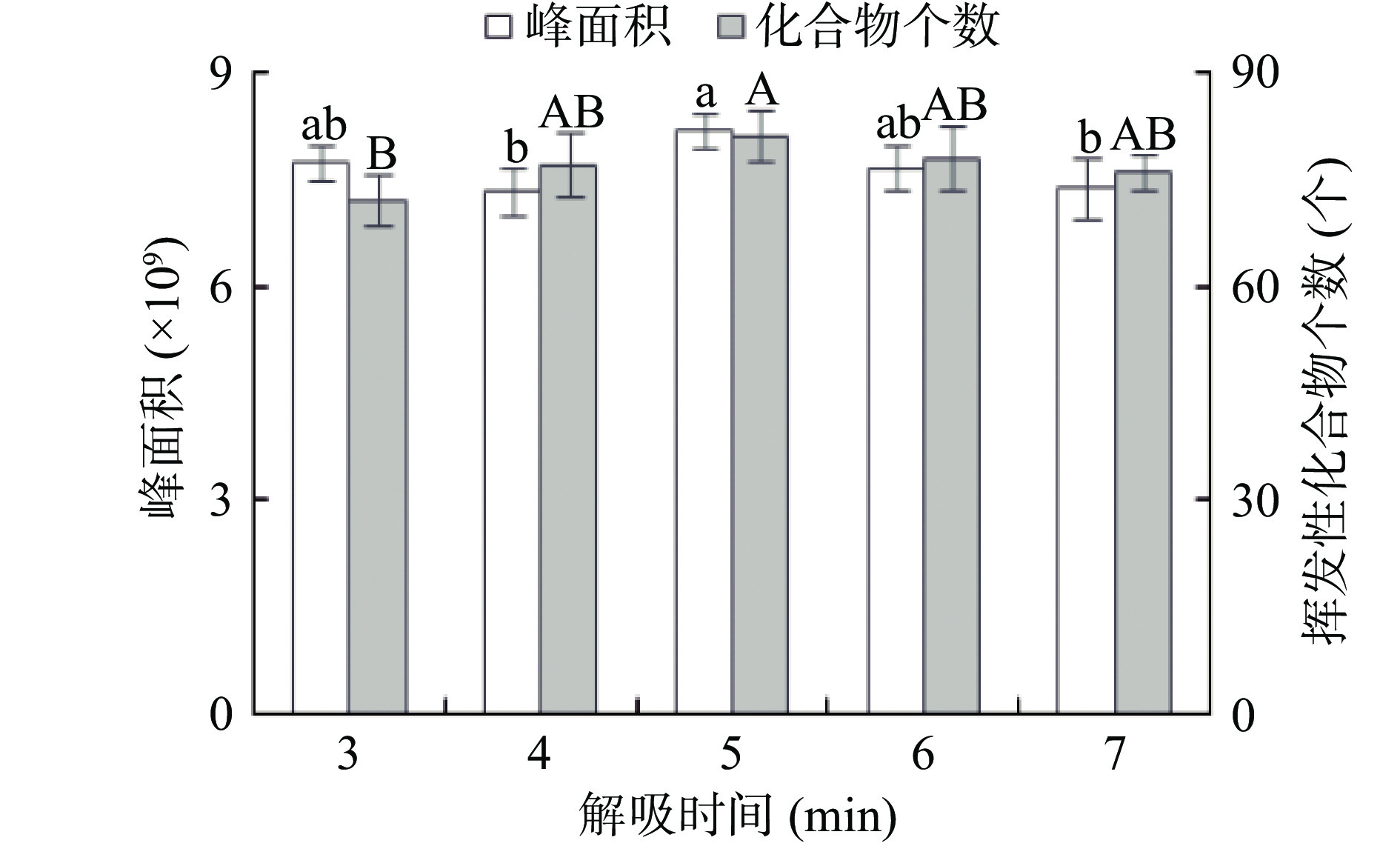
由图2可知,随着解吸时间的延长,洋葱挥发性化合物总峰面积和挥发性化合物个数变化不大。解吸时间为3~5 min,挥发性化合物个数逐渐增大,为81个,而峰面积在呈现略微减小后有增大的趋势,在5 min时总峰面积为8.2×109。而解吸时间在5~7 min检测出的峰个数和峰面积呈现下降趋势,这可能是因为挥发性化合物在高温下解吸时间过长会使一些成分发生氧化、异构等反应[18]。因此,本实验确定的解吸时间为5 min,即萃取头在进样口保持5 min使吸附在萃取头上的挥发性成分解吸下来之后打开吹扫阀吹扫掉多余物质。萃取纤维头在进样口解吸之后多停留2~3 min,以尽量减少萃取纤维头上干燥物质的残留。
2.2.2 萃取时间的选择
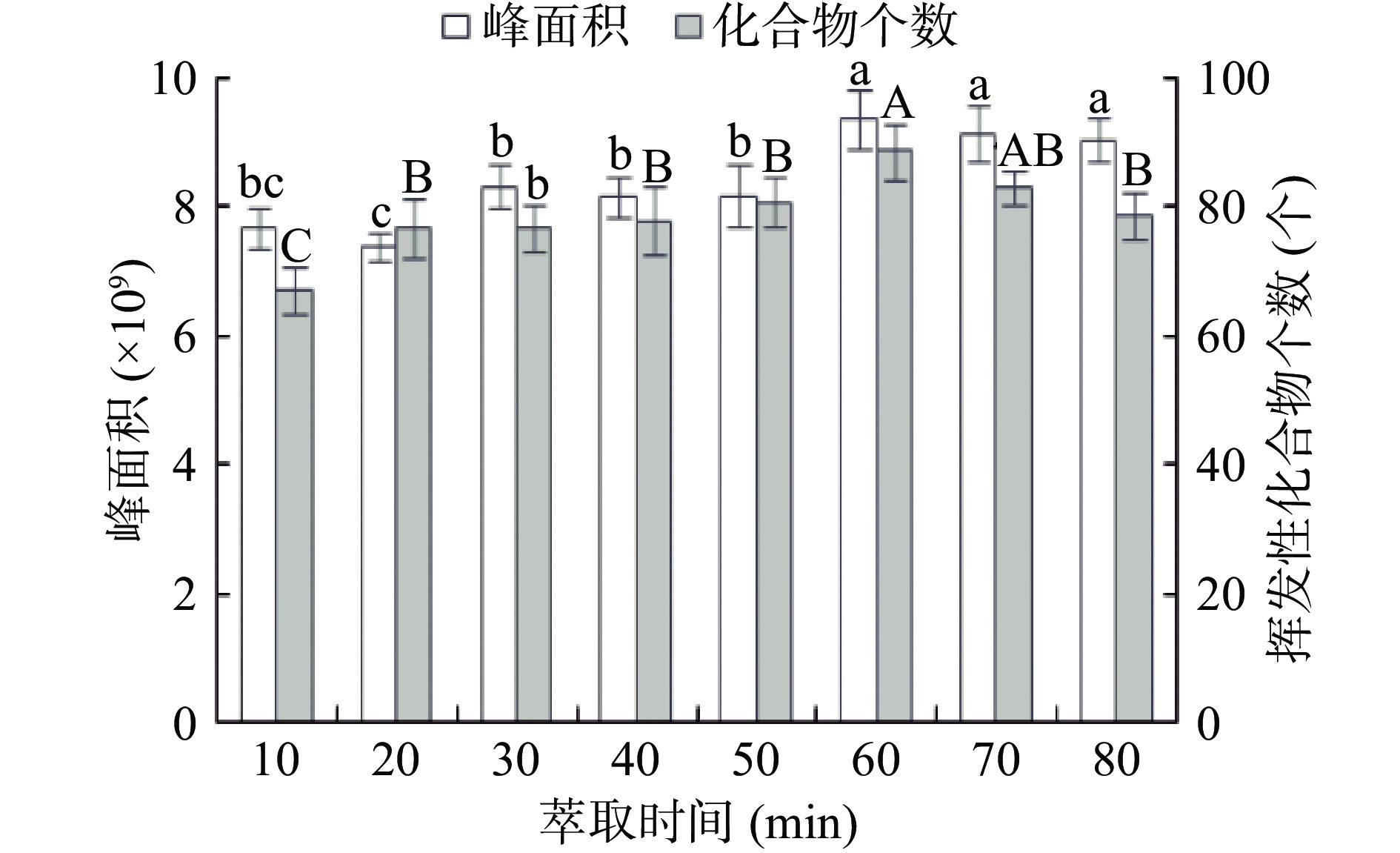
如图3所示,在萃取温度为40 ℃时,随着萃取时间的延长,总峰面积及挥发性化合物个数都呈增加趋势,萃取时间在60 min时,总峰面积和挥发性化合物个数均达到最大,此时共检测出89种挥发性化合物,总峰面积为9.4×109。在60 min之后,总峰面积基本趋于平稳,挥发性化合物个数略有下降。这可能是由于在达到萃取平衡前,萃取纤维头的吸附量随着萃取时间的延长而增加,当萃取体系中被萃取物和萃取纤维头固定相之间达到饱和后,萃取纤维头的吸附量不再随时间延长而改变[19]。
2.2.3 萃取温度的选择
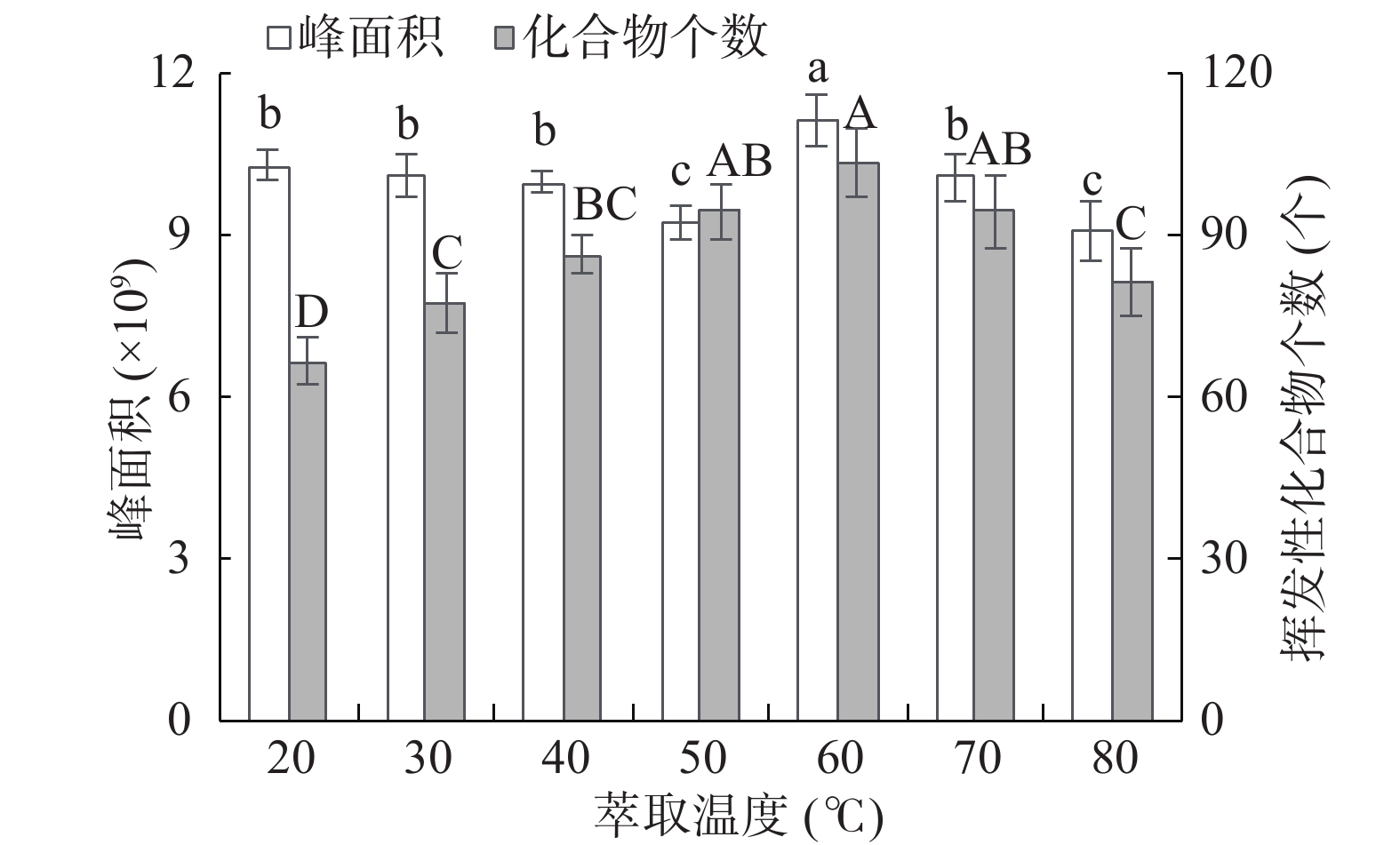
如图4所示,萃取时间在60 min条件下,随着萃取温度的升高,挥发性化合物个数总体趋势呈平稳增长,在60 ℃时达到最大值,共检出挥发性化合物103种,总峰面积随着萃取温度的升高变化不大,在60 ℃时也达到最大值,此时总峰面积为1.1×1010。这是由于随着萃取温度的升高,洋葱中挥发性化合物的扩散速度随之增大,从而提高了挥发性化合物的萃取效率,但是温度过高又会导致吸附在萃取头上物质的解吸与分解[20]。Brodnitz和Carson研究发现温度对蒜氨酸酶的活性有敏感影响,温度过高会导致蒜氨酸酶变性,使洋葱失去其辛辣的挥发性风味,并导致代谢的生物挥发性化合物的减少[21-22]。综上所述,选择60 ℃为最佳萃取温度。
2.3 洋葱挥发性成分分析
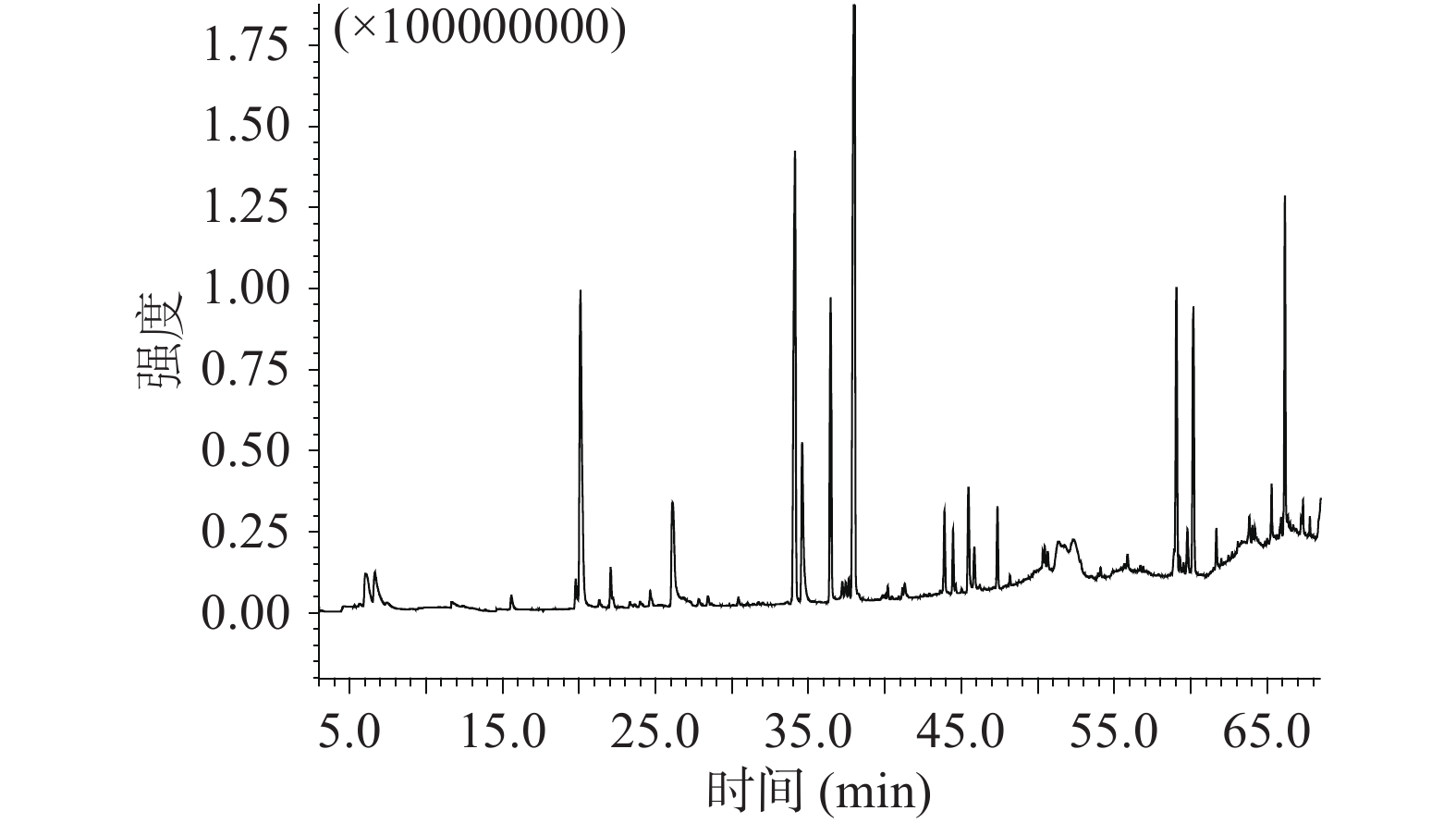
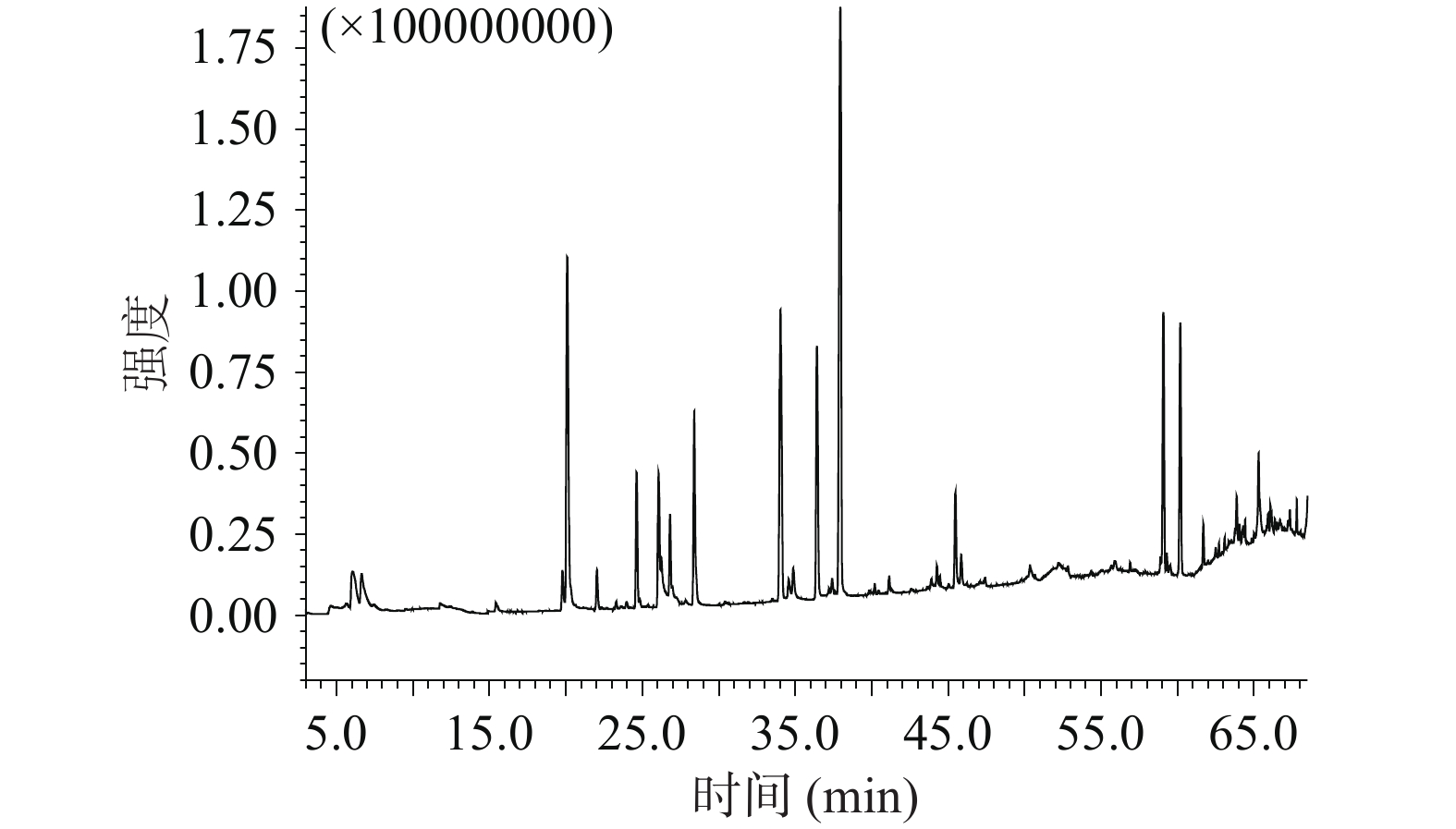
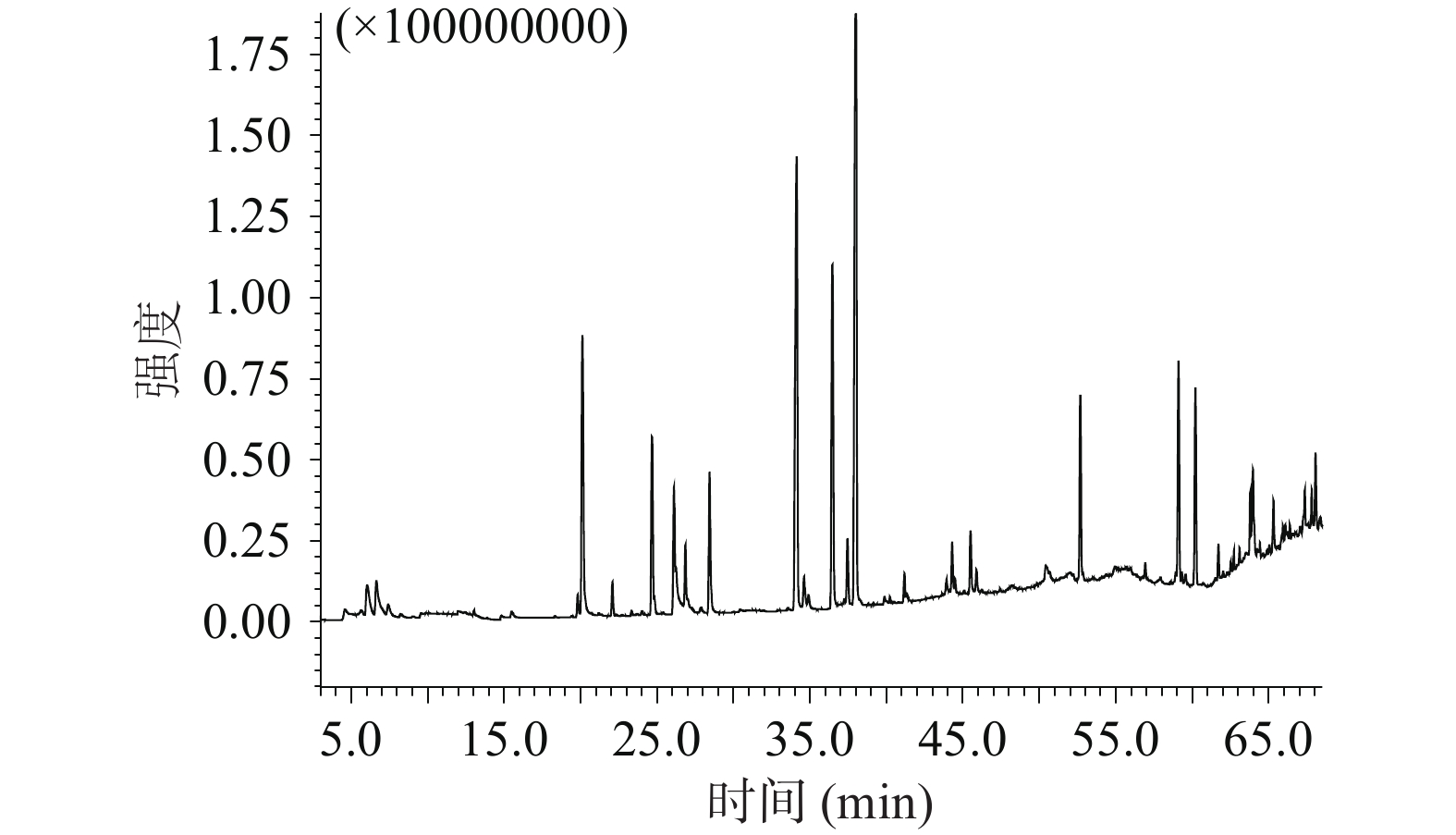
利用优化出的较优萃取条件对三种色泽洋葱的挥发性成分进行分析,得到白皮洋葱、红皮洋葱和黄皮洋葱的挥发性成分总离子流色谱图,如图5~图7所示。经过NIST 17谱库检索识别化合物,利用峰面积归一化法生成各挥发性物质组分的相对含量,得到不同色泽洋葱的挥发性化学成分种类及相对含量见表1、表2。
表 1 洋葱挥发性成分GC-MS分析结果Table 1. GC-MS analysis of volatile compounds in onion序号 保留时间(min) 化合物名称 CAS号 分子式 相对分子质量 相对含量(%) 白洋葱 红洋葱 黄洋葱 含硫化合物 1 6.04 Carbon disulfide
二硫化碳75-15-0 CS2 76.14 1.88 1.39 2 22.04 3,4-Dimethylthiophene
3,4-二甲基噻吩632-15-5 C6H8S 112.19 0.92 0.62 3 23.30 (E)-Allyl(propenyl)sulfane
(E)-烯丙基1-丙烯基硫醚104324-36-9 C6H10S 114.21 0.06 0.17 0.09 4 23.99 Diallyl sulfide
二烯丙基硫醚592-88-1 C6H10S 114.21 0.17 0.08 5 24.63 Methyl propyl disulfide
甲基丙基二硫醚2179-60-4 C4H10S2 122.25 0.37 3.36 4.15 6 26.07 2,4-Dimethylthiophene
2,4-二甲基噻吩638-00-6 C6H8S 112.19 3.84 3.57 2.85 7 26.23 2,5-Dimethylthiophene
2,5-二甲基噻吩638-02-8 C6H8S 112.19 2.07 1.65 8 26.81 (E)-1-Methyl-2-(propenyl)disulfane
(E)-1-甲基-2-丙烯基二硫醚23838-19-9 C4H8S2 120.24 2.00 9 28.40 (Z)-1-Methyl-2-(propenyl)disulfane
(Z)-1-甲基-2-丙烯基二硫醚23838-18-8 C4H8S2 120.24 0.19 5.24 3.05 10 34.04 Diisopropyl disulfide
二异丙基二硫醚4253-89-8 C6H14S2 150.30 12.41 10.05 13.11 11 34.87 Dimethyl trisulfide
二甲基三硫醚3658-80-8 C2H6S3 126.26 1.05 0.38 12 37.42 1-Allyl-2-isopropyl disulfane
1-烯丙基-2-异丙基二硫醚67421-85-6 C6H12S2 148.29 0.31 0.43 1.34 13 37.99 (E)-1-(Propenyl)-2-propyl disulfane
(E)-1-丙烯基-2-丙基二硫醚23838-21-3 C6H12S2 148.29 15.20 16.81 14.8 14 41.14 (E)-1-Allyl-2-(propenyl)disulfane
(E)-1-丙烯基-2-丙烯基二硫醚122156-02-9 C6H10S2 146.27 0.18 0.31 0.51 15 44.27 Methyl propyl trisulfide
甲基丙基三硫醚17619-36-2 C4H10S3 154.32 0.55 0.73 16 45.46 (E)-Propenyl propanedithioate
(E)-丙二硫代-1-烯-1-基丙酸酯67269-06-1 C6H10S2 146.27 2.24 2.56 1.32 17 45.85 (Z)-Propenyl propanedithioate
(Z)-丙二硫代-1-烯-1-基丙酸酯67230-81-3 C6H10S2 146.27 0.82 0.55 18 47.41 Methyl 1-(methylthio)propyl disulfide
甲基1-(甲硫基)丙基二硫醚53897-66-8 C5H12S3 168.34 0.16 0.07 19 52.29 2-Mercapto-3,4-dimethyl dihydrothiophene
2-巯基-3,4-二甲基噻吩137363-86-1 C6H10S2 146.27 3.73 20 52.68 Dipropyl trisulfide
二丙基三硫醚6028-61-1 C6H14S3 182.37 3.62 21 54.11 (E,E)-2,4-Nonadienal
(E,E)-2,4-壬二烯醛5910-87-2 C9H14O 138.21 0.25 0.03 22 55.66 1,2-Di((E)-propenyl)disulfane
1,2-2(E)-烯丙基二硫醚23838-23-5 C6H10S2 146.27 0.25 0.14 0.07 23 55.87 3,4-Dimethylthiophene-2,5-dione
2,5-二酮-3,4-二甲基噻吩10547-83-8 C6H6O2S 142.18 0.40 0.34 0.10 24 59.07 (E)-1-(Propenyl)-3-propyltrisulfane
(E)-1-烯丙基-3-丙基三硫醚23838-27-9 C6H12S3 180.35 6.22 6.43 4.48 25 60.17 (Z)-1-(Propenyl)-3-propyltrisulfane
(Z)-1-烯丙基-3-丙基三硫醚28383-26-8 C6H12S3 180.35 6.12 3.91 26 62.52 1-(1-(Methylthio)propyl)-2-propyldisulfane
1-甲硫丙烯基-2-丙烯基二硫醚126876-22-0 C7H16S3 196.40 0.19 0.22 27 67.34 1-Methyl-2-(1-(propenylthio)propyl)disulfane
甲基1-(1-丙烯硫基)丙基二硫醚126876-23-1 C7H14S3 194.38 0.55 0.94 醇类 28 7.42 Propyl mercaptan
丙硫醇107-03-9 C3H8S 76.16 0.39 29 20.09 (E)-2,4-Hexadien-1-ol
(E)-2,4-己二烯-1-醇111-28-4 C6H10O 98.14 9.7 12.01 7.34 30 37.64 1-Octen-3-ol
1-辛烯-3-醇3391-86-4 C8H16O 128.21 0.31 31 40.18 2-Ethyl-1-hexanol
2-乙基己醇104-76-7 C8H18O 130.23 0.20 0.20 0.12 32 44.45 1-Octanol
1-辛醇111-87-5 C8H18O 130.23 0.98 0.22 0.58 33 45.04 3-Methyl-2-butanol
3-甲基-2-丁醇598-75-4 C5H12O 88.15 0.08 34 48.17 (E)-2-Octen-1-ol
(E)-2-辛烯醇18409-17-1 C8H16O 128.21 0.16 0.01 35 50.65 1-Nonanol
1-壬醇143-08-8 C9H20O 144.25 0.28 0.09 0.24 36 56.90 Citronellol
香茅醇106-22-9 C10H20O 156.27 0.07 0.15 0.25 37 62.00 2-Tridecanol
2-十三醇1653-31-2 C13H28O 200.36 0.12 0.59 38 63.08 Benzyl alcohol
苯甲醇100-51-6 C7H8O 108.14 0.17 0.38 39 64.05 Phenylethyl Alcohol
苯乙醇60-12-8 C8H10O 122.16 0.32 2.88 40 67.81 Triethylene glycol monododecyl ether
3-十二烷醇3055-94-5 C18H38O4 318.49 0.82 醛类 41 6.64 Propanal
丙醛123-38-6 C3H6O 58.08 1.72 1.69 1.65 42 15.57 Hexanal
己醛66-25-1 C6H12O 100.16 0.32 43 19.78 2-Methyl-2-pentenal
2-甲基-2-戊烯醛623-36-9 C6H10O 98.14 0.58 1.02 0.44 44 21.32 Heptanal
庚醛111-71-7 C7H14O 114.19 0.10 0.02 45 27.84 Octanal
辛醛124-13-0 C8H16O 128.21 0.13 0.15 46 30.41 (E)-2-Heptenal
(E)-2-庚烯醛18829-55-5 C7H12O 112.17 0.14 47 34.57 Nonanal
壬醛124-19-6 C9H18O 142.24 4.34 0.76 0.92 48 37.21 (E)-2-Octenal
(E)-2-辛烯醛2548-87-0 C8H14O 126.20 0.30 0.15 0.10 49 40.46 2,5-Dihydroxybenzaldehyde
2,5-二羟基苯甲醛1194-98-5 C7H6O3 138.12 0.07 0.02 50 41.30 Decanal
癸醛112-31-2 C10H20O 156.27 0.17 51 43.89 (E)-2-Nonenal
(E)-2-壬烯醛18829-56-6 C9H16O 140.22 1.42 0.30 0.43 52 50.41 (E)-2-Decenal
(E)--2-癸烯醛3913-81-3 C10H18O 154.25 0.39 0.19 53 56.72 2-Undecenal
2-十一烯醛2463-77-6 C11H20O 168.28 0.10 0.03 酮类 54 59.53 2-Tridecanone
2-十三烷酮593-08-8 C13H26O 198.34 0.22 0.24 55 59.79 2,4-Octanedione
2,4-辛二酮14090-87-0 C8H14O2 142.20 0.94 56 62.01 6,10-dimethyl-5,9-undecadien-2-one
6,10-二甲基-5,9-十一双烯-2-酮689-67-8 C13H22O 194.31 0.24 0.17 57 65.04 1,4-Cyclohexanedione
1,4-环己二酮37-88-7 C6H8O2 112.13 0.17 其他 58 4.61 2-Aminopentane
2-氨基戊烷63493-28-7 C5H13N 87.16 0.40 59 44.62 Linalyl acetate
乙酸芳樟酯115-95-7 C12H20O2 196.29 0.12 60 50.35 Butanoic acid
丁酸107-92-6 C4H8O2 88.11 0.41 61 62.71 Heneicosane
二十一烷629-94-7 C21H44 296.57 0.15 0.27 表 2 各样品挥发性化学成分物质种类及其含量比较Table 2. Comparison of types of volatile compounds and their relative contents in onion类别 白洋葱 红洋葱 黄洋葱 种类 含量(%) 种类 含量(%) 种类 含量(%) 含硫化合物 15 47.53 23 64.01 25 60.06 醛类 11 9.54 6 3.99 11 4.12 醇类 7 11.70 9 13.36 8 13.60 酮类 3 1.40 0 0 3 0.58 其他 1 0.12 2 0.56 2 0.67 总量 70.29 81.92 79.03 三种色泽洋葱共检测出61种挥发性化合物,其中含硫化合物27种、醛类13种、醇类13种、酮类4种,其他4种。白皮洋葱中鉴定出37种挥发性成分,占流出组分总量的70.29%,主要成分有(E)-1-丙烯基-2-丙基二硫醚、二异丙基二硫醚、(E)-2,4-己二烯-1-醇、(E)-1-烯丙基-3-丙基三硫醚、壬醛、2,4-二甲基噻吩等;红皮洋葱中鉴定出40种挥发性成分,占流出组分总量的81.92%,主要有(E)-1-丙烯基-2-丙基二硫醚、二异丙基二硫醚、(E)-2,4-己二烯-1-醇、(E)-1-烯丙基-3-丙基三硫醚、甲基丙基二硫醚、(Z)-1-烯丙基-3-丙基三硫醚、二丙基三硫醚等;黄皮洋葱鉴定出49种挥发性成分,占流出组分总量的79.03%,主要有(E)-1-丙烯基-2-丙基二硫醚、(E)-2,4-己二烯-1-醇、二异丙基二硫醚、(E)-1-烯丙基-3-丙基三硫醚、(Z)-1-烯丙基-3-丙基三硫醚、(Z)-1-甲基-2-丙烯基二硫醚、2,4-二甲基噻吩等。对三种色泽洋葱各类挥发性成分进行对可以看出,黄皮洋葱的含硫化合物的相对含量高于白皮和红皮洋葱,白皮洋葱的醛类物质的种类和含量高于红皮和黄皮洋葱,红皮洋葱的醇类物质的种类和含量高于白皮和黄皮洋葱。由上述可见,3种不同色泽洋葱的挥发性物质种类和含量存在一定的差异。
由表1可以看出,三种色泽洋葱挥发性成分相比较,三者的共有成分为22种,主要是12种含硫化合物、5种醛类和5种醇类。含硫化合物在三种色泽洋葱的挥发性化合物构成中占比较大,特别是二异丙基二硫醚和(E)-1-丙烯基-2-丙烯基二硫醚,两种物质相对含量的总和在三种色泽洋葱的挥发性成分中占比率都超过了20%,对形成洋葱特有特征风味贡献较大,这与Rokayya等[23]的研究结果相似。三种色泽洋葱共有的挥发性成分有22种,如(E)-烯丙基-1-丙烯基硫醚、甲基丙基二硫醚、2,4-二甲基噻吩、(Z)-1-甲基-2-丙烯基二硫醚、二异丙基二硫醚、1-烯丙基-2-异丙基二硫醚、丙醛、2-乙基-2-丁烯醛、(E)-2,4-己二烯-1-醇等组分,组成洋葱的基本风味,但是不同品种洋葱中共有成分的含量存在一定的差异,比如红皮洋葱中(E)-1-丙烯基-2-丙烯基二硫醚的含量(16.81%)高于白皮和黄皮洋葱,而黄皮洋葱中二异丙基二硫醚的含量(13.11%)较高。
挥发性成分的组成与含量的不同,构成了不同色泽洋葱的特殊辛香味。含硫化合物是新鲜洋葱中主要挥发性成分,同时也构成了洋葱的特征风味。洋葱中的含硫化合物主要来源于洋葱的前体S-alk(en)ly-L半胱氨酸亚砜(ASCOs),当洋葱被切碎时,该前体被蒜氨酸酶催化发生水解反应[24]。洋葱中的含硫化合物包括单硫化物、二硫化物、三硫化物等物质,这些化合物能产生洋葱所特有的原生的、浓郁的辛香味[25]。洋葱中挥发性含硫化合物,如甲基丙基二硫醚、二甲基三硫醚等硫醚类化合物具有洋葱、坚果香味,这类化合物大多能够产生浓郁的辛辣味和扩散性气息,因此硫醚类化合物是洋葱特征风味的主要贡献物质[26]。通过本实验测定结果可以看出,白皮、红皮和黄皮洋葱中含硫化合物的相对含量分别为47.53%、64.01%和60.06%,红皮和黄皮洋葱的相对含量很接近,白皮洋葱中含硫化合物相对含量远低于其他两种,因此红皮和黄皮洋葱的辛辣味和扩散性气息比白皮洋葱更强烈。
白皮、红皮和黄皮洋葱中检测出的3,4-二甲基噻吩、2,4-二甲基噻吩和2,5-二甲基噻吩相对含量分别为0%、0.92%、0.62%,3.84%、3.57%、2.85%和0%、2.07%、1.65%,噻吩类物质是由硫代亚磺酸盐降解产生的,同时也是三丙基二硫醚等物质的前体物质,具有尖刺的气息和洋葱浓郁的特征气味[27]。红皮和黄皮洋葱中检出的噻吩类物质相对含量高于白洋葱,因此,红洋葱和洋葱的辛辣、刺鼻的风味和气味比白洋葱更浓郁。白皮、红皮和黄皮洋葱中醇类挥发性成分的相对含量分别为11.70%、13.36%和13.60%,红皮和黄皮洋葱的含量很接近,且高于白皮洋葱。三种洋葱中检测出的第三大类挥发性成分是醛类,白洋葱、红洋葱和洋葱中醛类挥发性成分的相对含量分别为9.54%、3.99%和4.12%,其中白皮洋葱的醛类挥发性成分含量远高于红皮和黄皮洋葱。由于不饱和化合物比饱和化合物的的香气强,甚至产生刺激性的气味,因此洋葱的风味与其检出的挥发性成分的碳链结构存在一定的关系。白皮、红皮和黄皮洋葱中不饱和键的醛类含量分别为2.93%、1.54%、1.21%,白皮洋葱中不饱和键的醛类相对含量较高可能是构成其特殊辛香气味的主要原因之一。2-甲基-2-戊烯醛是洋葱催泪因子(硫代丙醛-S-氧化物)的主要代谢产物[12],白皮、红皮和黄皮洋葱中的2-甲基-2-戊烯醛含量分别为0.58%、1.02%和0.44%,红皮洋葱中2-甲基-2-戊烯醛相对含量较高,因此这也是红皮洋葱比白皮和黄皮洋葱容易导致人眼睛流眼泪的间接原因[28]。饱和醛类中三种洋葱同时检出且含量较高的是丙醛,白皮、红皮和黄皮洋葱中丙醛相对含量分别为1.72%、1.69%和1.65%,丙醛是构成生洋葱香气的最重要的化合物之一,也是切碎洋葱后首先形成的挥发物之一[29]。洋葱中检出的第四大类挥发性成分是酮类,三种洋葱中只有白皮和黄皮洋葱中检出了酮类,相对含量分别为1.4%和0.58%。酮类物质具有果香和青草样的香气,对洋葱特征香气的贡献不大[26]。其他类中主要检出的挥发性成分是2-氨基戊烷、正十一烷等一些烷烃类,这类物质由于风味阈值较高,使其对食品的整体风味贡献不大,但是这类物质在协调和维持食品整体风味的过程中有着重要的作用[30]。
3. 结 论
本文采用HS-SPME结合GC-MS分析三种不同色泽洋葱的挥发性成分。首先对萃取纤维头和顶空固相微萃取条件进行优化,以总离子流图中的峰个数和总峰面积为考察指标,对影响萃取效果的萃取温度、萃取时间和解析时间进行优化,得出较优的萃取条件为:50/30 μm DVB /CAR/PDMS萃取纤维头,在加入5 mL饱和NaCl溶液的10 g洋葱样中,60 ℃温度下萃取60 min,插入气相色谱进样口解析5 min,用来测定洋葱中的挥发性成分。通过对三种色泽洋葱的挥发性成分进行测定分析,共鉴定出61种挥发性成分,其中白皮、红皮、黄皮洋葱分别测到37、40、49种挥发性成分,相对含量分别占流出组分总量的70.29%、81.92%、79.03%。三种色泽洋葱的共有挥发性成分有22种,含硫化合物在三种色泽洋葱的挥发性化合物构成中占比较大,特别是二异丙基二硫醚和(E)-1-丙烯基-2-丙烯基二硫醚,两种物质相对含量的总和在三种色泽洋葱的挥发性成分中占比率都超过了20%,对形成洋葱特有特征风味贡献较大。挥发性成分的组成与含量的不同,构成了不同色泽洋葱的特殊辛香味。含硫化合物是新鲜洋葱中主要挥发性成分,同时也构成了洋葱的特征风味,红皮和黄皮洋葱的含硫化合物的相对含量远高于白皮洋葱,因此红皮和黄皮洋葱的辛辣味和扩散性气息比白皮洋葱更强烈。2-甲基-2-戊烯醛是洋葱催泪因子的主要带谢产物,红皮洋葱中2-甲基-2-戊烯醛相对含量高于白皮和黄皮洋葱,因此红皮洋葱比白皮和黄皮洋葱容易导致人眼睛流眼泪。
通过分析表明,3种色泽洋葱的挥发性成分的种类和组成存在着一定差异,特别是洋葱含硫化合物种类和含量的差异导致了不同品种洋葱的特征风味。但是特征香气不仅与挥发性成分的含量和种类有关,更是与挥发性成分的阈值和各成分间相互作用相关联,因此需要进一步采用气相色谱-嗅闻技术确定洋葱特征挥发性物质,为洋葱精油生产提供理论依据,促进洋葱产业高质量发展。
-
表 1 洋葱挥发性成分GC-MS分析结果
Table 1 GC-MS analysis of volatile compounds in onion
序号 保留时间(min) 化合物名称 CAS号 分子式 相对分子质量 相对含量(%) 白洋葱 红洋葱 黄洋葱 含硫化合物 1 6.04 Carbon disulfide
二硫化碳75-15-0 CS2 76.14 1.88 1.39 2 22.04 3,4-Dimethylthiophene
3,4-二甲基噻吩632-15-5 C6H8S 112.19 0.92 0.62 3 23.30 (E)-Allyl(propenyl)sulfane
(E)-烯丙基1-丙烯基硫醚104324-36-9 C6H10S 114.21 0.06 0.17 0.09 4 23.99 Diallyl sulfide
二烯丙基硫醚592-88-1 C6H10S 114.21 0.17 0.08 5 24.63 Methyl propyl disulfide
甲基丙基二硫醚2179-60-4 C4H10S2 122.25 0.37 3.36 4.15 6 26.07 2,4-Dimethylthiophene
2,4-二甲基噻吩638-00-6 C6H8S 112.19 3.84 3.57 2.85 7 26.23 2,5-Dimethylthiophene
2,5-二甲基噻吩638-02-8 C6H8S 112.19 2.07 1.65 8 26.81 (E)-1-Methyl-2-(propenyl)disulfane
(E)-1-甲基-2-丙烯基二硫醚23838-19-9 C4H8S2 120.24 2.00 9 28.40 (Z)-1-Methyl-2-(propenyl)disulfane
(Z)-1-甲基-2-丙烯基二硫醚23838-18-8 C4H8S2 120.24 0.19 5.24 3.05 10 34.04 Diisopropyl disulfide
二异丙基二硫醚4253-89-8 C6H14S2 150.30 12.41 10.05 13.11 11 34.87 Dimethyl trisulfide
二甲基三硫醚3658-80-8 C2H6S3 126.26 1.05 0.38 12 37.42 1-Allyl-2-isopropyl disulfane
1-烯丙基-2-异丙基二硫醚67421-85-6 C6H12S2 148.29 0.31 0.43 1.34 13 37.99 (E)-1-(Propenyl)-2-propyl disulfane
(E)-1-丙烯基-2-丙基二硫醚23838-21-3 C6H12S2 148.29 15.20 16.81 14.8 14 41.14 (E)-1-Allyl-2-(propenyl)disulfane
(E)-1-丙烯基-2-丙烯基二硫醚122156-02-9 C6H10S2 146.27 0.18 0.31 0.51 15 44.27 Methyl propyl trisulfide
甲基丙基三硫醚17619-36-2 C4H10S3 154.32 0.55 0.73 16 45.46 (E)-Propenyl propanedithioate
(E)-丙二硫代-1-烯-1-基丙酸酯67269-06-1 C6H10S2 146.27 2.24 2.56 1.32 17 45.85 (Z)-Propenyl propanedithioate
(Z)-丙二硫代-1-烯-1-基丙酸酯67230-81-3 C6H10S2 146.27 0.82 0.55 18 47.41 Methyl 1-(methylthio)propyl disulfide
甲基1-(甲硫基)丙基二硫醚53897-66-8 C5H12S3 168.34 0.16 0.07 19 52.29 2-Mercapto-3,4-dimethyl dihydrothiophene
2-巯基-3,4-二甲基噻吩137363-86-1 C6H10S2 146.27 3.73 20 52.68 Dipropyl trisulfide
二丙基三硫醚6028-61-1 C6H14S3 182.37 3.62 21 54.11 (E,E)-2,4-Nonadienal
(E,E)-2,4-壬二烯醛5910-87-2 C9H14O 138.21 0.25 0.03 22 55.66 1,2-Di((E)-propenyl)disulfane
1,2-2(E)-烯丙基二硫醚23838-23-5 C6H10S2 146.27 0.25 0.14 0.07 23 55.87 3,4-Dimethylthiophene-2,5-dione
2,5-二酮-3,4-二甲基噻吩10547-83-8 C6H6O2S 142.18 0.40 0.34 0.10 24 59.07 (E)-1-(Propenyl)-3-propyltrisulfane
(E)-1-烯丙基-3-丙基三硫醚23838-27-9 C6H12S3 180.35 6.22 6.43 4.48 25 60.17 (Z)-1-(Propenyl)-3-propyltrisulfane
(Z)-1-烯丙基-3-丙基三硫醚28383-26-8 C6H12S3 180.35 6.12 3.91 26 62.52 1-(1-(Methylthio)propyl)-2-propyldisulfane
1-甲硫丙烯基-2-丙烯基二硫醚126876-22-0 C7H16S3 196.40 0.19 0.22 27 67.34 1-Methyl-2-(1-(propenylthio)propyl)disulfane
甲基1-(1-丙烯硫基)丙基二硫醚126876-23-1 C7H14S3 194.38 0.55 0.94 醇类 28 7.42 Propyl mercaptan
丙硫醇107-03-9 C3H8S 76.16 0.39 29 20.09 (E)-2,4-Hexadien-1-ol
(E)-2,4-己二烯-1-醇111-28-4 C6H10O 98.14 9.7 12.01 7.34 30 37.64 1-Octen-3-ol
1-辛烯-3-醇3391-86-4 C8H16O 128.21 0.31 31 40.18 2-Ethyl-1-hexanol
2-乙基己醇104-76-7 C8H18O 130.23 0.20 0.20 0.12 32 44.45 1-Octanol
1-辛醇111-87-5 C8H18O 130.23 0.98 0.22 0.58 33 45.04 3-Methyl-2-butanol
3-甲基-2-丁醇598-75-4 C5H12O 88.15 0.08 34 48.17 (E)-2-Octen-1-ol
(E)-2-辛烯醇18409-17-1 C8H16O 128.21 0.16 0.01 35 50.65 1-Nonanol
1-壬醇143-08-8 C9H20O 144.25 0.28 0.09 0.24 36 56.90 Citronellol
香茅醇106-22-9 C10H20O 156.27 0.07 0.15 0.25 37 62.00 2-Tridecanol
2-十三醇1653-31-2 C13H28O 200.36 0.12 0.59 38 63.08 Benzyl alcohol
苯甲醇100-51-6 C7H8O 108.14 0.17 0.38 39 64.05 Phenylethyl Alcohol
苯乙醇60-12-8 C8H10O 122.16 0.32 2.88 40 67.81 Triethylene glycol monododecyl ether
3-十二烷醇3055-94-5 C18H38O4 318.49 0.82 醛类 41 6.64 Propanal
丙醛123-38-6 C3H6O 58.08 1.72 1.69 1.65 42 15.57 Hexanal
己醛66-25-1 C6H12O 100.16 0.32 43 19.78 2-Methyl-2-pentenal
2-甲基-2-戊烯醛623-36-9 C6H10O 98.14 0.58 1.02 0.44 44 21.32 Heptanal
庚醛111-71-7 C7H14O 114.19 0.10 0.02 45 27.84 Octanal
辛醛124-13-0 C8H16O 128.21 0.13 0.15 46 30.41 (E)-2-Heptenal
(E)-2-庚烯醛18829-55-5 C7H12O 112.17 0.14 47 34.57 Nonanal
壬醛124-19-6 C9H18O 142.24 4.34 0.76 0.92 48 37.21 (E)-2-Octenal
(E)-2-辛烯醛2548-87-0 C8H14O 126.20 0.30 0.15 0.10 49 40.46 2,5-Dihydroxybenzaldehyde
2,5-二羟基苯甲醛1194-98-5 C7H6O3 138.12 0.07 0.02 50 41.30 Decanal
癸醛112-31-2 C10H20O 156.27 0.17 51 43.89 (E)-2-Nonenal
(E)-2-壬烯醛18829-56-6 C9H16O 140.22 1.42 0.30 0.43 52 50.41 (E)-2-Decenal
(E)--2-癸烯醛3913-81-3 C10H18O 154.25 0.39 0.19 53 56.72 2-Undecenal
2-十一烯醛2463-77-6 C11H20O 168.28 0.10 0.03 酮类 54 59.53 2-Tridecanone
2-十三烷酮593-08-8 C13H26O 198.34 0.22 0.24 55 59.79 2,4-Octanedione
2,4-辛二酮14090-87-0 C8H14O2 142.20 0.94 56 62.01 6,10-dimethyl-5,9-undecadien-2-one
6,10-二甲基-5,9-十一双烯-2-酮689-67-8 C13H22O 194.31 0.24 0.17 57 65.04 1,4-Cyclohexanedione
1,4-环己二酮37-88-7 C6H8O2 112.13 0.17 其他 58 4.61 2-Aminopentane
2-氨基戊烷63493-28-7 C5H13N 87.16 0.40 59 44.62 Linalyl acetate
乙酸芳樟酯115-95-7 C12H20O2 196.29 0.12 60 50.35 Butanoic acid
丁酸107-92-6 C4H8O2 88.11 0.41 61 62.71 Heneicosane
二十一烷629-94-7 C21H44 296.57 0.15 0.27 表 2 各样品挥发性化学成分物质种类及其含量比较
Table 2 Comparison of types of volatile compounds and their relative contents in onion
类别 白洋葱 红洋葱 黄洋葱 种类 含量(%) 种类 含量(%) 种类 含量(%) 含硫化合物 15 47.53 23 64.01 25 60.06 醛类 11 9.54 6 3.99 11 4.12 醇类 7 11.70 9 13.36 8 13.60 酮类 3 1.40 0 0 3 0.58 其他 1 0.12 2 0.56 2 0.67 总量 70.29 81.92 79.03 -
[1] LUBNA M CA, MOHANNAD A H, RASHIDA A, et al. Antibacterial and antioxidant potential of the phenolic extract and its fractions isolated from Allium ascalonicum (onion) peel[J]. Natural Product Research,2021,7(1):1−5.
[2] GONZALEZ-PENA D, CHECA A, ANCOS B, et al. New insights into the effects of onion consumption on lipid mediators using a diet-induced model of hypercholesterolemia[J]. Redox Biology,2017,11:205−212. doi: 10.1016/j.redox.2016.12.002
[3] HUANG W, TANG G, ZHANG L Y, et al. Effect of onion on blood lipid profile: A meta-analysis of randomized controlled trials[J]. Food Science & Nutrition,2021,9(7):3563−3572.
[4] LUCA A, MAHAJAN P V, EDELENBOS M. Changes in volatile organic compounds from wild rocket (Diplotaxis tenuifolia L. ) during modified atmosphere storage[J]. Postharvest Biology Technology,2016,114:1−9. doi: 10.1016/j.postharvbio.2015.11.018
[5] JUNG-HO K, JEONG S, NA-HYUNG K, et al. Variation of quercetin glycosides derivatives in three onion (Allium cepa L. ) varieties[J]. Saudi Journal of Biological Sciences,2017,24(6):1387−1391. doi: 10.1016/j.sjbs.2016.05.014
[6] COZZOLINO R, MALORNI L C, MARTIGENTTI A C, et al. Comparative analysis of volatile profiles and phenolic compounds of four southern Italian onion (Allium cepa L. ) landraces[J]. Journal of Food Composition and Analysis,2021,101:103990−103999. doi: 10.1016/j.jfca.2021.103990
[7] COLINA-COCA C, GONZALEZ-PENA D, VEGA E, et al. Novel approach for the determination of volatile compounds in processed onion by headspace gas chromatography-mass spectrometry (HS-GC-MS)[J]. Talanta,2013,103:137−144. doi: 10.1016/j.talanta.2012.10.022
[8] CHOI S M, LEE D J, KIM J Y, et al. Volatile composition and sensory characteristics of onion powders prepared by convective drying[J]. Food Chemistry,2017,231:386−392. doi: 10.1016/j.foodchem.2017.03.129
[9] 孙雪君, 徐怀德, 米林峰. 鲜洋葱和干洋葱挥发性化学成分比较[J]. 食品科学,2012,33(22):290−293. [SUN X J, XU H D, MI L F. Analysis of volatile compounds from fresh and dried Allium cepa L J]. Food Science,2012,33(22):290−293.
[10] LIU M P, SU Y, GUO Y L. Determination of highly volatile compounds in fresh onion (Allium cepa L. ) by room-temperatureenrichment headspace-trap coupled to cryotrapping GC-MS[J]. Separayion Science Plus,2018,1(8):83−538.
[11] CLARKE H, MANNION D T, O’SULLIVAN M G, et al. Development of a headspace solid-phase microextraction gas chromatography mass spectrometry method for the quantification of volatiles associated with lipid oxidation in whole milk powder using response surface methodology[J]. Food Chemistry,2019,292:75−80. doi: 10.1016/j.foodchem.2019.04.027
[12] LIANG X, WU J H, ZHAN Q Y, et al. Multiple headspace solidphase micro-extraction for the total content determination of tetramethylpyrazine in various vinegar samples by GC-FID[J]. Analytical Methods,2019,11(18):2443−2449. doi: 10.1039/C8AY02816H
[13] 江勇. 固相微萃取在食品快速分析中的应用[D]. 南昌: 南昌大学, 2010: 70−100. JIANG Y. Application of solid-phase microextraction in rapid analysis of food[D]. Nanchang: Nanchang University, 2010: 70−100.
[14] WANG J, DU Q, YOU X R, et al. Solvent-free high-throughput analysis of herbicides in environmental water[J]. Analytical Chemistry,2019,1071:8−16.
[15] SOUZA-SILVA É A, REYES-GARCES N, GOMEZ-RIOS G A, et al. A critical review of the state of the art of solid-phase microextraction of complex matrices III. Bioanalytical and clinical applications[J]. TRAC Trends in Analytical Chemistry,2015,71:249−264. doi: 10.1016/j.trac.2015.04.017
[16] FERNANDES S, GOIS A, MENDES F, et al. Typicality assessment of onions (Allium cepa) from different geographical regions based on the volatile signature and chemometric tools[J]. Foods (Basel, Switzerland),2020,9(3):1−15.
[17] D'AURIA M, RACIOPPI R. HS-SPME-GC-MS analysis of onion (Allium cepa L.) and shallot (Allium ascalonicum L.)[J]. Food Research,2017,1(5):161−165. doi: 10.26656/fr.2017.5.055
[18] 张文娟, 周考文. HS-SPME-GC-MS在食品挥发性物质分析中的应用[J]. 食品研究与开发, 2021, 42(17): 218−244. ZHANG W J, ZHOU K W. Application of HS-SPME-GC-MS in the analysis of volatile components in food[J]. Food Research and Development, 2021, 42(17): 218−244.
[19] MACHOY M, BAJER T, ŠILHA D, et al. Release of volatile compounds from sliced onion analysed by gas chromatography coupled to mass spectrometry and its antimicrobial activity[J]. Journal of Food and Nutrition Research,2019,58(4):393−400.
[20] 刘彩云, 赵军霞, 魏晋梅. 啤特果醋香气成分分析[J]. 中国调味品,2018,43(1):160−163. [LIU C Y, ZHAO J X, WEI J M, et al. Analysis of aroma components in piteguo vinegar[J]. China Condiment,2018,43(1):160−163. doi: 10.3969/j.issn.1000-9973.2018.01.037 [21] BRODNITZ M, PASCALE J V. Thiopropanal S-oxide: A lachrymatory factor in onions[J]. Journal of Agricultural and Food Chemistry,1971,20:269−272.
[22] CARSON J F. Chemistry and biological properties of onions and garlic[J]. Food Reviews International,1987,3(1-2):71−103. doi: 10.1080/87559128709540808
[23] ROKAYYA S, ABEER E, MONA A, et al. In-vitro evaluation of the antioxidant and anti-inflammatory activity of volatile compounds and minerals in five different onion varieties[J]. Separations,2021,8(5):57−63. doi: 10.3390/separations8050057
[24] BYSTRICKA J, MUSILOVA J, VOLLMANNOVA A, et al. Bioactive components of onion (Allium cepa L.)[J]. Acta Alimentaria,2013,42(1):11−22. doi: 10.1556/AAlim.42.2013.1.2
[25] ZALEPUGIN D Y, TILKUNOVA N A, CHERNYSHOVA I V. Stability of thiosulfinates from garlic (Allium sativum L. ) supercritical extracts in polar and nonpolar solvents[J]. Russian Journal of Physical Chemistry B,2015,9(7):1032−1042. doi: 10.1134/S1990793115070143
[26] ANNA T, FABRIZIO A, AMALIA P, et al. Characterization of volatile organic compounds in ‘Rossa di Tropea’ onion by means of headspace solid-phase microextraction gas chromatography-mass spectrometry (HS/SPME GC-MS) and sensory analysis[J]. Agronomy,2021,11(5):874−883. doi: 10.3390/agronomy11050874
[27] 方海田, 刘慧燕, 张光弟, 等. 宁夏3种葱属蔬菜的挥发性成分比较分析[J]. 中国调味品,2018,43(1):145−149. [FANG H T, LIU H Y, ZHANG G D, et al. Comparative analysis of volatile components in three Alliaceous vegetables in Ningxia[J]. China Condiment,2018,43(1):145−149. [28] CECCHI L, IER F, VIGNOLINI P, et al. Characterization of volatile and flavonoid composition of different cuts of dried onion (Allium cepa L. ) by HS-SPME-GC-MS, HS-SPME-GC×GC-TOF and HPLC-DAD[J]. Molecules,2020,25(2):1−14.
[29] COLLADO-FERNANDEZ M. Pungency and volatile compounds in some Spanish onion cultivars[J]. Acta Horticulturae,2018,1194(1194):999−1006.
[30] 张德莉, 田洪磊, 詹萍, 等. 基于HS-SPME-GC-MS技术的香葱油挥发性成分解析[J]. 食品研究与开发,2018,39(17):111−116. [ZHANG D L, TIAN H L, ZHAN P, et al. Analysis of volatile components of chive oil based on HS-SPME-GC-MS[J]. Food Research and Development,2018,39(17):111−116. doi: 10.3969/j.issn.1005-6521.2018.17.021 -
期刊类型引用(12)
1. 刘帅,荣晓辉,张书锋,屈磊,刘芳,井娟. 纳豆激酶递送系统研究进展. 中国现代应用药学. 2024(09): 1295-1302 .  百度学术
百度学术
2. 施雅,朱佳妮,赵博,米飞,顾然. 常见发酵食品中生物活性物质对心脏功能影响的研究进展. 食品与发酵科技. 2024(03): 92-98 .  百度学术
百度学术
3. 祁红兵,宋军霞,毛艳红. 纳豆固体发酵抗氧化功能研究. 农产品加工. 2024(18): 1-4+9 .  百度学术
百度学术
4. 屈家亮,柳惠平,张佑红. 纳豆激酶研究进展. 武汉工程大学学报. 2024(05): 527-533 .  百度学术
百度学术
5. 吴丹,杨苗苗,杜小平,祁蒙,杨水云. 依赖于豆粕原材料的纳豆激酶制备和纯化工艺研究. 中国调味品. 2023(03): 79-85 .  百度学术
百度学术
6. Chunfang Wang,Jinpeng Chen,Wenguo Tian,Yanqi Han,Xu Xu,Tao Ren,Chengwang Tian,Changqing Chen. Natto: A medicinal and edible food with health function. Chinese Herbal Medicines. 2023(03): 349-359 .  必应学术
必应学术
7. 王刚,王芝玉,安荣荣,滕玉婷,古梅,刘霞,高慧娟,董瑞丽. 固态发酵条件对纳豆激酶活性的影响及发酵条件的优化. 粮食加工. 2023(05): 33-37 .  百度学术
百度学术
8. 任莉莉,张胜海,程昆木,杨凌鉴,黄九林. 模拟体内环境下血栓形成及药物溶栓作用. 粘接. 2022(02): 1-5 .  百度学术
百度学术
9. 潘钰,夏海华,叶阳,曲晓军,于冲. 纳豆软胶囊功效成分安全性及免疫功能研究. 中国调味品. 2022(06): 84-89 .  百度学术
百度学术
10. 洪奕,夏海华,田洁萍,张淑梅,于冲,田缘,闫更轩,潘钰. 响应面法优化豆粕固体发酵产纳豆激酶培养条件. 中国调味品. 2022(08): 41-45 .  百度学术
百度学术
11. 樊璐,李宏梁,吕名蕊,严烨,黄峻榕. 纳豆糕点的制备及活菌数变化特性的研究. 农产品加工. 2022(15): 15-17+21 .  百度学术
百度学术
12. 高梦迪,苏钱琙,李杰,樊学晶,王朝阳,邓立高,李坚斌. 纳豆激酶微生物生产研究进展. 大豆科学. 2022(06): 740-746 .  百度学术
百度学术
其他类型引用(9)





 下载:
下载:
 下载:
下载:



