Production of Bacillus subtilis Microbioecologics by Fermentation of Hongqu Residue
-
摘要: 本研究通过单因素和响应面分析优化红曲废渣制备枯草芽孢杆菌微生态制剂的条件,对发酵过程中可溶性糖和可溶性蛋白质的含量进行追踪,以分析菌体增长的限制因素,并对该微生态制剂的储藏稳定性和体外抗氧化性进行评估。结果表明,当发酵条件为:红曲废渣浓度100 g/L,枯草芽孢杆菌接种量为10% (5 lg CFU/mL),摇床转速为220 r/min时,在37 ℃条件下发酵48 h可获得枯草芽孢杆菌最高产量为(9.3±0.3)lg CFU/mL。红曲废渣中可溶性葡萄糖的含量是限制枯草芽孢杆菌生长的主要因素。当可溶性糖含量较低时,枯草芽孢杆菌的生长基本停止。根据加速保存实验可计算出微生态制剂在20 ℃下保存3个月后的活菌数为8.7 lg CFU/mL,高于应用标准。微生态制剂具有较强的抗氧化性,其DPPH自由基清除能力为0.25 mg/mL(IC50),羟自由基的清除能力为0.69 mg/mL(IC50)。本研究证明红曲废渣可作为原料制备枯草芽孢杆菌微生态制剂,为微生物发酵废渣的可持续性绿色加工提供了实践依据。Abstract: In this study, single factor and response surface analysis were used to optimize the conditions for the production of Bacillus subtilis using Hongqu residue, the content of soluble sugar and soluble protein components during the fermentation were determined to analyze the limiting factors of bacterial growth, and the storage stability and the in vitro antioxidant activity of the microbioecologics were determined. The results showed that the highest yield of Bacillus subtilis in microbioecologics was (9.3±0.3) lg CFU/mL that was produced at 37 ℃ for 48 h with the conditions of 100 g/L Hongqu residue, and shaking speed of 220 r/min with 10% inoculation volume of 5 lg CFU/mL Bacillus subtilis. The content of soluble glucose in Hongqu residue was the main factor limiting the growth of Bacillus subtilis. When soluble sugar contents were low, the growth of Bacillus subtilis basically stopped. According to the accelerated preservation experiment, the viable count of probiotics stored at 20 ℃ for three months was 8.7 lg CFU/mL, which was higher than the criteria of microbioecologics application. The microbioecologics had strong antioxidant activity that scavenging capacity of DPPH free radical and hydroxyl free radical were 0.25 mg/mL (IC50) and 0.69 mg/mL (IC50) , respectively. This study proved that Hongqu residue could be used as a raw material to prepare Bacillus subtilis probiotics, which provided a practical basis for the sustainable green processing of microbial fermentation residue.
-
红曲废渣是红曲霉液态发酵并经色素提取后剩余的残渣,其中含有约40%碳水化合物、25%蛋白质、2.5%脂类以及少量的红曲色素、麦角固醇和壳聚糖等活性物质[1-3]。充分挖掘红曲废渣的应用价值,符合我国发展可持续性食品产业的战略。
我国每年红曲废渣的产量近万吨[4-6],但当前红曲废渣的开发应用较少,主要用于生产蛋白质饲料[7]或作为原材料提取莫纳克林K和γ-氨基丁酸[8]等活性物质。然而,红曲废渣不易消化吸收,直接用于动物饲料时料肉比较低[7,9];红曲废渣处理后仍保留大量营养物质,将其用于功能性物质提取,存在富营养污染的风险。相比之下,若以枯草芽孢杆菌发酵红曲废渣并将其制成微生态制剂,可充分利用红曲废渣中的营养成分,以实现废弃物的绿色高效利用。一方面,枯草芽孢杆菌是国际公认的可直接添加在动物饲料中的益生菌[10-11],具有调节机体胃肠道生态平衡[12-14]、促进生长[15-16]、增强机体免疫力[17-19]等多种功效,可用于制备具有保健功能的微生态制剂。另一方面,红曲中的营养成分,包括碳水化合物与蛋白质,可被枯草芽孢杆菌降解、利用,并生成具有较强抗氧化性的代谢物质[20-22]。
为了充分利用红曲废渣,本研究将其作为原料,发酵制备枯草芽孢杆菌微生态制剂。通过单因素和响应面优化确定最佳发酵条件;测定发酵过程中可溶性糖含量的变化,分析枯草芽孢杆菌对红曲废渣中可溶性糖和蛋白质的利用情况;利用加速贮藏实验评价微生态制剂中枯草芽孢杆菌活菌的储藏稳定性;对微生态制剂中可溶性成分的抗氧化性进行评估(包括铁还原力、DPPH自由基和羟自由基的清除能力)。为充分挖掘红曲废渣的价值,发展可持续性食品产业提供数据支持。
1. 材料与方法
1.1 材料与仪器
枯草芽孢杆菌(FZU.SWJS03) 福州大学食品科学技术研究所筛选获得;红曲废渣 广东省天益生物科技有限公司提供,干燥的红曲废渣经100目筛网后,4 ℃密封保存;D-木糖、D-半乳糖、D-甘露糖、D-葡萄糖、D-阿拉伯糖 色谱纯,源叶生物有限公司;甲醇 分析纯,德国MERCK公司;其他分析纯试剂 上海国药集团化学试剂有限公司。
THZ-82型恒温震荡器 常州国华电器有限公司;XPN-100/90/80型高速冷冻离心机 贝克曼库尔特仪器有限公司;LDZX-50KB型立式压力蒸汽灭菌锅 上海名元实业有限公司;HH-6型数显恒温水浴锅 常州蒙特仪器制造有限公司;UV-2000型紫外可见分光光度计 上海一恒科学仪器有限公司;SH220F石墨消解仪 山东海能科学仪器有限公司;Agilent 6890 A高效气相色谱仪 安捷伦有限公司;Kjeltec 8400 型全自动凯氏定氮仪 丹麦福斯集团公司。
1.2 枯草芽孢杆菌的发酵
1.2.1 枯草芽孢杆菌种子液的制备
配制普通液体培养基(蛋白胨10 g/L,酵母提取物5 g/L,氯化钠10 g/L),用0.1 mol/L NaOH溶液将培养基的初始pH调节至7.2。在37 ℃下恒温培养枯草芽孢杆菌12 h,使其达到指数生长期,然后将在枯草芽孢杆菌指数生长期的菌液离心并用无菌生理盐水(9 g/L NaCl溶液)洗涤两次。将重悬菌液的浓度调节至5 lg CFU/mL,制备枯草芽孢杆菌种子液。
1.2.2 单因素实验
将红曲废渣和去离子水在250 mL三角烧瓶中充分混合后,在121 ℃下高压灭菌20 min。固定接种量为3.0 mL种子液,以红曲废渣浓度100 g/L、枯草芽孢杆菌接种量10%、摇床转速220 r/min、发酵时间48 h为固定参数,设计单因素实验。依次改变发酵时间0、6、12、18、24、30、36、42、48 h、红曲废渣浓度50、75、100、125、150 g/L、枯草芽孢杆菌接种量5%、10%、15%、20%、25%、以及摇床转速160、180、200、220、240 r/min,固定其他基本实验条件,测定在37 ℃条件下对枯草芽孢杆菌生长的影响(活菌数的变化)。
1.2.3 响应面试验
根据单因素实验的结果和Box-Behnken中心组合试验设计原理,以枯草芽孢杆菌活菌数(Y)为响应值,以红曲废渣浓度(A)、枯草芽孢杆菌接种量(B)和摇床转速(C)为自变量,设计三因素三水平的响应面分析试验对发酵参数进行优化。每组试验重复3次,结果取其平均值。试验方案如表1所示。
表 1 中心组合设计的因素水平表Table 1. Factors and levels table of Box-Behnken Design (BBD)水平 因素 A 红曲废渣浓度(g/L) B 接种量(%) C 摇床转速(r/min) −1 75 5 200 0 100 10 220 1 125 15 240 1.3 测定方法
1.3.1 枯草芽孢杆菌活菌数
在无菌条件下准确量取1.0 mL待测样,取1.0 mL发酵液依次进行10倍稀释至合适倍数,平板涂布后进行恒温培养,24 h后观察计数。
1.3.2 可溶性蛋白测定
每隔6 h取发酵液,5000 r/min 离心20 min,弃去沉淀,取上清液置于消化管中,加入3.0 g硫酸钾、0.2 g硫酸铜和10.0 mL浓硫酸,然后在石墨消解仪中消化,待消化完全后,冷却至室温并在全自动凯氏定氮仪中进行消化,最后用稀盐酸溶液滴定。实验依据GB 5009.5-2016《食品安全国家标准食品中蛋白质的测定》中的凯氏定氮法和全自动凯氏定氮仪测定可溶性糖含量。
1.3.3 可溶性糖测定
每隔6 h取发酵液,5000 r/min 离心20 min,弃去沉淀,取上清液按照GB 5009.7-2016《食品安全国家标准食品中还原糖的测定》中的苯酚硫酸法进行测定。
1.3.4 单糖组成分析
每隔6 h取发酵液,5000 r/min 离心20 min,弃去沉淀,取上清液于密封的玻璃管中,移入2.0 mL三氟乙酸溶液(TFA,2 mol/L),密封振荡均匀,在120 ℃条件下水解5 h。反应结束后,利用氮吹仪吹干(水浴温度设置为70 ℃),加入 3.0 mL色谱级甲醇重复若干次,直至除尽三氟乙酸为止,备用。
分别称量10.0 mg的阿拉伯糖、甘露糖、葡萄糖、半乳糖、N-乙酰氨基葡萄糖、N-乙酰胞壁酸单糖于密封的玻璃管中,依次加入盐酸羟胺10.0 mg, 内标物肌醇10.0 mg和吡啶1.0 mL,于90 ℃水浴锅中振荡反应30 min。反应结束冷却,在相同条件下加入1.0 mL醋酸酐进行乙酰化,得到糖腈乙酸酯的衍生物。冷却,加入适量的甲醇,70 ℃下氮吹,反复3~4次除去乙酸酐和吡啶。混合单糖标准品(含各单糖1.0 mg)与经三氟乙酸水解后的样品均按上述步骤处理后加入1.5 mL色谱级甲醇溶解。将样品经0.22 μm的有机微孔滤膜过滤后,注入色谱进样瓶,通过气相色谱以RTX-1701石英毛细管(0.25 μm×30.0 m)和氢火焰离子化检测器(FID)分析单糖组分。程序升温:180~220 ℃(5 ℃/min), 220 ℃(5 min),220~280 ℃(10 ℃/min);载气:氮气(1.0 mL/min);进样量:1.0 μL。以肌醇作为内标,通过各组分峰面积计算其含量。
1.3.5 储藏稳定性
收集优化发酵后的枯草芽孢杆菌活菌制剂,将其初始浓度调整为4.1×109 CFU/mL。参考朱征宇等的方法[23],分别在30、37、50、60 ℃下对微生态制剂进行加速贮藏实验,测定枯草芽孢杆菌活菌数以考察稳定性。微生物的失活速率与菌种特性所处的营养条件及温度有关,其失活过程符合一级反应动力学。可表示为:
lgNt=−kt/2.303+lgN0 (1) 式中:N0表示初始活菌数,CFU/mL;Nt表示t时刻残存活菌数,CFU/mL;k表示失活常数,h−1;t表示失活时间,h。
同时,不同温度下的失活常数k与温度T的动力学关系符合Arrhenius方程,其对数形式为:
lgk=−E2.303RT+lgA (2) 可利用该公式计算不同温度下的失活常数k。式中:A为Arrhenius常数(通过不同温度条件下测定失活常数k并绘制拟合趋势线,由其X轴截距=lgA计算而得);E表示微生物失活所需的活化能,4.186 J/mol;R为摩尔气体常数,8.314 J/mol·K;T表示温度,K。
菌株的存活率可表示为:
存活率(%)=NtN0 (3) 1.3.6 抗氧化性
参考黄梦姣[24]测定铁还原力、DPPH·和羟自由基(·OH)清除能力的方法,略作修改后测定枯草芽孢杆菌微生态制剂溶液的抗氧化性。将1.0 mL发酵液与10.0 mL 50%甲醇充分混匀,在25 ℃暗室中浸泡6 h后用滤纸过滤,将滤过液定容至10.0 mL备用。
1.3.6.1 铁还原力
在1.0 mL不同体积浓度(20%、40%、60%、80%、100% ,v/v)的样品(枯草芽孢杆菌微生态制剂的可溶性物质浓度分别为0.04、0.09、0.17、0.34、0.51、0.68、0.85 mg/mL)中加入2.5 mL 0.2 mol/L磷酸盐缓冲液(pH6.5)和2.5 mL 10 g/L铁氰化钾溶液并混合均匀,50 ℃恒温水浴20 min。取出快速冷却后,再加入2.5 mL 100 g/L 三氯乙酸溶液,并以3000 r/min离心10 min。取上清液加入2.5 mL蒸馏水和0.5 mL 1 g/L FeCl3溶液静置10 min后于700 nm处测定其吸光值。以铁氰化钾溶液当量(mmol/L)表示样品的抗氧化能力,并将其抗氧化效果与0.1 mg/mL维生素C溶液进行对比。
1.3.6.2 1,1-二苯基-2-三硝基苯肼(DPPH)自由基清除能力
取1.0 mL不同体积浓度(20%、40%、60%、80%、100% ,v/v)的样品(枯草芽孢杆菌微生态制剂的可溶性物质浓度分别为0.04、0.09、0.17、0.34、0.51、0.68、0.85 mg/mL)与2.0 mL 0.1 mmol/L的DPPH·醇溶液混合,避光孵育30 min后,于517 nm处测定其吸光值(AS1)。在同样条件下,以样品与等体积的无水乙醇混合作为样品空白,测定其吸光值(AS0);以2.0 mL 0.1 mmol/L的DPPH·醇溶液与等体积的无水乙醇混合作为对照,测定其吸光值(AC)。根据下列公式计算枯草芽孢杆菌微生态制剂溶液对DPPH·的清除率,并将其效果与0.1 mg/mL维生素C溶液进行对比。
DPPH⋅清除率(%)=1−AS1−AS0AC×100 (4) 式中:AS1、AS0、AC分别表示样品、样品空白、空白对照的吸光值。
1.3.6.3 羟自由基(·OH)清除能力
将1.0 mL 9 mmol/L FeSO4和1.0 mL 9 mmol/L水杨酸溶液混合后,分别加入0.05、0.10、0.20、0.40、0.80、1.00 mL样品(枯草芽孢杆菌微生态制剂的可溶性物质浓度分别为0.04、0.09、0.17、0.34、0.51、0.68、0.85 mg/mL),再加入1.0 mL 8.8 mmol/L H2O2溶液,于37 ℃下反应30 min后,在510 nm处测定其吸光值(A S1)。在同样条件下,用1.0 mL蒸馏水代替H2O2溶液作为样品空白,测定吸光值(AS0);以1.0 mL蒸馏水代替样品作为空白对照,测定其吸光值(AC)。根据下列公式计算待测枯草芽孢杆菌微生态制剂溶液对·OH的清除率,并将其效果与0.4 mg/mL维生素C溶液进行对比。
⋅OH清除率(%)=1−AS1−AS0AC×100 (5) 式中:AS1、AS0、AC分别表示样品、样品空白、空白对照的吸光值。
1.4 数据处理
采用Design-Expert 8.0.6软件对Box-Behnken中心组合试验设计的结果进行数据处理,进行回归模型的建立和单因素方差分析。若无特别说明,以上所有实验数均重复3次,通过Excel计算平均值和标准偏差。
2. 结果与分析
2.1 枯草芽孢杆菌发酵红曲废渣的单因素实验
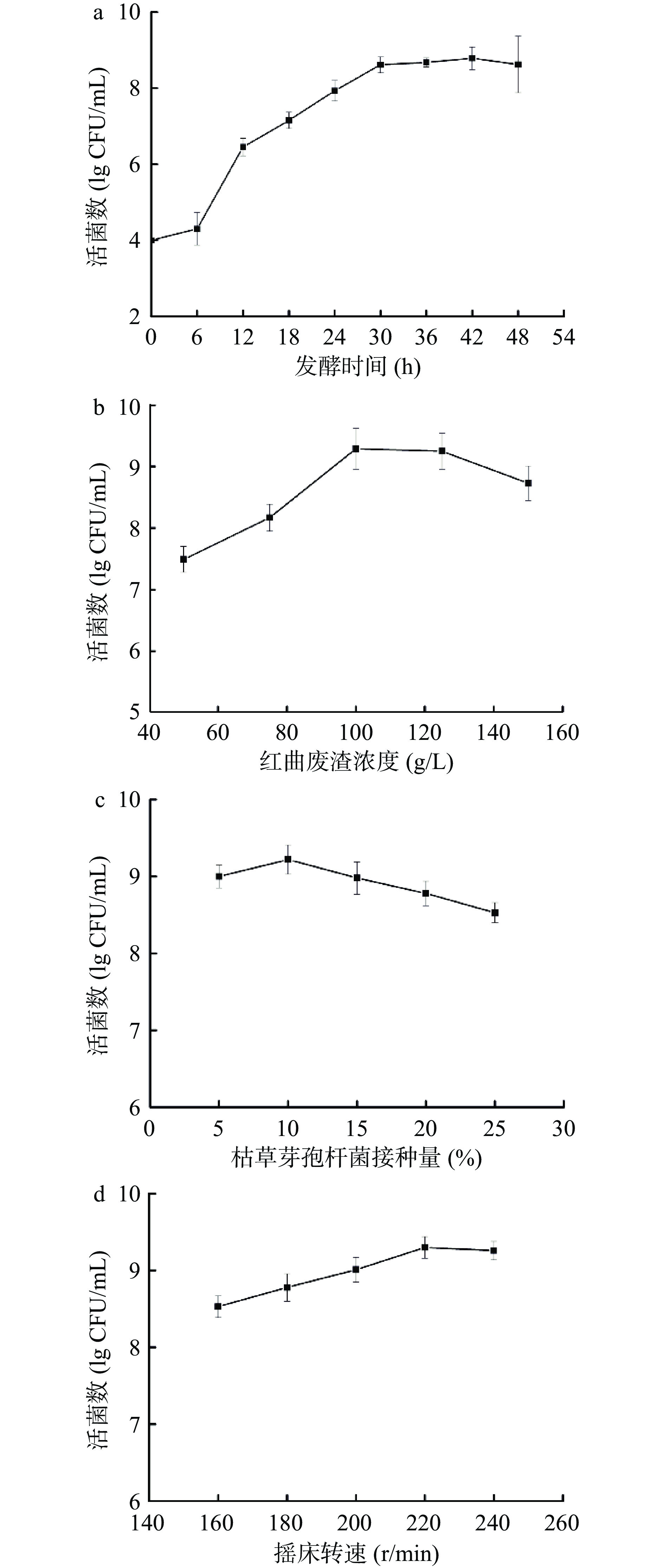
通过单因素实验对枯草芽孢杆菌的生长条件进行分析,结果如图1所示。图1a显示随着发酵时间的增加,枯草芽孢杆菌发酵红曲废渣的活菌数呈现先上升后平稳的趋势,在发酵30 h后基本进入平稳期,最大活菌数为8.8 lg CFU/mL。为保证发酵完全,在后续实验中固定发酵时间为48 h。图1b~d分别显示红曲废渣浓度、枯草芽孢杆菌接种量以及摇床转速对枯草芽孢杆菌生长量的影响,结果表明在这三个变量数值增大的过程中,枯草芽孢杆菌的活菌数均表现为先上升后下降的趋势。红曲废渣在浓度为100 g/L时,活菌数达到最大值,为9.3 lg CFU/mL(图1b)。红曲废渣浓度较低时,提高原料浓度可以为菌生长提供充足的碳源、氮源等营养物质;然而当其浓度过高时,培养基的流动性变差,传质效率降低,进而使得枯草芽孢杆菌生长受限。当枯草芽孢杆菌的接种量为10%时,活菌数达到最大值,为9.2 lg CFU/mL(图1c)。初始接种量小于10%时,会延长枯草芽孢杆菌增殖到峰值的时间;而初始接种量过大会使其快速吸收营养物质,迅速增殖导致溶氧量不足,反而使其增殖受限。当摇床转速为220 r/min时,活菌数达到最大值9.3 lg CFU/mL(图1d)。这是由于摇瓶里的溶氧量随摇瓶转速的提高而上升,较多的氧气可以促进枯草芽孢杆菌增殖;而转速过大时,枯草芽孢杆菌的流动过于剧烈反而造成菌体的死亡。为进一步优化发酵条件,选择红曲废渣浓度为75~125 g/L,枯草芽孢杆菌接种量为5%~15%、摇床转速为200~240 r/min进行后续响应面实验设计。
2.2 响应面优化枯草芽孢杆菌发酵红曲废渣条件
2.2.1 响应面试验设计及结果
根据单因素实验的结果,选择红曲废渣浓度(A),接种量(B),摇床转速(C)为自变量,以枯草芽孢杆菌的总活菌数为响应值(R),设计三因素三水平的响应面分析试验,在17个不同试验组合的条件下,试验设计方案见表2。
表 2 枯草芽孢杆菌发酵红曲废渣的响应面试验结果Table 2. Response surface test design of Hongqu residue fermented by Bacillus subtilis编号 A
(g/L)B
(%)C(r/min) R
(lg CFU/mL)编号 A
(g/L)B(%) C(r/min) R
(lg CFU/mL)1 100 10 220 9.3 10 125 5 220 8.6 2 125 10 200 7.8 11 125 10 240 7.8 3 100 5 240 7.4 12 100 10 220 9.3 4 75 15 220 7.2 13 75 10 200 7.2 5 100 5 200 8.2 14 100 15 200 7.1 6 100 5 220 7.0 15 100 10 220 9.3 7 100 10 220 9.3 16 125 15 220 7.4 8 100 10 220 9.3 17 75 10 240 7.7 9 100 10 240 7.5 使用Design-Expert 8.0软件对表2实验结果进行二次多项式回归拟合和回归方程的方差分析(表3),得到二次多项式回归方程:
表 3 回归方程的方差分析Table 3. ANOVA of regression equation差异来源 平方和 自由度 均方误差 F P 显著性 模型 13.22 9 1.47 1218.93 <0.0001 ** A 0.24 1 0.24 196.12 <0.0001 ** B 1.176−3 1 1.176−3 0.98 0.3561 C 0.14 1 0.14 117.00 <0.0001 ** AB 0.035 1 0.035 29.02 0.0010 ** AC 0.061 1 0.061 50.83 0.0002 ** BC 0.016 1 0.016 13.07 0.0086 ** A2 3.05 1 3.05 2532.88 <0.0001 ** B2 5.60 1 5.60 4644.40 <0.0001 ** C2 2.78 1 2.78 2310.40 <0.0001 ** 残差 8.435−3 7 1.205−3 失拟项 6.886−3 3 2.295−3 5.93 0.0592 纯误差 1.549−3 4 3.872−3 总和 13.23 16 注:*:P<0.05 ,表示显著;** :P<0.01 ,表示极显著。 Y=9.29+0.17A−0.012B+0.13C−0.094AB−0.12AC+0.063BC−0.85A2−1.15B2−0.81C2
回归方程的决定系数R2为0.99,其方差分析(见表3)的显著性检验表明,该回归模型P<0.0001,方程模拟表现极显著,失拟项P=0.0592>0.05,不显著,模型拟合良好,可用于红曲废渣培养枯草芽孢杆菌工艺优化预测。其中红曲废渣浓度、摇床转速对活菌数的影响均高度显著,三种因素对活菌数影响的排序为红曲废渣浓度(A)>摇床转速(C)>枯草芽孢杆菌接种量(B),并且一次项A、C,交互项AB、AC、BC,二次项A2、B2、C2对枯草芽孢杆菌总活菌数的影响极显著(P<0.01)。
2.2.2 交互作用分析
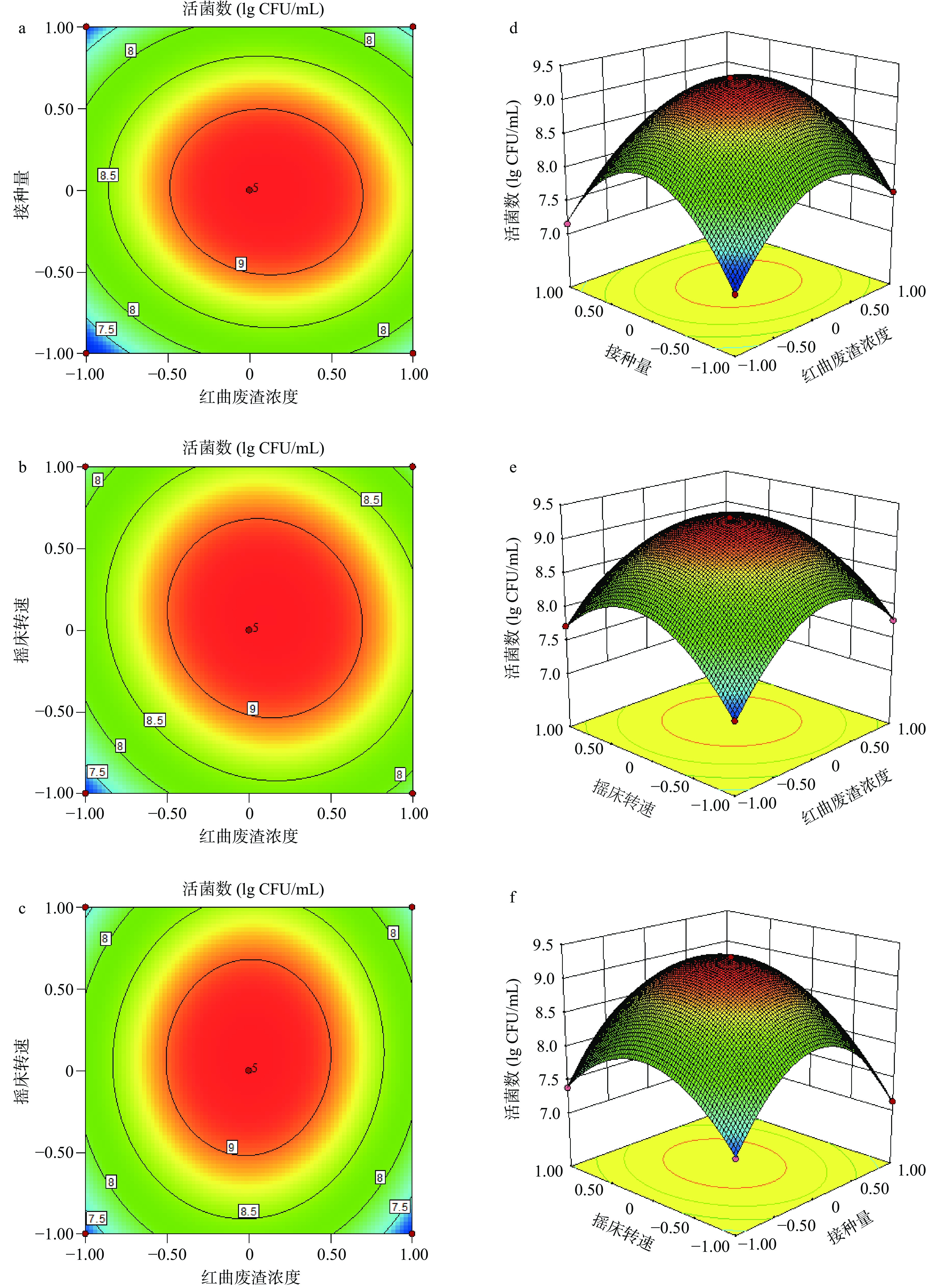
为了更为直观的说明三种因素间的交互作用对枯草芽孢杆菌活菌数的影响,通过回归方程绘制响应面的3D曲面图和等高线图,考察相应的拟合曲面。如图2所示,三个参数两两间的3D曲面均开口向下且等高线均呈椭圆形,表明三种因素两两之间存在交互作用,且存在两两间的最适组合使得总活菌数最高;其中,接种量对活菌数的影响大于红曲废渣浓度,另外两种因素的交互作用对活菌数的影响程度相近。
2.2.3 验证实验
通过响应面回归模型及软件分析得到最优发酵条件:红曲废渣浓度102 g/L,枯草芽孢杆菌接种量10%,摇床转速为224 r/min,预测可获得的最大活菌数为9.3 lg CFU/mL。考虑到实际条件,将验证实验的发酵条件修正为红曲废渣浓度100 g/L,枯草芽孢杆菌接种量10%,摇床转速220 r/min。在此条件下重复三次实验,枯草芽孢杆菌的活菌数为(9.3±0.3) lg CFU/mL,与理论预测值基本一致,说明回归模型可靠,模型的预测值能较好地反映发酵过程实际的活菌数。因此,对该菌株发酵条件的研究,可为其进一步放大乃至工业化生产提供理论基础。
2.3 枯草芽孢杆菌生长过程中发酵液营养物质含量的变化
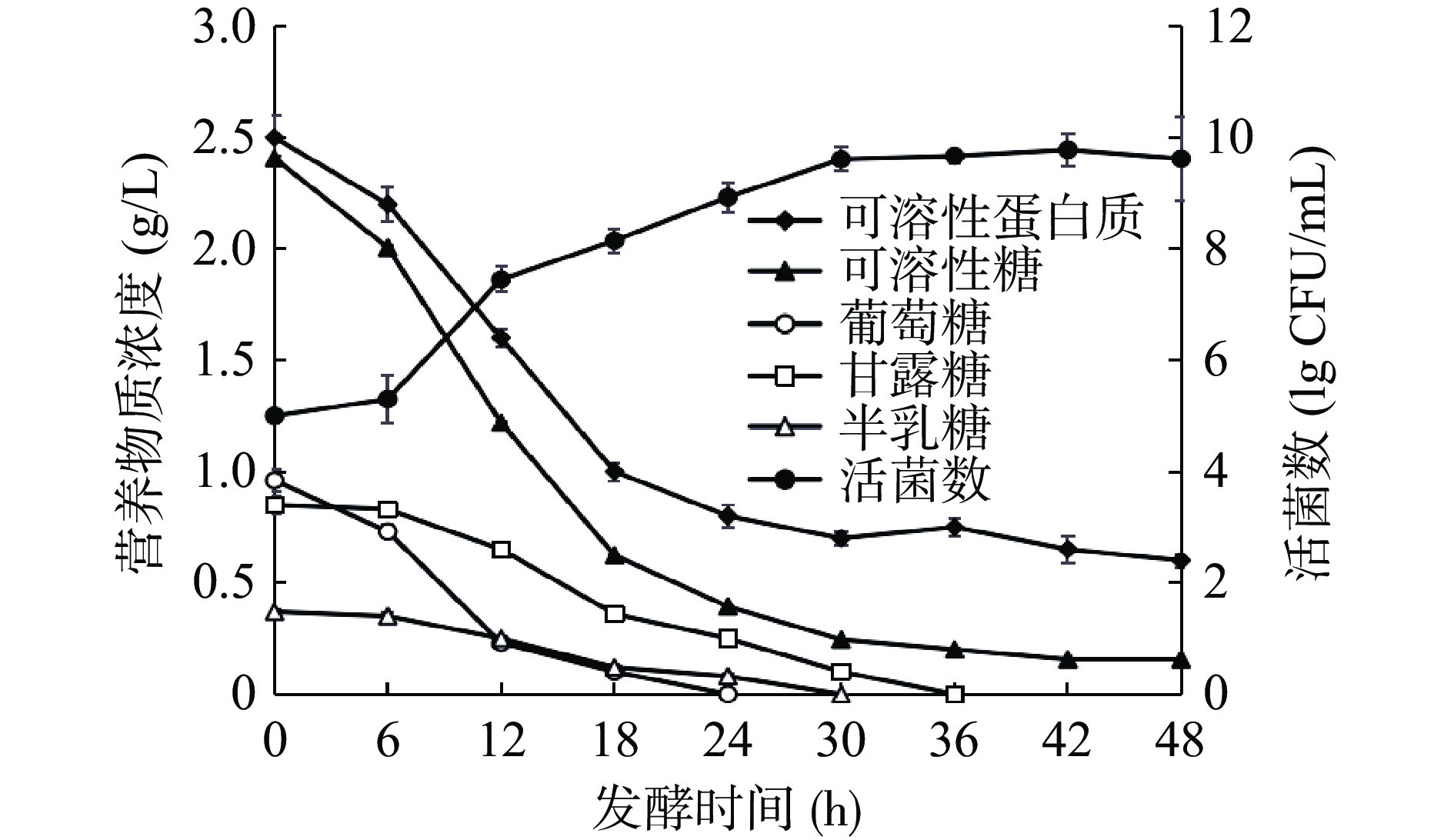
跟踪发酵液中可溶性糖、可溶性蛋白质的含量和活菌数的变化的相关性分析影响枯草芽孢杆菌生长的关键成分,结果如图3所示。在摇床转速为220 r/min,37 ℃条件下,当发酵时间为30 h时,枯草芽孢杆菌的增长进入平稳期,可溶性糖和可溶性蛋白质的含量分别从2.40和2.50 g/L降低至0.24和0.70 g/L。可溶性糖的消耗较大,推测其含量是枯草芽孢杆菌的生长的主要限制因素。为进一步分析枯草芽孢杆菌对营养物质具体单糖的利用情况,对发酵液中的单糖含量进行测定。结果表明,葡萄糖、甘露糖和半乳糖的含量与菌量的增加密切相关。从图3可看出,当葡萄糖、甘露糖和半乳糖逐步被使用完时,其生长基本停止。葡萄糖是枯草芽孢杆菌优先使用的碳源,也是其增殖的关键。在发酵时间为6 h时,葡萄糖含量从0.96 g/L降低到0.73 g/L,甘露糖和半乳糖的含量基本没有变化,此时菌量从5.0 lg CFU/mL增长到5.3 lg CFU/mL。发酵6~12 h的过程中,菌量增长了141倍,葡萄糖含量降低至0.23 g/L,而甘露糖和半乳糖的含量变化较小。可见说明葡萄糖是限制枯草芽孢杆菌的生长的主要因素,可通过额外添加葡萄的含量,进一步提高红曲废渣的利用率。
2.4 枯草芽孢杆菌微生态制剂的储藏稳定性分析
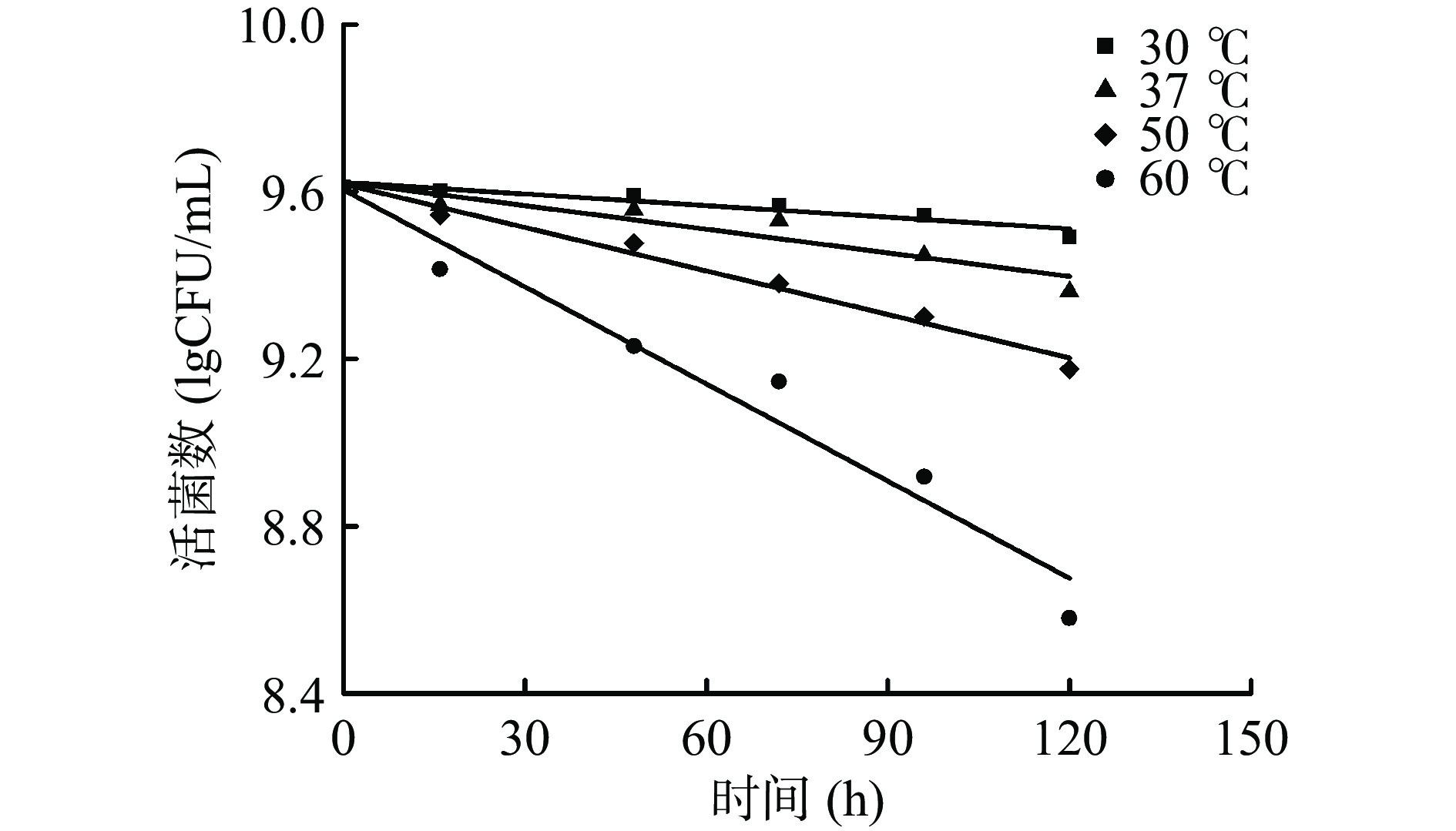
通过测定枯草芽孢杆菌微生态制剂在不同存放温度下的活菌数变化,评估其储藏稳定性,结果如图4所示。不同温度下,微生态制剂活菌数变化的拟合直线分别为:30 ℃,lgNt=−0.0009t+9.6,R2=0.88;37 ℃,lgNt=−0.0019t+9.6,R2=0.87;50 ℃,lgNt=−0.0035t+9.6,R2=0.98;60 ℃,lgNt=−0.0078t+9.6,R2=0.95。在四种不同的储藏温度条件下,枯草芽孢杆菌的活菌数均呈现下降趋势,且下降幅度与温度的增加有正相关性。初始浓度为9.6 lg CFU/mL的枯草芽孢杆菌在30、37、50和60 ℃下储藏120 h后,枯草芽孢杆菌的存活率分别为75.6%、56.1%、36.6%和8.9%。利用图4中的数据可进一步分析在其他温度下,微生态制剂的储藏稳定性。首先,通过公式(1)分别计算出不同温度下的失活常数k(k30 ℃= 0.0020(h−1)、k37 ℃=0.0044(h−1)、k50 ℃= 0.0081(h−1)、k60 ℃= 0.0180(h−1))。然后,再根据公式(2)将k与温度T作lgk-1/T图,作线性回归,可得回归方程:lgk=−2960.2/T−7.1。根据此方程可计算出在常温20 ℃条件下,微生态制剂的失活常数k20 ℃= 0.0010(h−1)。以此失活常数计算微生态制剂在20 ℃下保存三个月,微生态制剂的活菌数为8.7 lg CFU/mL,符合微生态制剂的活菌数要求[25-26]。
2.5 枯草芽孢杆菌微生态制剂的抗氧化性评估
将微生态制剂中的可溶性成分进行分离,并测定其抗氧化性,结果如图5所示。结果表明枯草芽孢杆菌微生态制剂可溶性成分的铁还原力、DPPH· 和羟自由基的清除能力均与可溶性成分的浓度呈量效关系。微生态制剂具有一定的抗氧化能力,其中DPPH自由基清除能力最强。微生态制剂可溶性成分的铁还原力为0.97 mmol/L,约为0.09维生素C当量(g/g),优于枯草芽孢杆菌N2−10(0.59 mmol/L)[27];DPPH自由基清除能力为0.25 mg/mL(IC50),约为0.08维生素C当量(g/g);羟自由基清除能力为0.69 mg/mL(IC50),约为0.23维生素C当量(g/g)(图5a~5c)。可见,通过红曲废渣制备的枯草芽孢杆菌微生态制剂具有较强的抗氧化能力。尤其是在DPPH自由基的清除能力方面,可有效减轻自由基对机体的损伤,维持机体健康。其原因一方面可能是由于红曲废渣中含有的色素、多糖、酚类等多种抗氧化成分[28],另一方面可能是枯草芽孢杆菌代谢过程中产生的抗氧化活性肽[20-21,29-30]等成分共同作用的结果。
3. 结论
以红曲废渣为原料制备枯草芽孢杆菌微生态制剂,通过单因素实验和响应面分析得到的最优的发酵条件为发酵时间48 h,红曲废渣浓度100 g/L,枯草芽孢杆菌接种量10%,摇床转速220 r/min,枯草芽孢杆菌的最大产量为(9.3±0.3)lg CFU/mL。该体系中可溶性糖是限制枯草芽孢杆菌生长的主要因素。枯草芽孢杆菌先利用葡萄糖,后利用甘露糖和半乳糖作为其生产所需的碳源。且该法获得的枯草芽孢杆菌微生态制剂稳定性较高,在常温下存放三个月后的活菌数为8.7 lg CFU/mL高于微生态制剂的应用要求。所得微生态制剂具有较强的抗氧化性,其可溶性成分的铁还原力为0.97 mmol/gL,约为0.09维生素C当量(g/g);DPPH自由基清除能力0.25 mg/mL(IC50),约为0.08维生素C当量(g/g);羟自由基清除能力为0.69 mg/mL(IC50),约为0.23维生素C当量(g/g)。本研究证明红曲废渣可作为原料制备枯草芽孢杆菌微生态制剂,为微生物发酵废渣的可持续性绿色加工提供了实践依据。
-
表 1 中心组合设计的因素水平表
Table 1 Factors and levels table of Box-Behnken Design (BBD)
水平 因素 A 红曲废渣浓度(g/L) B 接种量(%) C 摇床转速(r/min) −1 75 5 200 0 100 10 220 1 125 15 240 表 2 枯草芽孢杆菌发酵红曲废渣的响应面试验结果
Table 2 Response surface test design of Hongqu residue fermented by Bacillus subtilis
编号 A
(g/L)B
(%)C(r/min) R
(lg CFU/mL)编号 A
(g/L)B(%) C(r/min) R
(lg CFU/mL)1 100 10 220 9.3 10 125 5 220 8.6 2 125 10 200 7.8 11 125 10 240 7.8 3 100 5 240 7.4 12 100 10 220 9.3 4 75 15 220 7.2 13 75 10 200 7.2 5 100 5 200 8.2 14 100 15 200 7.1 6 100 5 220 7.0 15 100 10 220 9.3 7 100 10 220 9.3 16 125 15 220 7.4 8 100 10 220 9.3 17 75 10 240 7.7 9 100 10 240 7.5 表 3 回归方程的方差分析
Table 3 ANOVA of regression equation
差异来源 平方和 自由度 均方误差 F P 显著性 模型 13.22 9 1.47 1218.93 <0.0001 ** A 0.24 1 0.24 196.12 <0.0001 ** B 1.176−3 1 1.176−3 0.98 0.3561 C 0.14 1 0.14 117.00 <0.0001 ** AB 0.035 1 0.035 29.02 0.0010 ** AC 0.061 1 0.061 50.83 0.0002 ** BC 0.016 1 0.016 13.07 0.0086 ** A2 3.05 1 3.05 2532.88 <0.0001 ** B2 5.60 1 5.60 4644.40 <0.0001 ** C2 2.78 1 2.78 2310.40 <0.0001 ** 残差 8.435−3 7 1.205−3 失拟项 6.886−3 3 2.295−3 5.93 0.0592 纯误差 1.549−3 4 3.872−3 总和 13.23 16 注:*:P<0.05 ,表示显著;** :P<0.01 ,表示极显著。 -
[1] 陈旭峰. 红曲霉壳聚糖的制备[D]. 杭州: 浙江工业大学, 2004. CHEN X F. The preparation of chitosan by fermenting Monascus spp[D]. Hangzhou: Zhejiang University of Technology, 2004.
[2] 董晔, 杨姿, 贾梦琦, 等. 红曲废菌渣中有效成分的综合提取工艺[J]. 食品工业科技,2018,39(3):158−166. [DONG Y, YANG Z, JIA M Q, et al. The integrated extraction process of effective ingredients from Monascus mycelium[J]. Science and Technology of Food Industry,2018,39(3):158−166. DONG Y, YANG Z, JIA M Q, et al. The integrated extraction process of effective ingredients from Monascus mycelium[J]. Science and Technology of Food Industry, 2018, 39(3): 158-166.
[3] 邓毛程, 李静, 顾宗珠, 等. 红曲霉菌体蛋白复合酶解的研究[J]. 中国酿造,2011,30(12):148−151. [DENG M C, LI J, GU Z Z, et al. Enzymatic hydrolysis of cell protein of Mononscus[J]. China Brewing,2011,30(12):148−151. doi: 10.3969/j.issn.0254-5071.2011.12.042 DENG M C, LI J, GU Z Z, et al. Enzymatic hydrolysis of cell protein of Mononscus[J]. China Brewing, 2011, 30(12): 148-151. doi: 10.3969/j.issn.0254-5071.2011.12.042
[4] CHEN W P, FENG Y L, ISTVAN M, et al. Nature and nurture: Confluence of pathway determinism with metabolic and chemical serendipity diversifies Monascus azaphilone pigments[J]. Natural Product Reports,2019,36(4):561−572. doi: 10.1039/C8NP00060C
[5] 黄颖颖, 陈慎, 杨成龙, 等. 红曲色素和桔霉素代谢调控方法的研究进展[J]. 中国调味品,2018,43(2):188−194. [HUANG Y Y, CHEN S, YANG C L, et al. A review on metabolism regulation methods of pigment and citrinin in Monascus[J]. Chinese Condiment,2018,43(2):188−194. doi: 10.3969/j.issn.1000-9973.2018.02.045 HUANG Y Y, CHEN S, YANG C L, et al. A review on metabolism regulation methods of pigment and citrinin in Monascus[J]. Chinese Condiment, 2018, 43(2): 188-194. doi: 10.3969/j.issn.1000-9973.2018.02.045
[6] 戴秉扬. 红曲霉发酵优化及色素提取工艺研究[J]. 广东化工,2019,46(24):50−56. [DAI B Y. Monascus fermentation process optimization and pigment extraction[J]. Guangdong Chemical Industry,2019,46(24):50−56. DAI B Y. Monascus Fermentation process optimization and pigment extraction[J]. Guangdong Chemical Industry, 2019, 46(24): 50-56.
[7] 杨晓辉, 刘利军, 马玉龙. 红曲红色素生产中发酵废渣的综合利用[J]. 粮食与饲料工业,2007(8):30−31. [YANG X H, LIU L J, MA Y L. Comprehensive utilization of fermentation waste residue in production of Monascus red-pigment[J]. Cereal & Feed Industry,2007(8):30−31. doi: 10.3969/j.issn.1003-6202.2007.08.013 YANG X H, LIU L J, MA Y L. Comprehensive utilization of fermentation waste residue in production of Monascus red-pigment[J]. Cereal & Feed Industry, 2007 (8): 30-31. doi: 10.3969/j.issn.1003-6202.2007.08.013
[8] 邢宏博, 曾李, 许赣荣, 等. 红曲菌主要的活性物质及红曲产品在饲料行业应用前景[J]. 广东饲料,2020,29(3):28−31. [XING H B, ZENG L, XU G R, et al. Main active substances of Monascus and application prospect of Monascus products in feed industry[J]. Guangdong Feed,2020,29(3):28−31. doi: 10.3969/j.issn.1005-8613.2020.03.008 XING H B, ZENG L, XU G R, et al. Main active substances of Monascus and application prospect of Monascus products in feed industry[J]. Guangdong Feed, 2020, 29(3): 28-31. doi: 10.3969/j.issn.1005-8613.2020.03.008
[9] 周永红. 饲料原料中霉菌及霉菌毒素对饲料产品适口性的影响[J]. 饲料工业,2005,26(5):51−55. [ZHOU Y H. Effects of molds and mycotoxins in feed materials on palatability of feed products[J]. Feed Industry,2005,26(5):51−55. doi: 10.3969/j.issn.1001-991X.2005.05.015 ZHOU Y H. Effects of molds and mycotoxins in feed materials on palatability of feed products[J]. Feed Industry, 2005, 26(5): 51-55. doi: 10.3969/j.issn.1001-991X.2005.05.015
[10] 吕锋. 袋装混菌发酵全价饲料的研究[D]. 合肥: 安徽农业大学, 2010. LÜ F. The study of mixed fermentation of feed bags full price[D]. Hefei: Anhui Agricultural University, 2010.
[11] 宋立立, 张晨旭, 张连水. 枯草芽孢杆菌在发酵饲料中的应用研究进展[J]. 中国饲料,2021(9):17−21. [SONG L L, ZHANG C X, ZHANG L S. Research progress on application of Bacillus subtilis in fermented feed[J]. China Feed,2021(9):17−21. SONG L L, ZHANG C X, ZHANG L S. Research progress on application of Bacillus subtilis in fermented feed[J]. China Feed, 2021, 00(9): 17-21.
[12] MARIANA B M, JORL M D, JASONC W, et al. Effect of Bacillus subtilis C-3102 on nursing piglet fecal microflora, fecal consistency and growth performance[J]. Journal of Animal Science,2018,96:112−113.
[13] LAN R X, KIM I H. Effects of Bacillus licheniformis and Bacillus subtilis complex on growth performance and faecal noxious gas emissions in growing-finishing pigs[J]. Journal of The Science of Food and Agriculture,2019,99(4):1554−1560. doi: 10.1002/jsfa.9333
[14] ZAINELDIN A I, HEGAZI S, KOSHIO S, et al. Bacillus subtilisas probiotic candidate for red sea bream: Growth performance, oxidative status, and immune response traits[J]. Fish and Shellfish Immunology,2018,79:303−312. doi: 10.1016/j.fsi.2018.05.035
[15] JEONG J S, KIM I H. Effect of Bacillus subtilis C-3102 spores as a probiotic feed supplement on growth performance, noxious gas emission, and intestinal microflora in broilers[J]. Poultry Science,2014,93(12):3097−3103. doi: 10.3382/ps.2014-04086
[16] 杜晓雨, 赵恺, 赵志敏, 等. 枯草芽孢杆菌微生态制剂发酵研究进展[J]. 微生物学通报,2020,47(3):903−914. [DU X Y, ZHAO K, ZHAO Z M, et al. Progress on Bacillus subtilis microbial ecological agents by fermentation[J]. Microbiology China,2020,47(3):903−914. DU X Y, ZHAO K, ZHAO Z M, et al. Progress on Bacillus subtilis microbial ecological agents by fermentation[J]. Microbiology China, 2020, 47(3): 903-914.
[17] DI J, CHU Z P, ZHANG S H, et al. Evaluation of the potential probiotic Bacillus subtilis isolated from two ancient sturgeons on growth performance, serum immunity and disease resistance of Acipenser dabryanus[J]. Fish and Shellfish Immunology,2019,93:711−719. doi: 10.1016/j.fsi.2019.08.020
[18] LECLERE V, BECHET M, ADAM A, et al. Mycosubtilin overproduction by Bacillus subtilis BBG100 enhances the organism’s antagonistic and biocontrol activities[J]. Applied and Environmental Microbiology,2005,71(8):4577−4584. doi: 10.1128/AEM.71.8.4577-4584.2005
[19] MIN Y N, YANG H L, XU Y X, et al. Effects of dietary supplementation of synbiotics on growth performance, intestinal morphology, sIgA content and antioxidant capacities of broilers[J]. Journal of Animal Physiology and Animal Nutrition,2016,100(6):1073−1080. doi: 10.1111/jpn.12479
[20] 江敏, 胡小军, 王标诗, 等. 发酵法制备马氏珠母贝抗氧化多肽工艺及清除自由基的研究[J]. 食品与发酵科技,2017,53(4):32−38. [JIANG M, HU X J, WANG B S, et al. Fermentation technology and free radical scavenging of pinctada martensii antioxidant polypeptides[J]. Food and Fermentation Sciences & Technology,2017,53(4):32−38. JIANG M, HU X J, WANG B S, et al. Fermentation technology and free radical scavenging of pinctada martensii antioxidant polypeptides[J]. Food and Fermentation Sciences & Technology, 2017, 53(4): 32-38.
[21] 郭利娜, 朱玉, 刁明明, 等. 枯草芽孢杆菌发酵小米糠对其抗氧化肽含量与抗氧化活性的影响[J]. 食品科学,2015,36(13):196−201. [GUO L N, ZHU Y, DIAO M M, et al. Effect of fermentation by Bacillus subtilis on antioxidant peptide content and antioxidant activity of millet bran[J]. Food Science,2015,36(13):196−201. doi: 10.7506/spkx1002-6630-201513036 GUO L N, ZHU Y, DIAO M M, et al. Effect of fermentation by Bacillus subtilis on antioxidant peptide content and antioxidant activity of millet bran[J]. Food Science, 2015, 36(13): 196-201. doi: 10.7506/spkx1002-6630-201513036
[22] ZHANG Y W, LIU J, LU X, et al. Isolation and identification of an antioxidant peptide prepared from fermented peanut meal using Bacillus subtilis fermentation[J]. International Journal of Food Properties,2014,17(6):1237−1253. doi: 10.1080/10942912.2012.675605
[23] 朱征宇, 汪恩浩, 王媛. 应用统计分析和化学动力学参数评价生物制品的稳定性[J]. 中国生物制品学杂志,2008,21(2):126−130. [ZHU Z Y, WANG E H, WANG Y. Evaluation of stability of biologics by statistic analysis and chemical kinetic parameters[J]. Chinese Journal of Biologicals,2008,21(2):126−130. doi: 10.3969/j.issn.1004-5503.2008.02.012 ZHU Z Y, WANG E H, WANG Y. Evaluation of stability of biologics by statistic analysis and chemical kinetic parameters[J]. Chinese Journal of Biologicals, 2008, 21(2): 126-130. doi: 10.3969/j.issn.1004-5503.2008.02.012
[24] 黄梦姣. 茶渣深加工综合利用及咀嚼片的工艺研究[D]. 西安: 陕西科技大学, 2018. HUANG M J. Comprehensive utilization of tea residue deep processing and process research of chewable tablets[D]. Xi'an: Shaanxi University of Science & Technology, 2018.
[25] 梁红雁, 蒲万霞, 吴润, 等. 活菌制剂的质量控制指标及其研究现状[J]. 黑龙江畜牧兽医,2015(13):79−81. [LIANG H Y, PU W X, WU R, et al. Quality control index of live bacteria preparation and its research status[J]. Heilongjiang Animal Science and Veterinary Medicine,2015(13):79−81. LIANG H Y, PU W X, WU R, et al. Quality control index of live bacteria preparation and its research status[J]. Heilongjiang Animal Science and Veterinary Medicine, 2015, 00(13): 79-81.
[26] 张日俊. 微生态制剂的质量鉴别与选择、检测指标和标准[J]. 饲料工业,2010,31(20):1−4. [ZHANG R J. Quality identification, selection, detection index and standard of microecologics[J]. Feed Industry,2010,31(20):1−4. doi: 10.3969/j.issn.1001-991X.2010.20.001 ZHANG R J. Quality identification, selection, detection index and standard of microecologics[J]. Feed Industry, 2010, 31(20): 1-4. doi: 10.3969/j.issn.1001-991X.2010.20.001
[27] 张亚茹, 张伟涛, 王硕, 等. 枯草芽孢杆菌N-2-10体外益生特性评价[J]. 饲料工业,2020,41(24):12−17. [ZHANG Y R, ZHANG W S, WANG S, et al. Evaluation of in vitro probiotic properties of Bacillus subtilis N2-10[J]. Feed Industry,2020,41(24):12−17. ZHANG Y R, ZHANG W S, Wang S, et al. Evaluation of in vitro probiotic properties of Bacillus subtilis N2-10[J]. Feed Industry, 2020, 41(24): 12-17.
[28] 李燚. 红曲霉废弃物成分分析及应用的研究[D]. 天津: 天津科技大学, 2009. LI Y. The study on the determation of ingredients and the application of Monascus residue[D]. Tianjin: Tianjin University of Science and Technology, 2009.
[29] 陈敏. 虎斑乌贼生殖腺多肽的制备、纯化及其抗氧化活性的研究[D]. 广州: 华南理工大学, 2019. CHEN M. Study on the preparation, purification and antioxidant activity of peptides from cuttlefish (Sepia pharaonis) [D]. Guangzhou: South China University of Technology, 2019.
[30] 李艳艳, 张剑. 表面活性肽的研究进展[J]. 化学通报,2017,80(10):918−924. [LI Y Y, ZHANG J. Research progress in surfactin[J]. Chemistry,2017,80(10):918−924. LI Y Y, ZHANG J. Research progress in surfactin[J]. Chemistry, 2017, 80(10): 918-924.
-
期刊类型引用(2)
1. 顾丹丹,董雪,张金秀,王晓茹,赵宗硕,王立安. 小麦羊肚菌菌粮制备工艺优化及营养成分、理化性质和抗氧化活性分析. 食品工业科技. 2025(04): 237-245 .  本站查看
本站查看
2. 马莉,季爱兵,曾胤,严亮. 蘑菇多糖生物活性及提取研究进展. 热带农业科学. 2024(06): 123-130 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:






 下载:
下载:
