Analysis of Chemical Composition and Antioxidant Activities of Water-insoluble and Water-soluble Polysaccharides from Euglena gracilis
-
摘要: 目的:研究比较裸藻非水溶性和水溶性多糖抗氧化活性,并分析其主要结构特征,为后续研究裸藻多糖的结构与活性关系提供实验基础。方法:以裸藻为原料,提取裸藻中的非水溶性和水溶性多糖,经分离纯化后,采用紫外-可见吸收光谱、红外光谱、凝胶色谱、离子色谱等技术对多糖的基本结构进行分析;进一步以维生素C(VC)为对照,考察它们对DPPH和OH自由基的清除能力及还原能力。结果:裸藻非水溶性多糖(EGP-1)、裸藻水溶性多糖(EGP-2A-1和EGP-2B-1)的相对分子质量分别为1.01×104、2.91×106和1.70×106 Da。EGP-1是一种含有β-糖苷键和吡喃葡萄糖环的多糖,EGP-2A-1和EGP-2B-1是含有α-和β-糖苷键的吡喃葡萄糖环形式的多糖。EGP-1主要单糖为葡萄糖、甘露糖、岩藻糖和鼠李糖;EGP-2A-1和EGP-2B-1均由岩藻糖、鼠李糖、阿拉伯糖、盐酸氨基葡萄糖、半乳糖、葡萄糖、木糖、甘露糖和葡萄糖醛酸组成。体外抗氧化活性结果显示,3种组分多糖均具有抗氧化活性,其抗氧化能力为VC>EGP-2A-1>EGP-2B-1>EGP-1。结论:从裸藻中分离得到的多糖均具有抗氧化能力,且水溶性多糖的抗氧化活性强于非水溶性多糖,其中EGP-2A-1组分活性最佳。Abstract: Objective: The antioxidant activities and main structural characteristics of water-insoluble and water-soluble polysaccharides of Euglena gracilis were comparatively studied, which provided an experimental basis for the subsequent research of the structure-activity relationship of E. gracilis polysaccharides. Methods: The water-insoluble and water-soluble polysaccharides were extracted, separated and purified from E. gracilis. The basic structure of the polysaccharides was analyzed by UV, IR, HPGPC and IC techniques. The antioxidant activities of these polysaccharides were further investigated by measuring scavenging activities against 1,1-Diphenyl-2-picrylhydrazyl free radical (DPPH·) and hydroxyl radical (·OH), and reducing ability, compared with vitamin C (VC). Results: The molecular weights of E. gracilis water-insoluble polysaccharides (EGP-1) and E. gracilis water-soluble polysaccharides (EGP-2A-1 and EGP-2B-1) were 1.01×104, 2.91×106 and 1.70×106 Da, respectively. EGP-1 was a glucopyranose cyclic polysaccharide connected by β-glycosidic bonds, and EGP-2A-1 and EGP-2B-1 were glucopyranose cyclic polysaccharides containing α- and β-glycosidic bonds. The main monosaccharides found in EGP-1 were glucose, mannose, fucose and rhamnose; EGP-2A-1 and EGP-2B-1 were composed of fucose, rhamnose, arabinose, glucosamine, hydrochloride galactose, glucose, xylose, mannose and glucuronic acid. The results of antioxidant activities showed that three-component polysaccharides had antioxidant activity, the order of their antioxidant capacities was VC>EGP-2A-1>EGP-2B-1>EGP-1. Conclusions: Both the water-insoluble and water-soluble polysaccharides isolated from E. gracilis had antioxidant capacity, and the antioxidant activity of water-soluble polysaccharides was stronger than that of water-insoluble polysaccharides, and the EGP-2A-1 was the best.
-
Keywords:
- Euglena gracilis /
- polysaccharides /
- extraction /
- structure /
- antioxidant activity
-
裸藻是体长约50 μm的微藻类生物,它可以边进行光合作用边运动[1]。裸藻含有丰富的维生素、矿物质、氨基酸、不饱和脂肪酸、叶绿素、DHA、EPA等,共59种营养素,其营养价值超越其他所有藻类,完胜冬虫夏草、灵芝等生物,它可以全面的补充人体所需的营养[2]。裸藻作为一种新食品原料,在日本已成为一种必需的营养添加剂,广泛地应用于健康食品、保健品和天然调味料中[3-4]。近年来,裸藻因其具有丰富的营养物质及其生物活性代谢物而被广泛研究。
海藻中富含各种高分子多糖,这些多糖可分为非水溶性和水溶性两类[5]。先前的研究发现,藻类中水溶性多糖的结构新颖,活性多样,如抗癌、抗凝血、抗氧化、抗肿瘤和增强免疫等[6]。并且由于来源和结构(单糖组成、糖苷键和分子量等)的不同,藻类多糖的生物活性也有很大差异[7]。除裸藻外,其他藻类非水溶性多糖研究较少,裸藻副淀粉(非水溶性多糖)是裸藻体内特有的储存多糖,它是具有特定类型的β-1-3-葡聚糖,多项实验发现其具有调节免疫治疗痛风、降低胆固醇、调节血糖和抗氧化等作用[8]。裸藻副淀粉具有显著的细胞因子相关免疫增强和免疫刺激作用,可以作为一种安全有效的辅助调节免疫系统反应的天然因子[8]。此外,当加入到饮食中时,它具有降低胆固醇的作用,并参与调节人类餐后血糖和胰岛素的反应[9]。由于具有抗氧化特性,裸藻副淀粉可抑制四氯化碳引起的小鼠肝损伤,并防止特应性皮炎样病变的发展[9],它在健康和医疗方面具有巨大的生物技术潜力。但是目前对裸藻中多糖的研究多集中在非水溶性多糖(副淀粉)上,而对于裸藻水溶性多糖结构和活性的研究鲜有报道。研究表明,裸藻水提物的总抗氧化能力远超于裸藻、裸藻副淀粉和碱溶的裸藻副淀粉,裸藻的水提物具有强抗氧化性作用,但该作用是否与裸藻水溶性多糖有关尚未可知[10]。
本文以裸藻为研究对象,对其分离纯化后的非水溶性和水溶性多糖组分的官能团、分子量、单糖组成等基本结构进行研究,进而对其抗氧化活性比较分析,以期为进一步研究裸藻多糖构效关系提供实验基础,同时也为裸藻多糖的开发利用提供理论依据。
1. 材料与方法
1.1 材料与仪器
裸藻(藻粉) 上海光语生物科技有限公司;DEAE-52纤维素、Sephadex G-100凝胶、透析袋 北京索莱宝科技有限公司;中性蛋白酶 上海源叶生物科技有限公司;十二烷基硫酸钠(SDS) 上海麦克林生化科技有限公司;1,1-二苯基-2-三硝基苯肼(DPPH) 上海阿拉丁生化科技股份有限公司;不同分子量的葡萄糖标准品(纯度>98%) Sigma公司;无水乙醇、丙酮、乙醚、浓硫酸、H2O2 西陇科学股份有限公司;苯酚、水杨酸、硫酸亚铁、氯化钠等试剂 国药集团化学试剂有限公司。
Infinite M200 Pro酶标仪 瑞士帝肯公司;TU-1950紫外可见光分光光度计 北京普析通用仪器有限责任公司;UGC-24M氮吹仪 力辰科技公司;Nicolet iS50傅里叶红外光谱仪 Thermo Scientific;LC-10A高效液相色谱仪 Shimadzu公司;RI-10A示差检测器 Shimadzu;ICS5000离子色谱仪 ThermoFisher公司。
1.2 实验方法
1.2.1 裸藻多糖的制备
1.2.1.1 裸藻非水溶性多糖的提取
参考鞠海军[11]的方法,称取100 g裸藻粉末,悬浮于2 L的SDS溶液(8.5 g/L)中,超声辅助提取18.5 min(60 ℃,45 kHz,200 W),离心(4000 r/min,5 min)取沉淀,并往沉淀中加入3 L SDS溶液(1 g/L),置于95 ℃水浴1 h,离心弃上清,依次用水、丙酮、乙醚反复洗涤沉淀除去蛋白等杂质,离心取沉淀后,冷冻干燥得裸藻非水溶性多糖EGP-1。
1.2.1.2 裸藻水溶性多糖的提取
参考葛智超等[12]的方法并稍加修改,称取100 g裸藻藻粉,溶于4 L去离子水中,调节pH至7.5~7.9;超声辅助提取2 h(60 ℃,45 kHz,200 W),离心(5000 r/min,10 min)取上清液;旋蒸浓缩后,加入4倍体积无水乙醇;随后置于4 °C层析柜中,醇沉过夜;再离心(5000 r/min,10 min)取沉淀于50 ℃烘箱烘干(12 h),粉碎称重;将粉碎物溶于去离子水,至完全溶解并调节pH至7.0~8.0后,加入11.2%粗多糖重量的中性蛋白酶(100 U/mg)50 ℃水浴1 h,100 ℃沸水煮10 min;离心(5000 r/min,10 min)取上清,浓缩;最后用8~14 kDa分子量(MW)透析袋处理浓缩液2 d;浓缩冻干得裸藻水溶性粗多糖EGP-2。
1.2.2 多糖和蛋白含量的测定
采用苯酚-硫酸法对各组分多糖含量进行测定[11]。取1 mL样品(标准品),依次加入1 mL 5%苯酚和5 mL浓硫酸,于490 nm处测其吸光度。以D-无水葡萄糖标准溶液(0、10、20、50、80、100 mg/mL)建立标准曲线,回归方程为y=0.006x+0.05413,R2=0.99,根据其计算样品中多糖的含量。
采用考马斯亮蓝试剂盒对各组分中的蛋白含量进行测定。以牛血清蛋白(BSA)标准溶液建立标准曲线,回归方程为y=0.0052x+0.0391,R2=0.99,根据其计算样品中蛋白的含量。
1.2.3 裸藻水溶性多糖的分离纯化
1.2.3.1 离子层析柱分离纯化
采用DEAE-52纤维素柱对裸藻水溶性多糖进行分离纯化[13]。将制备的裸藻水溶性粗多糖,过0.45 μm滤膜后上样,以0、0.1、0.3、0.5、0.7 mol/L的NaCl溶液为洗脱液。用苯酚-硫酸法测多糖含量,收集单一组分的多糖溶液,用1000 Da透析袋在DI水的条件下透析48 h除去NaCl,旋蒸浓缩后冻干。
1.2.3.2 凝胶层析柱分离纯化
采用Sephadex G-100凝胶柱对DEAE-52过柱后得到的馏分进一步分离纯化[14]。样品以10 mg/mL的浓度,上样2 mL,以DI水为洗脱液,苯酚-硫酸法对多糖含量测定,收集单一组分多糖溶液,浓缩冻干得多糖组分,-20 ℃保存备用。
1.2.4 纯度鉴定
采用紫外-可见光吸收光谱扫描分析多糖组分纯度[11]。将裸藻水溶性多糖和非水溶性多糖分别溶解于DI水和0.50 mol/L NaOH溶液中配制成0.5 mg/mL的多糖溶液,再分别以DI水和0.50 mol/L NaOH为空白对照,在200~400 nm波长范围进行扫描。
1.2.5 结构鉴定
1.2.5.1 分子量测定
采用高效凝胶渗透色谱法(HPGPC)进行测定[15]。精密称取样品和标准品(标准品的分子量为5000、11600、23800、48600、80900、148000、273000、409800、667800、3693000 Da),分别采用DMSO溶液/0.05 mol/L NaCl溶液配制成5 mg/mL溶液,12000 r/min离心10 min,上清液用有机微孔滤膜(0.22 μm)过滤,然后将样品转置于1.8 mL进样小瓶中。
非水溶性多糖色谱方法:色谱柱:BRT806色谱柱(8 mm×300 mm);流动相:DMSO溶液;流速:0.6 mL/min,柱温:60 ℃;进样量:50 μL;检测器:示差检测器RI-10A。
水溶性多糖色谱方法:色谱柱:BRT105-104-102串联凝胶柱(8 mm×300 mm);流动相:0.05 mol/L NaCl溶液;流速:0.6 mL/min,柱温:40 ℃;进样量:20 μL;检测器:示差检测器RI-10A。
1.2.5.2 红外光谱
采集背景数据去除干扰后,在4000~650 cm−1区域扫描样品,对主要峰(强度和波数)进行识别和分析[13]。
1.2.5.3 单糖组成
通过对比样品与单糖标准品的出峰时间来确定组分的单糖组成[16]。精密称量样品10 mg,加入3 mol/L三氟乙酸10 mL,120 ℃水解3 h。准确吸取酸水解溶液转移至管中氮吹吹干,加入5 mL水涡旋混匀,取100 μL加入900 μL DI水,离心(12000 r/min,5 min)取上清液,进离子色谱仪分析。
色谱柱:DionexCarbopacTMPA20 (3 mm×150 mm);流动相:A:H2O,B:15 mmol/L NaOH,C:15 mmol/L NaOH &100 mmol/L NaOAC(3:20);流速:0.3 mL/min;进样量:5 µL;柱温:30 ℃;检测器:电化学检测器。
1.2.6 抗氧化活性分析
1.2.6.1 DPPH自由基清除能力
参考栗晓庆等[17]的方法,测定样品对DPPH自由基的清除能力。分别称取EGP-1、EGP-2A-1和EGP-2B-1和VC溶于水或DMSO中配制成样品溶液。量取样品和DPPH-乙醇溶液(0.2 mmol/L)各100 μL,充分混匀静置反应30 min,于517 nm处测定其吸光度。同时对照组用无水乙醇代替DPPH-乙醇溶液,空白组用水或DMSO替代样品溶液。按下列公式计算:
清除率(%)=(1−A样品−A对照A空白)×100 1.2.6.2 羟自由基清除能力
参考宋佳敏等[18]的方法,通过水杨酸法进行测定。按1.2.6.1方法制备EGP-1、EGP-2A-1和EGP-2B-1和VC的不同系列样品溶液。取0.5 mL样品溶液,依次加入FeSO4(6 mmol/L)和H2O2溶液(6 mmol/L)各0.5 mL,室温反应10 min,再加入6 mmol/L的水杨酸-乙醇溶液0.5 mL,摇匀,37 ℃反应30 min后,于510 nm处测定吸光度,对照组用水代替H2O2溶液,空白组用水代替样品。按下列公式计算清除率:
清除率(%)=(1−A样品−A对照A空白)×100 1.2.6.3 还原能力
参考董扬等[19]的方法,采用铁氰化钾法进行测定。按1.2.6.1方法制备EGP-1、EGP-2A-1和EGP-2B-1和VC的不同系列样品溶液。取样品溶液、1%铁氰化钾溶液和磷酸缓冲液(pH6.6)各1.0 mL,混匀后在50 ℃反应20 min,加入10%三氯乙酸2.0 mL,3000 r/min离心10 min,取上清液和水各2.0 mL、0.3%三氯化铁0.4 mL,50 ℃反应10 min,测定700 nm波长处的吸光度。对照组以水代替三氯化铁溶液。按下列公式计算还原力:
还原力=A样品−A对照 1.3 数据处理
所有试验在相同条件下重复测定3次,结果都以均值±标准差的方式表示。采用SPSS 25和Origin 2019软件进行作图和数据处理分析。
2. 结果与分析
2.1 裸藻各组分多糖和蛋白的含量
通过苯酚-硫酸法测得裸藻粗多糖中非水溶性多糖和水溶性多糖含量分别为93.89±2.36%和69.62±0.60%。
通过考马斯亮蓝法测得从裸藻中提取得到的非水溶性多糖和水溶性多糖每100 μg中的蛋白含量分别为0.10 μg和5.62 μg。
2.2 水溶性多糖分离纯化的结果
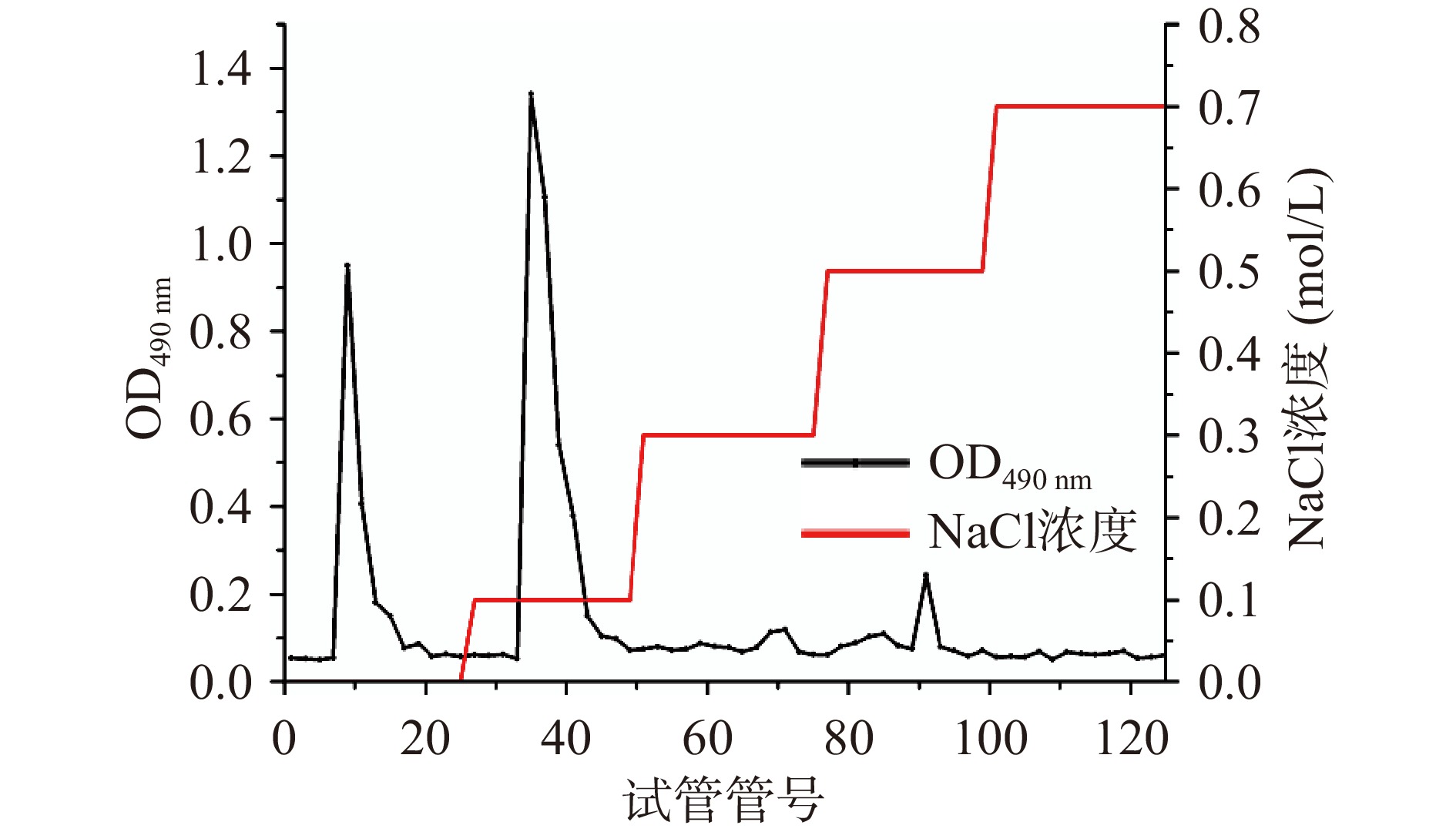
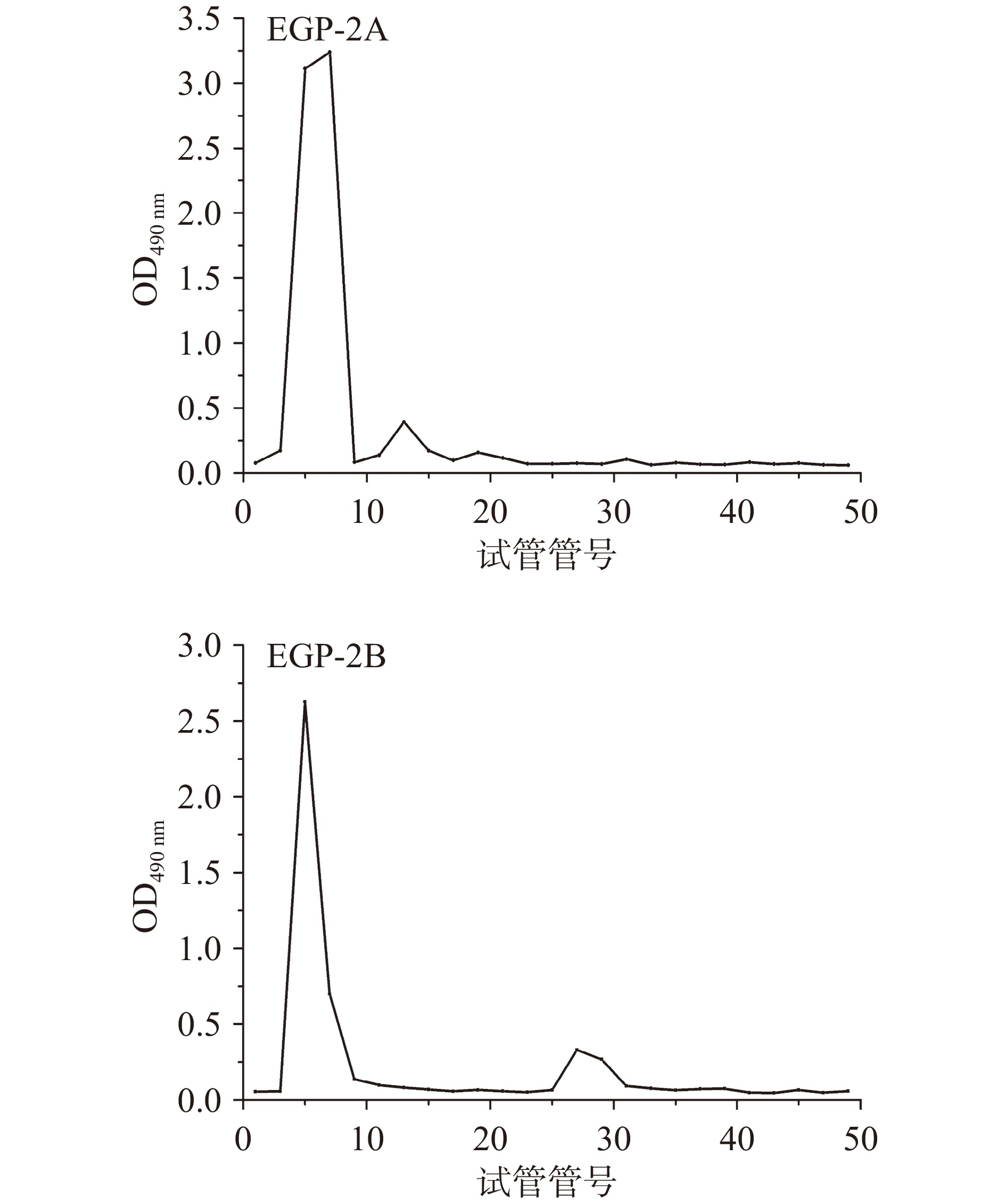
图1为EGP-2在DEAE-52层析柱上的洗脱曲线图。以0、0.1、0.3、0.5和0.7 mol/L的NaCl溶液梯度洗脱,得到2个主要洗脱组分(EGP-2A和EGP-2B),其他组分的含量较低,很难进行后续的实验。所以仅对DEAE-52柱层析分离得到的2个主要组分收集后进行透析并冷冻干燥备用,进一步采用Sephadex G-100继续分离纯化。EGP-2A和EGP-2B组分经Sephadex G-100凝胶层析柱洗脱得到两个主要的洗脱峰,如图2所示,收集两个主要组分,透析后将其命名为EGP-2A-1和EGP-2B-1。
2.3 多糖组分纯度鉴定
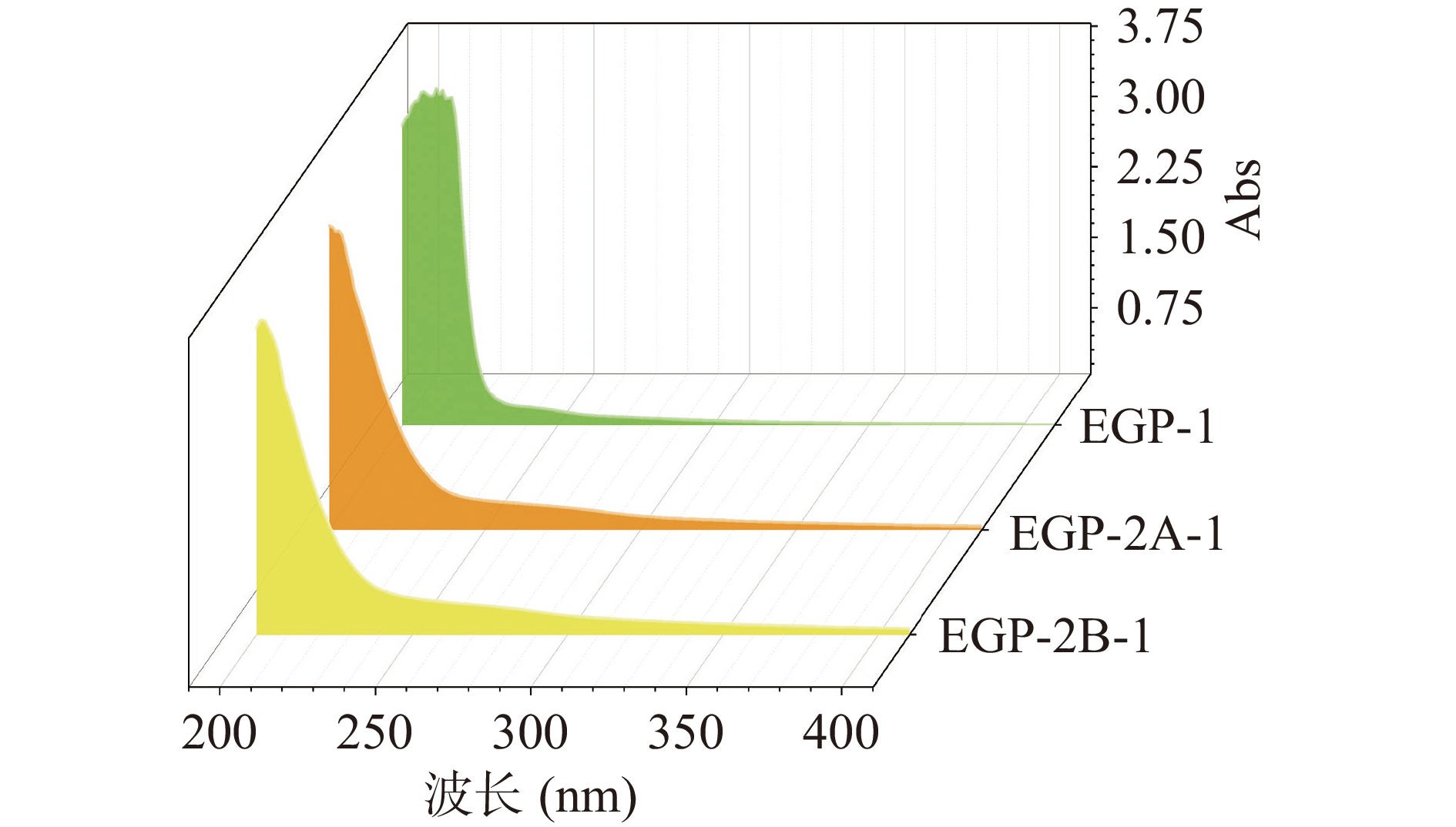
紫外可见分光光度法可于260和280 nm处定性测量核酸及蛋白质[20]。如图3所示,糖及其复合物于200 nm处拥有非常强的吸收峰,样品溶液符合多糖的紫外吸收特征,并且扫描结果显示在260和280 nm处的核酸和蛋白质吸收峰平坦,表明样品中均不含或含极少量蛋白质、核酸,具有较髙的纯度。
2.4 结构鉴定
2.4.1 分子量测定
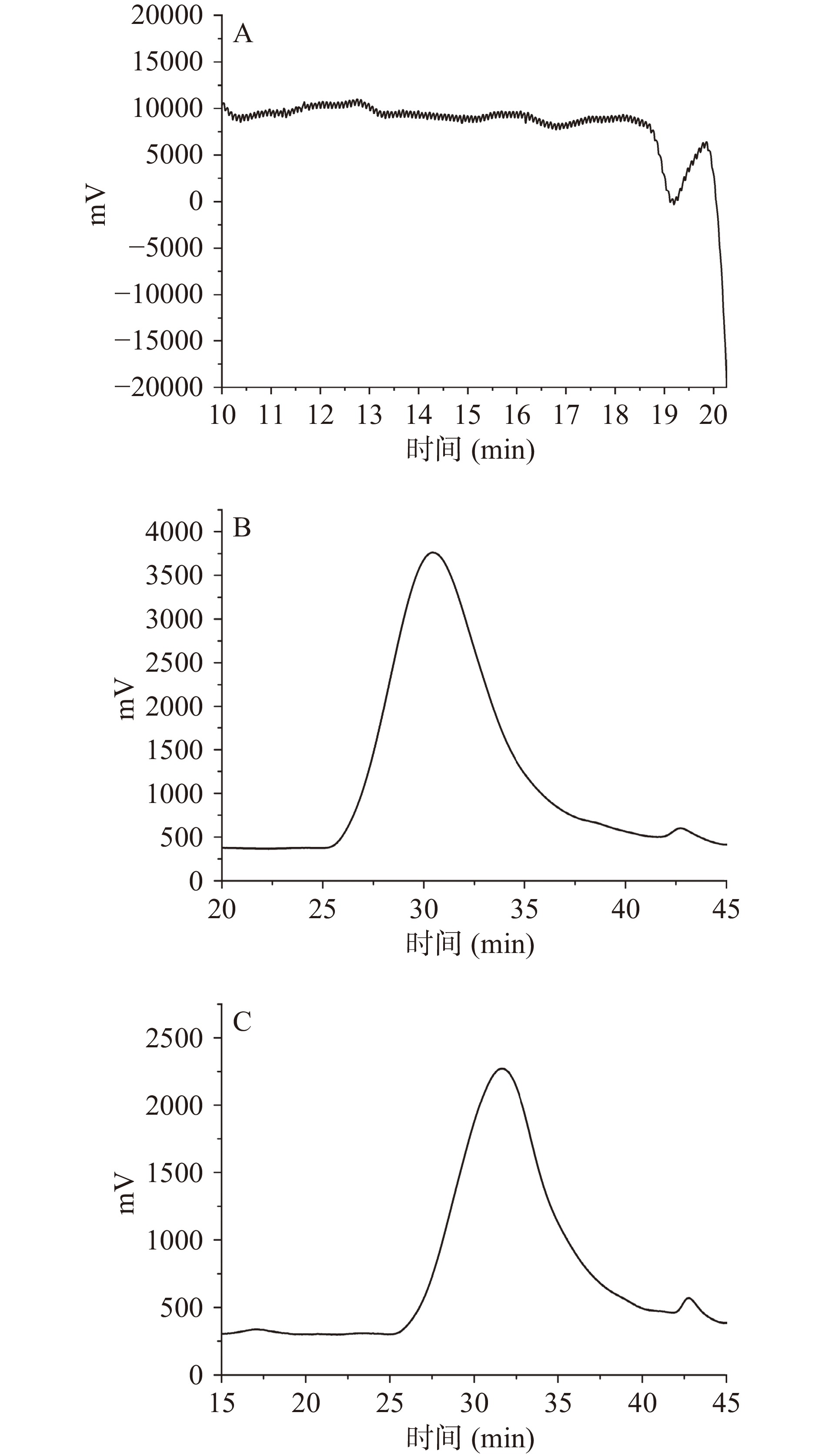
采用高效凝胶渗透色谱法测定EGP-1、EGP-2A-1和EGP-2B-1的分子量。如图4所示,三个组分的HPGPC图谱为单一对称峰,平均分子量分别为1.01×104、2.91×106和1.70×106 Da。多糖来源和制备方法的不同会导致单糖组成和分子量的较大差异,从而影响其生物功能活性[7]。同一来源的多糖由于其分子量的不同,往往具有不同的功能活性,较高分子量的多糖具有更为复杂的结构,其表现出的生物活性也更为广泛,分子量过低,难以形成具有活性的聚合结构[21]。因此,分子量较高的EGP-2A-1和EGP-2B-1可能在某些方面具有优势。
2.4.2 红外光谱
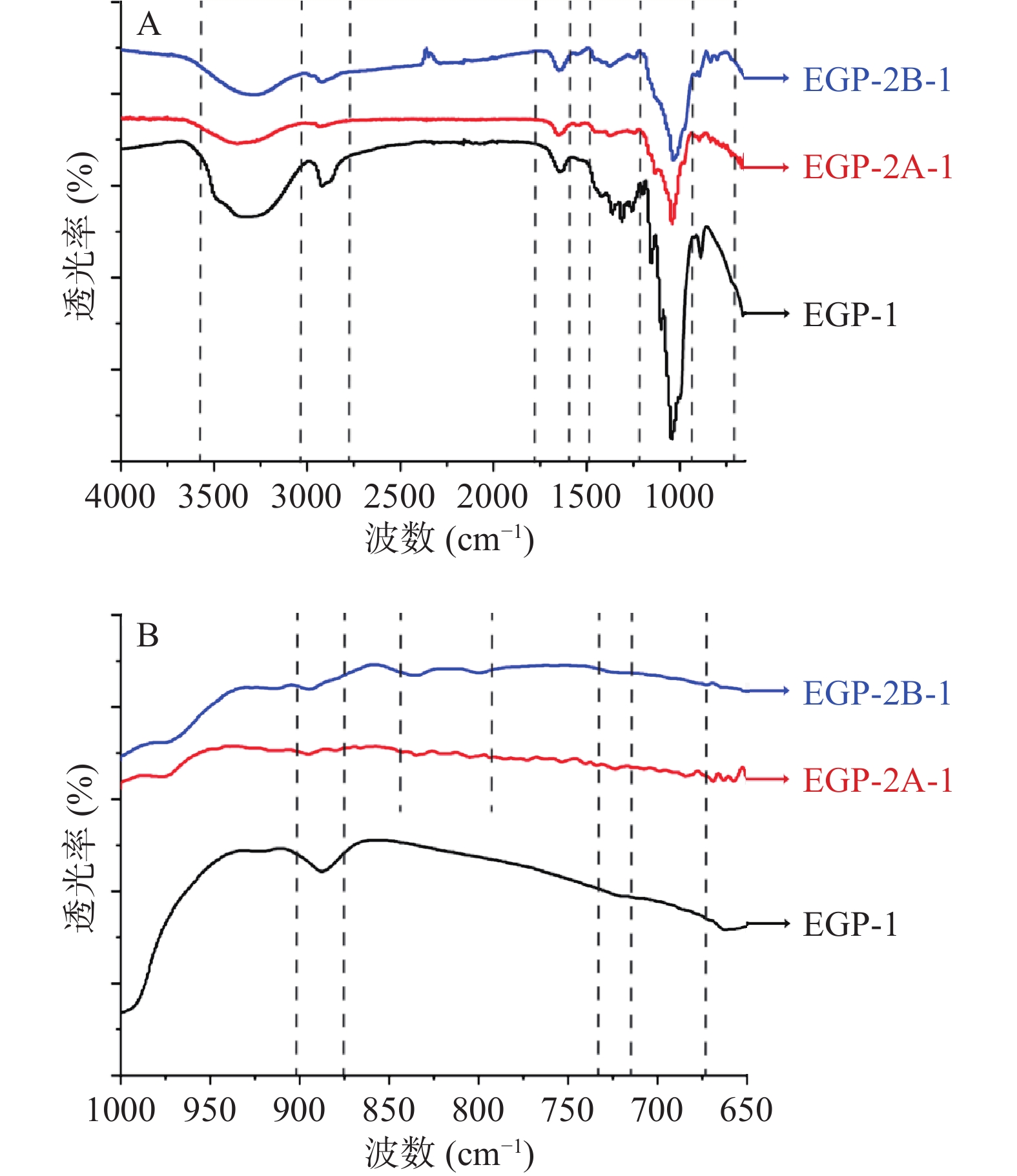
EGP-1、EGP-2A-1和EGP-2B-1的红外谱图如图5所示。结果显示,三种组分在3400和2930 cm−1附近具有O-H和C-H伸缩振动峰,符合糖类的一般结构特征[22-23];1650 cm−1附近的吸收峰反映了C=O的非对称振动,可能存在糖醛酸[24];1380 cm−1附近的吸收峰被认为是CH3−的对称变角振动引起的伸缩带[25];1250 cm−1处是吡喃糖环上的C-O-H和C-O-C的C-O伸缩振动引起的吸收峰,在1000~1200 cm−1附近是吡喃糖环的C-O-C和C-O-H的单键吸收峰[26];890 cm−1处是β-D-吡喃葡萄糖特征峰[27];834 cm−1附近的特征峰说明多糖含有α-吡喃糖苷键[28];803 cm−1处的吸收峰可能是样品含有吡喃甘露糖残基[29](表1)。以上结果表明,EGP-1是一种含有β-糖苷键和吡喃葡萄糖环的多糖,EGP-2A-1和EGP-2B-1是含有α-和β-糖苷键并具有吡喃糖环的多糖。
表 1 裸藻多糖傅里叶红外光谱数据Table 1. Fourier infrared spectroscopy data of Euglena gracilis polysaccharide吸收波数(cm−1) 振动方式或官能团 参考文献 EGP-1 EGP-2A-1 EGP-2B-1 3386.51 3384.35 3344.70 -OH伸缩振动 [22] 2925.11 2931.63 2925.86 糖类C-H不对称伸缩振动 [22] 1648.17 1651.61 1647.26 C=O在COO-中的不对称振动 [23] 1360.85 1380.51 1378.79 CH3-的对称变角振动 [24] 1259.61 1245.54 1244.02 吡喃糖环上的C-O-H和C-O-C的C-O伸缩振动 [25] 1049.96 1041.32 1040.91 吡喃糖环上的C-O-C和C-O-H单键 [26] 889.59 894.17 894.17 β-D-吡喃葡萄糖 [27] 834.80 836.09 α-D-吡喃糖苷振动 [28] 805.91 802.99 吡喃甘露糖 [29] 2.4.3 单糖组成
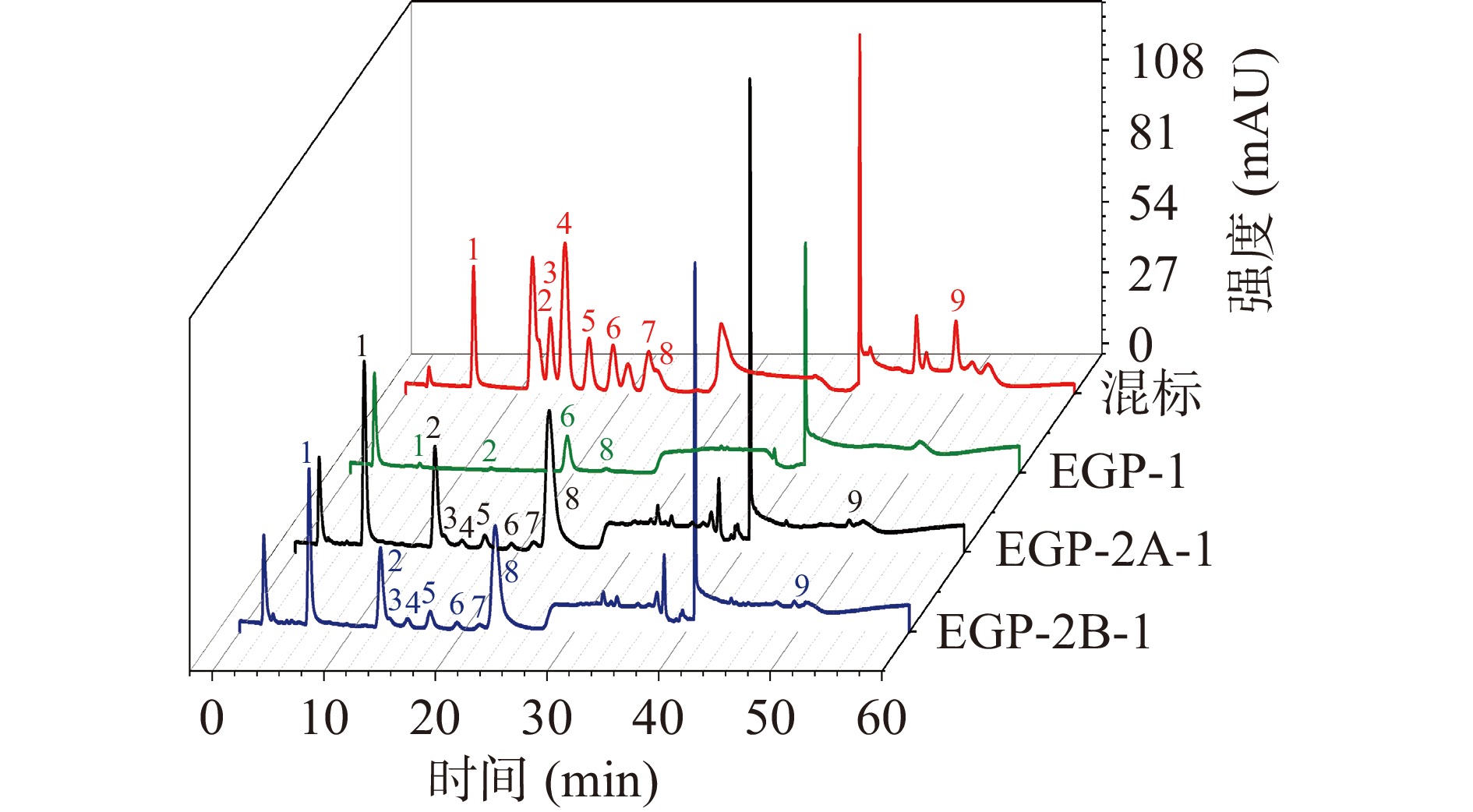
图6为混合单糖标品与EGP-1、EGP-2A-1和EGP-2B-1的离子色谱图。在三个样品中,EGP-1中鉴定出葡萄糖、甘露糖、岩藻糖和鼠李糖四种主要单糖,其摩尔比为0.873:0.066:0.030:0.030,其中葡萄糖摩尔含量最高。在鞠海军[11]的研究中,裸藻中分离出的非水溶性多糖的主要是β-葡聚糖,单糖主要为葡萄糖,与本文的结果一致。然而,与EGP-1相比,EGP-2A-1和EGP-2B-1组分含有至少9种单糖,并且二者的单糖组成类型相同,均为岩藻糖、鼠李糖、阿拉伯糖、盐酸氨基葡萄糖、半乳糖、葡萄糖、木糖、甘露糖和葡萄糖醛酸,只是摩尔比例略有差异,比分别为0.150:0.208:0.014:0.002:0.015:0.007:0.010:0.588:0.005 和 0.151:0.218:0.010:0.003:0.025:0.008:0.012:0.565:0.008。摩尔比值表明,两种多糖的甘露糖含量最高,葡萄糖醛酸含量较低,并且两种多糖均在其红外光谱803 cm−1和1650 cm−1附近出现特征峰。葛智超等[12]从裸藻中分离出分子量为3~5 kDa的水溶性多糖组分中含量较高的单糖为半乳糖、岩藻糖、木糖,该结果与EGP-2A-1和EGP-2B-1的结果不同,造成这种差异的可能原因是提取的是不同分子量段的多糖,导致其结构存在差异。
2.5 抗氧化活性分析
2.5.1 DPPH自由基清除能力
人类的多种疾病均与自由基有关,包括炎症、癌症、糖尿病等等。自由基属于强氧化剂,一旦在人体内蓄积过量,会加速细胞老化甚至凋亡[30]。抗氧化剂可消除自由基,对人体正常的新陈代谢有重要意义。
根据作用方式的不同,抗氧化剂主要分为两大类:初级(链断裂)抗氧化剂和次级(预防性)抗氧化剂[31]。初级抗氧化剂通常充当自由基的受体,抑制起始步骤或干扰自氧化的传播步骤,能够将氢原子捐赠给自由基[32]。次级抗氧化剂能够通过多种不同机制减缓氧化反应的速率[33]。例如,次级抗氧化剂可以提供H原子给初级抗氧化剂,用作氧清除剂或将氢过氧化物转换为非自由基物质[34]。
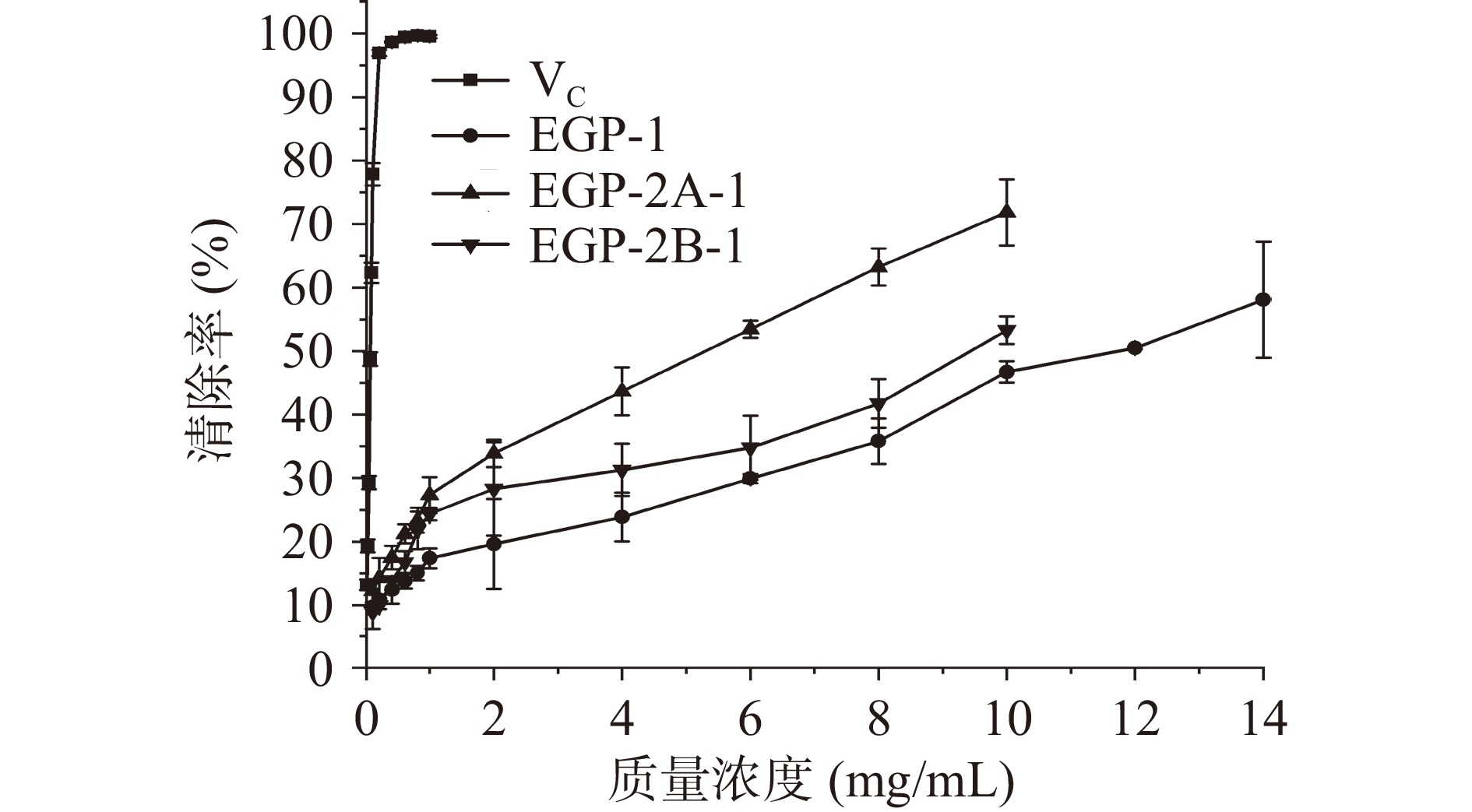
DPPH法是检测抗氧化能力的常用标准方法,DPPH自由基能够接受来自抗氧化剂的H原子形成稳定的分子,导致溶液颜色变浅。如图7所示,各样品均对DPPH·具有一定的清除活性,当多糖浓度从0.1增加到10.0 mg/mL时,3种多糖对DPPH自由基清除能力随样品浓度的升高而增大。IC50是指清除率为50%时物质的质量浓度,物质IC50值越小,表明其抗氧化性越好[35]。裸藻EGP-1、EGP-2A-1和EGP-2B-1的IC50值分别为11.954、5.397和9.458 mg/mL,说明3种样品的初级抗氧化能力较强。因此,还需对裸藻多糖样品的次级抗氧化活性进行研究,以确定它们的总抗氧化能力。
2.5.2 羟基自由基清除能力
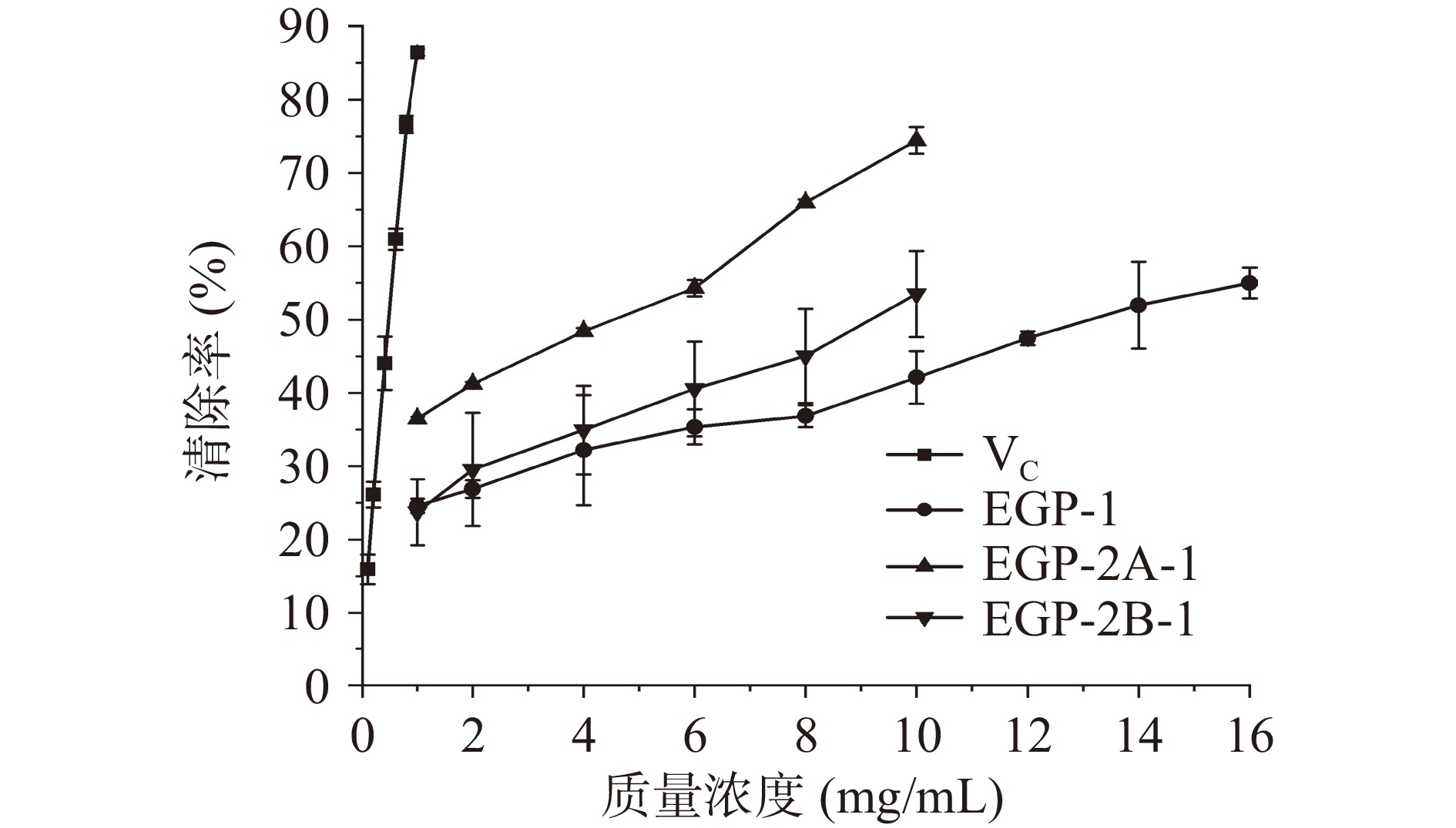
用水杨酸法测定裸藻多糖样品的次级抗氧化能力。3种多糖和VC对羟基自由基的清除能力如图8所示,其自由基清除率和样品浓度成线性依赖关系,存在明显的剂量效应。且在相同浓度下,样品的清除能力强弱依次为EGP-2A-1>EGP-2B-1>EGP-1,但其清除能力与VC相比还有一定的差距,经计算得EGP-1、EGP-2A-1、EGP-2B-1和VC的IC50值分别为13.264、4.327、9.142和0.539 mg/mL。先前的文献报道,羊栖菜多糖在浓度为9.85 mg/mL时,其羟自由基清除能力接近50%[36],紫菜、罗汉果和山药多糖在浓度为2 mg/mL时,清除率均低于20%[37]。相比之下,EGP-2A-1具有较好的次级抗氧化活性。
2.5.3 还原能力
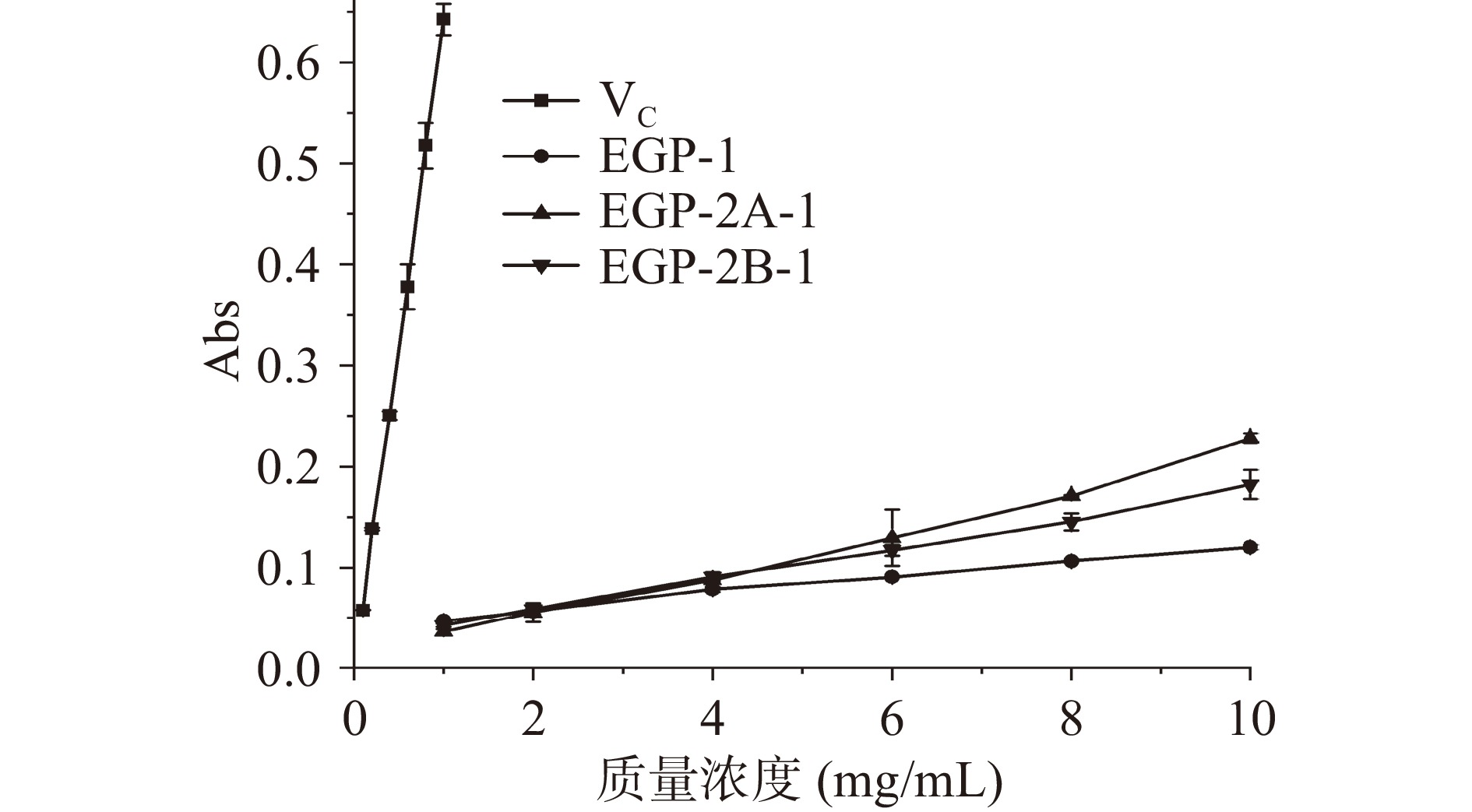
吸光度值表示物质的还原能力,物质的还原力越高,表明其抗氧化性越好[19]。如图9所示,裸藻多糖的还原能力随着样品浓度的增加而增强,在浓度为1~2 mg/mL时,EGP-2A-1和EGP-2B-1组分的还原能力低于EGP-1,而在4~10 mg/mL范围内,EGP-2A-1和EGP-2B-1的还原能力逐渐高于EGP-1,差距不断拉大。当浓度达到10 mg/mL时,EGP-2A-1和EGP-2B-1的吸光度分别为0.23和0.18。虽然阳性对照VC的还原能力远高于3种组分多糖,但本实验仍能证明裸藻多糖具有一定的还原能力,还原能力大小依次为:EGP-2A-1>EGP-2B-1>EGP-1。
2.5.4 总体抗氧化能力分析
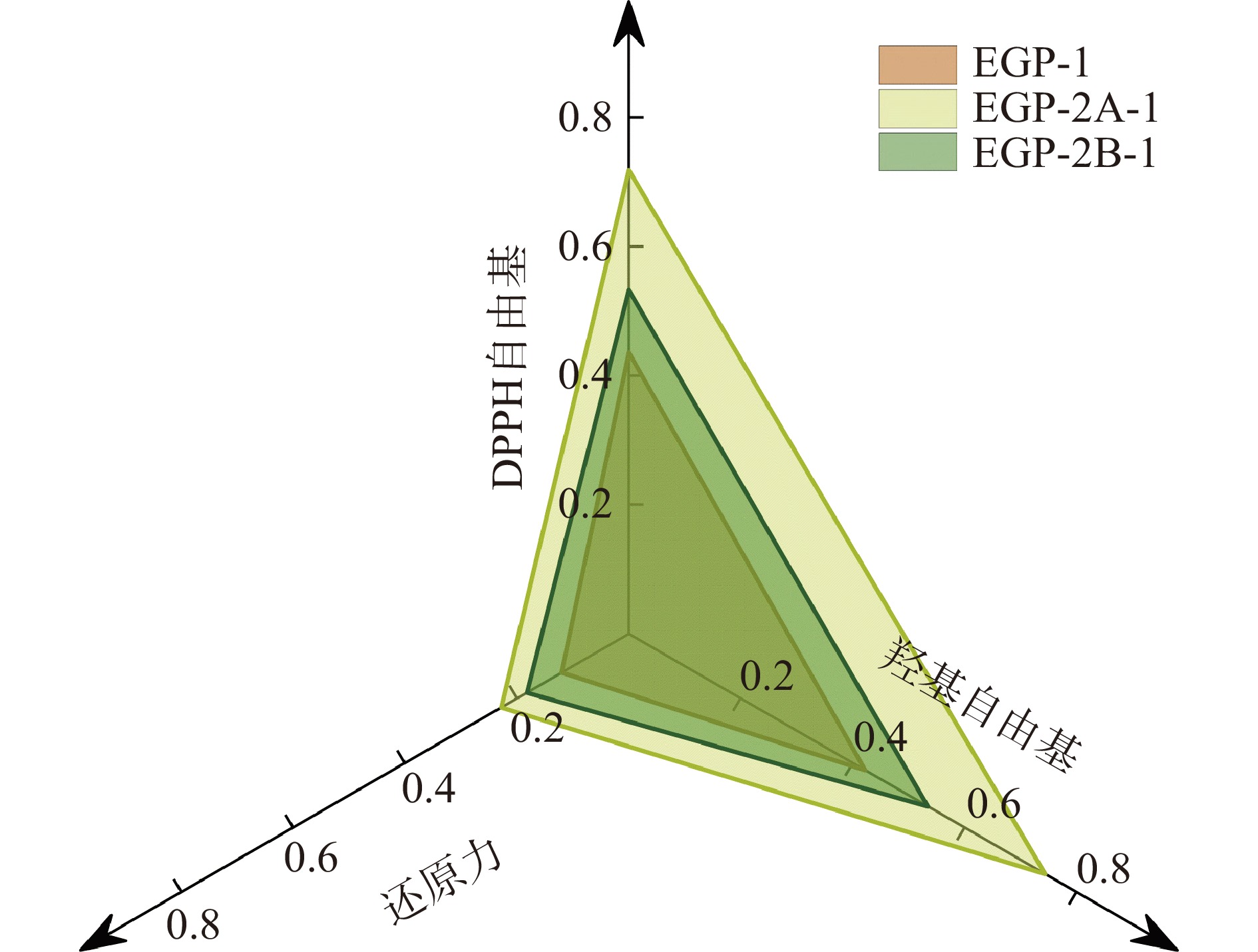
EGP-1、EGP-2A-1和EGP-2B-1组分在质量浓度10 mg/mL时的抗氧化能力可以通过在雷达图上面积的比较进行分析。如图10所示,EGP-2A-1的面积最大,说明该组分多糖的抗氧化能力最强。三种组分的抗氧化活性大小为:EGP-2A-1>EGP-2B-1>EGP-1。
有研究表明,分子量也是影响多糖抗氧化性的一方面因素,高分子量多糖的空间结构更稳定,这有利于维持生物活性,但也有研究表明低分子量多糖由于松散的构象,更容易被吸收,具有更好的活性[38]。在本研究中,分子量的大小为:EGP-2A-1>EGP-2B-1>EGP-1,可见分子量的大小对于裸藻多糖的抗氧化活性具有一定影响,在三种多糖组分中,分子量越大抗氧化活性越好。
Luo和Wang等[39-40]研究了石斛多糖单糖组成与抗氧化活性之间的关系,结果表明石斛多糖是否具有抗氧化活性受葡萄糖的影响,但是其活性大小受甘露糖、半乳糖和阿拉伯糖的影响。艾于杰[38]对茶多糖和抗氧化活性的构效关系研究发现,鼠李糖和甘露糖含量与抗氧化活性正相关,而随着葡萄糖醛酸、半乳糖和阿拉伯糖含量的增加,DPPH自由基清除能力降低。黄依佳等[41]对比了两种蓝藻多糖的羟基自由基清除能力及其单糖组成之间存在的差异,研究发现以甘露糖为主要单糖的CB-2-1比以葡萄糖为主要组分的CCB活性更好。
本研究纯化的三个组分中均含有葡萄糖,实验证明都具有抗氧化活性,与刘袆帆等的结果一致[42]。但是EGP-1的抗氧化活性最低,可能是由于EGP-1中葡萄糖含量为87.3%,成分较单一,并且甘露糖和鼠李糖只含有6.6%和3.0%,从而导致其活性不高。组分EGP-2A-1和EGP-2B-1均表现较好的清除DPPH活性,其中甘露糖和鼠李糖为主要单糖,并且EGP-2A-1组分中半乳糖和葡萄糖醛酸的含量低于EGP-2B-1,但是在EGP-2A-1中阿拉伯糖的含量更高,经过各种单糖的协同作用最后表现出裸藻多糖的DPPH清除能力为EGP-2A-1高于EGP-2B-1,存在极显著差异(P<0.01)。EGP-2A-1的羟基自由基清除能力远高于EGP-2B-1,具有极显著差异(P<0.01),根据两者的单糖组成分析,可能有甘露糖含量的影响,但是因两者单糖组成相似,并且多糖的活性还与糖苷键、空间构象等有密切关系,其更深入的原因需要进一步的研究。
3. 结论
本研究中,首次对裸藻水溶性多糖和非水溶性多糖的主要组分的结构进行研究分析,并对其抗氧化能力进行比较分析。通过不同方法对裸藻中水溶性多糖和非水溶性多糖进行提取,并进一步分离纯化后得到3个主要组分多糖EGP-1、EGP-2A-1和EGP-2B-1。结合紫外可见光、红外光谱、凝胶色谱、离子色谱等多种技术对3个组分多糖进行分析。紫外光谱表明3种样品均不含或含少量蛋白和核酸,纯度较高;红外光谱结果表明3个组分多糖均存在糖的羰基、羟基、吡喃环等多糖常见官能团和结构,其中EGP-1含有β-糖苷键,EGP-2A-1和EGP-2B-1中均含有α-和β-糖苷键。通过渗透色谱测定EGP-1、EGP-2A-1和EGP-2B-1的相对分子质量分别为1.01×104、2.91×106和1.70×106 Da。离子色谱分析表明EGP-1中鉴定出葡萄糖、甘露糖、岩藻糖和鼠李糖四种主要单糖,EGP-2A-1和EGP-2B-1组分均由岩藻糖、鼠李糖、阿拉伯糖、盐酸氨基葡萄糖、半乳糖、葡萄糖、木糖、甘露糖和葡萄糖醛酸组成。通过体外抗氧化研究发现,裸藻多糖对DPPH和OH自由基均具有清除作用,且均具有一定的还原能力。各组分活性存在差异,在相同质量浓度下,抗氧化活性VC>EGP-2A-1>EGP-2B-1>EGP-1。综上所述,裸藻多糖具有抗氧化能力,且其水溶性多糖的抗氧化能力强于非水溶性多糖,推测这可能是由于单糖组成和分子量的不同造成的,这种差异还可能与多糖的糖苷键类型、三螺旋结构等因素有关,因此后续还需进一步通过实验来深入探究裸藻多糖结构及其抗氧化活性之间的关系。
-
表 1 裸藻多糖傅里叶红外光谱数据
Table 1 Fourier infrared spectroscopy data of Euglena gracilis polysaccharide
吸收波数(cm−1) 振动方式或官能团 参考文献 EGP-1 EGP-2A-1 EGP-2B-1 3386.51 3384.35 3344.70 -OH伸缩振动 [22] 2925.11 2931.63 2925.86 糖类C-H不对称伸缩振动 [22] 1648.17 1651.61 1647.26 C=O在COO-中的不对称振动 [23] 1360.85 1380.51 1378.79 CH3-的对称变角振动 [24] 1259.61 1245.54 1244.02 吡喃糖环上的C-O-H和C-O-C的C-O伸缩振动 [25] 1049.96 1041.32 1040.91 吡喃糖环上的C-O-C和C-O-H单键 [26] 889.59 894.17 894.17 β-D-吡喃葡萄糖 [27] 834.80 836.09 α-D-吡喃糖苷振动 [28] 805.91 802.99 吡喃甘露糖 [29] -
[1] 陈建琴, 钱晶. pH值与绿眼虫包囊的形成[J]. 生物学通报,2005,40(6):38. [CHEN J Q, QIAN J. pH and the formation of green Euglena cysts[J]. Bulletin of Biology,2005,40(6):38. doi: 10.3969/j.issn.0006-3193.2005.06.030 [2] PRICE C A. The biology of Euglena. Volume 3: Physiology. Dennis E. Buetow[J]. The Quarterly Review of Biology,1983,58(2):256−256.
[3] 关于批准裸藻等8种新食品原料的公告(2013年第10号) [EB/OL]. http://www.nhfpc.gov.cn/sps/s7890/201311/533ed8492dd04ff3aa63c7edd40c256.shtml Announcement on approving 8 new food ingredients including Euglena (2013 No. 10) [M]. http://www.nhfpc.gov.cn/sps/s7890/201311/533ed8492dd04ff3aa63c7edd40c256.shtml
[4] 中岛绫香, 铃木健吾, 伊势川裕二. 抗病毒剂及抗病毒用食品: 中国, CN201680082968.0[P]. 2018-10-23. AYAKA N, KENGO S, YUJI I. Antiviral agents and antiviral foods: China, CN201680082968.0[P]. 2018-10-23.
[5] 王崇队, 张明, 杨立风, 等. 不同来源膳食纤维品质分析及抗氧化活性研究[J]. 食品科技,2019,44(5):78−83. [WANG C D, ZHANG M, YANG L F, et al. Quality analysis and antioxidant activity of dietary fiber from different sources[J]. Food Technology,2019,44(5):78−83. [6] XU S Y, HUANG X, KIT-LEONG C. Recent advances in marine algae polysaccharides: isolation, structure, and activities[J]. Marine Drugs,2017,15(12):388. doi: 10.3390/md15120388
[7] WEN Y, GAO L, ZHOU H, et al. Opportunities and challenges of algal fucoidan for diabetes management[J]. Trends in Food Science & Technology,2021,111:628−641.
[8] YAMAMOTO F Y, YIN F, ROSSI W, et al. β-1, 3 glucan derived from Euglena gracilis and algamune enhances innate immune responses of red drum (Sciaenops ocellatus L. )[J]. Fish Shellfish Immunol,2018,77:273−279. doi: 10.1016/j.fsi.2018.04.003
[9] THANKAMONY R L. Euglena as a potential natural source of value-added metabolites. A review[J]. Algal Research,2019,37:154−159. doi: 10.1016/j.algal.2018.11.024
[10] PHILLIPS F C, JENSEN G S, SHOWMAN L, et al. Particulate and solubilized β-glucan and non-β-glucan fractions of Euglena gracilis induce pro-and anti-inflammatory innate immune cell responses and exhibit antioxidant properties[J]. Journal of Pharmacy Research,2019,12:49−64.
[11] 鞠海军. 裸藻多糖分离提取、结构鉴定及生物活性研究[D]. 上海: 华东理工大学, 2020. JU H J. Separation, structure identification of paramylon and study on its bioactives[D]. Shanghai: East China University of Science and Technology, 2020.
[12] 葛智超, 李燕, 施文正, 等. 裸藻多糖提取工艺优化及抗氧化活性研究[J]. 食品与机械,2020,36(1):186−191. [GE Z C, LI Y, SHI W Z, et al. Optimization of the extraction process of polysaccharides from Euglena and its antioxidant activity[J]. Food and Machinery,2020,36(1):186−191. [13] LIU X, LIU D, CHEN Y, et al. Physicochemical characterization of a polysaccharide from Agrocybe aegirita and its anti-ageing activity[J]. Carbohydrate Polymers,2020,236(1-2):116056.
[14] 马佩佩, 王洪新, 童军茂. 库尔勒香梨多糖的分离纯化及抗氧化性质的研究[J]. 食品研究与开发,2010(6):53−55. [MA P P, WANG H X, TONG J M. Separation, purification and antioxidative activites of polysaccharides from Pyrus bretschneideri Rehd[J]. Food Research and Development,2010(6):53−55. doi: 10.3969/j.issn.1005-6521.2010.06.016 [15] SUN Y, HUO J, ZHONG S, et al. Chemical structure and anti-inflammatory activity of a branched polysaccharide isolated from Phellinus baumii[J]. Carbohydrate Polymers,2021,268:118214. doi: 10.1016/j.carbpol.2021.118214
[16] XIU L, SHENG S, HU Z, et al. Exopolysaccharides from Lactobacillus kiferi as adjuvant enhanced the immuno-protective against Staphylococcus aureus infection[J]. International Journal of Biological Macromolecules,2020,161:10−23. doi: 10.1016/j.ijbiomac.2020.06.005
[17] 栗晓庆, 吕俊平, 刘琪, 等. 裸藻多糖碱提工艺优化及其体外抗氧化活性研究[J]. 食品科技,2019,44(9):209−215. [LI X Q, LV J P, LIU Q, et al. Optimization of alkaline extraction and antioxidant activities of paramylon in vitro[J]. Food Science and Technology,2019,44(9):209−215. [18] 宋佳敏, 王鸿飞, 孙朦, 等. 响应面法优化金蝉花多糖提取工艺及抗氧化活性分析[J]. 食品科学,2018,39(4):275−281. [SONG J M, WANG H F, SUN M, et al. Optimization of extraction and antioxidant activity of polysaccharides from Cordyceps cicadae by response surface methodology[J]. Food Science,2018,39(4):275−281. doi: 10.7506/spkx1002-6630-201804041 [19] 董扬, 郝利民, 刘宇琪, 等. 不同破壁方法对灵芝孢子粗多糖抗氧化活性的影响[J]. 食品科学,2017,38(17):101−106. [DONG Y, HAO L M, LIU Y Q, et al. Effect of different cell wall disruption methods on in vitro antioxidant activity of crude polysaccharides Ganoderma lucidum spores[J]. Food Science,2017,38(17):101−106. doi: 10.7506/spkx1002-6630-201717017 [20] NIE S, XIE M, FU Z, et al. Study on the purification and chemical compositions of tea glycoprotein[J]. Carbohydrate Polymers,2008,71(4):626−633. doi: 10.1016/j.carbpol.2007.07.005
[21] JIAN H, QIAO F, CHEN J, et al. Physicochemical characterisation of polysaccharides from the seeds and leaves of miracle fruit (Synsepalum dulcificum) and their antioxidant α-glucosidase inhibitory activities in vitro[J]. Journal of Chemistry,2017,9:8948639.
[22] YANG D, LIN F, HUANG Y, et al. Separation, purification, structural analysis and immune-enhancing activity of sulfated polysaccharide isolated from sea cucumber viscera[J]. International Journal of Biological Macromolecules,2020,155(155):1003−1018.
[23] WANG W, MA X, JIANG P, et al. Characterization of pectin from grapefruit peel: A comparison of ultrasound-assisted and conventional heating extractions[J]. Food Hydrocolloids,2016,61(61):730−739.
[24] HE P, ZHANG A, ZHANG F, et al. Structure and bioactivity of a polysaccharide containing uronic acid from Polyporus umbellatus sclerotia[J]. Carbohydrate Polymers,2016,152:222−230. doi: 10.1016/j.carbpol.2016.07.010
[25] WU D, CHEN Y, WAN X, et al. Structural characterization and hypoglycemic effect of green alga Ulva lactuca oligosaccharide by regulating microRNAs in Caenorhabditis elegans[J]. Algal Research,2020,51:102083. doi: 10.1016/j.algal.2020.102083
[26] DING X, FENG S, CAO M, et al. Structure characterization of polysaccharide isolated from the fruiting bodies of Tricholoma matsutake[J]. Carbohydrate Polymers,2010,81(4):942−947. doi: 10.1016/j.carbpol.2010.04.010
[27] WANG Y, LIU Y, YU H, et al. Structural characterization and immuno-enhancing activity of a highly branched water-soluble β-glucan from the spores of Ganoderma lucidum[J]. Carbohydrate Polymers,2017,167(167):337−344.
[28] FENG S, LUAN D, NING K, et al. Ultrafiltration isolation, hypoglycemic activity analysis and structural characterization of polysaccharides from Brasenia schreberi[J]. International Journal of Biological Macromolecules,2019,135:141−151. doi: 10.1016/j.ijbiomac.2019.05.129
[29] YANG L, ZHANG L. Chemical structural and chain conformational characterization of some bioactive polysaccharides isolated from natural sources[J]. Carbohydrate Polymers,2009,40(33):349−361.
[30] 朱赓伯. 自由基与人体健康[J]. 家庭医学月刊,2005(23):34. [ZHU G B. Free radicals and human health[J]. Family Medicine Monthly,2005(23):34. [31] HUI S, LU J, ZHOU W. Structure characterization and antioxidant activity of fucoidan isolated from Undaria pinnatifida grown in New Zealand[J]. Carbohydrate Polymers,2019,212:178−185. doi: 10.1016/j.carbpol.2019.02.040
[32] DARAMOLA B, ADEGOKE G. Bitter kola (Garcinia kola) seeds and health management potential[J]. Nuts and seeds in health and disease prevention,2011:213−220.
[33] MISHRA R, BISHT S S. Antioxidants and their charecterization[J]. Journal of Pharmacy Research,2011,4(8):2744−2746.
[34] 李兴太, 纪莹. 线粒体氧化应激与天然抗氧化剂研究进展[J]. 食品科学,2015,36(7):268−277. [LI X T, JI Y. Recent advances in mitochondrial oxidative stress and natural antioxidants[J]. Food Science,2015,36(7):268−277. doi: 10.7506/spkx1002-6630-201507049 [35] 薛山. 紫薯不溶性膳食纤维超声辅助酶法提取工艺及抗氧化活性研究[J]. 食品与机械,2018,34(5):153−157,163. [XUE S. Extraction of insoluble dietary fiber from purple sweet potato by ultrasonic assisted enzyme method and the determination of its hydrroxyl radical scavenging ability[J]. Food and Machinery,2018,34(5):153−157,163. [36] 刘洪超. 羊栖菜多糖的提取分离、生物活性及结构鉴定[D]. 上海: 上海海洋大学, 2017. LIU H C. Study isolation, purification and determination of physiological activity on SFPS (Sargassum fusiforme)[D]. Shanghai: Shanghai Ocean University, 2017.
[37] 朱娇娇, 周安婕, 丁怡, 等. 3种天然植物多糖的抗氧化与降血糖活性研究[J]. 粮食与油脂,2018,31(8):96−100. [ZHU J J, ZHOU A J, DING Y, et al. Antioxidant and hypoglycemic activities of three natural plant polysaccharides[J]. Cereals & Oils,2018,31(8):96−100. doi: 10.3969/j.issn.1008-9578.2018.08.025 [38] 艾于杰. 抗氧化活性茶多糖构效关系研究[D]. 武汉: 华中农业大学, 2019. AI Y J. Study on the structure-activity relationship of antioxidant tea polysaccharides[D]. Wuhan: Huazhong Agricultural University, 2019.
[39] WANG D, BEI F, YAN W, et al. Optimum extraction, characterization, and antioxidant activities of polysaccharides from flowers of Dendrobium devonianum[J]. International Journal of Analytical Chemistry,2018,2018:1−8.
[40] LUO Q L, TANG Z H, ZHANG X F, et al. Chemical properties and antioxidant activity of a water-soluble polysaccharide from Dendrobium officinale[J]. International Journal of Biological Macromolecules,2016,89:219−227. doi: 10.1016/j.ijbiomac.2016.04.067
[41] 黄依佳, 吴剑荣, 朱莉, 等. 蓝藻多糖的分离、结构表征及抗氧化活性研究[J]. 食品与机械,2018,34(2):176−180. [HUANG Y J, WU J R, ZHU L, et al. Study on isolation, structure characterization and radical scavenging activity of Cyanobacteria polysaccharide[J]. Food and Machinery,2018,34(2):176−180. [42] 刘袆帆, 郭烁璇, 林映妤, 等. 石斛多糖的构效关系研究进展[J]. 现代食品科技,2021,37(1):308−338. [LIU Y F, GUO S X, LIN Y Y, et al. The relationship between the structure and function of Dendrobium polysaccharides: A review[J]. Modern Food Science and Technology,2021,37(1):308−338. -
期刊类型引用(1)
1. 胡玥,孙红男,张苗,木泰华. 食物源肽与淀粉相互作用的研究进展. 食品科学. 2023(09): 163-169 .  百度学术
百度学术
其他类型引用(7)








 下载:
下载:
 下载:
下载:



