Identification of Characteristic Peptides of Different Gelatins in Donkey-hide Gelatin Lump by High Performance Liquid Chromatography-High Resolution Mass Spectrometry
-
摘要: 为研究阿胶块中不同明胶的来源,本文以4种品牌的阿胶块为原料,向其中分别加入低含量(1 mg/mL)的牛明胶和猪明胶,采用高效液相色谱-质谱联用技术(high-performance liquid chromatography-mass spectrometry,HPLC-MS/MS)分别鉴定阿胶、牛明胶和猪明胶的特征性多肽。结果表明,在4种阿胶块中准确检测出阿胶、牛明胶和猪明胶的共有特征性多肽数量分别为18、3和5个,其中来自α1链的特征性多肽有10、1和1个,来自α2链的则有8、2和4个;同时,有羟基化修饰脯氨酸的共有特征性多肽数量分别为15、2和4个,不包含任何修饰基团的特征性多肽对应则有3、1和1个。这些共有的特征性多肽可为HPLC-MS/MS溯源鉴定阿胶块中的明胶源提供依据,对阿胶块产品的质量保障具有一定的参考意义。
-
关键词:
- 阿胶 /
- 高效液相色谱-质谱联用技术 /
- 溯源鉴定 /
- 牛明胶 /
- 猪明胶
Abstract: To study the source of different gelatins of donkey-hide gelatin lumps, four kinds of donkey-hide gelatin lumps were added with low content (1 mg/mL) of bovine gelatin and porcine gelatin respectively. High-performance liquid chromatography-mass spectrometry (HPLC-MS/MS) were chosen to identify the characteristic peptides of donkey-hide gelatin, bovine gelatin and porcine gelatin. The results showed that 18, 3 and 5 common characteristic peptides were accurately detected in the four kinds of donkey-hide gelatin lump for donkey-hide gelatin, bovine gelatin and porcine gelatin, respectively, with 10, 1 and 1 from the α1 chain and 8, 2 and 4 from the α2 chain. Meanwhile, the number of common characteristic peptides with hydroxylated modifications was 15, 2 and 4 respectively, while those without any modification groups were 3, 1 and 1. These common characteristic peptides would provide a basis for the HPLC-MS/MS traceable identification of the gelatin source in donkey-hide gelatin lump, which is of reference significance for the quality assurance of donkey-hide gelatin lump products. -
阿胶是驴皮胶原蛋白适度水解断裂而得到的产物,因其具有补血、抗疲劳、增强免疫力等保健功效,受到广大消费者的喜爱,并与人参、鹿茸并称为三大最具价值的传统中药材[1-2]。近年来,随着人们生活水平的提高以及保健意识的增强,人们对阿胶的购买力明显增长,阿胶市场规模逐年递增。据统计数据显示,从2009到2019年,阿胶市场规模复合年增长率达到18.1%,并且,《山东省医养健康产业发展规划(2018~2022年)》中明确提出做大阿胶市场,阿胶市场规模有望进一步扩大[3-4]。然而,驴皮资源紧缺造成阿胶价格上涨,在利益的驱使下,不法商家向阿胶中大量掺入其他相对低价的牛皮明胶或猪皮明胶,制成的掺假阿胶阻碍了阿胶市场的健康发展,引发了消费者的购买担忧[5-7]。因此,阿胶产品中胶类来源的鉴别研究对规范阿胶市场秩序具有重要意义。
目前,国内外已公开报道了多种用于哺乳动物明胶(尤其是猪明胶和牛明胶)鉴定的方法,包括红外光谱法[8]、电泳技术[9]、聚合酶链式反应技术[10-11]、酶联免疫吸附测定[12-13]、高效液相色谱-质谱联用技术(high-performance liquid chromatography-mass spectrometry,HPLC-MS/MS)[14-15]等。相比之下,HPLC-MS/MS技术是被认为准确度最高的明胶鉴定方法,受到国内外研究者的认可[16-17]。同时,HPLC-MS/MS也被用于阿胶的鉴定中,如Cheng等[18]运用HPLC-MS/MS开展了阿胶、牛皮明胶、猪皮明胶、龟甲胶和鹿角胶的鉴定研究,在每种明胶中鉴定出1个特征性多肽;焦阳等[19]利用HPLC-MS/MS确定了1个区别于阿胶的马皮源特征性多肽。本课题组在前期以阿胶、猪明胶和牛明胶为研究对象,运用HPLC-MS/MS确定了不同比例混合明胶中低含量目标明胶的多个特征性多肽[20]。目前市面上的阿胶产品中以阿胶块占比最大[21]。然而,目前关于阿胶块产品中的阿胶和其他来源明胶的溯源研究少有报道,这值得深入研究和探索。
基于阿胶市场的快速发展和阿胶的溯源研究现状,本文以目前阿胶市场占比最大的阿胶块为研究对象,向其中分别加入在食用明胶市场中占比最大的猪明胶和牛明胶,采用HPLC-MS/MS分别鉴定阿胶块中阿胶、猪明胶和牛明胶的特征性多肽,为阿胶块产品的准确鉴定提供理论依据。
1. 材料与方法
1.1 材料与仪器
4种阿胶块产品 分别来自东阿阿胶股份有限公司、山东福牌阿胶股份有限公司、北京同仁堂科技发展股份有限公司和九芝堂股份有限公司;牛皮明胶、猪皮明胶 美国sigma公司;胰蛋白酶(酶活力:19385 U/mg) 美国Promega Corporation公司;其他试剂 均为分析纯。
LGJ-1D-80型冷冻干燥机 北京亚泰科隆仪器技术有限公司;EASY-nLC™ 1000色谱系统、Q-Exactive质谱仪 美国Thermo Fisher Scientific公司;RP-C18液相色谱柱(0.15 mm×150 mm,5 μm) 美国Column Technology公司。
1.2 实验方法
1.2.1 阿胶块样品的处理
用去离子水将4种阿胶块产品在50 ℃水浴锅中分别溶解制成100 mg/mL的阿胶溶液,同时分别向其中加入低含量的牛明胶和猪明胶,使得牛明胶和猪明胶在整个溶液体系中的质量浓度均为1 mg/mL,搅拌均匀制成阿胶-牛明胶-猪明胶的混合溶液。置于离心机中以6000 ×g的速度离心25 min,所得上清液进一步通过0.45 μm的过滤器处理,将得到的滤液冻干,备用。
1.2.2 样品的酶解
样品参照课题组前期的方法进行酶解[22]。将冻干后的样品溶解于SDT缓冲液(4 mg/mL十二烷基硫酸钠、100 mmol/L二硫苏糖醇、150 mmol/L pH8.0三羟甲基氨基甲烷盐酸盐(Tris-HCl)溶液)并制成质量浓度为1 μg/μL的溶液,于沸水中加热3 min后在离心机中12000×g离心15 min。将上清液置于超滤离心管(截留分子质量为10 kDa)中,加入200 μL尿素裂解液(8 mol/L尿素,150 mmol/L pH8.0 Tris-HCl溶液)后以14000×g离心15 min。往浓缩物中加入200 μL尿素裂解液后再次离心。然后,加入100 μL 50 mmol/L的碘乙酰胺溶液,于暗室放置30 min后14000×g离心15 min。之后,加入100 μL尿素裂解液,14000×g离心15 min,重复此操作2次。加入100 μL的25 mmol/L NH4HCO3溶液并14000×g离心30 min,重复操作2次。最后,在浓缩物中加入含2 μg胰蛋白酶的40 μL 25 mmol/L NH4HCO3溶液,37 ℃放置反应20 h后14000×g离心20 min收集滤液,即得到明胶多肽溶液。
1.2.3 高效液相色谱-质谱检测
混合明胶酶解液运用Easy nLC-Orbitrap Fusion Tribrid质谱仪进行检测。流动相A为含有体积分数0.1%甲酸的水溶液,流动相B为体积分数84%的乙腈溶液(含有体积分数0.1%的甲酸)。RP-C18色谱柱以95%的A液进行平衡,样品由自动进样器上样到Zorbax 300SB-C18 peptide traps,经色谱柱以250 nL/min的流速洗脱60 min,流动相A线性梯度变化为流动相B。采用数据依赖采集模式动态收集丰度最高的10个母离子(m/z范围为300~1800)进行高能碰撞解离(high energy collision dissociation,HCD)模式碎裂。动态排除时间为20 s,归一化碰撞能量为27 eV。
1.3 数据处理
采用MASCOT软件(Matrix Science, London, UK; version 2.2)匹配分析所获得的质谱图,数据库设置为目标胶原蛋白(驴皮、牛皮和猪皮胶原蛋白)数据库。检索参数包括:半胱氨酸碘乙酰胺化(C)为固定修饰;氧化(M、P、K)为可能性修饰;最大漏切位点数为2;一级质谱错误率为±20×10−6;二级质谱错误率为±0.1 Da。当Mascot分数大于40时,多肽峰被认定为阳性鉴定或准确度极高(P<0.05)[23]。阿胶、牛明胶和猪明胶特征性多肽的比对分析是依据课题组前期建立的3种胶原蛋白理论特征性多肽数据库开展的[20]。
2. 结果与分析
2.1 阿胶块中阿胶、牛明胶和猪明胶的特征性多肽差异性分析
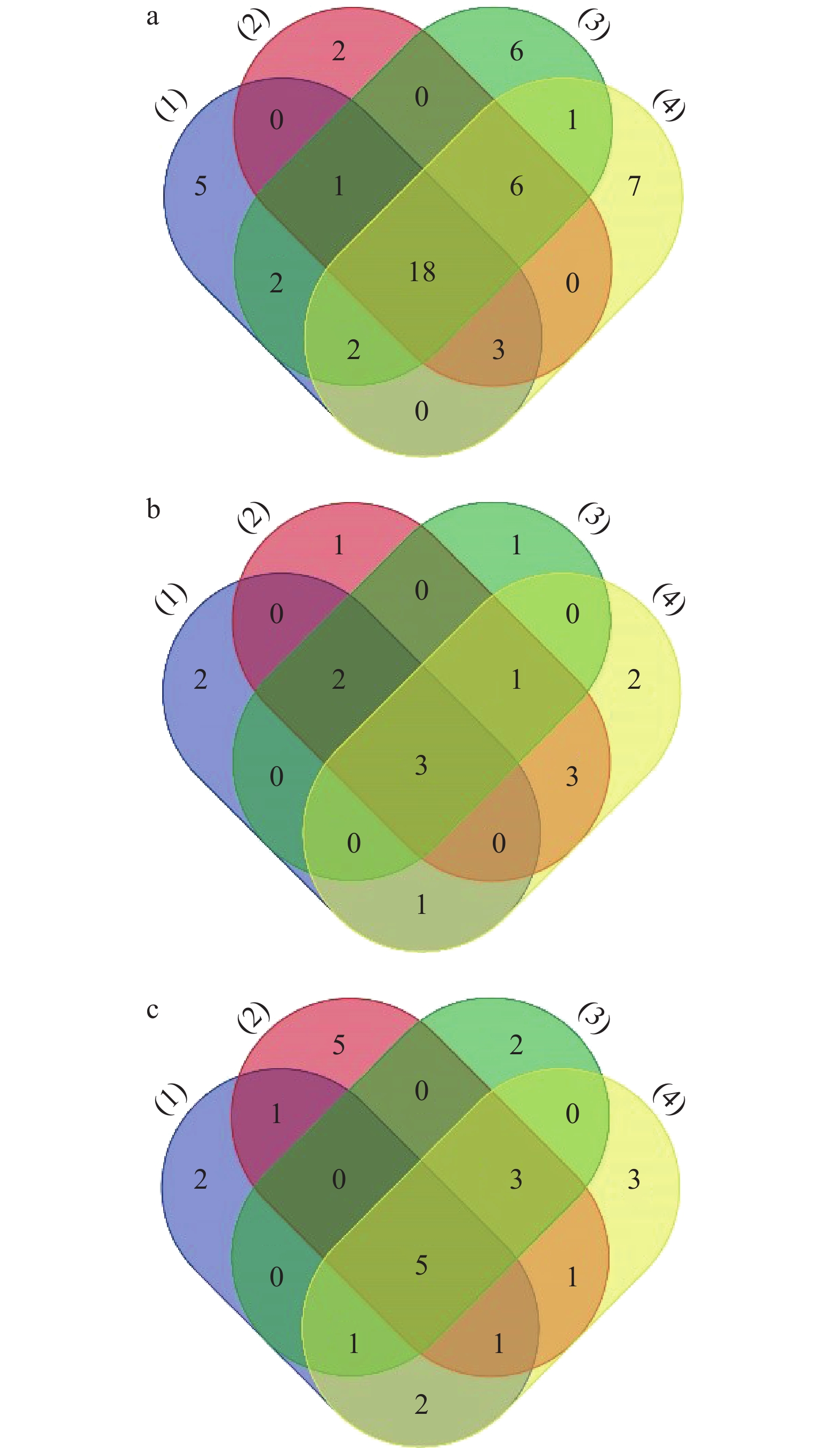
本课题组前期研究了不同加热温度对猪皮明胶鉴定效果的影响,结果发现不同温度下制备的猪皮明胶特征性多肽有所不同[22]。由于阿胶与其他来源的明胶类似,在不同生产厂家,阿胶块的生产工艺和参数可能会略有不同,其分子链的断裂程度会受到多种因素(如加热温度、提取时间、酸碱性等)的影响[24],进而可能会对阿胶溯源产生一定影响。因此,从广受消费者青睐的阿胶块中找出共有的阿胶特征性多肽对于阿胶块产品的溯源鉴定研究显得十分必要。故选取了4种知名品牌的阿胶块(同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块)分别鉴定阿胶特征性多肽,并通过韦恩图分析不同品牌阿胶块中阿胶特征性多肽的差异性,并确定4种阿胶块中共有的阿胶特征性多肽。由图1a可知,同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块经HPLC-MS/MS并匹配驴皮多肽数据库分别鉴定出31、30、36和37个阿胶特征性多肽,其中4种品牌的阿胶块共有18个特征性多肽,对阿胶块产品中阿胶成分的溯源鉴定有十分重要的意义。除此之外,同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块分别被鉴定出13、12、18和19个非共有阿胶特征性多肽,这些多肽的质谱峰只在1种、2种或者3种阿胶块的质谱图中被检出,因而不适宜用于阿胶块的溯源鉴定。
![]() 图 1 阿胶块中阿胶、牛明胶和猪明胶特征性多肽组成的差异性分析注:(1):同仁堂阿胶块;(2):福牌阿胶块;(3):东阿阿胶块;(4):九芝堂阿胶块;a:阿胶块中阿胶的特征性多肽组成的差异性分析;b:阿胶块中牛明胶的特征性多肽组成的差异性分析;c:阿胶块中猪明胶的特征性多肽组成的差异性分析。Figure 1. Differential analysis of the characteristic peptides composition of donkey-hide gelatin, bovine gelatin and porcine gelatin in donkey-hide gelatin lumps
图 1 阿胶块中阿胶、牛明胶和猪明胶特征性多肽组成的差异性分析注:(1):同仁堂阿胶块;(2):福牌阿胶块;(3):东阿阿胶块;(4):九芝堂阿胶块;a:阿胶块中阿胶的特征性多肽组成的差异性分析;b:阿胶块中牛明胶的特征性多肽组成的差异性分析;c:阿胶块中猪明胶的特征性多肽组成的差异性分析。Figure 1. Differential analysis of the characteristic peptides composition of donkey-hide gelatin, bovine gelatin and porcine gelatin in donkey-hide gelatin lumps除了鉴定阿胶块中的阿胶特征性多肽,若能同时找出其他来源明胶的特征性多肽,将有利于阿胶块产品中掺假明胶的鉴别分析。因此,本文以4种阿胶块为原料,向其中加入1 mg/mL的牛皮明胶和猪皮明胶,通过HPLC-MS/MS鉴定牛明胶和猪明胶的特征性多肽。由图1b可知,加入牛明胶后,经过过滤、离心、酶解等多种前处理工序后,与牛皮多肽数据库进行匹配,同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块中分别鉴定出8、10、7和10个牛明胶特征性多肽,其中有3个特征性多肽均能在4种阿胶块中被检出,可作为阿胶块中追溯是否掺有牛明胶的依据。然而,4种品牌的阿胶块中还分别有5、7、4和7个非共有的牛明胶特征性多肽被检出,这些特征性多肽不能同时在4种阿胶块中被鉴定出来可能是因为在阿胶块前处理的过程中丢失或者低含量难以被质谱仪检出。由图1c可知,加入猪明胶后,所得多肽与猪皮多肽数据库进行匹配,同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块中分别检测出12、16、11和16个猪明胶特征性多肽,其中有5个特征性多肽在4种阿胶块中均能被检出,因此可作为阿胶块中追溯是否掺有猪明胶的依据。相应地,4种阿胶块中分别有7、11、6和11个非共有的猪明胶特征性多肽被检出。在质谱检测中,氨基酸序列和修饰情况会影响多肽的检出效果[25-26],多肽的含量亦会影响其在质谱图中的信号强度[20]。此外,检测实验前处理过程同样可能对多肽产生影响,进而干扰其质谱检测。上述因素均可能导致多肽只能在部分阿胶块产品中被检出,这些不能被稳定检出的特征性多肽用于阿胶块中猪明胶的溯源具有较大风险,可能会引起“假阴性”结果的出现。
实验结果表明,当牛明胶和猪明胶在阿胶块中占比低时,依然可以在阿胶块中稳定地检测出3个牛明胶特征性多肽和5个猪明胶特征性多肽。一般情况下,在质谱峰中同时找到1种蛋白质的2个多肽即可证明该蛋白质的存在[27]。因此,上述结果说明HPLC-MS/MS能有效鉴别阿胶块中低含量的牛明胶和猪明胶。
2.2 阿胶块中阿胶的共有特征性多肽
研究不同品牌阿胶块中阿胶的共有特征性多肽,有利于减少不同厂家制备工艺的差异对阿胶鉴定效果带来的影响,这对阿胶块的溯源鉴定十分重要。结合图1a和表1可知,4种阿胶块中阿胶的共有特征性多肽数目为18个,其中10个来自于α1链,8个来自于α2链。值得说明的是,在这些共有特征性多肽中,有3个多肽是不含修饰基团的,分别是来自α1链的(R)1066GEAGPAGPAGPIGPVGAR1083(G)和(R)994GPPGPVGPPGLAGPPGESGR1013(E)以及来自于α2链的(R)1052GPAGPTGPVGK1062(D)。胶原蛋白含有大量的翻译后修饰,使得明胶肽段的鉴定更为复杂,因此,在溯源鉴定中不带修饰基团的特征性多肽往往更受青睐,其在裂解过程中产生的碎片离子更容易被识别和匹配,能有效降低质谱峰鉴定过程中的难度,提高多肽鉴定的准确度[28-29]。
表 1 阿胶的共有特征性多肽Table 1. Common characteristic peptides of donkey-hide gelatin阿胶的特征多肽序列 m/z 相对分子质量 实测值 理论值 误差(×10−6) α1: (K)835GDAG*PPGPAGPAGPPG*PIGSVGA*PG*PK861(G) 1148.56672+ 2295.1188 2295.1132 2.45 α1: (K)835GDAG*PPGPAGPAGPPGPIGSVGA*PG*PK861 (G) 1140.57072+ 2279.1268 2279.1183 3.75 α1: (K)835GDAGPPGPAGPAGPPGPIGSVGA*PGPK861 (G) 1124.57592+ 2247.1372 2247.1284 3.91 α1: (R)1066GEAGPAGPAGPIGPVGAR1083(G) 765.90822+ 1529.8018 1529.7950 4.43 α1: (R)472GE*PGPTGL*PGP*PGER486(G) 733.35162+ 1464.6886 1464.6845 2.81 α1: (R)994G*PPGPVGPPGLAG*P*PGESGR1013 (E) 900.95102+ 1799.8874 1799.8802 3.98 α1: (R)994G*PPGPVGPPGLAGP*PGESGR1013 (E) 892.95262+ 1783.8906 1783.8853 2.96 α1: (R)994GPPGPVGP*PGLAG*PPGESGR1013 (E) 892.95332+ 1783.8920 1783.8853 3.74 α1: (R)994GPPGPVGP*PGLAGPPGESGR1013 (E) 884.95572+ 1767.8968 1767.8904 3.62 α1: (R)994GPPGPVGPPGLAGPPGESGR1013(E) 876.95912+ 1751.9036 1751.8955 4.63 α2: (R)829AGETGASGP*PGFAGEK844(G) 724.83842+ 1447.6622 1447.6579 2.96 α2: (R)776GDGGP*PGVTGF*PGAAGR792 (T) 751.35712+ 1500.6996 1500.6958 2.57 α2: (R)776GDGGPPGVTGF*PGAAGR792(T) 743.36082+ 1484.7070 1484.7008 4.16 α2: (R)977GE*PGPVGSVGPVGAVGPR994 (G) 802.92662+ 1603.8386 1603.8318 4.21 α2: (R)977GEPG*PVGSVGPVGAVGPR994(G) 802.92702+ 1603.8394 1603.8318 4.71 α2: (R)881GL*PGVAGSLGE*PGPLGIAGP*PGAR904(G) 1073.07302+ 2144.1314 2144.1226 4.11 α2: (R)1052GPAGPTGPVGK1062(D) 469.26022+ 936.5058 936.5029 3.12 α2: (R)793TG*P*PGPSGISGPPG*P*PGAAGK813(E) 910.44812+ 1818.8816 1818.8748 3.73 注:*P为羟基化的脯氨酸;表2~表3同。 尽管翻译后修饰大大增加了特征性多肽的鉴定难度,但由于其在特征性多肽总数中所占比例很大,特征性多肽修饰情况(尤其是脯氨酸(Pro)残基上的羟基化修饰)的鉴定不容忽视。如表1所示,4种品牌阿胶中有15个共有特征性多肽(8个来自于α1链,7个来自于α2链)被鉴定出含有羟脯氨酸,在特征性多肽总数中占比83.3%。而且,脯氨酸残基的羟基化修饰情况较为复杂,既有修饰基团的数目不同,也有羟基化修饰位置的不同。例如,表1中有5个特征性多肽均来源于α1链的994GPPGPVGPPGLAGPPGESGR1013,m/z分别为900.95102+、892.95262+、892.95332+、884.95572+和876.95912+,包含的羟脯氨酸残基数量分别为3、2、2、1和0个。由于多肽质谱峰的价态为+2,所以每增加1个羟基化修饰意味着一级质谱峰值增加8 Da。另外,m/z为892.95262+和892.95332+的特征性多肽虽然都含有2个被羟基化的脯氨酸残基,但其修饰基团所处的位置是不同,大大增加了阿胶溯源的难度。有报道指出,脯氨酸残基的羟基化修饰引起的质量改变可能和一些氨基酸(亮氨酸、异亮氨酸)残基的质量差异较为接近,将对鉴定造成较大的干扰[29]。此时,高分辨率质谱仪检测是一种有效增强特征性多肽鉴定准确度的手段。Kleinnijenhuis等[17]报道显示,Orbitrap质量分析器提供的高分辨率能有效区分羟脯氨酸和亮氨酸、异亮氨酸之间的细微差别。在本文中,采用的Orbitrap质量分析器在一级质谱峰m/z 200时分辨率能达到70000,在HCD二级质谱图中m/z 200时分辨率能达到17500,为准确鉴定阿胶、牛明胶和猪明胶的特征性多肽提供了有利保障。
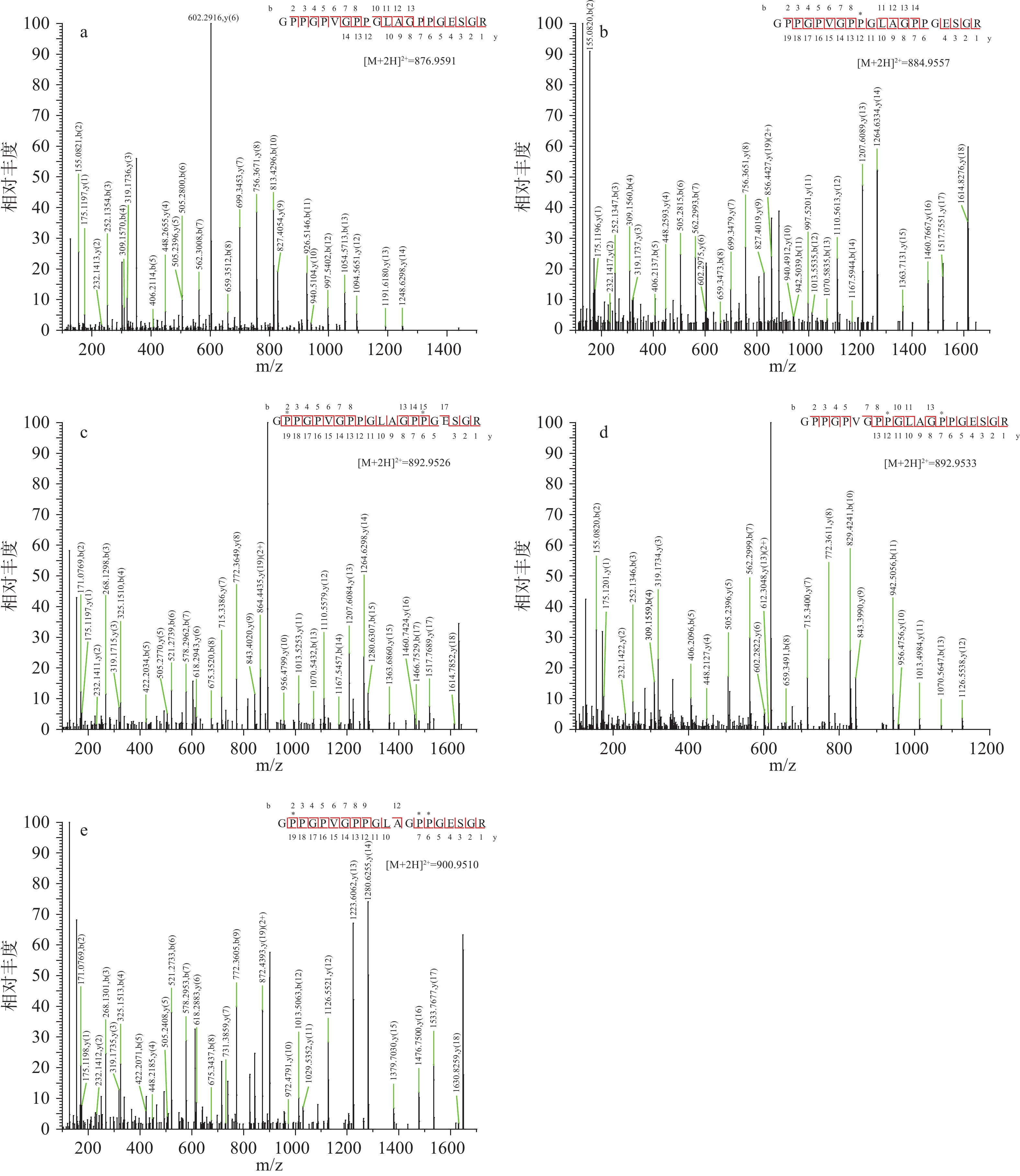
对于不同羟基化修饰水平,以5条来自阿胶共有特征性多肽片段994GPPGPVGPPGLAGPPGESGR1013为例,它们的相对分子质量的实测值与理论值匹配度良好,误差均小于5×10−6。5条阿胶共有特征性多肽二级质谱如图2所示。对于有羟基化修饰的位点,m/z为884.95572+峰值的肽段,通过y12-y11可证实Pro1002被羟基化(图2b);m/z为892.95262+的肽段,Pro995和Pro1008分别可通过y19-y18以及y6-y5被证实为羟脯氨酸残基(图2c);m/z为892.95332+的肽段与m/z为892.95262+的肽段具有相同的羟基化修饰数量,但有不同的羟基化修饰位置,同理,y12-y11与y7-y6分别准确地证实了Pro1002和Pro1007处的羟基化修饰(图2d)。对于具有多个羟基化修饰位点的肽段,m/z为900.95102+峰值的肽段,y19-y18、y7-y6以及y6-y5准确证实了Pro995、Pro1007和Pro1008被羟基化的情况(图2e)。这说明HCD碎裂生成的MS/MS系列y离子和b离子能够准确证实这5条特征性多肽具有相同的氨基酸序列以及不同的羟基化修饰水平。
![]() 图 2 不同羟基化修饰水平的阿胶特征性多肽的质谱鉴定注:a:阿胶α1链中的特征性多肽(R)994GPPGPVGPPGLAGPPGESGR1013(E)(无修饰);b:阿胶α1链中的特征性多肽(R)994GPPGPVGP*PGLAGPPGESGR1013(E)(Pro1002被羟基化);c:阿胶α1链中的特征性多肽(R)994G*PPGPVGPPGLAGP*PGESGR1013(E)(Pro995, Pro1008被羟基化);d:阿胶α1链中的特征性多肽(R)994GPPGPVGP*PGLAG*PPGESGR1013(E)(Pro1002, Pro1007被羟基化);e:阿胶α1链中的特征性多肽(R)994G*PPGPVGPPGLAG*P*PGESGR1013(E)(Pro995, Pro1007和Pro1008被羟基化)。Figure 2. Mass spectrometric identification of characteristic peptides of gelatin with different hydroxylated modification levels
图 2 不同羟基化修饰水平的阿胶特征性多肽的质谱鉴定注:a:阿胶α1链中的特征性多肽(R)994GPPGPVGPPGLAGPPGESGR1013(E)(无修饰);b:阿胶α1链中的特征性多肽(R)994GPPGPVGP*PGLAGPPGESGR1013(E)(Pro1002被羟基化);c:阿胶α1链中的特征性多肽(R)994G*PPGPVGPPGLAGP*PGESGR1013(E)(Pro995, Pro1008被羟基化);d:阿胶α1链中的特征性多肽(R)994GPPGPVGP*PGLAG*PPGESGR1013(E)(Pro1002, Pro1007被羟基化);e:阿胶α1链中的特征性多肽(R)994G*PPGPVGPPGLAG*P*PGESGR1013(E)(Pro995, Pro1007和Pro1008被羟基化)。Figure 2. Mass spectrometric identification of characteristic peptides of gelatin with different hydroxylated modification levels2.3 阿胶块中牛明胶的共有特征性多肽
当阿胶中掺入了牛明胶时,在质谱图中将出现来源于牛明胶肽段的质谱峰。若添加量较低,使用高分辨质谱仪则能有效提高多肽的检出率和准确度。阿胶块中加入低含量的牛明胶,经过HPLC-MS/MS的检测,同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块中分别鉴定出8、10、7和10个牛明胶特征性多肽,其中包含3个牛明胶的共有特征性多肽。如表2所示,特征性多肽序列和修饰情况的判别均来源于一级质谱图和二级质谱图的共同检验,其中,1个共有特征性多肽来自α1链,2个共有特征性多肽则源自α2链,所有质谱峰的误差值均<5×10−6,说明这3个共有特征性多肽鉴定的准确度高,可用于阿胶块产品中低含量牛明胶的鉴定分析。如上所述,未经修饰的多肽片段在明胶鉴别中备受关注。由表2可知,在牛明胶的3个共有特征性多肽中有1个源自α1链的特征性多肽不包含任何修饰情况,其序列为1066GETGPAGPAGPIGPVGAR1083,m/z为780.91352+。这个特征性多肽在文献中已多次被报道在牛明胶中检出,如Kleinnijenhuis等[17]在猪明胶中掺入低含量的牛明胶,成功检测出此特征性多肽并用于定量研究;Yilmaz等[28]将牛明胶掺入三种乳制品(酸奶、奶酪和冰淇淋)中,利用超高效液相色谱-质谱联用技术检出了35条牛明胶特征性多肽,这条多肽包含其中;Grundy等[30]报道了14条牛明胶特征性多肽,其中含有这条特征多肽;课题组前期在纯的牛明胶以及不同比例的牛明胶、猪明胶和阿胶的混合体系中,以及18O标记定量检测猪明胶和牛明胶的实验中也检出了此特征性多肽[20,31],表明其用于牛明胶的溯源鉴定中具有较高的稳定性。
表 2 牛明胶的共有特征性多肽Table 2. Common characteristic peptides of bovine gelatin牛明胶的特征多肽序列 m/z 相对分子质量 实测值 理论值 误差(×10−6) α1: (R)1066GETGPAGPAGPIGPVGAR1083(G) 780.91352+ 1559.8124 1559.8056 4.37 α2: (R)326GI*PGPVGAAGATGAR340(G) 634.34392+ 1266.6732 1266.6680 4.07 α2: (R)590GP*PGESGAAGPTGPIGSR607(G) 790.89032+ 1579.7660 1579.7590 4.41 2.4 阿胶块中猪明胶的共有特征性多肽
猪明胶是工业领域使用最多的食用明胶,同时在阿胶产品中也多次被曝光掺入了猪明胶[32-33]。因而,本文进一步研究了阿胶块中低含量猪明胶的特征性多肽。结合图1c和表3可知,同仁堂阿胶块、福牌阿胶块、东阿阿胶块和九芝堂阿胶块中鉴定出的猪明胶特征性多肽比牛明胶特征性多肽数量更多,分别为12、16、11和16个,其中5个为阿胶块中猪明胶的共有特征性多肽(1个共有特征性多肽是来自α1链,4个共有特征性多肽则源自α2链),其各个特征性多肽的误差值均<5×10−6,且均经过一、二级质谱的准确判定,其可信度高,可用于阿胶块产品中低含量猪明胶的鉴定分析。在上述5个猪明胶的共有特征性多肽中,有1个源自α1链的特征性多肽不包含任何修饰情况,其序列为1052GETGPAGPAGPVGPVGAR1069,m/z为773.90602+。同样,此猪明胶特征性多肽多次被报道在纯明胶或混合明胶中被检出,如Yilmaz等[28]在乳制品中掺入猪明胶,结果检出了54条猪明胶特征性多肽,其中包含这条特征性多肽;Grundy等[30]报道的5条猪明胶特征性多肽中亦含有这条特征多肽;同时,课题组在前期检测纯的猪明胶和混合明胶体系,以及18O标记定量检测猪明胶的特征性多肽的研究中也发现了这条特征多肽[20,22],表明其稳定性较高,在猪明胶的溯源中可发挥十分重要的作用。
表 3 猪明胶的共有特征性多肽Table 3. Common characteristic peptides of porcine gelatin猪明胶的特征多肽序列 m/z 相对分子质量 实测值 理论值 误差(×10−6) α1: (R)1052GETGPAGPAGPVGPVGAR1069(G) 773.90602+ 1545.7974 1545.7900 4.82 α2: (R)979GE*PGPAGSVGPAGAVGPR996(G) 774.89562+ 1547.7766 1547.7692 4.77 α2: (R) 574GI*PGEFGL*PG*PAGPR588 (G) 735.37572+ 1468.7368 1468.7310 3.92 α2: (R)574GI*PGEFGL*PGPAGPR588(G) 727.37852+ 1452.7424 1452.7361 4.32 α2: (R)382GPNGEVGSAGP*PGP*PGLR399(G) 824.41152+ 1646.8084 1646.8013 4.34 综合表1、表2和表3可知,如不考虑氨基酸残基修饰的情况,从4种阿胶块中检出阿胶、牛明胶和猪明胶的共有特征性多肽片段数量分别为10、3、4个,其中来自α1链的数目分别为4、1、1个,来自α2链的数目分别为6、2、3个。以上结果表明,不论阿胶、牛明胶或是猪明胶,α2链检出的特征性多肽片段均高于α1链,这主要是由于在驴皮、牛皮和猪皮胶原蛋白中,α2链的差异性大于α1链。前期研究表明,对于α1链,牛-猪、牛-驴和猪-驴胶原蛋白的相似度分别为95.9%、96.6%和95.3%;对于α2链,牛-猪、牛-驴和猪-驴胶原蛋白的相似度分别为95.3%、94.9%和94.7%[20]。因此,与α1链相比,稍高的差异使得α2链经过明胶制备、酶解等工序后能游离出更多被质谱检测到的特征性多肽片段。
3. 结论
本文以最受消费者青睐的阿胶块为原料,向其中分别加入低含量(1 mg/mL)的牛明胶和猪明胶,采用HPLC-MS/MS分别鉴定阿胶、牛明胶和猪明胶的特征性多肽。结果表明,不同品牌的阿胶块产品被检出的阿胶特征性多肽数目有所不同,其中18个特征性多肽为4种不同品牌阿胶块的共有特征性多肽,对阿胶块产品中阿胶成分的溯源鉴定具有十分重要的意义。当加入低含量的牛明胶和猪明胶时,在阿胶块中检测出3个牛明胶的共有特征性多肽和5个猪明胶的共有特征性多肽,这些稳定检出的特征性多肽可作为阿胶块中低含量牛明胶和猪明胶掺假的鉴定依据。该研究结果可为阿胶块产品的质量监管提供一定的理论依据。本文以阿胶块为原料开展了掺假鉴定研究,然而,其他产品(如阿胶口服液、阿胶糕等)的明胶溯源鉴定同样值得关注,后续将对其他类型的阿胶产品开展溯源研究,为阿胶产品的质量控制提供依据。
-
图 1 阿胶块中阿胶、牛明胶和猪明胶特征性多肽组成的差异性分析
注:(1):同仁堂阿胶块;(2):福牌阿胶块;(3):东阿阿胶块;(4):九芝堂阿胶块;a:阿胶块中阿胶的特征性多肽组成的差异性分析;b:阿胶块中牛明胶的特征性多肽组成的差异性分析;c:阿胶块中猪明胶的特征性多肽组成的差异性分析。
Figure 1. Differential analysis of the characteristic peptides composition of donkey-hide gelatin, bovine gelatin and porcine gelatin in donkey-hide gelatin lumps
图 2 不同羟基化修饰水平的阿胶特征性多肽的质谱鉴定
注:a:阿胶α1链中的特征性多肽(R)994GPPGPVGPPGLAGPPGESGR1013(E)(无修饰);b:阿胶α1链中的特征性多肽(R)994GPPGPVGP*PGLAGPPGESGR1013(E)(Pro1002被羟基化);c:阿胶α1链中的特征性多肽(R)994G*PPGPVGPPGLAGP*PGESGR1013(E)(Pro995, Pro1008被羟基化);d:阿胶α1链中的特征性多肽(R)994GPPGPVGP*PGLAG*PPGESGR1013(E)(Pro1002, Pro1007被羟基化);e:阿胶α1链中的特征性多肽(R)994G*PPGPVGPPGLAG*P*PGESGR1013(E)(Pro995, Pro1007和Pro1008被羟基化)。
Figure 2. Mass spectrometric identification of characteristic peptides of gelatin with different hydroxylated modification levels
表 1 阿胶的共有特征性多肽
Table 1 Common characteristic peptides of donkey-hide gelatin
阿胶的特征多肽序列 m/z 相对分子质量 实测值 理论值 误差(×10−6) α1: (K)835GDAG*PPGPAGPAGPPG*PIGSVGA*PG*PK861(G) 1148.56672+ 2295.1188 2295.1132 2.45 α1: (K)835GDAG*PPGPAGPAGPPGPIGSVGA*PG*PK861 (G) 1140.57072+ 2279.1268 2279.1183 3.75 α1: (K)835GDAGPPGPAGPAGPPGPIGSVGA*PGPK861 (G) 1124.57592+ 2247.1372 2247.1284 3.91 α1: (R)1066GEAGPAGPAGPIGPVGAR1083(G) 765.90822+ 1529.8018 1529.7950 4.43 α1: (R)472GE*PGPTGL*PGP*PGER486(G) 733.35162+ 1464.6886 1464.6845 2.81 α1: (R)994G*PPGPVGPPGLAG*P*PGESGR1013 (E) 900.95102+ 1799.8874 1799.8802 3.98 α1: (R)994G*PPGPVGPPGLAGP*PGESGR1013 (E) 892.95262+ 1783.8906 1783.8853 2.96 α1: (R)994GPPGPVGP*PGLAG*PPGESGR1013 (E) 892.95332+ 1783.8920 1783.8853 3.74 α1: (R)994GPPGPVGP*PGLAGPPGESGR1013 (E) 884.95572+ 1767.8968 1767.8904 3.62 α1: (R)994GPPGPVGPPGLAGPPGESGR1013(E) 876.95912+ 1751.9036 1751.8955 4.63 α2: (R)829AGETGASGP*PGFAGEK844(G) 724.83842+ 1447.6622 1447.6579 2.96 α2: (R)776GDGGP*PGVTGF*PGAAGR792 (T) 751.35712+ 1500.6996 1500.6958 2.57 α2: (R)776GDGGPPGVTGF*PGAAGR792(T) 743.36082+ 1484.7070 1484.7008 4.16 α2: (R)977GE*PGPVGSVGPVGAVGPR994 (G) 802.92662+ 1603.8386 1603.8318 4.21 α2: (R)977GEPG*PVGSVGPVGAVGPR994(G) 802.92702+ 1603.8394 1603.8318 4.71 α2: (R)881GL*PGVAGSLGE*PGPLGIAGP*PGAR904(G) 1073.07302+ 2144.1314 2144.1226 4.11 α2: (R)1052GPAGPTGPVGK1062(D) 469.26022+ 936.5058 936.5029 3.12 α2: (R)793TG*P*PGPSGISGPPG*P*PGAAGK813(E) 910.44812+ 1818.8816 1818.8748 3.73 注:*P为羟基化的脯氨酸;表2~表3同。 表 2 牛明胶的共有特征性多肽
Table 2 Common characteristic peptides of bovine gelatin
牛明胶的特征多肽序列 m/z 相对分子质量 实测值 理论值 误差(×10−6) α1: (R)1066GETGPAGPAGPIGPVGAR1083(G) 780.91352+ 1559.8124 1559.8056 4.37 α2: (R)326GI*PGPVGAAGATGAR340(G) 634.34392+ 1266.6732 1266.6680 4.07 α2: (R)590GP*PGESGAAGPTGPIGSR607(G) 790.89032+ 1579.7660 1579.7590 4.41 表 3 猪明胶的共有特征性多肽
Table 3 Common characteristic peptides of porcine gelatin
猪明胶的特征多肽序列 m/z 相对分子质量 实测值 理论值 误差(×10−6) α1: (R)1052GETGPAGPAGPVGPVGAR1069(G) 773.90602+ 1545.7974 1545.7900 4.82 α2: (R)979GE*PGPAGSVGPAGAVGPR996(G) 774.89562+ 1547.7766 1547.7692 4.77 α2: (R) 574GI*PGEFGL*PG*PAGPR588 (G) 735.37572+ 1468.7368 1468.7310 3.92 α2: (R)574GI*PGEFGL*PGPAGPR588(G) 727.37852+ 1452.7424 1452.7361 4.32 α2: (R)382GPNGEVGSAGP*PGP*PGLR399(G) 824.41152+ 1646.8084 1646.8013 4.34 -
[1] 韩晶. 阿胶通过抵抗免疫细胞凋亡起到免疫保护的作用[D]. 北京: 北京协和医学院, 2018. HAN J. The traditional Chinese medicine Ejiao is an immunoprotective agent against apoptosis[D]. Beijing: Peking Union Medical College, 2018.
[2] 刘艳艳, 董书光, 耿加亮, 等. 阿胶加工工艺过程中DNA降解规律研究[J]. 药学研究,2016,35(9):501−507. [LIU Y Y, DONG S G, GENG J L, et al. DNA degradation of Colla Corii Asini during processing[J]. Journal of Pharmaceutical Research,2016,35(9):501−507. [3] 朱茜. 预见2021: 《2020年中国阿胶产业全景图谱》(附市场规模、竞争情况、发展趋势等)[EB/OL]. (2021-01-13) [2021-3-10].https://www.qianzhan.com/analyst/detail/220/210113-de40df84.html. ZHU Q. Forecast of 2021: Panorama of China Ejiao industry in 2020 (with market size, competition, development trend, etc.)[EB/OL]. (2021-01-13) [2021-3-10]. https://www.qianzhan.com/analyst/detail/220/210113-de40df84.html.
[4] 王思婷. 预见2019: 《2019年中国阿胶产业全景图谱》: 行业门槛逐步提高 阿胶产品价格将进入调整期[EB/OL]. (2019-05-07) [2020-12-21]. https://www.qianzhan.com/analyst/detail/220/190506-abd58d3c.html. WANG S T. Forecast of 2019: Panorama of China Ejiao industry in 2019: The industry threshold gradually increases and the price of EJiao products will enter the adjustment period[EB/OL]. (2019-05-07) [2020-12-21]. https://www.qianzhan.com/analyst/detail/220/190506-abd58d3c.html.
[5] 沙小梅, 胡姿姿, 涂宗财, 等. 18O标记联合高效液相色谱-高分辨率质谱技术定量测定阿胶中的明胶[J]. 食品科学,2018,39(12):288−294. [SHA X M, HU Z Z, TU Z C, et al. Quantification of gelatin in donkey-hide gelatin by oxygen-18 labelling and high performance liquid chromatography linear ion trap/orbitrap high resolution mass spectrometry[J]. Food Science,2018,39(12):288−294. doi: 10.7506/spkx1002-6630-201812044 [6] 乔琰. 动物皮中脂溶性成分的指纹图谱研究[D]. 天津: 天津科技大学, 2015. QIAO Y. Study on fingerprints of liposoluble constituents in several animals[D]. Tianjin: Tianjin University of Science and Technology, 2015.
[7] 那丽丹. 代谢组学技术在阿胶原料及其产品质量控制中的应用初探[D]. 太原: 山西大学, 2015. NA L D. Application of metabolomics in quality control of raw materials and products of gelatin[D]. Taiyuan: Shanxi University, 2015.
[8] CEBI N, DOGAN C E, MESE A E, et al. A rapid ATR-FTIR spectroscopic method for classification of gelatin gummy candies in relation to the gelatin source[J]. Food Chemistry,2019,277:373−381. doi: 10.1016/j.foodchem.2018.10.125
[9] YAP B K, GAM L. Differentiation of bovine from porcine gelatin capsules using gel electrophoresis method[J]. Food Chemistry,2019,274:16−19. doi: 10.1016/j.foodchem.2018.08.111
[10] ABDULLAH AMQIZAL H I, AL-KAHTANI H A, ISMAIL E A, et al. Identification and verification of porcine DNA in commercial gelatin and gelatin containing processed foods[J]. Food Control,2017,78:297−303. doi: 10.1016/j.foodcont.2017.02.024
[11] LEE J H, KIM M R, JO C H, et al. Specific PCR assays to determine bovine, porcine, fish and plant origin of gelatin capsules of dietary supplements[J]. Food Chemistry,2016,211:253−259. doi: 10.1016/j.foodchem.2016.05.060
[12] TUKIRAN N A, ISMAIL A, MUSTAFA S, et al. Development of antipeptide enzyme-linked immunosorbent assay for determination of gelatin in confectionery products[J]. International Journal of Food Science & Technology,2016,51(1):54−60.
[13] TUKIRAN N A, ISMAIL A, MUSTAFA S, et al. Determination of porcine gelatin in edible bird's nest by competitive indirect ELISA based on anti-peptide polyclonal antibody[J]. Food Control,2016,59:561−566. doi: 10.1016/j.foodcont.2015.06.039
[14] WARD S, POWLES N T, PAGE M I. Peptide biomarkers for identifying the species origin of gelatin using coupled UPLC-MS/MS[J]. Journal of Food Composition and Analysis,2018,73:83−90. doi: 10.1016/j.jfca.2018.08.002
[15] FLAUDROPS C, ARMSTRONG N, RAOULT D, et al. Determination of the animal origin of meat and gelatin by MALDI-TOF-MS[J]. Journal of Food Composition and Analysis,2015,41:104−112. doi: 10.1016/j.jfca.2015.02.009
[16] JANNAT B, GHORBANI K, SHAFIEYAN H, et al. Gelatin speciation using real-time PCR and analysis of mass spectrometry-based proteomics datasets[J]. Food Control,2018,87:79−87. doi: 10.1016/j.foodcont.2017.12.006
[17] KLEINNIJENHUIS A J, VAN HOLTHOON F L, HERREGODS G. Validation and theoretical justification of an LC-MS method for the animal species specific detection of gelatin[J]. Food Chemistry,2018,243:461−467. doi: 10.1016/j.foodchem.2017.09.104
[18] CHENG X L, WEI F, XIAO X Y, et al. Identification of five gelatins by ultra performance liquid chromatography/time-of-flight mass spectrometry (UPLC/Q-TOF-MS) using principal component analysis[J]. Journal of Pharmaceutical and Biomedical Analysis,2012,62(2):191−195.
[19] 焦阳, 汪冰, 周倩倩, 等. 超高效液相色谱-质谱联用技术检测阿胶中马皮源成分[J]. 药物分析杂志,2019,39(5):864−869. [JIAO Y, WANG B, ZHOU Q Q, et al. Petection of equine-hide gelatin in Ejiao by UPLC-MS[J]. Chinese Journal of Pharmaceutical Analysis,2019,39(5):864−869. [20] SHA X M, HU Z Z, TU Z C, et al. The identification of three mammalian gelatins by liquid chromatography-high resolution mass spectrometry[J]. LWT - Food Science and Technology,2018,89:74−86. doi: 10.1016/j.lwt.2017.10.001
[21] 陆澜清. 2018年阿胶行业竞争现状与趋势分析 成本压力推动多元化发展[EB/OL]. (2018-05-04) [2020-12-24]. https://www.qianzhan.com/analyst/detail/220/180504-da15be21.html. LU L Q. Analysis of competition status and trend of Ejiao industry in 2018 cost pressure promotes diversified development[EB/OL]. (2018-05-04) [2020-12-24]. https://www.qianzhan.com/analyst/detail/220/180504-da15be21.html.
[22] SHA X M, HU Z Z, YE Y H, et al. Effect of extraction temperature on the gelling properties and identification of porcine gelatin[J]. Food Hydrocolloids,2019,92:163−172. doi: 10.1016/j.foodhyd.2019.01.059
[23] ZHANG Q T, TU Z C, WANG H, et al. Improved glycation after ultrasonic pretreatment revealed by high-performance liquid chromatography-linear ion Trap/Orbitrap high-resolution mass spectrometry[J]. Journal of Agricultural and Food Chemistry,2014,62(12):2522−2530. doi: 10.1021/jf5002765
[24] SCHRIEBER R, GAREIS H. Gelatine handbook: Theory and industrial practice[M]. Weinheim: Wiley-VCH, 2007.
[25] LIN S, SAMUEL W, MICHELLE G C, et al. Stable-isotope-labeled histone peptide library for histone post-translational modification and variant quantification by mass spectrometry[J]. Molecular & Cellular Proteomics,2014,13(9):2450−2466.
[26] SHA X M, WANG G Y, LI X, et al. Identification and quantification of gelatin by a high-resolution mass spectrometry-based label-free method[J]. Food Hydrocolloids, 2020, 101: 105476.
[27] WU L C, WANG S X, TIAN L, et al. Comparative proteomic analysis of the maize responses to early leaf senescence induced by preventing pollination[J]. Journal of Proteomics,2018,177:75−87. doi: 10.1016/j.jprot.2018.02.017
[28] YILMAZ M T, KESMEN Z, BAYKAL B, et al. A novel method to differentiate bovine and porcine gelatins in food products: NanoUPLC-ESI-Q-TOF-MSE based data independent acquisition technique to detect marker peptides in gelatin[J]. Food Chemistry,2013,141(3):2450−2458. doi: 10.1016/j.foodchem.2013.05.096
[29] ZHANG G F, LIU T, WANG Q, et al. Mass spectrometric detection of marker peptides in tryptic digests of gelatin: A new method to differentiate between bovine and porcine gelatin[J]. Food Hydrocolloids,2009,23(7):2001−2007. doi: 10.1016/j.foodhyd.2009.03.010
[30] GRUNDY H H, REECE P, BUCKLEY M, et al. A mass spectrometry method for the determination of the species of origin of gelatine in foods and pharmaceutical products[J]. Food Chemistry,2016,190:276−284. doi: 10.1016/j.foodchem.2015.05.054
[31] SHA X M, TU Z C, WANG H, et al. Gelatin quantification by oxygen-18 labeling and liquid chromatography-high-resolution mass spectrometry[J]. Journal of Agricultural and Food Chemistry,2014,62(49):11840−11853. doi: 10.1021/jf503876a
[32] CEBI N, DURAK M Z, TOKER O S, et al. An evaluation of fourier transforms infrared spectroscopy method for the classification and discrimination of bovine, porcine and fish gelatins[J]. Food Chemistry,2016,190:1109−1115. doi: 10.1016/j.foodchem.2015.06.065
[33] KANG S S N, LEE H G, KIM H. Development and comparison of a porcine gelatin detection system targeting mitochondrial markers for Halal authentication[J]. LWT-Food Science and Technology,2018,97:697−702. doi: 10.1016/j.lwt.2018.07.062
-
期刊类型引用(3)
1. 李亚俐,王雪莉,石柳,吴文锦,陈胜,陈朗,郭晓嘉,熊光权,汪兰,孙智达. 壳聚糖-绿原酸复合保鲜剂对冷藏鮰鱼片食用品质的影响. 肉类研究. 2025(01): 42-50 .  百度学术
百度学术
2. 武玫怡,焦文娟,赵甜甜,刘俊,周芳,刘伟峰,张业辉,南海军,陈晓瑛,黄利华. 高静水压与水煮处理对热带海参品质的影响. 肉类研究. 2025(01): 25-33 .  百度学术
百度学术
3. 崔燕,刘韩欣,朱麟,尚海涛,林旭东,陈曙颖,宣晓婷. 超高压杀菌对大黄鱼理化性质及滋味、风味的影响. 食品工业科技. 2025(05): 44-55 .  本站查看
本站查看
其他类型引用(3)





 下载:
下载:
 下载:
下载:



