Ethanol-ammonium Sulfate Aqueous Two-phase Extraction of Total Flavonoids from Peach Blossom and Its Antioxidant Activity
-
摘要: 以桃花为主要原料,采用乙醇-硫酸铵双水相体系进行总黄酮提取工艺研究。在单因素实验基础上,以硫酸铵质量分数、液料比、提取温度、提取时间这4个因素作为自变量,以黄酮得率为指标,通过响应面法对桃花总黄酮提取工艺进行优化。以DPPH·、OH·和O2−·清除率为指标,对桃花总黄酮的抗氧化能力进行评价。结果表明,黄酮提取的最佳工艺参数为:硫酸铵质量分数15.2%,提取时间26 min,液料比27.8:1(mL/g),提取温度51 ℃。在此条件下,黄酮得率理论值可达45.64%,验证值为45.65%,与理论值十分接近。抗氧化实验结果表明,桃花总黄酮表现出较强的自由基清除能力,当浓度为0.56 mg/mL时,DPPH·清除率为94.21%,当浓度为0.672 mg/mL时,OH·和
-
Keywords:
- peach blossom /
- flavonoid /
- aqueous two-phase extraction /
- response surface analysis /
- antioxidation
-
桃花是蔷薇科落叶乔木桃树的花,具有美容养颜和保健之功效,在食药领域应用广泛。研究表明,桃花中含有黄酮、多酚、多糖、类胡萝卜素、多种维生素、氨基酸及微量元素等多种化学成分[1-3],营养与药用价值较高。黄酮类化合物具有抗肿瘤、抗炎镇痛、免疫调节、降血糖、治疗骨质疏松、抗辐射等多种药理作用[4-6],工业应用前景广阔。根据文献报道[2,7],桃花中含有阿福豆苷(afzelin)、槲皮苷(quercitrin)、柚皮素(naringenin)以及三叶豆苷(trifolin)等多种黄酮化合物,说明桃花中黄酮类物质丰富[8]。
近年来,学者们主要采用以乙醇为溶剂的浸提法[7-8],并结合超声波辅助[9]、大孔树脂纯化[10]以及索氏提取[11]等方法,研究了桃花总黄酮的提取工艺。双水相提取技术是一种新型的萃取分离技术[12],根据物质在互不相溶两相间溶解性的差异,实现目标成分的萃取和分离,被广泛用于生物化学和生物化工产品的分离纯化[13]。目前,双水相萃取技术已有效应用于黄酮类化合物[14-16]等天然产物的提取。但双水相体系在桃花总黄酮中的提取研究尚未见报道。
因此,本研究采用乙醇-硫酸铵双水相体系提取桃花总黄酮,以黄酮的得率为指标,考察了硫酸铵质量分数、液料比、提取温度、提取时间等因素的影响,采用响应面分析法优化了提取工艺,并研究了黄酮提取物的抗氧化活性,以期为桃花的综合利用以及黄酮化合物等天然产物的深度开发提供科学依据。
1. 材料与方法
1.1 材料与仪器
桃花 产地为安徽省亳州市;芦丁上海阿拉丁生化科技股份有限公司;无水乙醇、硫酸铵、九水合硝酸铝、亚硝酸钠、氢氧化钠、七水合硫酸亚铁、1,1-二苯基-2-三硝基苯肼(DPPH)、水杨酸 分析纯,国药集团化学试剂有限公司;双氧水(30%质量浓度) 上海凌峰化学试剂有限公司;邻苯三酚、三羟甲基氨基甲烷(Tris)、抗坏血酸(VC) 上海麦克林生化科技有限公司;浓盐酸 西陇科学股份有限公司;蒸馏水 实验室自制。
CPA225D分析天平 德国赛多利斯集团公司;DF-101S集热式恒温加热磁力搅拌器 上海力辰邦西仪器科技有限公司;DZF型真空干燥箱 上海精宏实验设备有限公司;SK220H型超声波清洗器 上海科导超声仪器有限公司;TDZ5-WS式低速自动平衡离心机 长沙湘智离心机仪器有限公司;UV-1800PC型紫外可见分光光度计 上海美谱达仪器有限公司。
1.2 实验方法
1.2.1 桃花原料预处理
将桃花剥去花托和萼片,置于真空干燥箱(60 ℃,2 h)烘干,然后放入研钵中研磨至粉状,过60目筛。过筛后的桃花粉末避光冷藏(8 ℃)。
1.2.2 乙醇-硫酸铵双水相体系相图制作
用Albertson浊点法[17]测定并制作乙醇-硫酸铵体系相图。准确称取4.5 g硫酸铵于锥形瓶中,加入10 mL蒸馏水,用玻璃棒搅拌至硫酸铵完全溶解,静置。用滴定管向锥形瓶中缓慢滴加无水乙醇并震荡锥形瓶,直到混合溶液出现浑浊为止,记录此时消耗的无水乙醇体积。用滴定管向上述混合体系中滴加蒸馏水并振荡锥形瓶,直至体系重新变为澄清状态,记录此时消耗的蒸馏水体积。不断重复上述操作,记录所加入的乙醇体积和水体积,计算状态改变时体系中硫酸铵和乙醇的质量分数,并绘制双水相相图。
1.2.3 桃花总黄酮提取工艺
乙醇-硫酸铵双水相提取桃花总黄酮工艺如下[15]:准确称取一定量硫酸铵,置于烧杯中,并加入适量的乙醇溶液(质量分数为40%),在超声作用下,搅拌至颗粒完全溶解,静置直到溶液分相。按液料比准确称取一定量的桃花粉末,加入烧杯中,在恒温加热磁力搅拌器上加热一定时间后,倒入10 mL的离心管中,并在2500 r/min的条件下离心5 min,取上相澄清液作为待测液。
1.2.4 桃花总黄酮的测定
实验以芦丁为标准品,采用NaNO2-Al(NO3)3-NaOH显色法,选用510 nm为检测波长,测定桃花中总黄酮[18]。
1.2.4.1 芦丁标准曲线的绘制
称取10 mg芦丁于50 mL容量瓶中,加无水乙醇溶解,用60%浓度的乙醇定容至刻度,摇匀后,得到质量浓度为0.2 mg/mL的芦丁标准溶液。取6只标记好的10 mL容量瓶,分别加入0、1、2、3、4、5 mL芦丁标准溶液,加水至5 mL,加入5%的亚硝酸钠溶液0.3 mL,摇匀后静置5 min,加入10%的硝酸铝溶液0.3 mL,摇匀后静置6 min,再加入4%的氢氧化钠溶液2 mL,加水稀释至刻度线,摇匀后静置10min。以第一管为对照组,在510 nm处测定吸光度值。以浓度为横坐标、吸光度值为纵坐标绘制标准曲线。得到芦丁浓度与吸光度的线性回归方程:y=8.92857x+0.00429,R2=0.999。
1.2.4.2 桃花总黄酮得率测定
准确吸取2.5 mL待测液,置于100 mL容量瓶中,加蒸馏水稀释至刻度线,摇匀,静置,并从中准确吸取2.5 mL加入25 mL容量瓶中。然后,加入5%的亚硝酸钠溶液1 mL,摇匀,静置6 min,溶液无明显变化;再加入10%的硝酸铝溶液1 mL,摇匀,静置6 min,溶液变棕黄色;再加入4%的氢氧化钠溶液10 mL,溶液变为酒红色,加水定容至25 mL,摇匀,静置15 min。然后测定吸光度。
根据芦丁标准曲线,测量提取液中的黄酮浓度,然后根据式(1)计算桃花总黄酮得率。
Y=C×V×nm×100 (1) 式中:C—上相提取液的黄酮浓度,mg/mL;V—上相提取液的体积,mL;n—稀释倍数;m—称取的桃花粉末质量,mg;Y—桃花总黄酮得率,%。
1.2.5 单因素实验
硫酸铵质量分数对黄酮得率的影响:按照1.2.3的方法,固定液料比为35:1(mL/g),提取温度为50 ℃,提取时间为30 min,分别设置硫酸铵的质量分数为11%、13%、15%、17%、19%,检测黄酮得率。
液料比对黄酮得率的影响:按照1.2.3的方法,固定硫酸铵质量分数为15%,提取温度为50 ℃,提取时间为30 min,分别设置液料比为20:1、25:1、30:1、35:1、40:1(mL/g),检测黄酮得率。
提取温度对黄酮得率的影响:按照1.2.3的方法,固定硫酸铵质量分数为15%,液料比为30:1(mL/g),提取时间为30 min,分别设置提取温度为30、40、50、60、70 ℃,检测黄酮得率。
提取时间对黄酮得率的影响:按照1.2.3的方法,固定硫酸铵质量分数为15%,液料比为30:1(mL/g),提取温度为50 ℃,分别设置提取时间为15、20、25、30、35 min,检测黄酮得率。
1.2.6 响应曲面试验设计
在单因素实验基础上,进行响应曲面试验设计,选择硫酸铵质量分数、提取时间、液料比、提取温度这4个因素作为自变量,以黄酮得率为响应值。运用Box-Bchnken中心组合设计方案[19],利用Design-Expert8.0软件对实验数据进行回归分析。实验因素水平见表1。
表 1 响应面分析试验因素水平Table 1. Code and level of factors for the response surface analysis experiment因素 水平 −1 0 1 A硫酸铵质量分数(%) 13 15 17 B液料比(mL·g−1) 20:1 25:1 30:1 C提取温度(℃) 45 50 55 D提取时间(min) 20 25 30 1.2.7 抗氧化实验研究
通过对DPPH·、OH·、以及
O−2⋅ 自由基的清除能力测定实验,并分别以VC为对照,研究桃花总黄酮的抗氧化性能。1.2.7.1 样品溶液制备
按照1.2.6的方法所选出的优化条件,提取桃花总黄酮,然后加入一定量的无水乙醇稀释,得到黄酮质量浓度为0.112、0.224、0.336、0.448、0.56、0.672 mg/mL的待测样品溶液,分别记为1、2、3、4、5、6号,密闭冷藏(8 ℃)。
1.2.7.2 桃花总黄酮对DPPH·清除能力
参考文献[20]方法,并稍作修改。用80%的乙醇溶液配制0.15 mmol/L的DPPH溶液100 mL,避光保存。分别吸取1、2、3、4、5、6号样品溶液各2 mL,置于10 mL的离心管中,各加入DPPH溶液2 mL,摇匀后,静置30 min。同时,以无水乙醇代替DPPH溶液,作为对照组;以无水乙醇代替待测液,作为空白组。均在517 nm处测定吸光度,并根据式(2)计算自由基清除率。
I=(1−Ai−AjA0)×100 (2) 式中:I—自由基清除率,%;A0—加入DPPH溶液和无水乙醇的吸光度;Ai—加入DPPH溶液和粗提液的吸光度;Aj—加入无水乙醇和粗提液的吸光度。
1.2.7.3 桃花总黄酮对OH·清除能力
参考文献[21]方法,并稍作修改。精确吸取9 mmol/L的硫酸亚铁溶液2 mL,置于10 mL的离心管中,然后分别加入1、2、3、4、5、6号样品溶液各2 mL,再分别加入9 mmol/L水杨酸溶液2 mL和8.8 mmol/L的双氧水溶液2 mL,摇匀后,静置30 min。同时,以蒸馏水代替双氧水溶液,作为对照组;以蒸馏水代替待测液,作为空白组。均在510 nm处测定吸光度,根据式(2)计算自由基清除率。
1.2.7.4 桃花总黄酮对
O−2 ·的清除能力参考文献[22]方法,并稍作修改。精确吸取pH为8.2、浓度为50 mmol/L的Tris-HCl缓冲液4.5 mL,置于10 mL的离心管中,在25 ℃的水浴中放置20 min,然后分别加入1、2、3、4、5、6号样品溶液各2 mL,再加入25 mmol/L的邻苯三酚溶液0.4 mL,摇匀后,静置,在25 ℃的条件下反应4 min,随后立即滴加8 mol/L的盐酸溶液2滴。同时,以蒸馏水代替邻苯三酚溶液,作为对照组;以蒸馏水代替待测液,作为空白组。均在320 nm处测定吸光度,根据式(2)计算自由基清除率。
1.3 数据处理
采用Origin数据处理软件进行单因素实验数据分析和图表制作,采用Design-Expert 8.0软件进行响应面试验设计分析。
2. 结果与分析
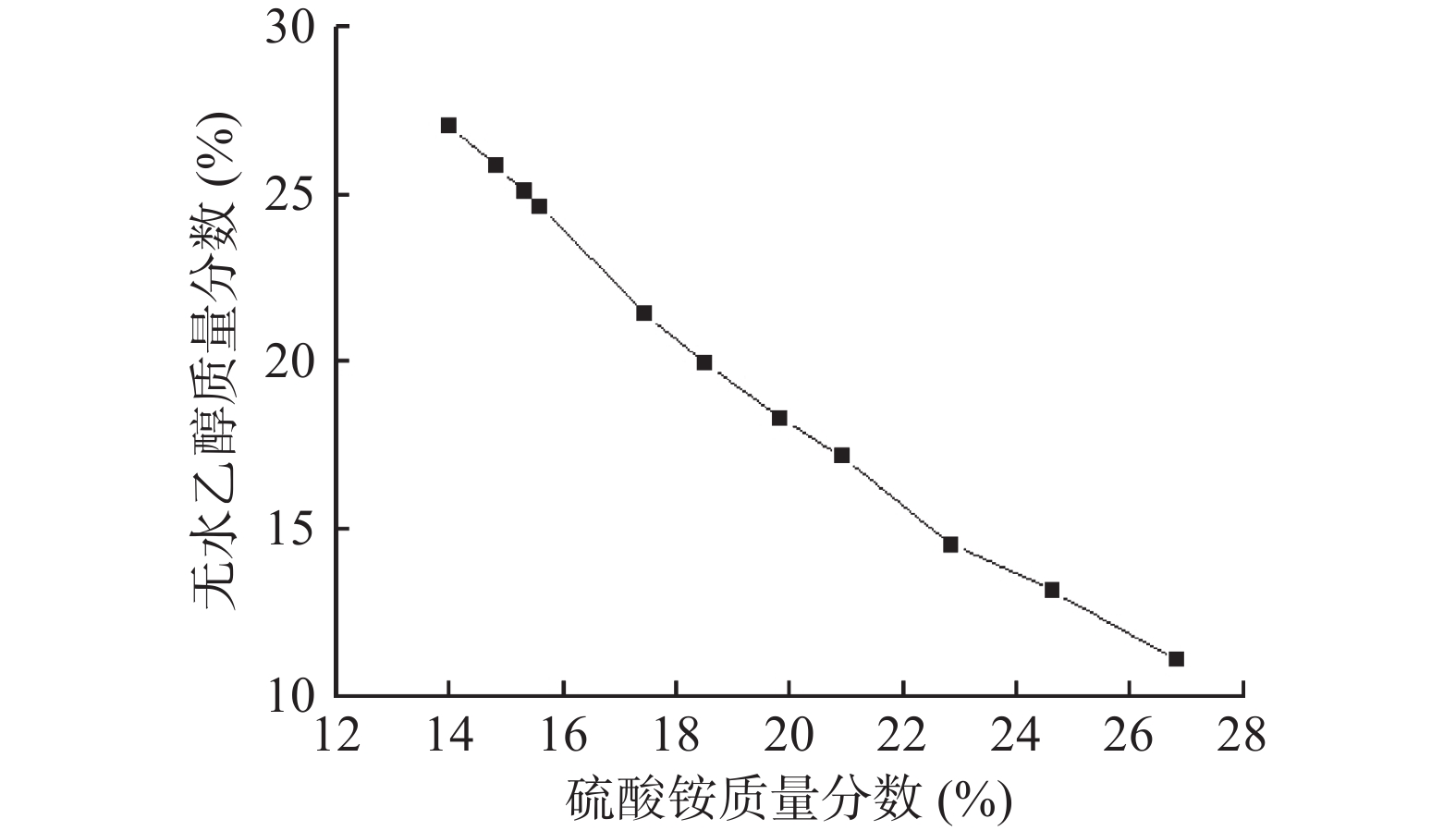
2.1 乙醇-硫酸铵双水相体系相图
乙醇-硫酸铵双水相体系相图如图1所示。曲线上的点为临界点,在曲线上方为两相区,其中上相为富乙醇相,而下相则为富盐相,黄酮类物质多具有二苯基色原酮的黄酮母体结构,极性较小,从而富集于上相[15],而如多糖等极性较大的物质则多富集于下相,因而可使桃花中的黄酮得以分离。因此,在实验时,乙醇和硫酸铵的质量分数应落于曲线之上,并取上相澄清液作为待测液进行研究。
2.2 单因素实验结果
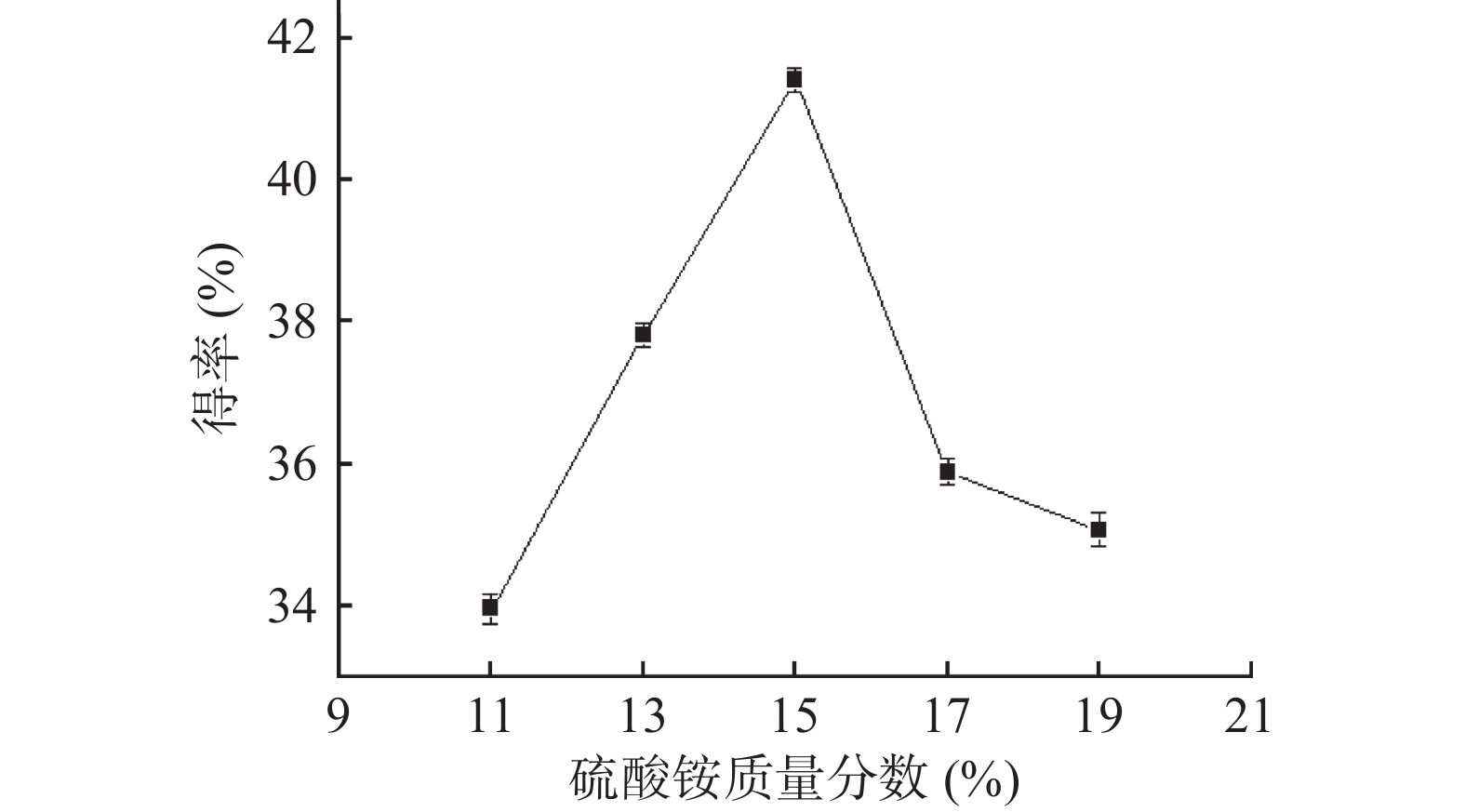
2.2.1 硫酸铵质量分数对黄酮得率的影响
如图2所示,随着硫酸铵质量分数的增加,黄酮得率先增加而后降低,当硫酸铵质量分数为15%时,黄酮得率达到最大值。可能的原因是,随着硫酸铵质量分数的增加,硫酸铵对双水相体系中水分子的束缚能力增强[23],使得上相中乙醇的质量分数增大,从而有利于促进黄酮物质的溶出,当硫酸铵质量分数进一步增加时,硫酸铵在上相中的浓度也随之增加,从而不利于黄酮物质的萃取。因此,选取硫酸铵质量分数为15%进行后续实验研究。
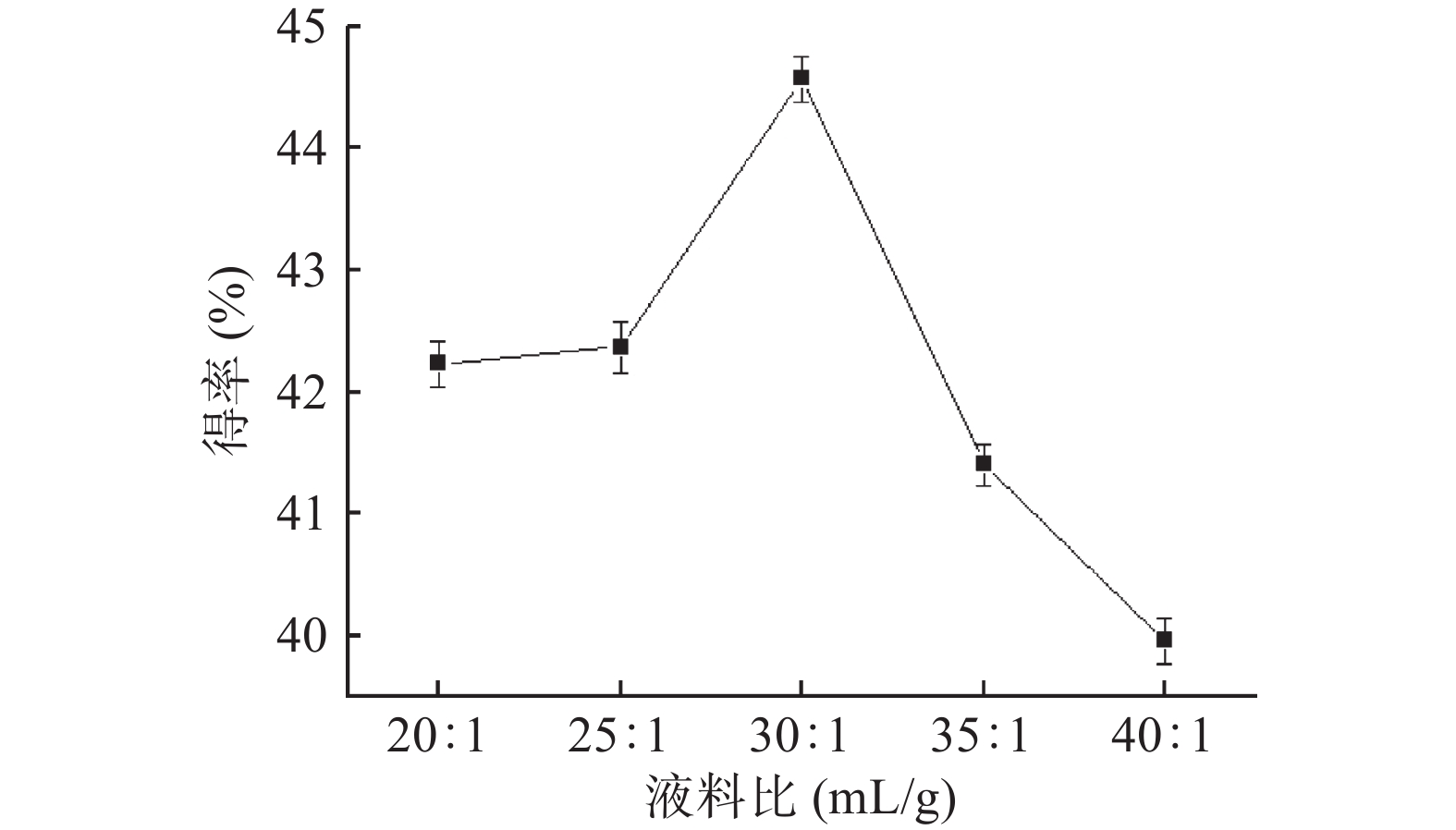
2.2.2 液料比对黄酮得率的影响
如图3所示,随着液料比的增加,黄酮得率先增加后降低,在液料比为30:1(mL/g)时达到最大值。可能原因是,溶剂用量的增加使得细胞内外的质量浓度差变大,传质推动力、内扩散的速率增大,从而有利于黄酮的溶出。但随着液料比进一步增加,溶剂量增多杂质成分溶出增多,影响黄酮类物质的浸出,从而导致其得率降低[19]。因此,30:1(mL/g)为黄酮提取的较佳料液比,由于35:1(mL/g)时黄酮得率大大降低,故选择20:1~30:1(mL/g)进行后续实验。
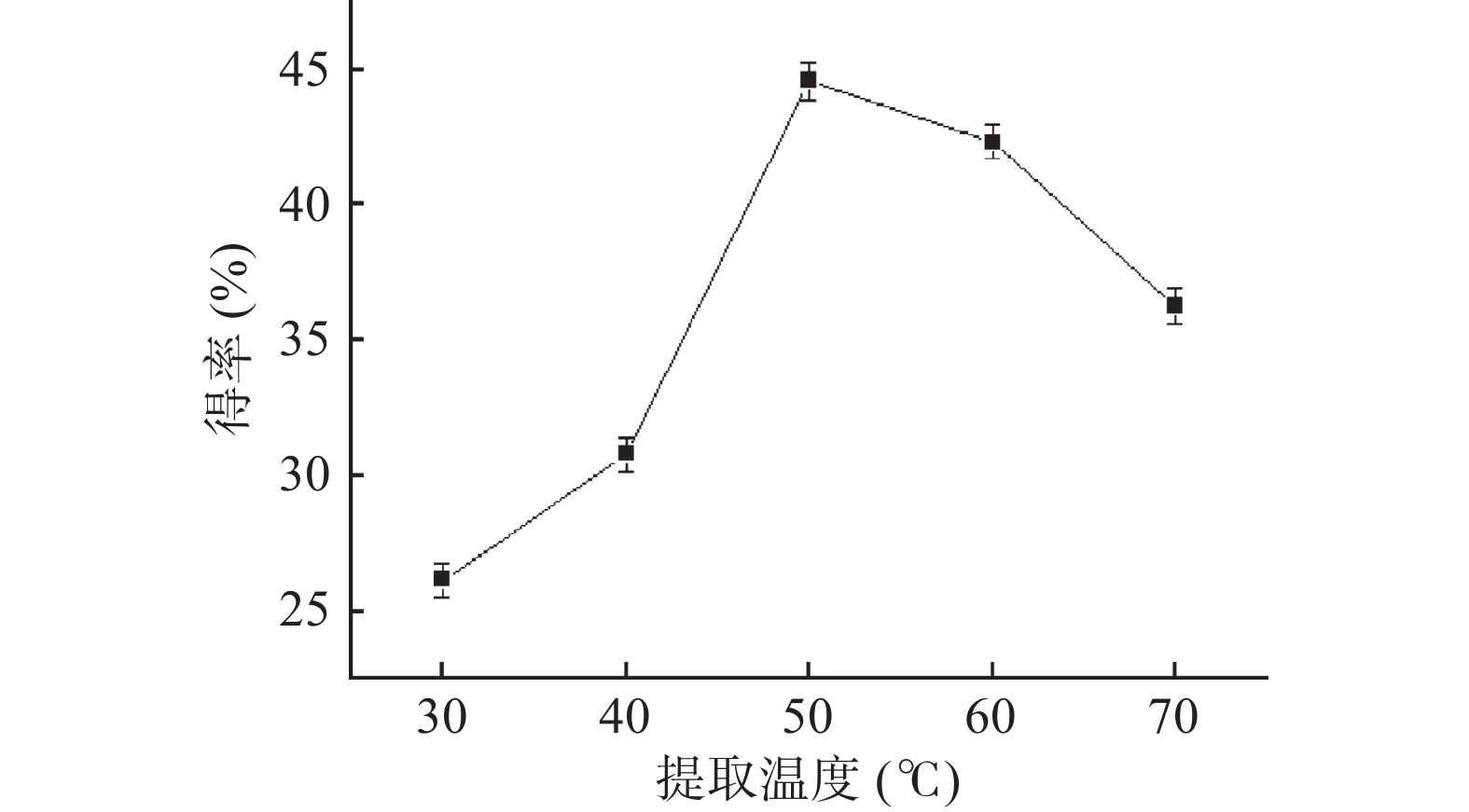
2.2.3 提取温度对黄酮得率的影响
如图4所示,随着提取温度的升高,黄酮得率先快速增加而后逐步降低,当提取温度为50 ℃时,达到最大值。可能的原因是,当温度升高时,黄酮的溶出率也相应增大,因此得率升高。但当温度过高时,黄酮类化合物的分子结构有可能会被破坏[22],从而导致得率降低。因此,黄酮提取的较佳温度为50 ℃。
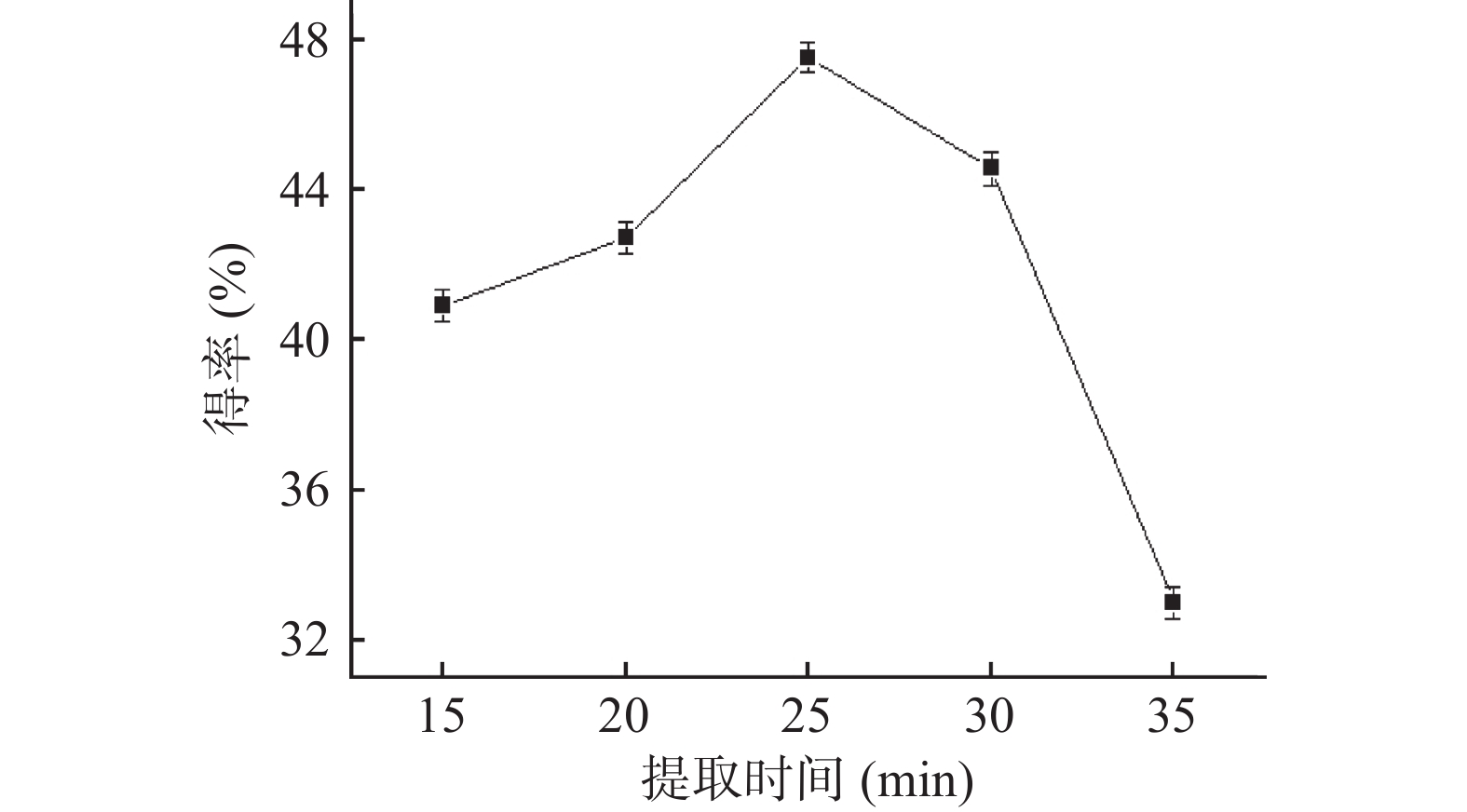
2.2.4 提取时间对黄酮得率的影响
如图5所示,随着提取时间的增加,黄酮得率先增加而后降低,当提取时间为25 min时,黄酮得率达到最大值。可能的原因是,随着提取时间的增加,黄酮化合物的溶出量逐步增加,当提取时间为25 min时,黄酮类化合物已基本溶出,继续加热可能会破坏黄酮的内部结构,从而导致黄酮得率降低。因此,较佳的提取时间为25 min。
2.3 响应面优化试验
根据Box-Benhnken设计原理,进行了4因素3水平共29个响应面分析试验,具体结果如表2所示。
表 2 响应面试验设计及结果Table 2. Designandresults for response surface test实验号 A B C D Y 得率(%) 1 −1 −1 0 0 35.78 2 1 −1 0 0 40.17 3 −1 1 0 0 40.79 4 1 1 0 0 40.21 5 0 0 −1 −1 38.91 6 0 0 1 −1 42.22 7 0 0 −1 1 40.77 8 0 0 1 1 44.79 9 −1 0 0 −1 37.94 10 1 0 0 −1 37.38 11 −1 0 0 1 38.45 12 1 0 0 1 41.51 13 0 −1 −1 0 37.96 14 0 1 −1 0 43.12 15 0 −1 1 0 41.03 16 0 1 1 0 44.29 17 −1 0 −1 0 35.25 18 1 0 −1 0 38.11 19 −1 0 1 0 39.16 20 1 0 1 0 41.53 21 0 −1 0 −1 38.51 22 0 1 0 −1 42.73 23 0 −1 0 1 42.23 24 0 1 0 1 44.57 25 0 0 0 0 44.27 26 0 0 0 0 44.62 27 0 0 0 0 45.32 28 0 0 0 0 45.01 29 0 0 0 0 44.37 2.3.1 模型建立和显著性分析
利用Design-Expert8.0软件对响应面实验数据进行分析和多元回归拟合,建立以黄酮得率为函数的二次回归方程,并对回归方程进行方差分析和显著性检验,结果见表3。黄酮得率(Y)与硫酸铵质量分数(A)、液料比(B)、提取温度(C)和提取时间(D)的二次回归方程为:
表 3 响应面试验回归模型方差分析Table 3. Variance analysis of regression model for response surface test方差来源 平方和 自由度 均方 F值 P值 显著性 模型 235.79 14 16.84 45.56 <0.0001 ** A 11.1 1 11.1 30.02 <0.0001 ** B 33.43 1 33.43 90.45 <0.0001 ** C 29.77 1 29.77 80.53 <0.0001 ** D 17.84 1 17.84 48.25 <0.0001 ** AB 6.18 1 6.18 16.71 0.0011 ** AC 0.06 1 0.06 0.16 0.6931 AD 3.28 1 3.28 8.86 0.01 * BC 0.9 1 0.9 2.44 0.1405 BD 0.88 1 0.88 2.39 0.1444 CD 0.13 1 0.13 0.34 0.5686 A2 124.6 1 124.6 337.07 <0.0001 ** B2 10.04 1 10.04 27.16 0.0001 ** C2 20.44 1 20.44 55.3 < 0.0001 ** D2 13.01 1 13.01 35.21 <0.0001 ** 残差 5.18 14 0.37 失拟项 4.4 10 0.44 2.26 0.2248 纯误差 0.78 4 0.19 总和 240.96 28 注:*表示差异显著,P<0.05;**表示差异极其显著,P<0.01。 Y=-531.72210+34.80771A+6.10558B+7.89725C+1.83433D−0.12425AB−0.012250AC+0.090500AD−0.019000BC−0.018800BD+7.10000E−003CD−1.09569A2−0.049760B2−0.071010C2−0.056660D2。
从表3可知,本实验所选用回归模型具有极好的显著性(P<0.01),模型决定系数R2=0.9785%,拟合度较高,校正系数R2adj=0.9570,说明该模型方程能够解释95.70%的响应值变化。失拟项P=0.2248>0.05,表明该模型失拟项不显著,模型整体的绝对误差较小,说明通过响应面分析模拟选择得率与各因素之间的函数作用关系具有一定的科学合理性[24]。根据F值可知,各因素对桃花总黄酮得率的影响程度由大到小依次为B>C>D>A,即液料比>提取温度>提取时间>硫酸铵质量分数。此外,A、B、C、D、AB、A2、B2、C2、D2对黄酮得率影响极显著(P<0.01),AD对黄酮得率影响显著(P<0.05)。
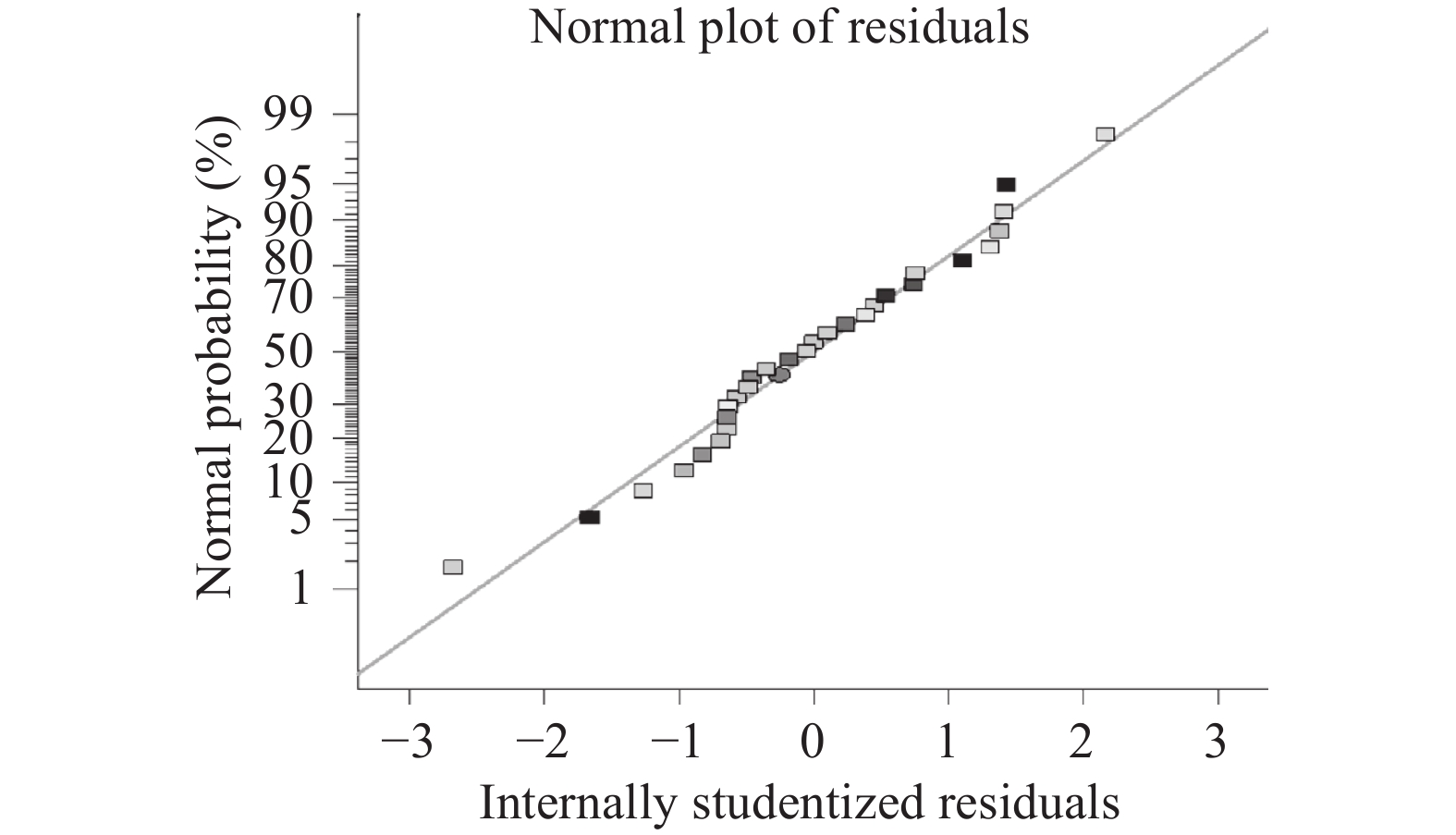
残差的正态分布规律如图6所示。由图6可知,实验中的实际测定值与预测值之间吻合性良好,二者的散点分布概率几乎为直线,说明测定结果整体标准偏差的平均值相较于得率可忽略不计[24]。
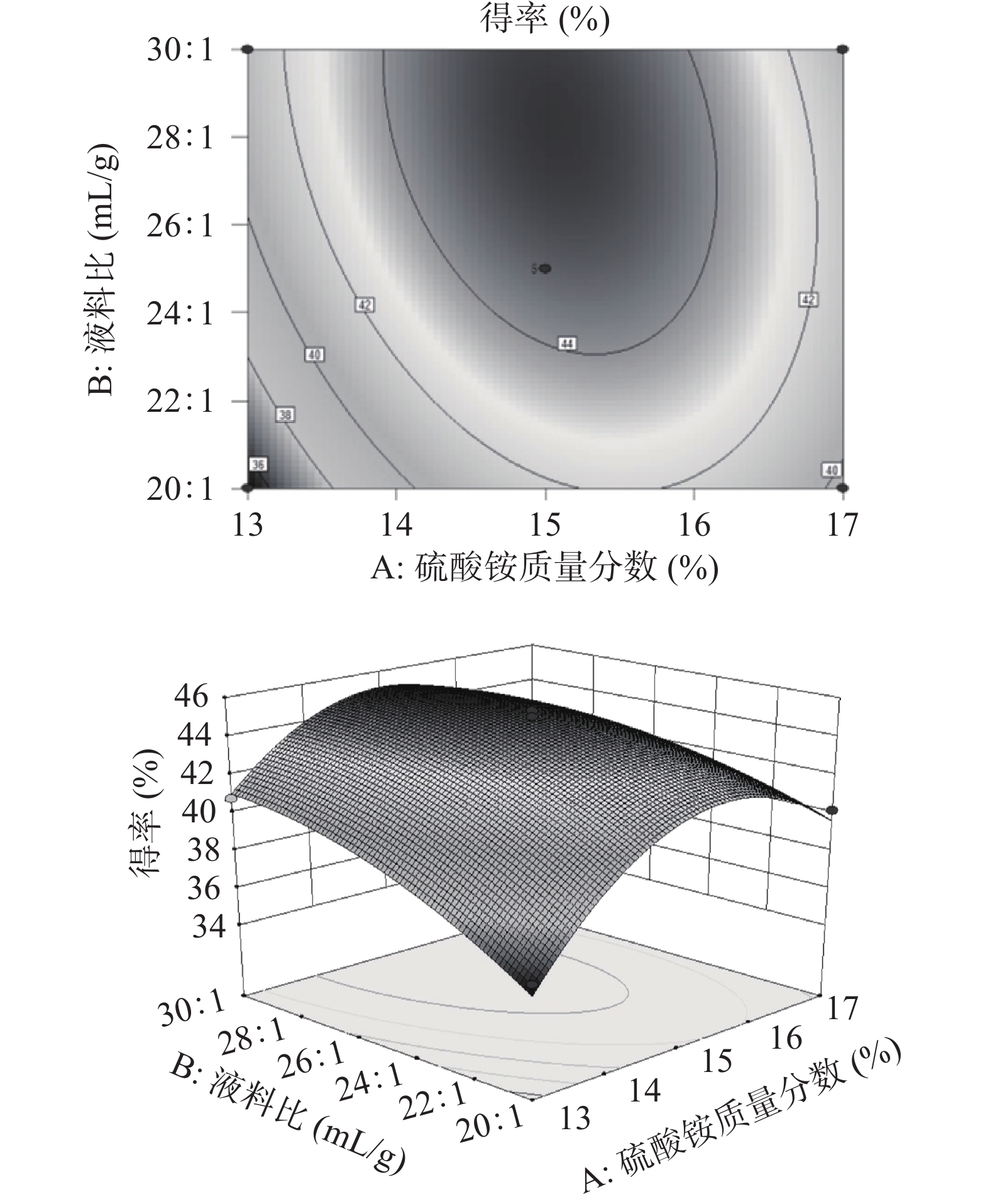
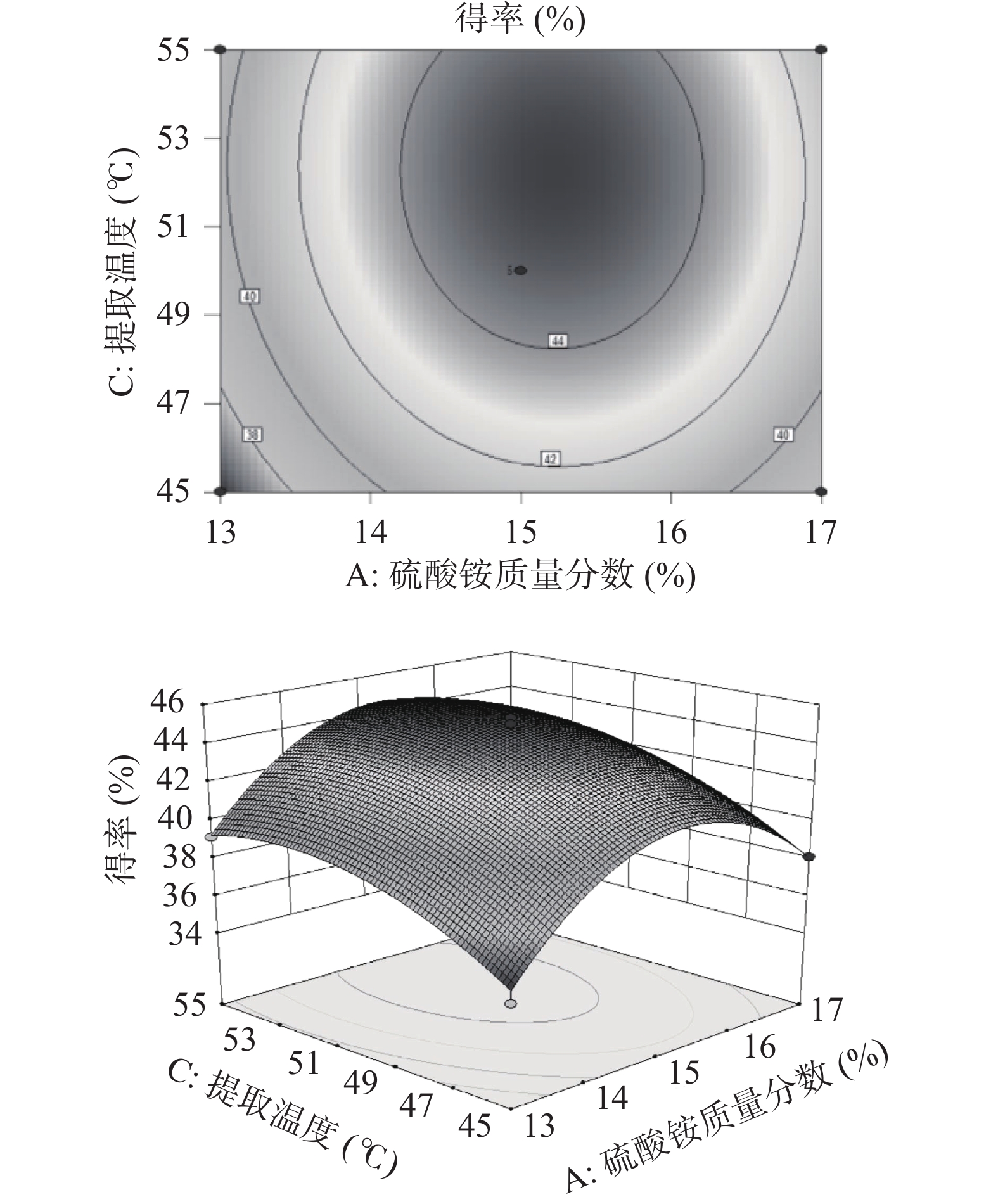
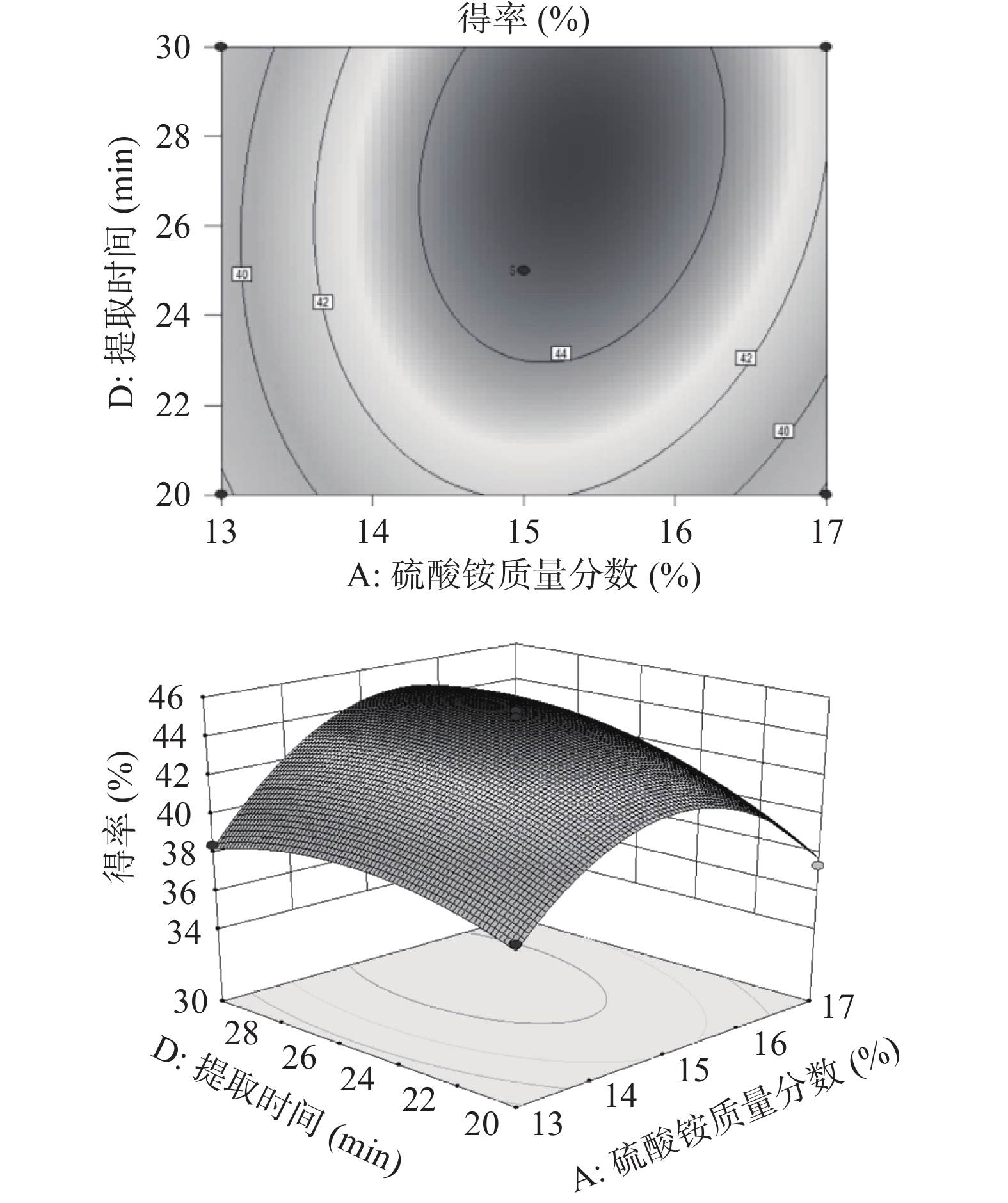
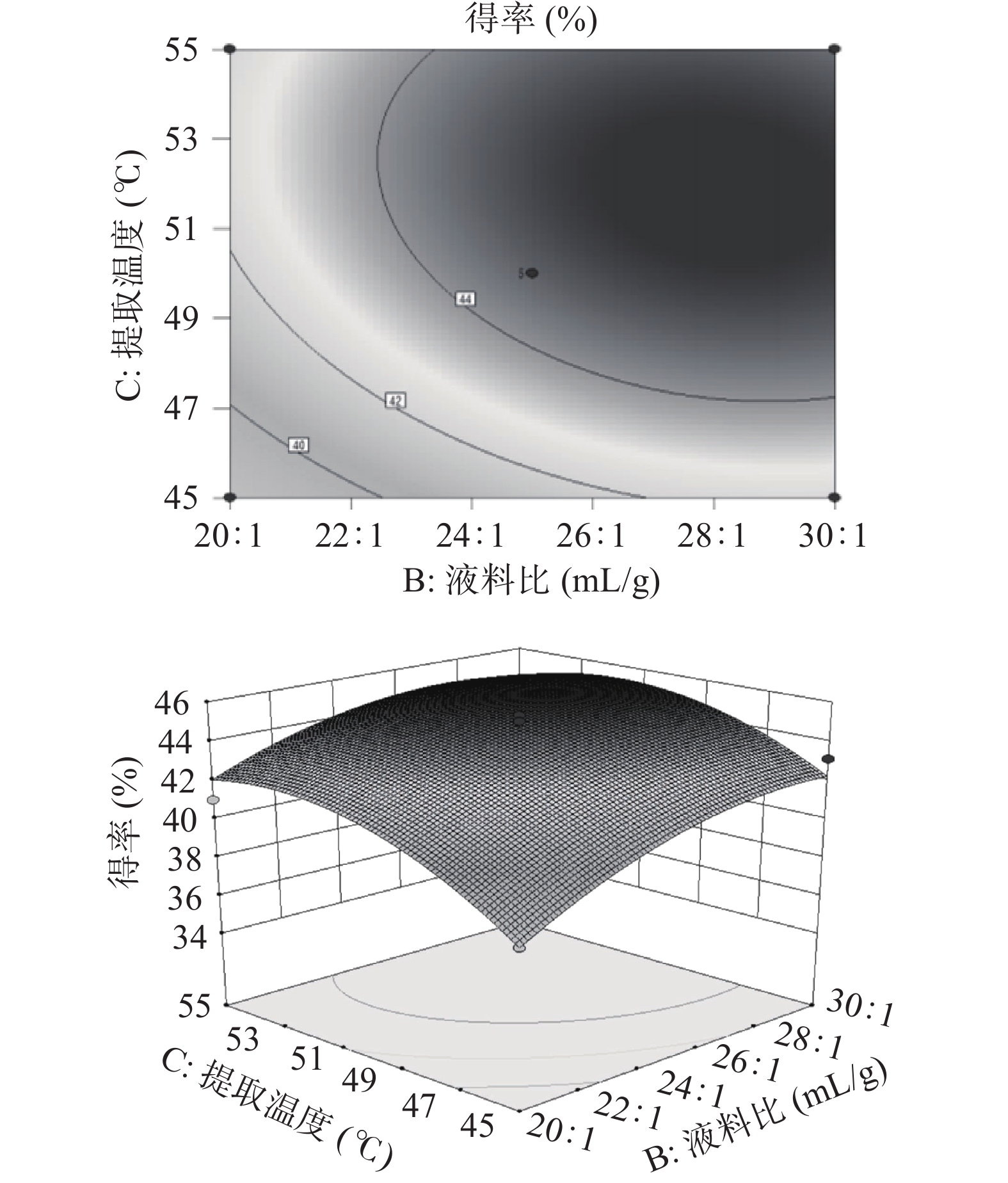
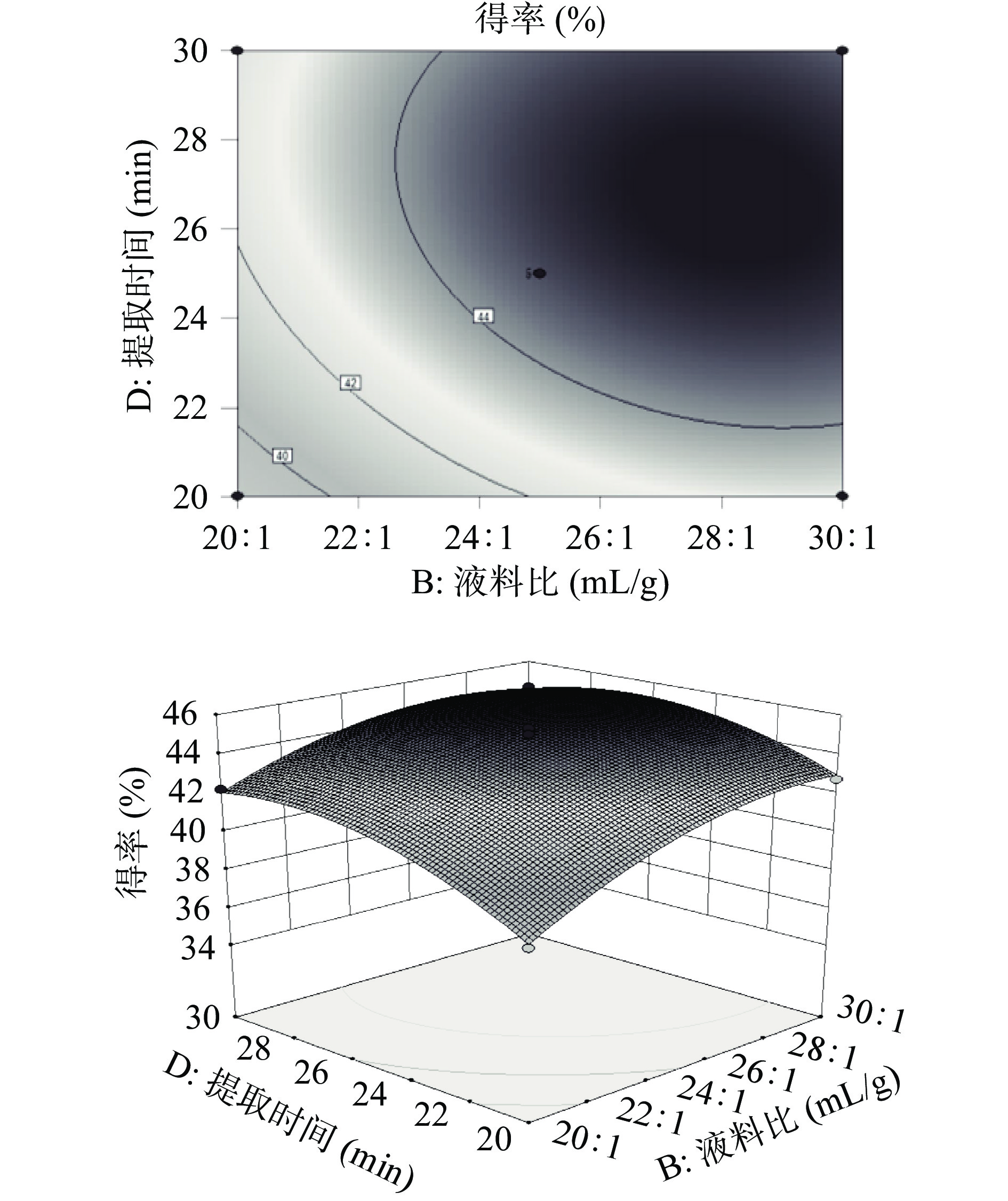
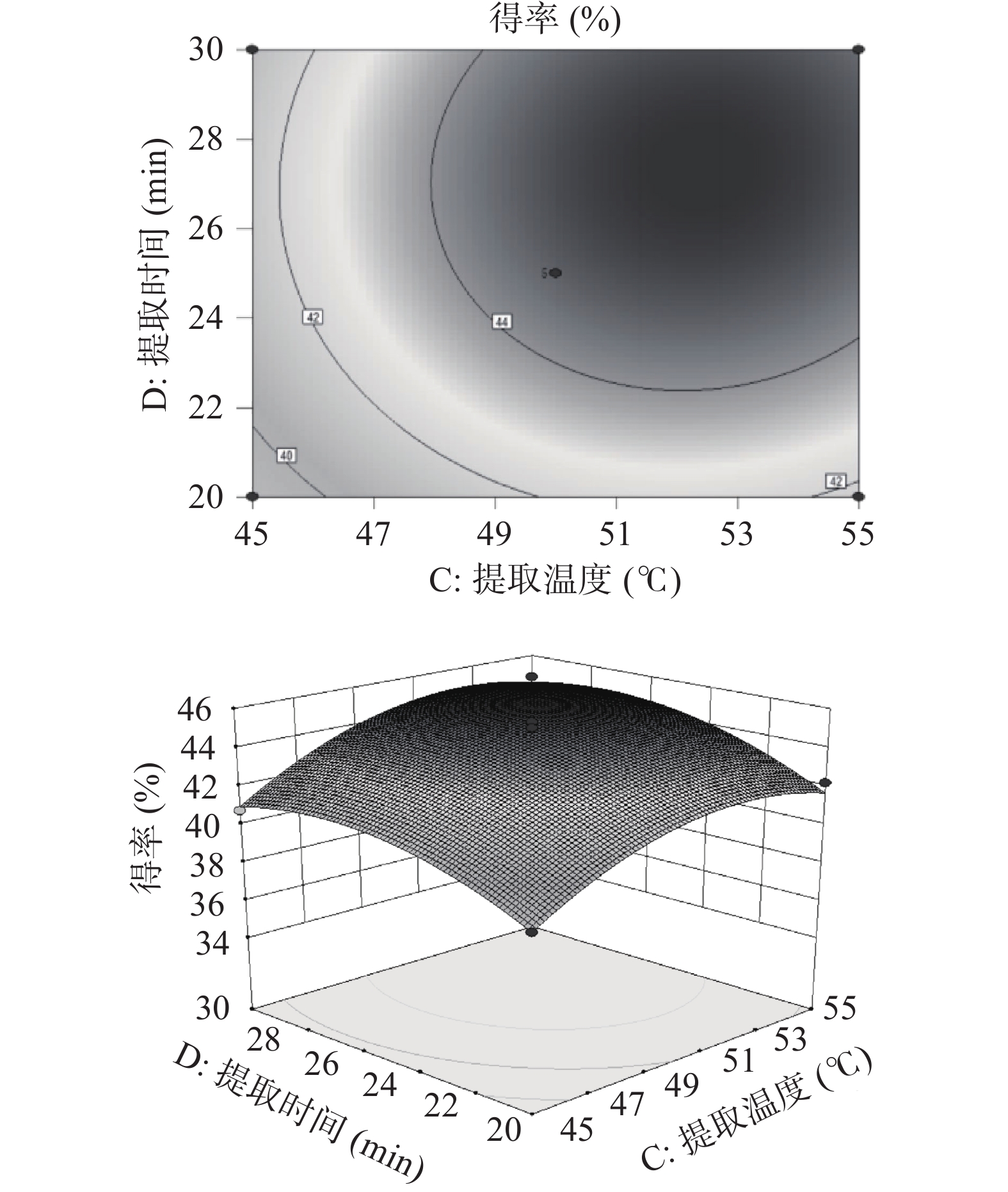
2.3.2 响应面交互作用分析
通过响应面分析软件对各个因素之间的交互作用进行分析,绘制了各因素交互作用的等高线图和响应曲面图(图7~图12)。等高线的性状可以反映各因素间交互作用的强弱关系[19]。硫酸铵质量分数和液料比的等高线呈椭圆形,其交互作用最为显著,其次为硫酸铵质量分数和提取时间。硫酸铵质量分数和提取温度、液料比和提取温度、液料比和提取时间以及提取温度和提取时间的交互作用不显著。这与表3的显著性分析结果一致。
2.3.3 验证性实验
响应面试验预测的最佳提取条件为:硫酸铵质量分数为15.18%、液料比为27.75:1(mL/g)、提取温度为51.11 ℃、提取时间为26.11 min。考虑到实验室实际操作,将硫酸铵质量分数调整为15.2%,液料比调整为27.8:1(mL/g),提取温度调整为51 ℃,提取时间调整为26 min。在此条件下,黄酮得率理论值可达45.64%。重复三次实验,黄酮得率分别为45.65%、45.61%、45.70%,平均值为45.65%,与理论值十分接近,实验结果与模型符合良好,说明该模型能较好地预测黄酮得率。
此外,和文献[11]报道相似,本实验桃花总黄酮得率较高,可能和植物所在的不同时期有关[25]。实验中所使用的原料为桃花花苞,采收时处于生长期,推测其生长状态良好,营养成分吸收充足[26]。
2.4 桃花总黄酮抗氧化实验结果
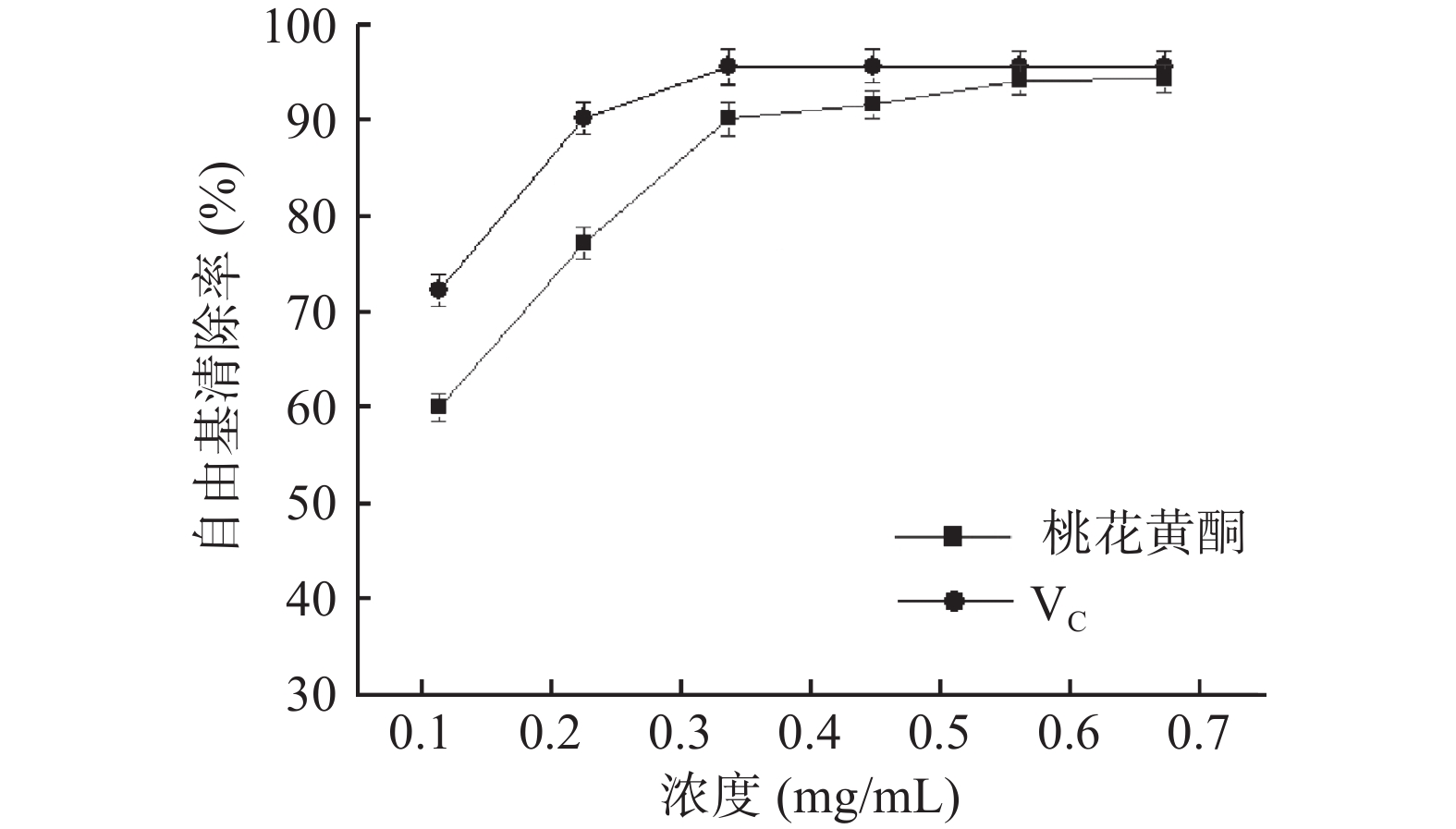
2.4.1 对DPPH·的清除能力
由图13可知,随着浓度的增加,VC清除DPPH·能力逐步升高,当浓度为0.336 mg/mL时,清除率已达到95.63%,继续增大浓度清除率无明显变化。随着浓度的增加,桃花总黄酮对清除DPPH·的能力逐步增加,当样品浓度为0.56 mg/mL时,其对DPPH·的清除率为94.21%,接近VC水平,说明桃花总黄酮对DPPH·有较强的清除能力,与文献[27-28]研究黄酮抗氧化的结论相似。
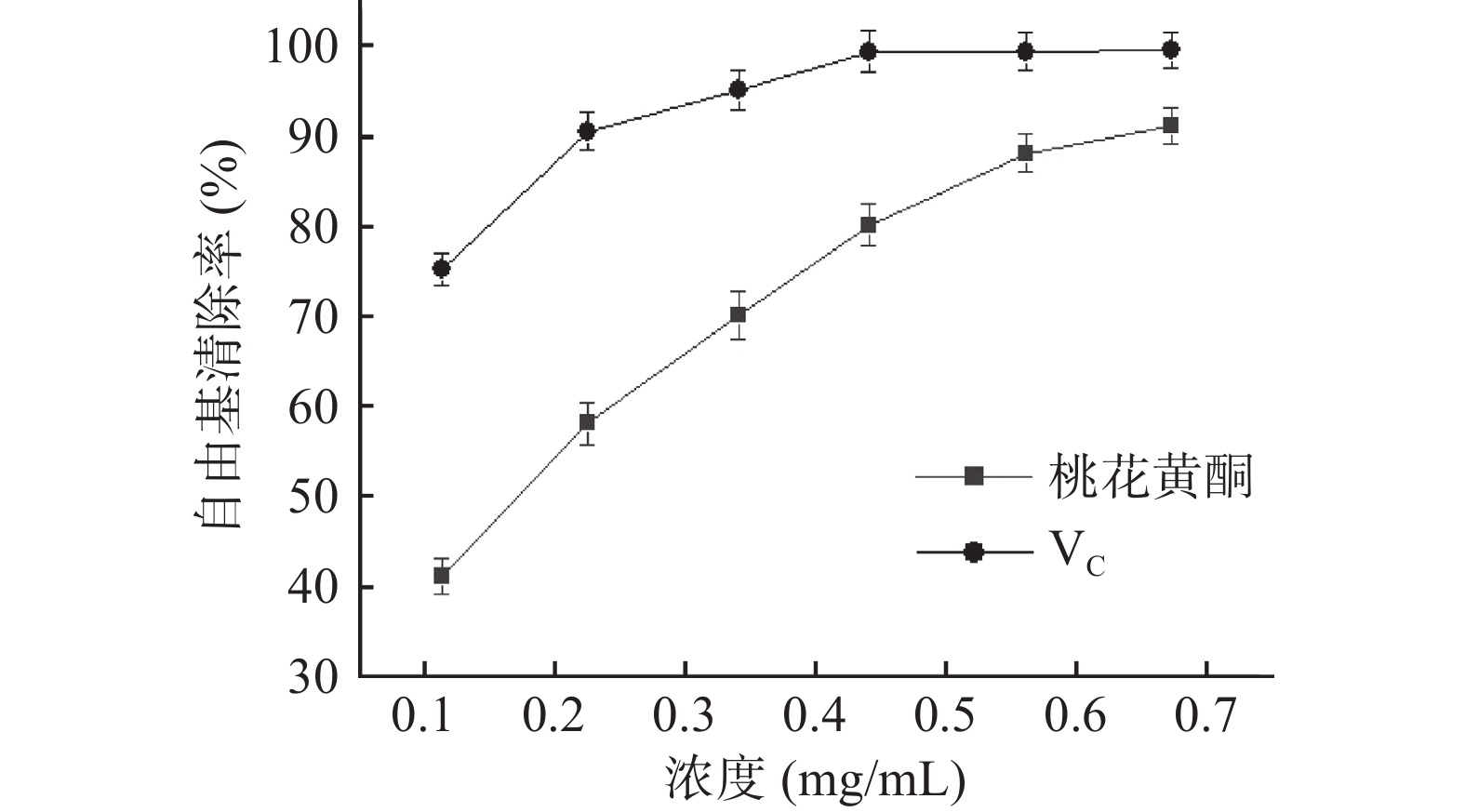
2.4.2 对OH·清除能力
如图14所示,随着浓度的增加,VC清除OH·能力逐步升高,当浓度为0.448 mg/mL时,清除率几乎可达100%[22]。在所考察的浓度范围内,桃花总黄酮对OH·的清除能力随浓度的增加呈明显上升趋势,当样品浓度为0.672 mg/mL时,清除率可达91.23%,说明其对OH·有较强的清除能力,与文献[22,29]研究黄酮抗氧化的结论相似。
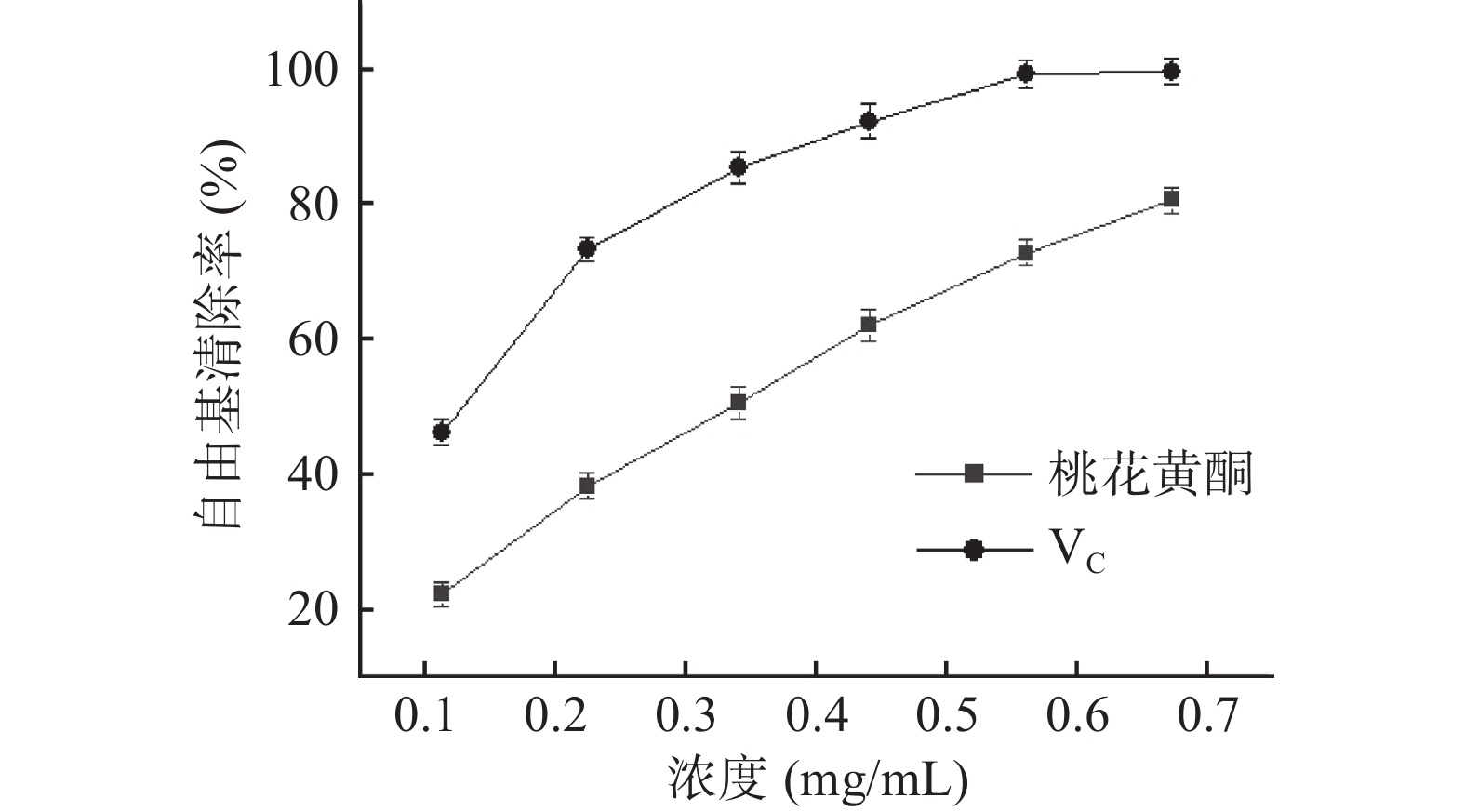
2.4.3 对
O−2⋅ 的清除能力如图15所示,随着浓度的增加,VC清除
O−2⋅ 能力逐步升高,当浓度为0.56 mg/mL时,清除率几乎可达100%。在所考察的浓度范围内,桃花总黄酮对O−2⋅ 的清除能力随浓度的增加呈明显上升趋势,当样品浓度为0.672 mg/mL时,清除率可达80.65%,说明其对O−2⋅ 具备良好的清除能力,与文献[22,30]研究黄酮抗氧化的结论相似。植物黄酮的抗氧化能力是存在植物体内所有黄酮化合物共同作用的结果[31]。黄酮结构上为多羟基酚类物质,具有很强的供氢能力,并且可直接参与自由基的清除[32]。本实验结果表明桃花黄酮对DPPH·、OH·和O2−·具有较强的清除能力,可作为一种潜在的天然抗氧化剂。
3. 结论
采用乙醇-硫酸铵双水相体系来提取桃花中总黄酮。在单因素实验的基础上,以硫酸铵质量分数、提取时间、液料比、提取温度4个影响因素为自变量,以黄酮得率为指标,通过响应曲面法设计优化总黄酮的提取工艺。最佳工艺参数为:硫酸铵质量分数15.2%、液料比27.8:1(mL/g)、提取温度为51 ℃、提取时间26 min。在此条件下,黄酮得率理论值可达45.64%,验证值为45.65%,与理论值十分接近。抗氧化实验结果表明,桃花总黄酮对DPPH·、OH·和O2−·表现出较强的清除能力,当浓度为0.56 mg/mL时,DPPH·清除率为94.21%,当浓度为0.672 mg/mL时,OH·和
O−2⋅ 清除率分别为91.23%和80.65%,表明其具有良好的抗氧化性能。该试验结果可为桃花中黄酮等活性物质的进一步研究开发提供参考,具有一定的理论研究及工业应用价值。 -
表 1 响应面分析试验因素水平
Table 1 Code and level of factors for the response surface analysis experiment
因素 水平 −1 0 1 A硫酸铵质量分数(%) 13 15 17 B液料比(mL·g−1) 20:1 25:1 30:1 C提取温度(℃) 45 50 55 D提取时间(min) 20 25 30 表 2 响应面试验设计及结果
Table 2 Designandresults for response surface test
实验号 A B C D Y 得率(%) 1 −1 −1 0 0 35.78 2 1 −1 0 0 40.17 3 −1 1 0 0 40.79 4 1 1 0 0 40.21 5 0 0 −1 −1 38.91 6 0 0 1 −1 42.22 7 0 0 −1 1 40.77 8 0 0 1 1 44.79 9 −1 0 0 −1 37.94 10 1 0 0 −1 37.38 11 −1 0 0 1 38.45 12 1 0 0 1 41.51 13 0 −1 −1 0 37.96 14 0 1 −1 0 43.12 15 0 −1 1 0 41.03 16 0 1 1 0 44.29 17 −1 0 −1 0 35.25 18 1 0 −1 0 38.11 19 −1 0 1 0 39.16 20 1 0 1 0 41.53 21 0 −1 0 −1 38.51 22 0 1 0 −1 42.73 23 0 −1 0 1 42.23 24 0 1 0 1 44.57 25 0 0 0 0 44.27 26 0 0 0 0 44.62 27 0 0 0 0 45.32 28 0 0 0 0 45.01 29 0 0 0 0 44.37 表 3 响应面试验回归模型方差分析
Table 3 Variance analysis of regression model for response surface test
方差来源 平方和 自由度 均方 F值 P值 显著性 模型 235.79 14 16.84 45.56 <0.0001 ** A 11.1 1 11.1 30.02 <0.0001 ** B 33.43 1 33.43 90.45 <0.0001 ** C 29.77 1 29.77 80.53 <0.0001 ** D 17.84 1 17.84 48.25 <0.0001 ** AB 6.18 1 6.18 16.71 0.0011 ** AC 0.06 1 0.06 0.16 0.6931 AD 3.28 1 3.28 8.86 0.01 * BC 0.9 1 0.9 2.44 0.1405 BD 0.88 1 0.88 2.39 0.1444 CD 0.13 1 0.13 0.34 0.5686 A2 124.6 1 124.6 337.07 <0.0001 ** B2 10.04 1 10.04 27.16 0.0001 ** C2 20.44 1 20.44 55.3 < 0.0001 ** D2 13.01 1 13.01 35.21 <0.0001 ** 残差 5.18 14 0.37 失拟项 4.4 10 0.44 2.26 0.2248 纯误差 0.78 4 0.19 总和 240.96 28 注:*表示差异显著,P<0.05;**表示差异极其显著,P<0.01。 -
[1] POONAM V, RAUNAK-KUMAR G, REDDY L C S, et al. Chemical constituents of the genus Prunus and their medicinal properties[J]. Current Medicinal Chemistry,2011,18:3758−3824. doi: 10.2174/092986711803414386
[2] TAKAGI S, YAMAKI M, MASUDA K, et al. Studies on the purgative drugs. III. On the constituents of the flowers of Prunus persica Batsch[J]. Yakugaku Zasshi Journal of the Pharmaceutical Society of Japan,1977,97(1):109−111.
[3] 柳琪, 滕薇, 苏本玉, 等. 桃花营养元素的分析与开发探讨[J]. 氨基酸和生物资源,1996,18(4):31−33. [LIU Q, TENG W, SUB Y, et al. Analysis of nutrition elements in peach blossom and its potential application[J]. Amino Acids and Biotic Resources,1996,18(4):31−33. [4] 杨凤田, 张雅玮, 李顺, 等. 油菜蜂花粉黄酮提取物抗氧化性测定及在色拉米中的应用[J]. 食品工业科技,2016,37(15):121−124,128. [YANG F T, ZHANG Y W, LI S, et al. Antioxidation of rape bee pollen flavonoid extracts and application in salami[J]. Science and Technology of Food Industry,2016,37(15):121−124,128. [5] KOPUSTINSKIENE D M, JAKSTAS V, SAVICKAS A, et al. Flavonoids as anticancer agents[J]. Nutrients,2020,12(2):457. doi: 10.3390/nu12020457
[6] XIE J H, DONG C J, NIE S P, et al. Extraction, chemical composition and antioxidant activity of flavonoids from Cyclocaryapaliurus (Batal. ) Iljinskaja leaves[J]. Food Chemistry,2015,186:97−105. doi: 10.1016/j.foodchem.2014.06.106
[7] KIM Y H, YANG H E, PARK B K, et al. The extract of the flowers of Prunus persica, a new cosmetic ingredient, protects against solar ultraviolet-induced skin damage in vivo[J]. Journal of Cosmetic Science,2002,53(1):27−34.
[8] 刘杰超, 张春岭, 吕真真, 等. 桃花中总酚和总黄酮的提取及抗氧化活性研究[J]. 食品安全质量检测学报,2013,4(6):1750−1756. [LIU J C, ZHANG C L, LV Z Z, et al. Extraction of total phenolics and flavanoids from peach blossomsand their antioxidant activity[J]. Journal of Food Safety and Quality,2013,4(6):1750−1756. [9] 梁永锋. 桃花中黄酮含量的测定及超声波辅助下提取工艺优化[J]. 江苏农业科学,2016,44(9):329−331. [LIANG Y F. Determination of flavonoid contents in peach blossom and optimization of ultrasonic assisted extraction process[J]. Jiangsu Agricultural Sciences,2016,44(9):329−331. [10] 曾臻, 刘后根, 洪艳平, 等. 大孔树脂纯化桃花总黄酮工艺及抗氧化性研究[J]. 江西农业大学学报,2017,39(1):182−189. [ZENG Z, LIU H G, HONG Y P, et al. A Study on purification of total flavonoids from Prunus persica by macroporousresin and their antioxidant activity[J]. Acta Agriculturae Universitatis Jiangxiensis,2017,39(1):182−189. [11] 高洪坤, 孙嘉晨, 侯磊磊, 等. 乙醇法提取桃花精油的工艺研究及桃花精油的成分分析[J]. 生物资源,2018,40(2):182−185. [GAO H K, SUN J C, HOU L L, et al. Extraction of peach blossom essential oil by ethanol and analysis of its components[J]. Biotic Resources,2018,40(2):182−185. [12] KARAKATSANIS A, LIAKOPOULOU-KYRIAKIDES M. Comparison of PEG/fractionated dextran and PEG/industrial gradedextran aqueous two-phase systems for the enzymic hydrolysis ofstarch[J]. Journal of Food Engineering,2007,80(4):1213−1217. doi: 10.1016/j.jfoodeng.2006.09.011
[13] 范芳. 双水相萃取技术的应用进展[J]. 化学与生物工程,2011,28(7):16−20. [FAN F. Application development of aqueous two-phase extraction technology[J]. Chemistry & Bioengineering,2011,28(7):16−20. doi: 10.3969/j.issn.1672-5425.2011.07.004 [14] XIE X, ZHU D, ZHANG W, et al. Microwave-assisted aqueous two-phase extraction coupled with high performance liquid chromatography for simultaneous extraction and determination of four flavonoids in Crotalaria sessiliflora L.[J]. Industrial Crops and Products,2017,95:632−642. doi: 10.1016/j.indcrop.2016.11.032
[15] YANG S X, LIU B, TANG M, et al. Extraction of flavonoids from Cyclocarya paliurus (Juglandaceae) leaves using ethanol/salt aqueous two-phasesystem coupled with ultrasonic[J]. Journal of Food Processing and Preservation,2020,44(6):e14469.
[16] 邹维, 崔恩浩, 丁岗芯, 等. 聚能超声-醇盐双水相耦合提取藜麦总黄酮[J]. 食品研究与开发,2021,42(4):83−89. [ZOU W, CUI E H, DING G X, et al. Extraction of total flavonoids from quinoa by polymeric ultrasound-alcohol combined with two-phase extraction[J]. Food Research and Development,2021,42(4):83−89. [17] ALBERTTSON P A. Partition of cell particles and macromolecules [M]. New York: Wiley Publishing, 1971.
[18] 李敏, 何亚萍, 柴娟. 柑橘皮总黄酮的提取及抗氧化性研究[J]. 应用化工,2016,45(3):501−503. [LI M, HE Y P, CHAI J. Study on the extraction of total flavonoids and antioxidantactivity from citrus peel[J]. Applied Chemical Industry,2016,45(3):501−503. [19] 郭莹, 周颖, 毕海丹, 等. 响应面优化超声波-微波协同提取凤眼莲黄酮工艺及其不同部位黄酮抗氧化活性分析[J]. 食品工业科技,2019,40(1):168−174,180. [GUO Y, ZHOU Y, BI H D, et al. Optimization of ultrasonic-microwave synergistic extraction of flavonoidsfrom Eichhornia crassipes by response surface methodology andanalysis of antioxidant activity of flavonoids from its different parts[J]. Science and Technology of Food Industry,2019,40(1):168−174,180. [20] OLUWASEUN R A, NOUR H A, OLUSEGUN A O. Optimization ofmicrowave-assisted extraction of flavonoids and antioxidants fromVernonia amygdalina leaf using response surface methodology[J]. Food and Bioproducts Processing,2018,107(1):36−48.
[21] 石玉平, 卢挺, 王永宁. 油菜蜂花粉中黄酮类物质清除羟基自由基的研究[J]. 食品科学,2004,25(11):300−302. [SHI Y P, LU T, WANG Y N. Studies on the hydroxy-group free radical eliminated of flavonoidsof Elaeagnus angustifoliaL flowrse[J]. Food Science,2004,25(11):300−302. doi: 10.3321/j.issn:1002-6630.2004.11.079 [22] 许远, 魏和平, 吴彦, 等. 响应面优化襄荷总黄酮提取及抗氧化研究[J]. 食品工业科技,2015,36(5):233−239. [XU Y, WEI H P, WU Y, et al. Study on optimization of extraction of total flavonoids fromZingiber strioatum by response surface methodologyand its antioxidant activity[J]. Science and Technology of Food Industry,2015,36(5):233−239. [23] 陈建福, 胡泽杰, 潘诗玲, 等. 超声波辅助双水相提取胡萝卜叶总黄酮的工艺研究[J]. 河南工业大学学报(自然科学版),2018,39(1):72−77. [CHEN J F, HU Z J, PAN S L, et al. Optimization of ultrasonic-assisted aqueous two-phase extraction of total flavonoids from carrot leaves[J]. Journal of Henan University of Technology(Natural Science Edition),2018,39(1):72−77. [24] 党金宁, 祁小妮, 李振亮, 等. 乙醇/硫酸铵双水相体系提取蕨麻多糖及其抑菌抗氧化活性[J]. 食品工业科技,2018,39(5):191−196,202. [DANG J N, QI X N, LI Z L, et al. Extraction of polysaccharide by ethanol /ammonium sulphate aqueous two-phase system from the Argentina anserina and its antibacterial and antioxidant activity[J]. Science and Technology of Food Industry,2018,39(5):191−196,202. [25] 邹玲, 周新萍, 白红进. 枣叶中黄酮类化合物含量及其动态变化[J]. 中国实验方剂学杂志,2017,23(17):63−67. [ZOU L, ZHOU X P, BAI H J. Flavonoid content and its dynamic changes in jujube leaves[J]. Chinese Journal of Experimental Traditional Medical Formulae,2017,23(17):63−67. [26] 刘萍. 罗布麻花、果实黄酮类含量为最佳采收期的确定[J]. 吉林农业大学学报,2010,32(3):277−279. [LIU P. Determination of the optimum harvest time for flavonoid content in flowers and fruit of Apocynum venetum[J]. Journal of Jilin Agricultural University,2010,32(3):277−279. [27] 秦晶晶, 钱慧琴, 赵媛, 等. 柿叶总黄酮提取工艺优化及其抗氧化活性[J]. 食品工业科技,2020,41(13):32−38,45. [QIN J J, QIAN H Q, ZHAO Y, et al. Optimization of the extraction technology of total flavonoids and in vitro antioxidant activity of extract from persimmon leaves[J]. Science and Technology of Food Industry,2020,41(13):32−38,45. [28] 杜丽娟, 苏秀芳, 黄成银. 余甘子叶总黄酮的超声波法提取工艺优化及其抗氧化能力研究[J]. 食品与机械,2020,36(3):185−189,193. [DULJ, SUX F, HUANG C Y. Optimization of ultrasonic-assisted extraction of total flavonoids from leaves of Phyllanthus emblica and its antioxidant capacity[J]. Food and Machinery,2020,36(3):185−189,193. [29] 朱会霞. 覆盆子黄酮抗氧化活性研究[J]. 现代食品科技,2012,28(10):1301−1305. [ZHU H X. Study on the antioxidant activity of raspberry flavones[J]. Modern Food Science and Technology,2012,28(10):1301−1305. [30] 黄琼, 黄晓梅. 玫瑰茄总黄酮超声波-微波协同提取及抗氧化活性[J]. 热带作物学报,2020,41(6):1242−1250. [HUANG Q, HUANG X M. Ultrasound-microwave assisted extraction and antioxidant activity of total flavonoids from Hibiscus sabdariffa L doi: 10.3969/j.issn.1000-2561.2020.06.024 J]. Chinese Journal of Tropical Crops,2020,41(6):1242−1250. doi: 10.3969/j.issn.1000-2561.2020.06.024
[31] 孙泽飞. 牡丹花类黄酮成分及抗氧化能力分析 [D]. 杨凌: 西北农林科技大学, 2015. SUN Z F. Studies on flavonoids composition of the peony and its antioxidant activity analysis [D]. Yangling: Northwest A & F University, 2015.
[32] 李玲, 闫旭宇. 野葛花黄酮和花青素的提取及抗氧化性研究[J]. 食品研究与开发,2018,39(20):23−28. [LI L, YAN X Y. Extraction and antioxidant activity of flavonoids and anthocyanins from Flos puerariae[J]. Food Research and Development,2018,39(20):23−28. doi: 10.3969/j.issn.1005-6521.2018.20.005 -
期刊类型引用(19)
1. 徐美,臧宇晴,李煦,范小振. 聚乙二醇-硫酸铵双水相体系萃取桑叶总黄酮工艺研究. 沧州师范学院学报. 2025(01): 33-37 .  百度学术
百度学术
2. 郭丽丽,李小兰,高欣缘,龚玉凤,秦楠. 黄芪茎叶总黄酮的超声辅助双水相提取工艺优化及其抗氧化活性. 食品研究与开发. 2025(05): 94-101 .  百度学术
百度学术
3. 梁金月,周洪鑫,张雨晴,王玲娜,李佳,赵东升. 金银花多酚和多糖同步提取工艺优化及其抗氧化活性研究. 中国食品添加剂. 2024(03): 1-10 .  百度学术
百度学术
4. 钱慧琴,方李珂,唐丽杰,张青瑾,张宵悦,李彦灵. 骨碎补总黄酮双水相提取工艺优化及抗氧化活性研究. 饲料工业. 2024(13): 120-128 .  百度学术
百度学术
5. 王海云. 超声波耦合双水相提取藜麦种子中总黄酮工艺优化及其抗氧化性测定. 中外食品工业. 2024(02): 4-7 .  百度学术
百度学术
6. 樊轻亚,程晓梅,夏小婧. 双水相手性萃取拆分马尼地平对映体. 辽宁化工. 2024(08): 1164-1166 .  百度学术
百度学术
7. 樊轻亚,王万好,程晓梅. 三种1, 4-二氢吡啶类药物的双水相手性萃取拆分研究. 四川化工. 2024(05): 1-7+11 .  百度学术
百度学术
8. 谭婉,卫阳飞,李枫林,鲁宁,龚永鹏,李全春,章毅. 黑果枸杞果实多糖的超声辅助双水相萃取工艺优化、单糖组成分析及胰脂肪酶抑制活性评价. 食品工业科技. 2024(22): 158-168 .  本站查看
本站查看
9. 秦晶晶,陈胜昔,叶翠红,李宏祥,王琪,苏慧慧. 提取方法对梧桐叶黄酮得率及其抗氧化活性影响研究. 饲料工业. 2024(23): 120-127 .  百度学术
百度学术
10. 李娟,耿晓桐,陈琼,彭博菡,李倩倩,王宁. 桃花不同溶剂提取物抗氧化活性分析及桃花软糖的研制. 粮食与油脂. 2023(03): 124-128 .  百度学术
百度学术
11. 高利,岳璐,杨增航,耿紫馨,秦晶晶. 超声辅助双水相体系优化辛夷总黄酮提取工艺及其抗氧化活性研究. 饲料研究. 2023(04): 90-94 .  百度学术
百度学术
12. 许晓路,戴国庆,韦涵峰,俞杰. 双水相提取金银花叶总黄酮工艺优化及其抗氧化活性. 食品工业科技. 2023(13): 242-248 .  本站查看
本站查看
13. 叶润,王泽夏,蔡静,孙伟,陈琼,罗婧. 半夏总黄酮双水相提取工艺优化及抗氧化活性分析. 中国食品添加剂. 2023(08): 102-110 .  百度学术
百度学术
14. 庄乾飞,刘丹丹,陈泽雨,尚祖飞,刘晓燕,马立志. 超声辅助双水相提取刺梨黄酮的工艺优化及其对黄嘌呤氧化酶活性的抑制作用. 食品工业科技. 2023(17): 222-230 .  本站查看
本站查看
15. 孙光,张蓉,刘凤丹,陈光吉,李世歌,尚以顺,宋莉,班骞,钟理,龙忠富,王茜,李小冬. 金荞麦茎叶总黄酮提取方法优化及其抗氧化活性. 草业科学. 2023(08): 2162-2170 .  百度学术
百度学术
16. 周飙,胡斌,柳鑫,周蕾. 超声辅助双水相提取绞股蓝皂苷工艺及其降糖活性分析. 食品工业科技. 2023(20): 197-205 .  本站查看
本站查看
17. 高慧娟,张佳奇,张乐乐,刘生杰. 乙醇-硫酸铵双水相体系萃取香椿籽总黄酮工艺优化及其抗氧化活性研究. 中成药. 2023(12): 3879-3883 .  百度学术
百度学术
18. 穆莎茉莉,袁晓霞,李国瑞,包英才. 蓖麻叶总黄酮纯化工艺优化及抗氧化研究. 内蒙古民族大学学报(自然科学版). 2023(06): 519-523 .  百度学术
百度学术
19. 魏甜甜,魏勃,王承,李凯,谢彩锋,杭方学. 黄冰糖低温浸渍茉莉花制备风味糖浆工艺优化. 食品工业科技. 2022(12): 181-187 .  本站查看
本站查看
其他类型引用(4)







 下载:
下载:










 下载:
下载:





