Optimization of Fermentation Technology and Determination of Physicochemical Properties of Pure Malt Wine
-
摘要: 以萌发麦芽为原料,采用半固态发酵技术酿造纯麦酒,并进行工艺优化及理化性质测定。设计单因素实验研究发酵过程中发酵时间、酒曲接种量以及糖化酶添加量对纯麦酒酒精含量的影响,并确定最佳单因素实验条件。在单因素实验结果的基础上,进行正交试验的设计,确定最佳工艺组合为发酵时间为4 d、酒曲接种量为2‰、糖化酶添加量为2%。在此条件下,所得纯麦酒酒精度为10.6%vol±0.3%vol,总酚含量为1.159±0.066 g/L,蛋白质含量为209.568±19.178 mg/L,总酸含量为6.4±0.2 g/L,还原糖含量为8.409±0.021 g/L,对羟基自由基的清除率可达86.75%±1.42%,总还原能力可达1.842±0.004。正交试验方差分析结果表明发酵时间与糖化酶添加量两个因素对于纯麦酒的酒精度影响显著(P<0.05),而接种量对纯麦酒酒精度的影响并不显著(P>0.05)。试验结果为纯麦酒的生产开发提供理论依据。Abstract: Pure malt wine was brewed from germinated malt by semi-solid fermentation technology, and the process optimization and physicochemical properties were determined. The single factor experiment was designed to study the effects of fermentation time, inoculation amount of koji and addition amount of glucoamylase on the alcohol content of pure malt wine, and to determine the best single factor. The experimental conditions were studied after the single factor level determination, meanwhile the orthogonal design was carried out, and the optimal combination was determined as follows: fermentation time of 4 d, inoculation amount of 2‰ koji and addition amount of 2% glucoamylase. Under these conditions, the alcohol content of pure malt wine was 10.6%vol±0.3%vol, the total phenol content was 1.159±0.066 g/L, the protein content was 209.568±19.178 mg/L, the total acid content was 6.4±0.2 g/L, reducing sugar content was 8.409±0.021 g/L, the scavenging rate of hydroxyl radical was 86.75%±1.42%, and the total reduction capacity could reach 1.842±0.004. Through the analysis of variance of orthogonal experiment, it was concluded that fermentation time and glucoamylase dosage had significant effect on the alcohol content of pure malt wine (P<0.05), while inoculation amount had no significant effect on the alcohol content of pure malt wine (P>0.05). The results would provide a theoretical basis for the production and development of pure malt wine.
-
Keywords:
- malt /
- pure malt wine /
- process optimization /
- physical and chemical properties /
- variance analysis
-
麦芽由我国重要的粮食作物大麦经发芽干燥制得,也是中医临床上常用的消食药[1]。在萌发过程中,麦芽会产生大量的酶类,包括淀粉酶、蛋白分解酶等能治疗食欲不振的消化酶,也包括多种维生素、卵磷脂、还原糖等成分,营养价值极高[2-4]。麦芽经过一定处理,会生成丰富的风味化合物。于淼等[5]采用顶空固相微萃取结合气相色谱-嗅闻-质谱联用仪的方法,从六款麦芽中鉴定出41种风味化合物,包括20种醛类、7种吡嗪类、4种醇类、1种酚类、9种杂环化合物类。正基于上述优秀的品质,麦芽得到了学者的广泛研究,也主要被应用在啤酒酿造行业。在啤酒酿造过程中,麦芽提供了主要的淀粉质原料,并且这些原料经过糖化等处理可以转化为可发酵性糖,以供酵母生长并产生酒精[6-7];同时,不同品种的麦芽会赋予啤酒不同的特性,使其口感及颜色也千差万别[8]。
随着生活水平的不断提高,人们对医疗保健方面投入的时间与精力越来越多,对于心脑血管等疾病防范意识也越来越强,学者对于麦芽的研究也由对其应用价值的研究逐渐转向对其保健价值的研究。SHOPSKA等[9]对不同类型麦芽的酚含量及抗氧化活性进行了比较研究,并表明麦芽提供了酒精发酵过程中酚类化合物总量的80%左右;LANDETE[10]的研究表明,麦芽中所富含的酚类化合物可以作为效果良好的抗氧化剂,能够中和人体组织进行生命活动所产生的与疾病有关的活性氧,经常食用可以降低癌症以及心脑血管疾病发生的概率。CÉLINE等[11]研究发现,麦芽中所含有的原花青素及儿茶素是影响麦芽抗氧化活性最重要的两种成分;GERHÄU-SER等[12]表明,麦芽中所含有的羟基肉桂酸衍生物和少量黄烷醇,会对自由基的清除发挥一定的作用。综上所述,麦芽具有良好的保健价值,而近年来,也有学者发现米酒曲具有抗肥胖或抗糖尿病的作用[13],这表明米酒曲潜在利用价值极大。因此,利用麦芽与米酒曲发酵生产具有保健功能的新型发酵酒,将具有良好的市场前景。
鉴于国内外市场多用麦芽进行啤酒酿造及功能食品研究,而以萌发麦芽接种米酒曲生产发酵酒的研究鲜有报道,故试验以萌发麦芽为原料生产纯麦酒,在料液质量体积比(m/v)为1:3、温度30 ℃的条件下,以酒精度为指标,探究发酵时间、酒曲接种量以及糖化酶添加量对纯麦酒酒精含量的影响,并在单因素实验基础上,设计正交试验进行优化,确定最佳酿造工艺,同时对产品进行了抗氧化能力测定,以便为纯麦酒生产提供理论依据。
1. 材料与方法
1.1 材料与仪器
麦芽 山东淄博瑞源生物科技有限公司;纯麦酒 广西大学朗姆酒研发实验室自酿;米酒曲 南宁一明生物科技有限公司;糖化酶(≥100 U/mg) 上海瑞永生物科技有限公司;DNS试剂、Folin-Ciocalteu试剂 南宁恒因生物科技有限公司;考马斯亮蓝、没食子酸、葡萄糖、碳酸钠 国药集团化学试剂有限公司。
JJ-2组织捣碎机 常州迅生仪器有限公司;SHP-250生化培养箱 上海精宏实验设备有限公司;YP201N电子天平 上海菁华科技仪器有限公司;PL-303分析天平 METTLER TOLEDO有限公司;UVmini-1240紫外-可见分光光度计 岛津仪器(苏州)有限公司;SN510C全自动高压灭菌锅 重庆雅玛拓科技有限公司;电子万用炉 北京市永光明医疗仪器有限公司;酒精计 余姚仪表二厂有限责任公司。
1.2 实验方法
1.2.1 纯麦酒的酿造工艺
精选麦芽→组织捣碎机粉碎→加水搅拌(料液质量体积比1:3)→高温灭菌→摊凉至室温→按质量比接种糖化酶→按质量比接种酒曲→30 ℃发酵→酒渣分离→澄清过滤→原酒→杀菌灌装→成品
1.2.2 关键操作要点
a. 精选麦芽:挑选籽粒饱满、色泽鲜亮、无长虫发霉及损坏的优质萌发麦芽备用。
b. 组织捣碎机粉碎:采用JJ-2组织捣碎机进行原料粉碎,所得麦芽粉细腻均一,无明显较大颗粒。
c. 加水搅拌:称取75 g麦芽粉与225 mL蒸馏水搅拌均匀,此时料液质量体积比为1:3。
d. 高温灭菌:设定灭菌温度121 ℃、灭菌时间20 min进行灭菌。
e. 接种糖化酶:摊凉完成后,在无菌环境下按照质量比接种糖化酶,与原料搅拌均匀并糖化30 min,随后接种酒曲。
f. 接种酒曲:在无菌环境下按照质量比接种酒曲,并搅拌均匀,随后放入30 ℃生化培养箱进行发酵。
1.2.3 单因素发酵实验
发酵时间:每瓶纯麦酒接种2‰酒曲(质量比,m/m)、2%糖化酶(质量比,m/m),在30 ℃发酵温度下,设置发酵时间条件分别为1、2、3、4、5 d,发酵结束后取出,进行酒精度的测定。
酒曲接种量:每瓶纯麦酒接种2%糖化酶,发酵4 d,在30 ℃发酵温度下,设置酒曲接种量条件分别为1‰、2‰、3‰、4‰、5‰,发酵结束后取出,进行酒精度的测定。
糖化酶添加量:每瓶纯麦酒接种2‰酒曲,发酵4 d,在30 ℃发酵温度下,设置糖化酶添加量条件分别为1%、2%、3%、4%、5%,发酵结束后取出,进行酒精度的测定。
1.2.4 纯麦酒发酵工艺正交设计优化
在单因素实验基础上,以发酵时间(A)、酒曲接种量(B)、糖化酶添加量(C)为正交试验的影响因素,每一个因素采用三个水平。鉴于酒精度是评价发酵酒质量最直观的指标,且参考孙婷婷等[14]以麦芽为原料研究新型发酵酒的过程中主要测量了产品的酒精度,故以酒精度为评价标准,设计L9(34)正交试验确定纯麦酒的最佳发酵参数,正交试验因素与水平见表1。
表 1 纯麦酒发酵条件正交优化试验因素和水平Table 1. Factors and levels of orthogonal experiments for fermentation conditions optimization of pure malt wine水平 因素 (A)发酵时间(d) (B)酒曲接种量(‰) (C)糖化酶添加量(%) 1 3 1 1 2 4 2 2 3 5 3 3 1.2.5 理化性质测定
1.2.5.1 酒精度测定
采用蒸馏法测定发酵液酒精度(参考文献[15-17],有改动)。用量筒取100 mL纯麦酒于1000 mL蒸馏烧瓶中,用100 mL去离子水冲洗量筒三次,洗液倒入蒸馏瓶中,再加入适量玻璃珠,连接冷凝装置,以取样用的原量筒作为接收器。开启冷却水,缓慢加热蒸馏,收集馏出液接近100 mL刻度线,放入干燥的酒精计,不得接触量筒壁,同时插入温度计,平衡一定时间并进行水平观测,读取刻度值并记录温度。根据酒精浓度-温度校正表将酒精计读数和温度,换算为20 ℃情况下酒精度。
1.2.5.2 总酚含量测定
采用Folin-Ciocalteu法测定发酵液总酚含量(参考文献[18],有改动)。以没食子酸为标准品,准确吸取0.0、10.0、20.0、30.0、40.0、50.0 mg/L的没食子酸标准液,分别加入5.0 mL去离子水,1.0 mL Folin-Ciocalteu试剂和3.0 mL碳酸钠溶液(7.5 g/100 mL),定容到10 mL,摇匀静置反应2 h显色,在波长765 nm下测定吸光值。以没食子酸浓度为横坐标,吸光值为纵坐标,绘制标准曲线,得线性回归方程:y=0.0106x+0.0145(R2=0.9961)。以样品代替标准液进行测定,并计算相应含量。
1.2.5.3 蛋白质含量测定
采用考马斯亮蓝法测定发酵液蛋白质含量(参考文献[19],有改动)。以牛血清蛋白为标准品,制备100 µg/mL标准溶液。分别吸取0、0.2、0.4、0.6、0.8、1.0 mL标准溶液于试管中,分别加去离子水补到1.0 mL,之后加入5.0 mL考马斯亮蓝试剂,摇匀静置15 min,于波长595 nm下测定吸光值。以牛血清蛋白浓度为横坐标,吸光值为纵坐标,绘制标准曲线,得到线性回归方程:y=0.0064x+0.0151(R2=0.9969)。以样品代替标准液进行测定,并计算相应含量。
1.2.5.4 总酸含量测定
采用酸碱滴定法进行发酵液总酸(以乙酸计)滴定(参考文献[20],有改动)。取1.0 mL样品液加入去离子水定容至50 mL,以0.1 mol/L NaOH溶液进行滴定,滴定至溶液微红色且30 s内不褪色,记录消耗NaOH溶液体积,并按照下式进行计算:
产酸量(g/L)=V1000×CNaOH×60 (1) 式中:V为发酵液样品滴定消耗的NaOH溶液体积,mL;CNaOH为NaOH标准溶液浓度,mol/L;60为乙酸的相对分子质量。
1.2.5.5 还原糖含量测定
采用DNS法测定发酵液还原糖含量(参考文献[21],有改动)。配制1.0 mg/mL葡萄糖标准溶液,依次吸取0、0.2、0.4、0.6、0.8、1.0 mL标准溶液于试管中,分别加去离子水补到2.0 mL,之后加入1.5 mL DNS试剂,置于沸水水浴5 min,取出后立即用冷水冷却到室温,并补足去离子水至25.0 mL,摇匀后在波长540 nm下测定吸光值。以葡萄糖浓度为横坐标,吸光值为纵坐标绘制标准曲线,得线性回归方程:y=0.4873x−0.0137(R2=0.9959)。以样品代替标准液进行测定,并计算相应含量。
1.2.5.6 羟基自由基清除能力的测定
对样品进行了羟基自由基清除能力的测定,方法如下(参考文献[22-27],有改动):配制9.0 mmol/L H2O2溶液、9.0 mmol/L硫酸亚铁溶液及9.0 mmol/L水杨酸钠溶液备用,取纯麦酒酒样及1.0 g/L VC各2.0 mL于试管中,加入9.0 mmol/L硫酸亚铁溶液及9.0 mmol/L水杨酸钠溶液各2.0 mL,最后加入9.0 mmol/L H2O2溶液2.0 mL,37 ℃水浴30 min,反应结束后于波长510 nm下测定吸光度(Ai)。以2.0 mL去离子水代替样品与上述溶液混合,测定吸光度(Ax),以2.0 mL样品与6.0 mL去离子水混合测定吸光度(Aj)。羟基自由基清除率计算公式如下:
羟基自由基清除率(%)=(1−Ai−AjAx)×100 (2) 1.2.5.7 总还原能力的测定
对样品进行了总还原能力的测定,方法如下(参考文献[28-31],有改动):配制0.2 mol/L磷酸缓冲液(pH6.6)、0.2 mol/L铁氰化钾溶液、0.1 g/100 mL三氯化铁溶液及10 g/100 mL三氯乙酸溶液备用,取纯麦酒酒样及1.0 g/L VC各1.0 mL于试管中,依次加入2.5 mL磷酸缓冲液及2.5 mL铁氰化钾溶液,摇匀混合后于50 ℃恒温水浴30 min后取出,流水冷却后加入1.0 mL三氯乙酸溶液终止反应。3500 r/min离心5 min后取2.5 mL上清液,加入2.5 mL蒸馏水及0.5 mL三氯化铁溶液,摇匀,静置5 min于700 nm波长下测定吸光度。以吸光度数值大小代表总还原能力强弱。
1.3 数据处理
标准曲线使用Excel进行绘制,所得试验数据通过Origin 2017版绘图软件进行展示,正交试验设计及方差分析通过Latin正交设计助手软件进行设计及分析,单因素实验结果使用SPSS Statistics 21.0软件进行显著性分析(基于LSD法与Waller-Duncan法),认为P<0.05时差异显著,试验结果用均值±标准差(
ˉX ±SD,n=3)表示。2. 结果与分析
2.1 单因素实验结果
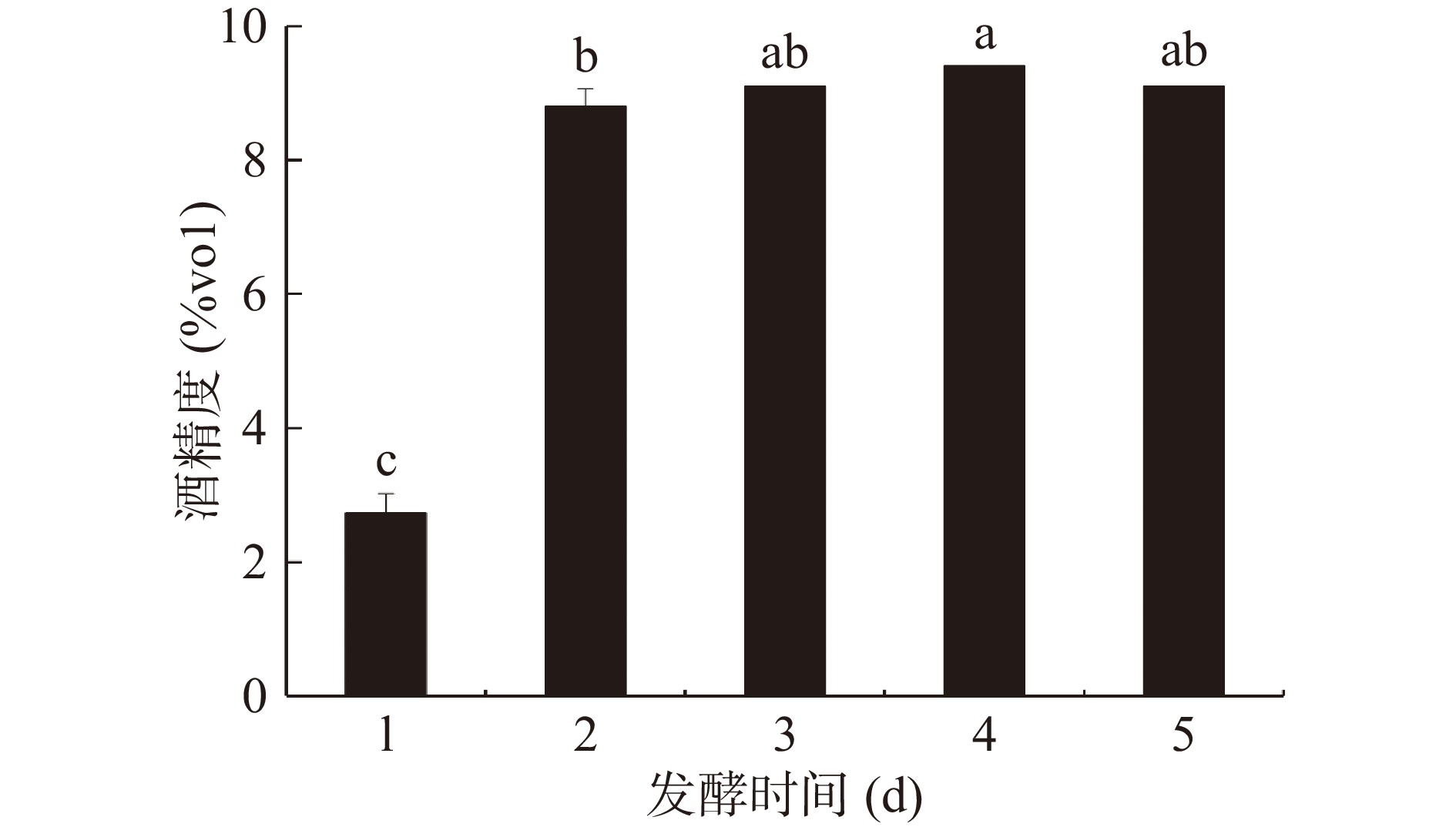
2.1.1 发酵时间对纯麦酒酒精含量的影响
发酵时间是影响酒精发酵过程的重要因素。由图1可知,纯麦酒的酒精度随着发酵时间的增长先增加后下降。发酵时间为1 d时,所测酒精度较低,仅为2.7%vol左右,这是由于发酵刚刚开始,微生物进行生长并未大量产生酒精引起的。发酵时间为1~2 d时,酒精含量大幅上升;在2~4 d时,纯麦酒的酒精度变化接近于平缓,且最高的酒精度出现在4 d,可达到9.4%vol。在发酵时间4~5 d时,酒精度略微降低,这可能是由于发酵后期营养物质及微生物数量均减少,导致酒精含量略微下降。因此,选择发酵时间为4 d。
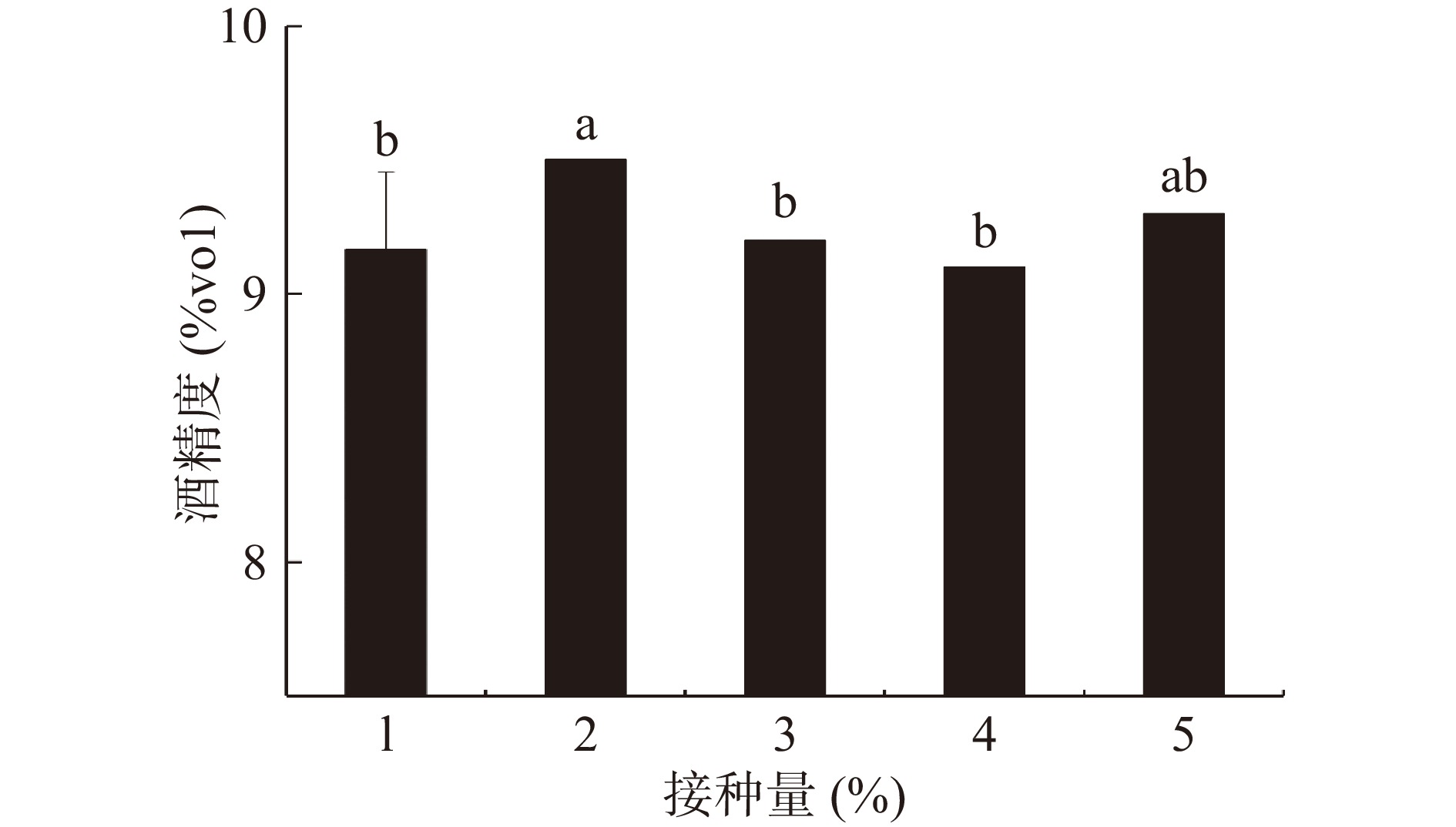
2.1.2 酒曲接种量对纯麦酒酒精含量的影响
纯麦酒在发酵过程中,酒曲的添加量会影响菌种的倍增时间,进而影响发酵进程。由图2可知,纯麦酒的酒精度随着酒曲接种量的增加先上升后降低。酒曲接种量为1 ‰~2 ‰时,酒精度略微上升,由9.2%vol上升到9.5%vol。在接种量为2 ‰~4 ‰时酒精度略微降低,由9.5%vol降低到9.1%vol,这可能是由于微生物数量上升,而发酵液营养有限,故导致酒精度下降。因此,选择酒曲接种量为2‰。
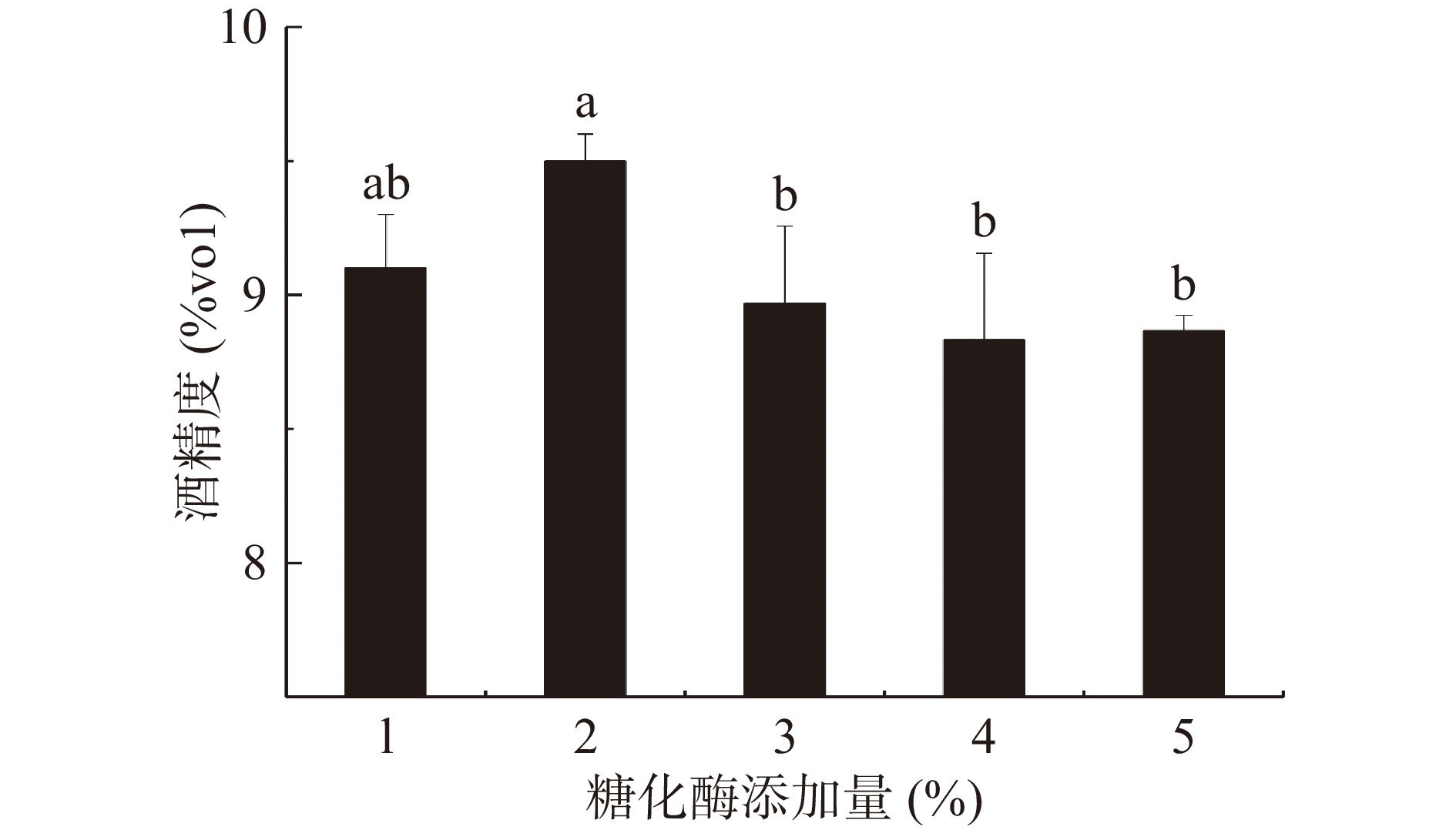
2.1.3 糖化酶添加量对纯麦酒酒精含量的影响
糖化酶的添加,可以促进发酵液大分子糖类物质转化为小分子可利用糖,减少了糖化时间,加快了发酵过程。由图3可知,纯麦酒的酒精度随着糖化酶添加量的增加先增大后减小。糖化酶添加量为1%~2%时,酒精度上升,并在添加量为2%时达到最大值9.5%vol。在超过2%添加量后,酒精度出现下降,这可能是由于过量的糖化酶导致可利用糖短时间内大量产生,微生物大量繁殖而使得营养物质含量降低过快,从而一定程度影响了酒精发酵。因此,选择糖化酶添加量为2%。
2.2 正交试验结果
在单因素实验基础上进行L9(34)正交试验优化纯麦酒的发酵条件,考察发酵时间(A)、酒曲接种量(B)、糖化酶添加量(C)对纯麦酒酒精度的影响,正交试验结果如表2所示,方差分析表如表3所示。
表 2 正交试验结果Table 2. Orthogonal test results实验号 A B C 酒精度(%vol) 1 3 1 1 8.4 2 3 2 2 9.0 3 3 3 3 9.5 4 4 1 2 10.5 5 4 2 3 9.6 6 4 3 1 9.0 7 5 1 3 8.9 8 5 2 1 9.6 9 5 3 2 9.4 K1 8.967 9.267 9.000 K2 9.700 9.400 9.633 K3 9.300 9.300 9.333 R 0.733 0.133 0.633 表 3 正交试验方差分析表Table 3. Analysis of variance of orthogonal test因素 偏差平方和 自由度 F值 F临界值 显著性 A 0.809 2 27.897 19.000 * B 0.029 2 1.000 19.000 C 0.602 2 20.759 19.000 * 误差 0.03 2 注:“*”表示显著差异(P<0.05)。 由表2的极差分析可知,各因素对纯麦酒酒精度的影响次序为发酵时间(A)>糖化酶添加量(C) >酒曲接种量(B)。根据平均值K得出最佳发酵条件组合为A2B2C2,即:发酵时间4 d,酒曲接种量2‰,糖化酶添加量2%。对组合进行实际验证,并进行三次重复试验,所得优化组合酒精度可达10.6%vol±0.3%vol,因此在料液质量体积比为1:3、温度30 ℃的情况下,纯麦酒最佳发酵组合为发酵时间4 d,酒曲接种量2‰,糖化酶添加量2%。
由表3的方差分析表可知,在以酒曲接种量(B)为误差所在列的情况下,所得因素A的F值为27.897,因素C的F值为20.759,两者的F值均大于F临界值(19.000),且在显著水平a=0.05的情况下,因素A与因素C达到了显著水平,故可得出结论:在已选定的条件下,发酵时间与糖化酶用量两个因素对于纯麦酒的酒精度影响显著(P<0.05),而酒曲接种量对纯麦酒酒精度的影响并不显著(P>0.05)。
2.3 纯麦酒理化性质测定
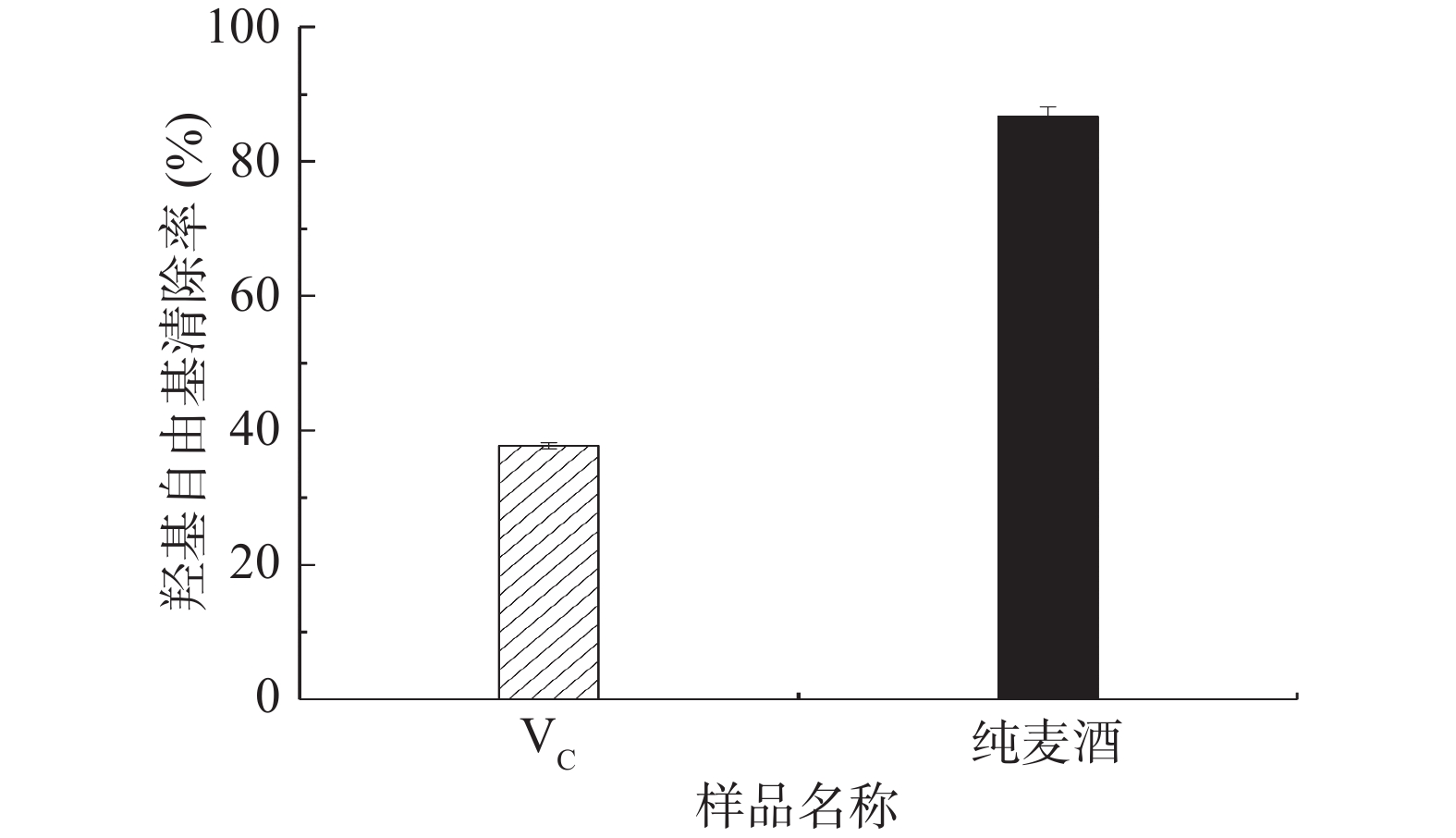
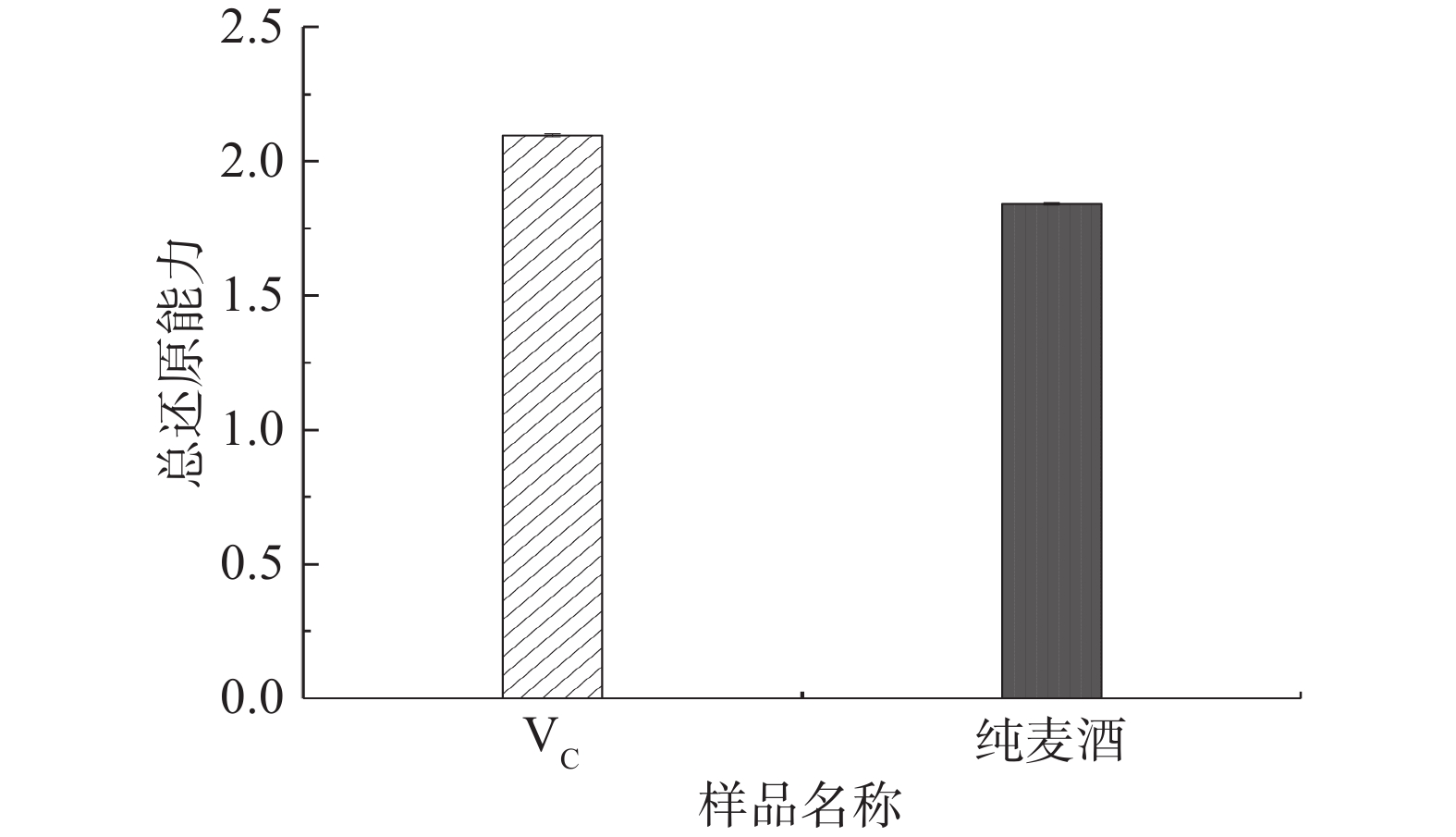
对实验所得最佳发酵组合A2B2C2进行部分理化性质测定,并与优化前进行对比,所得数据如表4所示,同时对最佳发酵组合A2B2C2进行了羟基自由基与总还原能力的测定,所得数据如图4与图5所示。
表 4 纯麦酒理化性质测定对比Table 4. Comparison of physical and chemical properties of pure malt wine指标 优化前含量 优化后含量 总酚含量(g/L) 1.004±0.034 1.159±0.066 蛋白质含量(mg/L) 191.182±12.623 209.568±19.178 总酸含量(g/L) 8.6±0.3 6.4±0.2 还原糖含量(g/L) 16.215±0.083 8.409±0.021 酒精度(%vol) 6.7±0.2 10.6±0.3 由表4可知,经过优化,纯麦酒的总酚含量、蛋白质含量及酒精度出现了上升,而总酸含量及还原糖含量出现了下降。总酚含量由优化前的1.004±0.034 g/L增长为1.159±0.066 g/L,是优化前的1.154倍;蛋白质含量由优化前的191.182±12.623 mg/L增长为209.568±19.178 mg/L,是优化前的1.096倍;酒精度由优化前的6.7%vol±0.2%vol增长为10.6%vol±0.3%vol,是优化前的1.582倍,增长较为显著。相比之下,总酸含量由优化前的8.6±0.3 g/L降为优化后的6.4±0.2 g/L,降幅较小;还原糖含量由优化前的16.215±0.083 g/L降为8.409±0.021 g/L,下降明显,这与酒精度上升的结果是相一致的。
羟基自由基对人体具有极大的危害性,若大量聚集在心血管周围,会导致动脉硬化、高血压等心脑血管疾病的发生[32]。由图4可知,优化后的纯麦酒对羟基自由基的清除率可达86.75%±1.42%,相比于VC的37.74%±0.42%,高出了49.01%左右,这表明纯麦酒对于羟基自由基具有良好的清除能力。王晓静[33]在研究红果参黄酮与VC的协同抗氧化活性的过程中,证明VC与黄酮类化合物均为抗氧化物质,但两者结构并不相同,导致对包括羟基自由基在内的多种自由基清除能力不同。在本试验中,由于纯麦酒总酚含量较高,推测是由酚类物质与羟基自由基发生了反应,降低了羟基自由基的活性。
当一种物质具有较强的还原能力时,可以使反应体系中普鲁士蓝含量增加,并在700 nm波长处产生最大吸光值[34]。由图5可知,VC的总还原能力可达2.097±0.006,而优化后的纯麦酒的总还原能力可达1.842±0.004,略低于VC,但也表现出良好的总还原能力,具有良好的抗氧化效果。谢国芳等[35]对金刺梨果实和叶中酚类、VC含量及其抗氧化能力进行了分析,并表明总还原能力与果实中酚类及酸类物质含量呈正相关。在本试验中,纯麦酒总酚含量达到1.159±0.066 g/L,总酸含量达到6.4±0.2 g/L,推测是酚类物质及酸类物质赋予了纯麦酒较强的还原能力。综合以上数据,可以证明纯麦酒具有良好的抗氧化活性。
3. 结论
本试验采用单因素实验及正交设计方法对纯麦酒发酵工艺进行了优化,并对优化前后的纯麦酒进行了理化性质测定及对比。试验结果表明,在30 ℃发酵温度、料液质量体积比为1:3的情况下,最佳发酵条件组合为:发酵时间为4 d、酒曲接种量为2‰、糖化酶添加量为2%。通过正交试验方差分析,得出发酵时间与糖化酶添加量两个因素对于纯麦酒的酒精度影响显著(P<0.05),而接种量对纯麦酒酒精度的影响并不显著(P>0.05)。对优化后的纯麦酒进行部分理化性质的测定,测得总酚含量为1.159±0.066 g/L,蛋白质含量为209.568±19.178 mg/L,总酸含量为6.4±0.2 g/L,还原糖含量为8.409±0.021 g/L,所得纯麦酒酒精度为10.6%vol±0.3%vol,是优化前的1.582倍。同时对纯麦酒进行羟基自由基与总还原能力的测定,发现纯麦酒对羟基自由基的清除率可达86.75%±1.42%,总还原能力可达1.842±0.004,这表明纯麦酒展现出良好的抗氧化活性。试验结果为麦芽进一步开发利用提供理论依据,为纯麦酒作为新品种开拓市场提供参考。
-
表 1 纯麦酒发酵条件正交优化试验因素和水平
Table 1 Factors and levels of orthogonal experiments for fermentation conditions optimization of pure malt wine
水平 因素 (A)发酵时间(d) (B)酒曲接种量(‰) (C)糖化酶添加量(%) 1 3 1 1 2 4 2 2 3 5 3 3 表 2 正交试验结果
Table 2 Orthogonal test results
实验号 A B C 酒精度(%vol) 1 3 1 1 8.4 2 3 2 2 9.0 3 3 3 3 9.5 4 4 1 2 10.5 5 4 2 3 9.6 6 4 3 1 9.0 7 5 1 3 8.9 8 5 2 1 9.6 9 5 3 2 9.4 K1 8.967 9.267 9.000 K2 9.700 9.400 9.633 K3 9.300 9.300 9.333 R 0.733 0.133 0.633 表 3 正交试验方差分析表
Table 3 Analysis of variance of orthogonal test
因素 偏差平方和 自由度 F值 F临界值 显著性 A 0.809 2 27.897 19.000 * B 0.029 2 1.000 19.000 C 0.602 2 20.759 19.000 * 误差 0.03 2 注:“*”表示显著差异(P<0.05)。 表 4 纯麦酒理化性质测定对比
Table 4 Comparison of physical and chemical properties of pure malt wine
指标 优化前含量 优化后含量 总酚含量(g/L) 1.004±0.034 1.159±0.066 蛋白质含量(mg/L) 191.182±12.623 209.568±19.178 总酸含量(g/L) 8.6±0.3 6.4±0.2 还原糖含量(g/L) 16.215±0.083 8.409±0.021 酒精度(%vol) 6.7±0.2 10.6±0.3 -
[1] 辛卫云, 白明, 苗明三. 麦芽的现代研究[J]. 中医学报,2017,32(4):613−615. [XIN W Y, BAI M, MIAO M S. Modern study analysis on malt[J]. Acta Chinese Medicine,2017,32(4):613−615. [2] 凌俊红. 麦芽的化学成分及炮制学研究[D]. 沈阳: 沈阳药科大学, 2005. LING J H. Studies on the chemical constituents and the processing procedures of malt [D]. Shenyang: Shenyang Pharmaceutical University, 2005.
[3] 王波. 大麦芽的主要成分及其在食品工业中的应用[J]. 麦类作物学报,2017,37(9):1224−1231. [WANG B. Main components of barley malt and its application in food industry[J]. Journal of Triticeae Crops,2017,37(9):1224−1231. doi: 10.7606/j.issn.1009-1041.2017.09.13 [4] 许晓梅, 陶兴无, 刘仁禄, 等. 苦瓜麦芽混合汁饮料的发酵工艺研究[J]. 食品工业科技,2016,37(12):195−199,205. [XU X M, TAO X W, LIU R L, et al. Study on the fermentation technology of the mixed juice drink of bitter melon juice and wort[J]. Science and Technology of Food Industry,2016,37(12):195−199,205. [5] 于淼, 马明娟, 毋思敏, 等. 六款特种麦芽风味物质和感官特性分析[J]. 食品工业科技,2020,41(20):246−250,265. [YU M, MA M J, WU S M, et al. Sensory and volatile compounds analysis of six kinds of specialty malts[J]. Science and Technology of Food Industry,2020,41(20):246−250,265. [6] CARVALHO D O, CORREIA E, LOPES L, et al. Further insights into the role of melanoidins on the antioxidant potential of barley malt[J]. Food Chem, 2014(Oct 1),160: 127−33.
[7] LIGUORI L, DE FRANCESCO G, ORILIO P, et al. Influence of malt composition on the quality of a top fermented beer[J]. J Food Sci Technol,2021,58(6):2295−2303. doi: 10.1007/s13197-020-04740-8
[8] HELLWIG M, HENLE T. Maillard reaction products in different types of brewing malt[J]. J Agric Food Chem, 2020, 68(48):14274-14285.
[9] SHOPSKA V, DENKOVA-KOSTOVA R, DZHIVODEROVA-ZARCHEVA M, et al. Comparative study on phenolic content and antioxidant activity of different malt types[J]. Antioxidants (Basel), 2021(Jul 14),10(7): 1124. doi: 10.3390/antiox10071124.
[10] LANDETE J M. Dietary intake of natural antioxidants: vitamins and polyphenols[J]. Crit Rev Food Sci Nutr,2013,53(7):706−21. doi: 10.1080/10408398.2011.555018
[11] CÉLINE L, ERIC M, MARTINE B, et al. Fate of polyphenols and antioxidant activity of barley throughout malting and brewing[J]. Journal of Cereal Science, 2012, 55(3):318-322.
[12] GERHÄUSER C. Beer constituents as potential cancer chemopreventive agents[J]. Eur J Cancer,2005,41(13):1941−54. doi: 10.1016/j.ejca.2005.04.012
[13] SON H K, SHIN H W, JANG E S, et al. Gochujang prepared using rice and wheat koji partially alleviates high-fat diet-induced obesity in rats[J]. Food Sci Nutr, 2020(Feb 6),8(3): 1562-1574.
[14] 孙婷婷, 李洲, 周世水. 一种新型麦芽酒的快速发酵工艺研究[J]. 安徽农业科学,2017,45(2):108−110,117. [SUN T T, LI Z, ZHOU S S. Research on a rapid fermentation process of a new-type malt wine[J]. Journal of Anhui Agricultural Science,2017,45(2):108−110,117. doi: 10.3969/j.issn.0517-6611.2017.02.035 [15] 王娅玲, 李维峰, 郭芬, 等. 木奶果果酒加工工艺优化[J]. 食品工业科技,2020,41(15):188−191,197. [WANG Y L, LI W F, GUO F, et al. Optimization of processing technology of Baccaurea ramiflora wine[J]. Science and Technology of Food Industry,2020,41(15):188−191,197. [16] 孟金明, 樊爱萍, 李全丽, 等. 芒果胡萝卜复合果酒发酵工艺的研究[J]. 食品工业科技,2020,41(5):156−162. [MENG J M, FAN A P, LI Q L, et al. Study on fermentation technology of mango-carrot compound fruit wine[J]. Science and Technology of Food Industry,2020,41(5):156−162. [17] 李国辉, 高红波, 王道兵, 等. 葡萄酒和黄酒中酒精度快速测定方法研究[J]. 酿酒科技,2018(1):22−25. [LI G H, GAO H B, WANG D B, et al. Rapid determination of alcohol content of grape wine/yellow rice wine[J]. Liquor-Making Science and Technology,2018(1):22−25. [18] 赵晓娟, 李敏仪, 黄桂颖, 等. Folin-Ciocalteu法测定苹果醋饮料的总多酚含量[J]. 食品科学,2013,34(8):31−35. [ZHAO X J, LI M Y, HUANG G Y, et al. Determination of total polyphenols in apple vinegar drink by Folin-Ciocalteu method[J]. Food Science,2013,34(8):31−35. doi: 10.7506/spkx1002-6630-201308007 [19] 宋凤艳, 周超君. 蜂蜜中蛋白质及氨基酸含量的测定[J]. 现代食品,2016(20):108−110. [SONG F Y, ZHOU C J. The content determination of protein and amino acid in honey[J]. Modern Food,2016(20):108−110. [20] 董婷, 高鹏, 蒋毅等. 电子束辐照对芒果品质的影响[J]. 食品工业科技,2021,42(2):279−283, 289. [DONG T, GAO P, JIANG Y, et al. Effect of electron beam irradiation on mango quality[J]. Science and Technology of Food Industry,2021,42(2):279−283, 289. [21] 郭有辉, 周娟, 胡露, 等. DNS光度法测定风味鱿鱼中淀粉、还原糖和蔗糖的含量[J]. 理化检验(化学分册),2019,55(4):463−466. [GUO Y H, ZHOU J, HU L, et al. Determination of starch, reducing sugar and sucrose in flavored squid by DNS photometric method[J]. Physical and Chemical Inspection (Chemical Volume),2019,55(4):463−466. [22] 王祎然, 韦明明, 张涵, 等. 酸汤中乳酸菌的鉴定及其耐酸、耐胆盐和抗氧化活性[J]. 食品工业科技,2020,41(16):121−126,139. [WANG Y R, WEI M M, ZHANG H, et al. Identification, acid and bile salt tolerance, and antioxidant ability of lactic acid bacteria isolated from sour soup[J]. Science and Technology of Food Industry,2020,41(16):121−126,139. [23] 李颖畅, 王亚丽, 刘明爽, 等. 不同处理方式对紫菜多酚清除氧自由基的影响[J]. 食品工业科技,2014,35(10):138−141. [LI Y C, WANG Y L, LIU M S, et al. Effect of different treatment on scavenging oxygen free radicals of polyphenols from Porphyra dentate[J]. Science and Technology of Food Industry,2014,35(10):138−141. [24] 潘俊, 刘秀嶶, 石萍萍, 等. 白肉灵芝化学成分及体外抗氧化活性分析[J]. 食品工业科技,2021,42(9):340−346. [PAN J, LIU X, SHI P P, et al. Chemical constituents and antioxidant activities in vitro of Ganoderma leucocontextum[J]. Science and Technology of Food Industry,2021,42(9):340−346. [25] 宋越冬, 陈晓庆, 张毓敏, 等. 荞麦叶黄酮的提取工艺优化及其抗氧化性[J]. 食品工业科技,2021,42(7):180−187. [SONG Y D, CHEN X Q, ZHANG Y M, et al. Optimization of extraction process of flavonoids from fagopyrum esculentum moench leaves and its antioxidant properties[J]. Science and Technology of Food Industry,2021,42(7):180−187. [26] NGUYEN N H, NGUYEN M T, NGUYEN H D, et al. Antioxidant and antimicrobial activities of the extracts from different garcinia species[J]. Evid based Complement alternat Med,2021,2021:5542938.
[27] SHEHATA M G, AWAD T S, ASKER D, et al. Antioxidant and antimicrobial activities and UPLC-ESI-MS/MS polyphenolic profile of sweet orange peel extracts[J]. Curr Res Food Sci,2021(May 26), 4: 326-335.
[28] 万景瑞, 蒋鹏飞, 史冠莹, 等. 三种发酵酒活性成分、抗氧化活性及其香气成分对比分析[J]. 食品工业科技,2020,41(21):253−260,265. [WAN J R, JIANG P F, SHI G Y, et al. Comparative analysis of active ingredients, antioxidant activity and aromatic components of three kinds of fermented wine[J]. Science and Technology of Food Industry,2020,41(21):253−260,265. [29] SHI Q, WANG X, TANG X, et al. In vitro antioxidant and antitumor study of zein/SHA nanoparticles loaded with resveratrol[J]. Food Sci Nutr, 2021(May 7), 9(7): 3530-3537.
[30] 彭颖, 黄晴, 李珂. 发酵对小根蒜挥发性物质、有机硫化合物及其抗氧化活性的影响[J]. 食品工业科技,2020,41(22):43−49,56. [PENG Y, HUANG Q, LI K. Effects of fermentation on volatile compounds, organic sulfur compounds and antioxidant activity of Allium macrostemon Bunge[J]. Science and Technology of Food Industry,2020,41(22):43−49,56. [31] 谭富耀, 盛赵越, 胡婷, 等. 超声波辅助提取麻城福白菊总黄酮工艺优化及其抗氧化活性分析[J]. 食品工业科技,2020,41(14):154−159. [TAN F Y, SHENG Z Y, HU T, et al. Ultrasonic-assisted extraction optimization of total flavonoids from Macheng Chrysanthemum morifolium and its antioxidant activity[J]. Science and Technology of Food Industry,2020,41(14):154−159. [32] TIWARI M K, MISHRA P C. Scavenging of hydroxyl, methoxy, and nitrogen dioxide free radicals by some methylated isoflavones[J]. J Mol Model, 2018(Sep 21), 24(10): 287.
[33] 王晓静, 陈莉华, 莫宇婷. 红果参黄酮与VC的协同抗氧化活性[J]. 食品与发酵工业,2014,40(12):111−115. [WANG X J, CHEN L H, MO Y T. Cooperative antioxidant effects of flavonoids from Hong Guo ginseng and VC[J]. Food and Fermentation Industries,2014,40(12):111−115. [34] OH J M, HEONJOO J, AH R C, et al. Antioxidant and antimicrobial activities of various leafy herbal teas[J]. Food Control,2013,31(2):403−409. doi: 10.1016/j.foodcont.2012.10.021
[35] 谢国芳, 徐小燕, 王瑞, 等. 金刺梨果实和叶中酚类、VC含量及其抗氧化能力分析[J]. 植物科学学报,2017,35(1):122−127. [XIE G F, XU X Y, WANG R, et al. Analysis of phenolic, VC and antioxidant activity of fruits and leaves of Rosa sterilis D. Shi[J]. Plant Science Journal,2017,35(1):122−127. doi: 10.11913/PSJ.2095-0837.2017.10122 -
期刊类型引用(3)
1. 李亚俐,王雪莉,石柳,吴文锦,陈胜,陈朗,郭晓嘉,熊光权,汪兰,孙智达. 壳聚糖-绿原酸复合保鲜剂对冷藏鮰鱼片食用品质的影响. 肉类研究. 2025(01): 42-50 .  百度学术
百度学术
2. 武玫怡,焦文娟,赵甜甜,刘俊,周芳,刘伟峰,张业辉,南海军,陈晓瑛,黄利华. 高静水压与水煮处理对热带海参品质的影响. 肉类研究. 2025(01): 25-33 .  百度学术
百度学术
3. 崔燕,刘韩欣,朱麟,尚海涛,林旭东,陈曙颖,宣晓婷. 超高压杀菌对大黄鱼理化性质及滋味、风味的影响. 食品工业科技. 2025(05): 44-55 .  本站查看
本站查看
其他类型引用(3)





 下载:
下载:



 下载:
下载:



