Simulation of Vitamin C Degradation during Microwave Assisted Foam-mat Drying Process
-
摘要: 受干燥条件影响,食品原料中营养成分常发生降解,为阐明微波泡沫干燥条件对蓝靛果中维生素C稳定性的作用规律,本研究在对各影响因素进行通径分析的基础上,分阶段建立维生素C降解动力学模型,并据此建立多物理场仿真模型。结果表明:干燥过程中物料温度和含水率对维生素C降解同时存在直接影响和间接影响,温度升高和含水率下降均会导致维生素C降解量增加,其直接通径系数分别为−0.113和0.715。根据降解动力学方程可得,预热干燥阶段维生素C的降解活化能为3.926 kJ/mol,起泡干燥阶段维生素C的降解反应热为−0.515 kJ/kg,干燥后期是维生素C降解的主要阶段,应控制干燥条件缩短此阶段持续时间。多物理场仿真模型的实测值与模拟值偏差为4.36%,说明所建模型能较好地反映蓝靛果中维生素C在不同干燥阶段的分布和降解规律,由模拟结果可以直接观察到边缘处维生素C的降解速率始终高于中心区,且二者差值随干燥进行而增加。研究结果可为蓝靛果干制加工和维生素C降解分析提供理论依据。Abstract: The bioactive ingredients in berries are prone to degradation under different drying conditions. In order to clarify the effects of microwave assisted foam-mat drying (MFD) conditions on the stability of vitamin C in Lonicera caerulea, the degradation kinetic models of vitamin C were established in different drying stages based on the path analysis results. The temperature and the moisture content of berry pulp had both direct and indirect effects on the stability of vitamin C, and their direct path coefficients were −0.113 and 0.715, respectively. The degradation activation energy of vitamin C in preheating drying stage was 3.926 kJ/mol. The reaction heat of vitamin C in foaming drying stage was −0.515 kJ/kg. The drying conditions should be controlled to shorten the duration of rapid heating drying stage due to the large proportion of vitamin C degradation. The deviation between measured value and simulated value of the multi-physics simulation model was 4.36%, indicating that the model can be used to describe and predict the degradation rules of vitamin C under different drying stages. It could be directly observed from the simulation results that the degradation rate of vitamin C at the edge was always higher than the central area, and the difference between the two areas increased with drying progresses. The results of this study provided theoretical basis for the drying of Lonicera caerulea and the analysis of vitamin C degradation.
-
Keywords:
- Lonicera caerulea /
- microwave foam-mat drying /
- vitamin C /
- degradation /
- simulation
-
蓝靛果忍冬(Lonicera caerulea L.)为忍冬科忍冬属植物,简称蓝靛果,具有较强的生命力和抗寒能力[1]。蓝靛果果实呈蓝紫色,富含多种维生素、矿物质及类黄酮等营养物质,尤其是高含量的维生素C、花青素等活性成分具有较强的抗氧化能力,能有效降低人体血液中胆固醇浓度、缓解高血压、预防冠心病,是一种营养价值、食用价值和经济价值都很高的野生浆果,也被誉为“第三代水果”[2-4]。新鲜蓝靛果含水量在85%以上,由于其表皮较薄且柔嫩多汁,不适宜长时间储存或远距离运输。因此除必要的冷藏及冷冻处理外,干燥是蓝靛果采后延长储存期和开发深加工产品的重要方式。将蓝靛果干制后制成果粉,可以添加到饮料、糕点、糖果、馅料等食品中,既能增加食品的风味和色泽,又能作为天然抗氧化剂延长食品的贮存期,还可以作为膳食营养补充剂提高食品的营养价值[5-6]。
由于蓝靛果类物料内浆状物的糖浓度较高,且长时间高温富氧环境会导致蓝靛果中活性物质大量降解,因此常规的干燥方法如热风干燥法、喷雾干燥法均不适于浆果干燥[7-9]。泡沫干燥方法通过向物料中加入起泡剂,增加物料干燥表面积、提高干燥速度,现已在香蕉、芒果、木瓜等高粘度物料的脱水加工中得到广泛应用[10-12]。采用微波技术辅助泡沫干燥法进行蓝靛果脱水干制,能够在相对较低的温度下实现快速干燥,有助于提高蓝靛果的干燥效率和产品品质。
加工过程中营养物质含量的变化是评价生产工艺的重要指标,国内外对果蔬原料加工过程营养物质降解规律的研究很多,主要包括对活性成分降解量、降解动力学、降解过程模拟等方面的研究[13-15]。Clary等[16]采用微波干燥法对葡萄进行干燥,发现微波干燥法制得的葡萄干中维生素C降解量明显低于日晒法,这种对营养物质降解量的对比,适用于对某一物料不同干燥方法的初步选择,并不能对营养物质的降解规律进行分析。Agarry等[17]运用线性回归法确定木瓜和马铃薯干燥过程中抗坏血酸的降解均属于一级动力学反应,并得到两种物料的表观活化能,这种通过建立降解动力学方程的研究,能够得到温度对营养物质稳定性的作用规律,实现对食品加工或贮藏温度的选择,但干燥过程中除物料温度变化外,含水率的变化同样会对营养物质稳定性产生较大影响,但这经常被忽视,有关于物料含水率对营养成分稳定性影响的研究鲜有报道,因而十分有必要对影响营养成分降解的因素进行全面分析,以便更好地指导干燥过程、优化干燥工艺。本文在前期研究基础上,通过物料状态参数对蓝靛果中维生素C稳定性影响的通径分析,研究不同温度、含水率条件下维生素C的降解规律,分阶段建立微波干燥条件下维生素C降解的动力学方程,据此建立多物理场仿真模型,研究结果可为浆果干制工艺优化提供有效途径和技术参考。
1. 材料与方法
1.1 材料与仪器
新鲜蓝靛果 东北农业大学园艺学院试验站,初始含水率为90%(w.b.);分子蒸馏单甘脂(GMS) 广州佳士力添加剂(海安)有限公司;大豆分离蛋白(SPI) 临沂市山松生物制品有限公司;羧甲基纤维素(CMC) 天津市致远化学试剂有限公司;抗坏血酸标准品 天津市富宇精细化工有限公司;碳酸氢钠 天津市科密欧化学试剂有限公司;2,6-二氯靛酚 北京笃信精细制剂厂;试剂均为分析纯。
微波工作站 加拿大FISO公司;T-420型红外热像仪 美国FLIR Systems公司;JYL-Y5型高速破壁料理机 九阳股份有限公司;JJ-1型电动搅拌器 江苏省金坛市医疗仪器厂;ARRW60型电子精密天平 上海奥豪斯公司。
1.2 实验方法
1.2.1 起泡果浆的制备
蓝靛果果浆制备:选择成熟度一致的蓝靛果鲜果,去除残叶、果梗等杂质后,清洗、沥干,倒入高速破壁集中,充分粉碎5 min,直至果浆细腻、均匀、无颗粒物。起泡剂制备:以蒸馏水为溶剂,称取质量比为6%的分子蒸馏单苷脂(GMS)和3%的大豆分离蛋白(SPI)作为起泡剂,加入质量浓度0.5%的羧甲基纤维素(CMC)为稳定剂,70 ℃水浴30 min。起泡果浆制备:将蓝靛果果浆与起泡剂按1:1的质量比进行混合,再用电动搅拌器搅拌6 min,即得起泡果浆,根据前期研究结果可得此条件制得的起泡果浆稳定性最好[18]。
1.2.2 干燥过程
将100 g起泡果浆均匀平铺于直径为16 cm玻璃盘中,将其置于微波工作站转盘中心。每隔1 min测定微波功率在600~1000 W条件下,玻璃盘半径0、2、4、6、8 cm处起泡果浆温度、含水率和维生素C含量变化,当物料含水率降至15%时停止干燥,收集干制品进行粉碎即得到蓝靛果果粉。
1.2.3 温度的测定
将红外热像仪固定在三脚架上测量物料温度分布,利用FLIR Tools软件分析物料温度分布数据,为减小试验操作引起的误差,每次拍摄应在3~4 s内完成。
1.2.4 含水率的测定
采用直接干燥法测定物料含水率[19]。通过称量干燥过程中物料的质量损失,计算干燥过程中物料含水率的变化。称取2.0000~5.0000 g(精确至0.0001 g)待测样品,放入铝盒中,尽量使样品均匀平铺,厚度小于5 mm,加盖称量后置于干燥箱中,干燥2~4 h后取出,干燥器冷却30 min后称重。重复以上操作,直至前后两次质量差小于2 mg,记录此时铝盒的重量。样品的含水率(w.b.)按式(1)计算:
X=m1−m2m1−m0×100 (1) 式中,X为样品含水率(%),m1为干燥前样品及铝盒总质量(g),m2为恒重时样品及铝盒总质量(g),m0为铝盒质量(g)。
1.2.5 维生素C含量测定
蓝靛果中维生素C含量采用2,6-二氯靛酚滴定法进行测定[20]。称取52 mg碳酸氢钠,溶解于200 mL温度为60 ℃的蒸馏水中;将50 mg的2,6-二氯靛酚溶解于上述碳酸氢钠溶液中。冷却后定容至250 mL容量瓶,移至棕色瓶保存。使用前需用标准抗坏血酸标定其滴定度。取2 g左右待测样品,用浸提剂溶解并过滤,稀释定容至100 mL容量瓶中。吸取10 mL滤液置于50 mL锥形瓶中,用标定过的2,6-二氯靛酚溶液滴定,直至溶液呈粉红色,且15 s不褪色,维生素C含量计算式如下:
VC==(V−V0)×D×AW×100 (2) 式中,V为滴定样品溶液时消耗的染料溶液体积(mL),V0为滴定空白样时消耗染料溶液体积(mL),D为2,6-二氯靛酚滴定度(mg/mL),W为样品重量(g),A为稀释倍数。
1.2.6 维生素C降解模型的控制方程
微波工作站内矩形波导微波谐振腔中的电场分布可用麦克斯韦方程组求解。电磁波在有损介质(如食品)中传播时,会有能量的损耗,一部分电磁波的能量会转化为介质热能。将微波能转化为热能的能力与该物料的介电损耗因子及电场强度呈正比,可以用Poynting公式进行计算[21]。即单位时间单位体积起泡果浆吸收微波能所产生的体积热符合式(3):
Q(x,y,z,t)=2πfε0ε″E2 (3) 式中,Q为体积热(J/m3∙s),f为微波频率2.45(GHz),ε0为介电常数8.85×10−12(F/m),ε″为介电损耗因子,E为电场强度(V/m)。
1.2.7 维生素C降解模型的网格划分
模型网格的划分对模型的正确求解至关重要。采用自由三角形网格对模型进行网格剖分。对于电磁场问题的求解,被加热物料网格的最大尺寸(Smax)通常由Nyquist准则确定[22],如式(4)所示:
Smax (4) 式中,λ为波长(m),εr为相对介电常数,μ′为相对磁导率。
Zhang等[23]对此进行研究,发现在求解微波场时,模型网格尺寸可近似为微波波长的1/6,如方程(5)所示:
{{\rm S}_{\max }} = \frac{1}{6} \times {\text λ} (5) 1.3 数据处理
采用Sigmaplot 12.5(SPSS, 美国)对试验结果进行绘图和数据拟合;采用SPSS 24.0(IBM, 美国)进行干燥条件对维生素C稳定性影响的通径分析;采用COMSOL软件对浆果微波泡沫干燥过程进行过程模拟。实验数据结果均为三次实验平均值。
2. 结果与分析
2.1 微波泡沫干燥过程蓝靛果中维生素C含量变化规律
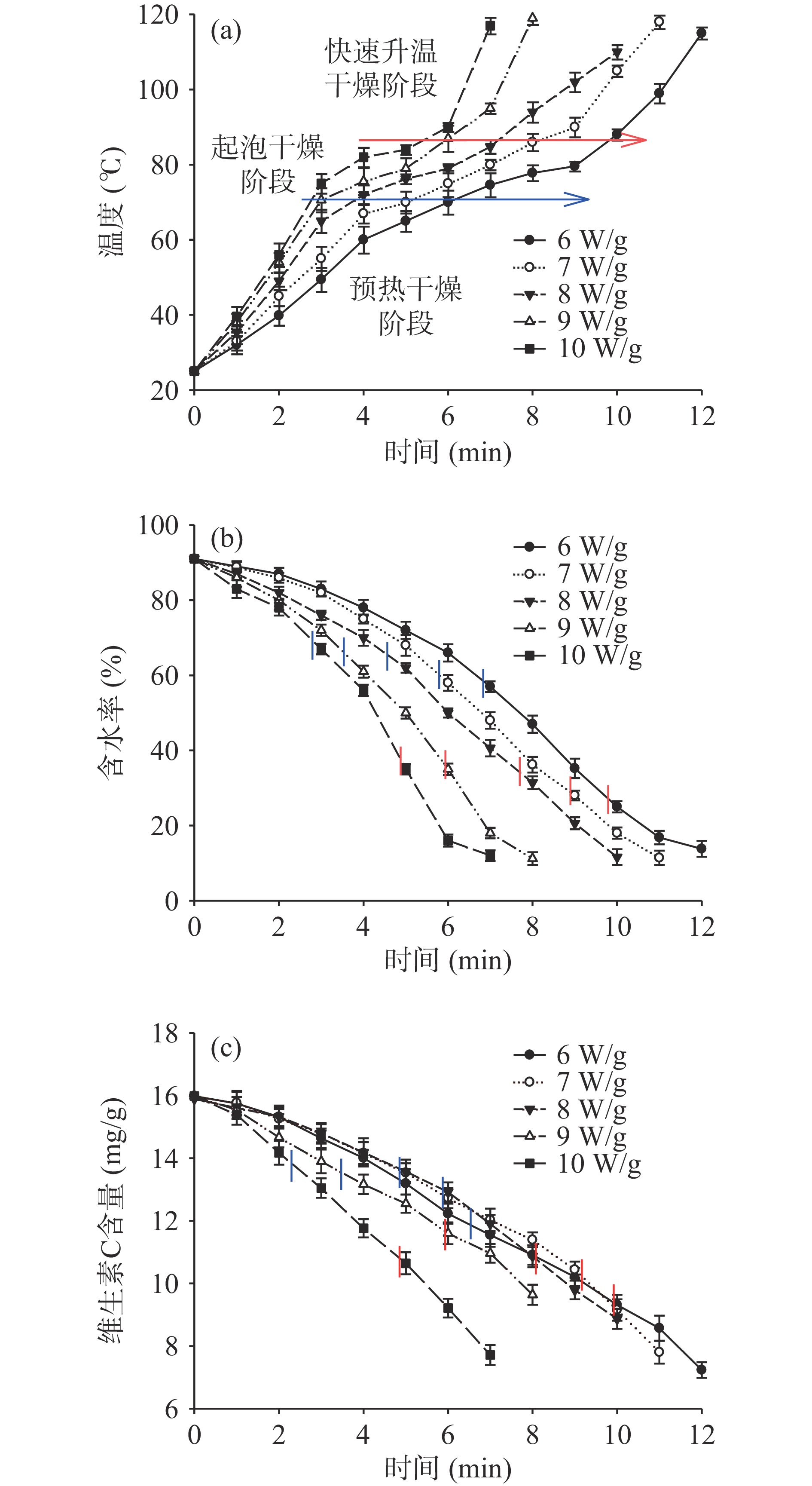
在微波强度6~10 W/g条件下,起泡果浆温度、含水率和维生素C含量的整体平均值变化如图1所示。由图1(a)和图1(b)可知,根据干燥过程中物料温度和含水率的变化特征,干燥过程大致分为三个阶段:预热干燥阶段物料温度由室温逐渐升高至75 ℃,此时物料含水率下降缓慢;起泡干燥阶段物料维持在75~85 ℃的温度区间,含水率开始快速下降至接近30%;快速升温阶段物料温度持续升高甚至高于100 ℃,含水率继续下降直至干燥终点。
由图1(c)可知,预热干燥阶段浆果中维生素C的降解量较低;除微波功率10 W/g外,起泡干燥阶段浆果中维生素C含量呈线性降低趋势,是因为此阶段物料温度在75 ℃上下浮动,该温度条件容易使热敏性维生素遭到破坏,同时此阶段物料含水率的快速下降导致糖浓度和酸浓度升高,亦不利于维生素C维持稳定性,这种高温、低含水率、高糖酸浓度导致的维生素C降解现象在快速升温阶段更加显著,该结果与桑葚干燥过程中营养物质的变化规律一致[24]。
2.2 维生素C降解量通径分析
通径分析是一种建立在多元回归基础上,分析多个自变量与因变量之间相关性的分析方法[25]。浆果温度、含水率和干燥时间等干燥条件为自变量,维生素C含量为因变量,采用通径分析法计算物料状态参数对维生素C含量的直接影响和间接影响,去除非显著项后,料状态参数各因素对维生素C稳定性影响的通径分析如表1所示。
表 1 影响因素对维生素C含量的通径分析Table 1. Path analysis of influencing factors on vitamin C content指标 相关系数 直接通径系数 间接通径系数 总和 X1 X2 X3 X1 −0.951** −0.113** −0.837* − −0.668* −0.170* X2 0.993** 0.715** 0.277* 0.106* − 0.172* X3 −0.982** −0.176** −0.806* −0.109* −0.697* − 注:**表示差异极显著(P<0.01),*表示差异显著(P<0.05);X1为温度,X2为含水率,X3为干燥时间。 由表1可知,温度与维生素C含量的相关系数为-0.951,二者呈负相关关系,其中直接通径系数为-0.113,通过含水率、干燥时间的间接通径系数分别为-0.668和-0.170,说明温度升高导致维生素C降解的原因既包括直接影响,也包括其他因素的间接影响,这与维生素C的热敏和光敏属性有关[26]。含水率与维生素C含量的相关系数为0.993,二者呈正相关关系,其中直接通径系数为0.715,通过其他因素产生的间接通径系数总和为0.277,说明高含水率有利于维持维生素C的稳定性,这与其水溶性本质有关[27]。干燥时间与维生素C含量呈负相关关系,且产生影响的主要为含水率变化产生的间接影响,说明随着干燥时间的延长,物料含水率的下降十分不利于维生素C保持稳定。
2.3 维生素C降解动力学分析
食品原料在加工过程中,其内部的营养成分尤其是小分子的活性物质常因外界环境和自身状态的改变发生不同程度的降解,其降解规律可用一级或二级反应动力学方程描述。为进一步明确蓝靛果干燥过程中维生素C的降解原因,有必要进行降解动力学分析。将不同微波强度条件下蓝靛果中维生素C含量变化值进行拟合,得到微波泡沫干燥过程中维生素C的降解符合一级反应动力学方程(6),对式(6)进行积分,可得式(7):
\rm c = {c_0}{{\text{e}}^{( - kt)}} (6) \rm {\text{ln}}\frac{c}{{{c_0}}} = {{ - }}kt (7) 式中,c0为维生素C初始含量(mg/g),c为t时刻维生素C含量(mg/g),t为干燥时刻(min),k为反应速率常数(min−1)。
反应速率常数k是反应发生快慢的表达,是反应活化能Ea和温度T的函数[28],它们之间符合Arrhenius方程,具体关系如式(8)所示:
\rm {k_T} = {A_T}{\text{exp}}\left( { - \frac{{{E_a}}}{{{R_g}T}}} \right) (8) 式中,kT为物料温度为T时的反应速率常数(min−1),AT为指前因子(min−1),Ea为反应活化能(kJ/mol),Rg为气体常数,8.314 J/(mol·K),T为物料温度(℃)。
依据Arrhenius方程建立的Erying公式,可用于描述压力变化对营养物质含量变化造成的影响[29]。对Erying公式进行改进,可以得到用于描述含水率改变时,反应速率常数k与降解反应热Ha和含水率M之间的关系,如式(9)所示:
\rm {k_M} = {A_M} \times \exp \left( {\frac{{ - {H_a} \times M}}{{{R_g} \times T}}} \right) (9) 式中,kM为含水率M条件下的反应速率常数(min−1),AM为指前因子(min−1),Ha为降解反应热(kJ/kg),M为物料含水率(%)。
由2.1分析可知,微波泡沫干燥过程不同干燥阶段物料状态和维生素C含量变化规律存在较大差异,因此有必要分阶段建立维生素C的降解动力学方程。
2.3.1 预热干燥阶段
预热干燥阶段为起泡果浆的蓄热阶段,由图1可知此阶段物料状态的改变主要来自于温度的升高,含水率变化量较小,因此可以用Arrhenius方程描述由于温度变化导致的维生素C降解过程,此时反应速率与温度的关系符合式(10)。
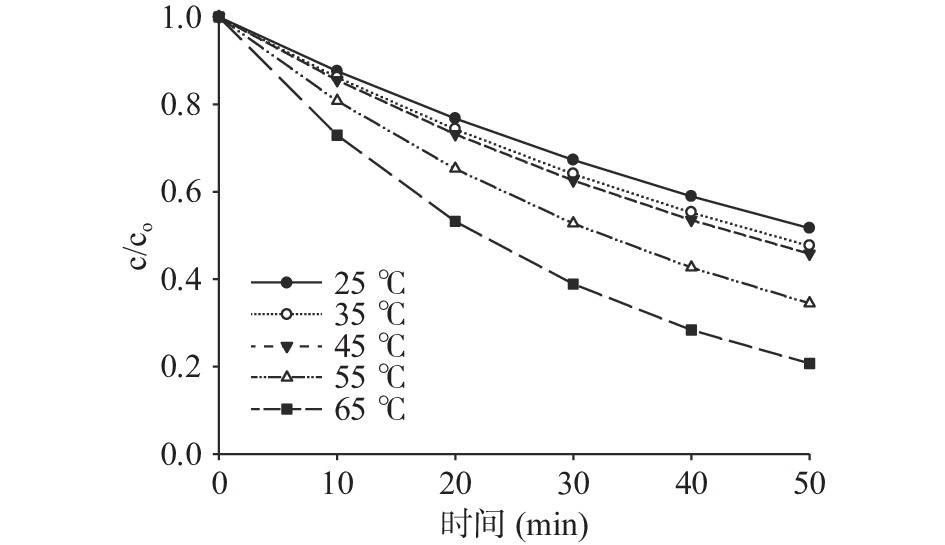
\rm {k_T} = {A_T} \times \exp \left[\frac{{ - {E_a}}}{R} \times \left(\frac{1}{T} - \frac{1}{{{T_0}}}\right)\right] (10) 设计实验研究温度对维生素C稳定性的影响,在起泡果浆含水率为90%条件下分别测定25~65 ℃时维生素C含量变化。
由图2可知,在含水率为90%条件下维生素C降解量随温度升高逐渐增加,在25~45 ℃条件下维生素C含量降解速率相对较低,在测定时间段内降解量小于50%,当温度高于55 ℃干燥35 min后维生素C降解量高于50%。微波泡沫干燥为短时快速干燥,干燥时间通常不超过15 min,由图可知,在含水率为90%的高含水率条件下,温度低于65 ℃时蓝靛果中维生素C降解量低于40%,此时维生素C相对稳定。对图2数据进行拟合,可得物料含水率为90%时,25~65 ℃条件下蓝靛果中维生素C的降解速率常数和降解活化能,如表2所示。
表 2 不同温度条件下维生素C降解速率常数和活化能Table 2. Degradation rate constants and activation energy of vitamin C in berry puree at different temperatureT(℃) 25 35 45 55 65 k(min−1) 0.0132±
0.00160.0148±
0.00120.0156±
0.00520.0213±
0.00120.0315±
0.0029Ea(kJ/mol) 3.926 2.3.2 起泡干燥阶段
起泡干燥阶段是物料中水分去除的主要阶段,由于此时物料吸收的微波能主要用于水分蒸发吸热,二者达到动态平衡,因而物料温度变化不大,仅在75 ℃上下浮动,由于此阶段物料状态的改变主要来自于含水率的快速下降,因此维生素C的降解过程可用改进的Erying方程(11)描述。
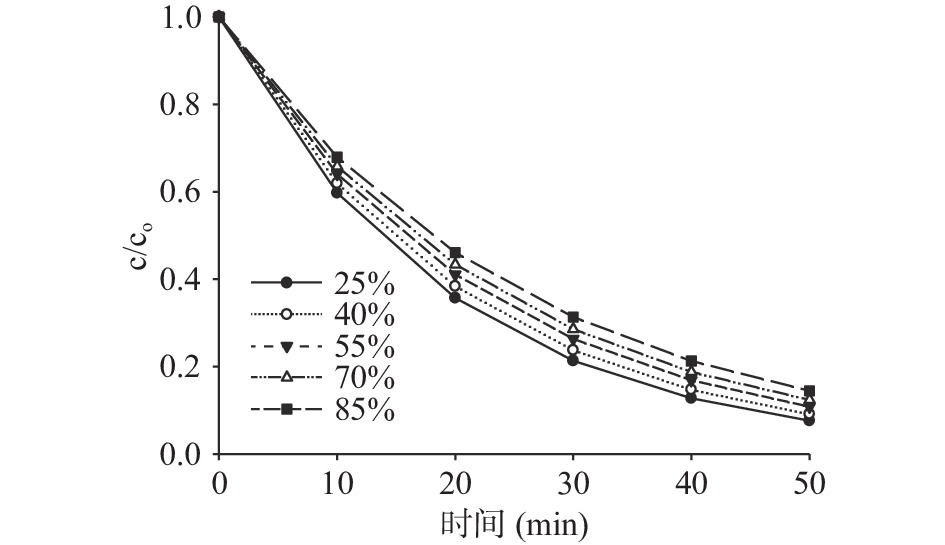
\rm {k_M} = {A_M} \times \exp \left[\frac{{ - {H_a} \times {M_{{H_2}O}}}}{{R \times T}} \times (M - {M_0})\right] (11) 为验证起泡干燥阶段含水率变化对维生素C稳定性的影响,分别测定含水率为25%、40%、55%、70%和85%条件下,物料在75 ℃时的维生素C含量变化。由图3可知,物料温度保持在75 ℃时,维生素C降解量与含水率呈反比,说明物料水分含量高对维生素C能起到一定的保护作用。
对图3中的数据与公式(11)进行拟合,可得起泡干燥阶段维生素C的降解速率常数和降解反应热如表3所示。
表 3 不同含水率下果浆中维生素C降解速率常数和反应热Table 3. Degradation rate constant and reaction heat of vitamin C in berry puree under different moisture contentsM(%) 25 40 55 70 85 k(10−2 min−1) 0.0515±
0.00140.0479±
0.00270.0445±
0.00350.0418±
0.00150.0387±
0.0063Ha(kJ/kg) −0.515 2.3.3 快速升温干燥阶段
快速升温阶段物料含水率较低,物料吸收的微波能一部分用于物料中剩余水分的继续蒸发,其余大部分表现为自身温度的继续升高,此阶段物料状态的改变既包含温度的变化,又包括含水率的变化,因而此时物料中维生素C的降解过程可由Arrhenius-Erying联合方程(12)描述。
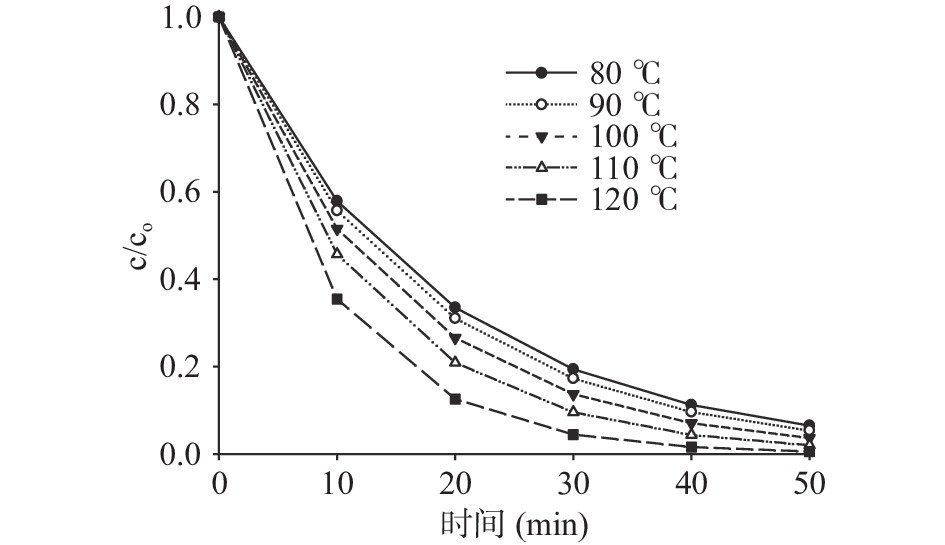
\begin{split}\rm k =& \rm{k_{ref}} \times \exp \left[\frac{{ - {E_a}}}{R} \times \left(\frac{1}{T} - \frac{1}{{{T_0}}}\right)\right] \times\\& \rm\exp \left[\frac{{ - {H_a} \times {M_{{H_2}O}}}}{{R \times T}} \times (M - {M_0})\right]\end{split} (12) 由图4可知,物料含水率低于30%,当物料温度由80 ℃升至120 ℃过程中,维生素C在10 min内的降解量超过50%;高于100 ℃条件下干燥20 min时,维生素C降解超过80%。此时维生素C含量下降与低含水率和过高温度的共同作用有关[30]。虽然微波泡沫干燥的快速升温阶段持续时间相对较短(约为1~3 min),但仍应控制干燥条件缩短此阶段的持续时间以减少物料中活性成分的降解,可通过变功率干燥模式、加入缓苏环节或引入真空条件等方式改进工艺[31]。
对上述结果进行拟合,可得此阶段降解速率常数、活化能及反应热如表4所示。
表 4 不同温度下维生素C降解速率常数、活化能和反应热Table 4. Degradation rate constants, activation energy and reaction heat of vitamin C in berry puree at different temperaturesT(℃) 80 90 100 110 120 k(10−2min−1) 0.0547±
0.04120.0585±
0.01520.0663±
0.00240.0783±
0.00270.1038±
0.0123Ea(kJ/mol) 2.239 Ha(kJ/kg) −1.362 2.4 维生素C降解模型
根据不同干燥阶段物料状态的变化,以能量守恒方程为基础,结合上述分析所得降解活化能和反应热,建立电磁场、温度场和浓度场多物理场耦合仿真模型,能够更加准确地描述在微波泡沫干燥过程中,物料内部同时进行的温度升高、含水率下降与维生素C降解过程。
为使所建模型更加符合实际,将物料的热特性参数和介电特征参数的动态变化表达式带入模型,建立起泡果浆微波泡沫干燥过程的能量守恒如方程(13)所示。
\begin{split}\rm Q(x,y,z,t) =&\rm {\text ρ} {C_p}\frac{{\partial T}}{{\partial t}}{\text{ + }}k{\Delta ^2}T + \\&{\text λ}\rm \frac{{\partial {M_E}}}{{\partial t}} + \left( {{c_0} - c} \right) \times {E_a} \end{split} (13) 式中,ρ为起泡果浆密度(kg/m3),CP为起泡果浆比热J/(kg·K),k为起泡果浆热导率W/(m·K),λ为蒸发潜热2.26×103 (kJ/kg),ME为蒸发量(kg);A为表面积(m2)。
任意时刻蓝靛果中维生素C的含量可根据式(14)计算[32]:
\rm C = a{C_0}\ln \frac{M}{T}{{ - }}b{C_0} (14) 式中,a、b为系数。
2.4.1 几何模型及网格划分
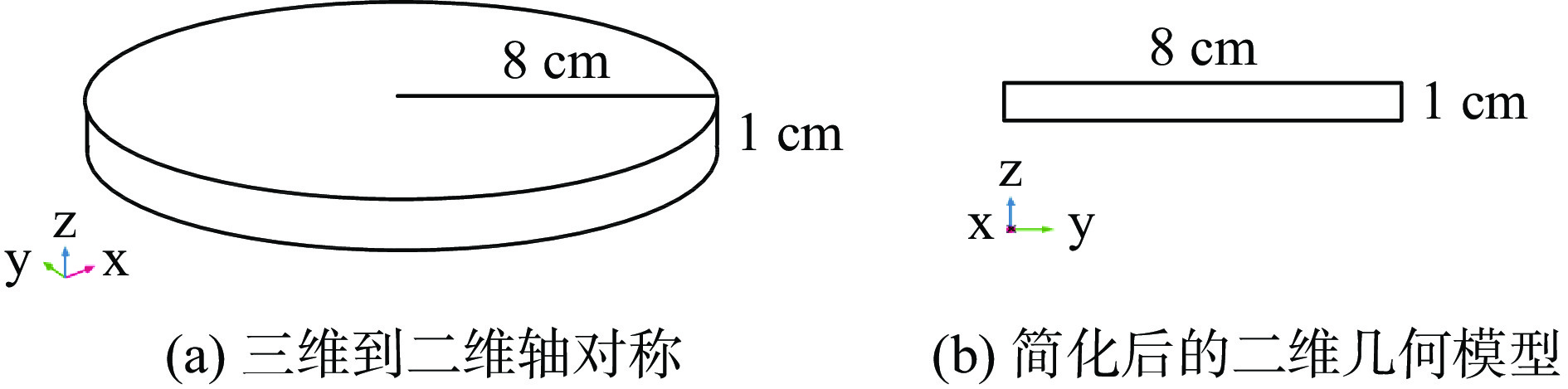
将盛装物料的玻璃圆盘视为轴对称结构,可在不影响仿真效果前提下,将三维结构简化为二维结构如图5(b)所示,以提高计算效率。
本研究采用的微波频率为2.45 GHz,确定果浆网格最大尺寸为λ/6,对于微波入射的果浆边界进行网格极细化剖分,边界最大网格尺寸为λ/18。活性成分降解几何模型的网格划分结果如图6所示。
2.4.2 初始条件与边界条件
假设物料内部的温度、含水率及维生素C含量在干燥开始时为均匀分布状态,初始温度为25 ℃,初始含水率为90%(w.b.),维生素C初始含量为15.98 mg/g。将微波产生的体积热作为边界热源。
2.4.3 模型的验证
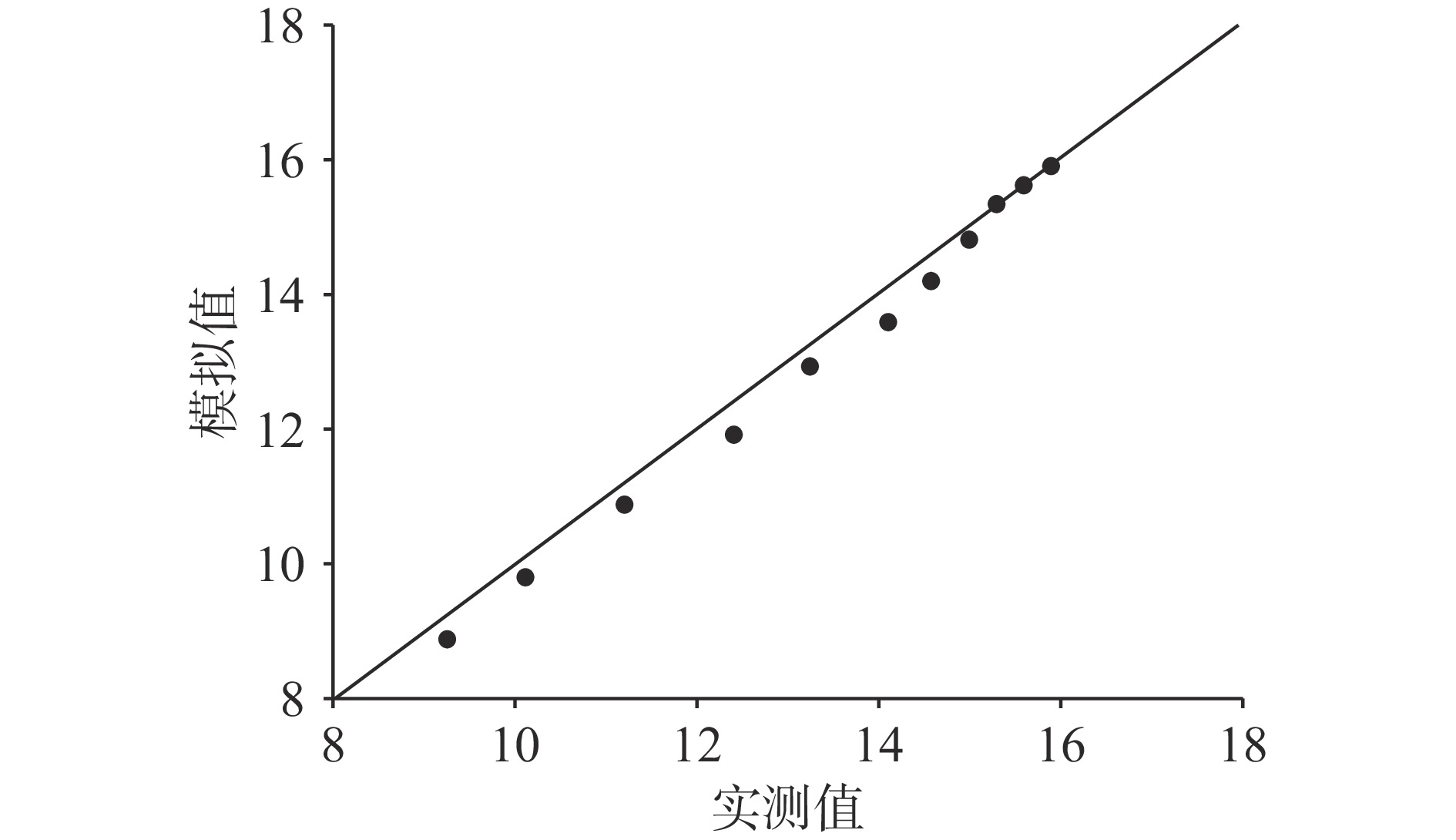
将控制方程及初始条件输入COMSOL Multiphysics软件,模拟微波泡沫干燥条件下蓝靛果中维生素C含量变化,模型计算结果与实验测定结果如图7所示。由图7可知,维生素C含量的实测值与模拟值均匀的分布在对角线两侧,计算实测值与模拟值的偏差,二者偏差为4.36%,说明所建模型能够较好地反映微波干燥过程中维生素C含量的变化。图7中实测值小于模拟值的原因,可能是由于模型建立时简化了泡沫的形成条件,而实际干燥过程中水分在物料表面和内部的气泡表面均有大量蒸发,因而导致模拟值高于实测值[33]。
2.4.4 维生素C降解速率分布模拟
降解速率(mol/m3·s)是对单位质量物料中营养物质在单位时间内降解量的表征,是分析该物质降解动力的重要指标。降解速率值越高代表该物质在所处环境中越容易降解,在污染物降解研究领域应寻求提高反应降解速率的途径[34],但本研究旨在寻求减少浆果中活性成分降解量的方式。
图8为微波强度为8 W/g时蓝靛果中维生素C在不同干燥阶段的降解速率分布模拟。由于其他微波强度下维生素C降解速率分布图的变化趋势较为相似,彼此间仅表现为图例赋值的差异,因此本文选取产品品质最好的中间强度8 W/g的模拟结果进行说明。由图可知,蓝靛果中维生素C含量分布不均匀,边缘降解量始终高于中心处,且随着干燥进行这种不同区域降解量的差异更加明显,该现象与果浆实际干燥状态及红外热像仪拍摄的浆果温度分布趋势一致,进一步说明物料边缘所处低含水率和高温环境不利于活性成分保持稳定。所建立的微波泡沫干燥过程模型,实现了对干燥过程的仿真模拟,通过仿真模型的结果分析,可以获得试验过程无法直接观察到或较难测定的物料参数变化,研究结果有助于揭示活性成分降解机理及进一步优化蓝靛果干燥条件。
3. 结论
试验表明,蓝靛果微波泡沫干燥中维生素C的稳定性与浆果自身状态参数变化密切相关,温度升高或含水率下降均会导致维生素C降解量增加,其中含水率为主要直接影响因素,其直接通径系数为0.715。温度升高是预热干燥阶段维生素C降解的主要因素,其降解活化能为3.926 kJ/mol;起泡干燥阶段维生素C降解主要受含水率下降的影响,其降解反应热为−0.515 kJ/kg;物料温度持续升高和含水率下降共同作用使快速升温阶段成为维生素C降解的主要阶段,改进工艺条件缩短此阶段将有助于提高所得干制品的品质。建立的多物理场仿真模型实测值与模拟值的偏差为4.36%,表明所建模型能够很好地描述维生素C的降解过程,通过仿真结果可以直观地获得试验时难以测量的参数变化,该模型在快捷性和准确性等方面具有优势,可为进一步优化浆果干制工艺提供依据。
-
表 1 影响因素对维生素C含量的通径分析
Table 1 Path analysis of influencing factors on vitamin C content
指标 相关系数 直接通径系数 间接通径系数 总和 X1 X2 X3 X1 −0.951** −0.113** −0.837* − −0.668* −0.170* X2 0.993** 0.715** 0.277* 0.106* − 0.172* X3 −0.982** −0.176** −0.806* −0.109* −0.697* − 注:**表示差异极显著(P<0.01),*表示差异显著(P<0.05);X1为温度,X2为含水率,X3为干燥时间。 表 2 不同温度条件下维生素C降解速率常数和活化能
Table 2 Degradation rate constants and activation energy of vitamin C in berry puree at different temperature
T(℃) 25 35 45 55 65 k(min−1) 0.0132±
0.00160.0148±
0.00120.0156±
0.00520.0213±
0.00120.0315±
0.0029Ea(kJ/mol) 3.926 表 3 不同含水率下果浆中维生素C降解速率常数和反应热
Table 3 Degradation rate constant and reaction heat of vitamin C in berry puree under different moisture contents
M(%) 25 40 55 70 85 k(10−2 min−1) 0.0515±
0.00140.0479±
0.00270.0445±
0.00350.0418±
0.00150.0387±
0.0063Ha(kJ/kg) −0.515 表 4 不同温度下维生素C降解速率常数、活化能和反应热
Table 4 Degradation rate constants, activation energy and reaction heat of vitamin C in berry puree at different temperatures
T(℃) 80 90 100 110 120 k(10−2min−1) 0.0547±
0.04120.0585±
0.01520.0663±
0.00240.0783±
0.00270.1038±
0.0123Ea(kJ/mol) 2.239 Ha(kJ/kg) −1.362 -
[1] CELLI G B, GHANEM A, BROOKS M. Haskap berries (Lonicera caerulea L. )-a critical review of antioxidant capacity and health-related studies for potential value-added products[J]. Food Bioprocess Technology,2014,7:1541−1554. doi: 10.1007/s11947-014-1301-2
[2] BASU A. Role of berry bioactive compounds on lipids and lipoproteins in diabetes and metabolic syndrome[J]. Nutrients,2019,11(9):1−11.
[3] RAUDSEPP P, ANTON D, ROASTO M, et al. The antioxidative and antimicrobial properties of the blue honeysuckle (Lonicera caerulea L. ), Siberian rhubarb (Rheum rhaponticum L. ) and some other plants, compared to ascorbic acid and sodium nitrite[J]. Food Control,2013,31(1):129−135. doi: 10.1016/j.foodcont.2012.10.007
[4] AS A, HJLA B. Lonicera caerulea: An updated account of its phytoconstituents and health-promoting activities[J]. Trends in Food Science and Technology,2021,107:130−149. doi: 10.1016/j.jpgs.2020.08.013
[5] HUI X, WU G, HAN D, et al. Bioactive compounds from blueberry and blackcurrant powder alter the physicochemical and hypoglycemic properties of oat bran paste[J]. LWT-Food Science and Technology,2021(4):111−167.
[6] SUN Y. Study on drying mechanism and technology of berry pulp under microwave assisted foam-mat drying[D]. Harbin: Northeast Agricultural University, 2018.
[7] BATU H S, KADAKAL E. Drying characteristics and degradation kinetics in some parameters of goji berry (Lycium Barbarum L.) fruit during hot air drying[J]. Italian Journal of Food Science,2021,33(1):16−28. doi: 10.15586/ijfs.v33i1.1949
[8] ZHAO G, HU C, LUO H. Effects of combined microwave-hot-air-drying on the physicochemical properties and antioxidant activity of Rhodomyrtus tomentosa berry powder[J]. Journal of Food Measurement and Characterization,2020,14(3):1−10.
[9] FU N, HUANG S, XIAO J, et al. Producing powders containing active dry probiotics with the aid of spray drying[J]. Advances in Food and Nutrition Research,2018,85:211−262.
[10] THUWAPANICHAYANAN R, PRACHAYAWARAKORN S, KUNWISAWA J, et al. Determination of effective moisture diffusivity and assessment of quality attributes of banana slices during drying[J]. LWT-Food Science and Technology,2011,44(6):1502−1510. doi: 10.1016/j.lwt.2011.01.003
[11] RAJKUMAR P, KAILAPPAN R, VISWANATHAN R, et al. Drying characteristics of foamed alphonso mango pulp in continuous type foam mat dryer[J]. Journal of Food Engineering,2007,79(4):1452−1459. doi: 10.1016/j.jfoodeng.2006.04.027
[12] HARDY Z, JIDEANI V. Foam-mat drying technology: A review[J]. Critical Reviews in Food Science and Nutrition,2015,57(12):2560−2572.
[13] ZHANG M, CHEN H Z, MUJUMDAR A S, et al. Recent developments in high-quality drying of vegetables, fruits, and aquatic products[J]. Critical Reviews in Food Science and Nutrition,2017,57(6):1239−1255. doi: 10.1080/10408398.2014.979280
[14] SUN Y, XUE H, LIU C H, et al. Comparison of microwave assisted extraction with hot reflux extraction in acquirement and degradation of anthocyanin from powdered blueberry[J]. International Journal of Agricultural and Biological Engineering,2016,9(6):186−199.
[15] MONICA A F, JOSEPH M, CRISTINA R. Drying of seabuckthorn (Hippophae rhamnoides L. ) berry: Impact of dehydration methods on kinetics and quality[J]. Drying Technology,2011,29(3):351−359. doi: 10.1080/07373937.2010.497590
[16] CLARY C D, MEJIAMEZA E, WANG S, et al. Improving grape quality using microwave vacuum drying associated with temperature control[J]. Journal of Food Science,2007,72(1):23−28. doi: 10.1111/j.1750-3841.2006.00234.x
[17] AGARRY S E, AREMU M O. Modeling of thermal degradation kinetics of ascorbic acid in pawpaw and potato[J]. Global Journal of Engineering Research,2011,10:1−9.
[18] SUN Y, ZHENG X Z, XU X W, et al. Drying properties and parameters of blue honeysuckles pulp under foam assisted microwave drying conditions[J]. International Journal of Food Engineering,2012,8(2):1168−1174.
[19] 中华人民共和国国家卫生和计划生育委员会. GB 5009.3-2016. 食品安全国家标准食品中水分的测定[S]. 北京: 中国标准出版社, 2017. National Health and Family Planning Commission of the People's Republic of China. GB 5009.3-2016. National food safety standard determination of moisture in food[S]. Beijing: China Standards Press, 2017.
[20] 中华人民共和国国家卫生和计划生育委员会. GB 5009.86-2016. 食品安全国家标准食品中抗坏血酸的测定[S]. 北京: 中国标准出版社, 2017. National Health and Family Planning Commission of the People's Republic of China. GB 5009.86-2016. National food safety standard determination of ascorbic acid in foods[S]. Beijing: China Standard Press, 2017.
[21] CHEN J, PITCHAI K, BIRLA S, et al. Heat and mass transport during microwave heating of mashed potato in domestic oven model development, validation, and sensitivity analysis[J]. Journal of Food Science,2015,79(10):1991−2004.
[22] RIZZOLI V, NERI A, MASOTTI D. Local stability analysis of microwave oscillators based on Nyquist's theorem[J]. Microwave and Guided Wave Letters, IEEE,1997,7(10):341−343. doi: 10.1109/75.631195
[23] ZHANG H, DATTA A K, TAUB I A. Electromagnetics, heat transfer, and thermo kinetics in microwave sterilization[J]. American Institute of Chemical Engineers Journal,2001,47(9):1957−1968. doi: 10.1002/aic.690470907
[24] 刘启玲, 王庆卫. 中短波红外干燥对桑葚干燥特性、营养品质及抗氧化活性的影响[J]. 食品工业科技,2021,42(12):39−45. [LIU Q L, WANG Q W. Effects of short and medium-wave infrared radiation drying on drying characteristics, nutritional quality and antioxidant activity of mulberry[J]. Science and Technology of Food Industry,2021,42(12):39−45. [25] TOEBE M, FILHO A C, STORCK L, et al. Sample size for estimation of direct effects in path analysis of corn[J]. Genetics and Molecular Research,2017,16(2):1−23.
[26] AABY K, GRIMSBO I H, HOVDA M B, et al. Effect of high pressure and thermal processing on shelf life and quality of strawberry purée and juice[J]. Food Chemistry,2018,260(15):115−123.
[27] VERBEYST L, BOGAERTS R, PLANCKEN I, et al. Modelling of vitamin C degradation during thermal and high-pressure treatments of red fruit[J]. Food and Bioprocess Technology,2013,6(4):1015−1023. doi: 10.1007/s11947-012-0784-y
[28] ABANO E. Kinetics and quality of microwave assisted drying of mango (Mangifera indica)[J]. International Journal of Food Science,2016,16:1−10.
[29] VERBEYST L, CROMBRUGGEN K V, VAN P I, et al. Anthocyanin degradation kinetics during thermal and high pressure treatments of raspberries[J]. Journal of Food Engineering,2011,105(3):513−521. doi: 10.1016/j.jfoodeng.2011.03.015
[30] CHEN Q, LI Z, BI J, et al. Effect of hybrid drying methods on physicochemical, nutritional and antioxidant properties of dried black mulberry[J]. LWT-Food Science and Technology,2017,80:178−184. doi: 10.1016/j.lwt.2017.02.017
[31] SUN Y, ZHANG Y H, XU W, et al. Analysis of the anthocyanin degradation in blue honeysuckle berry under microwave assisted foam mat drying[J]. Foods,2020,9(4):397−409. doi: 10.3390/foods9040397
[32] 孙宇, 朱勇, 秦庆雨, 等. 微波泡沫干燥树莓果浆活性成分降解过程模拟[J]. 东北农业大学学报,2018,49(12):79−89. [SUN Y, ZHU Y, QIN Q Y, et al. Simulation of degradation process of berry's active content subjected to microwave assisted foam drying conditions[J]. Journal of Northeast Agricultural University,2018,49(12):79−89. doi: 10.3969/j.issn.1005-9369.2018.12.010 [33] LIU C, LIU C H, XUE H, et al. Effect of microwave energy dissipation on drying process of berry puree under microwave foam drying conditions[J]. Drying Technology,2017,35(11):1388−1397. doi: 10.1080/07373937.2017.1329741
[34] TIAN Y S, MEI X X, LIANG Q, et al. Biological degradation of potato pulp waste and microbial community structure in microbial fuel cells[J]. RSC Advances,2017,7(14):8376−8380. doi: 10.1039/C6RA27385H
-
期刊类型引用(3)
1. 杨春晖,王文平,续丹丹,崔宇倩,鞠岩,许春艳,吕小婷. 不同原料酿造酱油功能成分及抗氧化活性比较. 食品工业科技. 2023(14): 318-325 .  本站查看
本站查看
2. 张荣,古丽吉合热·阿布拉. 新疆黑枸杞原花青素的提取及抗氧化活性研究. 食品工业. 2023(12): 27-31 .  百度学术
百度学术
3. 只德贤,张妮,李建颖. 微波超声协同提取白刺果原花青素工艺及抗氧化性研究. 食品工业科技. 2022(13): 171-179 .  本站查看
本站查看
其他类型引用(2)










 下载:
下载:











 下载:
下载:



