Anthocyanin Distribution and Sampling Method in Colored Potato Tubers
-
摘要: 为考察花色苷在马铃薯块茎中的含量分布差异,探讨兼具代表性和经济性的科学取样方法。试验选取颜色不同的三个彩色马铃薯品种(系):黑金刚、品系21-1和剑川红作为试验材料,从块茎大小、薯块纵向、横向三个角度分析了马铃薯花色苷的含量差异。结果表明:同株采收的马铃薯,大、中、小薯间花色苷含量存在显著性差异(P<0.05),差异程度受品种(系)因素影响;同一块茎中,花色苷含量沿横向分布存在显著性差异(P<0.05),横向分布上薯皮中花色苷含量显著高于薯肉。其中,剑川红薯皮中花色苷含量约是薯肉中的7倍,黑金刚薯皮中花色苷含量约是薯肉中的2.5倍,品系21-1薯皮中花色苷含量比薯肉中高1.5倍;在纵向分布上,花色苷含量亦存在显著性差异(P<0.05)。其中,黑金刚与21-1的块茎顶部和脐部花色苷含量显著高于中部,剑川红的块茎顶部花色苷显著高于中部和脐部;部分取样对整体的代表性方面:分别以块茎纵切后按取对角2份、随机取1份和取整薯三种方式取样,花色苷在三种取样方式下测定结果差异不显著(P˃0.05),表明通过纵切取少部分薯块样本即可满足对整体块茎花色苷含量水平的有效定量;样品打浆与样品研磨相比,显著降低了块茎花色苷的含量测定结果(P<0.05),不适用于研究分析。因此,纵切取对角的取样方式适用于马铃薯花色苷含量检测时块茎取样。Abstract: In order to investigate the difference of anthocyanin distribution in potato tuber and explore the most applicable method for sampling economically and scientifically, three colored potato materials, ‘Heijingang (variety)’, ‘21-1 (line)’ and ‘Jianchuanhong (variety)’ with various pigment accumulation were selected for the analysis of the tuber anthocyanin content depend on the size (large, middle and small) and length (longitudinal and the lateral) of the tuber, as well as the angle (transversely, vertically and diagonally) from where the tuber was cut for sampling. The results showed that the distribution of the potato anthocyanins in the same species was significantly different due to the material and size differences (P<0.05). In the same tuber, the allocation of anthocyanins was of significant difference along the horizontal area, which was significantly higher in the potato flesh (P<0.05). Specifically, the anthocyanins level in the skin of ‘Jianchuanhong’ was about 7-fold higher than the flesh, while it was 2.5-fold and 1.5-fold higher in ‘Heijingang’ and ‘21-1’ respectively. By comparison, in the longitudinal distribution, anthocyanins contents in the top and umbilical regions of the ‘Heijingang’ and ‘21-1’ were both significantly higher than the middle part, whereas the top of the ‘Jianchuanhong’ was significantly higher than the middle and the umbilical area (P<0.05). Relatively, the three methods utilized to cut the tubers from three angles did not reflect significant differences in terms of the anthocyanin quantification (P˃0.05), showing that sample lesser amount of the tuber through the diagonal cut might be a much more efficient and economical way for the potato pigment analysis. Lastly, this study also compared the analytical effects between tuber grinding and pulping, demonstrating that the pulping method could cause the anthocyanin loss drastically (P<0.05), which was not an appropriate way for the potato tuber pigment quantification. Thus, cutting the potato tuber from a morphologically diagonal angle with lesser amount would be a quite favorable approach for the lab detection of potato tuber anthocyanins.
-
Keywords:
- colored potato /
- anthocyanin /
- distribution difference /
- sampling methods
-
花色苷(anthocyanin)是植物中普遍存在的一种黄酮类次生代谢产物,可使植物器官呈现出红色、紫色、蓝色等颜色[1-2]。研究表明,花色苷在清除自由基、抗氧化[3-4]、抗炎[5]、调节血脂血糖[6]及抗癌抗肿瘤[7-9]等方面效果显著。同时,从植物中提取获得的花色苷亦可代替人工合成色素,能够作为食品添加剂[10-11]。随着对天然色素需求的不断增多以及大健康产业的持续发展,富含花色苷的植物已成为天然色素生产的重要来源[12-13]。
马铃薯(Solanum tuberosum L.)是全球第四大主粮作物,同时也是重要的工业原料[14]。彩色马铃薯因其所含花色苷稳定[15]、产量高、营养价值丰富、耐储藏等特点,作为获取天然花色苷的植物源材料之一[15]。近年来,我国的育种工作者加大了对彩色马铃薯的良种繁育,目前已培育出多个彩色马铃薯品种,例如“紫云1号”、“黑美人”、“黑金刚”等[16]。不同彩色马铃薯品种间花色苷含量差异较大[17],是故对花色苷的精确定量成为彩色马铃薯种质资源评价的重要依据。张静等[18]研究发现在整个马铃薯块茎中,花色苷的含量高低分布依次为“皮”>“环”>“肉”,这一分布趋势亦被报道于多数研究中[17-20]。Lewis等[21]研究发现马铃薯品种Desiree的花色苷首先在小块茎的茎端(脐部)产生,之后才在芽端(顶部)合成,由此表明花色苷在马铃薯块茎中的生物合成与积累存在分布性差异。
pH示差法与高效液相色谱法(High Performance Liquid Chromatography,HPLC)是科学研究和食品工业中常用的测定样品内花色苷含量的方法[22]。Lee等[22]在2008年通过pH示差法和HPLC分析了7种含有不同花色苷的果汁,结果表明在测定样品的花色苷总量时,pH示差法与HPLC法具有较高的相关性和一致度,pH示差法是一种简单、经济、快速并可靠的测定总花色苷的方法。样品提取液的最大吸收波长跟样品所含花色苷成份相关,成份相似则最大吸收波长相似[23]。
由于花色苷在块茎中较为不均匀的分布,因此对块茎的取样方法在一定程度上影响了花色苷定量的准确性,探索如何通过有效取样来实现对彩色马铃薯材料的鉴选与评价是研究花色苷在块茎中分布积累机制的前提,同时也将有助于确认专门针对块茎花色苷分析的科学取样与定量分析手段。基于此,本试验以云南农业大学薯类作物研究所自主培育的彩色马铃薯品系21-1和云南地方品种剑川红、主栽品种黑金刚为研究材料,通过采用不同的取样方法,考察了花色苷在三份马铃薯材料的块茎中的含量分布差异,探讨可代表整个块茎状态的合理取样方法,以期为富含花色苷的彩色马铃薯资源评价及后续深入探索其生物合成机制的研究提供相关参考。
1. 材料与方法
1.1 材料与仪器
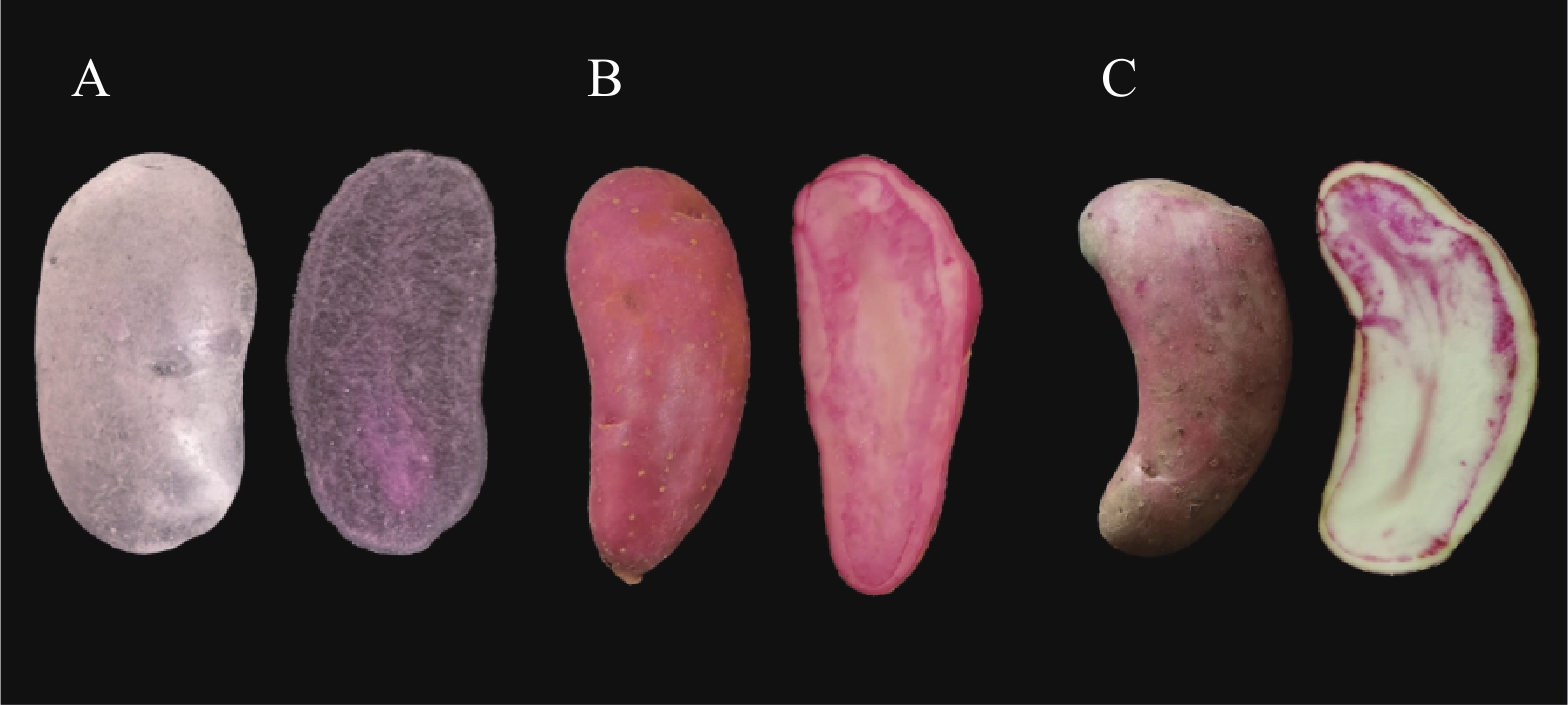
彩色马铃薯品系21-1(自育品系,来源于云南省地方品种剑川红的自交种)、品种黑金刚、品种剑川红 在云南农业大学校内试验基地种植,三份马铃薯材料的表型特征如表1和图1所示;无水乙醇 分析纯,天津大茂化学试剂厂;氯化钾 分析纯,成都金山化学试剂有限公司;乙酸钠 分析纯,上海源叶生物科技有限公司;其他试剂 均为国产分析纯。
表 1 试验材料Table 1. Test materials品种 薯形 薯皮色 薯肉色 黑金刚(A) 椭圆 紫色 紫色 21-1(B) 长椭圆 红色 红白镶嵌 剑川红(C) 长椭圆 红色 红色 紫外可见光分光光度计 北京普析通用仪器有限责任公司;PHS-3C pH计 上海仪电科学仪器股份有限公司;XZ-10 DTD超声波清洗机 宁波新芝生物科技股份有限公司;Allegra 64R Centrifuge高速冷冻台式离心机 贝克曼库尔特商贸(中国)有限公司;超纯水器 北京历元电子仪器有限公司;破壁料理机 沃佳健牌HH-1001。
1.2 实验方法
1.2.1 花色苷提取
马铃薯花色苷提取方法,采用Fuleki等[24]的方法进行改进,称取新鲜马铃薯样品1 g,加入5 mL提取液(酸化乙醇,95%乙醇与1.5 mol/L盐酸体积比85:15),磨碎,转移到50 mL离心管中,用15 mL提取液冲洗研钵两次,冲洗液转移至50 mL离心管中,摇匀1 min后,放入温度45 ℃,功率400 W超声清洗锅中,超声提取30 min,在5000 r/min条件下,离心5 min,然后吸取上清液。将滤渣加10 mL提取液重提一次,将2次提取液合并,在5000 r/min条件下,离心5 min取上清液4 ℃避光保存。
1.2.1.1 样品最大吸收波长比较
在pH示差法测定总花色苷含量时,为确定最大吸收波长,比较花色苷提取液与经pH1.0缓冲液(质量浓度为1.86 g/L的盐酸-氯化钾缓冲液,称取1.86 g氯化钾,加入蒸馏水至约980 mL,测其pH,用盐酸调节至pH1.0,移入1 L容量瓶,用蒸馏水稀释至容量瓶)稀释的提取液,在可见光下测量最大吸收波长差异。
1.2.1.2 同株不同大小块茎花色苷比较
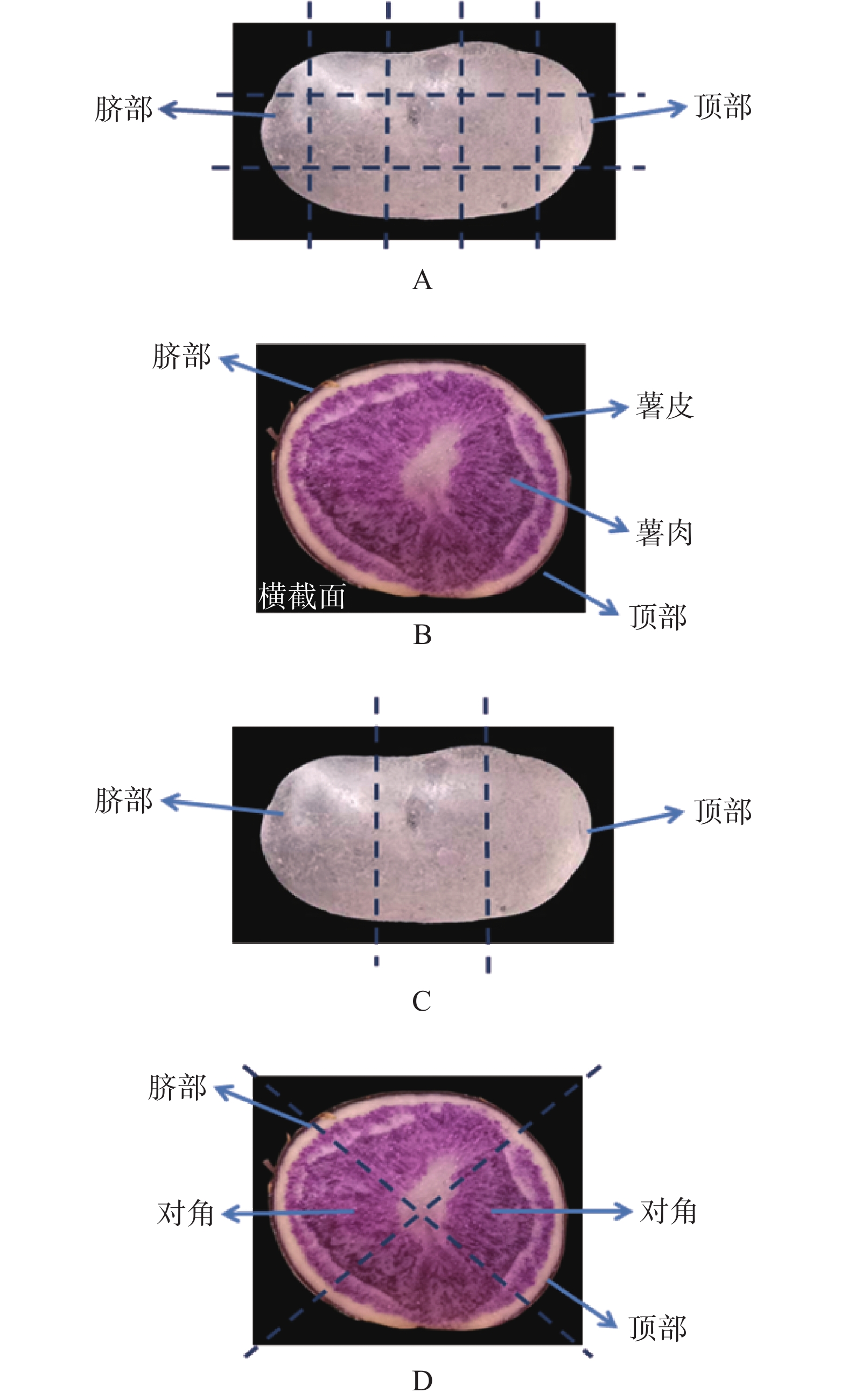
将单株收获的马铃薯,清洗晾干后,按大薯(≥100 g)、中薯(50~100 g)、小薯(≤50 g)分级,然后整薯切碎研磨(见图2A),测定花色苷含量。
1.2.1.3 块茎薯皮薯肉花色苷比较
用刮皮刀将薯皮与薯肉分离(见图2B),分别测定薯皮与薯肉花色苷含量,比较花色苷含量差异。
1.2.1.4 块茎横切不同部位花色苷比较
沿着从顶部到脐部等距横切马铃薯块茎,将其分成顶部、中部、脐部三部分(见图2C),分别测各部分花色苷含量。
1.2.1.5 块茎纵切不同部位花色苷比较
将块茎纵切成不同等份取对角或取其中一份(见图2D)测其花色苷含量。
1.2.1.6 不同样品破碎方式对花色苷提取效果比较
为找到更省力更简单的方法,比较块茎经刀片打浆机打浆与切碎研磨处理后花色苷提取差异。
1.2.2 最大吸收波长扫描
取花色苷提取液1 mL用pH1.0缓冲溶液(质量浓度为1.86 g/L的盐酸-氯化钾缓冲液)稀释5倍,扫描400~650 nm之间的可见吸收光谱,以确定每个品种(系)在可见光区的最大吸收波长λmax。
1.2.3 总花色苷测定
采用pH示差法[23-25]测定块茎中总花色苷含量。取花色苷提取液1 mL用pH1.0(称取1.86 g氯化钾,加入蒸馏水至约980 mL,测其pH,用盐酸调节至pH1.0,移入1 L容量瓶,用蒸馏水稀释至容量瓶)和pH4.5(称取54.43 g乙酸钠,加入蒸馏水约960 mL,测其pH,用盐酸调节pH至4.5,移入1 L容量瓶,用蒸馏水稀释至容量瓶)的缓冲溶液稀释5倍,室温下避光平衡60 min,以蒸馏水为空白,分别在最大吸收波长λvis-max和700 nm波长处测定吸光度Amax、A700。
总花色苷含量(total anthocyanins content, TAC)按矢车菊素-3-葡萄糖苷表示,公式如下:
(1) (2) 式中:△A表示提取液在两种pH下吸光度的差值;M表示花色苷分子量449.2 g/mol;DF表示稀释倍数,本实验中为5倍;V表示提取液体积(mL),本实验中为30 mL;ε表示矢车菊素-3-葡萄糖苷消光系数26900 L/cm·mol;L表示比色皿宽度,本实验中为1 cm;mf表示样品质量,g。
1.3 数据处理
每个处理进行三次重复,采用SPSS Statistics 26进行数据处理与统计分析,通过Duncan法(P<0.05)进行ANOVO分析,使用GraphPad Prism 8进行图形绘制。
2. 结果与分析
2.1 不同品种(系)最大吸收波长比较
将三个马铃薯品种(系)的花色苷提取液分别经提取液和pH1.0缓冲液稀释,直到最大吸收波长处的吸光度在分光光度计的线性范围内,本研究中稀释倍数为5倍。光谱扫描结果见表2,不同材料的薯皮和薯肉的花色苷提取液经提取液稀释与经pH1.0缓冲液稀释5倍后最大吸收波长差异显著(P<0.05),pH1.0缓冲液稀释后最大吸收波长向前偏移。21-1与剑川红最大吸收波长相近,表明二者的花色苷成份较为相似;黑金刚最大吸收波长与21-1,剑川红最大吸收波长差异较大,一定程度上反映出黑金刚与其他两个品种(系)的花色苷成分有所差异;同一品种的的薯皮和薯肉的最大吸收波长相近,表明其花色苷成份相似。通过该试验确定黑金刚、21-1、剑川红花色苷测定所使用的最大吸收波长分别为528、505、505 nm。
表 2 花色苷提取液与缓冲稀释液在可见光区的最大吸收波长比较Table 2. Comparison of the maximum absorption wavelengths of anthocyanins extract and buffer diluent in visible light region品种 可见光最大吸收波长(nm) 薯皮提取液 缓冲液稀释(薯皮) 薯肉提取液 缓冲液稀释(薯肉) 黑金刚 537.2a 527.8b 537.6a 528.0b 21-1 515.2c 504.8d 513.8c 504.2d 剑川红 515.6c 504.8d 513.8c 503.2d 注:不同字母表示差异显著,P<0.05。 2.2 同株不同大小块茎的花色苷含量比较
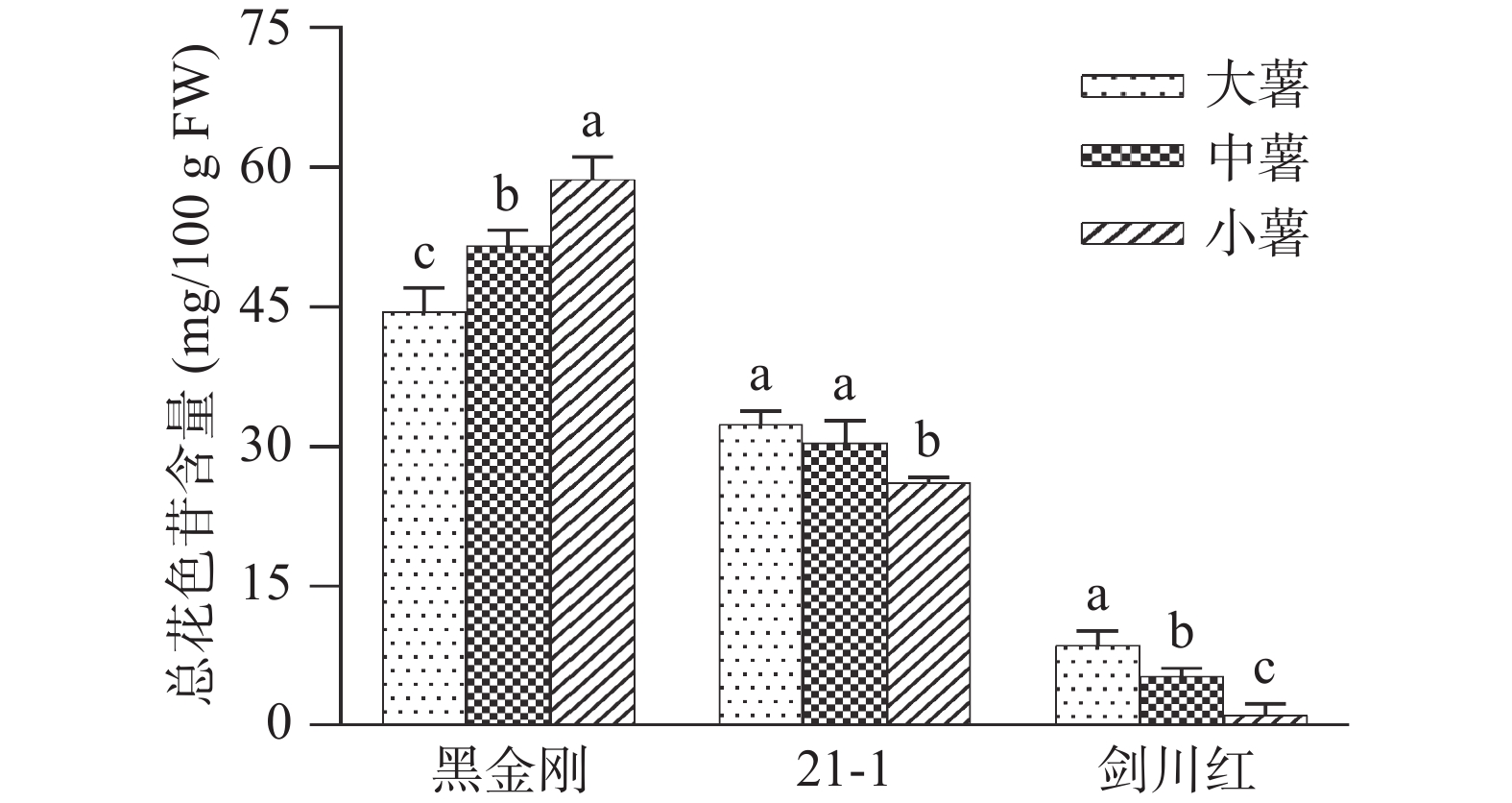
不同品种(系)大、中、小薯的花色苷含量如图3所示。黑金刚大、中、小薯花色苷含量存在显著性差异(P<0.05),其中,小薯的花色苷含量最高,大薯含量最低。品系21-1的三种类型薯块的花色苷含量在大薯和中薯间差异不显著(P˃0.05),但显著高于小薯(P<0.05)。相比之下,剑川红大、中、小薯的花色苷含量均存在显著差异,表现为大薯>中薯>小薯(P<0.05)。总体上,三个品种(系)花色苷含量不同,而且大、中、小薯间差异明显。
2.3 彩色马铃薯薯皮与薯肉间花色苷含量的差异比较
三个品种(系)横向不同部位花色苷含量如图4所示。黑金刚薯皮中花色苷的含量为105.7 mg/100 g FW,薯肉中花色苷含量为42.9 mg/100 g FW,薯皮中花色苷含量是薯肉中花色苷含量的2.5倍,黑金刚薯皮与薯肉花色苷含量达到显著性差异(P<0.05);21-1薯皮中花色苷含量为34.5 mg/100 g FW,薯肉中花色苷含量为22.5 mg/100 g FW,薯皮与薯肉中花色苷含量差异显著(P<0.05)。剑川红薯皮中花色苷含量为19.5 mg/100 g FW,薯肉中花色苷含量为2.7 mg/100 g FW,薯皮中花色苷是薯肉花色苷含量的7.2倍,两者差异达显著水平(P<0.05)。
2.4 彩色马铃薯块茎花色苷纵向分布差异比较
不同品种纵向不同部位花色苷含量如图5所示。对黑金刚品种在形态学上的块茎顶部、中部、脐部花色苷含量进行方差分析,结果显示其顶部、中部、脐部花色苷存在显著性差异(P<0.05),中部花色苷低于顶部和脐部,顶部和脐部花色苷含量差异不显著(P˃0.05)。品系21-1块茎中3个部位花色苷含量差异显著(P<0.05),中部含量低于顶部和脐部,顶部与脐部的花色苷含量差异不显著(P˃0.05)。剑川红顶部花色苷含量从顶部到脐部花色苷逐渐降低,纵向分布上差异显著(P<0.05),顶部花色苷含量显著高于中部和脐部(P<0.05),中部和脐部差异不显著(P>0.05)。
2.5 彩色马铃薯块茎纵切不同等份取样方式差异比较
黑金刚、21-1、剑川红纵切不同等份取对角花色苷含量测定结果如图6A所示。黑金刚、21-1、剑川红纵切不同等份取对角花色苷含量方差分析结果显示,整薯、纵切四等份取对角、纵切八等份取对角所测花色苷含量无显著性差异(P˃0.05)。
通过对三个品种(系)马铃薯块茎纵切两等份、四等份、八等份,各取其一份与整薯花色苷含量测定结果相比如图6B所示。黑金刚、21-1、剑川红4种取样方法花色苷含量方差分析显示,4种取样方法花色苷测定结果无显著性差异(P˃0.05)。
2.6 不同粉碎方式对花色苷含量测定结果比较
三个品种(系)马铃薯块茎采用打浆与研磨两种粉碎方式进行花色苷含量测定结果比较见图7,结果显示,三个品种(系)打浆处理的花色苷含量测定结果显著(P<0.05)低于研磨处理花色苷含量测定结果。黑金刚研磨测定的花色苷含量为47.91 mg/100 g FW,打浆机打浆测定的花色苷含量为18.01 mg/100 g FW,打浆比研磨使花色苷含量测定降低了60.0%;21-1研磨测定的花色苷含量为35.19 mg/100 g FW,打浆机打浆测定的花色苷含量为22.49 mg/100 g FW,花色苷含量测定结果降低了30%;剑川红研磨测定的花色苷含量为4.47 mg/100 g FW,打浆机打浆测定的花色苷含量为0.55 mg/100 g FW,花色苷含量测定结果降低80%。三个品种(系)的方差分析结果都表明打浆后使花色苷含量测定结果急剧下降。
3. 讨论与结论
本研究通过比较同种马铃薯薯皮和薯肉及不同品种花色苷的最大吸收波长,结果表明,同种马铃薯薯皮、薯肉颜色相近,花色苷最大吸收波长相近,表明所含的花色苷种类相似。不同品种(系)间花色苷最大吸收波长不同,表明不同品种(系)间花色苷种类不同,这与殷丽琴等[23]研究结果一致。品系21-1是由剑川红实生种培育而来,因此与剑川红颜色相近,最大吸收波长亦相近,表明二者之间的花色苷种类相似(见表2)。本研究发现花色苷提取液最大吸收波长与经pH1.0缓冲液稀释后的最大吸收波长不同,查阅相关文献可知[26],采用经pH1.0缓冲液稀释后扫描得到的最大吸收波长进行相应的定量结果最为可靠。为了数据可比性兼统一标准,美国分析化学家协会AOAC(Association of Official Analytical Chemists)颁布了《果汁、饮料、天然着色剂和葡萄酒中总单体花色苷的含量 pH示差法》的标准规定,最大吸收波长一般采用520 nm[27]。
本研究还发现同一植株中大、中、小薯花色苷含量存在显著性差异(P<0.05)(见图3),且差异趋势因品种(系)而异,可能原因是同一植株中大、中、小薯处于不同发育阶段导致。李倩等[28]研究发现不同马铃薯品种的花色苷含量随块茎发育阶段呈不同变化,颜色较深的品种Adirondack在块茎膨大初期即升到较高水平,在发育后期略微下降;而颜色较浅的品种All Red花色苷含量在薯块刚开始膨大时较少,随后逐渐累积,在薯块最大时花色苷含量达到峰值。是故在研究彩色马铃薯花色苷合成及含量相关研究时,必须选择大小一致的块茎进行研究。
前人研究已证实,花色苷合成具有组织特异性[29-30],跟颜色呈正相关[2]。一般颜色较深的部位花色苷含量较高,颜色较浅则较低。花色苷在马铃薯全身都存在,花、叶、茎、块茎内都含有,而且积累存在差异。本研究通过对三个品种(系)的薯皮和薯肉花色苷测定结果发现(见图4),薯皮中花色苷含量显著高于薯肉,而且差异倍数与品种本身有关,这与前人[18-20]的研究结果一致。此外,次生代谢产物在马铃薯块茎上即存在径向和纵向上的分布差异[31]。通过试验分析,彩色马铃薯花色苷含量在块茎中纵向分布含量差异显著(见图5),而且随品种而变化,有些品种的顶部和脐部花色苷含量高,如黑金刚、品系21-1,而有些品种的顶部花色苷含量高,脐部含量低,如剑川红。Lewis等[21]研究发现马铃薯品种Desiree的花色苷首先在块茎的茎端(脐部)产生,之后才在芽端(顶端)产生,表明花色苷的生物合成与积累在块茎的纵向上分布不均匀。彩色马铃薯内花色苷在横向和纵向上的分布差异,直接影响着块茎取样方式的选择。考虑到块茎内存在花色苷横向和纵向上的分布差异,因此如果为了获得整个马铃薯块茎的花色苷含量,取一个同时包含横向和纵向各部位的样本才具有代表性。根据本研究的结果,块茎纵切后随机取1份、取对角2份与取整个块茎三种取样方式对花色苷含量的分析结果无明显变化(图6),反映出通过纵切取少部分的薯块样本即可代表整体马铃薯块茎的花色苷含量水平。因此该取样方法能够有效适用于珍贵的种质资源取样,以及转基因株系等材料在有限条件下的快速花色苷定量分析。Griffiths等[32]在研究中测定马铃薯糖苷生物碱时也是采用的纵切取对角的方法,由此表明这一取样方式亦能够较好地应用于马铃薯块茎中次生代谢成分的快速检测。
在样本量充足的情况下,本研究设想通过使用更为省力快捷的打浆机来代替研磨,以达到省力及样本量大目的,试验结果表明,打浆机处理样品后花色苷含量的测定结果明显降低,这与一些报道结果相似[33],很可能是打浆后的样品花色苷遭到破坏或部分氧化,所以无法准确用于定量花色苷。因此,利用打浆的方式来代替研磨在植物鲜样的花色苷定量分析研究中可行性较低,不建议采用。
本文研究的意义在于,明确了彩色马铃薯花色苷在块茎中分布存在差异性会导致取样方式不同对检测结果产生影响,得出了反映整体样本真实状态的取样方式。
彩色马铃薯花色苷合成是一个复杂的催化过程,受调节基因合成的转录因子和结构基因编码的酶共同影响[34]。通常,MYB、bHLH和WD40是调控植物中花色苷生物合成的主要转录因子,由结构基因编码的PAL(苯丙氨酸解氨酶)、CHS(查尔酮合酶)、F3H(黄烷酮-3-羟化酶)、ANS(花青素合成酶)等是关键的限速酶[35]。花色苷的代谢机制与其他碳同化产物高度偶联[36],因此在一定程度上,彩色马铃薯块茎中差异分布与积累的花色苷或许也影响了其他初生/次生代谢产物的合成。本研究主要关注于马铃薯花色苷,并未对如淀粉、蛋白质、还原糖、糖苷生物碱等块茎特异成分开展具体分析,是故后续的研究将关注于花色苷合成与其他重要碳代谢通路之间的互作及在块茎不同部位的积累差异。
-
表 1 试验材料
Table 1 Test materials
品种 薯形 薯皮色 薯肉色 黑金刚(A) 椭圆 紫色 紫色 21-1(B) 长椭圆 红色 红白镶嵌 剑川红(C) 长椭圆 红色 红色 表 2 花色苷提取液与缓冲稀释液在可见光区的最大吸收波长比较
Table 2 Comparison of the maximum absorption wavelengths of anthocyanins extract and buffer diluent in visible light region
品种 可见光最大吸收波长(nm) 薯皮提取液 缓冲液稀释(薯皮) 薯肉提取液 缓冲液稀释(薯肉) 黑金刚 537.2a 527.8b 537.6a 528.0b 21-1 515.2c 504.8d 513.8c 504.2d 剑川红 515.6c 504.8d 513.8c 503.2d 注:不同字母表示差异显著,P<0.05。 -
[1] 庄维兵, 刘天宇, 束晓春, 等. 植物体内花青素苷生物合成及呈色的分子调控机制[J]. 植物生理学报,2018,54(11):1630−1644. [ZHUANG W B, LIU T Y, SHU X C, et al. The molecular regulation mechanism of anthocyanin biosynthesis and coloration in plants[J]. Plant Physiology Journal,2018,54(11):1630−1644. [2] RAIGOND P, SINGH B, DUTT S, et al. Potato nutrition and food security[M]. Singapore: Springer, 2020: 173-189.
[3] 李仲叶, 韩豪, 江海, 等. 花色苷抗氧化活性的研究现状及展望[J]. 食品工业,2019,40(8):245−250. [LI Z Y, HAN H, JIANG H, et al. Research status and prospects of the antioxidant activity of anthocyanins[J]. The Food Industry,2019,40(8):245−250. [4] BRUNETTI C, M D FERDINANDO, FINI A, et al. Flavonoids as antioxidants and developmental regulators: Relative significance in plants and humans[J]. International Journal of Molecular Sciences,2013,14(2):3540−3555. doi: 10.3390/ijms14023540
[5] 位路路. 黑果腺肋花楸花色苷提取物对脂多糖诱导巨噬细胞炎症的抑制作用[D]. 沈阳: 沈阳农业大学, 2018. WEI L L. The inhibition of aronia melanocarpa anthocyanin extracts on macrophages inflammation induced by lipopolysaccharide[D]. Shenyang: Shenyang Agricultural University, 2018.
[6] 饶炎炎, 桑英, 唐琳琳, 等. 红树莓果酒发酵过程中功效成分、香气物质及体外降血糖功效的动态变化[J]. 食品科学,2020,41(6):222−230. [RAO Y Y, SANG Y, TANG L L, et al. Dynamic changes in aroma, functional components and hypoglycemic effect in vitro of red raspberry wine during fermentation[J]. Food Science,2020,41(6):222−230. doi: 10.7506/spkx1002-6630-20190408-062 [7] LIPPERT E, RUEMMELE P, OBERMEIER F, et al. Anthocyanins prevent colorectal cancer development in a mouse model[J]. Digestion,2017,95(4):275−280. doi: 10.1159/000475524
[8] CHAREPALLI V, REDDIVARI L, RADHAKRISHNAN S, et al. Anthocyanin-containing purple-fleshed potatoes suppress colon tumorigenesis via elimination of colon cancer stem cells[J]. Journal of Nutritional Biochemistry,2015:1641−1649.
[9] 黄旭东. 紫色马铃薯不同部位花色苷抗前列腺癌细胞活性研究[D]. 杭州: 浙江大学, 2017. HUANG X D. Studies on the anti-prostate cancer cell viability of anthocyanins from different parts of purple potato[D]. Hangzhou: Zhejiang University, 2017.
[10] 尤诗莹. 功能性食品添加剂领域——天然食用色素的研究进展[J]. 饮食科学,2017,12(380):36−37. [YOU S Y. Research progress of natural food coloring in the field of functional food additives[J]. Diet Science,2017,12(380):36−37. [11] MARKAKIS P. Anthocyanins as food additives[J]. Anthocyanins as Food Colors,1982:245−253.
[12] WALLACE, GIUSTI. Anthocyanins—nature’s bold, beautiful, and health-promoting colors[J]. Foods,2019,8(11):550. doi: 10.3390/foods8110550
[13] SINGH J, MEEHNIAN H, GUPTA P, et al. Biotechnological Approaches: Food colours[M]. Springer India, 2020.
[14] AKHTAR, M HUMAYOUN, ZAHEER, et al. Potato production, usage, and nutrition-a review[J]. Critical Reviews in Food Science & Nutrition, 2016, 56(5): 711-721 .
[15] MISHRA T, RAIGOND P, THAKUR N, et al. Recent updates on healthy phytoconstituents in potato: A nutritional depository[J]. Potato Research,2020(2):1−21.
[16] 宋威武, 吴承金, 陈火云, 等. 彩色马铃薯花色苷及育种研究进展[C]//马铃薯产业与健康消费(2019). 2019: 133−137. SONG W W, WU C G, CHEN H Y, et al. Research progress on anthocyanins and breeding of colored potato[C]// Potato industry and health consumption(2019). 2019: 133−137.
[17] 殷丽琴, 彭云强, 钟成, 等. 高效液相色谱法测定8个彩色马铃薯品种中花青素种类和含量[J]. 食品科学,2015(18):143−147. [YIN L Q, PENG Y Q, ZHONG C, et al. Determination of anthocyanidin composition of different pigmented potato (Solanum tuberosum L.) cultivars by HPLC[J]. Food Science,2015(18):143−147. doi: 10.7506/spkx1002-6630-201518026 [18] 张静, 郭华春, 姚春雪. 11个云南地方马铃薯品种块茎的花色苷含量及其分布[C]//马铃薯产业与粮食安全(2009). 2009. ZHANG J, GUO H C, YAO C X. Anthocyanins content and distribution in tubers of 11 Yunnan native potato varieties[C]// Potato industry and food security(2009). 2009.
[19] JANSEN G, FLAMMEL W. Coloured potatoes (Solanum tuberosum L.) – anthocyanin content and tuber quality[J]. Genetic Resources & Crop Evolution,2006,53(7):1321.
[20] 白粉娥, 成宇峰. 两种彩色马铃薯品种花色苷成分分析及其总抗氧化活性的比较研究[J]. 保鲜与加工,2018,18(2):108−113. [BAI F E, CHENG Y F. Comparative study of anthocyanins component and total antioxidant activity between two colorful potato cultivars[J]. Storage and Process,2018,18(2):108−113. doi: 10.3969/j.issn.1009-6221.2018.02.018 [21] LEWIS C E, WALKER J R L, LANCASTER J E, et al. Light regulation of anthocyanin, flavonoid and phenolic acid biosynthesis in potato minitubers in vitro[J]. Australian Journal of Plant Physiology,1998,25(8):915−922.
[22] LEE J, RENNAKER C, WROLSTAD R E. Correlation of two anthocyanin quantification methods: HPLC and spectrophotometric methods[J]. Food Chemistry,2008,110(3):782−786. doi: 10.1016/j.foodchem.2008.03.010
[23] 殷丽琴, 韦献雅, 钟成, 等. 不同品种彩色马铃薯总花色苷含量与总抗氧化活性[J]. 食品科学,2014,35(5):96−100. [YIN L Q, WEI X Y, ZHONG C, et al. Total anthocyanin content and total antioxidant activities in different varieties of pigmented potato (Solanum tuberosum L.)[J]. Food Science,2014,35(5):96−100. doi: 10.7506/spkx1002-6630-201405019 [24] FULEKI T, FRANCIS F J. Quantitative methods for anthocyanins. 1. Extraction and determination of total anthocyanin in cranberries[J]. Journal of Foodence,1968,33(1):72−77.
[25] FULEKI T, FRANCIS F J. Quantitative methods for anthocyanins. : 2. Determination of total anthocyanin and degradation index for cranberry juice[J]. Journal of Foodence,1968,33(1):78−83.
[26] LEE J, DURST, ROBERT W, et al. Determination of total monomeric anthocyanin pigment content of fruit juices, beverages, natural colorants, and wines by the pH differential method: Collaborative study[J]. Journal of AOAC International,2005,88(5):69−78.
[27] WROLSTAD R E. Aoac official method 2005.02: Total monomeric anthocyanin pigment content of fruit juices, beverages, natural colorants, and wines by the pH differential method[M]. 2005: 1−2.
[28] 李倩, 柳俊, 谢从华, 等. 彩色马铃薯块茎形成和贮藏过程中花色苷变化及抗氧化活性分析[J]. 园艺学报,2013,40(7):1309−1317. [LI Q, LIU J, XIE C H, et al. Variation of anthocyanin of colored-flesh potato tubers and measurement of their antioxidant activity during the tuber development and storage[J]. ACTA Horticulturae Sinica,2013,40(7):1309−1317. [29] YL A, JL B, XZ B, et al. Genome-wide analysis of MYB gene family in potato provides insights into tissue-specific regulation of anthocyanin biosynthesis[J]. Horticultural Plant Journal,2020,7(2):129−141.
[30] OERTEL A, MATROS A, HARTMANN A, et al. Metabolite profiling of red and blue potatoes revealed cultivar and tissue specific patterns for anthocyanins and other polyphenols[J]. Planta,2017,246(2):281−297. doi: 10.1007/s00425-017-2718-4
[31] SHEPHERD T, DOBSON G, VERRALL S R, et al. Potato metabolomics by GC-MS: What are the limiting factors?[J]. Metabolomics,2007,3(4):475−488. doi: 10.1007/s11306-007-0058-2
[32] GRIFFITHS D W, DALE M. Effect of light exposure on the glycoalkaloid content of solanum phureja tubers[J]. Journal of Agricultural & Food Chemistry,2001,49(11):5223−5227.
[33] 范志红. 怎样减少鲜榨汁的营养损失?[J]. 健康之家,2014(11):85. [FAN Z H. How to reduce the nutritional losses of fresh juicing?[J]. Health,2014(11):85. [34] 范祺祺, 董文, 熊兴耀, 等. 植物地下器官花色苷合成及其调控研究进展[J]. 中国蔬菜,2019(6):21−28. [FAN Q Q, DONG W, XIONG X Y, et al. Advances in anthocyanin synthesis and regulation in plant subterranean organs[J]. China Vegetables,2019(6):21−28. [35] YING L, YURY T, SCHOUTEN R E, et al. Anthocyanin biosynthesis and degradation mechanisms in solanaceous vegetables: A review[J]. Frontiers in Chemistry,2018,52(6):1−17.
[36] JAAKOLA, LAURAL. New insights into the regulation of anthocyanin biosynthesis in fruits[J]. Trends in Plant Science,2013,18(9):477−483. doi: 10.1016/j.tplants.2013.06.003





 下载:
下载:






 下载:
下载:



