Antibacterial Activity and Stability of Methanol Extract from Thamnolia subuliformis in Vitro
-
摘要: 为初步探究雪地茶体外抑菌活性及其稳定性,采用平板打孔法测定雪地茶甲醇提取物对常见致病菌的体外抑菌活性,以金黄色葡萄球菌作为指示菌,测定不同温度、pH、紫外照射时间等因素对抑菌稳定性的影响,使用石油醚、乙酸乙酯、正丁醇分级萃取甲醇提取物,确定其抑菌活性物质的极性,并测定其松萝酸含量。结果表明雪地茶甲醇提取物对革兰氏阳性菌如金黄色葡萄球菌、枯草芽孢杆菌、斯氏李斯特菌、表面葡萄球菌、伊氏李斯特氏菌,革兰氏阴性菌如甲型副伤寒杆菌、乙型副伤寒杆菌以及致病真菌白色念珠菌等具有良好的抑菌效果。其中,对金黄色葡萄球菌的最小抑菌浓度和最小杀菌浓度分别为0.625、10 mg/mL;抑菌稳定性实验结果表明,温度对雪地茶甲醇提取物的抑菌活性无显著影响(P>0.05),100 ℃处理30 min后仍具有较高的抑菌活性;紫外光照射40 min及50 min的处理组抑菌活性显著下降(P<0.05),但抑菌率仍保持在90%以上;pH对雪地茶甲醇提取物的抑菌稳定性影响最大,当pH接近生理中性时(pH=6.0),其抑菌活性与对照组(pH=4.83)无显著差异(P>0.05),表现出较高抑菌活性,当pH较高(8.0、10.0)或较低(2.0、4.0)时,处理组的抑菌活性极显著下降(P<0.05),且随着pH的升高或降低而降低;雪地茶甲醇提取物中松萝酸含量为0.8613%,乙酸乙酯萃取物中松萝酸含量为0.9379%。本实验结果证实雪地茶甲醇提取物具有一定的广谱抑菌效果且作用浓度较低,稳定性较好,可用于天然食品防腐剂和植源性抑菌药物的开发利用。Abstract: The objective of the study was preliminarily explore the antibacterial activity and stability of Thamnolia subuliformis in vitro, the plate drilling method was used to determine the antibacterial activity of methanol extract of Thamnolia subuliformis against common pathogenic bacteria in vitro. The indicator bacteria of Staphylococcus aureus was used to determine the effects of factors such as different temperature, pH and UV irradiation time on antibacterial stability. Petroleum ether, ethyl acetate and n-butanol were used to extract the methanol extract, determine the polarity of its antibacterial active substances, and determine the content of usnic acid. The results showed that the methanol extract of Thamnolia subuliformis had good antibacterial effect on Gram-positive bacteria such as Staphylococcus aureus, Bacillus subtilis, Listeria stephensi, Staphylococcus surface, Listeria evansi, Salmonella paratyphi A, Salmonella paratyphi B of Gram-negative bacteria and Candida albicans. The minimum inhibitory concentration and minimum bactericidal concentration against Staphylococcus aureus were 0.625 and 10 mg/mL respectively; The results of antibacterial stability test showed that temperature had no significant effect on the antibacterial activity of methanol extract of Thamnolia subuliformis (P>0.05), and it still had high antibacterial activity after treatment at 100 ℃ for 30 min; The antibacterial activity of UV irradiation for 40 min and 50 min decreased significantly (P<0.05), but the antibacterial rate remained above 90%; pH had the greatest effect on the antibacterial stability of methanol extract of Thamnolia subuliformis. When the pH was close to physiological neutral (pH6.0), its antibacterial activity was not significantly different from that of the control group (pH4.83)(P>0.05), showing high antibacterial activity. When the pH was high (8.0, 10.0) or low (2.0, 4.0), the antibacterial activity of the treatment group decreased significantly (P<0.05), and decreased with the increase or decrease of pH, The content of usnic acid in methanol extract and ethyl acetate extract of Thamnolia subuliformis was 0.8613% and 0.9379%, respectively. The results showed that the methanol extract of Thamnolia subuliformis had a certain broad-spectrum antibacterial effect, low concentration and good stability. It can be used for the development and utilization of natural food preservatives and plant-derived antibacterial drugs.
-
Keywords:
- Thamnolia subuliformis /
- methanol extract /
- bacteriostasis /
- Staphylococcus aureus /
- stability /
- usnic acid
-
雪地茶(Thamnolia subuliformis (Ehrh.) W. Culb.)又名太白茶、石白茶,地茶科地茶属植物,在云南地区主要分布于迪庆、丽江、大理苍山等海拔4000 m以上的高寒地区,当地居民常以水煎服或泡茶饮用治疗中暑、心烦口渴、肺热咳嗽、咽喉肿痛、阴虚潮热、癫痫、失眠、目疾、高血压等症[1]。近年来,雪地茶抗氧化、抗衰老、抗炎、减肥等功效[2-4]逐渐被报道,其广泛的生理作用得益于它丰富的代谢产物[5]。雪地茶次生代谢产物来源于其共生菌,多为水不溶性,主要包括萜类、甾醇类以及乙酸酯-多聚丙二酸酯途径形成的蒽醌类、缩酚酸类及其衍生物等,其中缩酚酸及其衍生物是地衣生物所特有的化学成分,如坝巴酸、松萝酸、富马原岛衣酸、扁枝衣二酸等多种地衣酸都被证实具有良好的抑菌活性[6-9]。前人研究表明,雪地茶中包含甲基苔色酸、雪茶素、4-甲基-2,6-二羟基苯甲醛等19种酚酸、缩酚酸及衍生物[10],然而其抑菌活性却无人探究。随着人们对饮食健康的重视,寻找、研究、开发新的毒副作用小的防腐剂已成为目前急需解决的问题。因此,本实验以雪地茶为研究对象,探究其水和甲醇提取物的抑菌活性及外界环境因素对其抑菌稳定性的影响,为雪地茶开发成抗菌素和天然防腐剂提供一定的理论依据。
1. 材料与方法
1.1 材料与仪器
雪地茶(Thamnolia subuliformis (Ehrh.) W. Culb.) 采集于云南省香格里拉地区,经大理大学生药学实验室张德全副教授进行植物学鉴定后保存于4 ℃冰箱;金黄色葡萄球菌(Staphylococcus aureus ATCC 25923)、枯草芽孢杆菌(Bacillus cereus ATCC 6633)、斯氏李斯特菌(Listeria seeligeri CICC 21671)、甲型副伤寒杆菌(Salmonella paratyphi-A BNCC 336664)、乙型副伤寒杆菌(Salmonella paratyphi-B BNCC 103169)、白色念珠菌(Candida albicans ATCC 10231)、表面葡萄球菌(Staphylococcus epidermidis ATCC 12228)、伊氏李斯特氏菌(Listeria monocytogenes CICC 21663)、单增李斯特菌(Listeria monocytogenes CMCC 21633)、大肠埃希菌(Escherichia coli CMCC(B) 441027)、福氏志贺菌(Shigellaflexneri CMCC 21534)、肺炎克雷伯菌(Klebsiella pneumoniae ATCC 4352)、绿脓杆菌(Pseudomonas aeruginosa ATCC 27853)、酵母菌(Saccharomyces BNCC 142268) 由大理州质量技术监督综合检测中心提供;营养琼脂、LB肉汤等常规试剂 北京陆桥技术股份有限公司。
T6新世纪型紫外可见分光光度计 北京普析通用仪器有限责任公司;Scientz-ND型系列冷冻干燥机、SB-5200DTDN型超声波清洗机 宁波新芝生物科技股份有限公司;RE-3000型旋转蒸发仪 上海亚荣生化仪器厂;VS-1300L-U型超净工作台 苏净集团泰安公司制造;GHP-9270型隔水式恒温培养箱、DKZ-3型震荡水槽、HWS-28型电热恒温水浴锅 上海一恒科学仪器有限公司;GZX-9160MBE型数显鼓风干燥机 上海博迅实业有限公司医疗设备厂;PHS-3C型pH计 上海仪电科学仪器股份有限公司;ZW20S19W型紫外灯 江阴市飞扬器械有限公司;4500Qtrap型质谱仪 美国AB SCIEX公司;Ultimate3000型超高效液相色谱仪 美国Thermo Scientific公司。
1.2 实验方法
1.2.1 雪地茶提取物体外抑菌活性实验
1.2.1.1 雪地茶提取物的制备
雪地茶甲醇提取物的制备:参考汪琼等[11]的方法加以修改。雪地茶清洗经过鼓风干燥机50 ℃烘10 h后干燥至样品变脆后粉碎,过60目筛。按照料液比1:10 g/mL加入75%甲醇溶液,超声浸提30 min后抽滤,重复浸提后收集上清液,50 ℃旋转蒸发至10 mL后−20 ℃冷冻3 h成固体,真空冷冻干燥12 h(冷阱温度降到−25 ℃,真空度设置为50 Pa)成粉末,置于−20 ℃冰箱避光密封保存。
雪地茶甲醇分级提取物的制备:参考邓云霞等[12]的方法加以修改。将两次超声提取的甲醇提取物上清液减压浓缩至一定体积,使用石油醚、乙酸乙酯、正丁醇等体积分别萃取,直至萃取剂无色。旋转蒸发至10 mL后−20 ℃冷冻3 h成固体,真空冷冻干燥12 h(冷阱温度降到−25 ℃,真空度设置为50 Pa)成粉末,置于−20 ℃冰箱避光密封保存。
雪地茶水提物的制备:参考付长华[13]的方法加以修改。取过60目筛粉碎好的雪地茶粉末,按料液比1:10 g/mL加入蒸馏水,80 ℃水浴浸提30 min,抽滤,重复浸提后收集上清液,50 ℃旋转蒸发至10 mL后置于−20 ℃冷冻3 h成固体,真空冷冻干燥12 h成粉末,置于−20 ℃冰箱避光密封保存。
1.2.1.2 雪地茶提取物体外抑菌活性
采用平板打孔法[14]探究雪地茶提取物的体外抑菌活性,甲醇提取物使用甲醇进行溶解,水提物使用无菌水溶解。刮取斜面保存菌体于无菌蒸馏水中,采用麦氏比浊法,使用无菌水调整菌液浓度至106 CFU/mL备用。将营养琼脂或马铃薯葡萄糖琼脂培养基和106 CFU/mL的菌液,按每20 mL培养基中加入1 mL菌液比例混匀。用100 μL的枪头在凝固的琼脂上打孔,挑出孔内的琼脂,每个孔中加入20 μL的100 mg/mL雪地茶提取物,阳性对照使用5 mg/mL的左氧氟沙星,阴性对照为水和甲醇。每组设置三个平行实验,4 ℃扩散2 h后,置于37 ℃培养箱中,培养24 h观察抑菌圈的形成。参考LI等[15]的研究对雪地茶抑菌活性进行判断:抑菌圈直径大于6 mm判断为有抑菌活性,小于等于6 mm为无抑菌活性;3次重复实验均达到有抑菌活性结果者判为合格;阴性对照组应无抑菌圈,否则实验视为无效。抑菌圈直径大于6 mm小于8 mm为低度敏感;大于8 mm小于14 mm为中度敏感;大于14 mm小于20 mm为高度敏感;大于20 mm为极度敏感。
1.2.2 雪地茶甲醇提取物对金黄色葡萄球菌的抑菌活性
1.2.2.1 最小抑菌浓度(Minimum Inhibitory Concentration, MIC)和最小杀菌浓度(Minimum Bactericidal Concentration, MBC)的测定
采用二倍稀释法[16],将20 mg甲醇提取物用3%二甲基亚砜(Dimethyl sulfoxide, DMSO) 0.06 mL复溶制成待测液,用无菌LB肉汤稀释样品至一定浓度梯度(10.000、5.000、2.500、1.250、0.625、0.313、0.156、0.078、0.039、0.020 mg/mL)。不同浓度样品接种2% (V/V)活化后的菌液(106 CFU/mL),置于37 ℃ 110 r/min的恒温培养箱振荡培养24 h,以加入等体积的3% DMSO代替提取物作为空白对照。
1.2.2.2 雪地茶甲醇提取物对金黄色葡萄球菌生长的影响
从斜面上刮取菌体,接种到5 mL新鲜的LB液体培养基中,37 ℃ 110 r/min振荡培养至生长对数期,稀释到106 CFU/mL。总体积为30 mL,对照组为3% DMSO,实验组为MIC(提取物的终浓度为0.625 mg/mL)和2 MIC(提取物的终浓度为1.250 mg/mL),迅速混匀置于37 ℃静置培养。雪地茶提取物对金黄色葡萄球菌的生长影响实验时间点选择0、2、4、6、8、10、12、14、24、26、28、30、33 h等13个时间点,以加入等体积的3% DMSO代替提取物作为空白对照,每组设置三次平行实验,采用分光光度计600 nm检测雪地茶提取物对金黄色葡萄球菌生长的影响[17]。绘制吸光度-时间曲线,从而获得金黄色葡萄球菌生长曲线的变化趋势。
1.2.3 雪地茶抑菌活性的稳定性探究实验
1.2.3.1 温度对雪地茶甲醇提取物抑菌活性的影响
参考YIN等[18]的方法并进行一定修改。将雪地茶甲醇提取物100 mg/mL原液分别在室温(对照组,18 ℃)、40、60、80、100 ℃的水浴中处理30 min,采用1.2.1.2方法测定体外抑菌活性。
1.2.3.2 pH对雪地茶甲醇提取物抑菌活性的影响
参考ZANGENEH等[19]的方法并进行一定的修改。分别用0.1 mol/L HCl和0.1 mol/L NaOH将雪地茶提取物100 mg/mL原液的pH调整为2.0、4.0、6.0、8.0、10.0,以未调节pH的提取物为对照(pH4.83),采用1.2.1.2方法测定抑菌活性。
1.2.3.3 短波紫外线对雪地茶甲醇提取物抑菌活性的影响
参照刘海燕等[20]的方法进行一定修改。将雪地茶甲醇提取物100 mg/mL原液置于紫外灯下(20 W,紫外灯距样品25 cm)分别照射10、20、30、40、50 min,以未进行照射的提取物为对照,采用1.2.1.2方法测定抑菌活性。
1.2.4 雪地茶甲醇提取物中松萝酸含量的测定
1.2.4.1 松萝酸标品和样品的制备
标准品的制备:精密称取松萝酸标准品0.0500 g,用50%甲醇水定容50 mL,得到浓度1000 μg/mL储备液,用50%甲醇水分别稀释成2、5、10、25、50、100、200 μg/L的标准曲线,制得标准曲线y=54121.4x−14121.9 (r=0.99966)。
样品的制备:称取样品10.000 mg,用10%甲醇水定容至100 mL,再稀释10倍得到待测液。
1.2.4.2 液相条件和质谱条件
超高效液质联用法(Ultra-performance liquid chromatography-tandem mass spectrometry, UPLC-MS)条件:色谱柱Waters Acquility UPLC BEH C18柱(2.1 mm×100 mm,1.7 μm),流动相A:水;B:甲醇;洗脱程序(以流动相B体积分数表示):0~0.5 min,10%;0.5~2 min,10%~30%;2~7 min,30%~95%;7~9 min,95%;9~20 min,10%,流速0.3 mL/min,进样量5.0 μL,柱温40 ℃。质谱条件:离子源:电喷雾离子源负离子模式(ESI-);离子喷雾电压(Ionspray voltage):-4500 V;气帘气(Curtain gas):30 L/h;碰撞气(Collision Gas):Medium;脱溶剂温度:550 ℃;雾化气1(Ion Source Gas1):50 L/h[21]。其他见表1。
表 1 松萝酸的UPLC-MS/MS测定参数Table 1. Determination parameters of usnic acid by UPLC-MS/MS化合物 保留时间(min) 分子式 母离子(m/z) 子离子(m/z) 驻留时间(ms) 去簇电压DP/V 碰撞能量CE/V 松萝酸 11.45 C18H16O7 342.9 328*
258.8
299100 −60 −28.38
−29.23
−24.18注:*表示定量离子。 1.3 数据处理
每个处理重复三次,实验结果以均值±标准偏差(Mean±SD)表示,数据采用Graphpad prism 8.0和SPSS 26.0软件进行数据处理并分析,统计学方法采用单因素方差分析,P<0.05表明具有显著性差异,P<0.01表明具有极显著差异。
2. 结果与分析
2.1 雪地茶水提物和甲醇提取物的抑菌活性
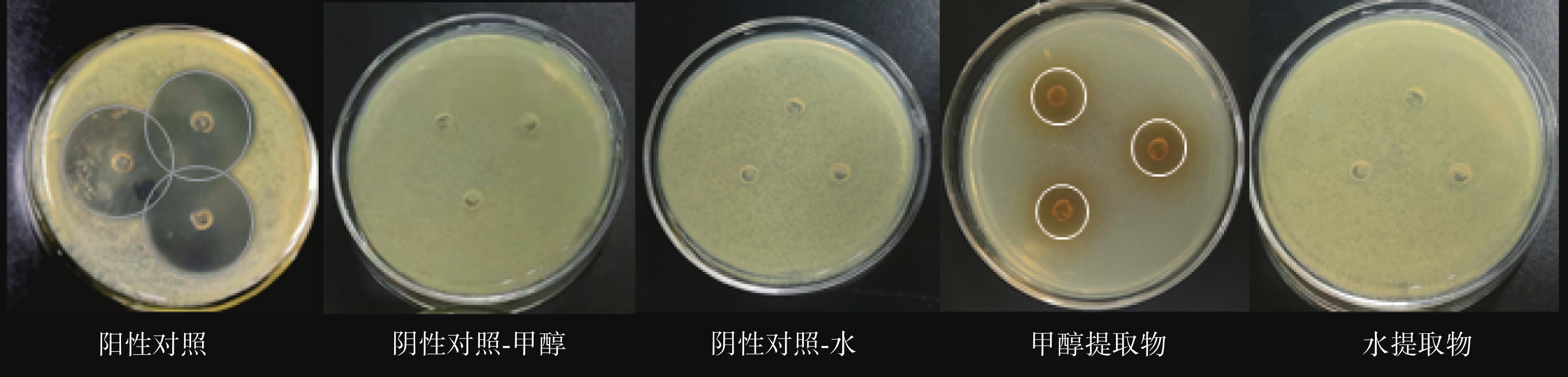
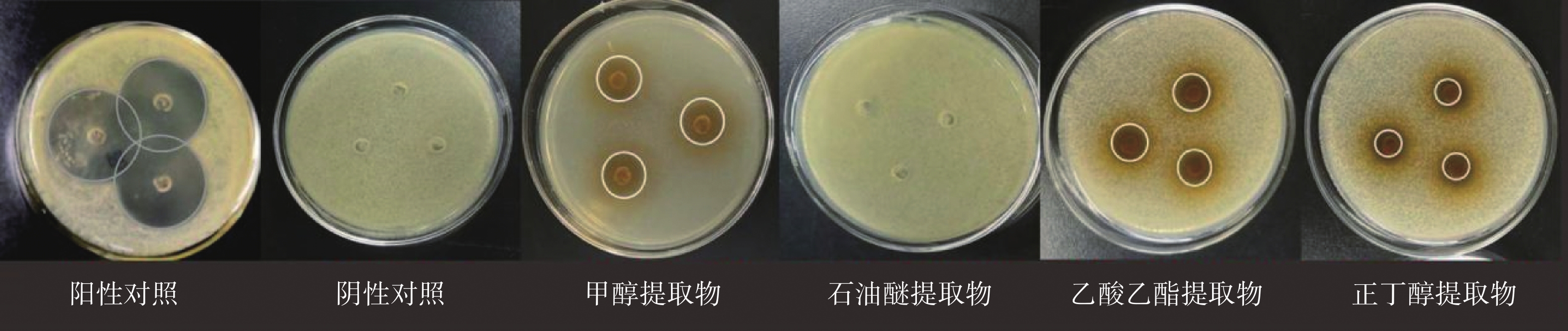
本实验以金黄色葡萄球菌为研究对象,探究雪地茶水提物和甲醇提取物的抑菌活性,如图1所示,雪地茶水提物对金黄色葡萄球菌无明显抑菌作用,而甲醇提取物则呈现出一定的抑菌作用。结果表明雪地茶的主要抑菌成分溶于有机溶剂甲醇,在水中的溶解度较小,这一结果与KOSANIĆMARIJANA[22]、房敏峰等[23]研究结果一致,证实地衣类植物的多数抑菌成分难溶于水,易溶于有机溶剂。同时,汪琼等[11]对雪地茶甲醇提取物的成分组成进行探究,发现其甲醇提取物中含有鳞片衣酸、坝巴酸、松萝酸等物质,这些具有抗菌活性的地衣酸类物质均易溶于有机溶剂而不溶于水[24],进一步佐证了本实验结果。由图2可知将雪地茶甲醇提取物进一步使用不同极性有机溶剂进行萃取,发现乙酸乙酯提取物的抑菌圈较大(17.2 mm),石油醚相无抑菌圈,正丁醇相有抑菌圈但相对较小(10.4 mm),因此推断甲醇提取物中的抑菌成分基本锁定在乙酸乙酯相中。
在上述实验结论的基础上,进一步探究了雪地茶甲醇提取物对多种致病性革兰氏阳性菌(金黄色葡萄球菌、枯草芽孢杆菌、斯氏李斯特菌、表面葡萄球菌、伊氏李斯特氏菌、单增李斯特菌)、革兰氏阴性菌(甲型副伤寒杆菌、乙型副伤寒杆菌、大肠埃希菌、福氏志贺菌、肺炎克雷伯菌、绿脓杆菌)以及真菌(白色念珠菌、酵母菌)的抑菌活性,结果如表2所示,单增李斯特菌、大肠埃希菌、福氏志贺菌、肺炎克雷伯菌、绿脓杆菌、酵母菌无抑菌效果,6种致病性细菌对雪地茶甲醇提取物高度敏感(抑菌圈直径大于14 mm小于20 mm),且其敏感性排序为:金黄色葡萄球菌>伊氏李斯特氏菌>乙型副伤寒杆菌>枯草芽孢杆菌>斯氏李斯特菌>甲型副伤寒杆菌,表面葡萄球菌、白色念珠菌为极度敏感(抑菌圈直径>20 mm),说明雪地茶甲醇提取物具有较为广泛的广谱抑菌效果,具有可开发为广谱抑菌药物和天然防腐剂的潜力。目前对地衣活性抑菌物质的抑菌机制研究较为深入的是松萝酸,被证实可通过破坏致病微生物包膜物质的结构和功能、抑制其大分子生命物质的合成、抑制其正常的生理代谢等方面抑制病原微生物的生长和繁殖[25]。松萝酸可以通过改变耐甲氧西林金黄色葡萄球菌菌体细胞膜通透性,干扰其蛋白质代谢来抑制细菌的生长,破坏其固有形态,在亚抑菌浓度就能够抑制生物被膜的形成,对于白色念珠菌主要通过改变成熟菌体的生物膜厚度来发挥其抑菌作用[26]。MONIKA等[27]发现松萝酸可以通过阻碍金黄色葡萄球菌和枯草芽孢杆菌RNA的合成来抑制细菌生长。然而对于雪地茶的抑菌活性及其机理暂无报道,为拓展其资源的开发利用,进一步阐明其抑菌作用机制十分必要。
表 2 雪地茶甲醇提取物抑菌作用Table 2. Antibacterial effect of methanol extract from Thamnolia subuliformis菌种名称 革兰氏染色 抑菌圈直径(mm) 金黄色葡萄球菌 阳性 16.8±0.9 枯草芽孢杆菌 15.7±1.6 斯氏李斯特菌 15.4±0.8 表面葡萄球菌 20.0±1.6 伊氏李斯特氏菌 16.7±0.7 单增李斯特菌 0.0 甲型副伤寒杆菌 阴性 15.2±2.1 乙型副伤寒杆菌 16.5±2.0 大肠埃希菌 0.0 福氏志贺菌 0.0 肺炎克雷伯菌 0.0 绿脓杆菌 0.0 白色念珠菌 真菌 22.4±0.5 酵母菌 0.0 2.2 雪地茶甲醇提取物对金黄色葡萄球菌的抑菌活性
在确定了雪地茶甲醇提取物的抗菌活性后,实验进一步以食品中常见且致病性较高的金黄色葡萄球菌为对象,对其MIC及MBC进行测定,结果表明(表3)雪地茶甲醇提取物对金黄色葡萄球菌的抑制效果较强,MIC和MBC分别为0.625和10 mg/mL。与其他中草药相比,雪地茶甲醇提取物的作用浓度较低且抑菌活性较强,崔新洁等[28]对24种中药的水提和醇提物进行抑菌活性研究,其中14种中药提取物的MIC大于200 mg/mL,6种中药的MIC在100~200 mg/mL,仅4种中药的MIC小于100 mg/mL,其中活性最高的为五倍子水提液(MIC:0.390 mg/mL)。本实验结果说明雪地茶甲醇粗提物的抑菌活性较高,具有较高的开发潜力,但其主要活性物质的鉴定及体内作用浓度还有待进一步探究。
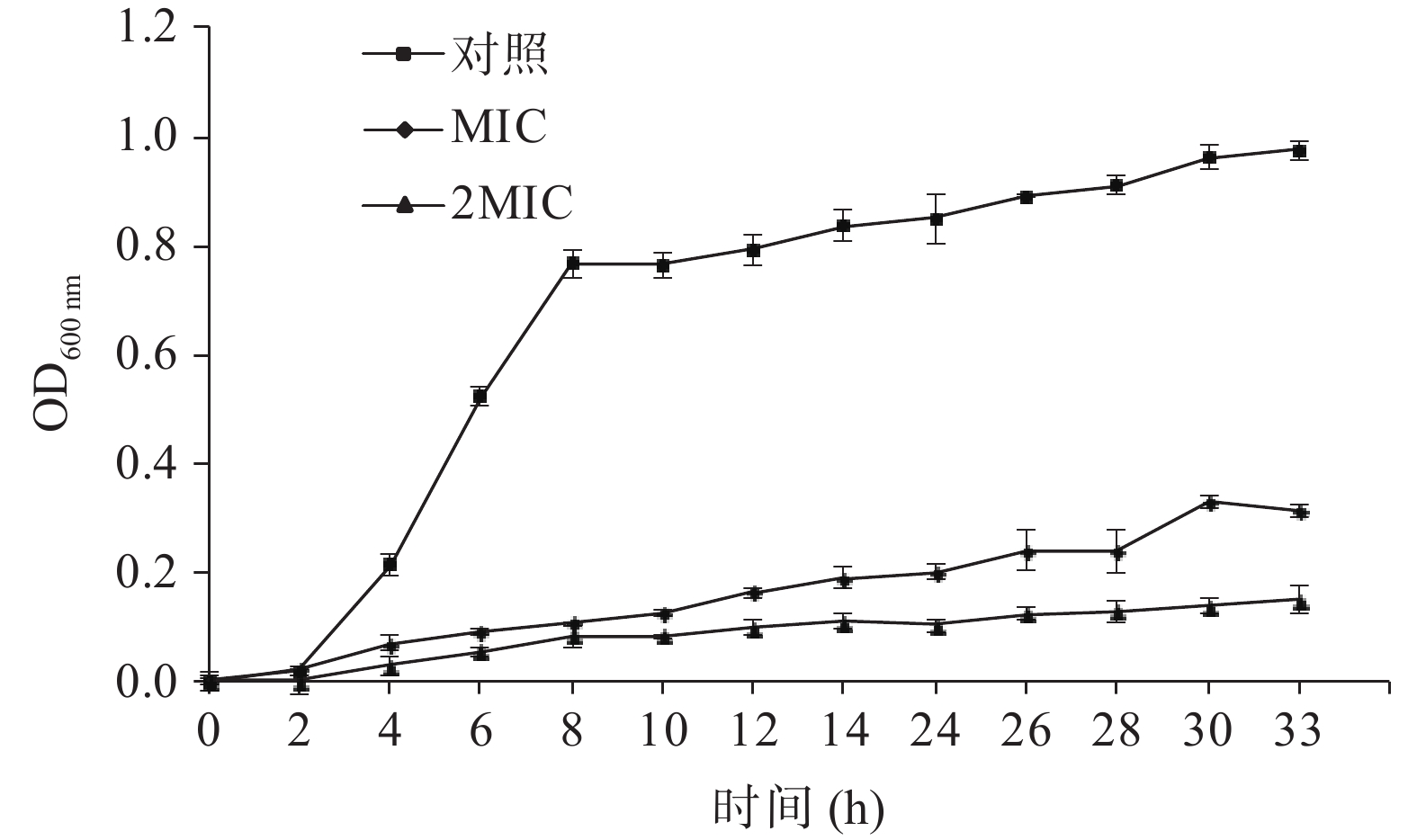
表 3 雪地茶甲醇提取物的最低抑菌浓度Table 3. Minimum inhibitory concentration of methanol extract of Thamnolia subuliformis质量浓度(mg/mL) 10.000 5.000 2.500 1.250 0.625 0.313 0.156 0.018 0.039 金黄色葡萄球菌 MBC − − − MIC + ++ +++ +++ 注:“−”表示无菌生长,“+”表示菌体生长少,“++”表示菌体生长较多,“+++”表示菌体生长很多。 为进一步验证雪地茶甲醇提取物对金黄色葡萄球菌生长的影响,实验采用MIC和2MIC的样品浓度处理观察其对金黄色葡萄球菌生长曲线的影响(图3)。在0~2 h内,对照和处理组菌体的生长速率无显著差别,2~8 h对照组菌体进入对数期,8 h以后基本处于稳定期;而加样处理组的菌体在2~33 h生长速率明显较慢,且浓度越大,抑制效果越明显,该现象与高飞雄等[29]用植酸处理沙门氏菌的生长曲线相似。说明样品中某些物质的存在抑制了金黄色葡萄球菌的正常生长繁殖,使其菌体数量显著下降;导致菌体对数生长期缩短、生长速率缓慢,从而达到抑菌作用。
2.3 雪地茶甲醇提取物抑菌活性的稳定性探究
2.3.1 温度对雪地茶甲醇提取物的抑菌活性影响
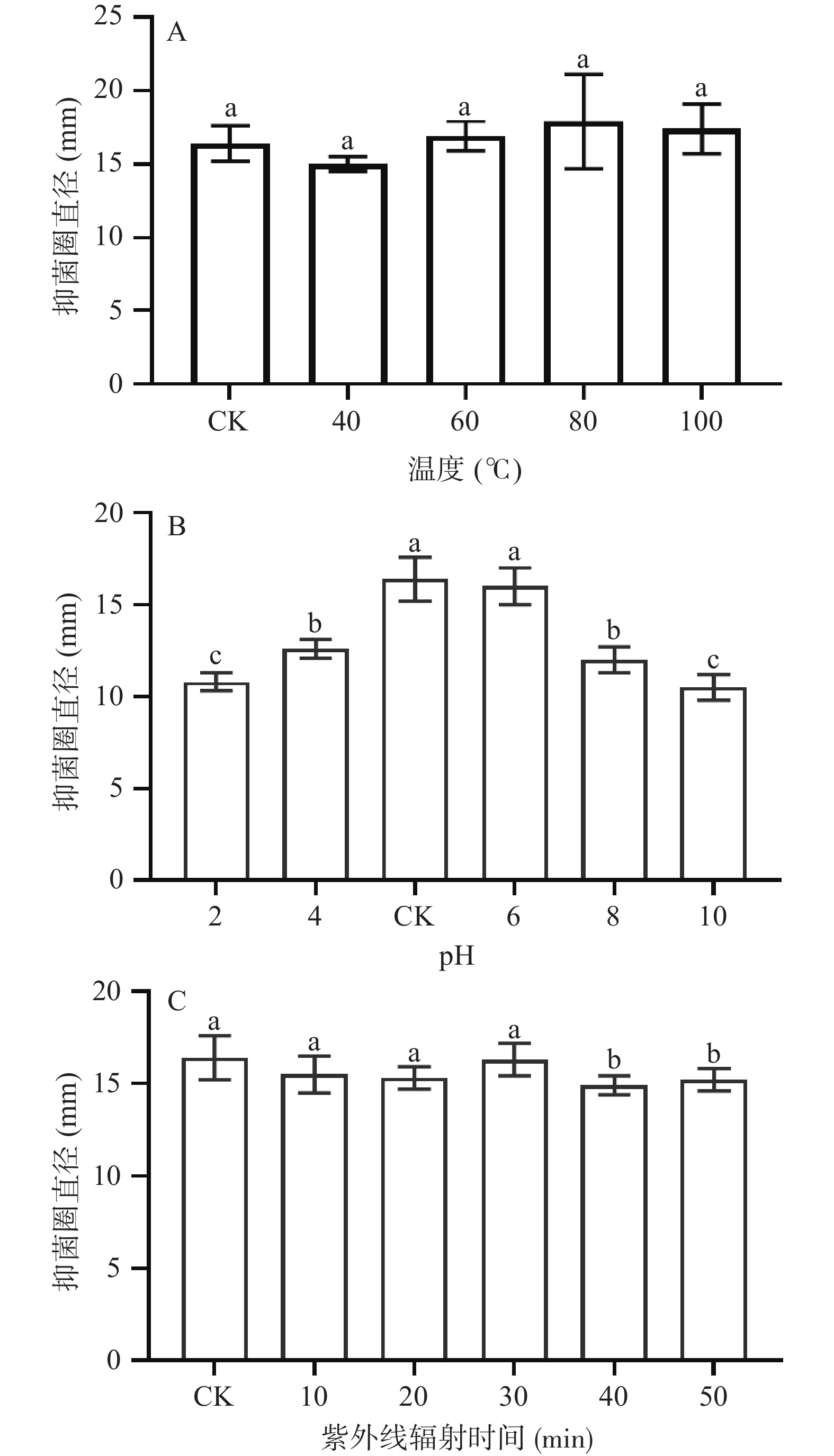
为探究雪地茶甲醇提取物的抑菌稳定性,实验采用不同温度、pH和紫外照射处理雪地茶甲醇提取物,结果见图4。由图4A可知,雪地茶甲醇提取物经不同温度处理后,与对照相比其抑菌活性没有显著差异(P>0.05),即使用100 ℃高温处理30 min后也保持较高的抑菌活性,说明雪地茶甲醇提取物有较好的热稳定性。地衣类生物可能存在的潜在抑菌活性物质酚酸类物质的熔点沸点较高,在100 ℃下的温度不易发生分解[30],因此常规操作温度更不会对其造成影响。另外,其他中草药中获取的多种抑菌物质也是一样,丁香提取物和诃子的水提物在高温处理下,也不会影响其抑菌效果[31-32]。雪地茶甲醇提取物的热稳定性是其后续资源开发利用的前提和保障。
2.3.2 pH对雪地茶甲醇提取物的抑菌活性影响
雪地茶甲醇提取物对供试菌在较宽的pH范围内都有抑菌活性,但是随pH的变化有所波动(图4B),具体表现为随着处理pH的升高(2.0~10.0)其抑菌活性先升高后降低,当pH为6.0时(接近其本身pH4.83)时抑菌活性达到最大。在酸性条件(pH2.0、4.0)下,其抑菌活性较对照组分别降低34.15%和23.17%,碱性条件下(pH8.0、10.0)其抑菌活性较对照组下降了26.83%和35.98%。本实验结果表明外界pH影响雪地茶甲醇提取物的稳定性,在弱酸环境下,其抑菌活性较为稳定,此结果与酚类物质的酸碱稳定性结果相一致[33],在碱性环境下,其潜在的抑菌活性物质酚酸类化合物的酚羟基被破坏,水解生成醌类物质,导致其抑菌活性降低[34]。
2.3.3 紫外线对雪地茶甲醇提取物的抑菌活性影响
不同紫外照射时间对雪地茶甲醇提取物的影响见图4C,与对照相比,当处理时间为10、20、30 min时,其抑菌活性比较稳定,但随着处理时间的延长(40、50 min),其抑菌活性略有下降,但仍为对照组的90%以上。前人研究表明,一些功能性植物提取物如原花青素[35]、黄酮[36]、多酚[37]等物质在长时间紫外辐射的环境中其含量持续降低,说明目标物质发生了分解。结合本实验研究结果,推测雪地茶甲醇提取物中的抑菌活性成分经紫外线处理后受到了一定的破坏。
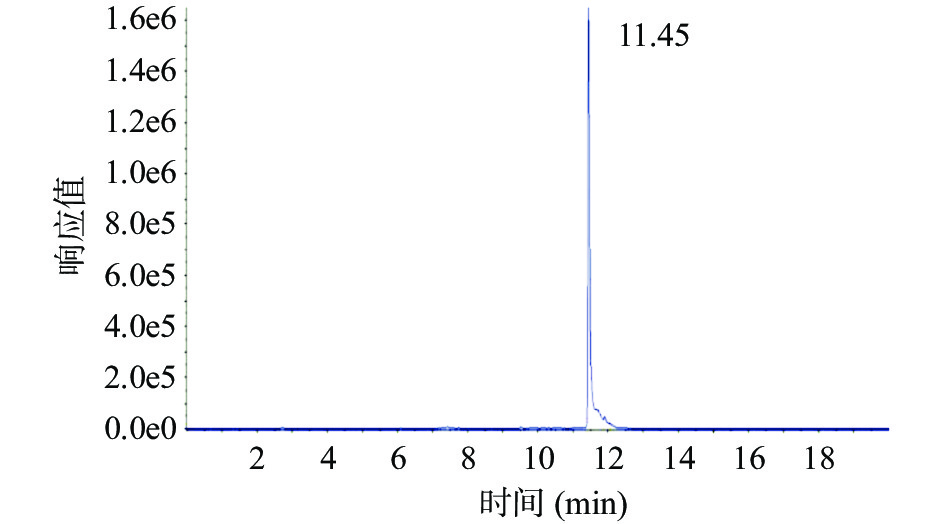
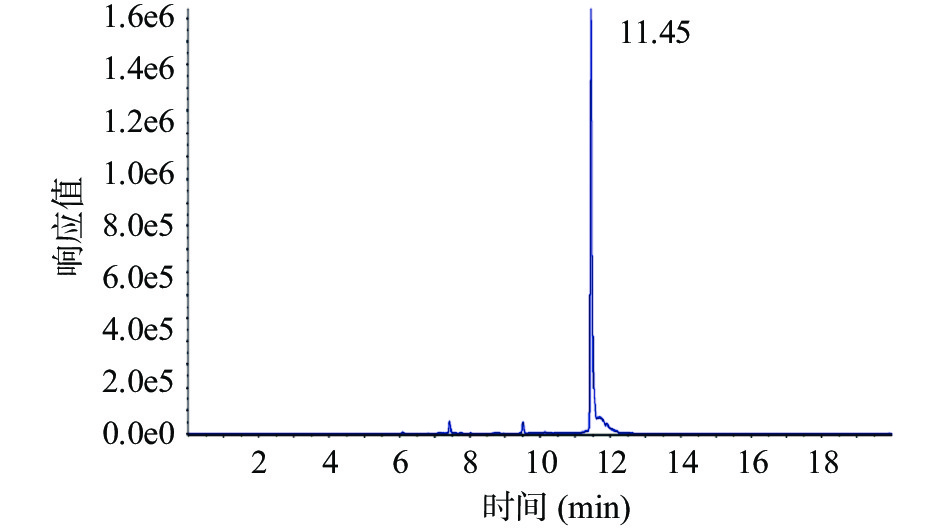
2.4 雪地茶甲醇提取物中松萝酸的含量测定
由图5和图6可知,雪地茶甲醇提取物中的松萝酸含量为0.8613%,其乙酸乙酯萃取物中的松萝酸含量为0.9379%,乙酸乙酯萃取物中松萝酸的含量高于甲醇提取物中的松萝酸含量。乙酸乙酯提取物的抑菌圈也大于甲醇提取物,但二者之间是否有必然联系,还需进一步的分离纯化来验证抑菌活性。
3. 讨论与结论
本研究制备雪地茶甲醇粗提物的目的是得到包含更多有效抑菌成分的提取物,对于雪地茶是否具有抗菌作用及抗菌稳定性进行初步探索。结果显示,雪地茶甲醇提取物具有较好的抑菌活性,水提物无抑菌活性,说明雪地茶抑菌活性物质主要溶于甲醇,并且甲醇提取物具有广谱的抑菌效果,对革兰氏阳性菌、革兰氏阴性菌、真菌都有抑菌活性,其抑菌机理有待进一步研究。以金黄色葡萄球菌为指示菌,探究其抑菌稳定性,热处理对雪地茶提取物的抑菌活性无明显影响;pH在接近强酸和强碱时,提取物抑菌活性呈极显著下降趋势(P<0.01),但仍然有抑菌活性;紫外照射在40 min以上,抑菌活性也会略微下降。结果表明食品加工过程中,常见的热处理不会对其抑菌活性产生影响,在紫外光灭菌处理时,尽量不超过30 min。其抑菌活性物质在温度、pH、紫外线的照射的影响下,都比较稳定。进一步对甲醇提取物进行分级萃取,发现抑菌活性成分主要集中在乙酸乙酯萃取物中,根据前人研究以松萝酸为代表的缩酚酸及其衍生物可能为抑菌主要活性成分[7],测定甲醇提取物及乙酸乙酯萃取物中的松萝酸含量,乙酸乙酯提取物的抑菌圈直径大于甲醇提取物直径,乙酸乙酯提取物中的松萝酸含量大于甲醇提取物的含量,推测抑菌活性可能与松萝酸含量有关,但需要进一步分离纯化验证。本研究为雪地茶甲醇提取物应用于食品防腐、抑菌提供了理论依据,目前对于雪地茶抑菌的研究甚少,本研究为雪地茶抑菌活性物质的分离纯化、抑菌机理的探究提供了数据支撑。
-
表 1 松萝酸的UPLC-MS/MS测定参数
Table 1 Determination parameters of usnic acid by UPLC-MS/MS
化合物 保留时间(min) 分子式 母离子(m/z) 子离子(m/z) 驻留时间(ms) 去簇电压DP/V 碰撞能量CE/V 松萝酸 11.45 C18H16O7 342.9 328*
258.8
299100 −60 −28.38
−29.23
−24.18注:*表示定量离子。 表 2 雪地茶甲醇提取物抑菌作用
Table 2 Antibacterial effect of methanol extract from Thamnolia subuliformis
菌种名称 革兰氏染色 抑菌圈直径(mm) 金黄色葡萄球菌 阳性 16.8±0.9 枯草芽孢杆菌 15.7±1.6 斯氏李斯特菌 15.4±0.8 表面葡萄球菌 20.0±1.6 伊氏李斯特氏菌 16.7±0.7 单增李斯特菌 0.0 甲型副伤寒杆菌 阴性 15.2±2.1 乙型副伤寒杆菌 16.5±2.0 大肠埃希菌 0.0 福氏志贺菌 0.0 肺炎克雷伯菌 0.0 绿脓杆菌 0.0 白色念珠菌 真菌 22.4±0.5 酵母菌 0.0 表 3 雪地茶甲醇提取物的最低抑菌浓度
Table 3 Minimum inhibitory concentration of methanol extract of Thamnolia subuliformis
质量浓度(mg/mL) 10.000 5.000 2.500 1.250 0.625 0.313 0.156 0.018 0.039 金黄色葡萄球菌 MBC − − − MIC + ++ +++ +++ 注:“−”表示无菌生长,“+”表示菌体生长少,“++”表示菌体生长较多,“+++”表示菌体生长很多。 -
[1] 程挚. 云南丽江白雪茶化学成分研究[D]. 昆明: 西南林业大学, 2015. CHENG Z. Study on chemical constituents of Thamnolia vermicularis grown in Yunnan[D]. Kunming: Southwest Forestry University, 2015.
[2] LI C, GUO X D, LEI M, et al. Thamnolia vermicularisa extract improves learning ability in APP/PS1 transgenic mice by ameliorating both Abeta and Tau pathologies[J]. Acta Pharmacologica Sinica,2017,38(1):9−28. doi: 10.1038/aps.2016.94
[3] U H Y, XUEQING S, DAN L, et al. The protective effects of β-sitosterol and vermicularin from Thamnolia vermicularis(Sw.) Ach. against skin aging in vitro[J]. Anais Da Academia Brasileira De Ciências,2019,4(91):e20181088.
[4] RA YEONG C, JU R H, JIYOUNG Y, et al. Anti-obesity property of Lichen Thamnolia vermicularis extract in 3T3-L1 cells and diet-induced obese mice[J]. Preventive Nutrition and Food Science,2017,22(4):285−292. doi: 10.3746/pnf.2017.22.4.285
[5] 林春榕, 罗永会, 张翠香, 等. 云南丽江产白雪茶多糖提取工艺及抗氧化作用[J]. 食品研究与开发,2013,34(8):16−19. [LIN Chunrong, LUO Yonghui, ZHANG Cuixiang, et al. Research on extraction technology and anti-oxidation effect of polysaccharide from Thamnolia vermicularis grown in Lijiang, Yunnan[J]. Food Research and Development,2013,34(8):16−19. [6] 程璐, 翟亚楠, 孙立彦, 等. 地衣及其内生真菌活性次级代谢产物研究进展[J]. 菌物学报,2021,40(1):14−30. [CHENG Lu, ZHAI Yanan, SUN Liyan, et al. Research progress on bioactive secondary metabolites of lichens and endolichenic fungi[J]. Mycosystema Mycosystema,2021,40(1):14−30. [7] MARIJANA K, BRANISLAV R, TATJANAS, et al. Cladonia lichens and their major metabolites as possible natural antioxidant, antimicrobial and anticancer agents[J]. LWT-Food Science and Technology,2014,59(1):1−27. doi: 10.1016/j.lwt.2014.05.020
[8] MARIJANA K, NEDELJKO M, SLOBODAN J, et al. Evernia prunastri andPseudoevernia furfuraceae lichens and their major metabolites as antioxidant, antimicrobial and anticancer agents[J]. Food & Chemical Toxicology,2013,53:112−118.
[9] 马宇翔, 唐燕霞, 包海鹰. 硬枝树花中4个单体化合物的抑菌活性[J]. 菌物研究,2015,13(3):168−174. [MA Yuxiang, TANG Yanxia, BAO Haiying. Antibacterial activities of four compounds extracted from Ramalina conduplicans[J]. Mycosystema Mycosystema,2015,13(3):168−174. [10] 程挚. 云南白雪茶研究现状及开发利用[J]. 安徽农业科学,2015,43(11):289−290. [CHENG Zhi. Current research and exploitation of Thamnolia vermicularis in Yunnan[J]. Journal of Anhui Agricultural Sciences,2015,43(11):289−290. doi: 10.3969/j.issn.0517-6611.2015.11.108 [11] 汪琼, 程挚, 鄢波. 丽江白雪茶化学成分的研究[J]. 广西植物,2017,37(12):1586−1591. [WANG Qiong, CHENG Zhi, YAN Bo. Chemical constituents from Thamnolia vermicularis in Lijiang[J]. Guihaia,2017,37(12):1586−1591. doi: 10.11931/guihaia.gxzw201703034 [12] 邓云霞, 邵志宇, 张夙滢, 等. 雪茶的化学成分研究[J]. 中药材,2017,40(5):1109−1111. [DENG Yunxia, SHAO Zhiyu, ZHANG Suying, et al. Chemical constituents of Thamnolia subuliformis[J]. Journal of Chinese Medicinal Materials,2017,40(5):1109−1111. [13] 付长华. 药用茶叶提取物的制备工艺研究[J]. 实用中西医结合临床,2019,19(9):173−174. [FU Changhua. Research on the preparation technology of medicinal tea extract[J]. Practical Clinical Journal of Integrated Traditional Chinese and Western Medicine,2019,19(9):173−174. [14] 谭才邓, 朱美娟, 杜淑霞, 等. 抑菌试验中抑菌圈法的比较研究[J]. 食品工业,2016,37(11):122−125. [TAN Caideng, ZHU Meijuan, DU Shuxia, et al. Study on the inhibition zone method in antimicrobial test[J]. The Food Industry,2016,37(11):122−125. [15] LI Z H, CAI M, LIU Y S, et al. Antibacterial activity and mechanisms of essential oil from Citrus medica L. var. sarcodactylis[J]. Molecules,2019,24(8):1577. doi: 10.3390/molecules24081577
[16] 戚馨月, 曹瑶, 周建新, 等. 花生壳分级提取物抑菌活性及其稳定性[J]. 食品工业科技,2020,41(3):120−124. [QI Xinyue, CAO Yao, ZHOU Jianxin, et al. Antibacterial characteristics and stability of fractionated extracts from peanut Hull[J]. Science and Technology of Food Industry,2020,41(3):120−124. [17] LIU G, REN G, ZHAO L. Antibacterial activity and mechanism of bifidocin a against Listeria monocytogenes[J]. Food Control,2017,73:854−861. doi: 10.1016/j.foodcont.2016.09.036
[18] YIN M, XIAOJUAN Z, ZHENGHONG X. Identification of antibacterial substances of Lactobacillus plantarum DY-6 for bacteriostatic action[J]. Food Science & Nutrition,2020,8(6):1−10.
[19] ZANGENEH M, KHORRAMI S, KHALEGHI M. Bacteriostatic activity and partial characterization of the bacteriocin produced by L. plantarum sp. isolated from traditional sourdough[J]. Food Science & Nutrition,2020,8(11):6024−6030.
[20] 刘海燕, 张建伟. 明日叶提取物抑菌活性成分稳定性的研究[J]. 食品研究与开发,2016,37(10):39−42. [LIU Haiyan, ZHANG Jianwei. Study on stability of antibacterial activity compositions extracted from Ashitaba[J]. Food Research and Development,2016,37(10):39−42. doi: 10.3969/j.issn.1005-6521.2016.10.010 [21] 赵颖, 宋丹, 钟国跃, 等. HPLC法测定雪地茶中松萝酸[J]. 中草药,2009,40(S1):281−282. [ZHAO Ying, SONG Dan, ZHONG Guoyue, et al. Determination of usnic acid in Xuedi tea by HPLC[J]. Chinese Herbal Medicine,2009,40(S1):281−282. [22] KOSANIĆ M R B. Lichen secondary metabolites as potential antibiotic agents. In: Ranković B , editor. Lichen secondary metabolites bioactive properties and pharmaceutical potential[M]. Springer International Publishing, 2015, 81−104.
[23] 房敏峰, 王启林, 胡正海. 地衣化学成分和药理作用研究进展[J]. 中草药,2011,42(12):2571−2576. [FANG Minfeng, WANG Qilin, HU Zhenghai. Advances in studies on chemical constituents from lichen and their pharmacological effects[J]. Chinese Traditional and Herbal Drugs,2011,42(12):2571−2576. [24] 牛东玲, 胡礼芳, 马茜, 等. 松萝酸活性作用机理及其物种资源研究概况[J]. 广西植物,2019,39(1):136−142. [NIU Dongling, HU Lifang, MA Qian, et al. Review on bioactivity mechanism and species resources of usnic acid[J]. Guihaia,2019,39(1):136−142. doi: 10.11931/guihaia.gxzw201801035 [25] PARAMASIVAM N, RAJA M B S, SUBRAMANIAN M, et al. Usnic acid inhibits biofilm formation and virulent morphological traits of Candida albicans[J]. Microbiological Research,2015,179:20−28. doi: 10.1016/j.micres.2015.06.009
[26] 袁中伟, 谷可欣, 张天翼, 等. 松萝酸对耐甲氧西林金黄色葡萄球菌的抑菌作用机制研究[J]. 甘肃农业大学学报,2019,54(4):22−29. [YUAN Zhongwei, GU Kexin, ZHANG Tianyi, et al. Antibacterial mechanism of usnic acid on methicillin-resistant Staphylococcus aureus[J]. Journal of Gansu Agricultural University,2019,54(4):22−29. [27] MONIKA M D, GRZEGORZ W, BEATA G K. Antibacterial activity of lichen secondary metabolite usnic acid is primarily caused by inhibition of RNA and DNA synthesis[J]. Fems Microbiology Letters,2014,353(1):57−62. doi: 10.1111/1574-6968.12409
[28] 崔新洁, 夏瑾, 尤金彪. 24味中药对金黄色葡萄球菌生物膜作用的研究[J]. 时珍国医国药,2017,28(5):1079−1081. [CUI Xinjie, XIA Jin, YOU Jinbiao. Study on twenty-four traditional chinese medicines against Staphylococcus aureus biofilm in vitro[J]. Lishizhen Medicine and Materia Medica Research,2017,28(5):1079−1081. [29] 高飞雄, 梁引库, 李云祥. 蒲公英植酸对沙门氏菌抑制作用及其抑菌机理研究[J]. 天然产物研究与开发,2019,31(6):975−980. [GAO Feixiong, LIANG Yinku, LI Yunxiang. Antibacterial effect and mechanism of dandelion phytic acid on Salmonella[J]. Natural Product Research and Development,2019,31(6):975−980. [30] 柯发敏, 张开莲. 没食子酸的研究进展[J]. 泸州医学院学报,2011,34(4):440−442. [KE Famin, ZHANG Kailian. Research progress of gallic acid[J]. Journal of Luzhou Medical College,2011,34(4):440−442. [31] 孙长花, 于智勇, 丁娟芳, 等. 丁香提取物抑菌作用及稳定性研究[J]. 生物学杂志,2021,38(1):61−65. [SUN Changhua, YU Zhiyong, DING Juanfang, et al. Study on bacteriostasis and stability of clove extract[J]. Journal of Biology,2021,38(1):61−65. doi: 10.3969/j.issn.2095-1736.2021.01.061 [32] 黄海英, 李晓娟, 李正英. 诃子水提物抑菌活性成分稳定性[J]. 北方园艺,2020(5):104−108. [HUANG Haiying, LI Xiaojuan, LI Zhengying. Study on the stability of antibacterial active components by aqueous extract of Erminalia[J]. Northern Horticulture,2020(5):104−108. [33] 陈锦英, 罗忠明. 芝麻酚稳定性的研究[J]. 食品研究与开发,2015,36(4):14−18. [CHEN Jinying, LUO Zhongming. Study on stability of sesamol[J]. Food Research and Development,2015,36(4):14−18. doi: 10.3969/j.issn.1005-6521.2015.04.005 [34] 赵磊, 林文轩, 迟茜, 等. 甜叶菊废渣提取物抑菌活性及抑菌稳定性研究[J]. 食品工业科技,2016,37(24):168−172. [ZHAO Lei, LIN Wenxuan, CHI Qian, et al. Antibacterial activity and stability of Stevia rebaudiana waste extract[J]. Science and Technology of Food Industry,2016,37(24):168−172. [35] 过尘杰, 傅瑜. 环境因素对杨梅叶原花色素的稳定性影响[J]. 科技风,2017(5):218−220. [GUO Chenjie, FU Yu. Effects of environmental factors on the stability of proanthocyanidins from bayberry leaves[J]. Technology Wind,2017(5):218−220. [36] 冯靖, 彭效明, 李翠清, 等. 银杏叶黄酮的抗氧化性及其稳定性研究[J]. 食品科技,2019,44(4):244−249. [FENG Jing, PENG Xiaoming, LI Cuiqing, et al. Antioxidant activity and stability of flavonoids from ginkgo leaves[J]. Food Technology,2019,44(4):244−249. [37] 林国荣, 杨丽洪. 加工条件对葡萄多酚稳定性影响的研究[J]. 食品科技,2019,44(11):267−272. [LIN Guorong, YANG Lihong. Study on the effect of processing conditions on the stability of grape polyphenols[J]. Food Technology,2019,44(11):267−272. -
期刊类型引用(7)
1. 王安婧,朱越,韩诗晴,韩柱,诸葛慧,贾小转,王迎超,杨振中. 基于序贯分析策略的丹红注射液与临床常用输液溶媒配伍稳定性及安全性评价. 药物分析杂志. 2024(03): 493-500 .  百度学术
百度学术
2. 彭剑岚,朱永苹,林寿宁,廖冬燕,尹静雯. 黄芪及其活性成分治疗胃癌的作用机制研究进展. 中华中医药学刊. 2023(04): 196-201 .  百度学术
百度学术
3. 李建文,郭海波,马婷婷,冯浩彬,靳玲. 核磁共振波谱技术在药品质量与安全方面的应用研究. 广东化工. 2023(10): 195-196 .  百度学术
百度学术
4. 钟勇,刘菡菡,赵永发,谢俊. 注射用红花黄色素的质量控制及安全性研究. 临床医药实践. 2023(07): 509-512 .  百度学术
百度学术
5. 梁泰帅,郑淑涵,赵肖琼. 独脚金内酯(SLs)对盐碱胁迫下恒山黄芪种子萌发和幼苗生长的影响. 种子. 2023(12): 90-95+102 .  百度学术
百度学术
6. 张弘弛,刘瑞,高志慧,李慧,杨阳. 恒山黄芪毛状根遗传转化体系的建立及活性成分含量测定. 北方园艺. 2022(09): 93-99 .  百度学术
百度学术
7. 姜莉,王成,邢颖,徐怀德. 不同提取方法对黄芪提取液活性成分及抗氧化性的影响. 食品研究与开发. 2022(16): 119-126 .  百度学术
百度学术
其他类型引用(3)





 下载:
下载:
 下载:
下载:



