Ultrasonic-assisted Ezymatic Hydrolysis of Peanut Protein to Prepare α-Amylase Inhibitory Peptide
-
摘要: 本文以花生粕为原料,通过碱溶酸沉法提取花生蛋白,利用凯式定氮法测得其含量87.7%。继续采用超声波辅助酶法制取花生多肽,以多肽得率和α-淀粉酶抑制率为指标,考察了酶的种类、超声功率、超声时间、底物浓度、酶添加量和酶解时间等因素对α-淀粉酶抑制肽的影响,确定最优蛋白酶为风味蛋白酶,在单因素的基础上设计响应面试验对酶解条件进行优化,确定制备α-淀粉酶抑制肽最佳工艺条件为:超声功率150 W、超声时间30 min、液料比20:1 mL/g、酶添加量5000 U/g、酶解时间2 h。在此条件下多肽得率为41.92%,α-淀粉酶抑制率为50.62%,与未经过超声波辅助的花生多肽α-淀粉酶抑制率35.45%相比有显著提升。根据α-淀粉酶抑制肽最佳工艺,将蛋白酶解液超滤分级分离,得到四个不同组分>10 kDa、5~10 kDa、3~5 kDa、<3 kDa,其中<3 kDa组分分子量抑制率达到最高60.21%。利用Sephadex G-15凝胶分离纯化<3 kDa组分,得到P1、P2、P3三个组份,其中P3最高抑制率可达到73.30%。花生肽具有较好的ɑ-淀粉酶抑制效果,在开发功能性食品研究中有较大的应用价值。Abstract: In this paper, peanut protein was extracted from peanut meal by alkaline solution and acid precipitation. The content of peanut protein was 87.7% by Kjeldahl method. Peanut polypeptides were prepared by ultrasonic-assisted enzymatic method. The effects of enzyme type, ultrasonic power, ultrasonic time, substrate concentration, enzyme addition amount and enzymolysis time on α-amylase inhibitory peptide were investigated using the yield of polypeptide and α-amylase inhibition rate as indexes. The optimal protease was flavor protease. Response surface test was designed to optimize the enzymolysis conditions on the basis of single factor. The optimal conditions were determined as follows: Ultrasonic power 150 W, ultrasonic time 30 min, liquid-solid ratio 20:1 mL/g, enzyme dosage 5000 U/g, enzymolysis time 2 h. Under these conditions, the yield of polypeptide was 41.92%, and the inhibitory rate of α-amylase was 50.62%, which was significantly higher than that of peanut polypeptide α-amylase which was 35.45% without ultrasonic assistance. According to the optimal process of α-amylase inhibitory peptide, the hydrolysate was separated by ultrafiltration and obtained four different fractions >10 kDa, 5~10 kDa, 3~5 kDa and <3 kDa, among which the molecular weight inhibition rate of <3 kDa fraction reached the highest 60.21%. Sephadex G-15 gel was used to separate and purify the <3 kDa components, and three components, P1, P2 and P3 were obtained. The highest inhibition rate of P3 reached 73.30%. Peanut peptide had good α-amylase inhibitory effect and had great application value in developing functional food.
-
花生粕是饲料、肥料和酿造的原料,是花生油提取后的副产品[1]。花生粕的蛋白质含量约为40%~50%,包含8种必需氨基酸,但花生蛋白质中的赖氨酸和蛋氨酸含量相对不足。与大豆蛋白相比,花生粕蛋白更易于吸收且抗营养因子较低[2]。花生粕蛋白的酶促水解不仅可以充分利用花生粕中的蛋白质,而且还可以产生具有生物活性的小肽,解决了花生蛋白必需氨基酸不足的缺陷。已有研究描述了食物来源的短链生物活性肽,其残基范围为2~20个氨基酸[3]。 除了基本营养外,还具有类似激素的生理功能[4]。这些肽可能具有多种药理或生理作用,包括抗氧化剂、抗糖尿病药和降低血压[5-7],具体取决于氨基酸的组成及其序列。Liu等[8]从花生蛋白分离物中分离出一种血管紧张素转化酶(angiotensin converting enzyme,ACE)抑制肽,其氨基酸序列为Cys-Val-Thr-Pro-Ala-Leu-Arg。Ye和Ng[9]从花生中分离出一种新型的抗真菌肽,其序列与花生过敏原Ara H1相似。在人肠中对氨基酸的吸收很差,但是分子量小于1000 Da的寡肽很容易被吸收[10]。
食物来源的生物活性肽在药理活性方面被广泛研究[11-13]。 具有特定氨基酸序列的肽在减少和维持饮食相关疾病(例如糖尿病(diabetes,DM))的发作方面具有特别重要的意义[14]。DM是一种复杂的代谢综合症,由生产减少、生物利用度不足和胰岛素对血浆葡萄糖水平升高的敏感性差引起。在复杂的碳水化合物进一步转化成更简单的形式(葡萄糖)并吸收到血液系统之前,α-淀粉酶起着引发化学分解的基本作用。研究表明,在饮食混合碳水化合物后,抑制α-淀粉酶可以大大降低餐后血糖水平的升高[15]。因此为控制II型糖尿病,具有α-淀粉酶抑制潜能的功能性食品和营养保健品得到了广泛认可。本研究将花生粕提取蛋白进行酶解,以α-淀粉酶抑制率和多肽得率为评价指标,筛选出最佳蛋白酶,通过酶解条件优化实验获得最佳酶解工艺条件,获得α-淀粉酶抑制肽。
1. 材料与方法
1.1 材料与仪器
花生粕 青岛长寿食品有限公司;风味蛋白酶(1.5万U/g)、碱性蛋白酶(20万U/g)、胰蛋白酶(250万U/g) 北京索莱宝科技有限公司;中性蛋白酶(100 U/g)、木瓜蛋白酶(≥100万U/g)、α-淀粉酶 上海源叶生物科技有限公司;牛血清蛋白 长春德尔塔生物技术有限公司。
LG0.2真空冷冻干燥机 沈阳航天新阳速冻设备制造有限公司;HC-3018高速离心机 安徽中科中佳科学仪器有限公司;SPD-20A UVmini-1240紫外可见分光光度计 日本岛津公司;
1.2 实验方法
1.2.1 花生蛋白制备
将花生粕以10:1 mL/g液料比与蒸馏水混合,以1 mol/L NaOH溶液将pH调至8.0,常温磁力搅拌1 h后5000 r/min离心15 min,离心后取上层清液以1 mol/L HCL溶液调节pH至4.5,4000 r/min离心10 min后取下层沉淀,加适量蒸馏水用1 mol/L NaOH溶液调至中性使其充分溶解,将溶解后的蛋白液用透析袋透析24 h后冷冻干燥备用[16]。
1.2.2 花生多肽制备
称取花生蛋白加入蒸馏水,按液料比为20:1 mL/g配制成溶液,进行超声波预处理,超声波预处理条件为超声功率150 W,超声温度35 ℃,超声时间20 min。预处理结束后调节温度和pH至各蛋白酶最适条件(见表1),蛋白酶添加量为4000 U/g,酶解3 h。酶解后沸水浴灭酶10 min,冰水浴冷却,以10000 r/min,离心20 min,收集上清液测其多肽得率及α-淀粉酶抑制率后冷冻干燥备用[17]。
表 1 不同蛋白酶最适反应条件Table 1. Optimal reaction conditions for different enzymes蛋白酶种类 酶解条件 温度(℃) pH 风味蛋白酶 50 7 胰蛋白酶 50 7 碱性蛋白酶 50 10 木瓜蛋白酶 55 7 中性蛋白酶 50 7 1.2.3 花生蛋白酶解工艺优化
1.2.3.1 蛋白酶的筛选
为了筛选出酶解花生蛋白的最优蛋白酶种类,对比了5种蛋白酶对花生蛋白的酶解效果,在表1中所列的各蛋白酶的最适条件下,以花生蛋白液料比20:1mL/g,超声功率150 W,超声时间30 min,酶添加量5000 U/g,酶解3 h。以α-淀粉酶抑制率和多肽得率为指标,筛选出最优蛋白酶,进行下一步试验。
1.2.3.2 单因素实验
准确称取一定量的花生蛋白,以1.2.2的酶解工艺,设计花生蛋白液料比(10:1、15:1、20:1、25:1、30:1)、超声功率(50、100、150、200、250 W)、超声时间(10、20、30、40、50 min)、酶添加量(2000、3000、4000、5000、6000 U/g)、酶解时间(1、2、3、4、5 h)的五个因素实验,研究五个因素对制备α-淀粉酶抑制肽的影响,进而确定因素以及水平范围内响应面试验的设计。
1.2.3.3 响应面试验
在单因素实验结果的基础上,以α-淀粉酶抑制率为主要指标,采用单因素实验结果中对花生粕蛋白酶解效果影响较大的三个因素进行响应面试验。采用Design-Expert.V8.0.6统计软件,设计三因素三水平二次回归方程,拟合各因素和α-淀粉酶抑制率的函数关系。试验因素水平见表2。
表 2 酶解工艺响应面水平与因素设计Table 2. Response surface level and factor design table of enzymatic hydrolysis process水平 因素 A液料比(mL/g) B超声时间(min) C酶添加量(U/g) −1 15:1 20 4000 0 20:1 30 5000 1 25:1 40 6000 1.2.4 测定方法
1.2.4.1 花生蛋白含量测定
利用凯氏定氮法测定花生粕蛋白含量,方法参考国标GB 5009.5-2016《食品安全国家标准—食品中蛋白质的测定》。
1.2.4.2 α-淀粉酶活性抑制率的测定
在0.5 mL PBS溶液中加入0.25 mL酶解溶液和等体积的1.5 U/mL α-淀粉酶溶液,于37 ℃加热10 min后,再加入0.5 mL 1%可溶性淀粉溶液,取0.25 mL酶解溶液和等体积的1.5 U/mL α-淀粉酶溶液,加入到0.5 mL PBS溶液中于37 ℃加热10 min后,再加入0.5 mL 1%可溶性淀粉溶液,充分混匀,反应5 min后加入1 mL DNS终止反应,沸水浴10 min冷却至室温后加入5 mL水,于540 nm测定吸光度OD值[18-22]。
α−淀粉酶抑制率(%)=(1−ODC−ODDODA−ODB)×100 式中:ODA为空白管;ODB为空白对照管;ODB为抑制管;ODD为抑制对照管。
1.2.4.3 多肽得率测定
采用双缩脲法绘制牛血清蛋白标准曲线[23-24]。将牛血清蛋白配制成10 mg/mL的标准蛋白溶液,分别取0.0、0.2、0.4、0.6、0.8、1.0 mL于试管中,加蒸馏水补至1 mL,再加入4 mL双缩脲试剂,混匀均匀后静置30 min,于540 nm处分别测其OD值。以标准蛋白浓度为横坐标,吸光度为纵坐标,绘制标准曲线。标准曲线为y=0.04136x+0.05146,R2=0.9997。
多肽液样品含量测定:取1 mL样品溶液加入等体积的10%(W/V)的三氯乙酸混合均匀后,静止10 min,于4000 r/min离心20 min,取上清液1 mL,并加入4 mL双缩脲试剂,混合后室温静置30 min,测定540 nm处吸光度。
W(%)=c×D×Vm×100 式中:W表示多肽得率,%;c表示根据吸光度值计算出的溶液质量浓度,mg/mL;D表示溶液稀释倍数;V表示溶液体积,mL;m表示花生蛋白取样量,mg。
1.2.5 超滤分离
花生蛋白酶解液经水相0.45 µm微孔滤膜过滤,选择截取分子量分别为10、5、3 kDa的超滤膜对酶解液进行分级分离,将所得多肽组分分别收集后迅速冷冻干燥,−20 ℃保存备用。
1.2.6 Sephadex G-15凝胶分离纯化
方法根据江明珠、陈佳欣等人的修改稍作调改[25-26]。将处理好的Sephadex G-15装入1.6 cm×100 cm的玻璃层析柱中。选取无菌水进行洗脱试验,上样浓度为10 mg/mL,上样量为2 mL,洗脱流速为0.8 mL/min,用紫外检测仪在220 nm处进行检测,收集器每4 min一管,将收集的各个洗脱峰冷冻干燥得到花生多肽,测定各组分ɑ-淀粉酶抑制率。
1.3 数据处理
所有实验均进行三次平行实验,数据采用平均值±标准差的形式,采用Orign 8.5、Design Expert 8.0.6 软件对试验数据进行处理。
2. 结果与分析
2.1 蛋白酶筛选结果
由图1可知,五种蛋白酶的多肽得率都超过了30%,对α-淀粉酶也有一定的抑制效果,说明五种酶对花生多肽都有一定得酶解效果,其中风味蛋白酶无论是在α-淀粉酶抑制率还是多肽得率,都表现出不错的结果。碱性蛋白酶和中性蛋白酶的多肽得率也表现出不错的效果,但其α-淀粉酶抑制率低于风味蛋白酶,考虑可能是由于蛋白酶解程度越大,多肽得率越高,生成的小分子肽段越多导致具有抑制活性的肽段越少,因此,选择风味蛋白酶进行后续实验。
2.2 单因素实验结果
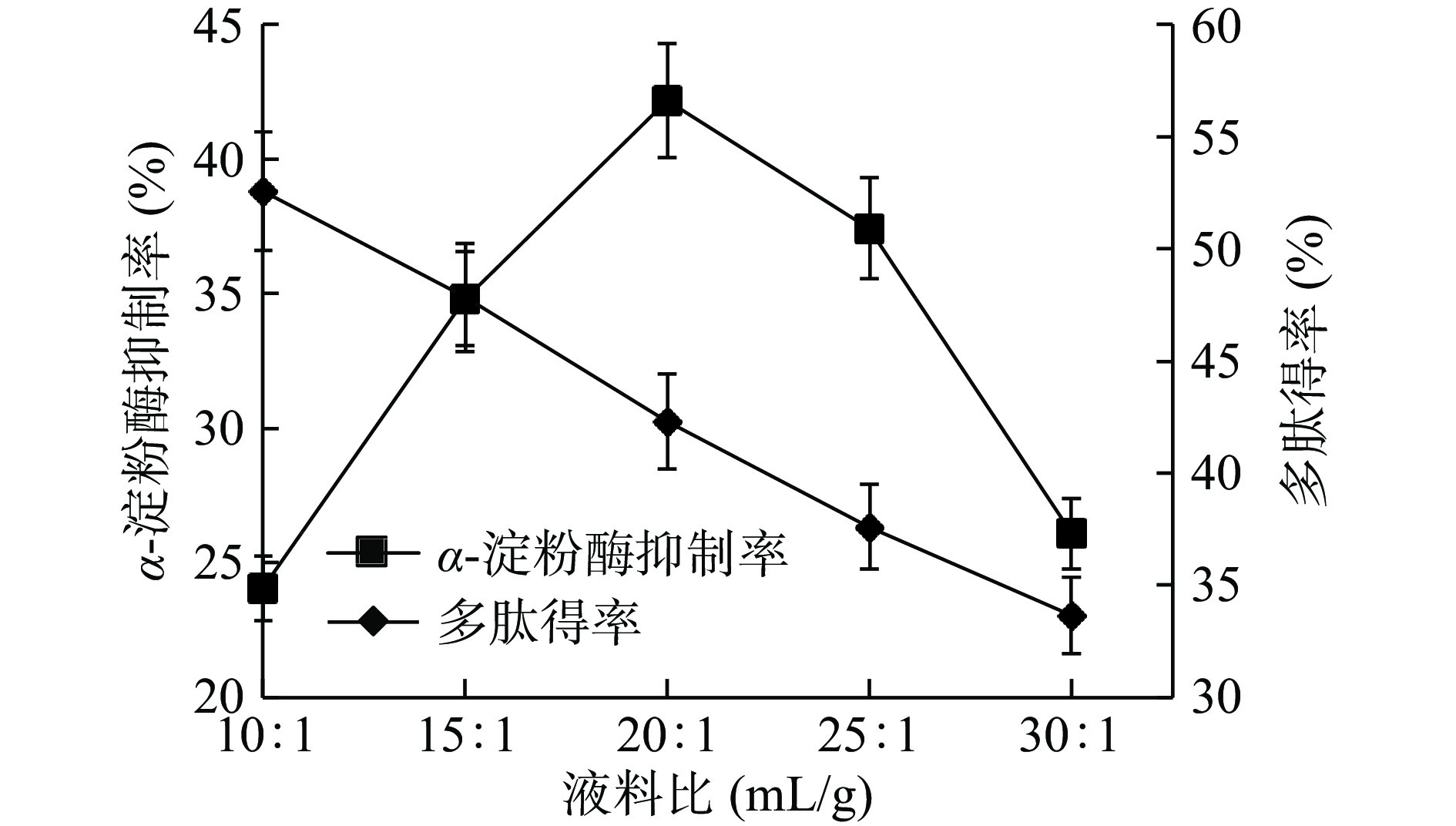
2.2.1 料液比对蛋白酶解液的影响
由图2可知,酶添加量一定时,多肽得率随液料比的增大而降低,这是因为底物浓度越低,其与酶结合的几率就越低,多肽得率也越低[25]。α-淀粉酶活性抑制率呈现先上升后下降的趋势,在液料比为20:1 mL/g时α-淀粉酶活性抑制率最高为42.19%。因此风味蛋白酶制备花生粕多肽的最佳料液比为20:1 mL/g。
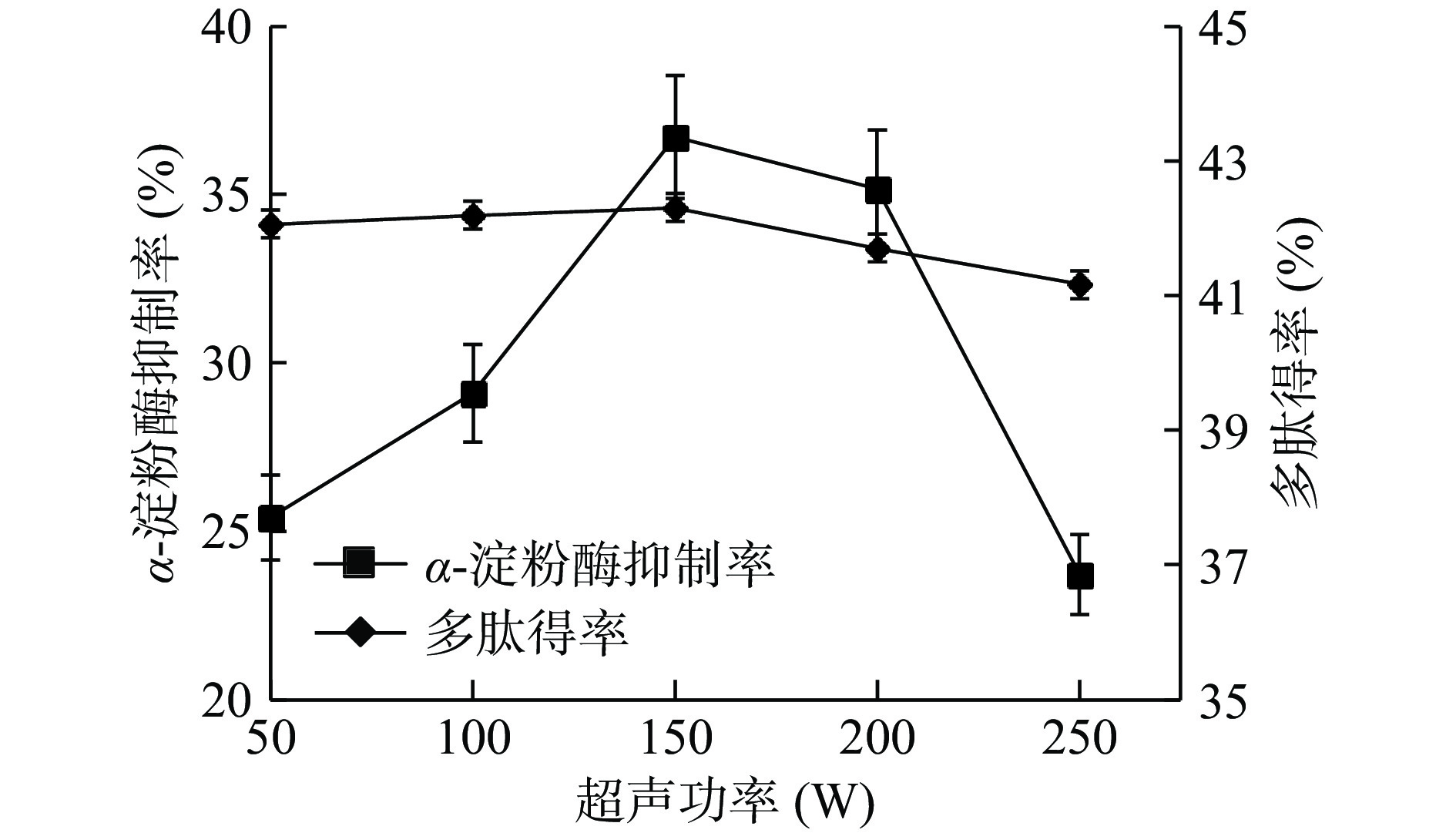
2.2.2 超声功率对蛋白酶解液的影响
超声波预处理能破坏花生蛋白的结构,使酶的结合位点增多,更容易使花生蛋白酶解为小分子肽段。由图3可知,多肽得率和α-淀粉酶抑制率都随超声功率的增大呈现先上升后下降的趋势,当超声功率为150 W时,α-淀粉酶活性抑制率为最大值36.7%,但当超声功率继续升高时,花生蛋白结构被破坏,酶结合位点持续增多,大分子蛋白被酶解为更小的分子量的短肽,导致α-淀粉酶抑制率降低。因此风味蛋白酶制备花生粕多肽的最佳超声功率为150 W。
2.2.3 超声时间对蛋白酶解液的影响
由图4可知,超声功率一定时,随着超声时间的延长,多肽得率和α-淀粉酶活性抑制率都呈现出先上升再下降的趋势,当超声时间为30 min时,多肽得率和α-淀粉酶活性抑制率达到最大值分别为42.3%和40.07%。这可能是因为超声波空化作用对蛋白分子产生的剪切作用力和瞬间高压,能够使花生蛋白结构被破坏,酶结合位点增多,具有抑制活性的产物抑制率随之增加,因此风味蛋白酶制备花生粕多肽的最佳超声时间为30 min。
2.2.4 酶添加量对蛋白酶解液的影响
由图5可知,随着酶添加量的增大,蛋白液不断被酶解解,多肽得率随之上升,α-淀粉酶抑制率先上升后下降,增大酶添加量使其与底物充分接触,大分子蛋白质被水解成不同分子量的肽段,α-淀粉酶抑制率出现降低[27]。当酶添加量为5000 U/g时,α-淀粉酶活性抑制率达到最大值为51.62%。因此风味蛋白酶制备花生粕多肽的最佳酶添加量为5000 U/g。
2.2.5 酶解时间对蛋白酶解液的影响
由图6可知,随着酶解时间的延长,多肽得率逐渐升高,ɑ-淀粉酶活性抑制率出现先升高后降低的趋势,这是因为具有ɑ-淀粉酶抑制作用的有效肽段随着水解的继续进行,被酶解成无抑制活性的小肽,从而活性抑制率降低[28],当酶解时间为2 h时,ɑ-淀粉酶活性抑制率达到最大值40.78%。考虑到以上原因,风味蛋白酶制备花生粕多肽最佳酶解时间为2 h。
2.3 响应面优化试验设计及结果
采用Design-Expert.V8.0.6统计软件设计,响应面优化试验结果见表3,回归方差分析见表4。
表 3 响应面试验设计及结果Table 3. Design and results of response surface experiment试验号 液料比 超声时间 酶添加量 α-淀粉酶抑制率(%) 1 0 1 1 44.76 2 0 0 0 50.51 3 0 0 0 49.58 4 0 1 −1 39.9 5 1 1 0 41.58 6 1 −1 0 43.76 7 0 −1 −1 41.63 8 0 0 0 51.62 9 −1 0 1 45.52 10 0 0 0 51.07 11 −1 −1 0 40.85 12 1 0 1 47.31 13 1 0 −1 42.55 14 −1 1 0 39.01 15 0 −1 1 46.55 16 −1 0 −1 40.89 17 0 0 0 50.99 表 4 响应面试验回归模型方差分析Table 4. Variance analysis for the fitted regression equation方差来源 平方和 自由度 均平方 F值 P值 显著性水平 模型 450.15 9 50.02 114.92 < 0.0001 *** A 12.60 1 12.60 28.95 0.0010 ** B 2.49 1 2.49 5.71 0.0482 * C 97.02 1 97.02 222.92 < 0.0001 *** AB 0.065 1 0.065 0.15 0.7106 AC 5.59 1 5.59 12.85 0.0089 ** BC 1.78 1 1.78 4.09 0.0827 A2 14.78 1 14.78 33.97 0.0006 ** B2 28.00 1 28.00 64.33 < 0.0001 ** C2 267.04 1 267.04 613.55 < 0.0001 *** 残差 3.05 7 0.44 失拟项 1.85 3 0.62 2.05 0.2489 不显著 净误项 1.20 4 0.30 总离差 453.20 16 注:“***”表示差异极显著P<0.001;“**”表示差异较显著P<0.01;“*”表示差异显著P<0.05;R2=0.9306,R2Adj=0.9846。 采用Design-Expert.V8.0.6统计软件,对表3中的试验数据进行二次多项式回归拟合,最终获得二次项回归方程为:
α-淀粉酶抑制率Y=+55.88+1.26A−0.0.56B+3.48C+0.13AB−1.18AC+0.67BC−1.87A2−2.582−7.96C2。
从表4可以看出,该模型P<0.0001,差异极显著,因变量与所考察的自变量之间线性关系显著R2=0.9306,模型调整确定系数R2Adj=0.9846,说明该模型可信度较高,拟合度较好[29]。失拟项不显著P=0.2489>0.05,说明本实验所得二次回归方程能够很好对响应值进行预测[30-31]。从方差分析结果可以看出各因素对ɑ-淀粉酶抑制率的影响力大小的顺序为:C>A>B,即酶添加量>液料比>超声时间。
2.4 响应面分析及最优条件确定
通过回归方程绘制花生粕多肽酶解工艺条件的响应面分析图,响应面图呈开口向下的凹形曲面,表明ɑ-淀粉酶抑制率存在极大值,由等高线的中心位置可以表明ɑ-淀粉酶抑制率的最优条件存在于设计因素水平的范围之内。响应面交互作用受曲面坡度的影响,曲面陡表明该因素对ɑ-淀粉酶抑制率的影响显著,曲面平缓表明该因素ɑ-淀粉酶抑制率的影响不显著[32];等高线形状反映两因素交互作用的强弱,椭圆形表明两因素交互作用强,圆形则表明两因素交互作用弱;等高线密集表明对ɑ-淀粉酶抑制率的影响较大,稀疏表明对ɑ-淀粉酶抑制率的影响较小,结果如图7所示。
通过Design-Expert 8.0.6软件优化得到花生蛋白制备α-淀粉酶抑制肽的最佳工艺条件:液料比为21.35 mL/g,超声时间为29.25 min,酶添加量为5195.75 U/g,在此试验下,α-淀粉酶抑制率为51.4112%。采用这一结果并根据实际情况,将工艺条件改为:液料比为20:1 mL/g,超声时间为30 min,酶添加量为5000 U/g,得到实验结果为50.62%。与理论值较为接近,说明经过响应面优化得到的超声波辅助酶解花生蛋白制备α-淀粉酶抑制肽工艺参数具有较高可靠性。
2.5 超滤分离纯化花生粕多肽的结果
花生蛋白酶解液经超滤分级分离后得到分子量不同的四个组分,取样品浓度为5 mg/mL分别测定各个多肽组分对ɑ-淀粉酶的抑制率,结果如表5所示。
表 5 超滤后各组分间对α-淀粉酶的抑制率Table 5. Inhibition rates of α -amylase among components after ultrafiltration组分 分子量(kDa) 抑制率(%) 1 >10 13.20±0.03 2 5~10 22.89±0.05 3 3~5 45.77±0.07 4 <3 60.21±0.04 由表5可知,不同分子量组分的ɑ-淀粉酶抑制活性不同。ɑ-淀粉酶抑制活性随着分子量的降低而显著增加。当花生粕多肽分子量<3 kDa时,其对ɑ-淀粉酶抑制率最高。Gu X从榨油后的杏仁残渣中提取的两种降血糖肽,肽A肽B的分子量分别为341.37和291.31[33]。Yuwen Fang从丝胶中提取纯化鉴定出的降血糖肽的分子量为632、689、774 kDa[34]。由此可以看出,超滤后具有较高活性的肽段分子量都比较小,因此选择分子量<3 kDa的组分进一步纯化。
2.6 Sephadex G-15凝胶分离纯化结果
将分子量<3 kDa的多肽组分进行Sephadex G-15凝胶纯化,得到三个组分峰(P1、P2、P3),结果见图8,由图可知,P3为主要组分峰。分别收集各个组分峰,−20 ℃冷冻干燥,测定各组分峰对α-淀粉酶抑制率。结果见图9。
将收集后的3个组分峰多肽,配制成1 mg/mL浓度相同的溶液,分别测其对ɑ-淀粉酶的抑制率。由图9可知,P1、P2、P3三个组分的抑制率分别为63.08%、57.56%、73.30%。P3组分多肽明显高于其他组分。凝胶过滤层析中,大分子物质由于直径较大,不易进入凝胶颗粒的微孔,小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,较大分子化合物后洗脱出来,由此可以推测,三个组分的分子质量大小为P1>P2>P3。
3. 结论
本实验以花生粕为原料提取花生蛋白,经过超声波预处理后酶解花生蛋白获得粗肽,以多肽得率和α-淀粉酶抑制率为指标筛选最适蛋白酶,在单因素实验上,选取液料比、超声时间、酶添加量进行Box-Behnken试验设计,得到最优工艺条件为:液料比为20:1 mL/g,超声时间为30 min,酶添加量为5000 U/g,在此条件下,α-淀粉酶抑制率为50.62%。与未经过超声处理组的α-淀粉酶抑制率35.45%相比,有显著提升,为继续提高多肽的抑制活性,对粗肽进行分离纯化。经超滤分级分离,得到四个不同组分,分别为>10 kDa、5~10 kDa、3~5 kDa、<3 kDa,其中<3 kDa分子量抑制率达到最高60.21%。利用Sephadex G-15凝胶分离纯化<3 kDa组分,得到P1、P2、P3三个组份,其中P3最高抑制率可达到73.30%。由此可见,花生多肽对ɑ-淀粉酶抑制率效果显著,当然如果想要继续提高抑制率,还需对酶解液进一步纯化处理。
-
表 1 不同蛋白酶最适反应条件
Table 1 Optimal reaction conditions for different enzymes
蛋白酶种类 酶解条件 温度(℃) pH 风味蛋白酶 50 7 胰蛋白酶 50 7 碱性蛋白酶 50 10 木瓜蛋白酶 55 7 中性蛋白酶 50 7 表 2 酶解工艺响应面水平与因素设计
Table 2 Response surface level and factor design table of enzymatic hydrolysis process
水平 因素 A液料比(mL/g) B超声时间(min) C酶添加量(U/g) −1 15:1 20 4000 0 20:1 30 5000 1 25:1 40 6000 表 3 响应面试验设计及结果
Table 3 Design and results of response surface experiment
试验号 液料比 超声时间 酶添加量 α-淀粉酶抑制率(%) 1 0 1 1 44.76 2 0 0 0 50.51 3 0 0 0 49.58 4 0 1 −1 39.9 5 1 1 0 41.58 6 1 −1 0 43.76 7 0 −1 −1 41.63 8 0 0 0 51.62 9 −1 0 1 45.52 10 0 0 0 51.07 11 −1 −1 0 40.85 12 1 0 1 47.31 13 1 0 −1 42.55 14 −1 1 0 39.01 15 0 −1 1 46.55 16 −1 0 −1 40.89 17 0 0 0 50.99 表 4 响应面试验回归模型方差分析
Table 4 Variance analysis for the fitted regression equation
方差来源 平方和 自由度 均平方 F值 P值 显著性水平 模型 450.15 9 50.02 114.92 < 0.0001 *** A 12.60 1 12.60 28.95 0.0010 ** B 2.49 1 2.49 5.71 0.0482 * C 97.02 1 97.02 222.92 < 0.0001 *** AB 0.065 1 0.065 0.15 0.7106 AC 5.59 1 5.59 12.85 0.0089 ** BC 1.78 1 1.78 4.09 0.0827 A2 14.78 1 14.78 33.97 0.0006 ** B2 28.00 1 28.00 64.33 < 0.0001 ** C2 267.04 1 267.04 613.55 < 0.0001 *** 残差 3.05 7 0.44 失拟项 1.85 3 0.62 2.05 0.2489 不显著 净误项 1.20 4 0.30 总离差 453.20 16 注:“***”表示差异极显著P<0.001;“**”表示差异较显著P<0.01;“*”表示差异显著P<0.05;R2=0.9306,R2Adj=0.9846。 表 5 超滤后各组分间对α-淀粉酶的抑制率
Table 5 Inhibition rates of α -amylase among components after ultrafiltration
组分 分子量(kDa) 抑制率(%) 1 >10 13.20±0.03 2 5~10 22.89±0.05 3 3~5 45.77±0.07 4 <3 60.21±0.04 -
[1] BOYE J, ZARE F, PLETCH, A. Pulse proteins: Processing, characterization, functional properties and applications in food and feed[J]. Food Research International,2009,43(2):414−431.
[2] WU H, WANG Q, MA T, et al. Comparative studies on the functional properties of various protein concentrate preparations of peanut protein[J]. Food Research International,2009,42(3):343−348. doi: 10.1016/j.foodres.2008.12.006
[3] CIAN R E, MARTÍNEZ-AUGUSTIN O, DRAGO S R. Bioactive properties of peptides obtained by enzymatic hydrolysis from protein byproducts of Porphyra columbina[J]. Food Research International,2012,49(1):364−372. doi: 10.1016/j.foodres.2012.07.003
[4] KARIMI A, AHMADI GAVLIGHI H, AMINI SARTESHNIZI R, et al. Effect of maize germ protein hydrolysate addition on digestion, in vitro antioxidant activity and quality characteristics of bread[J]. Journal of Cereal Science,2021,97:103148. doi: 10.1016/j.jcs.2020.103148
[5] 张洪梅, 王薇, 谢金莲, 等. 花生蛋白肽的生物活性研究进展[J]. 农村科学实验,2017(8):100. [ZHANG Hongmei, WANG Wei, XIE Jinlian, et al. Research progress on bioactivity of peanut protein peptide[J]. Rural Science Experiment,2017(8):100. [6] 许静, 张春红. 花生多肽的制备及其功能性质的研究进展[J]. 农业科技与装备,2010(5):18−19,22. [XU Jing, ZHANG Chunhong. Research progress on preparation and functional properties of peanut polypeptides[J]. Agricultural Science & Technology and equipment,2010(5):18−19,22. doi: 10.3969/j.issn.1674-1161.2010.05.005 [7] 向艳丽, 石思蓉, 覃晓莉, 等. 大豆多肽Lunasin对类风湿关节炎大鼠T细胞免疫指标的影响[J]. 中国应用生理学杂志,2018,34(1):13−15. [XIANG Yanli, SHI Sirong, QIN Xiaoli, et al. Effects of Lunasin on T cell immunity in rats with rheumatoid arthritis[J]. Chinese Journal of Applied Physiology,2018,34(1):13−15. doi: 10.12047/j.cjap.5619.2018.004 [8] LIU Lina, ZHANG Shenghua, HE Dongping. Detection of an angiotensin converting enzyme inhibitory peptide from peanut protein isolate and peanut polypeptides by western blot and dot blot hybridization[J]. European Food Research and Technology,2009,230(1):89−94. doi: 10.1007/s00217-009-1136-7
[9] YE X Y, NG T B. Hypogin, a novel antifungal peptide from peanuts with sequence similarity to peanut allergen.[J]. The Journal of Peptide Research: Official Journal of the American Peptide Society,2001,57(4):300−306.
[10] ZHENG L, REN J, SU G, YANG B, ZHAO M. Comparison of in vitro digestion characteristics and antioxidant activity of hot- and cold-pressed peanut meals[J]. Food Chemistry,2013,141(4):4246−4252. doi: 10.1016/j.foodchem.2013.06.081
[11] ARISE R O, ABEEB Y A, EMMANUEl O E. In vitro antioxidant and α-amylase inhibitory properties of watermelon seed protein hydrolysates[J]. Environmental and Experimental Biology,2016,14(4):1102−1208.
[12] MUDGIL P, KILARI B P, KAMAL H, et al. Multifunctional bioactive peptides derived from quinoa protein hydrolysates: Inhibition of α-glucosidase, dipeptidyl peptidase-IV and angiotensin I converting enzymes[J]. Journal of Cereal Science,2020,96:103130. doi: 10.1016/j.jcs.2020.103130
[13] HUI Xiaodan, WU Gang, HAN Duo, et al. The effects of bioactive compounds from blueberry and blackcurrant powders on the inhibitory activities of oat bran pastes against α-amylase and α-glucosidase linked to type 2 diabetes[J]. Food Research International,2020,138(PA):109756.
[14] ANUSHA D, NEELAM Y, SHALINI P. Potential applications of food derived bioactive peptides in management of health[J]. International Journal of Peptide Research and Therapeutics,2016,22(3):377−398. doi: 10.1007/s10989-016-9514-z
[15] LORDAN S, SMYTH T J, SOLER-VILA A, et al. The α-amylase and α-glucosidase inhibitory effects of Irish seaweed extracts[J]. Food Chemistry,2013,141(3):2170−2176. doi: 10.1016/j.foodchem.2013.04.123
[16] 耿军凤, 张丽芬, 陈复生. 超声波辅助提取对花生蛋白结构与功能特性的影响[J]. 食品研究与开发,2020,41(9):61−69. [GENG Junfeng, ZHANG Lifen, CHEN Fusheng. Effects of ultrasonic assisted extraction on structure and functional characteristics of peanut protein[J]. Food Research and Development,2020,41(9):61−69. doi: 10.12161/j.issn.1005-6521.2020.09.011 [17] 宋玲钰, 刘战伟, 宗爱珍, 等. 降胆固醇活性花生多肽制备工艺的研究[J]. 中国食物与营养,2016,22(12):43−47. [SONG Lingyu, LIU Zhanwei, ZONG Aizhen, et al. Study on preparation of cholesterol-lowering active peanut polypeptides[J]. Food and Nutrition in China,2016,22(12):43−47. doi: 10.3969/j.issn.1006-9577.2016.12.011 [18] 邵元元. 五倍子没食子酸高效制备及其对α-淀粉酶的抑制作用[D]. 长沙: 湖南农业大学, 2014. SHAO Y Y. Preparation of gallnut gallic acid and its inhibition on α-amylase [D]. Changsha: Hunan Agricultural University, 2014.
[19] 叶凯, 李小强, 周金虎, 等. 响应面法酶解藜麦蛋白制备α-淀粉酶抑制肽的工艺研究[J]. 中国调味品,2019,44(12):6−11. [YE Kai, LI Xiaoqiang, ZHOU Jinhu, et al. Preparation of α-amylase inhibitory peptide from quinoa protein by response surface enzymatic hydrolysis[J]. China Condiments,2019,44(12):6−11. doi: 10.3969/j.issn.1000-9973.2019.12.002 [20] 苏可盈. 四种黑茶蛋白的降血糖活性及其机理的研究[D]. 广州: 华南理工大学, 2019. SU K Y. Study on hypoglycemic activity and mechanism of four black tea proteins[D]. Guangzhou: South China University of Technology, 2019.
[21] 让一峰. 白芸豆α-淀粉酶抑制剂的制备及其在低GI方便粥中的应用[D]. 无锡: 江南大学, 2016. RANG Y F. Preparation of α-amylase inhibitor of white kidney bean and its application in convenient porridge with low GI [D]. Wuxi: Jiangnan University, 2016.
[22] 马二兰, 林莹, 涂连, 等. 芋头球蛋白的提取纯化及其α-淀粉酶和α-葡萄糖苷酶抑制活性研究[J/OL]. 食品工业技: 1−13 [2021-03-16]. MA Erlan, LIN Ying, TU Lian, et al. Study on the extraction and purification of taro globulin and its α-amylase and α-glucosidase inhibition activities [J/OL]. Science and Technology of Food Industry : 1−13[2021-03-16].
[23] 徐霞. 藜麦蛋白质及多肽对高脂血症小鼠降脂作用及其降脂产品开发研究[D]. 成都: 成都大学, 2020. XU X. Study on the lipid-lowering effect of quinoa protein and peptide on hyperlipidemia mice and the development of lipid-lowering products [D]. Chengdu: Chengdu University, 2020.
[24] 周浩纯, 李赫, 赵迪, 等. 亚麻籽饼粕蛋白提取工艺优化及其水解物抑制α-淀粉酶活性研究[J]. 食品研究与开发,2020,41(21):61−68. [ZHOU Haochun, LI He, ZHAO Di, et al. Study on the extraction process of flaxseed meal protein and the inhibition of α-amylase activity by hydrolysate[J]. Food Research and Development,2020,41(21):61−68. [25] 江明珠. 超声波预处理辅助酶解制备大豆降糖肽及其作用机理[D]. 镇江: 江苏大学, 2018. JIANG Z M. Preparation of soybean glucose-lowering peptide by ultrasonic pretreatment assisted enzymatic hydrolysis and its mechanism [D]. Zhenjiang: Jiangsu University, 2018.
[26] 陈佳欣. 核桃粕酪氨酸酶抑制肽制备、结构鉴定及其活性研究[D]. 北京: 北京林业大学, 2019. CHEN J X. Preparation, structure identification and activity of tyrosinase inhibitory peptide from walnut meal [D]. Beijing: Beijing Forestry University, 2019.
[27] 李明杰. 南极大磷虾多肽制备工艺优化、脱氟及其体外活性的研究[D]. 青岛: 中国海洋大学, 2012. LI M J. Study on preparation process optimization, defluorination and in vitro activity of polypeptides from Antarctic krill [D]. Qingdao: Ocean University of China, 2012.
[28] 李建杰, 荣瑞芬. 复合酶解制备核桃多肽工艺条件的优化[J]. 中国油脂,2011,36(1):22−26. [LI Jianjie, RONG Ruifen. Optimization of technological conditions for preparation of walnut polypeptide by compound enzymatic hydrolysis[J]. China Oils and Fats,2011,36(1):22−26. [29] 黄孟阳, 李华健, 张明宇, 等. 响应曲面法优化微波干燥草果研究[J]. 中国调味品,2018,43(12):13−17,31. [HUANG Mengyang, LI Huajian, ZHANG Mingyu, et al. Optimization of microwave drying of straw and fruit by response surface methodology[J]. China Condiments,2018,43(12):13−17,31. doi: 10.3969/j.issn.1000-9973.2018.12.003 [30] 毕云枫, 李彤昕, 闫璐, 等. 复合酶法制备人参膳食纤维的研究[J]. 食品研究与开发, 2020, 41(16): 114−119. BI Yunfeng, LI Tongxin, YAN Lu, et al. Food Research and Development, 2020, 41(16): 114−119.
[31] 肖楚洁, 周炎. 响应面法优化香辣藕片生产工艺[J]. 中国调味品,2018,43(12):105−110. [XIAO Chujie, ZHOU Yan. Optimization of the production process of spicy lotus root slices by response surface methodology[J]. China Condiments,2018,43(12):105−110. doi: 10.3969/j.issn.1000-9973.2018.12.020 [32] 赵强, 余四九, 王廷璞, 等. 响应面法优化秃疮花中生物碱提取工艺及抑菌活性研究[J]. 草业学报,2012,21(4):206−214. [ZHAO Qiang, YU Sijiu, WANG Tingpu, et al. Optimization of extraction process and antibacterial activity of alkaloids from flowers of alopecia alopecuroides by response surface methodology[J]. Acta Prataculturae Sinica,2012,21(4):206−214. doi: 10.11686/cyxb20120425 [33] GU X, GAO T, HOU Y, et al. Identification and characterization of two novel α-glucosidase inhibitory peptides from almond (Armeniaca sibirica) oil manufacture residue[J]. LWT,2020,134:110215. doi: 10.1016/j.lwt.2020.110215
[34] FANG Y, WANG S, WU J, et al. The kinetics and mechanism of α-glucosidase inhibition by F5-SP, a novel compound derived from sericin peptides[J]. Food & Function,2016,8(1):323.
-
期刊类型引用(14)
1. 邱月,王旭骅,谢雪华,丁玉庭,吕飞. 低温等离子体杀菌对肉品食用品质的影响规律与机制研究进展. 食品与发酵工业. 2024(06): 332-340 .  百度学术
百度学术
2. 吴家秀,郭雪滢,刘旭,赵玉华. 鲜食甘栗冷等离子体杀菌工艺优化及其品质分析. 食品科技. 2024(03): 25-33 .  百度学术
百度学术
3. 孙嘉莉,王英,敖羽,张文乐,张绍君,包晓玮. 沿面放电等离子体灭活苹果汁中耐高渗酵母的模型. 食品科学. 2024(08): 161-167 .  百度学术
百度学术
4. 杜曼婷,游紫燕,黄俐,李可,栗俊广,白艳红. 介质阻挡放电低温等离子体处理对宰后羊肉色泽和氧化稳定性的影响. 食品科学. 2024(13): 190-197 .  百度学术
百度学术
5. 刘爱民,仝潇洋,张怡,乔勇进. 浅议预制菜产业技术风险分析与对策. 农产品加工. 2024(22): 19-24 .  百度学术
百度学术
6. 徐迪莎,丁怡萱,廖月琴,贾俊琦,董儒仪,苏浩恩,张宾,林慧敏. 低温等离子体对蓝圆鲹在冷藏过程中的品质影响. 食品安全质量检测学报. 2023(13): 266-273 .  百度学术
百度学术
7. 程腾,薛冬,郑凯茜,相启森,白艳红. 冷等离子体处理对生鲜鸡胸肉杀菌效果及品质影响. 包装工程. 2023(13): 84-92 .  百度学术
百度学术
8. 程腾,薛冬,冯坤,吕静,相启森. 大气压冷等离子体在即食肉制品中的应用研究进展. 食品工业科技. 2023(15): 427-433 .  本站查看
本站查看
9. 应可沁,李子言,程序,钱婧,章建浩,严文静. 等离子体活化水作为解冻介质对牛肉杀菌效能及品质的影响. 食品工业科技. 2022(02): 338-345 .  本站查看
本站查看
10. 张关涛,张东杰,李娟,王洪江,金露达,关宇航,徐敏琳. 低温等离子体技术在食品杀菌中应用的研究进展. 食品工业科技. 2022(12): 417-426 .  本站查看
本站查看
11. 郭依萍,李冉,叶可萍,李仲情,陈永芳,张园园. 气调包装协同低温等离子体杀菌对狮子头保鲜效果的影响. 核农学报. 2022(09): 1815-1825 .  百度学术
百度学术
12. 岑南香,刘宸成,陈姑,桑晓涵,符婉丽,刘雅夫,王佳媚. 低温等离子体处理对羊肉脂质与蛋白质氧化性质的影响. 食品工业科技. 2022(14): 85-93 .  本站查看
本站查看
13. 姜竹茂,桑晓涵,潘芸芸,陈增鑫,王佳媚,位正鹏,杨青,王金梅. 低温等离子体对鲅鱼脂质与蛋白质氧化的影响. 食品与发酵工业. 2022(23): 217-224 .  百度学术
百度学术
14. 钱婧,王晨,严文静,章建浩. 天然精油协同等离子体对盐水鸭杀菌保鲜及脂质氧化的调控. 肉类研究. 2022(11): 23-28 .  百度学术
百度学术
其他类型引用(9)





 下载:
下载:









 下载:
下载:



