Research Progress in Subcritical Water Extraction of Bioactive Substances from Plants
-
摘要: 植物源生物活性物质如多酚、多糖等,因具有抗氧化和抗肿瘤等特性在功能性和保健食品中发挥着重要作用。多糖、多酚类物质通过氢键、疏水键等非共价键与蛋白质、脂质等物质在植物组织中紧密结合。如何利用绿色高效的方法从植物组织中提取生物活性成分已成为食品行业的研究热点。亚临界水不仅与有机溶剂溶解生物活性物质的能力接近,能削弱多糖、多酚与其他物质间的紧密结合,而且具有无毒、无污染、无溶剂残留的特点,可广泛用于生物活性物质的提取。本文介绍了亚临界水提取技术的特点和影响因素,其中重点综述了亚临界水提取植物源生物活性物质的效果及机理,以及其与物理技术(如微波、超声、强脉冲光)联用的优势。这为生物活性物质的高效制备提供技术支持,也为亚临界水技术在食品中应用提供理论依据和参考。Abstract: Plant derived bioactive substances such as polyphenols and polysaccharides play an important role in functional and health food because of their antioxidant and anti-tumor properties. Polysaccharides and polyphenols are closely linked with proteins and lipids through non-covalent bonds such as hydrogen bond and water release bond. How to extract bioactive components from plant tissue by green and efficient method has become a hot research topic in food industry. Subcritical water is not only close to the ability of organic solvents to dissolve bioactive substances, but also can weaken the close combination between polysaccharides, polyphenols and other substances. It has the characteristics of non-toxic, pollution-free, solvent-free residue, and can be widely used in the extraction of bioactive substances. In this paper, the characteristics and influencing factors of subcritical water extraction technology are introduced, especially the effect and mechanism of subcritical water extraction of bioactive substances from plants, and the advantages of its combination with physical technology (such as microwave, ultrasound, intense pulsed light). This provides technical support for the efficient preparation of bioactive substances, and also provides theoretical basis and reference for the application of subcritical water technology in food.
-
Keywords:
- subcritical water /
- technical principle /
- bioactive substances /
- yield /
- antioxidant activity
-
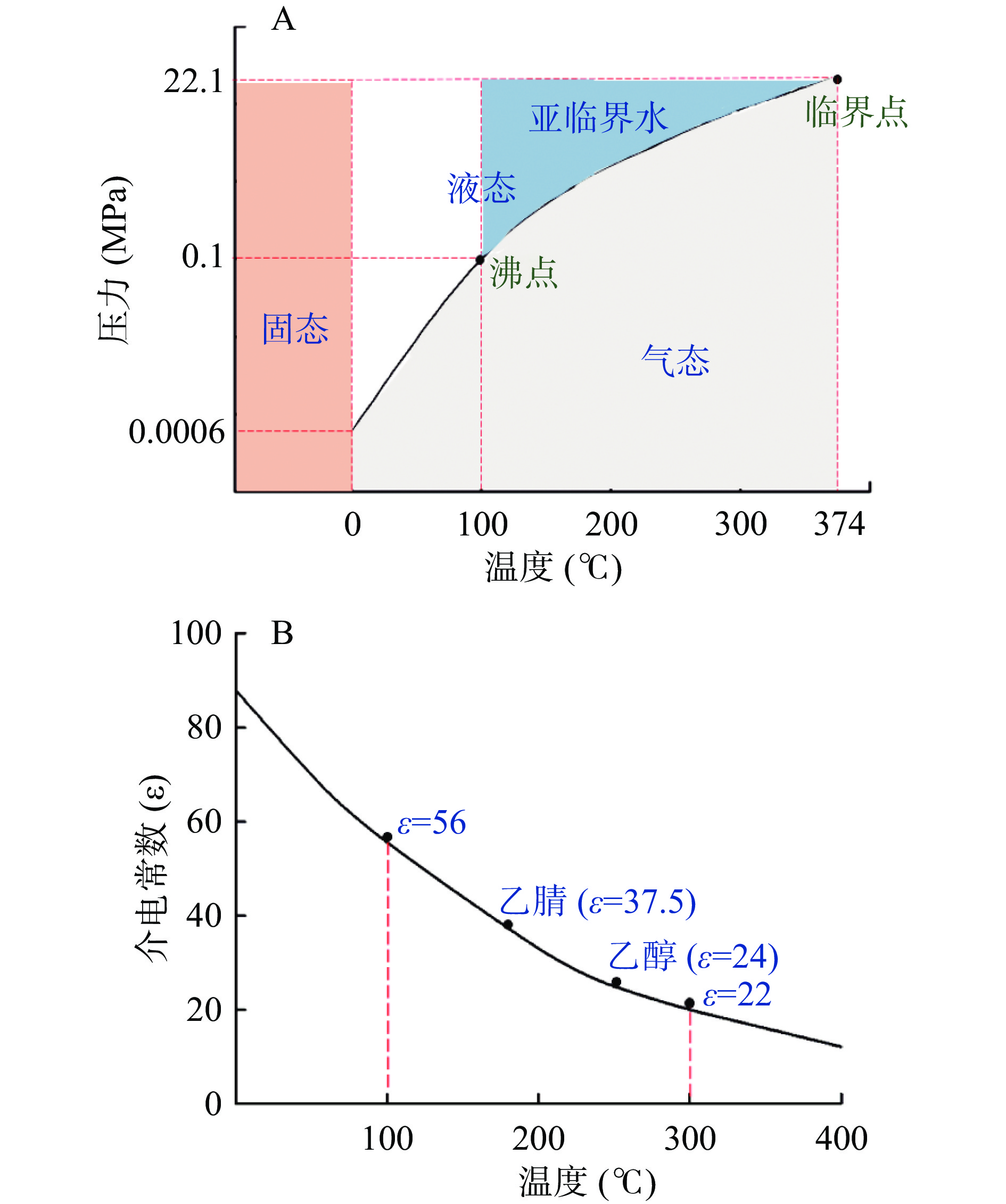
常压下水有固态、液态、气态三种状态,温度超过100 ℃时水为气态,如控制压力为0.1~22.1 MPa,温度为100~374 ℃条件下仍能保持液态的水称为亚临界水(图1A)。亚临界水当温度升高至250 ℃时,介电常数为25,其性质更接近有机溶剂(如乙醇介电常数为24,图1B),即具有较强的溶解多糖、多酚等物质的能力,且其没有有机溶剂残留、污染环境。利用其这个特性,实现生物活性物质的绿色、安全提取。目前,亚临界水提取(Subcritical Water Extraction,SWE)技术广泛用于从植物中提取生物活性物质,如桃棕中酚类化合物[1]、水飞蓟中黄酮类化合物[2]、桑叶中1-脱氧野尻霉素[3]等提取。
植物源活性成分主要包括多糖、多酚等,它们具有许多功能活性,如多糖具有免疫活性[4]、抗氧化活性[5]、免疫调节和镇静活性[6];多酚类物质具有抗肿瘤活性[7],能预防心血管疾病、癌症和神经退行性疾病[8]。这些活性成分在植物体内通过氢键与其他成分紧密结合,植物源生物活性物质的提取方法有很多(表1)。如何高效地从复杂的植物体中提取生物活性物质并保持其原有活性是目前研究的热点内容。本文介绍了亚临界水提取技术的特点、影响因素,重点综述了亚临界水提取植物源生物活性物质的机理和效果,以及与其他技术联用提取生物活性物质,最后展望了亚临界水提取技术的发展前景。
表 1 植物源生物活性物质常见提取方法比较Table 1. Comparison of common extraction methods of bioactive substances from plants1. 亚临界水提取技术
亚临界水提取技术是利用亚临界水的极性打破目标物质与蛋白质、果胶等物质之间的紧密结合,使目标物质进入亚临界水中,从而达到目标物质的提取。
1.1 亚临界水提取技术的特点
传统的提取方法如有机溶剂提取法存在提取时间长、易残留有毒溶剂等问题[11],而亚临界水提取以安全、低廉和环境友好的水作为唯一提取溶剂,并且高温改变了亚临界水的性质,使其极性降低、溶解能力增强,可以高效破坏目标物质与其他物质之间的分子间氢键,具有环保、提取率高和提取速度快的特点[12]。亚临界水可以选择性地提取黄酮类化合物,并且亚临界水提取的产率明显高于甲醇、乙醇或热水提取[13]。此外,亚临界水对分子结构有改性作用,可明显增强物质的生物活性如抗氧化性和抗肿瘤特性[14]。
1.2 亚临界水提取效果的影响因素
亚临界水可以打破目标物质与其他物质之间的氢键[15],打破速度愈快,目标物质提取速率愈高。影响亚临界水提取效果的因素有许多,如温度、液料比和时间等。其中温度是亚临界水提取过程中的重要因素,温度升高,水的极性越低,扩散系数增强,氢键更易断裂,水更快地渗入到植物基质中,增加亚临界水与目标物质之间的接触面积,缩短提取时间,提高提取效率。Kim等[16]发现温度从120 ℃升高到160 ℃,亚临界水从蜜柑果皮中提取得到的橙皮苷和柚皮苷产率分别增加了38.7%和12.9%。在一定范围内,液料比越大,提取速度越快,这是因为液料比提供了植物材料和亚临界水之间的浓度梯度,液料比增加,亚临界水与提取物之间的接触面积增加,浓度梯度差越大,目标物质溶出的速度越快。刁春仁等[17]发现液料比从10:1 g/mL增加到15:1 g/mL,亚临界水提取可溶性膳食纤维的得率增加了10%。时间对亚临界水的提取效果有双重影响,在一定范围内时间与提取效果呈正相关,但提取时间过久会导致得率显著降低。刁春仁等[17]发现亚临界水提取前期膳食纤维的得率随时间延长而增加,16 min后膳食纤维得率开始下降,这可能是由于提取时间过久,膳食纤维不稳定分解所致。
2. 亚临界水提取生物活性物质的机理
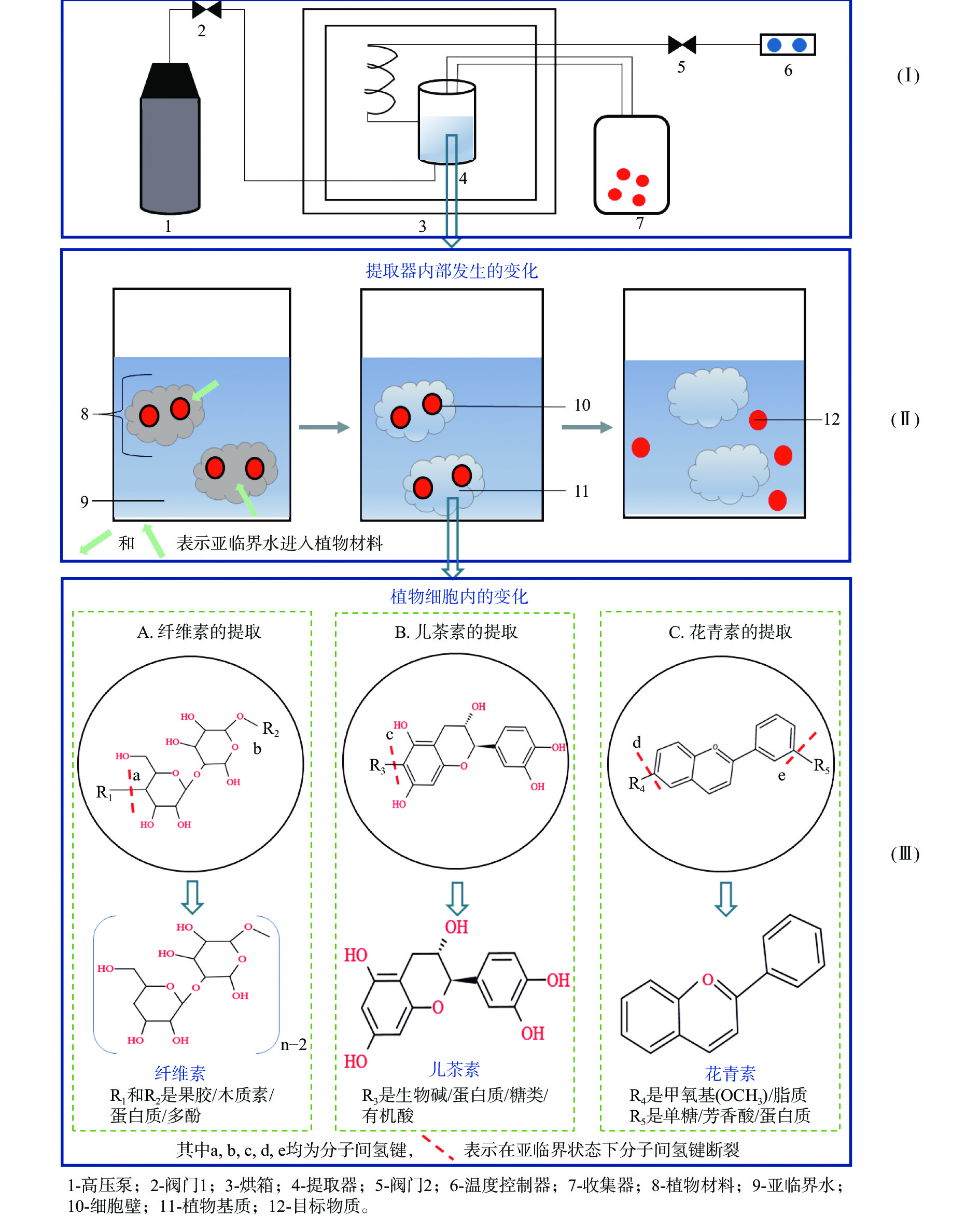
根据亚临界水的形成过程,亚临界水提取与有机溶剂提取原理相似,即相似相溶原理,利用了亚临界水的极性来提取目标物质。如图2(I)所示:高压泵提供的压力和烘箱提供的温度使提取器内的液态水成为亚临界水作为提取剂,实现对目标物质的提取。具体的提取机理如图2(II)所示:植物组织内的蛋白质、果胶、多糖、多酚和其他一些物质通过氢键紧密结合,在高温高压条件下,植物组织的细胞壁破裂,亚临界水逐渐进入植物组织内,目标物质与其他物质之间的氢键被亚临界水破坏甚至断裂[18],扩散速率随着温度增加不断提高,目标物质很快溶解出来,分布在亚临界水中,最后被洗脱出来。
亚临界水提取不同生物活性物质的原理基本相同。提取不同活性物质时,亚临界水破坏目标物质与其他物质之间相连的不同位置的分子间氢键。以常见的多糖、多酚和花青素的提取为例。如图2(III)所示,提取多糖(以提取纤维素为例)时,亚临界水打破的是纤维素与果胶、木质素、蛋白质和多酚[19]之间连接的分子间氢键;提取多酚(以提取儿茶素为例)时,亚临界水打破的是儿茶素与生物碱、蛋白质、糖和有机酸[20]之间的分子间氢键;提取花青素时,亚临界水破坏花青素与甲氧基、单糖、脂质、芳香酸、蛋白质[21]之间的分子间氢键。
利用亚临界水提取其他活性物质时,如提取膳食纤维,亚临界水会破坏膳食纤维与纤维素、果胶[22]等物质之间的分子间氢键,不断促进膳食纤维溶出;提取精油时,亚临界水与植物基质间不断进行分子扩散,亚临界水使植物基质中的脂溶性成分与纤维素、半纤维素[23]等物质相连的分子间氢键断裂,这些成分随后转移到亚临界水中,最后洗脱得到精油;提取植物蛋白时,亚临界水会破坏植物蛋白与脂质[24]等物质间紧密连接的分子间氢键,植物蛋白溶出分布在亚临界水中,随后被洗脱出来。
3. 亚临界水提取生物活性物质的效果
目前,亚临界水提取技术已广泛用于提取植物中的生物活性物质如多糖、多酚等物质,不仅可以缩短提取时间、提高目标物质的得率,还能增加其生物活性,如抗氧化[12]和抗肿瘤[14]等特性。但目前研究较多的是亚临界水提取生物活性物质的得率和抗氧化性。
3.1 亚临界水提取多糖类物质的效果
3.1.1 多糖的得率
与热水提取法相比,亚临界水提取技术可明显提高生物活性物质的得率。陈梦[25]用HWE法和SWE法提取慈姑多糖,结果发现SWE法得率明显高于HWE法(见表2)。邓辰辰等[26]比较了SWE法和HWE法提取灵芝多糖的得率,结果发现前者比后者高0.48%。徐曼旭等[27]在最佳亚临界水提取条件下得到的薏米多糖提取率为3.66%,明显高于水浸提法(1.64%)和超声辅助提取法(2.06%)。
目前除了与其他方法进行对比之外,优化亚临界水提取工艺也受到了愈来愈多人的关注。赵斌等[28]用单因素实验和响应面法优化得到最佳的亚临界水提取条件:pH=6,液料比20:1 mL/g,温度150 ℃,时间10 min,结果发现SWE法得率比HWE法高3.97%。顾艳耿等[29]通过响应面法优化得到粗茶多糖的最佳提取条件:液料比30:1 mL/g、温度150 ℃、提取时间12 min,在该条件下粗茶多糖得率约为传统热水浸提得率的2倍。
果胶是一类杂多糖,具有胶凝、增稠、稳定的性质[30]。一般是在加热条件下用酸提取果胶[31],但这种方法耗时且提取率低。Muñoz-Almagro等[32]发现SWE法与柠檬酸提取法相比,可可豆壳中的果胶得率提高了2.6%。
3.1.2 多糖的抗氧化性
与传统提取方法相比,亚临界水提取的多糖对DPPH·(1,1-diphenyl-2-picrylhydrazyl)和·OH的清除能力以及FRAP铁离子(Ferric ion reducing antioxidant power)的还原能力明显提高。陈梦[25]利用SWE法得到的慈姑多糖(Sagittariasagittifolia polysaccharides,SSP)对DPPH·的清除率是HWE-SSP对DPPH·清除率的1.29倍。杨文雅等[33]用SWE法得到的蛹虫草多糖对DPPH·的清除率比HWE法高0.79%。Essien等[34]发现与乙醇提取法相比,亚临界水提取的番石榴叶多糖对DPPH·的清除能力和FRAP铁离子的还原能力分别约提高2倍和1.2倍。
3.2 亚临界水提取多酚类物质的效果
3.2.1 亚临界水提取多酚类物质的得率
植物多酚类物质含有多个酚羟基,具有很强的抗氧化和清除自由基能力,从天然植物中寻找抗氧化剂是目前的研究热点,因此有许多学者寻求高效提取多酚类物质的方法。目前发现亚临界水提取技术较热水提取、有机溶剂提取、索氏抽提法明显提高植物多酚的得率(见表3)。颜征[35]发现SWE法提取的莲房多酚较HWE法得率高22%。Rodrigues等[36]发现与SOX法相比,150 ℃时SWE法得到的木瓜种子残渣中总酚得率提高了2倍以上。闫林林等[37]研究表明,优化后的SWE法提取的石榴叶总酚得率较HWE法和有机溶剂提取分别提高46.3%和14.6%。戚聿研[38]发现与有机溶剂和热水提取法相比,亚临界水提取芝麻粕酚类化合物的含量分别增加了约6.9倍和7.3倍。Lachos-Perez等[39]利用亚临界水从脱脂橙皮中提取黄烷酮的得率较索氏抽提法和超声辅助提取法分别提高了7.72%和7.48%。
表 3 亚临界水提取与其他提取方法总酚得率的比较Table 3. Comparison of total phenol yield between subcritical water extraction and other extraction methods3.2.2 亚临界水提取多酚类物质的抗氧化性
与其他提取方法相比,亚临界水提取的多酚物质表现出更高的抗氧化性。戚聿研[38]发现与热水提取和80%乙醇提取相比,亚临界水提取得到的芝麻粕多酚的DPPH·清除能力分别提高了25倍和13倍以上,这是因为亚临界水提取出来的酚类化合物含量更高。Rodrigues等[40]发现亚临界水提取的驱虫苋多酚类物质与索氏抽提法相比,其FRAP铁离子还原能力提高了11.6%。刘轩墀[41]研究表明,亚临界水提取的板栗壳多酚的DPPH·和ABTS·+清除能力以及FRAP铁离子还原能力较有机溶剂提取物分别提高了2倍、3倍和8倍以上。Guthrie等[42]发现与乙醇提取法相比,亚临界水提取得到的猕猴桃皮多酚的DPPH·和ABTS+·清除能力分别提高了14.2%和21.0%。
3.3 亚临界水提取其他生物活性物质的效果
亚临界水提取技术除了可以提高多酚、多糖类物质的得率,还能提高膳食纤维、精油和植物蛋白等生物活性物质的得率。
3.3.1 膳食纤维
膳食纤维被称为“第七营养素”,对人体健康有很多益处如辅助降血脂[43]、促进肠道功能[44]。利用亚临界水提取技术较传统方法可明显提高膳食纤维的得率。刁春仁等[17]发现与HWE法相比,SWE法提取藕渣中的可溶性膳食纤维得率提高了16.8%。孟祥河等[45]研究表明,亚临界水提取膳食纤维的得率与热水提取、超声辅助提取和微波辅助提取法相比,分别提高了9.23%、2.22%和2.69%。
3.3.2 精油
精油是一种具有强烈挥发性化合物的复杂混合物,是许多植物的次生代谢产物,亦称为挥发油[46],是一种可以替代化学抗菌剂的天然抗菌剂[47]。Samadi等[23]利用亚临界水提取得到的麦芽糖叶精油的得率和生物活性高于水蒸馏法;而且提取效率较传统方法提高了2.5倍,时间缩短了8.4倍。Mottahedin等[48]研究表明,利用亚临界水从姜黄根中提取得到的精油得率比加氢蒸馏法高0.54%。
3.3.3 植物蛋白
植物蛋白是人类膳食蛋白质的重要来源[23],常规的植物蛋白提取方法耗时且提取率低,利用亚临界水提取植物蛋白可提高其提取率。Fan等[49]发现,与传统的超声波+冻融法相比,超声+亚临界水提取螺旋藻多肽的得率提高了28.2%。
4. 亚临界水与其他技术联用提取生物活性物质
在提取蛋白、多糖等生物活性物质时,单独使用亚临界水提取技术尚且不能满足更高提取效果的要求,需要与其他技术手段如微波、超声和强脉冲光联用,各自发挥优势,协同提取活性物质。
4.1 微波
微波提取是将微波加热与溶剂萃取相结合的提取技术,它利用电磁场的作用使植物材料中的目标成分与基质有效分离。微波与亚临界水提取技术结合提取物质时,植物基质中的偶极分子在高频微波能的作用下不断旋转导致氢键断裂[50],从而加速亚临界水对植物基质的渗透,促进目标物质的提取。Flórez等[51]利用微波辅助亚临界水提取绿茶中的黄烷醇,研究发现黄烷醇的提取率比传统的热水提取法高8.31%。杜易平等[52]发现与传统的加热回流提取法相比,微波辅助亚临界水提取法得到的杨黄多糖得率提高了11.04%。
4.2 超声
超声提取利用超声波的机械效应和空化效应增大对细胞壁的破坏[53],能够加快亚临界水提取生物活性成分的速率。Yang等[54]比较了热水提取、超声提取、亚临界水提取以及超声强化亚临界水提取枸杞多糖的得率,结果发现超声强化亚临界水提取法分别比其他方法高6.49%、4.53%和3.45%。赵超[55]发现超声强化亚临界水提取法的得率分别比亚临界水提取法、超声提取法和热水提取法高0.58%、1.39%和1.75%。Ma等[56]研究发现,与亚临界水提取法和水蒸气蒸馏萃取法相比,超声辅助亚临界水提取的山奈花有效成分得率分别提高1.63%和10.1%。
4.3 强脉冲光
强脉冲光是一种高强度光源经过聚焦和滤光后形成的一种宽谱光[57]。强脉冲光处理可以破坏植物细胞基质,亚临界水能够促进目标物质从植物基质内释放出来,两者结合可提高目标物质的含量。Kim等[58]发现,与单独使用亚临界水提取法相比,强脉冲光和亚临界水结合提取得到的槲皮素得率增加14.0%。Hwang等[59]利用强脉冲光和亚临界水提取技术从柑橘果皮中提取橙皮苷和柚皮苷,研究发现强脉冲光处理使橙皮苷和柚皮苷的提取量分别提高了22.1%和33.6%。
5. 结论与展望
亚临界水的无毒、无溶剂残留且高效环保的特性,除用于生物活性物质的提取外,在环境污染物的监测和食品营养成分的分析等领域也广泛使用。该技术属于绿色高效的新型技术手段,能够实现对生物资源的综合利用,具有广阔的应用前景。为了更好地利用亚临界水提取技术,未来可深入研究以下几个方面:
a.亚临界水已广泛用于提取生物活性物质,并提高其得率;但在提取过程中温度过高会使某些热敏化合物降解产生一些副产物,如何控制温度提高目标物质的纯度还需进一步研究;b.亚临界水提取技术能提高生物活性物质的抗氧化和抗肿瘤等特性,但目前关于活性物质的抗氧化性研究较多,对其分子结构和其他活性的影响研究较少,还需深入研究;c.亚临界水提取技术提高生物活性物质的得率和抗氧化性的机制尚不清楚,可进行深入研究;d.亚临界水提取生物活性物质目前还处于实验室的小规模提取和后续研究中,大规模提取设备的开发还处于起步阶段,如何将其扩大到工业化提取规模、缩小提取成本还需进一步研究。
-
表 1 植物源生物活性物质常见提取方法比较
Table 1 Comparison of common extraction methods of bioactive substances from plants
表 2 亚临界水提取与热水提取多糖得率的比较
Table 2 Comparison of the yield of polysaccharides extracted by subcritical water and hot water
表 3 亚临界水提取与其他提取方法总酚得率的比较
Table 3 Comparison of total phenol yield between subcritical water extraction and other extraction methods
-
[1] GIOMBELLI C, IWASSA I J, SILVA C D, et al. Valorization of peach palm by-product through subcritical water extraction of soluble sugars and phenolic compounds[J]. The Journal of Supercritical Fluids,2020,165:1−8.
[2] 隋博. 水飞蓟籽的亚临界萃取工艺及籽粕品质研究[D]. 郑州: 郑州大学, 2018. SUI B. Study on Silybum marianum extraction by subcritical extraction technology and the quality of seed meal[D]. Zhengzhou: Zhengzhou University, 2018.
[3] 马芸芸. 亚临界水提取桑叶1-脱氧野尻霉素及纯化研究[D]. 北京: 北京林业大学, 2018. MA Y Y. Subcritical water extraction of 1-deoxynojirimycin in mulberry leaves and purification[D]. Beijing: Beijing Forestry University, 2018.
[4] 黄青, 李丽媛, 刘晴晴, 等. 灵芝多糖和猪苓多糖及其复方的免疫调节作用研究进展[J]. 食品科学,2020,41(17):275−282. [HUANG Q, LI L Y, LIU Q Q, et al. Advances in immunoregulation effects of Ganoderma lucidum polysaccharide and/or Polyporus umbellatus polysaccharide[J]. Food Science,2020,41(17):275−282. doi: 10.7506/spkx1002-6630-20190813-149 [5] 王家腾, 王贺聪, 刘蕾. 香菇多糖构效关系的研究进展[J]. 食品科学,2019,40(19):363−369. [WANG J T, WANG H C, LIU L. Progress in research on structure-function relationship of lentinan[J]. Food Science,2019,40(19):363−369. doi: 10.7506/spkx1002-6630-20181016-162 [6] JIAO Y K, HUA D H, HUANG D, et al. Characterization of a new heteropolysaccharide from green guava and its application as an α-glucosidase inhibitor for the treatment of type II diabetes[J]. Food & Function,2018,9(7):3997−4000.
[7] 石芳, 廖霞, 李瑶, 等. 植物多酚通过PI3K/Akt信号通路抗肿瘤作用研究进展[J]. 食品科学,2016,37(15):259−264. [SHI F, LIAO X, LI Y, et al. Plant polyphenols exert anti-tumor activity by the PI3K/Akt signaling pathway: A review[J]. Food Science,2016,37(15):259−264. doi: 10.7506/spkx1002-6630-201615044 [8] YANG C Y, HA W, LIN Y, et al. Polyphenols isolated from Xanthoceras sorbifolia Husks and their anti-tumor and radical-scavenging activities[J]. Molecules,2016,21(12):1−11.
[9] HIRONDART M, ROMBAUT N, FABIANO-TIXIER A S, et al. Comparison between pressurized liquid extraction and conventional soxhlet extraction for rosemary antioxidants, yield, composition, and environmental footprint[J]. Foods,2020,9(5):1−13.
[10] CHI Y Z, LI Y, ZHANG G, et al. Effect of extraction techniques on properties of polysaccharides from Enteromorpha prolifera and their applicability in iron chelation[J]. Carbohydrate Polymers,2018,181:616−623. doi: 10.1016/j.carbpol.2017.11.104
[11] 刘婷婷, 秦宇婷, 吴玉莹, 等. 溶剂法提取分蘖葱头有机硫化合物及其GC-MS分析[J]. 食品科学,2017,38(12):151−156. [LIU T T, QIN Y T, WU Y Y, et al. Solvent extraction and GC-MS analysis of organic sulfur-containing compounds from tillering onion[J]. Food Science,2017,38(12):151−156. doi: 10.7506/spkx1002-6630-201712023 [12] KO M J, NAM H H, CHUNG M S. Subcritical water extraction of bioactive compounds from Orostachys japonicus A. Berger (Crassulaceae)[J]. Scientific Reports,2020,10(1):10890. doi: 10.1038/s41598-020-67508-2
[13] KO M J, CHEIGH C I, CHO S W, et al. Subcritical water extraction of flavonol quercetin from onion skin[J]. Journal of Food Engineering,2011,102(4):327−333. doi: 10.1016/j.jfoodeng.2010.09.008
[14] 陈剑兵, 李英迪, 谭兴和, 等. 亚临界水改性果胶的抗氧化和抗肿瘤活性研究[J]. 食品科技,2020,45(6):316−321. [CHEN J B, LI Y D, TAN X H, et al. Antioxidant and antitumor activity of pectin modified by subcritical water[J]. Food Science and Technology,2020,45(6):316−321. [15] BENITO-ROMÁN Ó, BLANCO B, SANZ M T, et al. Subcritical water extraction of phenolic compounds from onion skin wastes (Allium cepa cv. Horcal): Effect of temperature and solvent properties[J]. Antioxidants (Basel, Switzerland),2020,9(12):1233.
[16] KIM D S, LIM S B. Kinetic study of subcritical water extraction of flavonoids from Citrus unshiu peel[J]. Separation and Purification Technology,2020,250:117259. doi: 10.1016/j.seppur.2020.117259
[17] 刁春仁, 张海晖, 李亚群, 等. 藕渣中可溶性膳食纤维的亚临界水萃取[J]. 食品工业,2018,39(8):35−39. [DIAO C R, ZHANG H H, LI Y Q, et al. Extraction of soluble dietary fiber from lotus root dregs by subcritical water[J]. The Food Industry,2018,39(8):35−39. [18] ZHAO L L, FAN H Z, ZHANG M, et al. Edible flowers: Review of flower processing and extraction of bioactive compounds by novel technologies[J]. Food Research International,2019,126:1−39.
[19] 杨伟, 李波, 徐响, 等. 蛋白质-多酚-多糖三元复合物的结构和功能特性研究进展[J]. 食品工业科技,2017,38(17):329−334. [YANG W, LI B, XU X, et al. Advances in research on the structural and functional characteristics of noncovalent interactions of protein, polyphenol and polysaccharide[J]. Science and Technology of Food Industry,2017,38(17):329−334. [20] 陆昌琪, 毛世红, 童华荣, 等. 儿茶素及其衍生物合成研究进展[J]. 食品科学, 2018, 39(11): 316-326. LU C Q, MAO S H, TONG H R, et al. Progress in the synthesis of catechins and its derivatives[J]. Food Science, 2018, 39(11): 316-326.
[21] 王晨, 谢岩黎, 范亭亭. 花青素与小麦蛋白相互作用及对蛋白质结构的影响[J]. 食品科学,2019,40(20):60−66. [WANG C, XIE Y L, FAN T T. Interactions of cyanidin-3-O-glucoside with gliadin and glutenin and their effects on protein structure[J]. Food Science,2019,40(20):60−66. doi: 10.7506/spkx1002-6630-20180725-308 [22] 张百胜, 陈海霞, 张娟梅. 亚临界水法提取麸皮可溶性膳食纤维工艺优化[J]. 食品研究与开发,2014,35(14):50−53. [ZHANG B S, CHEN H X, ZHANG J M. Optimization of subcritical water extraction process of soluble dietary fiber from wheat bran[J]. Food Research and Development,2014,35(14):50−53. doi: 10.3969/j.issn.1005-6521.2014.14.015 [23] SAMADI M, ABIDIN Z Z, YUNUS R, et al. Subcritical water extraction of essential oil from Aquilaria malaccensis leaves[J]. Separation Science & Technology,2020,55(15):2779−2798.
[24] 陈辉. 现代营养学(高等学校教材)[M]. 北京: 化学工业出版社, 2005. CHEN H. Modern Nutrition (Textbooks for Colleges and Universities)[M]. Beijing: Chemical Industry Press, 2005.
[25] 陈梦. 慈姑多糖的亚临界水萃取、结构表征及其免疫活性研究[D]. 镇江: 江苏大学, 2018. CHEN M. Studies on subcritical water extraction, characterization and immune activities of polysaccharides from Sagittaria sagittifolia[D]. Zhenjiang: Jiangsu University, 2018.
[26] 邓辰辰, 相继芬, 董兴叶, 等. 亚临界水提取灵芝多糖的工艺研究[J]. 河南工业大学学报(自然科学版),2016,37(2):105−108. [DENG C C, XIANG J F, DONG X Y, et al. Subcritical water extraction technology of polysaccharide from Ganoderma lucidum[J]. Journal of Henan University of Technology (Natural Science),2016,37(2):105−108. [27] 徐曼旭, 于国萍, 付饶, 等. 薏米多糖亚临界水萃取工艺的优化[J]. 食品工业,2014,35(1):94−97. [XU M X, YU G P, FU R, et al. Optimization of extracting technology foe polysaccharide of coix seed by subcritical water[J]. The Food Industry,2014,35(1):94−97. [28] 赵彬, 张海晖, 张继贤, 等. 小麦胚芽多糖的亚临界水萃取的工艺研究[J]. 食品工业,2017,38(7):45−49. [ZHAO B, ZHANG H H, ZHANG J X, et al. Study on the optimization for the extraction of polysaccharide from wheat germ by subcritical water[J]. The Food Industry,2017,38(7):45−49. [29] 顾艳耿, 胡仲秋, 邱月, 等. 亚临界水法提取茶多糖及抗氧化活性研究[J]. 食品科技,2019,44(6):194−201. [GU Y G, HU Z Q, QIU Y, et al. Extraction and antioxidant activity of tea polysaccharide by subcritical water from tea[J]. Food Science and Technology,2019,44(6):194−201. [30] VERKEMPINK S H E, KYOMUGASHOA C, SALVIA L, et al. Emulsion stabilizing properties of citrus pectin and its interactions with conventional emulsifiers in oil-in-water emulsions[J]. Food Hydrocolloids,2018,85:144−157. doi: 10.1016/j.foodhyd.2018.07.014
[31] PEREIRA P H F, OLIVEIRA T, ROSA M F, et al. Pectin extraction from pomegranate peels with citric acid[J]. International Journal of Biological Macromolecules,2016,88:373−379. doi: 10.1016/j.ijbiomac.2016.03.074
[32] MUÑOZ-ALMAGRO N, VALADEZ-CARMONA L, MENDIOLA J A, et al. Structural characterization of pectin obtained from cacao pod husk. Comparison of conventional and subcritical water extraction[J]. Carbohydrate Polymers,2019,217:69−78. doi: 10.1016/j.carbpol.2019.04.040
[33] 杨文雅, 李长征, 张海晖, 等. 蛹虫草多糖的亚临界水萃取及其抗氧化活性研究[J]. 食品工业科技,2016,37(5):252−257. [YANG W Y, LI C Z, ZHANG H H, et al. Study on the optimization for the extraction and antioxidant activity of polysaccharide from Cordyceps militaris by subcritical water[J]. Science and Technology of Food Industry,2016,37(5):252−257. [34] ESSIEN S, YOUNG B, BAROUTIAN S. Subcritical water extraction for selective recovery of phenolic bioactives from kānuka leaves[J]. The Journal of Supercritical Fluids,2020,158:1−5.
[35] 颜征. 莲房多酚的亚临界水萃取、组成及活性评价[D]. 镇江: 江苏大学, 2020. YAN Z. Subcritical water extraction, composition and activity evaluation of lotus polyphenols[D]. Zhenjiang: Jiangsu University, 2020.
[36] RODRIGUES L G G, MAZZUTTI S, VITALI L, et al. Recovery of bioactive phenolic compounds from papaya seeds agroindustrial residue using subcritical water extraction[J]. Biocatalysis and Agricultural Biotechnology,2019,22:1−8.
[37] 闫林林, 郑光耀, 韦朝宽. 响应面法优化石榴叶总酚的亚临界水提取工艺[J]. 食品工业科技,2017,38(19):184−190. [YAN L L, ZHENG G Y, WEI C K. Optimization of subcritical water extraction for total phenolics from pomegranate (Punica granatum L.) leaves by response surface methodology[J]. Science and Technology of Food Industry,2017,38(19):184−190. [38] 戚聿妍. 亚临界水提取芝麻粕中酚类化合物及水解芝麻蛋白的研究[D]. 哈尔滨: 哈尔滨工业大学, 2016. QI Y Y. Studies on the extraction of phenolic compounds from sesame seed meal and the hydrolysis of sesame protein by subcritical water[D]. Harbin: Harbin Institute of Technology, 2016.
[39] LACHOS-PEREZ D, BASEGGIO A M, MAYANGA-TORRES P C, et al. Subcritical water extraction of flavanones from defatted orange peel[J]. Journal of Supercritical Fluids,2018,138:7−16. doi: 10.1016/j.supflu.2018.03.015
[40] RODRIGUES L G G, MAZZUTTI S, SIDDIQUE I, et al. Subcritical water extraction and microwave-assisted extraction applied for the recovery of bioactive components from chaya (Cnidoscolus aconitifolius Mill. )[J]. The Journal of Supercritical Fluids,2020:104976.
[41] 刘轩墀. 板栗壳亚临界水提取物的多酚组成与抗氧化及消化酶抑制活性研究[D]. 北京: 北京林业大学, 2019. LIU X C. Study on polyphenols composition and antioxidant and digestive enzyme inhibitory activities of subcritical water extracts from chestnut shell[D]. Beijing: Beijing Forestry University, 2019.
[42] GUTHRIE F, WANG Y, NEEVE N, et al. Recovery of phenolic antioxidants from green kiwifruit peel using subcritical water extraction[J]. Food and Bioproducts Processing,2020,122:136−144. doi: 10.1016/j.fbp.2020.05.002
[43] PARK J H, UPADHAYA S D, KIM I H. Effect of dietary marine microalgae (Schizochytrium) powder on egg production, blood lipid profiles, egg quality, and fatty acid composition of egg yolk in layers[J]. Asian Australasian Journal of Animal Sciences,2015,28(3):391−397. doi: 10.5713/ajas.14.0463
[44] LIU H F, ZENG X Y, HUANG J Y, et al. Dietary fiber extracted from pomelo fruitlets promotes intestinal functions, both in vitro and in vivo[J]. Carbohydrate Polymers,2021,252:117186. doi: 10.1016/j.carbpol.2020.117186
[45] 孟祥河, 戴建波, 曹艳, 等. 亚临界水提取甘薯皮可溶性膳食纤维及其特性研究[J]. 农业工程学报,2019,35(21):303−308. [MENG X H, DAI J B, CAO Y, et al. Extraction of soluble dietary fiber from sweet potato peel by subcritical water and its characteristics[J]. Transactions of the Chinese Society of Agricultural Engineering,2019,35(21):303−308. [46] PATRIGNANI F, SIROLI L, SERRAZANETTI D I, et al. Innovative strategies based on the use of essential oil and their components to improve safety, shelf-life and quality of minimally processed fruits and vegetables[J]. Trends in Food Science and Technology,2015,46:311−319. doi: 10.1016/j.jpgs.2015.03.009
[47] SADEKUZZAMAN M, MIZAN M F R, KIM H S, et al. Activity of thyme and tea tree essential oils against selected foodborne pathogens in biofilms on abiotic surfaces[J]. LWT-Food Science and Technology,2018,89:134−139. doi: 10.1016/j.lwt.2017.10.042
[48] MOTTAHEDIN P, ASL A H, KHAJENOORI M. Extraction of curcumin and essential oil from Curcuma longa L. by subcritical water via response surface methodology[J]. Journal of Food Processing and Preservation,2017,41(4):1−9.
[49] FAN X D, HU S F, WANG K, et al. Coupling of ultrasound and subcritical water for peptides production from Spirulina platensis[J]. Food and Bioproducts Processing,2020,121:105−112. doi: 10.1016/j.fbp.2020.01.012
[50] 解梦梅. 微波提取柑橘皮中柠檬烯和果胶的试验研究[D]. 济南: 山东大学, 2020. XIE M M. Experimental study on microwave extraction of limonene and pectin from citrus peel[D]. Jinan: Shandong University, 2020.
[51] FLÓREZ, NOELIA, CONDE E, et al. Microwave assisted water extraction of plant compounds[J]. Journal of Chemical Technology & Biotechnology,2015,90(4):590−607.
[52] 杜易平, 张亚婕, 李艳, 等. 微波辅助亚临界水提取杨黄多糖[J]. 实用药物与临床,2017,20(12):1407−1409. [DU Y P, ZHANG Y J, LI Y, et al. Extraction of polysaccharide from Inonotus vaninii with microwave-subcritical water method[J]. Practical Pharmacy and Clinical Remedies,2017,20(12):1407−1409. [53] 王鹏旭, 成传香, 马亚琴, 等. 超声声学效应在果蔬酚类化合物提取中的研究进展[J]. 食品科学,2019,40(17):338−347. [WANG P X, CHENG C X, MA Y Q, et al. Research progress of ultrasonic acoustic effect in extraction of phenolic compounds from fruits and vegetables[J]. Food Science,2019,40(17):338−347. doi: 10.7506/spkx1002-6630-20180718-228 [54] YANG R F, ZHAO C, CHEN X, et al. Chemical properties and bioactivities of Goji (Lycium barbarum) polysaccharides extracted by different methods[J]. Journal of Functional Foods,2015,17:903−909.
[55] 赵超. 超声强化亚临界水提取枸杞多糖的研究[D]. 广州: 华南理工大学, 2014. ZHAO C. Ultrasound enhanced extraction of Lycium barbarum polysaccharide by subcritical water[D]. Guangzhou: South China University of Technology, 2014.
[56] MA Q, FAN X D, LIU X C, et al. Ultrasound-enhanced subcritical water extraction of essential oils from Kaempferia galangal L. and their comparative antioxidant activities[J]. Separation and Purification Technology,2015,150:73−79. doi: 10.1016/j.seppur.2015.06.013
[57] CHEN D J, WIERTZEMA J R, PENG P, et al. Catalytic intense pulse light inactivation of Cronobacter sakazakii and other pathogens in non-fat dry milk and wheat flour[J]. Food Chemistry,2020:332.
[58] KIM S W, KO M J, CHUNG M S. Extraction of the flavonol quercetin from onion waste by combined treatment with intense pulsed light and subcritical water extraction[J]. Journal of Cleaner Production,2019,231:1192−1199. doi: 10.1016/j.jclepro.2019.05.280
[59] HWANG H J, KIM H J, KO M J, et al. Recovery of hesperidin and narirutin from waste Citrus unshiu peel using subcritical water extraction aided by pulsed electric field treatment[J]. Food Science and Biotechnology,2021,30:217−226. doi: 10.1007/s10068-020-00862-z
-
期刊类型引用(3)
1. 李亚俐,王雪莉,石柳,吴文锦,陈胜,陈朗,郭晓嘉,熊光权,汪兰,孙智达. 壳聚糖-绿原酸复合保鲜剂对冷藏鮰鱼片食用品质的影响. 肉类研究. 2025(01): 42-50 .  百度学术
百度学术
2. 武玫怡,焦文娟,赵甜甜,刘俊,周芳,刘伟峰,张业辉,南海军,陈晓瑛,黄利华. 高静水压与水煮处理对热带海参品质的影响. 肉类研究. 2025(01): 25-33 .  百度学术
百度学术
3. 崔燕,刘韩欣,朱麟,尚海涛,林旭东,陈曙颖,宣晓婷. 超高压杀菌对大黄鱼理化性质及滋味、风味的影响. 食品工业科技. 2025(05): 44-55 .  本站查看
本站查看
其他类型引用(3)





 下载:
下载:
 下载:
下载:



