Separation and Preparation of Sanguinarine and Chelerythrine from Macleaya cordata Root by High Speed Counter-Current Chromatography
-
摘要: 本文旨在建立一种使用常规高速逆流色谱技术分离制备高纯度博落回血根碱和白屈菜红碱的方法。通过分析型高速逆流色谱对六种溶剂体系进行快速筛选,确定以三氯甲烷-甲醇-0.2 mol/L 盐酸水溶液(4:2:2,V/V/V)为两相溶剂体系并放大到制备型高速逆流色谱上,以上相为固定相,下相为流动相,流速8 mL/min,转速为455 r/min,进样量1000 mg,温度为25 ℃条件下分离制备博落回血根碱和白屈菜红碱。实验结果表明:此方法一次性能够从1000 mg博落回生物碱粗品分离得到博落回血根碱盐酸盐505 mg和白屈菜红碱盐酸盐435 mg。经超高效液相色谱(UPLC)检测,按照外标法计算,两者纯度分别为99.77%、99.73%。采用标准品对照法、1H NMR和13C NMR对目标产物进行了结构鉴定。分离所得产物的结构数据与文献一致。该方法具有后处理简单、成本低廉、分离产物纯度高、实用性强等特点,适用于血根碱和白屈菜红碱的大量制备。Abstract: The aim of this study was to develop a method for the separation and preparation of high purity sanguinarine and chelerythrine by conventional high speed counter-current chromatography. After comparing six kinds of solvent protocols of analytical high speed counter-current chromatography (HSCCC), the two phase system of chloroform-methanol-0.2 mol/L hydrochloric acid aqueous solution (4:2:2,V/V/V) was finally chosen as the operating solvent of preparative high speed counter-current chromatography (HSCCC), in which the upper phase was used as the stationary phase and the lower phase was used as the mobile phase. Under the conditions of ratations speed of 455 r/min, lower phase flow rate of 8 mL/min, the injection volume of 1000 mg, the temperature of 25 ℃, sanguinarine and chelerythrine was separated and preparated on HSCCC. The results showed that 505 mg of sanguinarine chloride and 435 mg of chelerythrine chloride could be obtained from 1000 mg of crude Macleaya cordata alkaloid at one time by this method. According to the calculation of external standard method, the purity of them were 99.77% and 99.73% respectively determined by UPLC. The structure of the two target product was identified by comparison with standards, 1H NMR and 13C NMR. The structure data of the separated products were in agreement with the literature. The method is suitable for the mass preparation of sanguinarine and chelerythrine, because it has many advantages such as simple post-treatment, low cost, high purity of separation products and strong practicability.
-
博落回(Macleaya cordata (Willd.) R. Br.),属罂粟科博落回属植物,可以全株入药,有祛风、散瘀消肿、镇痛解毒、杀虫等功效[1]。目前,据国内外有关博落回化学成分与药理活性研究报道可知,博落回中含有多种药理活性成分,其中以苯骈菲啶异喹啉类生物碱为主[2],这些生物碱在杀菌、抗炎、消肿、杀虫、抗癌、改善肝功能、促进动物生长方面有广阔的应用前景[3-11]。博落回植株中,以成熟果荚中生物碱含量最为丰富,而在生物碱中,又以血根碱与白屈菜红碱含量最高[10]。因此,血根碱与白屈菜红碱的药理活性研究备受关注,已有其在抗真菌、消炎、抗肿瘤、抗艾滋病和作为生物农药防治害虫等方面的活性报道[12-15],且已有报道血根碱能够有效清除自由基,减少生物大分子的氧化和羰基化损伤,是潜在的天然的食品抗氧化剂[16]。
采用薄层色谱、凝胶色谱、硅胶柱色谱、制备高效液相、重结晶等多种方法或其联用,可以从博落回植株不同部位分离得到十几种生物碱单体成分[17-21],但存在操作繁琐、样品不可逆吸附、成本较高等缺点,不适于大量制备。高速逆流色谱法(HSCCC)是一种液-液分配色谱技术,避免了样品的不可逆吸附,具有操作简单、成本低、条件温和、制备量大等优点,已广泛应用于天然产物活性成分的分离制备[22-26]。目前关于高速逆流色谱技术在博落回生物碱分离中应用报道较少,仅有利用离子液体改性高速逆流色谱法[27]、pH区带高速逆流色谱法[28-29]分离纯化博落回血根碱与白屈菜红碱的报道,但这两种方法在大量制备时,需要对两相溶剂进行离子改性或逆流色谱系统中额外增加pH在线检测器,存在操作较复杂、成本较高等不足,在实用性上有一定局限。
因此,为建立一种简便实用的利用常规的高速逆流色谱(HSCCC)分离制备高纯度的血根碱盐酸盐与白屈菜红碱盐酸盐的方法,本研究以博落回生物碱粗提物为研究对象,通过分析型HSCCC筛选最优的溶剂体系并应用到制备型HSCCC上,以期分离得到高纯度生物碱单体,为血根碱和白屈菜红碱的进一步研究应用提供实验基础。
1. 材料与方法
1.1 材料与仪器
博落回果荚 采自铜仁市大兴区山区野生博落回植株;血根碱盐酸盐标准品(HPLC测定纯度98.00%)、白屈菜红碱标准品(HPLC测定纯度98.00%) 均购自上海源叶生物科技有限公司;UPLC色谱分析所用乙腈 色谱纯,默克公司;水为二次蒸馏水;其余实验所用甲醇、氯仿、盐酸、硫酸、乙醇等试剂 均为市售分析纯试剂。
TEB-30A分析型高速逆流色谱仪、TEB-1000A制备型高速逆流色谱仪、TBP5002恒流泵、DC-0506低温恒温槽 上海同田生物技术股份有限公司;UV-2000紫外检测器 成都千年红科技有限公司;1290型超高效液相色谱仪 美国Aglient公司;PDF-50L玻璃反应釜、Z-62旋转蒸发仪 上海普渡生化科技有限公司;DHG-09620B鼓风干燥箱 上海副絮实验仪器;ZB-Ⅲ循环水真空泵 巩义予华仪器有限公司;CPA2250十万分之一天平 赛多利斯科学仪器。
1.2 实验方法
1.2.1 HSCCC进样原料的制备
采用酸水提取法粗提博落回生物碱。1 kg干燥粉碎的博落回果荚放置于50 L反应釜中,加入60% 乙醇溶液6 L, 0.1 mol/L的硫酸水溶液14 L,加热至回流,搅拌1~1.5 h,趁热用50目滤布过滤,得深褐色滤液。滤液用氢氧化钠调pH至10~10.5,静置12 h,抽滤,40 ℃鼓风干燥得深褐色博落回总碱粗品粉末。取100 g此深褐色粉末用适量无水乙醇回流提取3次,合并滤液,用硫酸调pH至1,静置12 h,抽滤得深红色博落回生物碱粗品[2]。取此深红色博落回生物碱粗品10 g,2 L水溶解,抽滤除去极少不溶物,澄清水溶液用氢氧化钠水溶液缓慢调pH至8~9,静置,抽滤,40 ℃鼓风干燥得灰色粉末固体,避光保存,为HSCCC进样原料。
1.2.2 HSCCC制备分离条件与过程
分析型HSCCC:在分液漏斗中配制三氯甲烷-甲醇-0.2 mol/L盐酸水(4:2:2,V/V/V)溶液两相溶剂体系共400 mL,将其充分振荡后静置,用锥形瓶收集上相为固定相,下相为流动相,两相超声脱气30 min,备用。主机转速1300 r/min,流速1 mL/min,分离温度25 ℃,检测波长280 nm,进样量1 mg,振荡全溶于1 mL流动相中,为分析型HSCCC进样溶液[27]。
制备型HSCCC:溶剂体系与分析型HSCCC相同。在10 L分液漏斗中配置两相溶剂共6 L。上相为固体相,下相为流动相,脱气30 min,备用。主机转速455 r/min,流速8 mL/min,分离温度25 ℃,检测波长280 nm,进样量1000 mg,振荡全溶于20 mL流动相中,为制备型HSCCC进样溶液[28-29]。
HSCCC分离过程:用较大流速将固定相泵入并充满色谱柱中,开启恒温循环水槽温度设定为25 ℃,开启主机电源,正接正传达到设定转速,待稳定后,以设定的分离流速泵入流动相。此时记录从开始泵入流动相至流动相在管柱出口流出时固定相的流出体积(V流出)以计算固定相的保留率。待流动相从管柱出口流出后且基线稳定后,将溶解在适量流动相中的样品从进样圈注入。管柱出口流出液在280 nm下连续检测,根据色谱图出峰情况,手动收集各组分。在不开逆流色谱主机下,自行测定仪器色谱柱加外接管路总体积(V总)。色谱柱体积(V柱体积)由实验仪器确定。
1.2.3 分离产物定性及样品纯度分析
使用超高效液相色谱(UPLC)对分离后样品进行定性分析与纯度分析。定性分析采用标准品对照法。标准品与分离产物在同等色谱条件下分别进样,对比两者保留时间与吸收光谱图;再将样品与标准品混合进样,观测其保留时间、峰型是否分裂、吸收光谱有无变化。定性实验重复三次。
样品纯度分析采用外标法。用十万分之一天平分别称取血根碱盐酸盐标准品、白屈菜红碱盐酸盐标准品、分离得血根碱盐酸盐样品、分离得白屈菜红碱盐酸盐样品2~3 mg,统一配制成浓度为0.05 mg/mL左右样品溶液,分别进行UPLC进样分析,求得峰面积。按下列公式计算两种分离得到的样品的纯度。实验重复三次,每次重复单个样品进样三次,观测其重复性及误差。
色谱条件为:紫外检测波长280 nm;C18色谱柱;进样量1 μL;流速0.5 mL/min;柱温25 ℃;0.05%磷酸水-乙腈体系作为流动相;采用梯度洗脱:流动相组成A(0.05%磷酸水溶液)-B(乙腈); 0~1 min 25%A;1~2 min 40%A;2~3 min 40%A;3~4 min 60%A;4~5 min 75%A;洗脱时间为5 min,后运行1 min[20-21]。
1.3 数据处理
核磁共振波谱表征由中国农业大学理学院分析测试中心代为检测,数据处理使用MestReNova 软件。图表数据处理、绘图使用origin pro 9.1软件。 化合物结构式绘制采用ChembioDraw 14.0 软件。
2. 结果与讨论
2.1 溶剂体系的选择
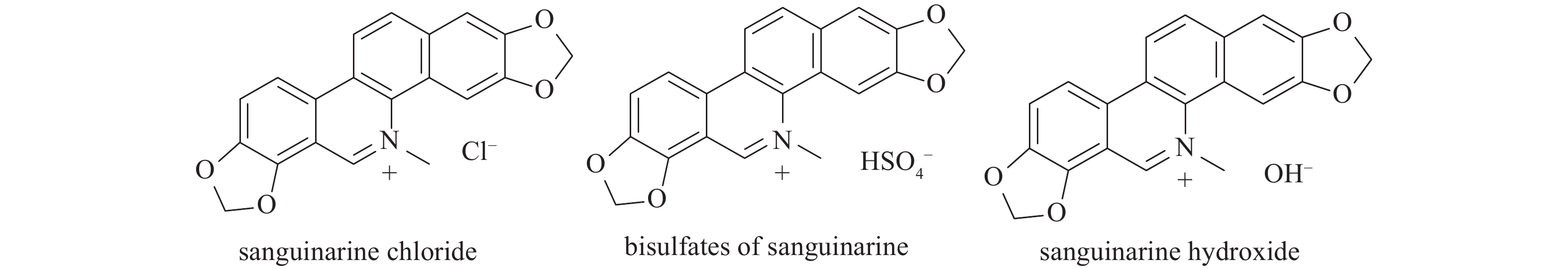
博落回血根碱与白屈菜红碱分子中N原子带有正电荷,不稳定,在溶液中易分解。通常将博落回生物碱成盐以保持其稳定性[2]。血根碱为例,在文献中已报道主要有三种形态:血根碱盐酸盐、血根碱硫酸氢盐、羟化血根碱(见图1)。
在考察合适的溶剂系统时,通过查阅文献[2,17-21]与反复实验,发现博落回生物碱盐酸盐、博落回生物碱硫酸氢盐在纯水、甲醇、乙醇、三氯甲烷、乙腈、乙酸乙酯、正己烷等常用溶剂中,溶解度太小,几乎不可能找到适合分离的溶剂体系。而在考察羟化博落回生物碱时发现其在三氯甲烷、甲醇、低浓度盐酸水溶液中均有较好的溶解度,在高浓度盐酸甲醇溶液中,又以盐酸盐形式析出。故本研究选择在碱性形态的羟化博落回生物碱作为HSCCC分离的进样原料,选择三氯甲烷-甲醇-低浓度盐酸水溶液两相体系作为分离体系,后处理使其以盐酸盐形式析出,方便进行终产物收集。
2.2 分析型HSCCC分离条件的优化
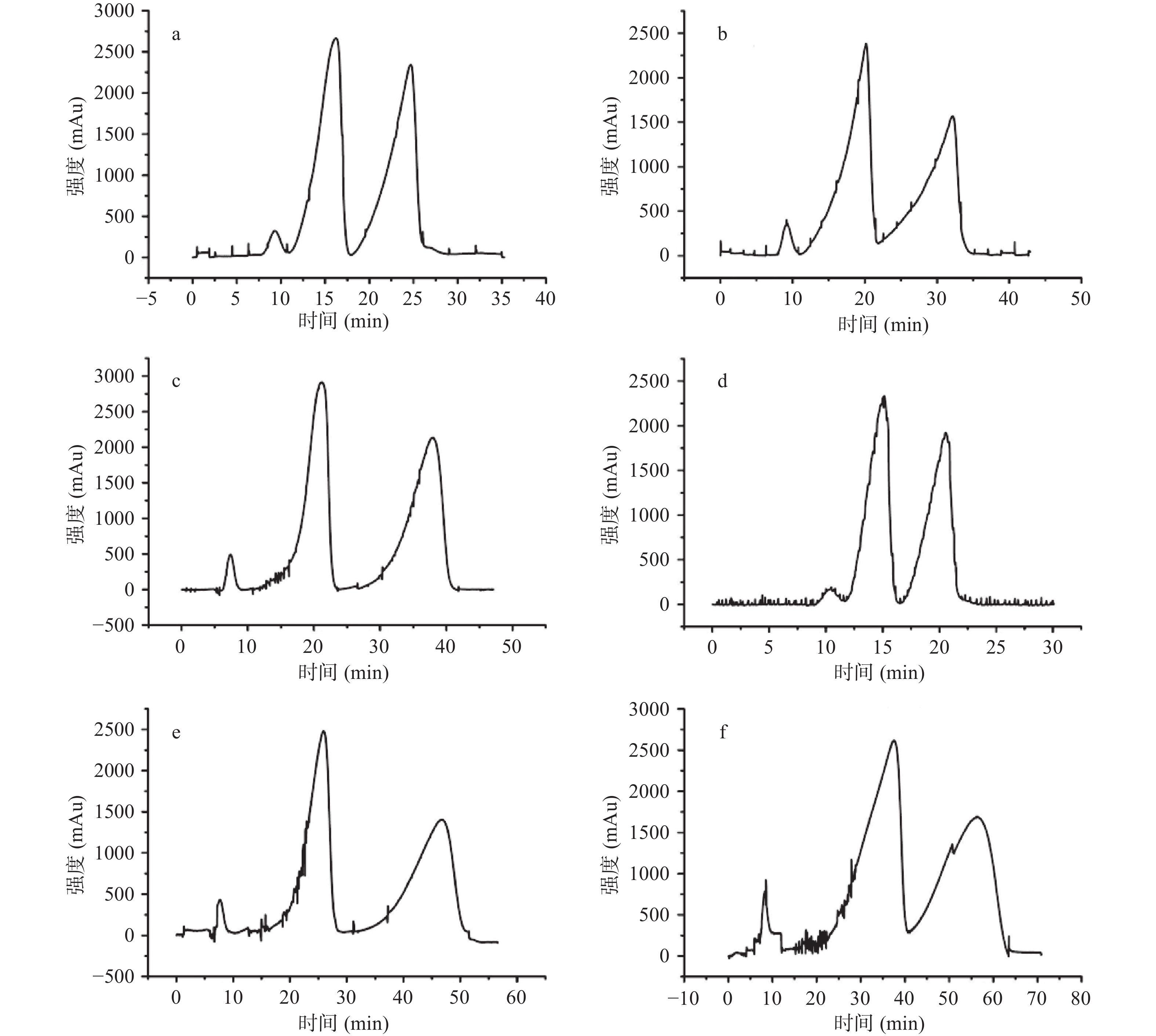
分析型高速逆流色谱仪进样分析实验一次通常只需30~50 min左右,柱体积也只有28 mL,方便快速,适用于条件摸索。在三氯甲烷-甲醇-低浓度盐酸水溶液两相溶剂系统下,设计六种溶剂体系分别进样进行实验,结果图谱见图2。
![]() 图 2 在六种不同溶剂体系下利用分析型高速逆流色谱分离博落回生物碱的实验结果注:溶剂体系a. CHCl3-CH3OH-0.2 mol/L HCl(4:3:2,V/V/V),T=67.8%; b. CHCl3-CH3OH-0.1 mol/L HCl(4:3:2,V/V/V), T=64.2%;c. CHCl3-CH3OH-0.2 mol/L HCl(4:2:2,V/V/V), T=64.2%; d. CHCl3-CH3OH-0.1 mol/L HCl(4:2:2,V/V/V), T=53.5%; e. CHCl3-CH3OH-0.2 mol/L HCl(4:1.5:2,V/V/V), T=64.3%; f. CHCl3-CH3OH-0.1 mol/L HCl(4:1.5:2,V/V/V), T=64.2%。Figure 2. Experimental results of the separation of Macleaya cordata alkaloids by analytical HSCCC with six different solvent systems
图 2 在六种不同溶剂体系下利用分析型高速逆流色谱分离博落回生物碱的实验结果注:溶剂体系a. CHCl3-CH3OH-0.2 mol/L HCl(4:3:2,V/V/V),T=67.8%; b. CHCl3-CH3OH-0.1 mol/L HCl(4:3:2,V/V/V), T=64.2%;c. CHCl3-CH3OH-0.2 mol/L HCl(4:2:2,V/V/V), T=64.2%; d. CHCl3-CH3OH-0.1 mol/L HCl(4:2:2,V/V/V), T=53.5%; e. CHCl3-CH3OH-0.2 mol/L HCl(4:1.5:2,V/V/V), T=64.3%; f. CHCl3-CH3OH-0.1 mol/L HCl(4:1.5:2,V/V/V), T=64.2%。Figure 2. Experimental results of the separation of Macleaya cordata alkaloids by analytical HSCCC with six different solvent systems由图2可知,在三氯甲烷-甲醇-低浓度盐酸水溶液这个溶剂系统中,在e、f体系中,分析时间明显延长,需要55~65 min;在a、b体系中,分析时间较短(27~35 min),但相邻色谱峰峰底存在重合情况;在b、d、f体系中(配制两相溶剂时盐酸水溶液浓度为0.1 mol/L),相邻色谱峰峰底也存在重合现象;在c体系(三氯甲烷-甲醇-0.2 mol/L 盐酸水溶液(4:2:2,V/V/V))中,相邻色谱峰峰底无重合现象,分离时间较短(42 min),确定为最优分离条件。在六种溶剂体系下,均有较好的固定相保留率,在64.2%~67.8%之间, 均满足逆流色谱分析时所要求的最低35% 的固定相保留率。
根据分析型高速逆流色谱对6种不同的溶剂系统在分离博落回生物碱的实验中的结果对比,本文选择三氯甲烷-甲醇-0.2 mol/L 盐酸水溶液(4:2:2, V/V/V)这一溶剂体系作为优选的溶剂体系直接应用到制备型高速逆流色谱上。
2.3 制备型HSCCC分离结果
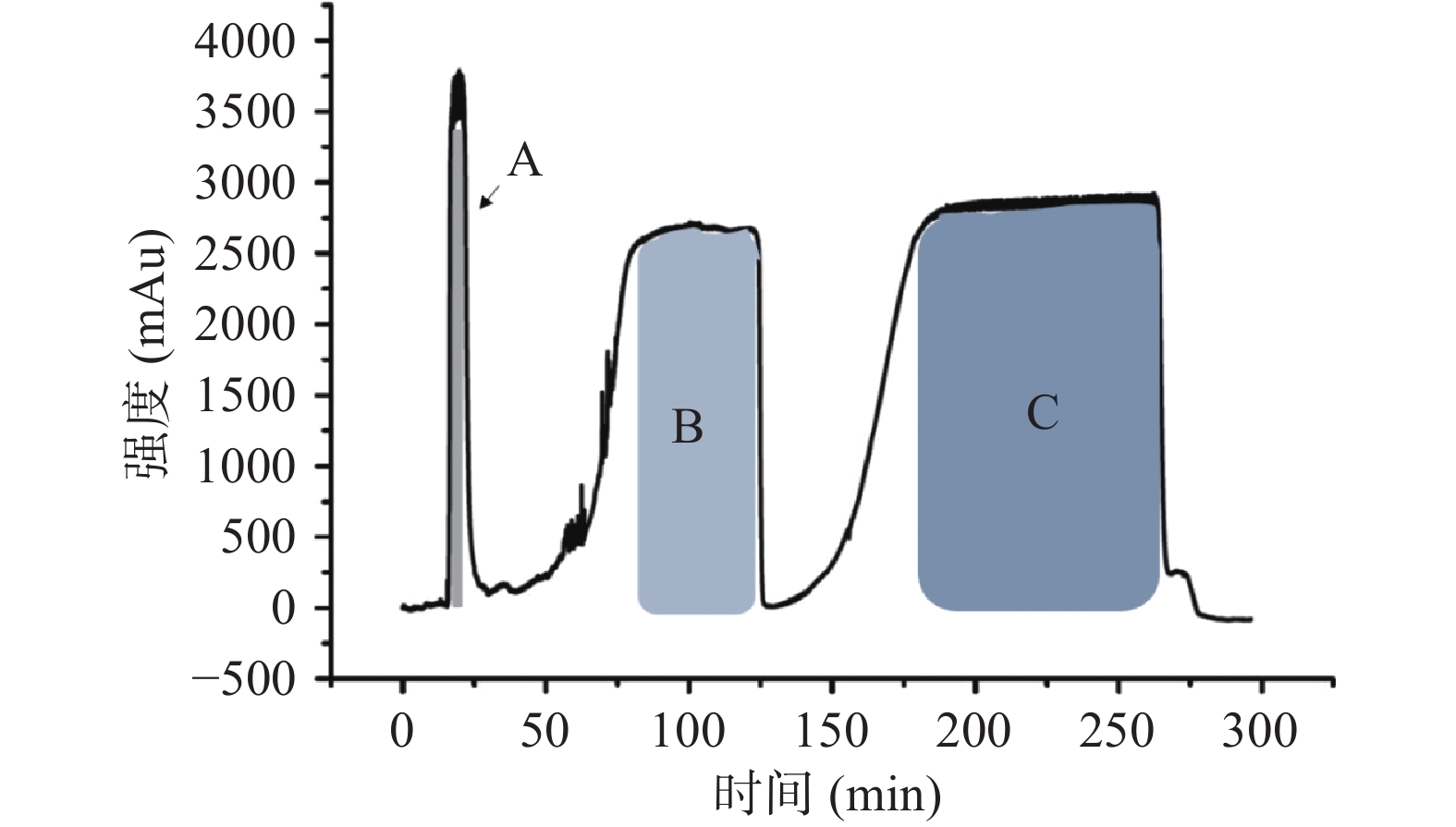
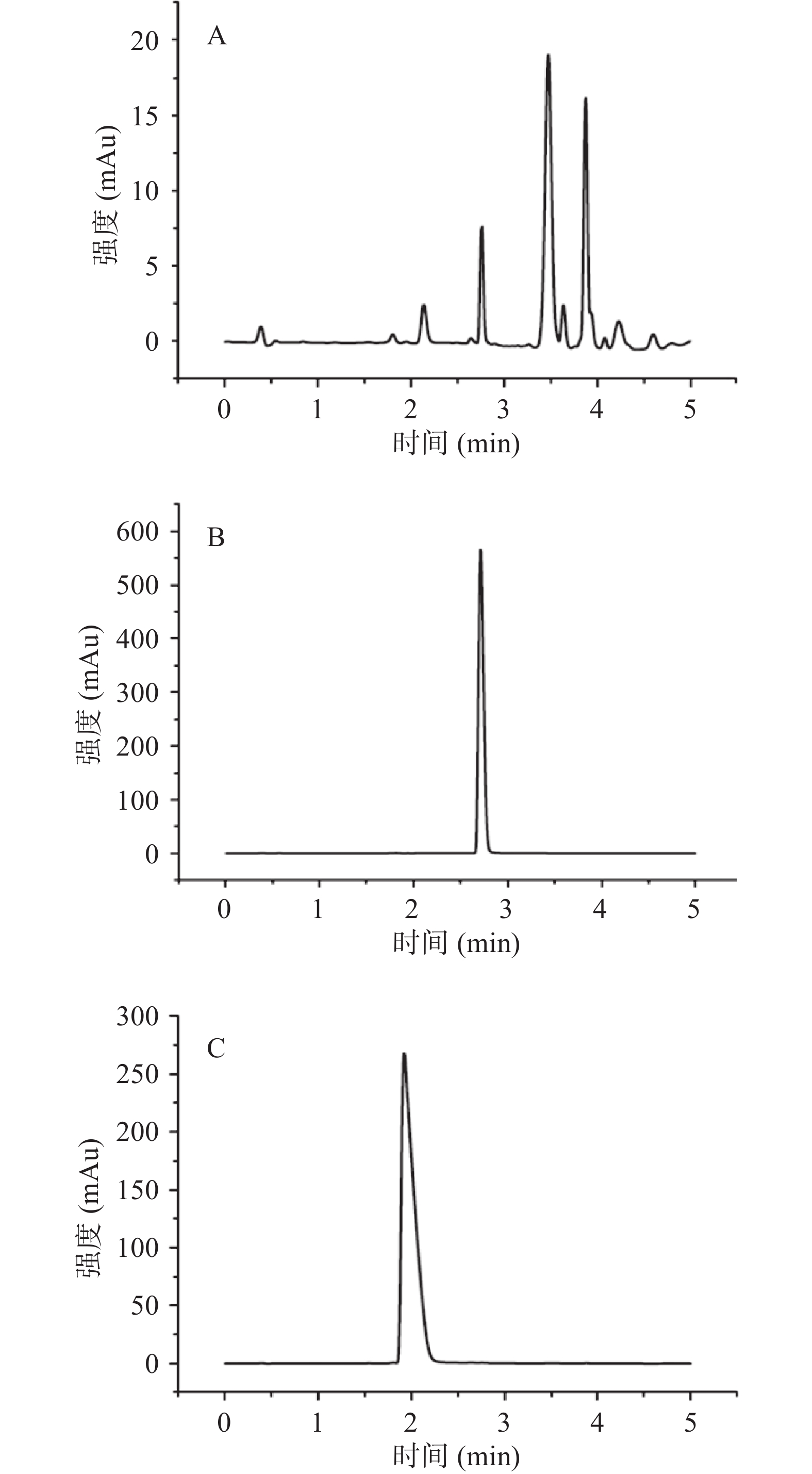
将优选的溶剂体系(三氯甲烷-甲醇-0.2 mol/L 盐酸水溶液(4:2:2,V/V/V))直接应用到制备型高速逆流色谱上,经一次HSCCC制备分离,结果从1000 mg博落回生物碱粗品中分离得到3个主要组分,分别标记为A、B、C三种组分(见图3),溶剂体系固定相保留率为77.2%,满足逆流色谱分析的要求。由图3可知,峰与峰之间分离完全,方便对应组分的收集。
根据图3中色谱图A、B、C三个出峰位置,用锥形瓶手动收集对应的组分(图中阴影部分)。收集的每种组分溶液,分别用旋转蒸发仪除去有机溶剂(主要为三氯甲烷,可循环利用)后,可见部分固体析出,用100 mL甲醇分散溶解后,加入4~6 mL的盐酸调pH至1左右,静置固体析出,抽滤,40 ℃鼓风干燥,得灰色的A组分盐酸盐12 mg,淡绿色B组分盐酸盐435 mg,淡红色C组分盐酸盐505 mg。其具体结构利用UPLC标准品对照法初步确认后,进一步用1H NMR、13C NMR加以确定。上述步骤中,最后成盐过程相当于一次重结晶纯化过程,有利于得到高纯度的最终产物。
2.4 血根碱盐酸盐与白屈菜红碱盐酸盐的定性分析与样品纯度测定
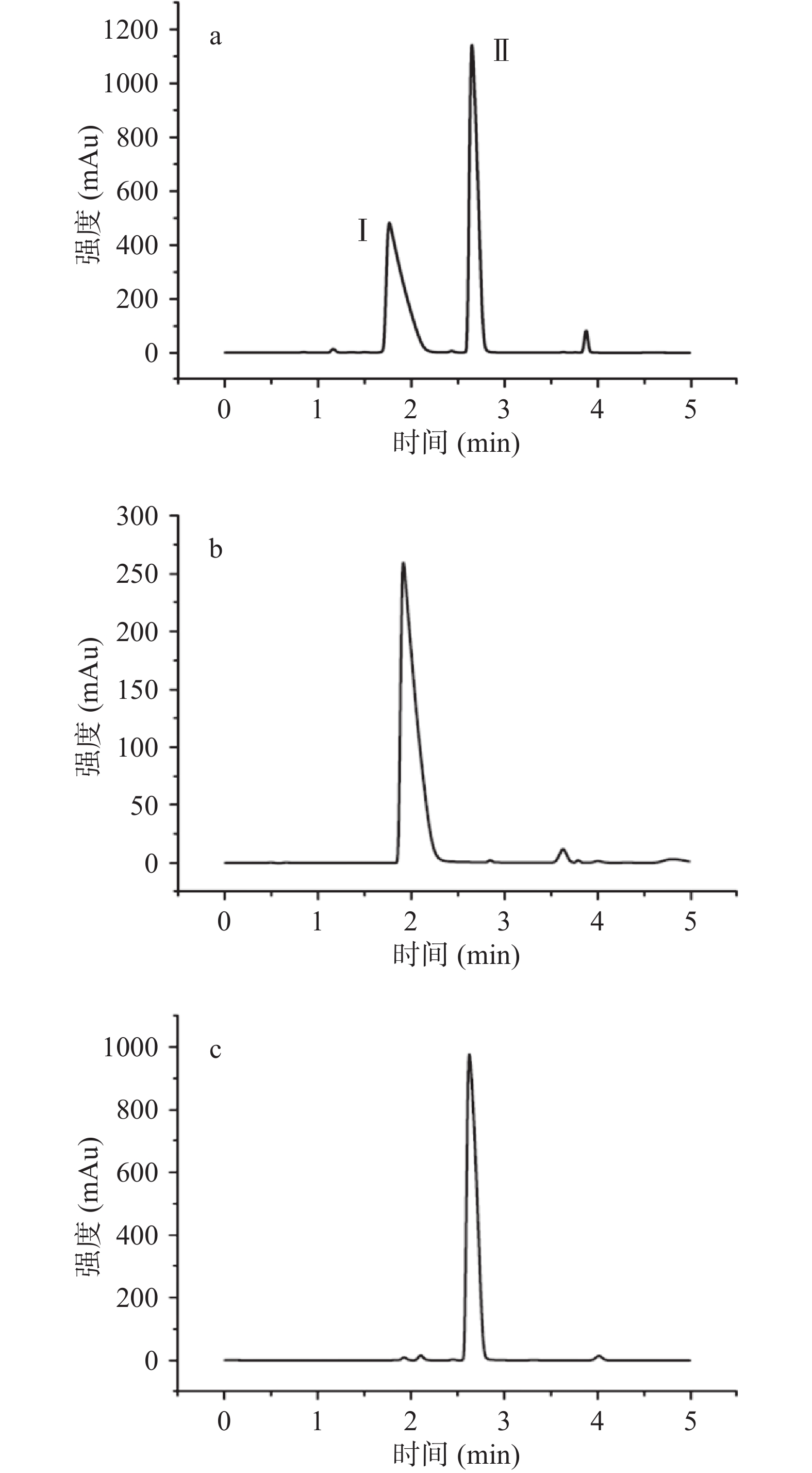
在色谱分离之前,将HSCCC进样原料进行UPLC分析(见图4a)。从图中可以看出,进样原料中主要有Ⅰ、Ⅱ两个组分,其余有些含量较少的杂质。对比进样原料与血根碱盐酸盐、白屈菜红碱盐酸盐的标准品的UPLC色谱图(见图4b、c),可初步确定Ⅰ峰(保留时间为1.91 min)为血根碱盐酸盐,Ⅱ峰(保留时间为2.76 min)为白屈菜红碱盐酸盐。
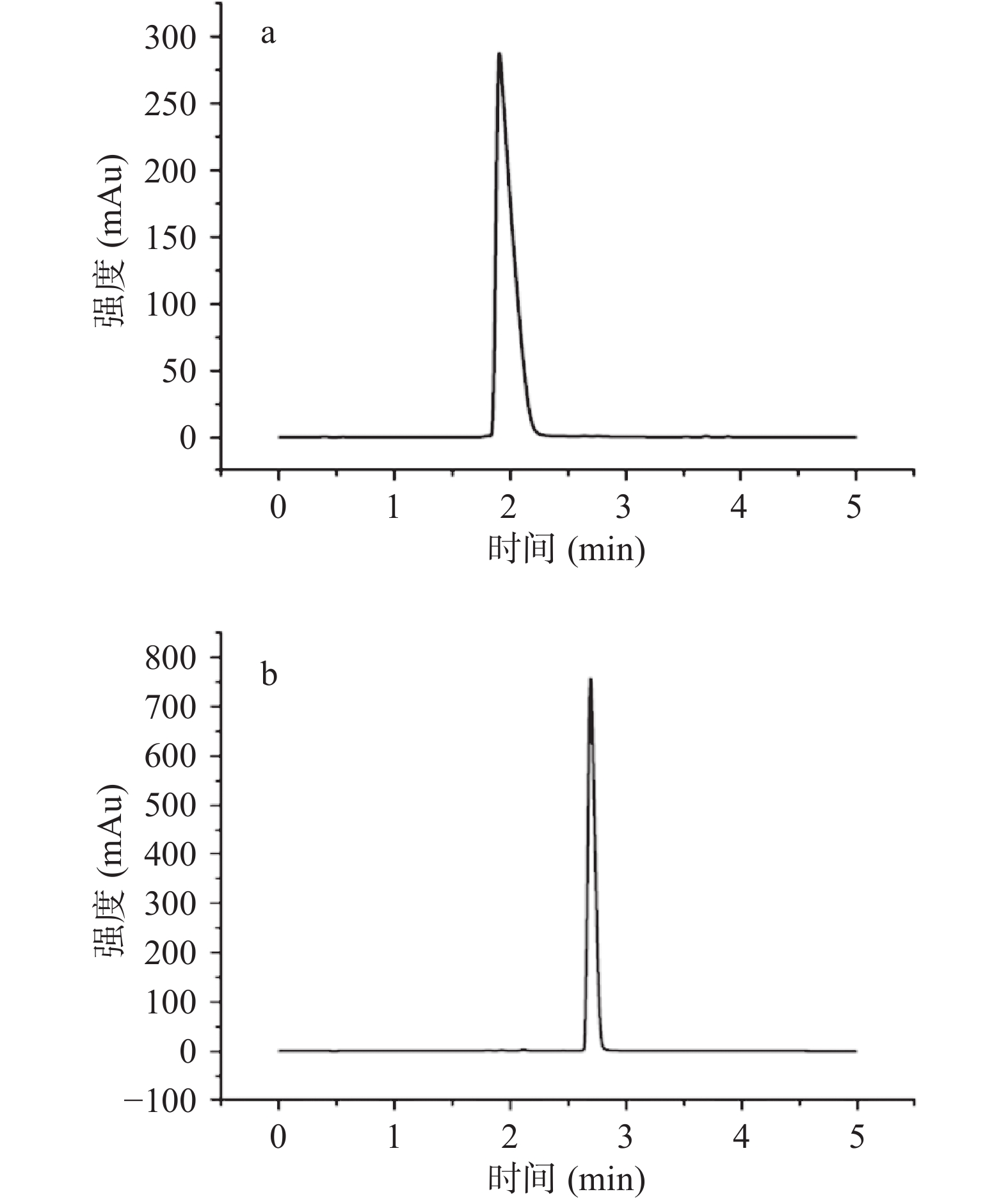
将制备型HSCCC分离得到A、B、C三组分盐酸盐进行UPLC色谱分析(见图5)。与HSCCC进样原料、标准品色谱图对比可初步确定:A组分为少量多种杂质的混合物(响应值很低);B组分为白屈菜红碱盐酸盐;C组分为血根碱盐酸盐。采用内标法,将适量B组分与白屈菜红碱盐酸盐标准品混合进行UPLC分析,将适量C组分与血根碱盐酸盐标准品混合进行UPLC分析(见图6a、b)。对比后,无新峰、无分裂,确定B组分为白屈菜红碱盐酸;C组分为血根碱盐酸盐。
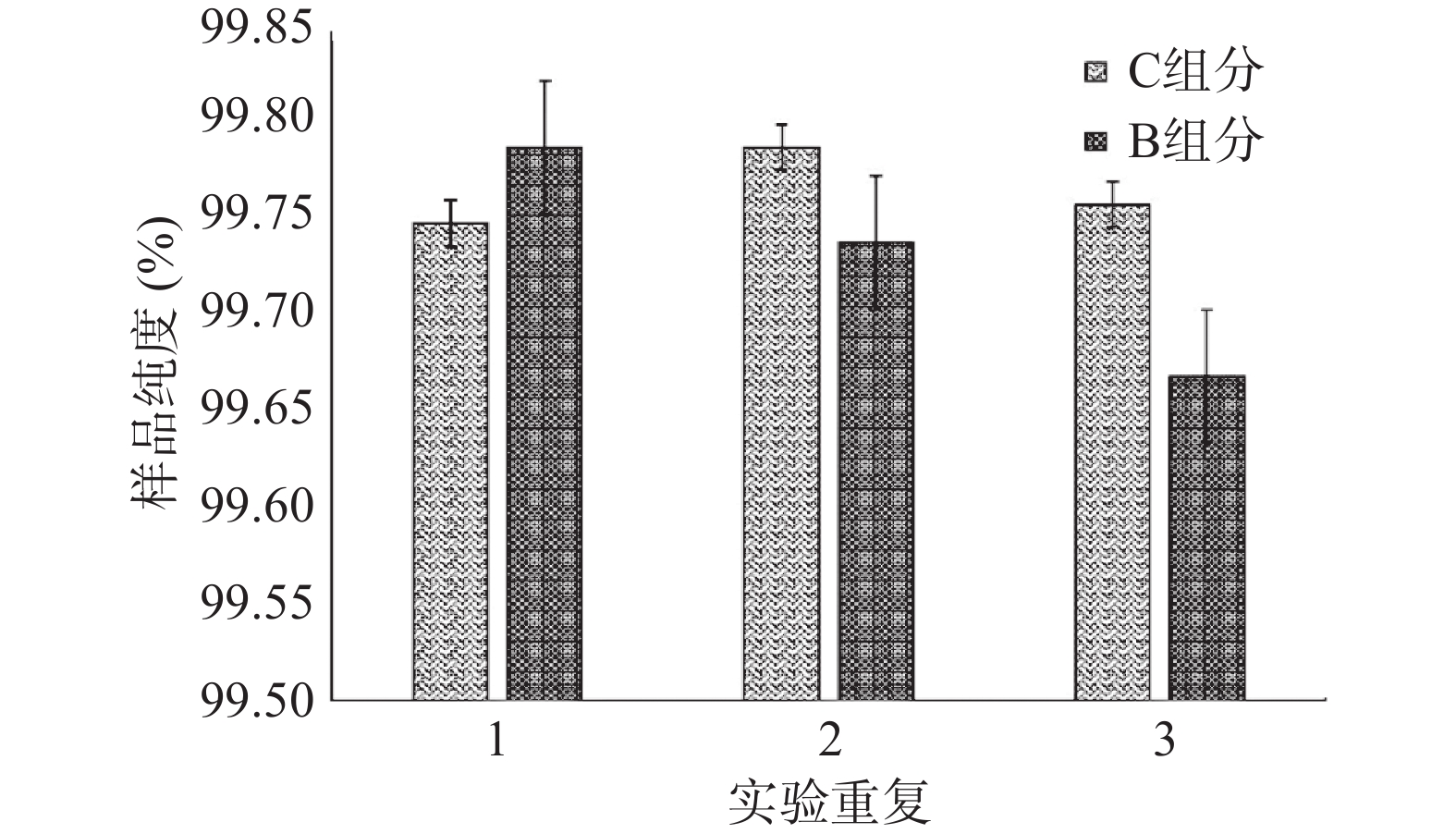
采用外标法测定B、C两个组分的纯度。实验重复三次,数据重现性好(见图7)。白屈菜红碱盐酸盐(B组分)纯度均值为99.73%;血根碱盐酸盐(C组分)纯度均值为99.77%。对比可知, HSCCC分离得到的两种生物碱的纯度均高于所购买的标准品的纯度(98.00%)。
2.5 血根碱盐酸盐与白屈菜红碱盐酸盐的核磁鉴定
将分离得到血根碱盐酸盐与白屈菜红碱盐酸盐进行1H NMR和13C NMR测定,数据如下。与已有文献对比,核磁数据相符,可以确定分离得到的B组分为白屈菜红碱盐酸盐,C组分为血根碱盐酸盐。
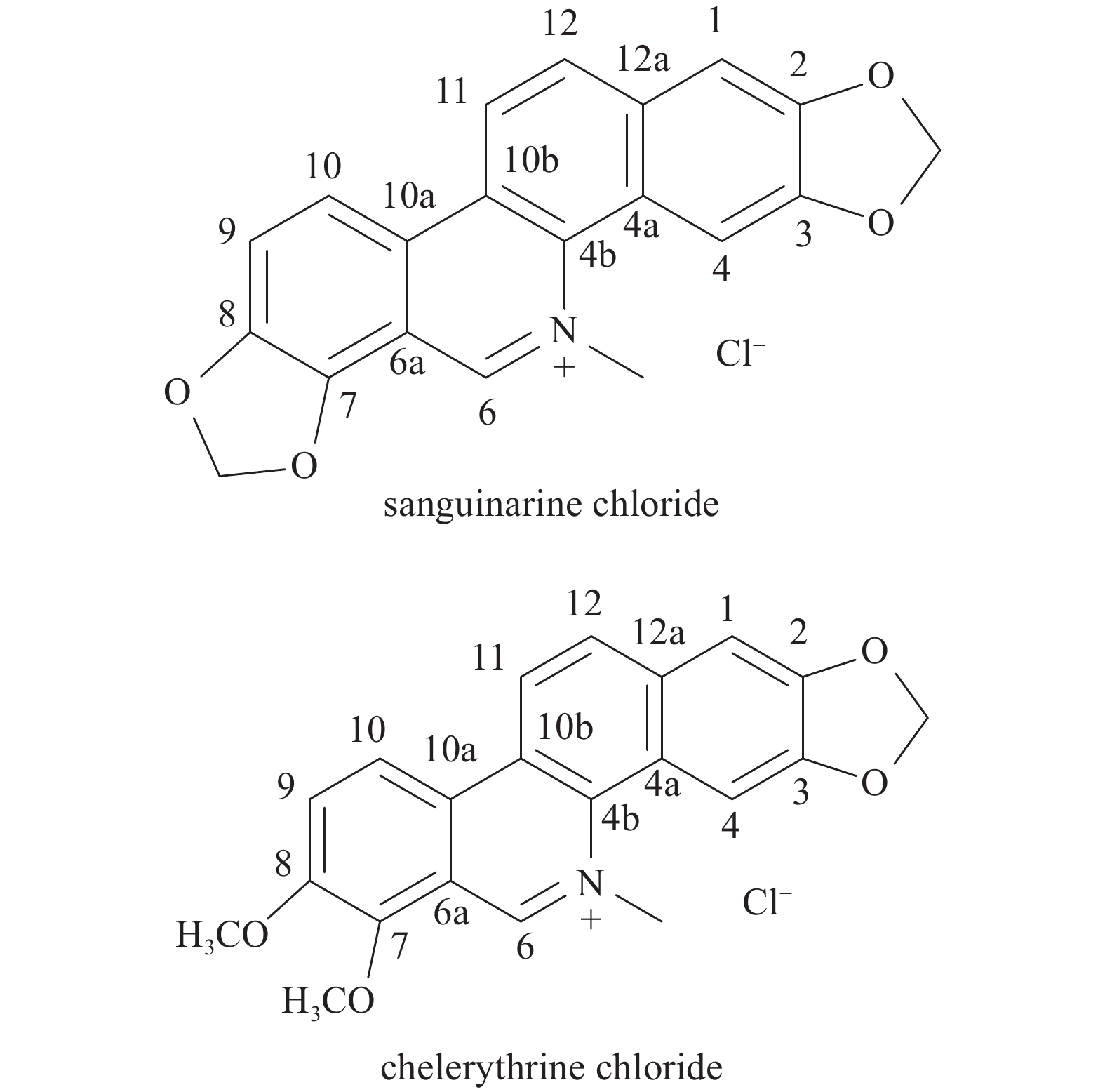
白屈菜红碱盐酸盐(B组分),淡绿色粉末。1H NMR(DMSO, 500MHz) δ: 10.12 (s, 1H, H-6),8.87(d, J=8.9 Hz, 1H, H-9),8.85 (d, J=8.9 Hz, 1H, H-10),8.34-8.29(m, 3H, H-1, H-11, H-12),7.80 (s, 1H, H-4),6.36 (s, 2H, -OCH2-),5.00 (s, 3H, -NCH3),4.18 (s, 3H, -OMe-7),4.13 (s, 3H, -OMe-8)。13C NMR(DMSO, 126MHz)δ 150.18(C-8),149.98(C-6),148.16(C-3),148.07(C-2),144.80(C-7),131.67(C-12a),131.08(C-4b),130.46(C-12),127.42(C-10a),125.49(C-9),124.67(C-10b),119.53(C-4a),118.75(C-6a),118.64(C-11), 118.15(C-10),105.18(C-1),103.67(C-4),102.14(-OCH2-2,3),61.60(OMe-7),56.41(-OMe-8),51.62(N-Me)。与文献[30]对照,确定为白屈菜红碱盐酸盐(Chelerythrine chloride)。数据中碳氢编号见图8。
血根碱盐酸盐(C组分),淡红色粉末。1H NMR(DMSO, 500MHz) δ: 10.16 (s, 1H, H-6),8.78 (d, J=9.0 Hz, 1H, H-12),8.64 (d, J=8.9 Hz, 1H, H-11),8.30 (d, J=9.1 Hz, 1H, H-10),8.28 (s, 1H, H-1),8.12 (d, J=8.8 Hz, 1H, H-9),7.77 (s, 1H, H-4),6.61 (s, 2H, -OCH2-2,3), 6.36 (s, 2H, -OCH2-7,8),4.93 (s, 3H, N-Me)。13C NMR(DMSO, 126MHz)δ 150.40(C-6),149.22(C-2),149.22(C-3),147.99(C-7),146.75(C-6),132.65(C-12a),131.95(C-4b),131.77(C-12),127.64(C-10a),126.15(C-10b),120.76(C-9),120.40(C-4a),119.34(C-11),117.81(C-10),109.96(C-6a),106.21(C-1),105.37(C-4), 104.71(-OCH2-7,8),103.25(-OCH2-2,3), 52.58(N-Me)。与文献[30]对照,确定为血根碱盐酸盐(Sanguinarine chloride)。数据中碳氢编号见图8。
3. 结论
利用分析型逆流色谱仪优选合适的分离体系和分离条件,然后将优选的溶剂系统和分离条件直接应用于制备型HSCCC仪器上。在优选的条件下,利用制备型高速逆流色谱仪器,一次能够从1000 mg博落回生物碱粗品中分离得到血根碱盐酸盐505 mg(纯度99.77%)和白屈菜红碱盐酸盐435 mg(纯度99.73%),二者结构经标准品对照法、1H NMR、13C NMR确认。本文建立了一种利用常规高速逆流色谱技术制备高纯度血根碱盐酸盐和白屈菜红碱盐酸盐的方法,为血根碱和白屈菜红碱的进一步开发利用奠定了一定的基础。
-
图 2 在六种不同溶剂体系下利用分析型高速逆流色谱分离博落回生物碱的实验结果
注:溶剂体系a. CHCl3-CH3OH-0.2 mol/L HCl(4:3:2,V/V/V),T=67.8%; b. CHCl3-CH3OH-0.1 mol/L HCl(4:3:2,V/V/V), T=64.2%;c. CHCl3-CH3OH-0.2 mol/L HCl(4:2:2,V/V/V), T=64.2%; d. CHCl3-CH3OH-0.1 mol/L HCl(4:2:2,V/V/V), T=53.5%; e. CHCl3-CH3OH-0.2 mol/L HCl(4:1.5:2,V/V/V), T=64.3%; f. CHCl3-CH3OH-0.1 mol/L HCl(4:1.5:2,V/V/V), T=64.2%。
Figure 2. Experimental results of the separation of Macleaya cordata alkaloids by analytical HSCCC with six different solvent systems
-
[1] 中国医学科学院药物研究所. 常用中草药栽培手册[M]. 北京: 人民卫生出版社, 1971: 75−77. Chinese Academy of Medical Sciences. Cultivation manual of commonly used Chinese herbal medicine[M]. BeiJing: People's Medical Publishing House, 1971: 75−77.
[2] 钟明. 博落回主要生物碱的分离、纯化及生物活性研究[D]. 长沙: 中南大学, 2011: 1−10. ZHONG M. Separation, purification and bioactivities of principal alkaloids from Macleaya cordata (Willd) R. Br. [D]. Changsha: Central South University, 2011: 1−10.
[3] QING Z X, XU Y Q, YANG P, et al. Study on alkaloids of fruit from Macleaya cordata[J]. Journal of Chinese Medicinal Materials,2016,39(2):312−314.
[4] FENG G, ZHANG J, LI X W, et al. Insecticidal activity of alkaloids from Macleaya microcarpa against several species of insect pests[J]. Journal of Tropical and Subtropical Botany,2008,5(3):39−42.
[5] 王朝元, 童胜兰, 胡鑫, 等. 博落回生物碱成分及其抗菌活性的研究[J]. 中南民族大学学报(自然科学版),2015,34(1):33−39. [WANG C Y, TONG S L, HU X, et al. Studies on alkaloid ingredients of Macleaya cordata and their antibacterial activity[J]. Journal of South-central University for Nationalities(Nat Sci Edition),2015,34(1):33−39. [6] 朱艳华, 王超, 阎雪莹. 博落回总碱对SGC 7901细胞毒性的研究[J]. 中华中医药学刊,2013,31(3):475−476. [ZHU Y H, WANG C, YAN X Y. Study on cytotoxicity of total alkaloids of Macleaya cordata on SGC 7901[J]. Chinese Archives of Traditional Chinese Medicine,2013,31(3):475−476. [7] SAI C M, WANG J A, LI B J, et al. Isolation and identification of alkaloids from Macleaya microcarpa by UHPLC-Q-TOF-MS and their cytotoxic activity in vitro, antiangiogenic activity in vivo[J]. BMC Chemistry,2020,14(1):124−131.
[8] 曾建国, 刘华. 博落回主要功能成分及其在动物生产中的应用[J]. 饲料工业,2019,40(7):1−6. [ZENG J G, LIU H. Main functional components of Macleaya cordata and its application in animal production[J]. Feed Industry,2019,40(7):1−6. [9] 张灵梅, 朱晋佳, 杨玲媛, 等. 博落回在畜禽生产中的应用研究[J]. 激光生物学报,2020,29(2):21−27. [ZHANG L M, ZHU J J, YANG L Y, et al. A study on the application of Macleaya cordata in livestock production[J]. Acta Laser Biology Sinica,2020,29(2):21−27. [10] 肖俐, 易键, 赵静, 等. 博落回提取物对大鼠急性酒精性肝损伤的保护作用[J]. 中南药学,2011,9(7):485−489. [XIAO L, YI J, ZHAO J, et al. Protective effect of Macleaya cordata extract on alcohol-induced acute hepatic injury in rats[J]. Central South Pharmacy,2011,9(7):485−489. doi: 10.3969/j.issn.1672-2981.2011.07.002 [11] 陈伟, 张锐, 雷思敏, 等. 博落回化学成分及其药理活性研究进展[J]. 中国实验方剂学杂志,2020,26(3):243−250. [CHEN W, ZHANG R, LEI S M, et al. Advances in chemical constituents and bioactivities of Macleaya cordata[J]. Chinese Journal of Experimental Traditional Medical Formulae,2020,26(3):243−250. [12] 叶冯芝, 冯锋, 柳文媛. 博落回的生物碱成分[J]. 中国中药杂志,2009,34(13):1683−1686. [YE F Z, FENG F, LIU W Y. Alkaloids from Macleaya cordata[J]. China Journal of Chinese Materia Medical,2009,34(13):1683−1686. [13] FAEHNRICH B, PASTOR A, HEIDE C, et al. Effects of isoquinoline alkaloids from Macleaya cordata on physiological, immunological and inflammatory parameters in healthy beagles: Alkaloids in dog nutrition[J]. Journal of Animal Physiology and Animal Nutrition,2019,103(2):661−667.
[14] 杨佳, 陈旻, 李明花, 等. 血根碱对人肺腺癌细胞迁移侵袭和Wnt/β-catenin信号通路的影响[J]. 肿瘤防治研究,2019,46(12):1057−1061. [YANG J, CHEN M, LI M H, et al. Effects of sanguinarine on invasion, migration and Wnt/β-catenin signaling pathway of lung adenocarcinoma cells[J]. Cancer Research Prevention Treatment,2019,46(12):1057−1061. [15] 康伟松, 程辟, 曾建国. 血根碱、白屈菜红碱离子对化合物的体外抗菌活性研究[J]. 中南药学,2014,12(5):406−410. [KANG W S, CHENG P, ZENG J G, et al. In vitro antibacterial activity of sanguinarine and chelerythrine ion-pair compounds[J]. Central South Pharmacy,2014,12(5):406−410. doi: 10.7539/j.issn.1672-2981.2014.05.006 [16] 姚雯, 杨天衡, 刘学波. 血根碱清除自由基及抑制生物大分子氧化的作用[J]. 食品科学,2014,35(9):137−141. [YAO W, YANG T H, LIU X B. Sanguinarine scavenges free radicals and protects against oxidative damage of biological macromolecules[J]. Food Science,2014,35(9):137−141. doi: 10.7506/spkx1002-6630-201409028 [17] 王荣, 刘艳芳, 王超然, 等. 生物碱的高效液相色谱分离分析与纯化制备研究进展[J]. 分析测试学报,2019,38(5):586−594. [WANG R, LIU Y F, WANG C R, et al. Research progress on high performance liquid chromatography in analysis an preparation of alkaloids[J]. Jouranl of Instrumental Analysis,2019,38(5):586−594. doi: 10.3969/j.issn.1004-4957.2019.05.014 [18] LI L Q, HUANG M Y, SHAO J L, et al. Rapid determination of alkaloids in Macleaya cordata using ionic liquid extraction followed by multiple reaction monitoring UPLC-MS/MS analysis[J]. J Pharm Biomed Anal,2017,135(Complete):61−66.
[19] 邓霖芳, 袁帅, 刘江云, 等. 博落回提取物中血根碱的离子交换树脂分离纯化工艺研究[J]. 中国药房,2019,16(30):2226−2231. [DENG L F, YUAN S, LIU J Y, et al. Study on separation and purification technology of sanguinarine from the extract of Macleaya cordata by ion exchange resin[J]. China Pharmacy,2019,16(30):2226−2231. [20] 余坤, 向锋, 卿志星, 等. 博落回根中生物碱的分离[J]. 中国药师,2017,20(11):1903−1906. [YU K, XIANG F, QING Z X, et al. Separation of alkaloids from the root of Macleaya cordata[J]. Chian Pharmacist,2017,20(11):1903−1906. doi: 10.3969/j.issn.1008-049X.2017.11.001 [21] 杨鹏, 向锋, 曾建国, 等. 博落回鲜叶中生物碱类化学成分的分离与结构鉴定[J]. 中国现代中药,2017,19(10):1371−1375. [YANG P, XIANG F, ZENG J G, et al. Isolation and identification of alkaloids from the fresh leaves of Macleaya cordata[J]. Modern Chinese Medicine,2017,19(10):1371−1375. [22] SCHWARZ M, WEBER F, DURAN G E, et al. HPLC-DAD-MS and antioxidant profile of fractions from amontillado sherry wine obtained using high-speed counter-current chromatography[J]. Foods,2021,10(1):131−131. doi: 10.3390/foods10010131
[23] MENG J, LI Q Y, CAO Z Y, et al. Rapid screening and separation of active compounds against α-amylase fromToona sinensis by ligand fishing and high-speed counter-current chromatography[J]. International Journal of Biological Macromolecules,2021,174:270−277. doi: 10.1016/j.ijbiomac.2021.01.195
[24] 吴梦琪, 黄海, 蔡狄宏, 等. 大孔吸附树脂-高速逆流色谱法分离纯化苦水玫瑰花渣中的鞣花酸[J]. 食品工业科技,2021,42(5):182−187. [WU M Q, HUANG H, CAI D H, et al. Separation and purification of ellagic acid from rosa setate x rosa rugosa waste by macroporous resin and high-speed counter current chromatography[J]. Science and Technology of Food Industry,2021,42(5):182−187. [25] 宋道光, 樊鑫宇, 徐顺连, 等. 高速逆流色谱法从小叶金钱草中分离制备三种黄酮苷类化合物[J]. 食品工业科技,2019,40(13):29−33. [SONG D G, FAN X Y, XU S L, et al. Preparation of three flavonoid glycosides compounds from Hydrocotyle sibthorpioides Lam. by high speed counter current chromatography[J]. Science and Technology of Food Industry,2019,40(13):29−33. [26] 潘汇, 蔡为荣, 谢亮亮, 等. 运用HSCCC法分离纯化荷叶中三种黄酮及抗氧化活性[J]. 食品工业科技,2018,39(16):161−165. [FAN H, CAI W R, XIE L L, et al. Isolation and purification of three flavonoid lotus leaf by HSCCC and antioxidant activity evaluation[J]. Science and Technology of Food Industry,2018,39(16):161−165. [27] LIU Y, WANG W, CHE F, et al. Isolation and purification of alkaloids from the fruits of Macleaya cordata by ionic-liquid-modified high-speed counter-current chromatography[J]. Journal of Separation Science,2020,43(12):1005−1017.
[28] IFTIKHAR A, JING C L, LI C, et al. Efficient extraction and purification of benzo[c]phenanthridine alkaloids from Macleaya cordata (Willd) R. Br. by combination of ultrahigh pressure extraction and pH-zone-refining counter-current chromatography with anti-breast cancer activity in vitro[J]. Phytochemical Analysis,2020,13(7):1−10.
[29] LIU Q, SUN C, MENG F, et al. Preparative separation of chelerythrine and canguinarine from Macleaya cordata by pH-Zone-Refining counter-current chromatography[J]. Journal of Liquid Chromatography & Related Technologies,2015,38(20):1789−1793.
[30] MAREK R, TOUSEK J, DOSTAL J, et al. 1H NMR and 13C NMR study of quaternary benzo[c]phenanthridine alkaloids[J]. Magnetic Resonance in Chemistry,1999,37(11):781−787. doi: 10.1002/(SICI)1097-458X(199911)37:11<781::AID-MRC556>3.0.CO;2-H







 下载:
下载:
 下载:
下载:
