Research Progress on Determination of Protein Components in Milk and Dairy Products
-
摘要: 乳蛋白是乳及乳制品中重要的组成成分,其含量和组成是影响营养、免疫等功能特性的重要因素。乳中蛋白组分复杂,不同组分含量差异大,随着乳蛋白功能特性研究的深入,快速准确测定乳蛋白组分的含量具有重要的意义和研究价值。本文对目前使用最多的酶联免疫法、毛细管电泳法、高效液相色谱法和高效液相色谱串联质谱法4类测定乳蛋白组分方法的原理、适用性和方法特点进行综述总结,为乳蛋白组分的准确测定和新方法建立提供可靠的技术参考,为乳品营养研究、乳产品开发、婴幼儿配方粉优化提供理论支持。
-
关键词:
- 乳蛋白 /
- 酶联免疫法 /
- 毛细管电泳法 /
- 高效液相色谱法 /
- 高效液相色谱串联质谱法
Abstract: Milk protein is an important component in milk and dairy products, and its content and composition are important factors influencing the functionality of milk such as nutrition and immunity. Protein components in milk are complex, and the content of different components varies greatly. With the development of functional properties of milk protein, it is of great significance and value to determine the content of milk protein components in a faster and more accurate way. Currently, enzyme-linked immunosorbent assay (ELISA), capillary electrophoresis (CE), high performance liquid chromatography (HPLC) and high performance liquid chromatography tandem mass spectrometry (HPLC-MS/MS) are the main methods used to determine protein components in milk. In this article, the measurement principle, applicability, and the characteristics of these methods are reviewed, which could provide reliable technical reference for accurate measurement and establishment of a novel method in milk protein evaluation, while this could also be a theoretical support for dairy nutrition research, development of dairy products and infant formula optimization. -
哺乳动物分泌的乳汁为初生幼崽提供生长发育所需的所有物质,乳蛋白作为乳汁中重要的功能成分,其含量和组成在不同物种、不同泌乳阶段会有很大的变化。人乳蛋白质含量为1.97%、牛乳蛋白质含量为3.24%、绵羊乳蛋白质含量为5.25%、水牛乳蛋白质含量为4.18%,人乳泌乳初期酪蛋白与乳清蛋白比例为2:8、泌乳中期和后期酪蛋白与乳清蛋白比例为4:6,牛乳酪蛋白与乳清蛋白比例为8:2[1-2]。人乳与牛乳各酪蛋白成分间的含量和比例及乳清蛋白中的主要成分都存在很大差异,人乳乳清蛋白中乳铁蛋白的含量在100~300 mg/100 mL[3-4],牛乳中乳铁蛋白含量在20 mg/100 g以下[5],人乳中含有及其微量的β-乳球蛋白,但是β-乳球蛋白确是牛乳乳清的主要蛋白质[2]。准确测定不同乳蛋白组分的含量、研究乳蛋白成分的比例对优质乳制品研发、泌乳牛选育和婴幼儿配方乳粉蛋白质母乳化至关重要。
目前定量测定乳蛋白含量的方法主要有酶联免疫法、毛细管电泳法、高效液相色谱法和高效液相色谱串联质谱法,本文对这4类方法的原理、适用性和方法特点进行综述和分析(见表1),为乳蛋白组分的准确测定和方法筛选提供可靠的技术参考,为乳品营养研究、乳产品开发、婴幼儿配方粉优化提供理论支持。
表 1 乳蛋白不同定量测定方法的比对Table 1. Comparison of different quantitative determination methods of milk protein原理 主要前处理 方法特点 方法应用 酶联免疫法 乳蛋白抗原与酶标抗体特异性结合,利用酶催化反应显色,间接定量测定。 试样混匀或磷酸盐溶液稀释,离心处理。 前处理简单,所需试剂少,大批量样品和微量蛋白测定有优势。但不能同时测定不同乳蛋白组分的含量。 乳铁蛋白LOD为2 mg/100 g,回收率在101.6%~109%,RSD为5.34%[8];
酪蛋白线性范围0.5~13.5 μg/g,测定准确度99%[9];
β-乳球蛋白LOD为0.038 μg/mL,线性范围0.047~
1.50 μg/mL,相关系数0.9923,批次误差8.88%[11]。毛细管电
泳法在一定电压条件下,不同乳蛋白在缓冲液条件下的迁移速度不同而实现分离。 a.试样加入尿素、盐酸胍等进行变性处理;
b.试样调节pH4.6沉淀酪蛋白。分离快速,所需样品量少,高含量乳蛋白组分测定准确性高。检测灵敏度相对低。 五种乳蛋白组分相关系数均大于0.99,回收率88.1% ~
110.8%,RSD为1.76%~3.28%[14];乳铁蛋白LOD和LOQ分别为21、70 mg/100 mL,回收率为87%~112%,RSD4.4%~
12.1%[16]。高效液相
色谱法不同乳蛋白在流动相条件下与色谱柱固相载体的亲和洗脱不同而实现分离。 a.试样调节pH4.6沉淀酪蛋白;
b.试样经磷酸盐提取,亲和柱净化;
c.试样加入尿素、盐酸胍等进行变性处理。此类方法应用广泛,根据测定目标蛋白选择不同的前处理方法,可得到良好的液相分离结果。检测灵敏度较高。 4种乳清蛋白组分LOD为0.002 g/L,相关系数大于0.99,回收率93.0%~97.0%[21]。乳铁蛋白LOD和LOQ分别为0.57、
1.90 mg/L,回收率分别为88.3%、90.2%和95.1%[26];IgG线性范围0.2~5.0 mg/mL,回收率86.0%~117.7%[30]。高效液相色
谱串联质谱法胰蛋白酶酶解蛋白质生成肽段,根据特异肽段含量间接测定乳蛋白组分含量。 试样经二硫苏糖醇还原,碘代乙酰胺烷基化,胰蛋白酶酶解。 检测灵敏度高,不需乳蛋白对照品即可定量,可实现多种乳蛋白的同时测定。前处理复杂费时,测定成本高。 乳铁蛋白LOD和LOQ分别为3.8、11 mg/kg,回收率74.5%~
103.6%,RSD7.7%[35];线性范围α-乳白蛋白40~1000 nmol/L
和β-乳球蛋白80~2000 nmol/L,LOQ为0.02 g/100 g; 加标回收率为84.7%~95.6%,RSD为1.6%~5.8%[36]。β-乳球蛋白线性范围2~100 μmol/L,LOD和LOQ分别为0.2、0.6 mg/100 mL,
RSD小于6.2%[38]。1. 酶联免疫法(ELISA)
1.1 方法原理
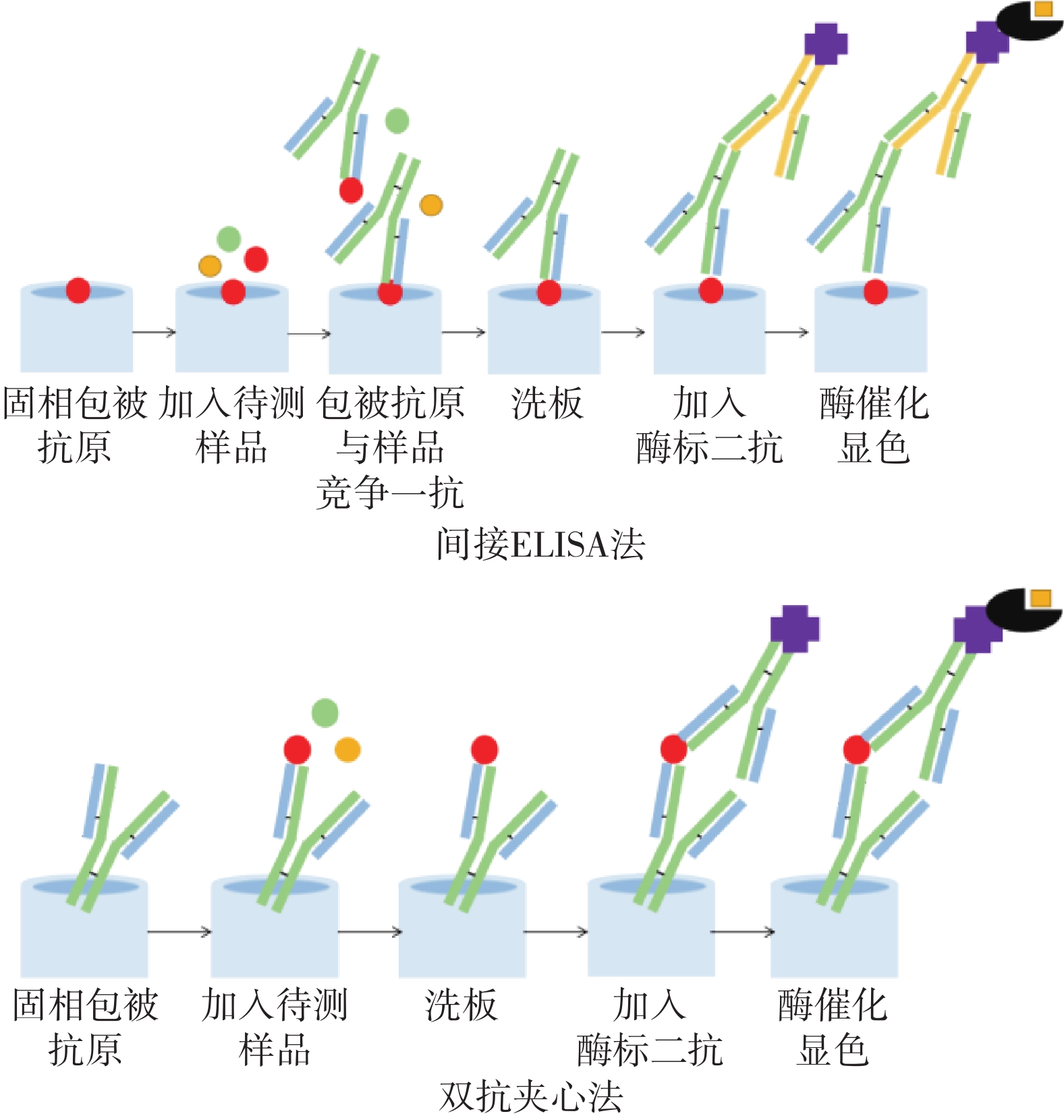
酶联免疫法采用乳蛋白分子作为抗原特异性诱导产生抗体,并制备相应的酶标抗体,根据抗原与酶标抗体特异性亲和,利用酶的催化反应使测定液显色,目标物的量与酶的量等比例,故可根据颜色反应的深浅来进行定性或定量分析。
酶联免疫法测定乳蛋白含量的方式主要有间接竞争法和双抗夹心法[6-13]。如图1所示,间接竞争法采用目标乳蛋白为包被抗原,乳蛋白抗体为一抗,酶标记抗体为二抗,样品中目标蛋白与包被的目标蛋白进行竞争性免疫结合抗体,通过显色反应和标准工作曲线计算乳蛋白含量。双抗夹心法以乳蛋白为抗原制备相应的抗体(一抗)进行包被固定,加入待测定样品溶液,洗板后加入辣根过氧化物酶标记的乳蛋白抗体(酶标二抗),显色反应后测定吸光度,根据标准工作曲线进行计算乳蛋白含量。
1.2 方法应用
目前不同乳源的乳蛋白酶联免疫试剂盒均有商业化产品,如人乳中酪蛋白、乳白蛋白、乳铁蛋白、骨桥蛋白和牛乳中骨桥蛋白含量[6]。
袁水林等[7]通过对β-乳球蛋白进行包被,制备β-乳球蛋白抗体和羊抗兔IgG过氧化物酶二抗,建立了牛乳中β-乳球蛋白含量间接ELISA测定方法,并以高效液相色谱法做为比对方法,验证了间接ELISA方法的可靠性。β-乳球蛋白是乳清蛋白中的主要成分,也是主要的乳蛋白过敏源,通过调整包被抗体浓度ELISA方法可应用于食品中β-乳球蛋白过敏源的测定。吴春香等[8]采用商品化酶联免疫试剂盒研究了婴儿配方奶粉中乳铁蛋白含量测定的准确性,通过验证试剂盒法的检出限、加标回收率、稳定性,与标签标示值、高效液相色谱法测定结果进行比对,确定酶联免疫法测定乳粉中乳铁蛋白含量准确、可靠,方法检出限为(LOD)2 mg/100 g,能够满足检测需求。
酪蛋白是牛乳中的主要蛋白质,分为α-酪蛋白、β-酪蛋白、κ-酪蛋白、γ-酪蛋白等单体,于艳丽等[9]采用ELISA方法测定了市售乳粉中酪蛋白含量,测定结果与标签标示值一致性达到99%以上,本研究直接测定酪蛋白总量,涵盖了α-酪蛋白、β-酪蛋白和κ-酪蛋白酪蛋白组分。宋宏新等[10]、赵金龙[11]等分别对牛乳中κ-酪蛋白和β-乳球蛋白的ELISA方法进行研究,从抗体选择、抗体包被浓度、反应条件优化等方面对酶联免疫法测定乳蛋白进行系统研究,验证了方法的可靠性。Michaela等[13]采用多克隆抗体模式针对天然α-酪蛋白、β-酪蛋白和κ-酪蛋白及其加热处理后的形式建立了酶联免疫测定方法,得到良好的测定特异性和抗干扰特性,同时研究了试剂盒内与试剂盒间的差异,确保了方法的稳定可靠。使用ELISA方法直接测定酪蛋白总量时,不同样品酪蛋白单体比例对酪蛋白总量会有影响。
1.3 方法特点
酶联免疫法测定乳蛋白含量的优势:所需样品量少(一般加样量为10~50 µL);样品前处理简单(直接混匀或稀释后混匀);酶联免疫法在批量化测定时具有显著优势,自动化程度高,测定快速;酶联免疫法具有高度的特异性,不同乳蛋白的交叉反应影响小,对微量蛋白组分的测定准确度高,在测定乳蛋白过敏源时适用性强。
由于酶联免疫法在乳蛋白测定中具有高度的专一性,不能同时对多个乳蛋白组分进行准确定量,不同乳蛋白组分的准确测定需要不同试剂盒进行分析;除此之外,酶联免疫试剂盒的准确性与所包被抗原或抗体的纯度和稳定性有直接关系,不同商品化厂家的产品测定结果会存在一定差异。
2. 毛细管电泳法(CE)
2.1 方法原理
毛细管电泳法分离乳及乳制品中乳蛋白组分是采用具有涂层的毛细管为乳蛋白分离载体,通过施加电压,不同乳蛋白在缓冲液条件下的迁移速度不同而实现分离,采用紫外检测器测进行定量测定。缓冲液中往往加入尿素溶液使蛋白质变性以达到良好的分离。
2.2 方法应用
乳蛋白的主要组分α-乳白蛋白、β-乳球蛋白、α-酪蛋白、β-酪蛋白、κ-酪蛋白、血清白蛋白、乳铁蛋白和免疫球蛋白G等在毛细管电泳中能够得到有效的分离和准确定量,经过验证,方法精密度RSD均小于5%,加标回收率为83.7%~113.4%,各乳蛋白在20 min内能够达到有效分离,且方法稳定可靠[14-16]。
除了乳蛋白各组分含量的测定,毛细管电泳还可有效分离乳蛋白组分的变异体,分析不同乳源乳蛋白的差异。冯慿等[17]研究了毛细管电泳分离A1-β-酪蛋白、A2-β-酪蛋白和B-β-酪蛋白变异体,通过方法线性、精密度、回收率等方法学验证,得到了良好的β-酪蛋白分离条件,该方法适用于液态牛乳和乳粉中A2-β-酪蛋白和总酪蛋白含量的测定,也为各乳蛋白变异体的含量和功能研究提供可能。Jasmina等[18]和Adel等[19]采用毛细管电泳法对驴乳和单峰驼乳中α-乳白蛋白、β-乳球蛋白、血清白蛋白、αs1-酪蛋白、αs2-酪蛋白、β-酪蛋白、κ-酪蛋白、乳铁蛋白、溶菌酶等蛋白组分进行有效分离,结果得到单峰驼乳与牛乳蛋白组分差异很大。
乳蛋白在生产加工过程会有不同程度的变性,热变性的α-乳白蛋白、β-乳球蛋白在pH4.6时与酪蛋白共沉淀,丁晓静等[20]采用毛细管电泳法系统的分析了牛初乳、原料乳及不同乳制品中α-乳白蛋白、β-乳球蛋白A及β-乳球蛋白B的含量,在样品处理阶段采用酸沉淀,取上清液进行毛细管电泳分析,结果得到牛初乳、原料乳中3种乳清蛋白组分的含量高于酸奶、UHT牛乳、复原乳和乳粉,明确了不同加工方式乳蛋白的变性比率。
2.3 方法特点
毛细管电泳法有效分离乳蛋白组分所需时间短、分析效率高,8种主要乳蛋白的分离时间在20 min内完成。方法所需样品和缓冲液使用量少,上样量一般为纳升级别,几毫升缓冲液就可完成一个测定程序。由于毛细管电泳优良的分离效率,同时测定不同乳蛋白组分含量,高丰度乳蛋白组分的测定准确性会高于低丰度蛋白测定准确性。纳升级别的进样量会限制测定方法灵敏度。
3. 高效液相色谱法(HPLC)
高效液相色谱法定量测定乳蛋白组分主要是酸沉淀后测定乳清蛋白、特异性亲和净化蛋白组分、变性处理测定酪蛋白和乳清蛋白三种形式。
3.1 酸沉淀测定乳清蛋白
乳样品经过溶解、调节pH4.6沉淀酪蛋白等前处理,采用高效液相色谱系统经过流动相梯度洗脱,分离乳样品中各乳清蛋白组分后进行定量测定。
采用乳中酪蛋白pH4.6等电点,热变性α-乳白蛋白和β-乳球蛋白与酪蛋白共沉淀的特性,研究活性乳清蛋白组分和含量[21-23],经过验证α-乳白蛋白、β-乳球蛋白A、β-乳球蛋白B和牛血清白蛋白,检出限为0.002 g/L,决定系数R2大于0.99,回收率93.0%~97.0%,可以准确测定乳及乳制品中活性乳清蛋白组分的含量。
Efstathia等[24]研究了不同种类乳中乳铁蛋白含量,使用牛乳来源乳铁蛋白对照,在液相条件下,作者采用比对各种乳样品和对照品光谱图及在样品测定液中加入对照品确定目标峰位置的方法排除不同乳清蛋白组分对乳铁蛋白的干扰,建立了不同乳中乳铁蛋白定性定量分析方法。Cai等[25]采用酸沉淀超高效液相色谱分离测定分析248份来自中国不同地区的人乳乳铁蛋白,得到不同泌乳阶段人乳中乳铁蛋白含量在102~385 mg/100 mL。
3.2 特异性亲和净化蛋白组分
3.2.1 方法原理
肝素是一种带多个负电荷的含硫酸酯的酸性多糖,乳中非热变性的乳铁蛋白可通过亲和层析结合肝素,通过磷酸盐淋洗和盐溶液洗脱,实现乳铁蛋白的分离[26-27]。金黄色葡萄球菌等细菌表面的蛋白质与免疫球蛋白IgG分子Fc部分以非免疫学的方式进行高选择性的特异性结合,乳样品中的免疫球蛋白经过磷酸盐提取,由IgG净化柱分离后测定含量[28-29]。
3.2.2 方法应用
乳样品经过溶解提取后,通过乳蛋白组分的特异性结合性质进行净化处理,由高效液相色谱对单一蛋白组分进行定量测定,已报道应用此类方法的有乳铁蛋白和免疫球蛋白G。
食品安全国家标准食品中乳铁蛋白的测定(征求意见稿)高效液相色谱法原理即样品中非热变性的乳铁蛋白经磷酸盐提取,肝素亲和柱净化,C4色谱柱(300 Å,5 μm,4.6 mm×250 mm)分离测定。Chen等[30]和贾云虹等[31]在利用肝素亲和柱分离乳铁蛋白前,使用乙酸或磷酸调节乳样品至pH4.6,除去酪蛋白和变性的乳清蛋白,通过响应面设计,确定了肝素亲和柱富集乳铁蛋白的最佳条件,能够得到单一对称的乳铁蛋白色谱峰,得到方法检出限和定量限(LOQ)分别为0.57和1.90 mg/L,不同水平添加量回收率在86%~99%之间,方法精密度相对标准偏差(RSD)为3.4%,建立了简便、快捷的婴儿配方奶粉中乳铁蛋白含量测定方法,可以满足生产企业日常检测和质量监督部门监督产品质量的要求。
孔祥虹等[32]建立了配方粉中免疫球蛋白G的高效液相测定方法,样品提取后经protein G亲和柱净化、凝胶色谱液相分离,经方法学验证,表明样品在0.2~5.0 mg/mL范围内线性相关性良好,加标回收率为86.0%~117.7%,能够满足奶粉中免疫球蛋白G含量的测定。
3.3 变性处理测定乳蛋白
样品中乳蛋白经盐酸胍、尿素、二硫苏糖醇等溶液变性处理后,破坏乳蛋白间的聚合,采用高效液相色谱梯度洗脱,优化仪器条件和参数达到各蛋白组分的有效分离。
王浩等[33]通过优化色谱柱型号、柱温、流动相梯度比例等条件建立了κ-酪蛋白、αS2-酪蛋白、αS1-酪蛋白、β-酪蛋白、α-乳白蛋白、β-乳球蛋白B和β-乳球蛋白A共7种蛋白成分的有效分离方法,回收率达88.9%~97.1%,相对标准偏差为0.8%~5.1%。豆剑伟等[34]使用C8色谱柱分别建立了分离测定乳中4种酪蛋白组分的方法,通过优化检测波长、流速、柱温等条件,4种酪蛋白组分得到有效的分离,加标回收率分别为92.74%~98.48%和95.2%~100.6%,测定准确性良好。
3.4 方法特点
乙酸或盐酸沉淀前处理操作快速简便,去除酪蛋白后,乳清蛋白组分得到更好的分离。α-乳白蛋白、β-乳球蛋白和乳铁蛋白对热处理敏感,活性乳蛋白含量的测定可以判断乳的热变性程度和加工处理强度。未进行变性处理的测定方式,分离后乳蛋白具有可制备特性。但文献中采用的乳蛋白对照品纯度范围在70%~95%,乳蛋白纯度的不确定性限制了乳蛋白的准确定量。样品与对照品中乳蛋白不同变异体的存在也为样品中乳蛋白的准确定性定量和有效分离带来困难。乳样品中微量蛋白组分的测定容易受酪蛋白、α-乳白蛋白和β-乳球蛋白等高含量蛋白组分的影响,在液相色谱图中不易检出或得到较小的色谱峰,使准确定量受限。
4. 高效液相色谱串联质谱法(HPLC-MS/MS)
4.1 方法原理
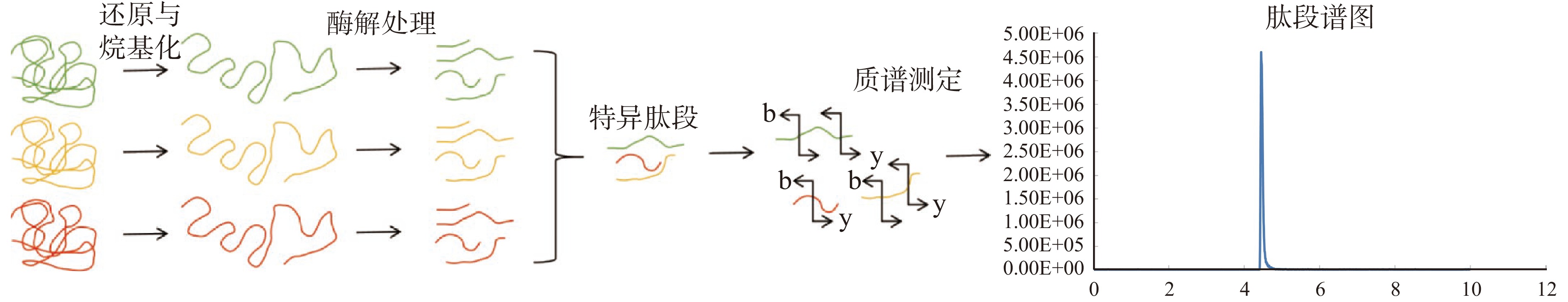
利用蛋白组学定量测定乳蛋白组分是采用胰蛋白酶特异性酶切目标蛋白生成肽段,通过定量测定目标蛋白肽段含量,根据肽段与乳蛋白等摩尔比例的关系,计算乳蛋白组分含量。高效液相色谱串联质谱法测定乳蛋白示意图如图2所示。
胰蛋白酶特异性酶切氨基酸链中精氨酸和赖氨酸位点的C末端(酶切位点后为脯氨酸时则失去酶切能力)生成多条肽段,使用高分辨质谱测定和分析不同肽段的氨基酸组成、长度、质谱信号强度、肽段特异性等,优选氨基酸个数为7~20个且不含有甲硫氨酸、半胱氨酸和色氨酸等易被氧化氨基酸的肽段作为定量测定特异肽段[35]。
4.2 方法应用
质谱法测定乳蛋白组分含量在定量测定时的校正方式主要有4种。合成同位素标记特异性肽段(和同位素标记标签肽)进行内标法校正,这种方式综合校正了酶解效率、前处理过程中的损失和基质效应[36-38]。Zhang等 [39]和Li等 [40]分别筛选了牛乳铁蛋白和骆驼乳铁蛋白特异肽段LRPVAAEIYGTK、DVTVLDNTDGK,通过合成内标特异肽段和乳铁蛋白内标肽段进行内标法校正,方法学研究结果得到不同牛乳制品乳铁蛋白和乳铁蛋白内标肽段的酶解效率均能达到90%以上,乳铁蛋白不同含量水平的加标回收测定结果在87.8%~104.7%,日内和日间精密度测定RSD均小于8%;骆驼乳铁蛋白添加量6、30和60 mg/100 g的测定回收率分别为74.5%、103.6%和97.1%,具有良好的方法准确性。杜鹃等[41]在建立乳清蛋白粉中α-乳白蛋白和β-乳球蛋白的质谱测定方法时分别选定了选定VGINYWLAHK和IDALNENK为目标蛋白质特异性肽段,采用同位素标记特异性肽段VGI*NYWL*AHK和I*DAL*NENK进行内标校正,经过方法学优化得到良好的方法回收率和测定准确性。
在样品测定液中加入已知量的外源非目标蛋白酶解液作为内标进行校正。冯小燕等[42]在研究α-酪蛋白的液相色谱-质谱测定方法时采用卵清蛋白酶解液中的特征离子对673.3/222.9作为内标离子对,用来控制不同样品体系、不同进样批次的离子化效率差异。此文献未给出方法回收率或者与同位素标记肽段结果的比较,不能判断外源非目标蛋白特征离子对作为内标方法的准确性。
加入非目标肽段的同位素标记特异性内标肽或者合成的非目标同质肽段进行内标法定量,校正了前处理过程中肽段的损失和基质效应。袁明美等[43]在研究牛乳及其制品中β-乳球蛋白的定量测定方法时,采用VLVLDTDYK为目标肽段,ETTVFENLPEK*为同位素内标肽段,方法学验证结果日内与日间精密度均小于8%,回收率结果91.5%~100.2%,验证了加入非目标肽段的特异性内标肽进行内标法定量的可靠性。詹丽娜等[44]在定量研究食品中牛乳过敏性酪蛋白时,αs1-酪蛋白、αs2-酪蛋白、β-酪蛋白、κ-酪蛋白定量肽段分别为HQGLPQEVLNENLLR、FALPQYLK、VLPVPQK和SPAQILQWQVLSNTVPAK,采用在目标肽段中加入一个氨基酸作为内标物,其中一组内标物为HQGGLPQEVLNENLLR、FVALPQYLK、SPAQILQWQVVLSNTVPAK和VALPVPQK,另一组内标物为HQGILPQEVLNENLLR、FIALPQYLK、SPAQILQWQALSNTVPAK和VILPVPQK,经过前处理条件的优化、方法验证和食品中牛乳酪蛋白过敏源测定得到可靠的测定稳定性。
经加标回收等方法学验证后直接用特异肽段外标法定量,在优化了前处理条件和方法学验证后,外标法能够得到准确的定量测定结果[45]。王震[46-47]以牛乳α-乳白蛋白和β-乳球蛋白为研究对象,系统地分析了不同质谱仪器、同位素内标特异性肽段与目标肽浓度比、进样小瓶、滤膜等条件对质谱响应信号的影响,结果得到不同质谱仪器和不同内标特异性肽段与标签肽浓度比对α-乳白蛋白内标特异性肽段的质谱响应值影响很大,RSD分别为70.89%和20.77%,β-乳球蛋白的内标特异性肽段的质谱响应值很稳定,RSD分别为5.61%和8.30%,不同材质进样小瓶、滤膜等前处理条件因素质谱响应值也得到α-乳白蛋白的内标特异性肽段差别较大,β-乳球蛋白的内标特异性肽段的质谱响应值差别很小;分析结论为同位素内标的质谱响应值变化主要受肽段氨基酸组成的影响;研究者分别利用内标法和外标法分析了15种婴幼儿奶粉中两种乳清蛋白的含量,得到α-乳白蛋白含量两种方法的结果比值在115.53%~151.94%,β-乳球蛋白含量98.35%~132.21%,且目标蛋白样品处理液浓度越低两种方法的结果越接近。
4.3 方法特点
蛋白组学在乳蛋白组分测定中的应用解决了无商业化乳蛋白组分标准品和标准品纯度低的问题。质谱的高通量、高灵敏度特点,使得多种成分的同时测定成为可能,为乳蛋白含量的测定提供一种准确的测定方法。非同位素标记法测定乳蛋白含量经过方法学验证和比对,均能得到满意的测定结果,也使得质谱法在不同乳源乳蛋白组分含量测定中适用性更强。
质谱法测定乳蛋白含量前处理繁琐,乳蛋白需要经过变性、烷基化和长时间的酶解;胰蛋白酶的纯度会直接影响肽段的含量和序列长度,优选质谱级和测序级胰蛋白酶;其中合成同位素标记特异性肽段与同位素标记标签肽显著增加测定成本;质谱仪检测器运行成本和测定环境要求严格。
5. 结论与展望
乳及乳制品中蛋白组分含量差异大,液态牛乳β-酪蛋白含量在1.0 g/100 g左右,乳铁蛋白含量在2~20 mg/100 g,碱性磷酸酶、乳过氧化物酶等蛋白酶类含量在µg/100 g水平或者更低。筛选合适的方法是准确测定不同含量乳蛋白成分的关键因素。乳蛋白在加工过程中会不同程度的变性,α-乳白蛋白、β-乳球蛋白和乳铁蛋白等对热敏感,准确测定乳制品中活性乳蛋白含量,对乳蛋白发挥生物活性更具意义。本文从测定方法原理、前处理、仪器和测定参数、方法特点等方面综述了目前应用较多乳蛋白测定方法:酶联免疫法、毛细管电泳法、高效液相色谱法和高效液相色谱串联质谱法,为不同乳蛋白成分的准确测定提供方法筛选依据。
随着乳蛋白功能特性研究的深入,在婴幼儿配方粉、保健食品中添加了乳铁蛋白、免疫球蛋白、乳脂肪球膜蛋白等功能性成分的产品往往具有更好的消费倾向性。准确测定乳及乳制品中蛋白组分的含量,建立标准测定方法,是乳品研发和质量控制与监管的重要环节。乳蛋白成分复杂,不同蛋白组分的分子量和含量都存在很大差异,蛋白组分的糖基化和磷酸化修饰程度、乳蛋白间的聚合与交联、发酵与加热等加工处理方式对蛋白含量有不同程度的影响,这些因素都对乳蛋白组分的准确定量带来不小的挑战。随着乳蛋白测定技术的发展,精准的样品前处理、乳蛋白理化和生化特性的研究、分离净化方法的联合使用[48-50]、高通量质谱检测器的应用,将会对乳蛋白组分准确定量提供更多可能性。
-
表 1 乳蛋白不同定量测定方法的比对
Table 1 Comparison of different quantitative determination methods of milk protein
原理 主要前处理 方法特点 方法应用 酶联免疫法 乳蛋白抗原与酶标抗体特异性结合,利用酶催化反应显色,间接定量测定。 试样混匀或磷酸盐溶液稀释,离心处理。 前处理简单,所需试剂少,大批量样品和微量蛋白测定有优势。但不能同时测定不同乳蛋白组分的含量。 乳铁蛋白LOD为2 mg/100 g,回收率在101.6%~109%,RSD为5.34%[8];
酪蛋白线性范围0.5~13.5 μg/g,测定准确度99%[9];
β-乳球蛋白LOD为0.038 μg/mL,线性范围0.047~
1.50 μg/mL,相关系数0.9923,批次误差8.88%[11]。毛细管电
泳法在一定电压条件下,不同乳蛋白在缓冲液条件下的迁移速度不同而实现分离。 a.试样加入尿素、盐酸胍等进行变性处理;
b.试样调节pH4.6沉淀酪蛋白。分离快速,所需样品量少,高含量乳蛋白组分测定准确性高。检测灵敏度相对低。 五种乳蛋白组分相关系数均大于0.99,回收率88.1% ~
110.8%,RSD为1.76%~3.28%[14];乳铁蛋白LOD和LOQ分别为21、70 mg/100 mL,回收率为87%~112%,RSD4.4%~
12.1%[16]。高效液相
色谱法不同乳蛋白在流动相条件下与色谱柱固相载体的亲和洗脱不同而实现分离。 a.试样调节pH4.6沉淀酪蛋白;
b.试样经磷酸盐提取,亲和柱净化;
c.试样加入尿素、盐酸胍等进行变性处理。此类方法应用广泛,根据测定目标蛋白选择不同的前处理方法,可得到良好的液相分离结果。检测灵敏度较高。 4种乳清蛋白组分LOD为0.002 g/L,相关系数大于0.99,回收率93.0%~97.0%[21]。乳铁蛋白LOD和LOQ分别为0.57、
1.90 mg/L,回收率分别为88.3%、90.2%和95.1%[26];IgG线性范围0.2~5.0 mg/mL,回收率86.0%~117.7%[30]。高效液相色
谱串联质谱法胰蛋白酶酶解蛋白质生成肽段,根据特异肽段含量间接测定乳蛋白组分含量。 试样经二硫苏糖醇还原,碘代乙酰胺烷基化,胰蛋白酶酶解。 检测灵敏度高,不需乳蛋白对照品即可定量,可实现多种乳蛋白的同时测定。前处理复杂费时,测定成本高。 乳铁蛋白LOD和LOQ分别为3.8、11 mg/kg,回收率74.5%~
103.6%,RSD7.7%[35];线性范围α-乳白蛋白40~1000 nmol/L
和β-乳球蛋白80~2000 nmol/L,LOQ为0.02 g/100 g; 加标回收率为84.7%~95.6%,RSD为1.6%~5.8%[36]。β-乳球蛋白线性范围2~100 μmol/L,LOD和LOQ分别为0.2、0.6 mg/100 mL,
RSD小于6.2%[38]。 -
[1] 杨月欣, 葛可佑. 中国营养科学全书[M]. 北京: 人民卫生出版社, 2019: 473. YANG Y X, GE K Y. Encyclopedia of nutrition science[M]. Beijing: People’s Medical Publishing House Co., Ltd., 2019: 473.
[2] 郭本恒. 乳品化学[M]. 北京: 中国轻工业出版社, 2001: 15-16 GUO B H. Dairy chemistry[M]. Beijing: China Light Industry Press Ltd., 2001: 15-16.
[3] KE X, CHEN Q, PAN X D, et al. Quantification of lactoferrin in breast milk by ultra-high performance liquid chromatography-tandem mass spectrometry with isotopic dilution[J]. The Royal Society of Chemistry,2016,6:12280−12285.
[4] YANG Z Y, JIANG R L, CHEN Q, et al. Concentration of lactoferrin in human milk and its variation during lactation in different Chinese populations[J]. Nutrients,2018,10:1235−1245. doi: 10.3390/nu10091235
[5] ÖZENÇ E, ŞEKER E, ACAR D B, et al. Milk lactoferrin concentrations in anatolian buffaloes with and without subclinical mastitis[J]. Buffalo Bulletin,2019,38(2):291−298.
[6] SIGNE B, LOTTE N J, STEFFEN H, et al. Osteopontin levels in human milk vary across countries and within lactation period: Data from a multicenter study[J]. Journal of Pediatric Gastroenterology and Nutrition,2018,67(2):250−256. doi: 10.1097/MPG.0000000000002004
[7] 袁水林, 熊鼎, 陈红兵, 等. 间接竞争ELISA法检测牛乳中β-乳球蛋白含量的准确性评价[J]. 食品科学,2014,35(18):100−104. [YUAN S L, XIONG D, CHEN H B, et al. Evaluation of the accuracy of indirect competitive ELISA used to detect milk β-lactoglobulin[J]. Food Science,2014,35(18):100−104. doi: 10.7506/spkx1002-6630-201418020 [8] 吴春香, 刘志楠, 赵源, 等. 酶联免疫吸附法快速检测婴儿配方奶粉中乳铁蛋白含量[J]. 食品安全质量检测学报,2018,9(4):803−807. [WU C X, LIU Z N, ZHAO Y, et al. Rapid detection of lactoferrin content in infant formula by enzyme-linked immunosorbent assay[J]. Journal of Food Safety and Quality Inspection,2018,9(4):803−807. doi: 10.3969/j.issn.2095-0381.2018.04.021 [9] 于艳丽, 蔡松铃. ELISA法快速检测婴儿配方奶粉中酪蛋白含量[J]. 食品安全质量检测学报,2017,8(8):2932−2935. [YU Y L, CAI S L. Detection of casein content in infant formula by ELISA[J]. Journal of Food Safety and Quality Inspection,2017,8(8):2932−2935. doi: 10.3969/j.issn.2095-0381.2017.08.016 [10] 宋宏新, 韩波, 李珊, 等. 检测牛乳κ-酪蛋白的间接竞争ELISA法与间接ELISA法比较[J]. 中国畜牧兽医,2018,45(4):1114−1119. [SONG H X, HAN B, LI S, et al. Comparison between indirect competitive ELISA and indirect ELISA in detecting bovine κ-casein[J]. Chinese Journal of Animal Husbandry and Veterinary Medicine,2018,45(4):1114−1119. [11] 赵金龙. β-乳球蛋白两种酶联免疫检测方法的建立和比较[D]. 天津: 天津科技大学, 2010. ZHAO J L. Establishment and comparison of two enzyme-linked immunoassay methods for β-lactoglobulin[D]. Tianjin: Tianjin University of Science and Technology, 2010.
[12] SCHACK L, LANGE A, KELSEN J, et al. Considerable variation in the concentration of osteopontin in human milk, bovine milk, and infant formulas[J]. Journal of Dairy Science,2009,92(11):5378−5385. doi: 10.3168/jds.2009-2360
[13] VÍTKOVÁ M, RAUCH P, FUKAL L. Optimisation of indirect competitive ELISA of α-, β-, and κ-caseins for the recognition of thermal and proteolytic treatment of milk and milk products[J]. Food and Agricultural Immunology,2002,36:53−62.
[14] 田兰, 陈春丽, 马晓丽, 等. 毛细管电泳法对乳及乳制品中乳源蛋白的测定[J]. 食品研究与开发,2013,34(4):81−84. [TIAN L, CHEN C L, MA X L, et al. Milk proteins determination in milk and milk products by capillary electrophoresis[J]. Food Research and Development,2013,34(4):81−84. doi: 10.3969/j.issn.1005-6521.2013.04.024 [15] WU R G, WANG Z P, ZHAO W F, et al. Multi-dimension microchip-capillary electrophoresis device for determination of functional proteins in infant milk formula[J]. Journal of Chromatography A,2013,1304:220−226. doi: 10.1016/j.chroma.2013.06.073
[16] ZHAO L G, YOU J, LIANG Z H. Determination of bovine lactoferrin in milk by cation exchange chromatography and dynamic coating capillary electrophoresis[J]. Journal of Analysis and Measurement,2014,33(3):339−343.
[17] 冯慿, 丁晓静, 高铁, 等. 毛细管区带电泳测定液态奶及奶粉中的A2β-酪蛋白及总β-酪蛋白[J]. 色谱,2020,38(6):722−729. [FENG P, DING X J, GAO T, et al. Determination of A2β-casein and total β-casein in cow milk and milk powder by capillary zone electrophoresis[J]. Chinese Journal of Chromatography,2020,38(6):722−729. [18] GUBIĆ J, TOMIĆ J, TORBICA A. Characterization of several milk proteins in domestic balkan donkey breed during lactation, using lab-on-a-chip capillary electrophoresis[J]. Chemical Industry & Chemical Engineering Quarterly,2016,22(1):9−15.
[19] ADEL O, NIAMH H, MARIA J O C. Quantification of major camel milk proteins by capillary electrophoresis[J]. International Dairy Journal,2016,58:31−35. doi: 10.1016/j.idairyj.2016.01.015
[20] 丁晓静, 杨媛媛, 李芸, 等. 毛细管电泳法对乳及乳制品中真蛋白的测定[J]. 食品科学,2010,31(22):361−366. [DING X J, YANG Y Y, LIU Y, et al. Use of capillary electrophoresis for determination of genuine proteins in milk and milk products[J]. Food Science,2010,31(22):361−366. [21] 朱鑫鑫, 刘晓辉, 赵征, 等. PURPLISH法分离和定量测定未变性的乳清蛋白成分[J]. 中国乳品工业,2012,40(5):51−54. [ZHU X X, LIU X H, ZHAO Z, et al. RP-HPLC for separation and quantitative determination of nature whey protein components[J]. China Dairy Industry,2012,40(5):51−54. doi: 10.3969/j.issn.1001-2230.2012.05.013 [22] 陈美霞. 不同热处理条件下牛奶中热敏指标与功能性蛋白变化规律研究[D]. 北京: 中国农业科学研究院, 2017. CHEN M X. Changes of heat indicators and functional proteins in milk under various heat treatments[D]. Beijing: Chinese Academy of Agricultural Sciences, 2017.
[23] 河北省奶业协会. T/DAHEB007-2020 活性蛋白牛乳(牛奶)[S]. 2020. Hebei Dairy Association. T/DAHEB007-2020 Active protein milk (milk)[S]. 2020.
[24] EFSTATHIA T, ARHONTOULA C, DIMITRA H, et al. A rapid HPLC method for the determination of lactoferrin in milk of various species[J]. Dairy Research,2019,86(2):238−241. doi: 10.1017/S0022029919000189
[25] CAI X K, DUAN Y F, LI Y, et al. Lactoferrin level in breast milk: A study of 248 samples from eight regions in China[J]. Food & Function,2018,9(8):4216−4222.
[26] WANG B, TIMILSENA Y P, BLANCH E, et al. Lactoferrin: Structure, function, denaturation and digestion[J]. Food Science and Nutrition,2017:580−596.
[27] INDIRA F, MARÍA D P, CELIA C, et al. Effffect of technological treatments on bovine lactoferrin: An overview[J]. Food Research International,2018,106:173−182. doi: 10.1016/j.foodres.2017.12.016
[28] HIDEKI W, HIROYUKI M, AYAKO O, et al. Optimizing pH response of affinity between protein G and IgG Fc[J]. Journal of Biological Chemistry,2009,284:12373−12383. doi: 10.1074/jbc.M809236200
[29] ROMAIN O, PAUL W, THIERRY M, et al. Single-step protein A and protein G avidity purification methods to support bispecific antibody discovery and development[J]. mAbs,2019,11(8):1464−1478. doi: 10.1080/19420862.2019.1660564
[30] CHEN M X, WEN F, ZHANG Y D, et al. Determination of native lactoferrin in milk by HPLC on HiTrap TM Heparin HP column[J]. Food Analytical Methods,2019,12(11):2518−2526. doi: 10.1007/s12161-019-01572-x
[31] 贾云虹, 宋晓青, 杨凯, 等. 高效液相色谱法测定婴儿配方奶粉中乳铁蛋白含量[J]. 中国奶牛,2015(13):49−52. [JIA Y H, SONG X Q, YANG K, et al. Determination of lactoferrin in infant formula milk powder by high performance liquid chromatography[J]. Chinese Dairy Cows,2015(13):49−52. doi: 10.3969/j.issn.1004-4264.2015.13.013 [32] 孔祥虹, 姜敏, 何强, 等. 高效凝胶色谱法测定配方奶粉中免疫球蛋白G[J]. 分析试验室,2017,36(4):456−459. [KONG X H, JIANG M, HE Q, et al. Quantitation of immunoglobulin G in formula milk powder by high performance gel permeation chromatography[J]. Chinese Journal of Analytics,2017,36(4):456−459. [33] 王浩, 张志国, 常彦忠, 等. RP-HPLC法对乳制品中主要牛奶蛋白的分离及定量测定[J]. 食品科学,2009,30(24):376−380. [WANG H, ZHANG Z Q, CHANG Y Z, et al. Isolation and quantification of main milk proteins in dairy products with reverse-phase HPLC[J]. Food Science,2009,30(24):376−380. doi: 10.3321/j.issn:1002-6630.2009.24.085 [34] 豆剑伟, 袁永俊, 刘纳, 等. 高效液相色谱法测定酪蛋白组分[J]. 食品与发酵科技,2016,52(4):90−92,101. [DOU J W, YUAN Y J, LIU N, et al. Determination casein subunits by high performance liquid chromatography[J]. Food Science and Technology,2016,52(4):90−92,101. [35] KE X, ZHANG J S, LAI S Y, et al. Quantitative analysis of cow whole milk and whey powder adulteration percentage in goat and sheep milk products by isotopic dilution-ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Anal Bioanal Chem,2017,409:213−224. doi: 10.1007/s00216-016-9987-9
[36] HU B, ZHANG J H, JIANG Y R, et al. Quantitative determination of osteopontin in bovine, buffalo, yak, sheep and goat milk by ultra-high performance liquid chromatography-tandem mass spectrometry and stable isotope dimethyl labeling[J]. Food Chemistry,2020:128489. doi: 10.1016/j.foodchem.2020.128489
[37] 王洋, 武利庆, 段非. 一种测定奶粉中β-乳球蛋白含量的方法: CN 103995077A[P]. 2014-08-20. WANG Y, WU L Q, DUAN F. A method for determination of β-lactoglobulin content in milk powder: CN 103995077A[P]. 2014-08-20.
[38] 任一平, 赖世云, 张京顺. 一种牛α乳白蛋白的定量检测方法: CN 102590413A[P]. 2012-07-18. REN Y P, LAI S Y, ZHANG J S. A method for quantitative detection of bovine α-lactoalbumin: CN 102590413A[P]. 2012-07-18.
[39] ZHANG J S, LAI S Y, CAI Z X, et al. Determination of bovine lactoferrin in dairy products by ultra-high performance liquid chromatography–tandem mass spectrometry based on tryptic signature peptides employing an isotope-labeled winged peptide as internal standard[J]. Analytica Chimica Acta,2014,829:33−39. doi: 10.1016/j.aca.2014.04.025
[40] LI X, LI Z M, XU E M, et al. Determination of lactoferrin in camel milk by ultrahigh-performance liquid chromatography-tandem mass spectrometry using an isotope-labeled winged peptide as internal standard[J]. Molecules,2019,24(22):4199−4210.
[41] 杜娟, 郑云鹏, 董洪涛, 等. 超高效液相色谱-串联三重四极杆质谱法测定乳清蛋白粉中α-乳白蛋白和β-乳球蛋白[J]. 分析测试学报,2020,39(7):900−905. [DU J, ZHENG Y P, DONG H T, et al. Determination of α-lactalbumin and β-lactoglobulin in whey powder by ultra performance liquid chromatography-triple quadrupole tandem mass spectrometry[J]. Journal of Analysis and Measurement,2020,39(7):900−905. doi: 10.3969/j.issn.1004-4957.2020.07.012 [42] 冯小燕, 张津, 吕美玲, 等. 利用液相色谱-质谱多反应监测方法测定食物中主要的牛奶过敏原α-酪蛋白[J]. 色谱,2013,31(6):510−513. [FENG X Y, ZHANG J, LÜ M L, et al. Detection of the major milk a-casein in food with liquid chromatography-tandem mass spectrometry in multiple reaction monitoring mode[J]. Chinese Journal of Chromatography,2013,31(6):510−513. doi: 10.3724/SP.J.1123.2013.01003 [43] 袁明美, 封聪, 王守云. LC-MS /MS 法测定牛乳及其制品中β-乳球蛋白的含量[J]. 化学研究,2017,28(2):219−223. [YUAN M M, FENG C, WANG S Y. Determination of β-lactoglobulin in milk and its products by LC-MS/MS[J]. Chemical Research,2017,28(2):219−223. [44] 詹丽娜, 陈 沁, 古淑青, 等. 超高效液相色谱-四极杆/静电场轨道阱高分辨质谱 检测食品中的牛奶过敏原酪蛋白[J]. 色谱,2017,35(4):405−412. [ZHAN L N, CHEN Q, GU SH Q, et al. Determination of milk allergen caseins in foods by ultra performance liquid chromatography-quadrupole/electrostatic field orbitrap high resolution mass spectrometry[J]. Chinese Journal of Chromatography,2017,35(4):405−412. doi: 10.3724/SP.J.1123.2016.10034 [45] 田荣荣, 白沙沙, 徐佳佳, 等. 不同来源乳中α-乳白蛋白、β-乳球蛋白和乳铁蛋白含量分析[J]. 食品工业科技,2020,41(4):311−315, 321. [TIAN R R, BAI S S, XU J J, et al. Content analysis of α-actoalbumin, β-lactoglobulin and lactoferrin in milk from different sources[J]. Science and Technology of Food Industry,2020,41(4):311−315, 321. [46] WANG Z, CHEN Q, WU Q, et al. Evaluation of mutual interference between bovine α-lactalbumin peptide and its isotope-labeled peptide in whey protein analysis using liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A,2018,1533:94−101. doi: 10.1016/j.chroma.2017.12.024
[47] 王震, 姚美伊, 凌云, 等. 同位素特异肽段在乳清蛋白定量分析中的应用[J]. 中国乳品工业,2018,46(3):41−44. [WANG Z, YAO M Y, LING Y, et al. Application of isotope specific peptide sin quantitative analysis of whey protein[J]. China Dairy Industry,2018,46(3):41−44. doi: 10.3969/j.issn.1001-2230.2018.03.011 [48] BILLAKANTI J, MCRAE J, MAYR M, et al. Advanced analytical tools for bovine lactoferrin identification and quantification in raw skim milk to finished lactoferrin powders[J]. International Dairy Journal,2019:99. doi: 10.1016/j.idairyj.2019.104546
[49] SEBNEM O B. Effect of different treatments on the stability of lysozyme, lactoferrin and b-lactoglobulin in donkey’s milk[J]. International Journal of Dairy Technology, 2018, 71(1): 36−45.
[50] YIN J Y, HUO J S, MA X X, et al. Study on the simultaneously quantitative detection for β-lactoglobulin and lactoferrin of cow milk by using protein chip technique[J]. Biomed Environ Sci,2017,30(12):875−886.





 下载:
下载:
 下载:
下载:



