Optimization of Enzymatic Extraction Process of Insoluble Dietary Fiber from Polygonatum sibiricum Residue by Response Surface Methodology and Its Characterization
-
摘要: 以黄精渣为原料,采用响应面优化酶法提取黄精渣不溶性膳食纤维(HIDF)。通过单因素实验研究料液比、木瓜蛋白酶浓度、木瓜蛋白酶酶解时间、α-淀粉酶浓度、α-淀粉酶酶解时间五种因素对HIDF得率的影响,并采用响应面(Box-Behnken)优化提取工艺参数;最后进行扫描电镜(SEM)、红外光谱分析(FTIR)和X射线衍射(XRD)观察以及功能性质测定。结果表明,最佳提取工艺为:料液比1:20 g/mL,木瓜蛋白酶浓度0.13%,木瓜蛋白酶酶解时间1.9 h,α-淀粉酶浓度0.29%,α-淀粉酶酶解时间2 h,HIDF得率为52.18%;HIDF的持水力、持油力和膨胀力分别为5.99±0.05 g/g、3.97±0.04 g/g和4.57±0.05 mL/g。综上,提取后的黄精膳食纤维具有较好的结构及物理性质,适合加工成功能性食品,可为提高黄精渣的利用率及进一步挖掘营养价值提供参考。Abstract: The insoluble dietary fiber (HIDF) was extracted from Polygonatum sibiricum residue by response surface methodology. Firstly, the effects of solid-liquid ratio, papain concentration, papain hydrolysis time, α-amylase concentration and α-amylase hydrolysis time on the extraction rate of HIDF were discussed by single factor experiments, the extraction process parameters were optimized by response surface methodology (Box-Behnken). Finally, infrared spectrum analysis, X-ray diffraction and scanning electron microscope observation were carried out, the functional properties were determined. The results showed that the optimum extraction conditions were as follows: Solid-liquid ratio 1:20 mL/g, papain concentration 0.13%, papain enzymolysis time 1.9 h, α-amylase concentration 0.29%, α-amylase hydrolysis time 2 h, the content of HIDF was 52.184%. The hydraulic holding capacity, oil holding capacity and swelling capacity of HIDF were 5.99±0.05 g/g, 3.965±0.04 g/g and 4.565±0.05 mL/g, respectively. Therefore, HIDF extracted from Polygonatum sibiricum residue had good physical and chemical properties and was suitable for processing into functional food, which provided a reference for improving the utilization rate of Polygonatum sibiricum residue and further excavating its nutritional value.
-
膳食纤维(dietary fiber,DF)被营养学家称为“第七大营养素”,由非淀粉多糖组成,它在小肠中既不被消化也不被吸收,但可以在大肠中完全或部分发酵[1]。根据溶解度,分为不溶性膳食纤维(insoluble dietary fiber,IDF)和水溶性膳食纤维(Water-soluble dietary fiber,SDF)[2]。IDF在增强人体饱腹感[3]的同时,能够吸附肠道内油脂、糖类等有机物,清除肠道毒素,促进胃肠道蠕动,并且对胰岛素进行调控[4],维持血糖稳定,在预防和缓解便秘、糖尿病、结肠癌、肥胖、中风、高血压等中有重要作用。目前国内外制备膳食纤维的主要方法有热水提取法、化学法、酶法、酶-化学结合法及生物发酵法等。其中最常用的是化学法,化学法存在易操作、成本低等优点,但化学法往往需要经过酸碱和高热的处理,得到的IDF有低品质、色泽较差、持水力和膨胀力较原料有所下降等问题[5]。而本文选用的酶法制备膳食纤维则提取工艺简单,提取得到的IDF具有纯度高、提取条件温和、易控制且无污染的优势。
黄精(Polygonatum sibiricum)属于百合科黄精属草本植物[6],具有补中益气、健脾润肺、益肾强骨之功效,还有延缓衰老、增强免疫功能、调血脂、降血糖、抗肿瘤等多种药理作用,是药食两用植物[7]。近年来对黄精属植物的功能成分研究报道较多,主要包括甾体皂苷类、多糖类、黄酮类、生物碱类、醌类、植物甾醇、挥发油、氨基酸、微量元素等[8]。目前黄精主要通过蒸煮炮制,获得黄精提取物,用于中成药的生产或作为中药饮片应用于临床[9]。由于市场对膳食纤维需求的增加以及人们环境保护意识的增强,越来越多的研究倾向于从植物或蔬菜以及其衍生物中提取膳食纤维。提取后的黄精渣一般都做丢弃处理,但这些黄精皮渣中仍含有大量膳食纤维等功能性成分。黄精的价值远没有被开发利用,且目前针对黄精渣的研究较少[10]。本研究以黄精渣为原料,进行膳食纤维的提取及工艺优化,并对其结构表征进行研究,以期提高黄精的综合利用,扩大黄精产业链的发展。
1. 材料与方法
1.1 材料与仪器
黄精茶渣、黄精皮渣等黄精渣 工业废弃,干燥24 h,粉碎,过60目筛,储存于干燥器直至进一步分析;木瓜蛋白酶(10万U/g)、α-淀粉酶(10000 U/g) 南宁庞博生物工程有限公司;玉米油 山东西王食品有限公司;柠檬酸、碳酸氢钠 国产食品添加剂。
扫描电镜 ZEISS 公司;VERTEX 70 傅里叶红外光谱仪 德国 Bruker 公司;FCD-2000恒温鼓风干燥箱 上海琅玕实验设备有限公司;SHB-Ⅲ循环水式多用真空泵 郑州长城科工贸有限公司;HH-6数显恒温水浴锅 国华电器有限公司;电子万用炉 天津市泰斯特仪器有限公司;HJ-6多头磁力加热搅拌器 国华仪器制造有限公司。
1.2 实验方法
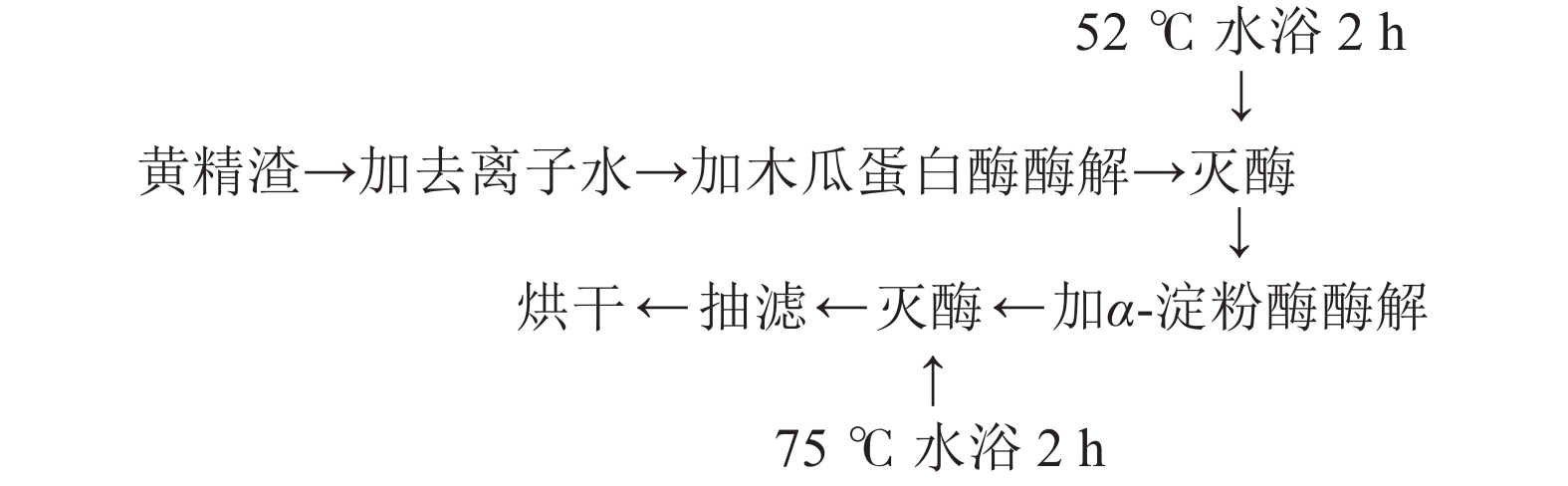
1.2.1 黄精渣中不溶性膳食纤维的制备流程
1.2.2 单因素实验
设定木瓜蛋白酶浓度0.125%,木瓜蛋白酶酶解时间2 h,α-淀粉酶浓度0.3%,α-淀粉酶酶解时间2 h,考察料液比(g/mL)在1:10、1:15、1:20、1:25、1:30时,对HIDF得率的影响。
设定料液比g/mL=1:20,木瓜蛋白酶酶解时间2 h,α-淀粉酶浓度0.3%,α-淀粉酶酶解时间2 h,考察木瓜蛋白酶浓度在0.05%、0.075%、0.1%、0.125%、0.15%时HIDF得率的影响。
设定料液比g/mL=1:20,木瓜蛋白酶浓度0.125%,α-淀粉酶浓度0.3%,α-淀粉酶酶解时间2 h,考察木瓜蛋白酶酶解时间在1.0、1.5、2.0、2.5、3.0 h时HIDF得率的影响。
设定料液比g/mL=1:20,木瓜蛋白酶浓度0.125%,木瓜蛋白酶酶解时间2 h,α-淀粉酶酶解时间2 h,考察α-淀粉酶浓度在0.1%、0.2%、0.3%、0.4%、0.5%时HIDF得率的影响。
设定料液比g/mL=1:20,木瓜蛋白酶浓度0.125%,木瓜蛋白酶酶解时间2 h,α-淀粉酶浓度0.3%,考察α-淀粉酶酶解时间在1.0、1.5、2.0、2.5、3.0 h时HIDF得率的影响。
1.2.3 响应面试验结果
基于单因素实验结果,选用五因素三水平响应面分析法,以HIDF得率为响应值进一步优化工艺,因素水平如表1所示。
表 1 Box-Behnken中心组合试验设计因素水平及编码Table 1. Factor level and coding of Box-Behnken center combination test因素 编码水平 −1 0 1 A 料液比(g/mL) 1:15 1:20 1:25 B 木瓜蛋白酶添加量(%) 0.1 0.125 0.15 C 木瓜蛋白酶酶解时间(h) 1.5 2 2.5 D α-淀粉酶添加量(%) 0.2 0.3 0.4 E α-淀粉酶酶解时间(h) 1.5 2 2.5 1.2.4 不溶性膳食纤维得率的计算
1.2.5 黄精渣中不溶性膳食纤维结构表征
1.2.5.1 扫描电镜(SEM)分析
样品放于双面胶带上,以3.00 kV的加速电压于扫描电镜观察台上收集图像,放大倍数为180倍和800倍。
1.2.5.2 傅里叶红外光谱(FTIR)分析
1.00 mg样品放置于样品台上。4000~400 cm−1扫描,扫描次数为64次,分辨率为4 cm−1。
1.2.5.3 XRD衍射分析
将样品放置于样品台上。管流:30 mA;管压:30 kV;E型:Cu;步长:0.02;起始角:5°;终止角:90°;扫描速度:2°/min;扫描模式:连续性扫描。
1.2.6 黄精渣中不溶性膳食纤维功能性质测定
1.2.6.1 持水力测定
准确称取待测粉末1.00 g,置于50 mL离心管中,加入20 mL蒸馏水,搅拌30 min,室温下静置24 h,以转速5000 r/min离心10 min,弃上清液,称湿质量[11]。
1.2.6.2 持油力测定
准确称取待测粉末1.00 g,置于50 mL离心管中,加入10 mL大豆油,搅拌30 min,室温下静置24 h,以转速5000 r/min离心20 min,小心倒去上层油脂,称得样品持油后质量[12]。
1.2.6.3 膨胀力测定
准确称取待测粉末1.00 g,置于25 mL量筒中,先记录其初始体积,再加入20 mL蒸馏水,振荡均匀后在室温下放置24 h,记录其膨胀后的体积[13]。
1.3 数据处理
响应面数据采用Design-Expert 8.0.5软件进行分析。
2. 结果与分析
2.1 单因素实验结果
HIDF得率受料液比的影响详见图1a。随料液比增加,HIDF得率先上升后下降,这是由于随料液比增大,样品与水接触面积增大,有利于样品HIDF溶出,增加HIDF得率;当料液比为1:20时,HIDF得率最大,达到48.60%;当料液比大于1:20 g/mL时,随料液比增加,HIDF得率逐渐下降,这可能因为黄精渣中IDF含量有限,当IDF在水中扩散达到平衡后,得率不再上升,随料液比继续增加,反而可能使其水解,导致得率下降[14]。这与白萝卜不溶性膳食纤维的提取类似,在提取白萝卜IDF时,IDF得率随料液比的增加也呈现先下降的规律[15]。因此,确定料液比1:15、1:20、1:25 g/mL为最佳优化范围。
HIDF得率受木瓜蛋白酶浓度的影响详见图1b。随木瓜蛋白酶浓度增加,HIDF得率总体呈上升趋势,这可能是由于木瓜蛋白酶浓度增大,木瓜蛋白酶水解黄精渣中的蛋白质。当木瓜蛋白酶用量在0.125%时,HIDF得率最大,达到49.90%,这是由于木瓜蛋白酶具有高效性,对蛋白质的水解效果最好[15];当木瓜蛋白酶用量超过0.125%以后,HIDF的得率不变,这是因为黄精渣中蛋白质含量有限,随木瓜蛋白酶浓度增加,HIDF得率不受影响。因此,确定木瓜蛋白酶浓度0.1%、0.125%、0.15%为最佳优化范围。
HIDF得率受木瓜蛋白酶酶解时间的影响详见图1c。随着反应时间的延长,HIDF得率逐步提高,2 h时达到最大值47.91%,但在2 h以后呈下降趋势。可能是2 h时酶与底物已充分结合,随时间的延长,HIDF中其他物质分解。因此,确定木瓜蛋白酶酶解时间1.5、2.0、2.5 h为最佳优化范围。
HIDF得率受α-淀粉酶浓度的影响详见图1d。随α-淀粉酶浓度增加,HIDF得率总体呈上升趋势,这可能是由于α-淀粉酶浓度增大,α-淀粉酶水解了黄精渣中的淀粉,当α-淀粉酶用量在0.3%时,HIDF得率最大,达到49.14%;此时是由于α-淀粉酶具有高效性,对淀粉的水解效果最好;当α-淀粉酶用量超过0.3%以后,HIDF的得率降低。这是因为α-淀粉酶用量过大,使黄精渣中一些半纤维素溶出,得到的HIDF含量就较少。因此,确定α-淀粉酶浓度0.2%、0.3%、0.4%为最佳优化范围。
HIDF得率受α-淀粉酶酶解时间的影响详见图1e。随着反应时间的延长,HIDF得率逐步提高,2 h时达到最大值48.70%,2 h以后先下降后不变。可能是2 h时酶与底物已充分结合,随时间的延长得率无明显差异。因此,确定α-淀粉酶酶解时间1.5、2.0、2.5 h为最佳优化范围。
2.2 响应面优化结果
2.2.1 回归模型建立与讨论
将表2数据用Design-Expert 8.0.5软件进行二次线性回归拟合,得到如下回归方程:Y=52.57−0.44A+1.32B−0.41C−0.21D−0.40E+0.69AB+0.88AC+0.75AD+7.5×10−3AE− 1.08BC−0.26BD−0.075BE−0.35CD+0.17CE− 0.062DE−2.44A2−1.58B2−3.73C2−2.57D2−4.83E2。由该方程知,二次项A2、B2、C2、D2和E2系数均为负,说明该方程存在最大值。
表 2 响应面分析结果Table 2. Results of response surface analysis实验号 A B C D E Y得率(%) 1 −1 0 0 −1 0 49.06 2 −1 0 −1 0 0 48.00 3 0 0 −1 1 0 47.25 4 0 0 0 1 −1 44.91 5 0 1 1 0 0 46.16 6 0 0 1 0 1 43.59 7 1 0 1 0 0 47.35 8 0 0 0 0 0 53.29 9 0 0 −1 0 −1 44.39 10 0 0 0 0 0 53.35 11 0 1 0 1 0 48.81 12 1 1 0 0 0 50.71 13 1 0 0 0 −1 45.51 14 0 0 0 0 0 50.80 15 0 −1 0 1 0 47.40 16 0 0 0 0 0 52.82 17 0 −1 0 −1 0 47.76 18 1 0 −1 0 0 45.95 19 1 −1 0 0 0 45.91 20 0 0 0 −1 −1 45.81 21 −1 0 0 0 1 44.91 22 −1 1 0 0 0 49.56 23 0 0 0 0 0 52.42 24 0 0 −1 0 1 43.75 25 −1 −1 0 0 0 47.5 26 0 1 0 0 −1 48.75 27 0 1 −1 0 0 49.58 28 0 0 0 0 0 52.74 29 0 −1 0 0 −1 45.56 30 −1 0 0 0 −1 46.00 31 0 −1 −1 0 0 45.26 32 0 0 1 −1 0 46.51 33 −1 0 1 0 0 45.87 34 1 0 0 1 0 47.25 35 0 0 0 1 1 44.00 36 1 0 0 −1 0 45.06 37 0 0 1 1 0 45.35 38 0 0 1 0 −1 43.57 39 0 −1 0 0 1 44.71 40 0 0 −1 −1 0 47.01 41 0 −1 1 0 0 46.16 42 0 0 0 −1 1 45.15 43 −1 0 0 1 0 48.25 44 0 1 0 0 1 47.6 45 1 0 0 0 1 44.45 46 0 1 0 −1 0 50.20 从表3方差分析的结果可以得知,模型的F值为25.47,整体模型P<0.0001,说明该模型极显著,且失拟项P=0.7831>0.05不显著,R2=0.9532,表明此模型的拟合程度较好,IDF得率可以用该模型进行分析和预测。对该回归方程系数进行显著性检验可知,影响极显著的有:B、A2、B2、C2、D2、E2(P<0.01),影响显著的有:A、C、AC、BC(P<0.05)。由F值得出,影响IDF得率的四个因素的主次顺序为B>A>C>E>D,即木瓜蛋白酶浓度>料液比>木瓜蛋白酶酶解时间>α-淀粉酶酶解时间>α-淀粉酶浓度。
表 3 响应面试验方差分析Table 3. Variance analysis of response surface method方差来源 平方和 自由度 均方 F值 P值 显著性 模型 317.74 20 15.89 25.47 <0.0001 ** A 3.03 1 3.03 4.85 0.037 * B 27.85 1 27.85 44.65 <0.0001 ** C 2.75 1 2.75 4.4 0.0461 * D 0.7 1 0.7 1.12 0.3005 E 2.51 1 2.51 4.03 0.0557 AB 1.88 1 1.88 3.01 0.0951 AC 3.12 1 3.12 4.99 0.0346 * AD 2.25 1 2.25 3.61 0.0691 AE 2.25E-04 1 2.25E-04 3.61E-04 0.985 BC 4.67 1 4.67 7.48 0.0113 * BD 0.27 1 0.27 0.43 0.5203 BE 0.023 1 0.023 0.036 0.8509 CD 0.49 1 0.49 0.79 0.3839 CE 0.11 1 0.11 0.17 0.6796 DE 0.016 1 0.016 0.025 0.8755 A2 51.76 1 51.76 82.99 <0.0001 ** B2 21.73 1 21.73 34.84 <0.0001 ** C2 121.72 1 121.72 195.14 <0.0001 ** D2 57.44 1 57.44 92.08 <0.0001 ** E2 203.21 1 203.21 325.79 <0.0001 ** 残差 15.59 25 0.62 失拟项 11.22 20 0.56 0.64 0.7831 不显著 误差 4.37 5 0.87 总和 333.33 45 注:**差异极显著(P<0.01),*差异显著(P<0.05)。 2.2.2 交互效应分析
响应曲面(图2)反映了当料液比、木瓜蛋白酶浓度、木瓜蛋白酶酶解时间、α-淀粉酶浓度、α-淀粉酶酶解时间,5个因素的任意两个变量取零点水平时,其他2个因素的交互作用对HIDF得率的影响。料液比和木瓜蛋白酶酶解时间对HIDF得率影响的等高线相对密集,表明料液比和木瓜蛋白酶酶解时间对得率影响较大;木瓜蛋白酶酶解时间和木瓜蛋白酶浓度对HIDF含量影响的等高线密集,表明木瓜蛋白酶酶解时间和木瓜蛋白酶浓度对得率影响更显著。
2.2.3 最佳方案确定与验证
通过对模型结果的分析处理,确定最优工艺条件为:料液比1:19.71 g/mL,木瓜蛋白酶浓度0.13%,木瓜蛋白酶酶解时间1.94 h,α-淀粉酶浓度0.29%,α-淀粉酶酶解时间1.98 h,此条件下HIDF得率52.92%。为了验证模型分析的准确性,选取料液比1:20 g/mL,木瓜蛋白酶浓度0.13%,木瓜蛋白酶酶解时间1.9 h,α-淀粉酶浓度0.29%,α-淀粉酶酶解时间2.0 h,进行验证,实验重复3次取平均值,所得HIDF得率为52.18%,与理论预测值相近,可见该模型具有重现性、可行。
2.3 扫描电镜(SEM)分析
HIDF的扫描电镜如图3所示,当放大倍数为180倍时,HIDF存在较多的纤维束,具有空腔且有一定的螺旋程度。当放大倍数为800倍时,纤维的空间网状结构十分疏松,孔隙较大,表面有较多的凸起,其表面呈现疏松多孔的结构,这些孔洞造就了其良好的亲水性,提升了膳食纤维整体的持水力和结合水力,同时也是膳食纤维具有良好吸附性的原因之一[16]。
2.4 傅里叶红外光谱(FTIR)分析结果
HIDF红外光谱分析如图4所示。3400 cm−1处出现较宽的吸收谱带,此处是由于纤维素和半纤维素O-H伸缩振动产生,主要来源于果胶(半乳糖醛酸)和半纤维素(木糖、甘露糖、半乳糖和阿拉伯糖)[17]。2920和2850 cm−1处出现吸收峰,此处是糖类甲基上C-H的收缩振动吸收峰,是多糖类物质的典型特征[18]。1620和1520 cm−1处出现吸收峰,此波段范围为芳香环的伸缩振动[19]。1240 cm−1处吸收峰代表木质素和半纤维素中C-O甲氧基的伸缩振动[20]。1030 cm−1处是纤维素和半纤维素C-O、C-C和C-O-C的拉伸[21],符合膳食纤维结构。
2.5 XRD衍射分析结果
HIDF的X射线衍射谱图如图5所示。X-射线衍射图谱可以反映物质的晶体结构。IDF的核心成分纤维素具有结晶性结构,HIDF在扫描角度2θ=21.42°处出现主衍射峰,在2θ=26.74°和2θ=34.39°出现两个次衍射峰,都表现出纤维素I型的特征衍射峰[22],对其亲水、亲油等物理化学性质都会产生一定影响[23]。
2.6 HIDF功能性质测定
通过实验分析,膳食纤维的水合作用主要取决于其表面亲水基团和结构中的松散空腔。由表4可知,HIDF持水力为(5.99±0.05)g/g,高于豆渣中不溶性膳食纤维(2.83±0.13)g/g[24]、大豆不溶性膳食纤维3.62 g/g[25]。持油力主要表现在膳食纤维对油脂的吸附能力,良好的吸附作用减少了人体肠道对脂肪的吸收,起到一定的减肥功效,HIDF持油力为(3.97±0.04)g/g,高于白萝卜不溶性膳食纤维2.12 g/g[26]、地瓜渣不溶性膳食纤维0.574 g/g[27]。膨胀力为(4.57±0.05)mL/g,高于麸皮不溶性膳食纤维3.10 mL/g[28]。表现出了良好的理化性质,适合加工成功能性食品。
表 4 黄精渣中膳食纤维的功能性质测定Table 4. Determination of functional properties of dietary fiber in Polygonatum sibiricum residue功能性质 持水力(g/g) 持油力(g/g) 膨胀力(mL/g) 测定结果 5.99±0.05 3.97±0.04 4.57±0.05 3. 结论
采用单因素和响应面优化酶法提取黄精渣中不溶性膳食纤维,并确定最佳提取工艺为:料液比1:20 g/mL,木瓜蛋白酶浓度0.13%,木瓜蛋白酶酶解时间1.9 h,α-淀粉酶浓度0.29%,α-淀粉酶酶解时间2 h,在此条件下HIDF得率为52.18%;功能实验结果表明,HIDF的持水力为(5.99±0.05)g/g,持油力为(3.97±0.04)g/g,膨胀力为(4.57±0.05)mL/g,性质良好,在功能强化型食品及保健品开发等方面具有广阔前景。通过对不溶性膳食纤维的结构进行表征可知,黄精渣中不溶性膳食纤维表现出纤维素I型的特征衍射峰,且具有较多的螺旋状纤维束和空腔,纤维的空间呈现网状结构,表面疏松多孔,含有较多的纤维素和半纤维素。响应面优化酶法提取黄精渣中不溶性膳食纤维的工艺、表征及物理性质测定,可为以后黄精不溶性膳食纤维的研发提供理论基础,为黄精渣开发利用提供参考,有利于黄精的进一步综合开发利用。
-
表 1 Box-Behnken中心组合试验设计因素水平及编码
Table 1 Factor level and coding of Box-Behnken center combination test
因素 编码水平 −1 0 1 A 料液比(g/mL) 1:15 1:20 1:25 B 木瓜蛋白酶添加量(%) 0.1 0.125 0.15 C 木瓜蛋白酶酶解时间(h) 1.5 2 2.5 D α-淀粉酶添加量(%) 0.2 0.3 0.4 E α-淀粉酶酶解时间(h) 1.5 2 2.5 表 2 响应面分析结果
Table 2 Results of response surface analysis
实验号 A B C D E Y得率(%) 1 −1 0 0 −1 0 49.06 2 −1 0 −1 0 0 48.00 3 0 0 −1 1 0 47.25 4 0 0 0 1 −1 44.91 5 0 1 1 0 0 46.16 6 0 0 1 0 1 43.59 7 1 0 1 0 0 47.35 8 0 0 0 0 0 53.29 9 0 0 −1 0 −1 44.39 10 0 0 0 0 0 53.35 11 0 1 0 1 0 48.81 12 1 1 0 0 0 50.71 13 1 0 0 0 −1 45.51 14 0 0 0 0 0 50.80 15 0 −1 0 1 0 47.40 16 0 0 0 0 0 52.82 17 0 −1 0 −1 0 47.76 18 1 0 −1 0 0 45.95 19 1 −1 0 0 0 45.91 20 0 0 0 −1 −1 45.81 21 −1 0 0 0 1 44.91 22 −1 1 0 0 0 49.56 23 0 0 0 0 0 52.42 24 0 0 −1 0 1 43.75 25 −1 −1 0 0 0 47.5 26 0 1 0 0 −1 48.75 27 0 1 −1 0 0 49.58 28 0 0 0 0 0 52.74 29 0 −1 0 0 −1 45.56 30 −1 0 0 0 −1 46.00 31 0 −1 −1 0 0 45.26 32 0 0 1 −1 0 46.51 33 −1 0 1 0 0 45.87 34 1 0 0 1 0 47.25 35 0 0 0 1 1 44.00 36 1 0 0 −1 0 45.06 37 0 0 1 1 0 45.35 38 0 0 1 0 −1 43.57 39 0 −1 0 0 1 44.71 40 0 0 −1 −1 0 47.01 41 0 −1 1 0 0 46.16 42 0 0 0 −1 1 45.15 43 −1 0 0 1 0 48.25 44 0 1 0 0 1 47.6 45 1 0 0 0 1 44.45 46 0 1 0 −1 0 50.20 表 3 响应面试验方差分析
Table 3 Variance analysis of response surface method
方差来源 平方和 自由度 均方 F值 P值 显著性 模型 317.74 20 15.89 25.47 <0.0001 ** A 3.03 1 3.03 4.85 0.037 * B 27.85 1 27.85 44.65 <0.0001 ** C 2.75 1 2.75 4.4 0.0461 * D 0.7 1 0.7 1.12 0.3005 E 2.51 1 2.51 4.03 0.0557 AB 1.88 1 1.88 3.01 0.0951 AC 3.12 1 3.12 4.99 0.0346 * AD 2.25 1 2.25 3.61 0.0691 AE 2.25E-04 1 2.25E-04 3.61E-04 0.985 BC 4.67 1 4.67 7.48 0.0113 * BD 0.27 1 0.27 0.43 0.5203 BE 0.023 1 0.023 0.036 0.8509 CD 0.49 1 0.49 0.79 0.3839 CE 0.11 1 0.11 0.17 0.6796 DE 0.016 1 0.016 0.025 0.8755 A2 51.76 1 51.76 82.99 <0.0001 ** B2 21.73 1 21.73 34.84 <0.0001 ** C2 121.72 1 121.72 195.14 <0.0001 ** D2 57.44 1 57.44 92.08 <0.0001 ** E2 203.21 1 203.21 325.79 <0.0001 ** 残差 15.59 25 0.62 失拟项 11.22 20 0.56 0.64 0.7831 不显著 误差 4.37 5 0.87 总和 333.33 45 注:**差异极显著(P<0.01),*差异显著(P<0.05)。 表 4 黄精渣中膳食纤维的功能性质测定
Table 4 Determination of functional properties of dietary fiber in Polygonatum sibiricum residue
功能性质 持水力(g/g) 持油力(g/g) 膨胀力(mL/g) 测定结果 5.99±0.05 3.97±0.04 4.57±0.05 -
[1] Wang C F, Song R Z, Wei S Q, et al. Modification of insoluble dietary fiber from ginger residue through enzymatic treatments to improve its bioactive properties[J]. Lwt Food Science & Technology,2020,125:109220.
[2] Xu Z H, Xiong X, Zeng Q Z, et al. Alterations in structural and functional properties of insoluble dietary fibers-bound phenolic complexes derived from lychee pulp by alkaline hydrolysis treatment[J]. Lwt Food Science & Technology,2020,127:109335.
[3] Kranz S, Brauchla M, Slavin J L, Miller K. B. What do we know about dietary fiber intake in children and health? The effects of fiber intake on constipation, obesity, and diabetes in children[J]. Advances in Nutrition: An International Review Journal,2012,3:47−53. doi: 10.3945/an.111.001362
[4] 狄志鸿, 杨善岩, 聂蓉蓉, 等. 膳食纤维降糖作用及机理研究进展[J]. 食品研究与开发,2014(20):138−141. [Di Z H, Yang S Y, Nie R G, et al. Research progress on the hypoglycemic effect and mechanism of dietary fiber[J]. Food research and development,2014(20):138−141. doi: 10.3969/j.issn.1005-6521.2014.20.035 [5] 李琦, 曾凡坤, 华蓉, 等. 麦麸膳食纤维理化特性、制备方法及应用研究进展[J]. 食品工业科技,2020,41(17):352−357, 367. [Li Q, Zeng F K, Hua R, et al. Research progress on the physical and chemical properties, preparation methods and application of wheat bran dietary fiber[J]. Food Industry Technology,2020,41(17):352−357, 367. [6] Zhou X, Zhang Y S, Zhao Y, et al. An LC fingerprint study of Poria cocos (Schw.) Wolf[J]. Chrom,2009,69(11/12):1283−1288.
[7] 仲兆金, 刘浚. 黄精有效成分三萜的研究进展[J]. 中成药,2011,23(1):58−62. [Zhong Z J, Liu J. Research progress on triterpenes, the effective constituents of Rhizoma Polygonati[J]. Chinese Patent Medicine,2011,23(1):58−62. [8] Lu J. P, Zhang J, Zhang Y. Z. The functional activities and application of Polygonatum sibiricum polysaccharides[J]. Journal of Food Safety & Quality,2013,4(1):273−278.
[9] 陈小林, 南海珍, 徐志南. 红曲菌发酵黄精渣生产monacolin K的探索性研究[J]. 药学研究,2019,38(1):12−15. [Chen X L, Nan H Z, Xu Z N. Exploratory study on the production of monacolin K from the fermented polygonatum residues of Monascus[J]. Pharmaceutical Research,2019,38(1):12−15. [10] 杨显辉, 代培春, 曾磊, 等. 黄精渣膳食纤维功能面包配方的应用研究[J]. 轻工科技,2019,35(10):18−21. [Yang X H, Dai P C, Zeng L, et al. Application research on formula of functional bread with polygonatum slag dietary fiber[J]. Light Industry Science and Technology,2019,35(10):18−21. [11] 刘学成, 王文亮, 弓志青, 等. 茶树菇膳食纤维改性及理化性质研究[J]. 食品工业科技,2021,42(4):142−148. [Liu X C, Wang W L, Gong Z Q, et al. Study on the modification and physicochemical properties of dietary fiber of Agrocybe cylindrica[J]. Food Industry Science and Technology,2021,42(4):142−148. [12] 薛山, 刘泽明. 鹰嘴芒皮渣水不溶性膳食纤维提取工艺优化及理化性质测定[J]. 北方园艺,2019(7):114−121. [Xue S, Liu Z M. Optimization of extraction process and determination of physical and chemical properties of water-insoluble dietary fiber from oleracea bark residue[J]. Northern Horticulture,2019(7):114−121. [13] 曾庆梅, 杨毅, 殷允旭, 等. 梨渣水不溶性膳食纤维的提取工艺研究[J]. 食品科学,2008(8):275−278. [Zeng Q M, Yang Y, Yin Y X, et al. Study on the extraction technology of water-insoluble dietary fiber from pear residue[J]. Food Science,2008(8):275−278. doi: 10.3321/j.issn:1002-6630.2008.08.059 [14] 唐小闲, 邱培生, 段振华, 等. 响应面法优化超声-微波辅助提取莲藕膳食纤维工艺研究[J]. 食品研究与开发,2019,40(6):132−139. [Tang X X, Qiu P S, Duan Z H, et al. Optimization of ultrasonic-microwave-assisted extraction of dietary fiber from lotus root by response surface methodology[J]. Food Research and Development,2019,40(6):132−139. doi: 10.3969/j.issn.1005-6521.2019.06.024 [15] 郭赵瑞, 张小康, 周苗苗, 等. 白萝卜不溶性膳食纤维的酸法提取及其理化性质研究[J]. 保鲜与加工,2021,21(3):56−60. [Guo Z R, Zhang X K, Zhou M M, et al. Extraction of insoluble dietary fiber from white radish by acid method and its physical and chemical properties study[J]. Preservation and Processing,2021,21(3):56−60. doi: 10.3969/j.issn.1009-6221.2021.03.009 [16] 高晓丽, 宿娅. 酶碱法提取梨渣水不溶性膳食纤维的研究[J]. 食品工程,2014(4):28−23. [Gao X L, Su Y. Study on the extraction of water-insoluble dietary fiber from pear residue by enzyme-alkali method[J]. Food Engineering,2014(4):28−23. doi: 10.3969/j.issn.1673-6044.2014.04.009 [17] 谢三都, 陈惠卿, 周春兰, 等. 橄榄渣膳食纤维理化和体外吸附特性及结构表征[J]. 食品与机械,2019,35(10):29−34. [Xie S D, Chen H Q, Zhou C L, et al. Physical and chemical properties andin vitro adsorption characteristics and structural characterization of dietary fiber from olive pomace[J]. Food and Machinery,2019,35(10):29−34. [18] 杜晓静, 白新鹏, 姜泽放, 等. 脱脂椰蓉可溶性膳食纤维制备工艺及单糖组成和理化特性分析[J]. 食品科学,2019,40(2):245−251. [Du X J, Bai X P, Jiang Z F, et al. Preparation technology of defatted coconut soluble dietary fiber and analysis of monosaccharide composition and physical and chemical properties[J]. Food Science,2019,40(2):245−251. doi: 10.7506/spkx1002-6630-20180118-250 [19] Chen H M, Fu X, L uo, Z G. Properties and extraction of pectin-enriched materials from sugar beet pulp by ultrasonic-assisted treatment combined with subcritical water[J]. Food Chemistry,2015,168:302−310. doi: 10.1016/j.foodchem.2014.07.078
[20] 周丽珍, 孙海燕, 刘冬, 等. 改性方法对豆渣膳食纤维的结构影响研究[J]. 食品科技,2011,36(1):143−147. [Zhou L Z, Sun H Y, Liu D, et al. Research on the influence of modification methods on the structure of soybean dregs dietary fiber[J]. Food Science and Technology,2011,36(1):143−147. [21] Zhang Y, Qi J R, Zeng W Q, et al. Properties of dietary fiber from citrus obtained through alkaline hydrogen peroxide treatment and homogenization treatment[J]. Food Chemistry,2019,311:125873.
[22] Alba K, Macnaughtan W, Laws A P, et al. Fractionation and characterisation of dietary fibre from blackcurrant pomace[J]. Food Hydrocolloids,2018,81:398−408. doi: 10.1016/j.foodhyd.2018.03.023
[23] 任雨离, 刘玉凌, 何翠, 等. 微波和微粉碎改性对方竹笋膳食纤维性能和结构的影响[J]. 食品与发酵工业,2017,43(8):145−150. [Ren Y L, Liu Y L, He C, et al. The influence of microwave and micro-pulverization on the properties and structure of dietary fiber from bamboo shoots[J]. Food and Fermentation Industries,2017,43(8):145−150. [24] Lin Y, Wang H, Rao W, et al. Structural characteristics of dietary fiber (Vigna radiata L. hull) and its inhibitory effect on phospholipid digestion as an additive in fish floss[J]. Food Control,2019,98:74−81. doi: 10.1016/j.foodcont.2018.11.016
[25] 吴长玲, 陈鹏, 李顺秀, 等. 空化射流条件下豆渣不溶性膳食纤维结构与功能性研究[J]. 农业机械学报,2021,52(3):350−356. [Wu C L, Chen P, Li S X, et al. Effect of cavitation jets on structure and function of okara insoluble dietary fiber[J]. Transactions of the Chinese Society of Agricultural Machinery,2021,52(3):350−356. doi: 10.6041/j.issn.1000-1298.2021.03.039 [26] 陈秉彦, 林晓姿, 李维新, 等. 高能机械处理方法对大豆不溶性膳食纤维结构及理化特性的影响[J]. 食品工业科技,2020,41(17):32−36, 44. [Chen B Y, Lin X Z, Li W X, et al. Effects of high-energy mechanical processing methods on the structure and physical and chemical properties of soybean insoluble dietary fiber[J]. Science and Technology of Food Industry,2020,41(17):32−36, 44. [27] 周贺霞, 刘菲, 王兴敏, 等. 超声波辅助酶法提取地瓜渣中不可溶性膳食纤维工艺研究[J]. 食品与发酵科技,2020,56(1):1−6. [Zhou H X, Liu F, Wang X M, et al. Ultrasonic-assisted enzymatic extraction of insoluble dietary fiber from sweet potato residues[J]. Food and Fermentation Science & Technology,2020,56(1):1−6. doi: 10.3969/j.issn.1674-506X.2020.01.001 [28] 钟雅云, 杨敏, 何沁峰, 等. 海带与小麦麸皮由来不溶性膳食纤维的酶辅助提取及其功能特性比较[J]. 中国食品学报,2019,19(11):124−131. [Zhong Y Y, Yang M, He Q F, et al. Enzyme-assisted extraction of insoluble dietary fiber derived from kelp and wheat bran and comparison of their functional characteristics[J]. Chinese Journal of Food Science,2019,19(11):124−131. -
期刊类型引用(3)
1. 李亚俐,王雪莉,石柳,吴文锦,陈胜,陈朗,郭晓嘉,熊光权,汪兰,孙智达. 壳聚糖-绿原酸复合保鲜剂对冷藏鮰鱼片食用品质的影响. 肉类研究. 2025(01): 42-50 .  百度学术
百度学术
2. 武玫怡,焦文娟,赵甜甜,刘俊,周芳,刘伟峰,张业辉,南海军,陈晓瑛,黄利华. 高静水压与水煮处理对热带海参品质的影响. 肉类研究. 2025(01): 25-33 .  百度学术
百度学术
3. 崔燕,刘韩欣,朱麟,尚海涛,林旭东,陈曙颖,宣晓婷. 超高压杀菌对大黄鱼理化性质及滋味、风味的影响. 食品工业科技. 2025(05): 44-55 .  本站查看
本站查看
其他类型引用(3)





 下载:
下载:









 下载:
下载:



