Research Progress about the Effects of Dietary Polyphenols on the Intestinal Microbiota
-
摘要: 人体肠道是一个复杂但稳定的微生态系统,其中肠道菌群对肠道及人体健康起着重要作用。健康的肠道中各菌间保持着微妙的平衡,但诸如膳食、年龄、药物、环境或生活习惯等多种因素均会打破肠道菌群平衡,而肠道菌群失衡是人体多种疾病发生发展的重要诱因。多酚是一类重要的植物次生代谢产物,具有多种生物学活性,如抗氧化、抗病毒、抗肿瘤、抗癌、抗菌、抗炎、预防心脑血管疾病等。大量研究报道证实,通过膳食补充多酚类物质对人类健康具有多种益处,特别是摄入膳食多酚对肠道健康和肠道菌群平衡有着显著的积极影响。本文归纳了近年来膳食多酚对肠道菌群影响相关研究进展,为科学、充分地利用多酚预防和治疗肠道疾病、保护肠道健康提供理论依据与参考。Abstract: The human gut is a complex but stable microecosystem. Intestinal microbiota plays an important role in maintaining human health. A healthy intestinal microflora is a delicate balance, but a variety of factors can also affect the balance of intestinal microflora, such as diet, age, medicine, environment or living habits, etc. The imbalanced of intestinal microflora is also a risk factor for the occurrence and development of a variety of diseases. Polyphenols are a large group of secondary metabolites from plants with versatile biological activities. A large number of studies indicate that dietary supplementation of polyphenols have the health promoting effects, like antioxidant, antiviral, antitumor, anticancer, anti-bacterial, anti-inflammatory and cardiovascular protective effects. They also find with beneficial effects for the intestinal health and modulating the gut microbiota. This paper summarize the recent progress of the research on the potential influence of dietary polyphenols on the intestinal flora. We aim to provide theoretical basis and reference for the scientific usage of polyphenols for preventing and treating intestinal diseases.
-
Keywords:
- dietary polyphenols /
- flavonoid /
- gut microbiota /
- dysbiosis /
- diseases
-
多酚(polyphenol)是一大类广泛存在于自然界、具有大量酚羟基结构单元的植物次生代谢产物。多酚协助植物应对环境胁迫或病虫害入侵,对植物具有重要生理意义[1]。多酚主要分为两大类:一类是包括水杨酸、咖啡酸、阿魏酸等在内的小分子酚酸类物质及黄酮类物质,另一类是单宁类的大分子物质。多酚能够有效清除自由基、影响细胞间的信号传导,也具有调节抗氧化相关基因表达的作用,发挥抗氧化、抗炎症、抗癌等生理作用,对人体健康具有重要意义[2]。
膳食多酚是指人体从日常饮食中摄取获得的多酚类物质。目前,膳食多酚按结构被划分为酚酸(phenolic acids)、类黄酮(flavonoids)、1,2-二苯乙烯(stilbenes)和木脂素(lignans)四大类[3],在人们日常食用的水果、蔬菜、谷类和豆类、茶、咖啡、蜂蜜和红酒等食物中广泛存在,上述食物是获取膳食多酚的最主要来源。具体而言,食物中最为常见的酚酸类物质是咖啡酸和阿魏酸,咖啡酸大量存在于蔬菜、水果和咖啡等食物中,而阿魏酸主要分布于谷类食物,如米糠和麦麸中。类黄酮类也在饮食中广泛存在,类黄酮又由多个亚类构成,如黄酮类、异黄酮类、黄酮醇类、黄烷酮类、黄烷醇类和花色素。黄酮醇类化合物在类黄酮中最常见,以槲皮素为主,这一物质在蔬菜中含量较高,特别是洋葱中含有较多的槲皮素[4]。黄烷醇类物质也是较为常见的黄酮类化合物,其中以儿茶素为代表,在红酒、巧克力、莲藕等中含量极为丰富。还有异黄酮类物质主要分布于豆类食物如大豆、豌豆及坚果中,花色素及单宁主要分布于草莓、蓝莓和樱桃等水果中。对于1,2-二苯乙烯类化合物而言,食物中存在多种结构形式,白藜芦醇是这类物质的代表,主要分布于葡萄、决明子、花生等食物中。木脂素主要来源于谷类以及纤维类食物中,如燕麦、黑麦和全谷物食品中[3,5]。研究表明,膳食多酚具有抗氧化、抑菌消炎、抗病毒、抗癌变和肿瘤、降血压降血脂、保护神经系统、增强免疫功能等多种生物学活性,可以清除自由基等代谢废物、舒张血管、促进损伤修复等,因此摄食富含多酚类的食物可降低慢性疾病发生率[2,6-8]。
益生元(prebiotics)是一类对肠道健康有益的食物组分,它能以有益的方式改变肠道菌群构成及代谢,为肠道中的有益菌提供营养物质,促进其在肠道中定植,诱导有益菌,并产生包括短链脂肪酸(SCFA,short chain fatty acid)在内的多种细菌代谢物,同时竞争性地拮抗有害菌在肠道中的增殖与定植[9]。肠道既是最大的消化系统也是最大的免疫器官,在人体消化吸收、机体免疫和神经调节等活动中发挥重要作用。肠道菌群是肠道微环境的组成部分,肠道菌群的平衡对于维持肠道健康有着重要意义。膳食多酚作为益生元发挥功效主要是通过刺激有益微生物群的生长并有效减少有害菌的定植而实现的,因此可以对肠道菌群进行靶向调节,这对维持肠道平衡和促进人体健康起到了非常积极的作用[9]。本文综述了近年来围绕膳食多酚对肠道菌群的调控研究,并总结了膳食多酚对肠道菌群调控机制,为深入系统且更科学地研究、开发与利用膳食多酚提供可借鉴的理论依据。
1. 肠道菌群
1.1 肠道菌群简介
人体肠道包含多达100万亿的肠道菌,有研究表明,肠道微生物主要以厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidetes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、疣微菌门(Verruco- nicrobia)和梭杆菌门(Fusobacteria)6大细菌门为主体。在健康的成年人肠道中,厚壁菌门和拟杆菌门占总体的90%以上。这些菌群中如双歧杆菌和乳酸菌,属于对人体健康起积极作用的有益菌,作为抗氧化剂调节代谢过程中的氧化应激反应,可以有效抑制大肠内氨、粪臭素及胺类致癌物等的形成,增加有机酸的生成,降低结肠及粪便pH,抑制病原菌生长;促进肠道上皮细胞DNA合成,促进肠上皮细胞的增殖。肠道微生物群与肠道细胞、黏膜屏障共同构成肠道微环境,且保持平衡状态,任何一方受到影响,都将破坏肠道菌群平衡,危害人体健康[10]。目前研究发现,膳食和药物等外界因素可以调节肠道菌群及其微环境的平衡,其中膳食调节起着最显著的作用,主要表现为膳食中的益生元物质可以改善肠道中有益菌的生长增殖情况,有助于有益菌与致病菌竞争肠道增殖环境,从而抑制致病菌的生长。此外益生元也可促进有益菌的代谢活动,产生对人体有益的代谢物,发挥其相应的生理功能,促进人体健康。
1.2 肠道菌群的生理功能
健康肠道中菌群的稳定是相对的,不同菌群之间需维持在一个相对稳定的比例,以协助宿主发挥多种重要的生理功能。
肠道菌群对人体生理功能的影响主要体现在三方面:a. 影响宿主代谢。肠道菌群可发酵碳水化合物、脂质和蛋白质等,并合成维生素、一些必需和非必需氨基酸、以及多种短链脂肪酸,并协助完成胆汁的生物转化;同时肠道菌群可将一些不被降解的糖类物质进行代谢降解,如纤维素、半纤维素、抗性淀粉、树胶、果胶等,这些物质将有助于宿主吸收对人体健康有益的营养物质,为人体生长发育提供营养和能量。研究表明,肠道菌群可将多酚中的糖苷降解为苷元,再进一步降解为芳香酸,由此发挥生理作用,如黄酮醇可以降解为羟苯乙酸,从而抑制血小板聚集[11-12]。b. 影响宿主免疫系统。有研究表明,肠道菌群可以协助B细胞、巨噬细胞和树突状细胞等抗原呈递细胞发挥免疫调节作用,特别是防止对肠道微生物具有免疫耐受性的病原菌入侵机体,进而对机体起到保护作用[13]。在对无菌小鼠进行的研究中发现,肠道菌群对淋巴组织的功能产生明显影响。同时,在一定条件下,肠道菌群协助免疫系统对病原菌产生反应,并对抗原耐受性的调控途径产生影响[14]。c. 影响肠道屏障功能。一些研究表明,正常的肠道菌群在定植过程中对肠道屏障功能的发育起着重要的作用,且肠道菌群通过诱导肠上皮细胞的增殖并促进肠上皮的完整,来保障肠道屏障功能的正常。因此肠道菌群是维持肠道屏障功能所必须的,在调节肠道屏障功能中起着重要的作用[15]。
1.3 肠道菌群失调与疾病
在健康状态下,肠道菌群维持在一种动态平衡状态,各种菌在一定范围内维持于相对稳定的状态,这也被称为肠道菌群稳态。而一旦这种稳定的平衡关系被打破,便可能导致肠道菌群失调。导致菌群失调的因素有很多,包括膳食、年龄、药物、压力、吸烟习惯以及缺乏锻炼等[12],其中膳食是肠道菌群的主要调控因子,将会直接影响肠道菌群的构成和功能。研究表明,母乳中含有的低聚糖不仅促进了婴儿肠道中乳酸菌和双歧杆菌的增殖,同时也加速了婴儿免疫系统的成熟[16]。年龄也是肠道菌群的另一项调控因子,随着机体的衰老,肠道菌群的多样性会发生巨大变化,最明显的表现是厚壁菌门和拟杆菌门的比例发生改变,这也会导致因衰老所引起的免疫炎症环境的变化。进一步研究表明,因身体衰老导致机能的退化会引起唾液功能受损、消化道消化困难和营养物质运转时间的延长,以及营养素吸收不规律所导致的营养不良也会引起肠道菌群失调[17-18]。此外,药物也是肠道生态环境的一个调节因子,特别是抗生素会显著改变肠道菌群的构成和功能[19-20]。抗生素会使肠道菌群的定植耐药性丧失,使得经抗生素治疗后肠道菌定植率大大降低;抗生素也会造成来自宿主的唾液酸增加,进一步被条件致病菌利用[21]。另外还有一些非膳食的环境因素也会引起肠道菌群的失调,如压力、吸烟习惯和缺乏锻炼等,以上诸多因素会引发机体氧化应激和炎症反应,导致肠道菌群紊乱[22]。目前,肠道菌群的失调可被分为几种情况,包括共生菌数量减少;病原菌无规律生长和肠道菌群多样性下降。但研究发现,最常见的肠道菌群失调情况是以上三种情形同时存在而导致的肠道菌群紊乱[23-24]。
肠道菌群失调同机体多种疾病相关,由于肠道菌群的组成受很多因素影响,如膳食习惯、生活习惯和锻炼习惯等,这些因素也是肥胖、二型糖尿病、心血管疾病等的致病因素[25]。已有研究得出,因肠道菌群失调造成的机体致病机理主要包括三个方面:a.大量增殖的革兰氏阴性菌加速细菌内毒素的释放,造成机体免疫力下降,增加患病风险;b.菌群发酵产物中短链脂肪酸含量下降,使肠黏膜细胞获得的能量不足,同时肠道pH升高,诱发疾病;c.失调的肠道菌群刺激机体产生炎症因子,加速疾病发生。在营养不良的个体中肠道菌群可调控免疫代谢进程的信号分子,通过干扰肠道上皮细胞和免疫细胞,形成一种炎症环境,加速糖尿病的进程及有关化合物的合成[26]。糖尿病患者一些特殊的肠道菌群,如肠球菌、肠杆菌、酵母菌等,不仅加速了肥胖和糖尿病的进程,也加速了主要微型血管的合成过程,进而诱发糖尿病并发症,如视网膜病变、肾病等[22]。肠道菌群失调也是肠道屏障完整性被破坏的触发因子,而肠道屏障功能的破坏也伴随着肌动蛋白表达的增强,同时如脂多糖、肽聚糖和尿毒症毒素等的一类物质通透性增强且转移加快,因此诱导脓毒血症的发展,同时也激活了机体免疫系统[25-26]。对于微生物相关分子模型将会引起与TLRs中的TLR4相关的促炎反应增强,进而引发一系列反应,最突出的是导致促炎反应中分子的释放,影响葡萄糖和胰岛素的代谢和响应,进一步消耗糖类化合物同时还导致大量氧自由基的释放,而这一途径将深入到肥胖和糖尿病发展进程中的代谢损伤[27]。
综上所述,饮食会对肠道菌群组成造成影响,因此可以通过合理调控饮食结构,对肠道菌群组成进行调节,提高益生元或有益成分的摄入。膳食多酚作为一种益生元,其结构中包含许多羟基,可与有害菌细胞膜上的脂质双分子层结合,影响其结构功能的发挥[28]。多酚在机体中发生反应生成过氧化氢,会破坏有害菌细胞膜结构。多酚参与体内多种酶反应,调节机体代谢;或与金属离子发生螯合反应,导致有害菌的相关反应中酶因缺乏辅基的结合位点而无法发生反应[29]。多酚通过以上多种途径调节机体活动,从而对肠道菌群进行调节,同时也对机体因菌群紊乱诱发的疾病产生一定影响。
2. 膳食多酚对肠道菌群的调控
多酚类物质经人体摄入后,会被机体识别为外源化合物,导致其生物利用率会显著低于一些微量及常量营养素[30]。酚类物质进入小肠后,因其复杂的结构和聚合度导致其在小肠部位吸收较少,且吸收主要在酚类物质发生去偶联反应之后[31]。较低复杂度的酚类物质可发生氧化反应、还原反应、水解反应及共轭反应等,所得产物将进入小肠上皮细胞和肝细胞。同时经过这一系列生物转化产生的多种活性代谢物,如葡萄糖醛酸、硫酸盐和甲基衍生物等,经循环系统至组织器官中,最终随尿液代谢排出体外。但大部分未被小肠吸收的多酚类物质会到达结肠,在结肠内微生物的作用下进行消化吸收,以被机体利用[32-33]。
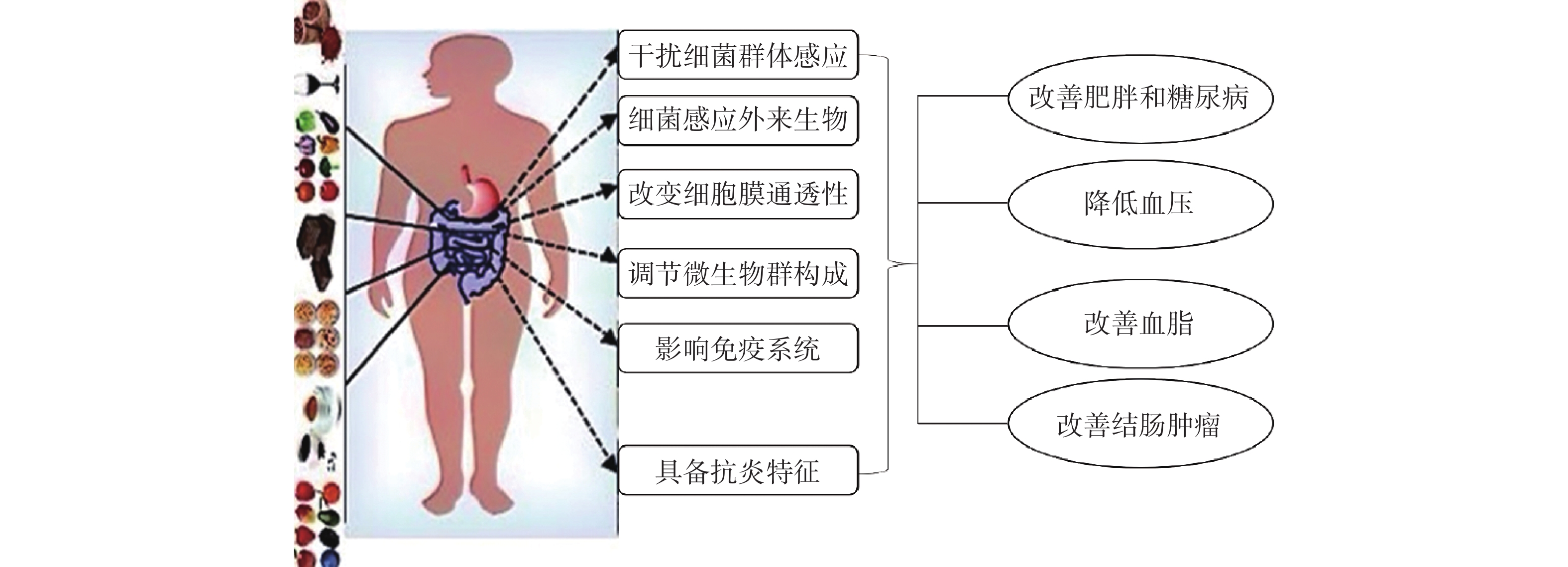
据报道,正常人体的肠道菌群中厌氧菌的数量比兼性厌氧菌和需氧菌的数量多2~3个数量级,由此可将其分为主要菌群和次要菌群。主要菌群数量在log(107~108)CFU/g以上,主要为原籍菌或常驻菌,包括优杆菌、拟杆菌、双歧杆菌等菌属;次要菌群在log(107~108)CFU/g以下,主要为外籍菌或过路菌,包括链球菌、肠球菌、大肠杆菌和乳杆菌等[10]。来自不同膳食中的多酚类物质对部分菌群的生长、增殖有着促进或抑制作用[10]。膳食多酚对肠道菌群发挥着促进有益菌生长、抑制有害菌生长的作用,从而对肠道菌群的结构和数量产生影响,调节人体肠道微生态的稳定情况,使有益菌对人体健康发挥相应的作用。目前,膳食多酚与肠道菌群间的相互作用已有许多学者进行研究并得出一系列结果,就几例膳食多酚对肠道菌群影响的典型研究进行归纳概括如下(图1)。
2.1 茶多酚
茶多酚是茶叶中多羟基酚类物质的总称,主要包括儿茶素类物质、4-羟基黄烷醇类、花色苷类、黄酮类、黄酮醇类和酚酸类等,其中以儿茶素和黄酮两种物质为主[34]。茶多酚能通过优先抑制肠道中致病菌但不影响有益菌生长的方式,创造有利于有益菌生长的肠道环境,从而促进有益菌生理活性的发挥,并调节肠道菌群结构[35]。于子婷等[36]通过饲喂小鼠不同剂量的茶多酚,并分析小鼠肠道微生物的多样性,发现茶多酚在达到一定浓度时可以增加肠道菌群微生物的多样性,其中对乳杆菌的增殖效果最为明显且具有剂量依赖性。吴根梁等[37]从陈年茯砖茶中提取出茶多酚,加入到含65岁老年人肠道菌群的混合培养基中进行体外静态厌氧培养,于0、4、8、12、24 h设置空白组和陈茶多酚组,培养相应时间后采样,检测相应的肠道菌群的情况。研究结果表明,陈年茯砖茶中的茶多酚类物质与老年人肠道菌群在体外相互作用下,菌群丰度和多样性均有所提高;此外在培养4 h和12 h的情况下,肠道中的埃希氏菌属和γ-变形菌纲_B38含量下降,拟杆菌属和双歧杆菌属等菌属含量有所提高,表明陈年茯砖茶的茶多酚类物质有益于改善老年人的肠道菌群结构。GUO等[38]提取绿茶中的茶多酚物质,并通过建立肥胖小鼠模型,探究茶多酚对肠道菌群的调节作用。研究发现,在高脂膳食组中菌群多样性降低并显著低于高脂膳食-绿茶多酚组,同时拟杆菌门丰度相对增加,厚壁菌门丰度相对下降,这一结果表明绿茶中的茶多酚能提高肠道菌群的多样性,调节菌群的构成比例,从而改善并维持肠道菌群的生态平衡,有益于人体健康。综上发现,茶多酚这一物质可以提高肠道菌群的多样性,改变部分菌群的丰度及比例,使得有益菌更好地发挥对人体健康的促进作用。
2.2 葡萄多酚
葡萄多酚存在于葡萄皮和葡萄籽中,主要包括酚酸类、黄烷醇类、黄烷酮类、黄酮醇类、花色苷以及白藜芦醇。葡萄多酚自身作为供氢体,可以形成稳定的自由基,在氧化反应中发挥作用,对机体起到抗氧化作用。葡萄多酚还具有潜在的益生元效应,可以调控肠道菌群的构成,并生成对宿主有益的短链脂肪酸[39]。研究发现,葡萄多酚普遍会对乳酸菌和双歧杆菌这两种肠道菌群产生影响,乳酸菌和双歧杆菌是对人体有益的益生菌,能够阻止致病菌的入侵和定植,也能促进肠道上皮细胞的增殖,而梭菌、大肠杆菌等则对人体有害,即会对人体结肠黏膜产生有害作用。生成的短链脂肪酸对肠道生态环境的改善也发挥重要作用,其可调节肠道中致病菌的移位,给肠道细胞供给能量,抑制炎症细胞释放炎症因子等,对保障人体健康有重要意义。ZHOU等[40]采集三名胃肠道健康志愿者的粪便,接种葡萄多酚后经体外发酵,观察肠道菌群的相关情况。研究发现,葡萄多酚会对部分肠道菌群产生影响并改变短链脂肪酸的结构。此外,发酵后的葡萄多酚促使双歧杆菌、乳杆菌等肠道菌群数量明显增多,并抑制溶组织梭菌和普雷沃氏菌属的生长,但对细菌总数没有显著影响。DOLARA等[41]探究经葡萄多酚饲养的小鼠粪便中的菌群主要为双歧杆菌、乳酸菌及拟杆菌等,而空白组为丙酸杆菌、梭菌及拟杆菌。两组相比,梭菌和乳酸菌的含量差别很大,且双歧杆菌在试验组中显著增加,但细菌总数未呈现显著变化。因此葡萄多酚可调节肠道菌群结构,从而发挥肠道菌群对人体健康的有益作用。杨昌铭等[42]通过建立高脂膳食诱导小鼠血脂代谢紊乱模型,并随机分为对照组、高脂组和原花青素B2干预组三组,探究原花青素B2对肠道菌群的影响。研究发现,与高脂组相比原花青素B2组占优势的菌属为拟杆菌属,其可显著增加高脂膳食小鼠粪便中丁酸的含量,从而改善肠道环境,调节肠道菌群结构,缓解高脂膳食诱导的血脂代谢紊乱。LARROSA等[43]通过DSS(硫酸葡聚糖)诱发结肠炎啮齿动物模型,探究葡萄中白藜芦醇对人体肠道菌群的影响。研究发现,对照组中主要的菌群为大肠杆菌和肠细菌,经DSS给药后粪便中乳酸杆菌和双歧杆菌属为主要菌属,相较于对照组中大肠杆菌和肠细菌增加较少。QIAO等[44]探究白藜芦醇对高脂饮食小鼠体内肠道菌群的影响,结果表明,白藜芦醇可调节高脂饮食引起的肠道菌群失调,增加拟杆菌门与厚壁菌门的比例,增加乳酸菌和双歧杆菌的生长,调节肠道微生物的组成结构,从而起到维护肠道菌群环境平衡的作用。因此葡萄中的白藜芦醇也可调节人体肠道菌群结构,对人体健康发挥有益作用。
2.3 果蔬多酚
果蔬中含有的多酚类功能成分,可以显著调节机体血压、血糖、血脂并起到抗癌、抗氧化、抑菌消炎等生理功能,在维持人体健康和疾病预防中发挥着重要作用。果蔬中多酚类物质可选择性地促进双歧杆菌等有益菌的生长、抑制类杆菌、肠球菌、葡萄球菌等有害菌的生长,通过此途径调整肠道菌群的数量和比例,优化菌群结构,使菌群结构保持平衡,从而发挥对人体健康有益的作用[45]。张军丽等[46]通过建立小鼠腹泻模型,然后灌胃复合菌-荔枝多酚,探究其对肠道菌群的影响作用。研究表明,复合菌-荔枝多酚能增加腹泻后小鼠肠道菌群的数量,增强肠道菌群的微生态稳定性,但并未增加群落的多样性。出现这一结果的原因可能是由于荔枝多酚可以抑菌、增强机体免疫力和预防疾病,因此需要抑制有害菌的增殖。唐诗等[47]探究了猕猴桃皮渣多酚提取物对肠道菌群的影响。研究发现,空白组肠道微生物主要是厚壁菌门,其次为变形菌门,拟杆菌门含量较少;而加入多酚提取物的样品组肠道菌群构成以厚壁菌门、拟杆菌门及放线菌门为主。两组相比,发现多酚组中拟杆菌门与厚壁菌门的比例显著升高。这一结果说明猕猴桃皮渣多酚提取物对肠道益生菌的增殖有一定促进作用,其可以发酵肠道内益生元,从而获得有利于肠道微生态的代谢产物,同时在一定程度上可抑制有害菌的增殖。因此这种多酚提取物可改善肠道内环境,为促进肠道健康发挥积极作用。PUUPPONEN-PINIA等[48]发现,莓果酚对葡萄球菌有很好的抑制作用,部分莓果酚可抑制沙门氏菌,但对乳酸菌群不会产生影响,表明莓果酚可以抑制人体肠道中的致病菌。KABUKI等[49]对芒果种子提取物的研究发现,从芒果种子中提取出富含单宁和黄酮两种多酚提取物能抑制革兰氏阳性菌的生长增殖但对革兰氏阴性菌无影响,对乳酸菌也没有活性。因此可选择性调节肠道菌群,促进人体健康。黄酮类化合物可以促进肠道有益菌群的生长增殖。陈玉慧等[50]从青钱柳中分离纯化得到青钱柳黄酮和三萜,采用体外厌氧粪样混合培养的方式,评价青钱柳黄酮和三萜对人体肠道菌群的调节作用。研究表明,青钱柳黄酮和三萜类物质可以有效促进肠道中双歧杆菌和乳酸菌等有益菌的生长增殖,对梭状菌和拟杆菌产生抑制作用,改变肠道菌群的结构但不会显著影响肠道菌群的数量。由于益生元能够通过刺激人体肠道中的有益菌的生长而对人体健康产生积极的影响,因此青钱柳中的黄酮和三萜可能发挥着益生元的作用,作为抗氧化剂抑制代谢过程中的氧化应激反应,从而为肠道中有益菌的生长提供有利环境。因此青钱柳黄酮和三萜可调节肠道菌群结构,维持肠道微生态环境的稳定,进而对人体健康发挥积极作用。
2.4 其他
蜂产品,如蜂胶等中含有丰富的多酚类物质,以酚酸类和黄酮类为主,具有良好的生物学活性,如抗癌、抗病毒、抗氧化、抗炎症等[51]。蜂胶多酚也如同其他膳食多酚一样,会对人体肠道菌群的结构、多样性等方面有一定的调节作用。本团队[52]通过硫酸葡聚糖诱导大鼠溃疡性肠炎,饲喂含蜂胶的膳食,研究蜂胶对大鼠溃疡性结肠炎的影响,结果表明,添加蜂胶可以改善结肠炎的相关症状,同时显著增加肠道菌群的多样性。槲皮素和柚皮素是广泛存在于多种膳食中的黄酮醇类物质。石塔拉等[53]在体外用不同浓度槲皮素干预常见的几种肠道单菌的生长增殖情况,结果表明,在体外200 μmol/L槲皮素可促进肠道内2种乳酸杆菌的生长,抑制中性菌和2种有害菌的增殖。因此膳食槲皮素可促进肠道益生菌的生长,并作为益生元,调节肠道菌群结构。柚皮素和槲皮素对所有被分析的肠道菌群的生长均有抑制作用,同时抑制效果与其添加剂量相关联。然而其糖苷,即柚皮苷和芦丁对肠道菌群的生长没有抑制作用,但在一定条件下具有促进作用。另外对橙皮素和芦丁苷、橙皮苷也进行了相同的研究,虽然在此情况下,苷元影响较弱,但也有剂量依赖性[54]。
可可作为目前许多备受欢迎的休闲食品的组分,其中所含的多酚类物质具有增强免疫力、抗炎症、降低血小板活性、降低胆固醇水平等生理功能,可有效预防心脑血管疾病。可可多酚也为人体多项生理功能的发挥起到关键性的作用。TZOUNIS等[54]通过临床随机实验,令两组志愿者分别摄食高含量可可和低含量可可的黄烷醇饮料,进行4周代谢,收集其摄食前后的粪便样品,并结合荧光原位杂交发检测细菌情况。研究发现,可可可以促使双歧杆菌和乳酸杆菌等肠道微生物含量增加,同时促使梭状芽孢杆菌等厚壁菌门类的肠道微生物丰度下降。因此食用可可黄烷醇可显著影响人体肠道菌群的生长。在黑巧克力中已检出黄烷酮单体,可通过日常摄食达到促进肠道健康的作用。TZOUNIS等[54]进行体外实验,对黄烷醇单体即儿茶素和表儿茶素进行分批厌氧培养。研究发现,黄烷醇单体可以促进大肠中菌群的增殖。其中,儿茶素可促进双歧杆菌、乳酸杆菌以及真细菌中球菌的生长,同时对大肠杆菌也有一定程度的影响,并抑制溶组织梭菌的生长。在低浓度条件下,表儿茶素也可促进真细菌中球菌的生长,但对其他菌属没有显著影响。两种黄酮醇单体对细菌总数均没有明显影响。在黄烷酮单体对肠道菌群的诱导下,肠道中糖化代谢增强,进而代谢得到短链脂肪酸、丙酸和丁酸等对人体肠道健康有益的代谢物。
以上研究表明,多酚类物质可以改变肠道菌群的组成,即促进有益菌生长,亦可抑制有害菌生长。大部分来源的膳食多酚几乎不会抑制乳酸菌群的生长,还可能会刺激某些乳酸菌菌株的生长。另外还有研究发现,肠道菌群可以将多酚转化为能够影响肠道及机体健康的生物活性物质。膳食中的多酚类物质可以调节细菌代谢物的酶活性,减少人群患癌风险。这些研究均表明多酚类物质能影响肠道菌群组成并发挥调控作用,对调节人体健康发挥积极作用(表1)。
表 1 膳食多酚对肠道菌群的调控Table 1. Regulation of dietary polyphenols on intestinal microbiota多酚种类 多酚对肠道菌群的影响 多酚对菌群结构及多样性等的影响 参考文献 茶多酚 对乳杆菌的增殖效果明显,呈剂量依赖性 提高了肠道菌群多样性 于子婷等[36] 肠道中埃希氏菌属和γ-变形菌纲_B38含量下降,拟杆菌属和双歧杆菌属含量提高 吴根梁等[37] 拟杆菌门丰度增加,厚壁菌门丰度下降 GUO等[38] 葡萄多酚 提高了双歧杆菌、乳杆菌含量,抑制溶组织梭菌和普雷沃氏菌属的生长,但细菌总数没有明显变化 调节肠道菌群结构,发挥对人体的
有益作用ZHOU等[40] 双歧杆菌含量显著增加,梭菌和乳酸菌含量有所变化,但细菌总数没有明显变化 DOLARA等[41] 拟杆菌属含量提高,并增加了粪便中丁酸的含量 杨昌铭等[42] 乳酸杆菌和双歧杆菌成为主要菌属,大肠杆菌和肠细菌相对减少 LARROSA等[43] 提高了拟杆菌门和厚壁菌门的比例,促进乳酸菌和双歧杆菌的生长 QIAO等[44] 果蔬多酚 复合菌-荔枝多酚 抑制了部分有害菌的增殖 调节肠道菌群结构,维持肠道微环境稳态,但肠道群落多样性无明显变化 张军丽等[46] 猴桃皮渣多酚
提取物厚壁菌门、拟杆菌门及放线菌门成为主要菌属,使拟杆菌门与厚壁菌门比例显著升高 唐诗等[47] 莓果酚 对葡萄球菌的生长有良好的抑制效果,同时对沙门氏菌的生长也有抑制作用,对乳酸菌没有明显影响 PUUPPONEN-PINIA等[48] 芒果种子多酚
提取物促进革兰氏阳性菌的生长,抑制革兰氏阴性菌的生长 KABUKI等[49] 苹果黄酮 双歧杆菌含量增多,乳酸菌含量明显减少 ESPLEY等[50] 青钱柳黄酮和
三萜促进双歧杆菌和乳酸菌的生长,抑制梭菌和拟杆菌的生长 陈玉慧等[50] 蜂胶多酚 调节菌群结构,缓解炎症症状 增加了肠道菌群多样性 WANG等[52] 可可多酚 促使双歧杆菌和乳杆菌增殖,使梭状芽孢杆菌等厚壁菌门类的微生物丰度下降 调节肠道菌群结构,发挥对人体健康积极的作用,尚未对肠道菌群多样性产生影响 TZOUNIS等[54] 促进双歧杆菌、乳酸杆菌以及真细菌中球菌的生长,并对大肠杆菌的生长状态产生一定的影响 TZOUNIS等[54] 3. 膳食多酚与肠道菌群的相互作用
膳食多酚可作为肠道菌群的发酵底物,因其不能被小肠吸收,可直接到达结肠被肠道菌群利用,此外其代谢物也可通过与肠上皮细胞的相互作用,进一步影响肠道菌群的结构和数量。因此膳食多酚可通过调节肠道菌群的构成来维持肠道健康。膳食多酚一方面可促进肠道中有益菌的增殖,抑制有害菌的增殖,并调节肠道菌群的构成及生理功能。另一方面肠道菌群中的有益菌能发挥益生元的作用,促进多酚在肠道中的代谢,加速肠道对多酚及其他营养物质的吸收。因此肠道菌群对多酚在肠道中的生物转化起到一定的作用,而多酚也是肠道菌群发酵利用的良好底物。肠道菌群与膳食多酚之间相互作用,共同发挥对人体健康的有益影响。
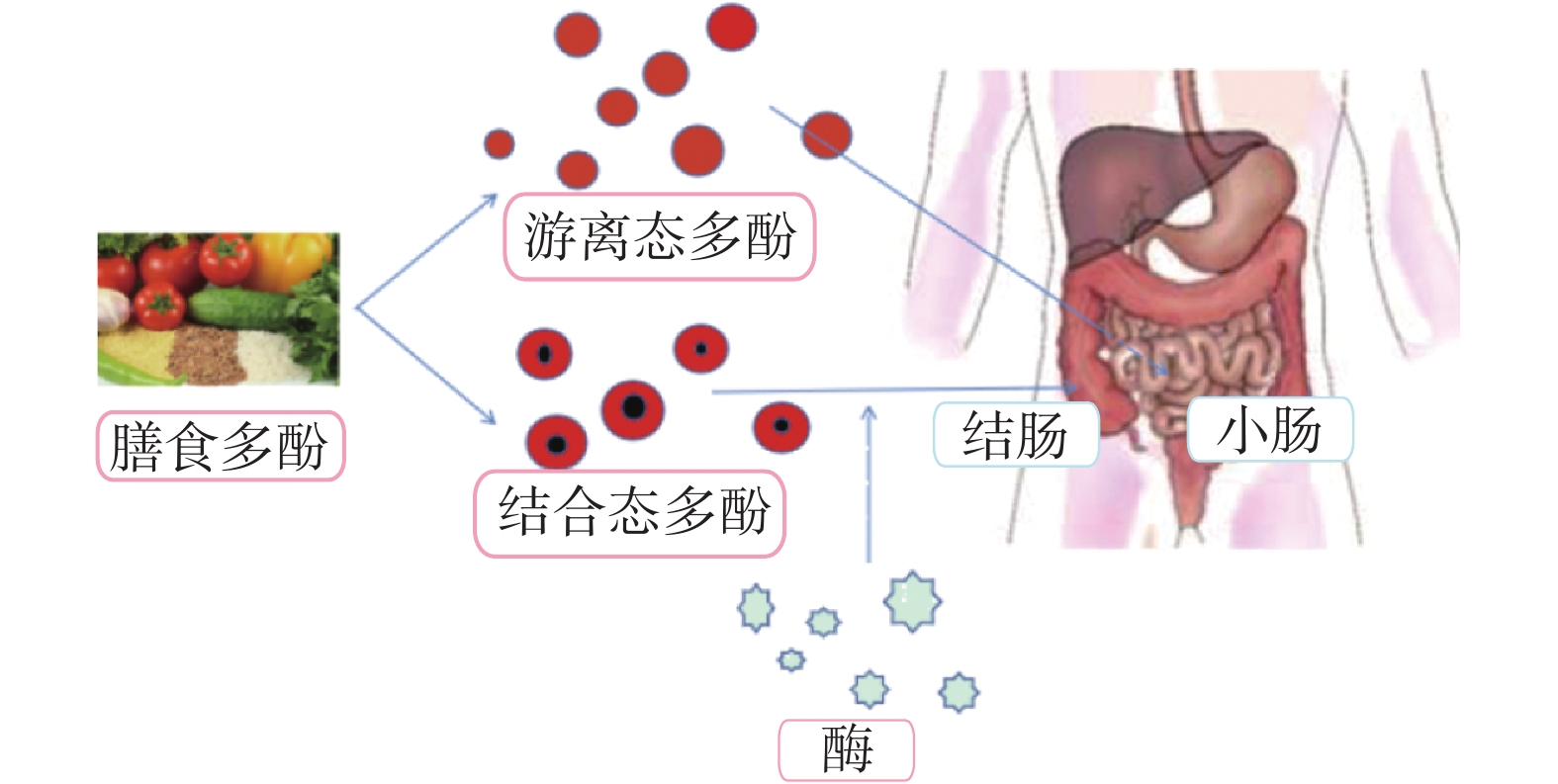
膳食多酚按存在形态被分为游离态多酚和结合态多酚,游离态多酚在小肠中吸收,结合态多酚往往需要到达结肠部位,在此处所分泌的相关代谢酶的作用下降解为游离态,进而被人体吸收利用。肠道微生物对膳食多酚的作用主要表现在两个方面:一是肠道微生物直接作用于结合态多酚,将其降解为游离态多酚;二是在肠道分泌的相关酶作用下将多酚分解代谢并加以吸收利用[55](图2)。
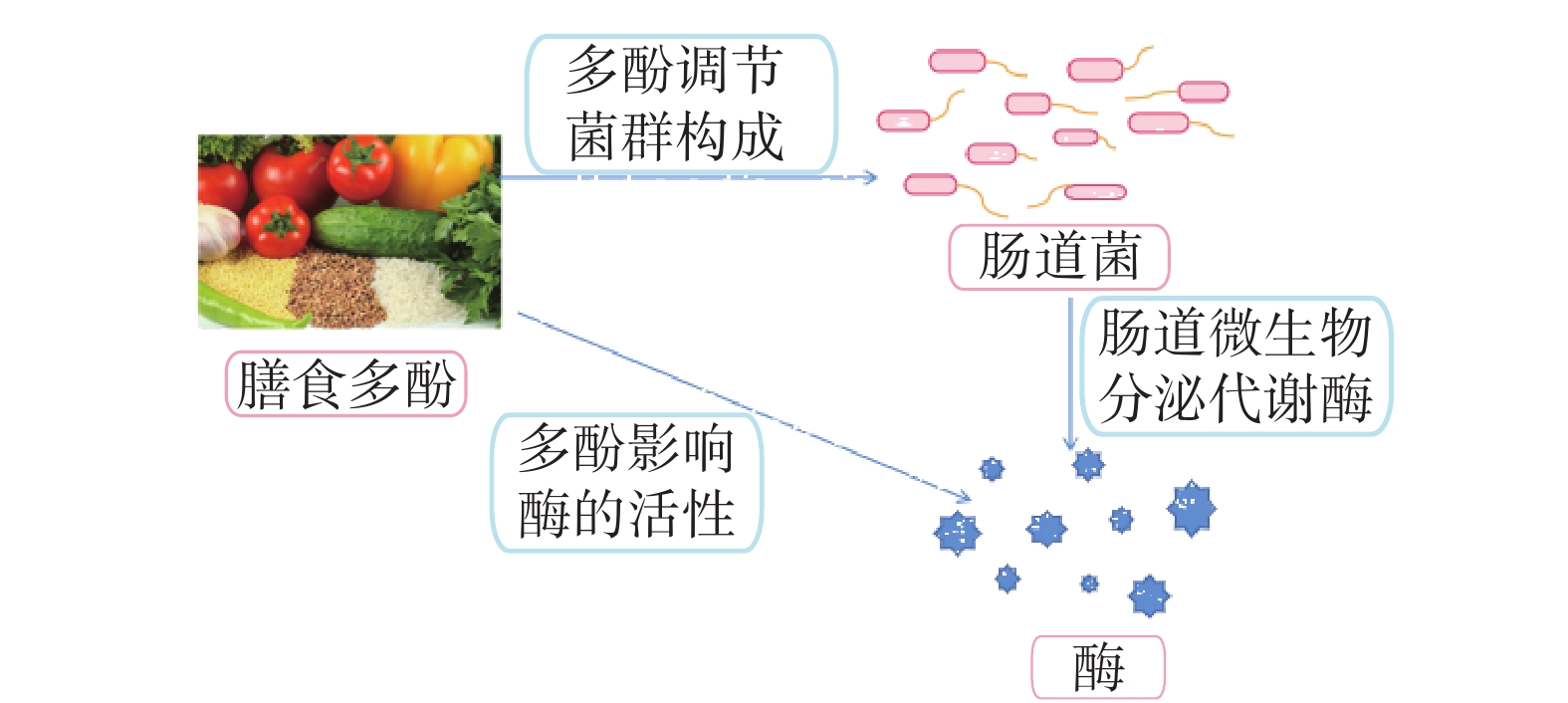
膳食多酚对肠道微生物的影响也表现在两个方面:一是膳食多酚影响肠道菌群的构成;二是膳食多酚影响肠道中酶的活性。具体而言,膳食多酚可选择性地促进有益菌生长,抑制有害菌生长,改变肠道菌群的构成,从而更好地发挥维持人体健康的作用。膳食多酚对酶系统产生的影响可通过多种途径实现,具体途径为:多酚通过改变肠道微生物的种类与数量来影响肠道中酶的种类与数量;多酚与机体中的金属离子螯合,使部分酶因缺乏辅基而丧失功能活性;多酚还可直接抑制酶的活性(图3)。
LEE等[56]探究茶多酚及其代谢物与肠道菌群间的相互作用。茶多酚在粪便中所含的诸多菌群的作用下代谢加速,包括表儿茶素、儿茶素、三甲氧基没食子酸、没食子酸和咖啡酸等,在肠道菌作用下产生了菌群可利用的芳香族代谢物。茶多酚及其衍生物可显著抑制产气梭菌、艰难梭菌和拟杆菌的生长,而其他梭菌菌属、双歧杆菌以及乳酸菌则没有显著变化。因此肠道菌群促进多酚代谢,使其代谢物在肠道中得到积累,从而发挥相应的生理作用;而多酚及其代谢也可对肠道菌群的生长情况产生相应的促进或抑制作用。此外,梭菌和拟杆菌会增加结肠癌的患病风险,茶多酚对梭菌和拟杆菌生长的抑制作用会降低结肠癌的患病风险[57-58]。益生菌中的乳酸菌和双歧杆菌可以维持肠道菌群平衡和肠道微生态环境。乳酸菌和双歧杆菌可降低大肠中胺源致癌物的增加。芳香族代谢物的存在不会对益生元生长产生影响,因此在多酚代谢物存在的情况下肠道中有益菌仍可定植,并调控肠道菌群的数量和结构,促进有益菌生长,抑制有害菌生长,进而维持肠道菌群平衡[59]。这项研究表明,肠道菌群与多酚及其代谢物之间存在着复杂的相互关系。经日常饮食摄入的多酚类物质会对人体肠道菌群造成波动。酚类物质可调控菌群生长,既可刺激肠道中有益菌生长,也可抑制病原菌的生长,促进肠道对营养物质的吸收利用。
FOGLIANO等[60]在体外研究中发现,不溶于水的可可馏分的细菌发酵与双歧杆菌和乳酸菌的增殖以及丁酸盐的生成有关,这些微生物的变化与血浆三酰基甘油和C反应蛋白的降低有关,表明膳食中添加富含黄酮醇的食物成分会对机体健康产生有益影响。有研究表明,单体黄烷-3醇和富含黄烷-3醇来源的物质,如巧克力、绿茶和黑加仑或葡萄籽提取物,可在体内调节肠道菌群,产生诸如乳酸菌一类的有益菌,并抑制如梭状芽孢杆菌一类的有害菌,生成的有益菌可调节人体肠道,促进营养物质吸收,被抑制的有害菌可降低疾病的发生[61]。
VENDRAME等[62]通过对饮用野生蓝莓饮料六周前后的志愿者粪便进行研究,研究发现,饮用蓝莓饮料后粪便中双歧杆菌和嗜酸乳杆菌数量增加。双歧杆菌和乳酸菌的细菌活性对人体健康有着积极作用,可以抑制微生物群中致癌酶活性,降低癌变机率;抑制病原菌生长。这项研究表明,饮用野生蓝莓饮料可以调节肠道菌群结构,促进有益菌增殖,使野生蓝莓饮料中的有益成分加速吸收。FEMIA等[61]设置空白对照组和多酚组饲喂大鼠15周后,发现对照组大鼠粪便中主要的微生物为拟杆菌、梭状芽孢杆菌和丙酸杆菌,而多酚处理组发现的是拟杆菌、乳酸杆菌和双歧杆菌。由于乳酸菌和双歧杆菌被认为对肠道功能有益,而梭菌对结肠粘膜会产生有害作用,因此,这些肠道菌群结构的改变提供了对致癌物、炎症或氧化应激加强的保护。
总而言之,膳食中的多酚类物质及其代谢物与肠道菌群间存在着复杂的相互作用,共同促进人体健康。
4. 结语与展望
多酚类物质被认为是膳食中的重要健康因子,可发挥益生元功效。因其具有抗氧化、抗炎和其他有益作用,对心脏代谢、神经系统及肿瘤防御等疾病方面有着非常积极的影响,也对不健康膳食习惯所造成的肠道菌群紊乱和维持肠道菌群稳定过程发挥了重要的调节作用,而膳食多酚对肠道菌群在宿主的多种生理和代谢机制中起着重要作用。但多酚因其复杂的结构特征导致其生物利用率较低,为解决这一问题,研究者需研发更多方法,提高其在胃肠道间的转运效率,并促进其向肠道目标部位输送更高浓度的多酚类化合物,以提高其利用率。尽管多酚类物质生理功能方面的机制仍需进一步研究,但目前研究已取得许多积极的进展,这也为多酚类物质在调节肠道菌群及预防因肠道菌群紊乱诱发的相关疾病方面的应用提供了思路。
-
表 1 膳食多酚对肠道菌群的调控
Table 1 Regulation of dietary polyphenols on intestinal microbiota
多酚种类 多酚对肠道菌群的影响 多酚对菌群结构及多样性等的影响 参考文献 茶多酚 对乳杆菌的增殖效果明显,呈剂量依赖性 提高了肠道菌群多样性 于子婷等[36] 肠道中埃希氏菌属和γ-变形菌纲_B38含量下降,拟杆菌属和双歧杆菌属含量提高 吴根梁等[37] 拟杆菌门丰度增加,厚壁菌门丰度下降 GUO等[38] 葡萄多酚 提高了双歧杆菌、乳杆菌含量,抑制溶组织梭菌和普雷沃氏菌属的生长,但细菌总数没有明显变化 调节肠道菌群结构,发挥对人体的
有益作用ZHOU等[40] 双歧杆菌含量显著增加,梭菌和乳酸菌含量有所变化,但细菌总数没有明显变化 DOLARA等[41] 拟杆菌属含量提高,并增加了粪便中丁酸的含量 杨昌铭等[42] 乳酸杆菌和双歧杆菌成为主要菌属,大肠杆菌和肠细菌相对减少 LARROSA等[43] 提高了拟杆菌门和厚壁菌门的比例,促进乳酸菌和双歧杆菌的生长 QIAO等[44] 果蔬多酚 复合菌-荔枝多酚 抑制了部分有害菌的增殖 调节肠道菌群结构,维持肠道微环境稳态,但肠道群落多样性无明显变化 张军丽等[46] 猴桃皮渣多酚
提取物厚壁菌门、拟杆菌门及放线菌门成为主要菌属,使拟杆菌门与厚壁菌门比例显著升高 唐诗等[47] 莓果酚 对葡萄球菌的生长有良好的抑制效果,同时对沙门氏菌的生长也有抑制作用,对乳酸菌没有明显影响 PUUPPONEN-PINIA等[48] 芒果种子多酚
提取物促进革兰氏阳性菌的生长,抑制革兰氏阴性菌的生长 KABUKI等[49] 苹果黄酮 双歧杆菌含量增多,乳酸菌含量明显减少 ESPLEY等[50] 青钱柳黄酮和
三萜促进双歧杆菌和乳酸菌的生长,抑制梭菌和拟杆菌的生长 陈玉慧等[50] 蜂胶多酚 调节菌群结构,缓解炎症症状 增加了肠道菌群多样性 WANG等[52] 可可多酚 促使双歧杆菌和乳杆菌增殖,使梭状芽孢杆菌等厚壁菌门类的微生物丰度下降 调节肠道菌群结构,发挥对人体健康积极的作用,尚未对肠道菌群多样性产生影响 TZOUNIS等[54] 促进双歧杆菌、乳酸杆菌以及真细菌中球菌的生长,并对大肠杆菌的生长状态产生一定的影响 TZOUNIS等[54] -
[1] 王彦淇, 郭玉蓉, 王永涛. 等. 不同品种苹果非浓缩还原汁的多酚组成及与抗氧化能力的关系[J]. 中国食品学报,2020,20(5):74−83. [LI H X, GUO Y R, WANG Y T, et al. Analyses of phenolic composition and antioxidant activities of NFC apple juices from different cultivars[J]. Journal of Chinese Institute of Food Science and Technology,2020,20(5):74−83. [2] 颜才植, 叶发银, 赵国华. 食品中多酚形态的研究进展[J]. 食品科学,2015,36(15):249−254. [YAN C Z, YE F Y, ZHAO G H. A review of studies on free and bound polyphenols in foods[J]. Food Science,2015,36(15):249−254. doi: 10.7506/spkx1002-6630-201515046 [3] 戴倩倩, 樊雨梅, 张晓旭. 等. 朝鲜蓟茎叶副产物青贮过程中多酚及其功能活性的研究[J]. 中国食品学报,2020,20(2):263−270. [DAI Q Q, FAN Y M, ZHANG X X, et al. Studies on polyphenol and its function activity of by-production of Artichoke’s stem and leaves during the ensile[J]. Journal of Chinese Institute of Food Science and Technology,2020,20(2):263−270. [4] 隋晓楠, 黄国, 刘贵辰. 大豆蛋白质-植物多酚互作的研究进展[J]. 中国食品学报,2019,19(7):1−10. [SUI X N, HUANG G, LIU G C. A review on the interactions between soy protein-plant polyphenols[J]. Journal of Chinese Institute of Food Science and Technology,2019,19(7):1−10. [5] 于娟, 纪海玉, 白云. 等. 红茶多酚对H22荷瘤小鼠的免疫调节和抗氧化作用[J]. 中国食品学报,2019,19(10):49−55. [YU J, JI H Y, BAI Y, et al. Immunoregulatory and antioxidant activities of black tea polyphenols on H22-bearing mice[J]. Journal of Chinese Institute of Food Science and Technology,2019,19(10):49−55. [6] 左丹, 廖霞, 李瑶, 等. 基于肠道吸收机制的膳食多酚代谢研究进展[J]. 食品科学,2017(7):266−271. [ZUO D, LIAO X, LI Y, et al. Progress in research on dietary polyphenols metabolism based on a mechanism involving intestinal absorption[J]. Food Science,2017(7):266−271. doi: 10.7506/spkx1002-6630-201707042 [7] 文秋, 杨瑞瑞, 金晓露. 植物多酚对畜禽肠道健康的保护作用研究进展[J]. 中国科学:生命科学,2020,50(9):914−926. [WEN Q, YANG R R, JIN X L. Research advances on the beneficial effects of plant polyphenols on intestinal health in farm animals[J]. Science in China: Life Sciences,2020,50(9):914−926. [8] AMIT S, ANUPAM B, ABHAY P. Targeting histone deacetylases with natural and synthetic agents: An emerging anticancer strategy[J]. Nutrients,2018,10(6):731. doi: 10.3390/nu10060731
[9] JACOBS, PROBIOTICS P. What are they and how do they affect obesity?[J]. Journal of Pediatric Surgical Nursing,2017,6(3):53−55. doi: 10.1097/JPS.0000000000000140
[10] 张静之, 包春辉, 施征, 等. 肠道菌群参与炎症性肠病发病机制研究新进展[J]. 世界华人消化杂志,2016,24(33):4505−4513. [ZHANG J Z, BAO C H, SHI Z, et al. Role of intestinal microbiota in pathogenesis of inflammatory bowel disease[J]. World Chinese Journal of Digestology,2016,24(33):4505−4513. doi: 10.11569/wcjd.v24.i33.4505 [11] MARCHESI J R, ADAMS D H, FAVA F, et al. The gut microbiota and host health: A new clinical frontier[J]. Gut,2016,65:330−339. doi: 10.1136/gutjnl-2015-309990
[12] KRISHNAN S, ALDEN N, LEE K. Pathways and functions of gut microbiota metabolism impacting host physiology[J]. Current Opinion in Biotechnology, 2015, 36 : 137-145.
[13] BULL M J, PLUMMER N T. Part 1: The human gut microbiome in health and disease[J]. Integr Med,2014,13(6):17−22.
[14] WU H J, WU E. The role of gut microbiota in immune homeostasis and autoimmunity[J]. Gut Microbes,2012,3(1):4−14. doi: 10.4161/gmic.19320
[15] THOREUX K, SENEGAS-BALAS F, BERNARD-PERRONE F, et al. Modulation of proliferation, second messenger levels, and morphotype expression of the rat intestinal epithelial cell line IEC-6 by fermented milk[J]. Journal of Dairy Ence,1996,79(1):33−43.
[16] SEKIROV I, RUSSELL S. L, ANTUNES L C, et al. Gut microbiota in health and disease[J]. Physiol Rev,2010,90:859−904. doi: 10.1152/physrev.00045.2009
[17] MICHAEL C, ANTHONY B. The impact of diet and lifestyle on gut microbiota and human health[J]. Nutrients,2015,7(1):17−44.
[18] XIAO M B, LIANG C, BEI G, et al. Gut microbiome response to sucralose and its potential role in inducing liver inflammation in mice[J]. Frontiers in Physiology,2017:8.
[19] RAN A, ELLEN W, AD A M M, et al. Age-dependent changes in GI physiology and microbiota: Time to reconsider?[J]. Gut,2018:2213−2222.
[20] WU X K, MA C F, HAN L, et al. Molecular characterisation of the faecal microbiota in patients with type II diabetes[J]. Current Microbiology,2010(61):69−78.
[21] LOOFT T, ALLEN H K. Collateral effects of antibiotics on mammalian gut microbiomes[J]. Gut Microbes,2012,3(5):463−467. doi: 10.4161/gmic.21288
[22] WILLING B P, RUSSELL S L, FINLAY B B. Shifting the balance: Antibiotic effects on host-microbiota mutualism[J]. Nat Rev Microbiol,2011,9:233−243. doi: 10.1038/nrmicro2536
[23] MODI S R, COLLINS J J, RELMAN D A. Antibiotics and the gut microbiota[J]. Journal of Clinical Investigation,2014,124(10):4212−4218. doi: 10.1172/JCI72333
[24] 杨立娜, 吴凯为, 朱力杰, 等. 益生元、多酚、蛋白质和多不饱和脂肪酸对肠道健康的影响[J]. 食品工业科技,2017(22):336−340. [YANG L N, WU K W, ZHU L J, et al. Effect of prebiotics, phytochemicals, protein and polyunsaturated fatty acids on intestinal health[J]. Science and Technology of Food Industry,2017(22):336−340. [25] FERNANDES R, VIANA S D, NUNES S, et al. Diabetic gut microbiota dysbiosis as an inflammaging and immunosenescence condition that fosters progression of retinopathy and nephropathy[J]. Biochimica et Biophysica Acta(BBA)-Molecular Basis of Disease,2018:1865.
[26] FRANKS, PAUL. Exposing the exposures responsible for type 2 diabetes and obesity[J]. Science,2016,354(6308):69−73. doi: 10.1126/science.aaf5094
[27] RÉMY BURCELIN. Gut microbiota and immune crosstalk in metabolic disease[J]. Molecular Metabolism,2016,5(9):771−781. doi: 10.1016/j.molmet.2016.05.016
[28] GOMES J M G. Metabolic endotoxemia and diabetes mellitus: A systematic review[J]. Metabolism-clinical & Experimental,2017,68:133−144.
[29] KEARN J, LUDLOW E, DILLON J, et al. Fluensulfone is a nematicide with a mode of action distinct from anticholinesterases and macrocyclic lactones[J]. Pesticide Biochemistry and Physiology,2014,109:44−57. doi: 10.1016/j.pestbp.2014.01.004
[30] WANG X Y, WANG D Y, YU H X, et al. Toxicity evaluation of purified terephthalic acid wastewater by using model Caenorhabditis elegans[J]. The Journal of Applied Ecology, 2007, 18(7): 1669−1672.
[31] BLANDINO G, INTURRI R, LAZZARA F, et al. Impact of gut microbiota on diabetes mellitus[J]. Diabetes & Metabolism,2016:303−315.
[32] APPELDOORN M M, VINCKEN J P, GRUPPEN H, et al. Procyanidin dimers A1, A2, and B2 are absorbed without conjugation or methylation from the small intestine of rats[J]. Journal of Nutrition,2009,139(8):1469. doi: 10.3945/jn.109.106765
[33] MANACH, WILLIAMSON, MORAND, et al. Bioavailability and bioefficacy of polyphenols in humans I. Review of 97 bioavailability studies[J]. The American Journal of Clinical Nutrition, 2005.
[34] BOWEY E, ADLERCREUTZ H, ROWLAND I. Metabolism of isoflavones and lignans by the gut microflora: A study in germ-free and human flora associated rats[J]. Food Chem Toxicol,2003,41:631−636. doi: 10.1016/S0278-6915(02)00324-1
[35] 邝生鲁. 现代精细化工高新技术与产品合成工艺[M]. 科学技术文献出版社, 2000. KUANG S L. Moderm fine chemical high and new technology and product synthesi technology[M]. Scientific and Technical Literature Press, 2000.
[36] 于子婷. 不同浓度茶多酚服用对小鼠肠道菌群的影响研究[J]. 实验动物科学,2019,36(2):38−41, 46. [YU Z T. Effects of different concentrations of tea polyphenols on intestinal flora in mice[J]. Laboratory Animal Science,2019,36(2):38−41, 46. doi: 10.3969/j.issn.1006-6179.2019.02.007 [37] 吴根梁, 侯爱香, 李珂, 等. 陈年茯砖茶多酚类对老年人肠道菌群的影响研究[J]. 茶叶科学,2018,38(3):319−330. [WU G L, HOU A X, LI K, et al. Effects of polyphenols of Old Fu Brick Tea on the elderly intestinal flora[J]. Journal of Tea Science,2018,38(3):319−330. doi: 10.3969/j.issn.1000-369X.2018.03.013 [38] GUO X, CHENG M, ZHANG X, et al. Green tea polyphenols reduce obesity in high-fat diet-induced mice by modulating intestinal microbiota composition[J]. International Journal of Food Science & Technology,2017,52(8):1723−1730.
[39] 徐维盛, 杨月欣. 植物膳食多酚及其定量分析方法的研究进展[J]. 食品安全质量检测学报,2013(3):737−744. [XU W Y, YANG Y X. Technologies in quantification of plant polyphenols and its research progress[J]. Journal of Food Safety and Quality Inspection,2013(3):737−744. [40] ZHOU L, WANG W, HUANG J, et al. In vitro extraction and fermentation of polyphenols from grape seeds (Vitis vinifera) by human intestinal microbiota[J]. Food & Function,2016,7(4):1959−1967.
[41] DOLARA P, LUCERI C, DE FILIPPO C, et al. Red wine polyphenols influence carcinogenesis, intestinal microflora, oxidative damage and gene expression profiles of colonic mucosa in F344 rats[J]. Mutation Research,2005,591(1):237−246.
[42] 杨昌铭, 肖瀛, 吴其国, 等. 原花青素对小鼠血脂代谢紊乱与肠道菌群干预的影响[J]. 食品科学,2020,41(13):120−126. [YANG C M, XIAO Y, WU Q G, et al. Preventive effect of proanthocyanidin on gut microbiome in dyslipidemic mice[J]. Food Science,2020,41(13):120−126. doi: 10.7506/spkx1002-6630-20190703-053 [43] LARROSA M, YANEZ-GASCO M J, SELMA M V, et al. Effect of a low dose of dietary resveratrol on colon microbiota, inflammation and tissue damage in a DSS-Induced colitis rat model[J]. Journal of Agricultural & Food Chemistry,2009,57(6):2211.
[44] QIAO Y, SUN J, XIA S, et al. Effects of resveratrol on gut microbiota and fat storage in a mouse model with high-fat-induced obesity[J]. Food & Function,2014,5(6):1241−1249.
[45] 王凤, 赵成英, 田桂芳, 等. 果蔬功能成分与肠道菌群相互作用研究进展[J]. 生物产业技术,2017(4):53−61. [WANG F, ZHAO C Y, TIAN G F, et al. Research progress of interactions between functional components of fruits/vegetables and gut microbiota[J]. Biotechnology & Business,2017(4):53−61. [46] 张军丽, 涂杜, 彭新宇, 等. 复合菌-荔枝多酚对腹泻小鼠肠道形态结构和肠道菌群的影响[J]. 食品科学,2018,39(23):142−148. [ZHANG J L, TU D, PENG X Y, et al. Effect of co-administration of mixed probiotic culture and litchi polyphenol on intestinal morphology and intestinal flora of mice with diarrhea[J]. Food Science,2018,39(23):142−148. doi: 10.7506/spkx1002-6630-201823022 [47] 唐诗. 猕猴桃皮渣多酚提取及其对肠道菌群的影响作用研究[C]. 中国营养学会、亚太临床营养学会、江苏省科学技术协会、中国疾病预防控制中心营养与健康所、农业农村部食物与营养发展研究所、中国科学院上海营养与健康研究所. 营养研究与临床实践——第十四届全国营养科学大会暨第十一届亚太临床营养大会、第二届全球华人营养科学家大会论文摘要汇编. 中国营养学会、亚太临床营养学会、江苏省科学技术协会、中国疾病预防控制中心营养与健康所、农业农村部食物与营养发展研究所、中国科学院上海营养与健康研究所: 中国营养学会, 2019: 510−511. TANG S. Study on the extraction of polyphenols from kiwifruit skin residue and its effect on intestinal flora[C]. Chinese Nurtition Society, Asia-pacific Clinical Nutrition Society, Jiangsu Association for Science and Technology, Institute of Nutrition and Health, Chinese Center for Disease Control and Prevention, Institute of Food and Nutrition Development, Ministry of Agriculture and Rural Affairs, Shanghai Institute of Nutrition and Health, Chinese Academy of Sciences. Nutrition Research and Clinical Practice: abstracts of the 14th National Congress of Nutrition Science and the 11th Asia-Pacific Conference of Clinical Nutrition, and the 2nd Global Chinese Congress of Nutrition Scientists. Chinese Nutrition Society, Asia-pacific Clinical Nutrition Society, Jiangsu Association for Science and Technology, Institute of Nutrition and Health, Chinese Center for Disease Control and Prevention, Institute of Food and Nutrition Development, Ministry of Agriculture and Rural Affairs. Shanghai Institute of Nutrition and Health, Chinese Academy of Sciences: Chinese Nutrition Society, 2019: 510−511.
[48] R PUUPPONEN-PIMIÄ, NOHYNEK L, S HARTMANN-SCHMIDLIN, et al. Berry phenolics selectively inhibit the growth of intestinal pathogens[J]. Journal of Applied Microbiology,2010:98.
[49] KABUKI T, NAKAJIMA H, ARAI M, et al. Characterization of novel antimicrobial compounds from mango (Mangifera indica L.) kernel seeds[J]. Food Chemistry,2000,71(1):61−66. doi: 10.1016/S0308-8146(00)00126-6
[50] 陈玉慧, 郭彤彤, 张鑫, 等. 青钱柳黄酮及三萜调节人体肠道菌群作用研究[J]. 中国野生植物资源,2019,38(2):6−10, 15. [CHEN Y H, GUO T T, ZHANG X, et al. Modulatory effect of flavonoids and triterpenoids from Cyclocarya Paliurus on human intestinal microbiota[J]. Wild Plant Resources in China,2019,38(2):6−10, 15. doi: 10.3969/j.issn.1006-9690.2019.02.002 [51] 张红城. 蜜蜂所在蜂胶多酚类成分的提取鉴定方面取得新进展[J]. 中国蜂业,2015,66(11):16−16. [ZHANG H C. New progress has been made in the extraction and identification of polyphenols from propolis[J]. Apiculture of China,2015,66(11):16−16. doi: 10.3969/j.issn.0412-4367.2015.11.005 [52] WANG K, JIN X, YOU M, et al. Dietary propolis ameliorates dextran sulfate sodium-induced colitis and modulates the gut microbiota in rats fed a western diet[J]. Nutrients,2017,9(8):875. doi: 10.3390/nu9080875
[53] 石塔拉. 膳食槲皮素对抗生素诱导菌群失衡小鼠肠道菌群的影响研究[C]. 中国营养学会、亚太临床营养学会、江苏省科学技术协会、中国疾病预防控制中心营养与健康所、农业农村部食物与营养发展研究所、中国科学院上海营养与健康研究所. 营养研究与临床实践——第十四届全国营养科学大会暨第十一届亚太临床营养大会、第二届全球华人营养科学家大会论文摘要汇编. 中国营养学会、亚太临床营养学会、江苏省科学技术协会、中国疾病预防控制中心营养与健康所、农业农村部食物与营养发展研究所、中国科学院上海营养与健康研究所: 中国营养学会, 2019: 509. SHI T L. Effects of dietary quercetin on intestinal microflora in mice with antibiotic-induced imbalance[C]. Chinese Nutrition Society, Asia-pacific Clinical Nutrition Society, Jiangsu Association for Science and Technology, Institute of Nutrition and Health, Chinese Center for Disease Control and Prevention, Institute of Food and Nutrition Development, Ministry of Agriculture and Rural Affairs, Shanghai Institute of Nutrition and Health, Chinese Academy of Sciences. Nutrition research and Clinical Practive: abstracts of the 14th National Congress of Nutrition Science and the 11th Asia-Pacific Conference of Clinical Nutrition, and the 2nd Global Chinese Congress of Nutrition Scientists. Chinese Nutrition Society, Asia-pacific Conference of Clinical Nutrition, and the 2nd Global Chinese Congress of Nutrition Scientists. Chinese Nutrition Society, Asia-pacific Clinical Nutrition Society, Jiangsu Association for Science and Technology, Institute of Nutrition and Health, Chinese Center for Disease Control and Prevention, Institute of Food and Nutrition Development, Ministry of Agriculture and Rural Affairs, Shanghai Institute of Nutrition and Health, Chinese Academy of Sciences: Chinese Nutrition Society, 2019: 509.
[54] TZOUNIS X, VULEVIC J, KUHNLE G G C, et al. Flavanol monomer-induced changes to the human faecal microflora[J]. British Journal of Nutrition,2008,99(4):782−792. doi: 10.1017/S0007114507853384
[55] 杨华, 叶发银, 赵国华. 膳食多酚与肠道微生物相互作用研究进展[J]. 食品科学,2015,36(3):223−227. [YANG H, YE F Y, ZHAO G H. Advances in interactions between gut microflora and dietary polyphenols[J]. Food Science,2015,36(3):223−227. doi: 10.7506/spkx1002-6630-201503043 [56] LEE H C, JENNER A M, LOW C S, et al. Effect of tea phenolics and their aromatic fecal bacterial metabolites on intestinal microbiota[J]. Res in Microbiol,2006,157(9):876−884. doi: 10.1016/j.resmic.2006.07.004
[57] ZHEN-LIN L, BEN-HUA Z, WEI W, et al. Impact of the consumption of tea polyphenols on early atherosclerotic lesion formation and intestinal bifidobacteria in High-Fat-Fed ApoE-/- mice[J]. Front Nutr,2016,3:42.
[58] VINCENZO F, MARIA L C, PAOLA V, et al. In vitro bioaccessibility and gut biotransformation of polyphenols present in the water-insoluble cocoa fraction[J]. Molecular Nutrition & Food Research, 2011, 55(Supplement 1): S44−S55.
[59] 聂启兴, 胡婕伦, 钟亚东, 等. 几类不同食物对肠道菌群调节作用的研究进展[J]. 食品科学,2019,40(11):321−330. [NIE Q X, HU J L, ZHONG Y D, et al. Research progress in the regulation of intestinal flora by several types of foods[J]. Food Science,2019,40(11):321−330. doi: 10.7506/spkx1002-6630-20180113-171 [60] FOGLIANO V, VERDE V, RANDAZZO G, et al. Method for measuring antioxidant activity and its application to monitoring the antioxidant capacity of wines[J]. Journal of Agricultural & Food Chemistry,1999,47(3):1035−1040.
[61] FEMIA A P. Antitumorigenic activity of the prebiotic inulin enriched with oligofructose in combination with the probiotics Lactobacillus rhamnosus and Bifidobacterium lactis on azoxymethane-induced colon carcinogenesis in rats[J]. Carcinogenesis,2002,23(11):1953−1960. doi: 10.1093/carcin/23.11.1953
[62] VENDRAME M, GEMMA C, PENNYPACKER K R, et al. Cord blood rescues stroke-induced changes in splenocyte phenotype and function[J]. Experimental Neurology,2006,199(1):191−200. doi: 10.1016/j.expneurol.2006.03.017





 下载:
下载:
 下载:
下载:



