Extraction Process Optimization and Antioxidant Activity of Polyphenols from Bangia fusco-purpurea
-
摘要: 为研究红毛藻多酚提取工艺及其抗氧化活性,采用溶剂浸提法提取多酚,选取提取时间、提取温度、乙醇体积分数、料液比为单因素,进一步通过正交试验优化确定最佳提取工艺。以DPPH和ABTS自由基清除率为指标,评价红毛藻多酚的抗氧化活性。结果显示,红毛藻多酚的最佳提取工艺为:浸提温度70 ℃,浸提时间70 min,乙醇体积分数60%,料液比1:10 g/mL,此条件下多酚提取量为(9.67 ± 0.14)mg/g。抗氧化活性评价显示,红毛藻多酚对DPPH和ABTS自由基有一定的清除能力,其IC50值分别为0.313、0.445 mg/mL。研究结果表明正交优化提取红毛藻多酚的工艺简单可行,此方法提取多酚具有较强的抗氧化活性。红毛藻多酚具有开发为天然抗氧化剂的潜力,有较好的应用前景。Abstract: In order to study the extraction process and antioxidative activity of polyphenols from Bangia fusco-purpurea, solvent extraction was used to extract polyphenols. The polyphenol content in the extract was used as an index. The extraction time, extraction temperature, ethanol volume fraction, and liquid-liquid ratio were single factors. Further, the optimal extraction process was determined by orthogonal experiment optimization. The clearance rate of DPPH and ABTS free radical were used as indicators to evaluate the antioxidative activity of B. fusco-purpurea polyphenols. The results showed that the optimum extraction conditions were as follows: Extraction temperature 70 ℃, extraction time 70 min, volume fraction of ethanol 60%, ratio of material to liquid 1:10 g/mL.Under these conditions, the extraction amount of B. fusco-purpurea polyphenols was (9.67 ± 0.14) mg/g. Antioxidant activity evaluation showed that B. fusco-purpurea polyphenols had a certain scavenging ability to DPPH• and ABTS+•, with IC50 values of 0.313, 0.445 mg/mL. The results showed that the orthogonal optimization process for extracting B. fusco-purpurea polyphenol was simple and feasible, the polyphenols had certain antioxidant capacity. B. fusco-purpurea polyphenol has the potential to be developed as a natural antioxidant and has a good application prospect.
-
Keywords:
- Bangia fusco-purpurea /
- polyphenol /
- extract technology /
- antioxidant activity
-
红毛藻(Bangia fusco-purpurea)又名红毛菜,是一类原始红藻,属红藻门,红毛菜目,红毛藻属。红毛藻是泛暖温带海藻,主要生长在北大西洋亚热带海区和温带海区以及北太平洋的西部,我国东海和南海沿岸地区是红毛藻的主产地[1]。红毛藻味道鲜美,含有丰富的营养成分,如各种氨基酸、糖质、脂肪酸以及Ca、Mg和K等人体必需元素,其中总氨基酸为38.62%、总糖为27%、总脂肪酸为3.77%、钾为3%[1-3]。有相关文献记载,红毛藻有抗氧化[4]、降血压、滋阴祛火和防治疾病等作用[5],深受我国南部沿海地区以及东南亚地区消费者的喜爱。福建省莆田市是我国红毛藻的主要产地之一,每年约有100 t(干重)的产量,每吨红毛藻价格约10~30万元,通常被作为食品原料销售。目前,红毛藻加工行业存在产品种类单一、附加值低和竞争力弱的问题,开发利用程度较低[6]。
海藻多酚是海藻植物中多酚类化合物的总称,大多以间苯三酚的衍生物和聚合物的形式存在,是具有拒食功能海藻的次级代谢产物[7]。因其具有抑菌[8-9]、抗氧化[10]、抗癌[11]、降血糖[12-13]及治疗肥胖[14-15]等生理活性和药用功能,常被用于食品、化妆品、药品及保健品等领域中。抗氧化是海藻多酚的重要生物活性,海藻多酚分子中的酚性羟基能够切断氧化过程中产生的过氧化物自由基、羟基自由基的链式反应,从而达到抑制和减缓氧化的效果[16],在食品、化妆品和生物医药领域具有重要的开发应用前景。目前国内外对红毛藻的研究多集中在红毛藻多糖、藻红蛋白及其生理学特性,而对关于红毛藻多酚的相关研究较少,现对红毛藻中酚类物质的研究仅仅是检测出红毛藻多酚含量[17],而关于红毛藻中多酚的提取方法和抗氧化能力研究未有相关报道。为充分利用我国丰富的红毛藻资源,应对其进行较为系统的研究,从而提高红毛藻资源的利用率。
因此,本论文以干红毛藻为原料,从其富含的酚类成分的提取工艺优化和抗氧化活性分析入手,采用单因素结合正交试验优化多酚的提取工艺,并以多酚对1,1-苯基-2-苦肼基(1,1-diphenyl-2-picrylhydrazy,DPPH)及2,2'-联氨-双-3-乙基苯并噻唑啉-6-磺酸(2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)的清除率考察红毛藻多酚的抗氧化活性,旨在获得红毛藻多酚的最优化提取工艺,研究红毛藻的抗氧化活性,为红毛藻的综合加工利用奠定前期基础。
1. 材料与方法
1.1 材料与仪器
红毛藻 福建莆田南日镇人工养殖产品,购于2019年1月;ABTS、DPPH、福林酚、没食子酸 标准品 上海麦克林生化科技有限公司;无水乙醇、无水碳酸钠、过硫酸钾、维生素 C(Vitamin C, VC) 分析纯,西陇化工股份有限公司。
SB-1100旋转蒸发仪 上海爱朗仪器有限公司;RE-AA真空冷冻干燥机 美国Thermo公司;SPH-200B恒温培养振荡器 上海世平实验设备有限公司;En Spire2300型酶标仪 美国伯腾仪器有限公司;H2050R离心机 厦门亿辰科技有限公司;DHG-101B型烘箱 佰辉仪器设备有限公司。
1.2 实验方法
1.2.1 红毛藻多酚的提取
将50 ℃恒温干燥后的红毛藻粉碎过60目筛,得到红毛藻藻粉。取1.0 g的藻粉加入一定量的乙醇溶剂,在设定好的温度下浸提一定时间,再经8000 r/min离心15 min,取上清液测定多酚的提取量。
1.2.2 没食子酸标准曲线的绘制
以参考文献方法[18],以没食子酸为对照品,采用福林酚法,测定样品溶液在762 nm波长处的吸光度值,以没食子酸标准品的浓度X(mg/mL)作为横坐标、762 nm处测得的吸光值Y为纵坐标,制作标准曲线,得到的回归方程为Y=125.79X+0.0564,R2=0.9991。
1.2.3 红毛藻多酚含量计算
吸取1 mL多酚提取液于具塞试管中,加入1.5 mL福林酚试剂,混匀静置3 min,随后加入3 mL 12%的Na2CO3溶液, 定容至10 mL,混匀避光反应2 h,于762 nm测定吸光值。利用标准曲线计算红毛藻多酚浓度,按下式计算红毛藻多酚提取量:
多酚提取量(mg/g)=C×V×nm 式中:C为红毛藻多酚的浓度,mg/mL;V为多酚提取液总体积,mL;n为稀释倍数;m为红毛藻粉质量,g。
1.2.4 单因素实验
1.2.4.1 提取时间对多酚提取效果的影响
准确称取5份1.0 g红毛藻藻粉,分别置于100 mL的离心管中,固定浸提温度70 ℃,料液比1:20 g/mL,乙醇体积分数65%,设定浸提时间40、50、60、70、80 min,研究多酚提取量的变化趋势。
1.2.4.2 提取温度对多酚提取效果的影响
准确称取5份1.0 g红毛藻藻粉,分别置于100 mL的离心管中,固定乙醇体积分数65%,料液比1:20 g/mL,提取时间1 h,设定提取温度60、65、70、75、80 ℃,研究多酚提取量的变化趋势。
1.2.4.3 料液比对多酚提取效果的影响
准确称取5份1.0 g红毛藻藻粉,分别置于100 mL的离心管中,固定乙醇体积分数65%,提取温度70 ℃,提取时间1 h,设定料液比1:10、1:20、1:30、1:40、1:50(g/mL),研究多酚提取量的变化趋势。
1.2.4.4 乙醇体积分数对多酚提取效果的影响
准确称取5份1.0 g红毛藻藻粉,分别置于100 mL的离心管中,固定提取温度70 ℃,料液比1:20 g/mL,提取时间1 h,设定乙醇体积分数50%、55%、60%、65%、70%,研究多酚提取量的变化趋势。
1.2.5 正交试验设计
以单因素实验结果,运用L9(34)正交试验(表1),研究提取时间、提取温度、料液比和乙醇体积分数对红毛藻多酚提取的影响,对提取工艺进行优化。
表 1 正交试验因素水平表Table 1. Factors and levels of orthogonal test水平 A提取时间(min) B提取温度(℃) C料液比(g/mL) D乙醇体积分数(%) 1 50 65 1:10 55 2 60 70 1:20 60 3 70 75 1:30 65 1.2.6 抗氧化试验
1.2.6.1 DPPH自由基清除能力测定
按参考文献方法[19]适当修改,现配制0.1 mmol/L的DPPH乙醇溶液,及不同浓度的多酚样品溶液,在试管中先加入2 mL DPPH乙醇溶液再加入1.5 mL的多酚样品溶液,混匀后置于37 ℃,暗条件下反应30 min,结束后测定517 nm 处吸收值,以VC作对照,计算DPPH自由基的清除率。
DPPH自由基清除率(%)=(1−A1−A2A0)×100 式中: A0:1.5 mL蒸馏水+2 mL DPPH乙醇溶液的吸光值;A1:1.5 mL样品溶液或VC+2 mL DPPH乙醇溶液的吸光值;A2:1.5 mL样品溶液或VC+2 mL无水乙醇的吸光值。
1.2.6.2 ABTS自由基清除能力测定
参考文献方法[20],将7 mmol/L ABTS与2.45 mmol/L过硫酸钾等比例混合静置过夜12 h,配得ABTS母液,无水乙醇将母液稀释至其在 734 nm处吸光度稳定在0.70 ± 0.02。取不同浓度的多酚样品溶液0.1 mL加入ABTS稀释液1 mL,混匀并于室温反应6 min,测定734 nm处的吸光度,以VC为对照,计算ABTS自由基清除率。
ABTS自由基清除率(%)=(1−A1−A2A0)×100 其中,A0:0.1 mL 蒸馏水 + 1 mL ABTS溶液的吸光值;A1:0.1 mL样品溶液或VC + 1 mL ABTS溶液的吸光值;A2:0.1 mL样品溶液或VC + 1 mL无水乙醇吸光值。
1.3 数据处理
每个试验重复3次,结果以平均值 ± 标准差(X ± SD)表示,采用 Excel 2010 处理数据,SPSS 19.0对数据进行统计分析,并用Origin8.5作图,差异显著分析中,*表示差异显著,P<0.05,**表示差异极显著,P<0.01。
2. 结果与分析
2.1 单因素实验结果
2.1.1 提取时间对红毛藻多酚提取量的影响
由图1可知,提取初始时,增加提取时间使得红毛藻多酚提取量不断增加,在60 min时达到最高,但继续增加提取时间,多酚的提取率反而降低。这可能是由于浸提60 min时,多酚溶出已达到平衡,随提取时间增加,溶液中溶出的红毛藻多酚逐渐被氧化损耗,使多酚物质被分解致使变性,结构遭到破坏,导致红毛藻多酚的提取量下降[21],此外长时间的提取会造成资源浪费。因此,选择60 min作为红毛藻多酚的最佳提取时间。
2.1.2 提取温度对红毛藻多酚提取量的影响
由图2可知,红毛藻多酚提取量随着提取温度的升高呈直线升高而后下降,当提取温度70 ℃时,多酚提取量达到最高,为8.60 mg/g。当温度增加至80 ℃时,多酚提取量降低。这可能是由于温度的升高加快了分子运动,增加酚类物质溶出,从而提高了红毛藻多酚的提取量。但温度过高可能使得多酚的分子结构发生变化,另外高温加速了红毛藻多酚的氧化及降解,导致红毛藻多酚提取量降低[22]。因此,选择温度70 ℃作为红毛藻多酚的最佳提取温度。
2.1.3 料液比对红毛藻多酚提取量的影响
由图3可知,在料液比 1:10 g/mL溶液过于黏稠,提取不充分,随着料液比的增加,溶液黏度下降,使细胞内外多酚有较高的浓度差,促进使红毛藻中酚类物质向提取液中扩散[23],在料液比增大到1:20 g/mL时,多酚提取量达到最大,为8.35 mg/g。但当继续提高溶剂的体积,多酚的提取量随之下降,是因为当提取剂达到一定量时,多酚已基本浸出,而此时有多糖、色素等其他物质溶出,出现反渗透现象,导致多酚提取量下降。因此,选择1:20 g/mL作为红毛藻多酚提取的最佳料液比。
2.1.4 乙醇体积分数对红毛藻多酚提取量的影响
由图4可知,当乙醇浓度在50%~60%时,红毛藻多酚提取量随着体积分数增加而增长,乙醇体积分数达到60%时,多酚的提取量达到最大。而后,随乙醇浓度的提高,多酚提取量呈下降趋势。这情况可能是由于乙醇浓度过高,多酚与溶剂极性相差较大,蛋白质变性,导致多酚溶解度降低,同时醇溶性杂质、色素成分的溶出也会影响提取效果[24-25]。因此,选择体积分数为60%的乙醇作为最佳提取溶剂。
2.2 正交试验结果
运用正交试验优化溶剂浸提法提取红毛藻中总多酚,平行测定三次,得出工艺优化结果见表2。优化得到红毛藻多酚的最佳提取工艺:A3B2C1D2,即提取时间70 min、提取温度70 ℃、料液比1:10 g/mL、乙醇体积分数60%。由极差结果可知,影响提取效果的主次顺序为:C(料液比)>A(提取时间)>B(提取温度)>D(乙醇体积分数)。采用SPSS进行方差分析,进一步研究各因素对红毛藻总酚提取效果的影响结果见表3。由此得知,料液比、提取时间、提取温度、乙醇体积分数均极显著影响红毛藻多酚提取效果(P<0.01)。在最佳条件下提取红毛藻多酚对其进行平行验证试验,得到多酚提取量为(9.67 ± 0.14)mg/g。此方法提取的红毛藻多酚提取量高于昆布(1.79 mg/g)[26]和龙须菜(1.62 mg GAE/g)[27],说明此方法提取红毛藻多酚是可行的。
表 2 正交试验结果Table 2. The results of orthogonal test试验号 A B C D 多酚提取量(mg/g) 1 1 1 1 1 8.33 ± 0.13 2 1 2 2 2 8.61 ± 0.17 3 1 3 3 3 6.05 ± 0.15 4 2 1 2 3 7.6 ± 0.14 5 2 2 3 1 6.19 ± 0.16 6 2 3 1 2 8.70 ± 0.17 7 3 1 3 2 6.74 ± 0.13 8 3 2 1 3 9.23 ± 0.14 9 3 3 2 1 8.95 ± 0.11 k1 7.67 7.56 8.76 7.83 k2 7.50 8.01 8.39 8.02 k3 8.31 7.90 6.33 7.63 R 0.81 0.45 2.43 0.39 表 3 方差分析结果Table 3. The variance analysis results因素 偏差平方和 自由度 均方 F值 显著性 A 3.264 2 1.632 77.913 ** B 1.006 2 0.503 24.023 ** C 30.711 2 15.355 733.015 ** D 0.684 2 0.342 16.337 ** 误差 0.377 18 0.021 注:**表示极显著,P<0.01;*表示显著,P<0.05。 2.3 抗氧化结果
2.3.1 红毛藻多酚对DPPH自由基清除能力
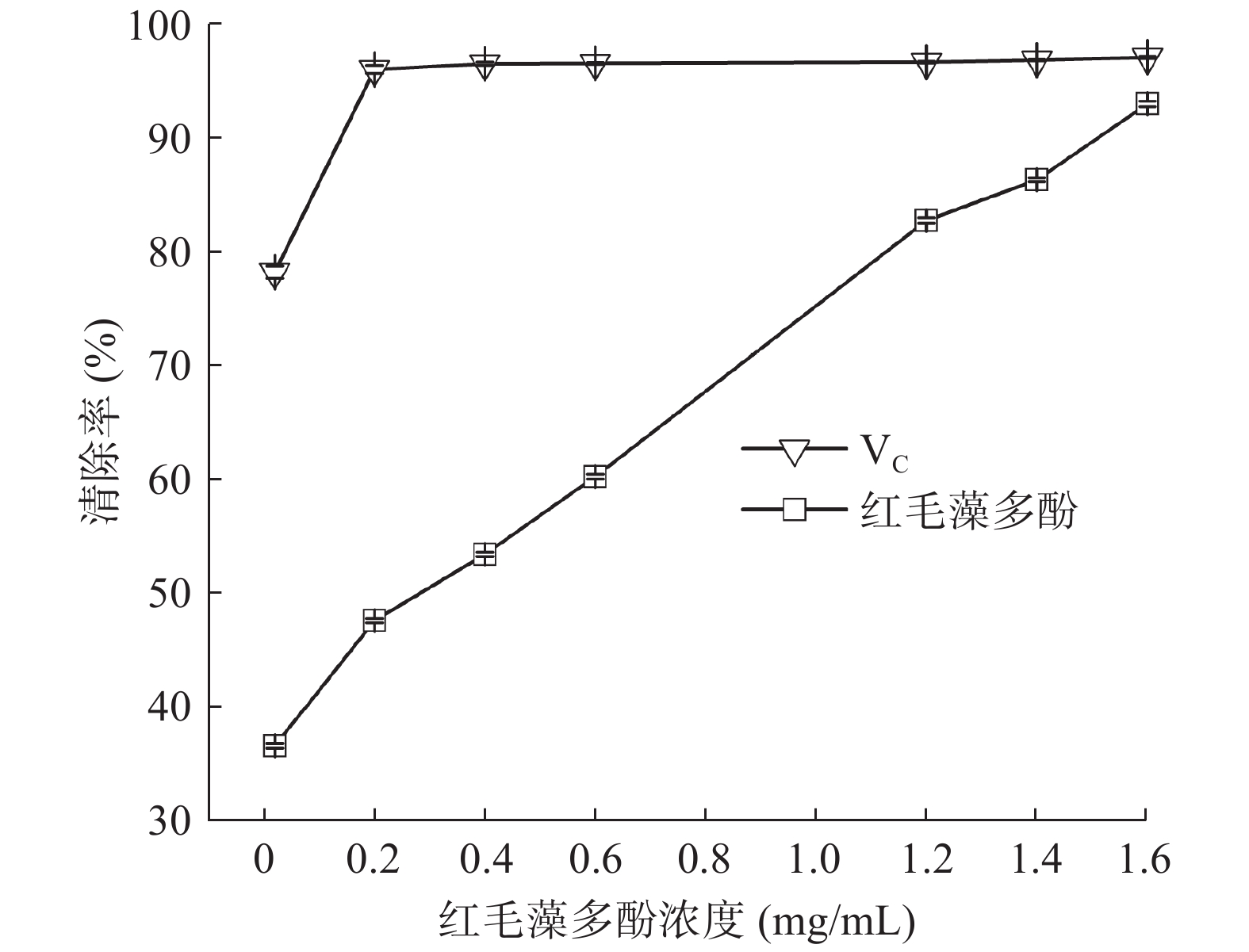
DPPH醇溶液呈紫色,在517 nm处有最大吸收,海藻多酚可捕捉DPPH自由基的单电子,使其颜色变浅,从而降低吸收值,因而根据吸收值的变化,判断多酚抗氧化效果[28]。由图5可知,红毛藻多酚自由基清除率随质量浓度增加而增大,其浓度从0.2 mg/mL增加至1.6 mg/mL时,多酚对DPPH自由基的清除率从36.7%上升至93.1%。VC的清除率在高浓度时一直保持在96.9%。由试验结果得到红毛藻多酚IC50为0.313 mg/mL,多酚在较低浓度时对DPPH自由基的清除能力低于VC,但增加多酚浓度其抑制效果逐渐接近VC,增幅较为明显。红毛藻多酚的抗氧化结果可能与红毛藻原料的处理方式有关,日晒、烘干使得多酚由于高温或空气氧化原因被降解,抗氧化活性降低[29]。研究认为某种物质清除自由基的IC50小于10 mg/mL,表明其具有一定的抗氧化作用[30],由此可见红毛藻多酚仍表现出较好的清除DPPH自由基效果。
2.3.2 红毛藻多酚对ABTS自由基清除能力
ABTS被氧化后得到稳定的蓝绿色ABTS +·,当反应体系中存在抗氧化活性成分时,ABTS自由基与其反应被清除,使得溶液颜色变浅,从而在734 nm处的吸光度降低。研究表明,吸光度越低,多酚的抗氧化能力越强,颜色越浅[31]。由图6可知,低浓度时多酚的清除自由基能力始终低于VC,但随着多酚浓度的增加,清除率不断提高,并显示浓度依赖性。红毛藻多酚浓度在0.445 mg/mL时抑制率达到50%。而当多酚浓度在1.4 mg/mL时,自由基清除率达到96.6%,与同浓度的VC清除效果相差较小,表明红毛藻多酚具有较好的清除ABTS自由基的能力。
3. 结论
采用单因素实验和正交试验对红毛藻多酚的提取工艺进行优化,最佳提取工艺组合为:提取时间70 min、提取温度70 ℃、料液比1:10 g/mL、乙醇体积分数60%,得到多酚提取量为(9.67 ± 0.14)mg/g。此乙醇溶液浸提红毛藻多酚的提取方法具有低毒性和操作简单的优势,具有可行性。由抗氧化试验结果表明,红毛藻多酚具有良好的抗氧化能力,其清除DPPH自由基、ABTS自由基的IC50值分别为0.313、0.445 mg/mL。红毛藻多酚清除自由基能力与多酚浓度呈正相关,且其抗氧化效果均高于铜藻、泡叶藻、树皮藻[32],呈现较突出的抗氧化作用。红毛藻中含有较为丰富的多酚,具有较强的抗氧化活性,可发展成为天然抗氧化剂或食品添加剂,从而提高红毛藻多酚的综合利用价值。本研究为进一步深入开展对红毛藻多酚提取、活性的研究提供基础参考,为拓展红毛藻深加工产品领域提供思路。
-
表 1 正交试验因素水平表
Table 1 Factors and levels of orthogonal test
水平 A提取时间(min) B提取温度(℃) C料液比(g/mL) D乙醇体积分数(%) 1 50 65 1:10 55 2 60 70 1:20 60 3 70 75 1:30 65 表 2 正交试验结果
Table 2 The results of orthogonal test
试验号 A B C D 多酚提取量(mg/g) 1 1 1 1 1 8.33 ± 0.13 2 1 2 2 2 8.61 ± 0.17 3 1 3 3 3 6.05 ± 0.15 4 2 1 2 3 7.6 ± 0.14 5 2 2 3 1 6.19 ± 0.16 6 2 3 1 2 8.70 ± 0.17 7 3 1 3 2 6.74 ± 0.13 8 3 2 1 3 9.23 ± 0.14 9 3 3 2 1 8.95 ± 0.11 k1 7.67 7.56 8.76 7.83 k2 7.50 8.01 8.39 8.02 k3 8.31 7.90 6.33 7.63 R 0.81 0.45 2.43 0.39 表 3 方差分析结果
Table 3 The variance analysis results
因素 偏差平方和 自由度 均方 F值 显著性 A 3.264 2 1.632 77.913 ** B 1.006 2 0.503 24.023 ** C 30.711 2 15.355 733.015 ** D 0.684 2 0.342 16.337 ** 误差 0.377 18 0.021 注:**表示极显著,P<0.01;*表示显著,P<0.05。 -
[1] 田其然. 经济红藻红毛菜的生物学特性研究[D]. 汕头: 汕头大学, 2007. [2] 黄文, 黄建明, 董飞强, 等. 红毛菜的营养成分特征和价值[J]. 海洋水产研究,1998(2):57−61. [3] 吴靖娜, 陈晓婷, 路海霞, 等. 红毛藻营养成分分析与评价[J]. 食品与生物技术学报,2019,38(6):131−136. doi: 10.3969/j.issn.1673-1689.2019.06.018 [4] Cofrades S, Lopez-Lopez I, Bravo L, et al. Nutritional and antioxidant properties of different brown and red Spanish edible seaweeds[J]. Food Science & Technology International,2010,16(5):361−370.
[5] 纪乃茹, 李月, 姜泽东, 等. 红毛藻研究进展[J]. 食品工业,2020,41(2):238−241. [6] 付晓苹. 红毛藻及坛紫菜藻红蛋白的分离纯化与相关性质的研究[D]. 厦门: 集美大学, 2007. [7] Ank G, Da Gama B A P, Pereira R C. Polyphenols from Stypopodium zonale (Phaeophyceae): Intrapopulational variation, induction by simulated herbivory, and epibiosis effects[J]. Aquatic Botany,2013,111:125−129. doi: 10.1016/j.aquabot.2013.06.007
[8] Emer S, Nissreen A G. Antibacterial derivatives of marine algae: An overview of pharmacological mechanisms and applications[J]. Marine Drugs,2016,14(4):91.
[9] Kim H J, Dasagrandhi C, Kim S H, et al. In vitro antibacterial activity of phlorotannins from edible brown algae, eisenia bicyclis against streptomycin-resistant Listeria monocytogenes[J]. Indian Journal of Microbiology,2018,58(1):105−108. doi: 10.1007/s12088-017-0693-x
[10] Van T T T, Hieu V M N, Vi T N H, et al. Antioxidant activities and total phenolic content of macroalgae from central coast of Vietnam[J]. Asian Journal of Chemistry,2013,25(12):6639−6642. doi: 10.14233/ajchem.2013.14395
[11] 李亚娴. 羊栖菜多酚粗品的纯化及其抗肿瘤活性研究[D]. 大连: 大连海洋大学, 2016. [12] Pantidos N, Boath A, Lund V, et al. Phenolic-rich extracts from the edible seaweed, Ascophyllum nodosum, inhibit α-amylase and α-glucosidase: Potential anti-hyperglycemic effects[J]. Journal of Functional Foods,2014,10:201−209. doi: 10.1016/j.jff.2014.06.018
[13] Lee S H, Jeon Y J. Anti-diabetic effects of brown algae derived phlorotannins, marine polyphenols through diverse mechanisms[J]. Fitoterapia,2013,86:129−136. doi: 10.1016/j.fitote.2013.02.013
[14] Yuan Y, Zhang J, FAN J J, et al. Microwave assisted extraction of phenolic compounds from four economic brown macroalgae species and evaluation of their antioxidant activities and inhibitory effects on α-amylase, α-glucosidase, pancreatic lipase and tyrosinase[J]. Food Research International,2018,113:288−297. doi: 10.1016/j.foodres.2018.07.021
[15] Montero L, Sánchez-Camargo A D, Ibáñez, E, et al. Phenolic compounds from edible algae: Bioactivity and health benefits[J]. Current Medicinal Chemistry,2019,25(37):4808−4826. doi: 10.2174/0929867324666170523120101
[16] 彭雍博, 罗宣, 汪秋宽, 等. 海藻多酚功能性作用机制及其应用研究[J]. 大连海洋大学学报,2017,32(4):484−492. [17] 赵国玲, 刘承初. 不同种类海藻多酚含量和还原力的对比研究[C]//中国水产学会, 中国水产学会学术年会论文摘要集.海口: 中国水产学会, 2009: 161. [18] 孙洲悦, 陈思远, 陈永雄, 等. 辣木叶多酚提取条件的优化及其抑菌性能研究[J]. 食品工业,2018,39(5):70−74. [19] 崔錾, 吕芳, 王天一, 等. 天浆壳多酚的提取工艺优化及其抗氧化活性评价[J]. 食品工业科技,2017,38(22):167−172. [20] 马慧, 茹鑫, 王津, 等. 4种茶叶水提物及茶多酚的体外抗氧化性能研究[J]. 食品研究与开发,2019,40(8):65−70. doi: 10.3969/j.issn.1005-6521.2019.08.011 [21] 胡会刚, 赵巧丽. 菠萝皮渣多酚的提取分离及其抗氧化活性评价[J]. 食品科技,2020,45(1):286−293. [22] Yang L, Jiang J G, Li W F, et al. Optimum extraction process of polyphenols from the bark of Phyllanthus emblica L. based on the response surface methodology[J]. Journal of Separation Science,2009,32(9):1437−1444. doi: 10.1002/jssc.200800744
[23] 洪璇, 陈仲巍, 李鹤宾, 等. 鸡桑叶多酚提取工艺优化及其抗氧化性能[J]. 食品工业科技,2018,39(13):73−77. [24] 付钦宝. 荷叶多酚的提取、抗氧化活性及其应用研究[D]. 芜湖: 安徽工程大学, 2017. [25] Jovanović A A, Đorđević V B, Zdunić G M, et al. Optimization of the extraction process of polyphenols from Thymus serpyllum L. herb using maceration, heat- and ultrasound-assisted techniques[J]. Separation and Purification Technology,2017,179:369−380. doi: 10.1016/j.seppur.2017.01.055
[26] 史建鑫. 昆布多酚提取、抗氧化与抑菌活性的研究[D]. 南昌: 南昌大学, 2017. [27] 陈洪彬, 杨敏, 宋露露, 等. 龙须菜多酚提取工艺优化及其体外抗氧化活性[J]. 食品与机械,2017,33(4):139−143. [28] 王敏, 田珍燕, 王蔚新. 板栗壳多酚的提取及其抗氧化性能的研究[J]. 食品研究与开发,2018,39(22):66−72. doi: 10.3969/j.issn.1005-6521.2018.22.012 [29] Dang T T, Quan V V, Schreider M J, et al. The effects of drying on physico-chemical properties and antioxidant capacity of the brown alga (Hormosira banksii (Turner) Decaisne)[J]. Journal of Food Processing and Preservation,2017,41(4):1−11.
[30] 段宙位, 窦志浩, 何艾, 等. 青金桔皮中多酚的提取及其抗氧化性研究[J]. 食品工业科技,2015,36(10):244−248. [31] 谢惠, 韩娅婷, 邵佩兰, 等. 红枣可溶性膳食纤维的抗氧化活性研究[J]. 食品工业科技,2017,38(22):37−41. [32] 许亚如. 褐藻多酚的抗氧化活性研究[D]. 宁波: 宁波大学, 2014. -
期刊类型引用(12)
1. 李德卿,朱军,邹潇潇,吴晓鹏,申铉日,鲍时翔. 莫氏马尾藻多酚提取工艺优化及其抗氧化活性分析. 粮食与油脂. 2024(04): 80-84 .  百度学术
百度学术
2. 何袅袅,蔡树芸,阎光宇,杨婷,陈伟珠,洪专,张怡,张怡评. 铜藻多酚的提取工艺及其稳定性和抑制酪氨酸酶活性. 食品研究与开发. 2024(09): 104-110 .  百度学术
百度学术
3. 董玉婷,马家乐,郑明静,王永兴,朱艳冰,杨远帆,姜泽东,倪辉,李清彪. 红毛藻膳食纤维制备工艺优化. 食品研究与开发. 2024(15): 107-116 .  百度学术
百度学术
4. 邓莹,刘杰,李海洋,陈莎,刘继雄,李明霞,龙昭军,李小丹. 牛马藤多糖的提取工艺优化及抗氧化活性研究. 广州化工. 2024(11): 28-32 .  百度学术
百度学术
5. 何袅袅,陈雅鑫,蔡树芸,施丽君,陈伟珠,陈晖,洪专,张怡,张怡评. 铜藻多酚的分离纯化及抗氧化活性研究. 食品工业科技. 2023(03): 183-191 .  本站查看
本站查看
6. 牛佳雯,雒江菡,张雨欣,李婧,禚昊. 道地药材月见草总多酚的提取工艺研究. 安徽农业科学. 2023(01): 166-168+174 .  百度学术
百度学术
7. 常高萍,林巧燕,张敏,郭佳瑄,李志朋,杜希萍,姜泽东. 红毛藻不同乙醇浓度提取物的生物活性及其成分分析. 化学试剂. 2023(02): 98-105 .  百度学术
百度学术
8. 王纪辉,耿阳阳,刘亚娜,张时馨,胡伯凯,梁美,谭化美,何佳丽. 不同溶剂浸提下核桃果实不同部位多酚物质响应及其组成. 南京师大学报(自然科学版). 2022(03): 35-45 .  百度学术
百度学术
9. 何袅袅,陈雅鑫,蔡树芸,陈伟珠,张怡评,洪专. 海藻多酚提取分离及生物活性研究进展. 食品工业. 2022(10): 190-194 .  百度学术
百度学术
10. 陶凤庭,潘创,戚勃,胡晓,赵永强,杨贤庆,杨莉莉. 坛紫菜分离蛋白的提取与结构解析. 大连海洋大学学报. 2022(05): 850-857 .  百度学术
百度学术
11. 龙晓珊,廖森泰,刘书成,刘凡,黎尔纳,庞道睿,穆利霞,王卫飞,邹宇晓. 肉桂多酚清除自由基及抑制α-葡萄糖苷酶活性的能力. 现代食品科技. 2021(08): 119-126 .  百度学术
百度学术
12. 林宝妹,邱珊莲,吴妙鸿,张帅,李海明,洪佳敏. 嘉宝果果皮多酚提取工艺优化及生物活性测定. 江苏农业科学. 2021(21): 191-196 .  百度学术
百度学术
其他类型引用(6)






 下载:
下载:







 下载:
下载:



